YUFLYMA injektioneste, liuos, esitäytetty kynä 80 mg
 Lääketurva
Lääketurva
Riskienminimointimateriaalit
Potilas
Huomioitavaa

Tähän lääkevalmisteeseen kohdistuu lisäseurantaa. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan epäillyistä lääkkeen haittavaikutuksista. Ks. kohdasta Haittavaikutukset, miten haittavaikutuksista ilmoitetaan.
Vaikuttavat aineet ja niiden määrät
Yuflyma 80 mg injektioneste, liuos esitäytetty kynä
Yksi esitäytetty 0,8 ml:n kerta-annoskynä sisältää 80 mg adalimumabia.
Adalimumabi on rekombinantti ihmisen monoklonaalinen vasta-aine, joka on tuotettu kiinanhamsterin munasarjasoluissa (CHO).
Täydellinen apuaineluettelo, ks. kohta 6. 1.
Lääkemuoto
Injektioneste, liuos (injektio)
Kliiniset tiedot
Käyttöaiheet
Nivelreuma
Yuflyman ja metotreksaatin yhdistelmä on tarkoitettu:
keskivaikeaa tai vaikeaa, aktiivista nivelreumaa sairastavien aikuispotilaiden hoitoon silloin, kun varsinaisilla taudin kulkuun vaikuttavilla reumalääkkeillä (DMARD = disease-modifying anti-rheumatic drugs), kuten metotreksaatilla, ei ole saatu riittävää vastetta.
vaikean aktiivisen ja progressiivisen nivelreuman hoitoon aikuisilla, jotka eivät ole aiemmin saaneet metotreksaattihoitoa.
Yuflymaa voidaan antaa myös yksinään, jos potilas ei siedä metotreksaattia tai metotreksaattihoidon jatkaminen ei ole tarkoituksenmukaista.
Adalimumabin on metotreksaattiin yhdistettynä osoitettu vähentävän nivelvaurion etenemistä röntgenkuvista mitattuna ja parantavan fyysistä toimintakykyä.
Psoriaasi
Yuflyma on tarkoitettu keskivaikean tai vaikean kroonisen läiskäpsoriaasin hoitoon aikuispotilailla, joille harkitaan systeemistä hoitoa.
Hidradenitis suppurativa (HS-tauti)
Yuflyma on tarkoitettu keskivaikean ja vaikean aktiivisen hidradenitis suppurativan (acne inversa, märkivä hikirauhastulehdus)) hoitoon aikuisille ja nuorille 12 vuoden iästä alkaen, kun tavanomaisella systeemisellä HS-hoidolla ei ole saatu riittävää vastetta (ks. kohdat Farmakodynamiikka ja Farmakokinetiikka).
Crohnin tauti
Yuflyma on tarkoitettu keskivaikean tai vaikean aktiivisen Crohnin taudin hoitoon aikuisille potilaille, joilla täysimääräinen ja adekvaatti kortikosteroidihoito ja/tai immunosuppressanttihoito ei ole saanut aikaan hoitovastetta, sekä potilaille, jotka eivät siedä tällaisia hoitoja tai joilla on tällaisille hoidoille jokin lääketieteellinen vasta-aihe.
Lasten Crohnin tauti
Yuflyma on tarkoitettu keskivaikean tai vaikean aktiivisen Crohnin taudin hoitoon vähintään 6-vuotiailla lapsipotilailla, kun tavanomaisilla hoidoilla (mm. primaarinen ravitsemushoito ja kortikosteroidi ja/taiimmunomodulaattori) ei ole saavutettu riittävää vastetta tai ne ovat olleet huonosti siedettyjä tai kyseiset hoidot ovat vasta-aiheisia.
Ulseratiivinen koliitti
Yuflyma on tarkoitettu keskivaikean tai vaikean aktiivisen ulseratiivisen koliitin hoitoon aikuispotilaille, joilla vaste tavanomaisille hoidoille mukaan lukien kortikosteroidit ja 6-merkaptopuriini (6-MP) tai atsatiopriini (AZA) on ollut riittämätön, tai potilaille, jotka eivät siedä tällaisia hoitoja tai joilla on tällaisille hoidoille jokin lääketieteellinen vasta-aihe.
Ulseratiivinen koliitti lapsilla
Yuflyma on tarkoitettu keskivaikean tai vaikean, aktiivisen ulseratiivisen koliitin hoitoon lapsille 6 vuoden iästä alkaen, kun tavanomaisilla hoidoilla (mm. kortikosteroidit ja/tai 6-merkaptopuriini (6-MP) tai atsatiopriini (AZA)) ei ole saatu riittävää vastetta tai ne ovat olleet huonosti siedettyjä tai kyseiset hoidot ovat vasta-aiheisia.
Uveiitti
Yuflyma on tarkoitettu ei-infektioperäisen intermediaarisen, posteriorisen ja panuveiitin hoitoon aikuispotilaille, joilla vaste kortikosteroideille on riittämätön, joiden kortikosteroidien käyttöä täytyy rajoittaa, tai joille kortikosteroidihoito ei sovi.
Lasten uveiitti
Yuflyma on tarkoitettu lasten kroonisen ei-infektioperäisen anteriorisen uveiitin hoitoon 2 vuoden iästä alkaen, kun tavanomaiselle hoidolle ei ole saatu riittävää vastetta tai tavanomainen hoito on ollut huonosti siedettyä, tai se ei ole tarkoituksenmukaista.
Ehto
Hoito tulee toteuttaa indikaation mukaiseen hoitoon perehtyneen lääkärin aloittamana ja valvonnassa. Hoitoa saaville potilaille tulee antaa erityinen potilaskortti.
Annostus ja antotapa
Yuflyma-hoito tulee toteuttaa indikaation mukaisten sairauksien diagnosointiin ja hoitoon perehtyneen lääkärin aloittamana ja valvonnassa. Silmätautien erikoislääkäreitä kehotetaan konsultoimaan asianmukaista erikoislääkäriä ennen Yuflyma-hoidon aloitusta (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet). Yuflyma-hoitoa saaville potilaille tulee antaa Potilaskortti.
Kun potilas hallitsee pistämistekniikan kunnolla, hän voi pistää Yuflyma-annoksensa itse, jos lääkäri pitää tätä soveliaana ja seuraa tarvittaessa potilaan tilaa.
Muut samanaikaiset hoidot (esim. kortikosteroidit ja/tai immunomoduloivat hoidot) tulee optimoida Yuflyma-hoidon aikana.
Yuflyma on saatavana 40 mg:n ja 80 mg:n esitäytettynä kynänä. Siksi Yuflymaa ei voida antaa potilaille, jotka tarvitsevat vähemmän kuin täyden 40 mg:n annoksen. Jos tarvitaan vaihtoehtoinen annos, tulee käyttää muita tällaista vaihtoehtoa tarjoavia adalimumabivalmisteita.
Annostus
Nivelreuma
Yuflyman suositusannos aikuisille nivelreumapotilaille on 40 mg adalimumabia kerta-annoksena joka toinen viikko pistoksena ihon alle. Metotreksaattihoitoa tulee jatkaa Yuflyma-hoidon aikana.
Glukokortikoidien, salisylaattien, steroideihin kuulumattomien tulehduskipulääkkeiden tai kipulääkkeiden käyttöä voidaan jatkaa Yuflyma-hoidon aikana. Yhdistäminen muihin taudin kulkuun vaikuttaviin reumalääkkeisiin metotreksaattia lukuun ottamatta, ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Farmakodynamiikka.
Jos vaste Yuflyma-annokselle 40 mg joka toinen viikko heikkenee monoterapiahoidon aikana, voi annostuksen suurentaminen tasolle 40 mg adalimumabia kerran viikossa tai 80 mg joka toinen viikko hyödyttää osaa potilaista.
Saatavilla olevien tietojen perusteella hoitovaste saavutetaan yleensä 12 viikon kuluessa. Jos hoitovastetta ei saavuteta tämän ajan kuluessa, hoidon jatkamista tulee harkita uudelleen.
Psoriaasi
Aikuispotilailla suositellaan Yuflyma-hoidon aloittamista aloitusannoksella 80 mg ihon alle, jonka jälkeen potilas jatkaa annoksella 40 mg ihon alle joka toinen viikko alkaen viikon kuluttua aloitusannoksesta.
Yuflyma 40 mg injektioneste, liuos esitäytetyssä kynässä on saatavilla ylläpitoannokseen.
Jos potilaalla ei saavuteta vastetta 16 viikon hoidon aikana, hoidon jatkamista tulee harkita tarkoin.
Potilaat, joilla vaste ei ole riittävä Yuflyma-annoksella 40 mg joka toinen viikko 16 viikon hoidon jälkeen, voivat hyötyä annoksen suurentamisesta 40 mg:aan kerran viikossa tai 80 mg:aan joka toinen viikko. Jos potilaalla ei saavuteta riittävää vastetta annoksen suurentamisen jälkeen, viikottaisen 40 mg:n annoksen tai joka toinen viikko otettavan 80 mg:n annoksen jatkamisen hyödyt ja riskit tulee harkita tarkoin (ks. kohta Farmakodynamiikka). Jos riittävä vaste saavutetaan annostuksella 40 mg kerran viikossa tai 80 mg joka toinen viikko, voidaan annostus myöhemmin laskea takaisin 40 mg:aan joka toinen viikko.
Hidradenitis suppurativa
Hidradenitis suppurativaa (HS-tautia) sairastaville aikuispotilaille suositeltava Yuflyma-annos on ensin 160 mg päivänä 1 (kaksi 80 mg:n injektiota samana päivänä tai yksi 80 mg:n injektiota päivässä kahtena peräkkäisenä päivänä) ja tämän jälkeen 80 mg kaksi viikkoa myöhemmin päivänä 15. Kaksi viikkoa myöhemmin (päivänä 29) siirrytään käyttämään 40 mg:n annosta kerran viikossa tai 80 mg:n annosta joka toinen viikko. Antibioottihoitoa voidaan tarvittaessa jatkaa Yuflyma-hoidon aikana. On suositeltavaa, että potilas käsittelee HS-leesiot paikallisesti käytettävällä antiseptisella ihohuuhteella päivittäin Yuflyma-hoidon aikana.
Jos oireet eivät lievity 12 viikon kuluessa, hoidon jatkamista on harkittava tarkoin.
Jos hoito on keskeytettävä, hoito voidaan aloittaa uudelleen Yuflyma-annoksella 40 mg kerran viikossa tai 80 mg joka toinen viikko (ks. kohta Farmakodynamiikka).
Pitkäaikaishoidon jatkamisen hyödyt ja riskit on arvioitava säännöllisin väliajoin (ks. kohta Farmakodynamiikka).
Crohnin tauti
Keskivaikeaa tai vaikeaa aktiivista Crohnin tautia sairastavien aikuispotilaiden Yuflyma-hoito tulisi aloittaa annoksella 80 mg viikolla 0, jonka jälkeen 40 mg viikolla 2. Jos hoitovaste on saavutettava nopeammin, voidaan hoito aloittaa antamalla potilaalle 160 mg Yuflymaa viikolla 0 (joko kaksi 80 mg:n injektiota samana päivänä tai yksi 80 mg:n injektiota päivässä kahtena peräkkäisenä päivänä), 80 mg viikolla 2. On kuitenkin tiedostettava, että suurempia aloitusannoksia käytettäessä haittatapahtumariski on suurempi
Aloitusvaiheen jälkeen suositusannos on 40 mg injektiona ihon alle joka toinen viikko. Mikäli potilas on keskeyttänyt Yuflyma-hoidon ja taudin merkit ja oireet uusiutuvat, Yuflyma-hoito voidaan aloittaa uudelleen. Hoidon uudelleenaloittamisesta tilanteessa, jossa edellisen annoksen antamisesta on kulunut yli 8 viikkoa, on vain vähän kokemusta.
Kortikosteroidiannosta voidaan pienentää ylläpitohoidon aikana hoitosuositusten mukaisesti.
Jos vaste Yuflyma-annokselle 40 mg joka toinen viikko heikkenee, voi annostuksen suurentaminen tasolle 40 mg Yuflymaa kerran viikossa tai 80 mg joka toinen viikko hyödyttää osaa potilaista.
Myös sellaiset potilaat jotka eivät ole saaneet vastetta viikkoon 4 mennessä, voivat hyötyä ylläpitohoidon jatkamisesta 12 viikkoon asti. Jos potilas ei saavuta vastetta tämän ajan kuluessa, hoidon jatkamista on harkittava tarkoin.
Ulseratiivinen koliitti
Keskivaikeaa tai vaikeaa ulseratiivista koliittia sairastavien aikuispotilaiden suositettu aloitusannos on 160 mg viikolla 0 (joko kaksi 80 mg:n injektiota samana päivänä tai yksi 80 mg:n injektiota päivässä kahtena peräkkäisenä päivänä) ja 80 mg viikolla 2. Aloitusvaiheen jälkeen suositusannos on 40 mg injektiona ihon alle joka toinen viikko.
Kortikosteroidiannosta voidaan pienentää ylläpitohoidon aikana hoitosuositusten mukaisesti.
Jos vaste Yuflyma-annokselle 40 mg joka toinen viikko heikkenee, voi annostuksen suurentaminen tasolle 40 mg Yuflymaa kerran viikossa tai 80 mg joka toinen viikko hyödyttää osaa potilaista.
Saatavilla olevien tietojen perusteella hoitovaste saavutetaan yleensä 2–8 viikon kuluessa. Yuflyma-hoitoa ei tule jatkaa potilailla, jotka eivät saa vastetta tässä ajassa.
Uveiitti
Uveiittia sairastavilla aikuispotilailla suositellaan Yuflyma-hoidon aloittamista aloitusannoksella 80 mg, jonka jälkeen annetaan 40 mg joka toinen viikko alkaen viikon kuluttua aloitusannoksesta. Yuflyma 40 mg injektioneste, liuos esitäytetyssä kynässä on saatavilla ylläpitoannokseen. Kokemusta hoidon aloituksesta yksinään adalimumabivalmisteella on rajallisesti. Yuflyma-hoito voidaan aloittaa yhdessä kortikosteroidin ja/tai toisen ei-biologisen immunomoduloivan hoidon kanssa. Samanaikaista kortikosteroidiannosta voidaan pienentää hoitosuositusten mukaisesti kahden viikon kuluttua Yuflyma-hoidon aloituksesta.
On suositeltavaa, että jatkuvan, pitkäaikaisen hoidon hyödyt ja riskit arvioidaan vuosittain (ks. kohta Farmakodynamiikka).
Erityisryhmät
Iäkkäät potilaat
Annoksen muuttaminen ei ole tarpeen.
Munuaisten ja/tai maksan vajaatoiminta
Aadalimumabia ei ole tutkittu näissä potilasryhmissä. Annossuosituksia ei voida antaa.
Lapsipotilaat
Yuflyma on saatavana 40 mg:n ja 80 mg:n esitäytettynä kynänä. Siksi Yuflymaa ei voida antaa lapsipotilaille, jotka tarvitsevat vähemmän kuin täyden 40 mg:n annoksen. Jos tarvitaan vaihtoehtoinen annos, tulee käyttää muita tällaista vaihtoehtoa tarjoavia adalimumabivalmisteita.
Hidradenitis suppurativa nuorilla (12 vuoden iästä alkaen, kun paino on vähintään 30 kg)
Nuorilla HS-tautia sairastavilla potilailla ei ole tehty kliinisiä adalimumabitutkimuksia. Adalimumabin annostus näillä potilailla on määritetty farmakokineettisen mallinnuksen ja simulaation avulla (ks. kohta Farmakokinetiikka).
Suositeltu Yuflyma-annos on 80 mg ihonalaisena injektiona viikolla 0, jonka jälkeen ihonalaisena injektiona 40 mg joka toinen viikko alkaen viikosta 1.
Nuorille potilaille, joilla vaste 40 mg Yuflyma-annokselle joka toinen viikko on riittämätön, voidaan harkita annostuksen suurentamista 40 mg:aan joka viikko tai 80 mg:aan joka toinen viikko.
Antibioottihoitoa voidaan tarvittaessa jatkaa Yuflyma-hoidon aikana. On suositeltavaa, että potilas käsittelee HS-leesiot paikallisesti käytettävällä antiseptisella ihohuuhteella päivittäin Yuflyma-hoidon aikana.
Jos oireet eivät lievity 12 viikon kuluessa, hoidon jatkamista on harkittava tarkoin.
Jos hoito on keskeytettävä, Yuflyma-hoito voidaan aloittaa uudelleen asianmukaisella tavalla.
Pitkäaikaishoidon jatkamisen hyödyt ja riskit on arvioitava säännöllisin väliajoin (ks. aikuisia koskevat tiedot kohdasta Farmakodynamiikka).
Ei ole asianmukaista käyttää adalimumabia alle 12 vuoden ikäisille lapsille tämän käyttöaiheen hoidossa.
Lasten Crohnin tauti
Yuflyman suositusannos Crohnin tautia sairastaville 6–17-vuotiaille potilaillen lasketaan painon perusteella (taulukko 1). Yuflyma annetaan ihonalaisena injektiona.
Taulukko 1. Adalimumabiannos Crohnin tautia sairastaville lapsipotilaille
| Potilaan paino | Induktioannos | Ylläpitoannos viikolta 4 alkaen |
| < 40 kg | 40 mg viikolla 0 ja 20 mg viikolla 2* Jos nopeampi hoitovaste on tarpeen, voidaan antaa seuraava annos (on kuitenkin muistettava, että suurempia aloitusannoksia käytettäessä haittatapahtumariski voi olla suurempi): 80 mg viikolla 0 ja 40 mg viikolla 2 | 20 mg joka toinen viikko |
| ≥ 40 kg | 80 mg viikolla 0 ja 40 mg viikolla 2 Jos nopeampi hoitovaste on tarpeen, voidaan antaa seuraava annos (on kuitenkin muistettava, että suurempia aloitusannoksia käytettäessä haittatapahtumariski voi olla suurempi): 160 mg viikolla 0 ja 80 mg viikolla 2 | 40 mg joka toinen viikko |
*Huomio: Yuflyma on saatavana 40 mg:n ja 80 mg:n esitäytettynä kynänä. Siksi Yuflymaa ei voida antaa potilaille, jotka tarvitsevat vähemmän kuin täyden 40 mg:n annoksen.
Potilaat, joilla vaste ei ole riittävä, voivat hyötyä annoksen suurentamisesta:
- < 40 kg: 20 mg joka viikko
- ≥ 40 kg: 40 mg joka viikko tai 80 mg joka toinen viikko
Hoidon jatkamista on harkittava tarkoin, jos potilas ei saavuta vastetta viikkoon 12 mennessä.
Ei ole asianmukaista käyttää adalimumabia alle 6 vuoden ikäisille tämän käyttöaiheen hoidossa.
Ulseratiivinen koliitti lapsilla
Ulseratiivista koliittia sairastavien 6–17-vuotiaiden potilaiden suositeltu Yuflyma-annos lasketaan painon perusteella (taulukko 2). Yuflyma annostellaan injektiona ihon alle.
Taulukko 2. Yuflyma-annos ulseratiivista koliittia sairastavilla pediatrisilla potilailla
| Potilaan paino | Aloitusannos | Ylläpitoannos alkaen viikolta 4* |
| < 40 kg |
|
|
| ≥ 40 kg |
|
|
| * Pediatristen potilaiden, jotka täyttävät 18 vuotta Yuflyma-hoidon aikana, tulee jatkaa hoitoa heille määrätyllä ylläpitoannoksella. | ||
Hoidon jatkamista on harkittava tarkoin, jos potilas ei saavuta vastetta viikkoon 8 mennessä.
Ei ole asianmukaista käyttää adalimumabia alle 6 vuoden ikäisille tämän käyttöaiheen hoidossa.
Lasten uveiitti
Yuflyman suositusannos uveiittia sairastaville lapsipotilaille 2 vuoden iästä alkaen lasketaan painon perusteella (taulukko 3). Yuflyma annetaan ihonalaisena injektiona.
Ei ole olemassa kokemuksia lasten uveiitin hoidosta adalimumabilla ilman samanaikaista metotreksaattihoitoa.
Taulukko 3. Yuflyma-annos uveiittia sairastaville lapsipotilaille
| Potilaan paino | Annos |
| < 30 kg | 20 mg joka toinen viikko yhdessä metotreksaatin kanssa |
| ≥ 30 kg | 40 mg joka toinen viikko yhdessä metotreksaatin kanssa |
Huomio: Yuflyma on saatavana 40 mg:n ja 80 mg:n esitäytettynä kynänä. Siksi Yuflymaa ei voida antaa potilaille, jotka tarvitsevat vähemmän kuin täyden 40 mg:n annoksen.
Kun Yuflyma-hoito aloitetaan, voidaan antaa 40 mg:n latausannos < 30 kg potilaille tai 80 mg:n latausannos
≥ 30 kg potilaille viikkoa ennen ylläpitohoidon aloittamista. Kliinistä tutkimustietoa adalimumabilatausannoksen käytöstä alle 6-vuotiailla lapsilla ei ole (ks. kohta Farmakokinetiikka).
Ei ole asianmukaista käyttää adalimumabia alle 2 vuoden ikäisille lapsille tämän käyttöaiheen hoidossa.
On suositeltavaa, että jatkuvan, pitkäaikaisen hoidon hyödyt ja riskit arvioidaan vuosittain (ks. kohta Farmakodynamiikka).
Lasten läiskäpsoriaasi
Läiskäpsoriaasia sairastavien 4–17-vuotiaiden potilaiden Yuflyman suositeltu annos lasketaan painon perusteella (taulukko 4). Yuflyma annetaan ihonalaisena injektiona.
Taulukko 4. Yuflyma-annos läiskäpsoriaasia sairastaville lapsipotilaille
| Potilaan paino | Annos |
| 15 kg – < 30 kg | − |
| ≥ 30 kg | Aloitusannos on 40 mg, jonka jälkeen annetaan 40 mg joka toinen viikko alkaen viikon kuluttua aloitusannoksesta. |
Huomio: Yuflyma on saatavana 40 mg:n ja 80 mg:n esitäytettynä kynänä. Siksi Yuflymaa ei voida antaa potilaille, jotka tarvitsevat vähemmän kuin täyden 40 mg:n annoksen.
Jos potilas ei saavuta vastetta 16 viikon kuluessa, hoidon jatkamista on harkittava tarkoin.
Jos uusintahoito adalimumabilla on aiheellista, noudatetaan edellä annettuja ohjeita annoksesta ja hoidon kestosta.
Adalimumabin turvallisuutta on arvioitu läiskäpsoriaasia sairastavilla lapsipotilailla keskimäärin 13 kuukauden ajan.
Ei ole asianmukaista käyttää adalimumabia alle 4 vuoden ikäisille tämän käyttöaiheen hoidossa.
Antotapa
Yuflyma annetaan ihonalaisena injektiona.
Katso tarkat käyttöohjeet pakkausselosteesta.
Adalimumabia voi olla saatavilla myös muita vahvuuksia ja annostelumuotoja.
Vasta-aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille.
Aktiivinen tuberkuloosi tai jokin muu vakava infektio, kuten sepsis, sekä opportunistiset infektiot (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Keskivaikea tai vaikea sydämen vajaatoiminta (NYHA III/IV) (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Varoitukset ja käyttöön liittyvät varotoimet
Jäljitettävyys
Biologisten lääkevalmisteiden jäljitettävyyden parantamiseksi annetun lääkevalmisteen nimi ja eränumero tulisi kirjata ylös selkeästi.
Infektiot
TNF-salpaajia käyttävät potilaat ovat herkempiä vakaville infektioille. Heikentynyt keuhkojen toiminta voi lisätä infektioiden kehittymisen riskiä. Potilaita tulee täten seurata huolellisesti infektioiden (mm. tuberkuloosin) varalta ennen Yuflyma-hoidon aloittamista, hoidon aikana ja sen jälkeen. Koska adalimumabin eliminoituminen voi viedä neljä kuukautta, seurantaa tulee jatkaa siihen saakka.
Yuflyma-hoitoa ei tule aloittaa potilailla, joilla on aktiivinen infektio (krooninen tai paikallinen), ennen kuin infektio on hallinnassa. Potilailla, jotka ovat altistuneet tuberkuloosille sekä potilailla, jotka ovat matkustaneet korkean tuberkuloosin tai endeemisen mykoosin (kuten histoplasmoosi, koksidioidomykoosi tai blastomykoosi) riskialueilla, Yuflyma-hoidon hyödyt ja riskit on huomioitava ennen hoidon aloittamista (ks. Muut opportunistiset infektiot).
Potilaita, joille kehittyy uusi infektio Yuflyma-hoidon aikana, tulee seurata huolellisesti ja heille on tehtävä täydellinen diagnostinen arvio. Jos potilaalle kehittyy uusi, vakava infektio tai sepsis, tarvittava antimikrobinen tai antimykoottinen hoito on aloitettava ja Yuflyman antaminen on keskeytettävä, kunnes infektio saadaan hallintaan. Lääkärien tulee noudattaa varovaisuutta harkitessaan Yuflyman käyttöä potilailla, joilla on ollut toistuvia infektioita tai perussairaus, joka voi altistaa infektioille, mukaan lukien samanaikainen immunosuppressiivisen lääkityksen käyttö.
Vakavat infektiot
Vakavia infektioita, mukaan lukien sepsis, joka johtuu bakteereista, mykobakteereista, invasiivisista sieni-infektioista, parasiiteista, viruksista tai muista opportunistisista infektioista, kuten listerioosista, legionelloosista ja pneumokystoosista, on raportoitu adalimumabia käyttävillä potilailla.
Muita kliinisissä tutkimuksissa havaittuja vakavia infektioita ovat pneumonia, pyelonefriitti, septinen niveltulehdus ja sepsiksen kaltaiset infektiot. Infektioihin liittyvää sairaalahoitoa tai kuolemaan johtavia tapauksia on raportoitu.
Tuberkuloosi
Adalimumabihoitoa saaneilla potilailla on raportoitu tuberkuloosia, mukaan lukien tuberkuloosin reaktivaatiota ja uusia tapauksia. Raportit sisälsivät sekä keuhkotuberkuloosia että keuhkojen ulkopuolista (eli disseminoitunutta) tuberkuloosia.
Ennen Yuflyma-hoidon aloittamista tulee kaikki potilaat tutkia sekä aktiivisen että inaktiivisen (”latentin”) tuberkuloosin varalta. Tähän tutkimukseen tulee kuulua huolellinen potilaan arviointi, jotta saadaan selville potilaan aikaisemmin sairastama tuberkuloosi ja aiemmat kontaktit aktiivista tuberkuloosia sairastavan henkilön kanssa sekä aikaisemmat ja/tai käynnissä olevat immunosuppressiiviset hoidot. Asianmukaisia seulontatestejä (tuberkuliinikoe ja keuhkoröntgen) voidaan joutua tekemään kaikille potilaille (paikallisten vaatimusten mukaisesti). Nämä kokeet ja niiden tulokset on suositeltavaa merkitä potilaskorttiin. Lääkäriä muistutetaan, että tuberkuliini-ihotestissä saatetaan saada väärä negatiivinen tulos, jos kyseessä on vakavasti sairas tai immuunivajavuudesta kärsivä potilas.
Jos todetaan aktiivinen tuberkuloosi, Yuflyma-hoitoa ei saa aloittaa (ks. kohta Vasta-aiheet).
Alla kuvatuissa tilanteissa Yuflyma-hoidon hyötyjen ja riskien suhdetta on harkittava hyvin huolellisesti.
Jos potilaalla epäillään latenttia tuberkuloosia, on tuberkuloosin hoitoon perehtynyttä lääkäriä konsultoitava.
Jos potilaalla todetaan latentti tuberkuloosi, sen hoito profylaktisella tuberkuloosihoidolla on käynnistettävä ennen Yuflyma-hoidon aloittamista ja paikallisten suositusten mukaisesti.
Profylaktista tuberkuloosihoitoa on harkittava ennen Yuflyma-hoidon aloittamista myös siinä tapauksessa, että potilaalla on useita tai merkittäviä tuberkuloosin riskitekijöitä, mutta latentin tuberkuloosin osoituskoe on negatiivinen, ja potilaalla, jolla on aiemmin ollut latentti tai aktiivinen tuberkuloosi, eikä hoidon asianmukaisesta toteutuksesta ole varmuutta.
Adalimumabihoitoa saaneilla potilailla on ilmennyt tuberkuloosin reaktivaatiotapauksia tuberkuloosin profylaktisesta hoidosta huolimatta. Joillekin potilaille, joita on aiemmin hoidettu menestyksekkäästi aktiivisen tuberkuloosin vuoksi, on uudelleen kehittynyt tuberkuloosi adalimumabihoidon aikana.
Potilaita tulee myös kehottaa kääntymään lääkärin puoleen, jos heillä esiintyy tuberkuloosi-infektioon viittaavia merkkejä/oireita (esim. sitkeää yskää, laihtumista/painon laskua, lämmännousua, voimattomuutta) Yulfyma-hoidon aikana tai sen jälkeen.
Muut opportunistiset infektiot
Adalimumabia saavilla potilailla on tavattu opportunistisia infektioita, kuten invasiivisia sieni-infektioita. TNF-salpaajia saavilla potilailla näitä infektioita ei ole välttämättä tunnistettu, mikä on johtanut asianmukaisen hoidon viivästymiseen ja joskus kuolemaan.
Jos potilaalle kehittyy sellaisia merkkejä ja oireita kuten kuume, huonovointisuus, painonlasku, hikoilu, yskä, hengenahdistus, ja/tai keuhkoinfiltraatteja tai muita vakavia systeemisiä sairauksia, liittyi niihin sokki tai ei, invasiivista sieni-infektiota tulisi epäillä ja Yulfyman anto lopettaa viipymättä. Diagnoosi ja empiirisen antifungaalisen hoidon aloitus tulisi tehdä yhteistyössä lääkärin kanssa, jolla on kokemusta invasiivisten sieni-infektioiden hoidosta.
B-hepatiitin uudelleenaktivoituminen
B-hepatiittiviruksen kroonisilla kantajilla (eli pinta-antigeeni-positiivisilla) on todettu B-hepatiitin uudelleenaktivoitumista TNF-salpaajahoidon, myös adalimumabihoidon, aikana. Jotkin tapaukset ovat johtaneet kuolemaan. Potilaat on tutkittava HBV-infektion varalta ennen Yuflyma-hoidon aloittamista. Jos potilas osottautuu HBV-tartunnan kantajaksi, suositellaan hepatiitti B-infektion hoitoon perehtyneen lääkärin konsultoimista.
Jos HBV-kantaja tarvitsee ehdottomasti Yuflyma-hoitoa, häntä on seurattava tarkasti aktiiviseen HBV-infektioon viittaavien merkkien ja oireiden varalta koko hoitojakson ajan ja useita kuukausia hoidon päättymisen jälkeen. TNF-salpaajahoitoa saavien HBV-kantajien hoitamisesta samanaikaisesti viruslääkkeillä B-hepatiitin uudelleenaktivoitumisen estämiseksi ei ole riittävästi tietoa. Jos potilaan B-hepatiitti aktivoituu uudelleen, on Yuflyma-hoito lopetettava ja tehokas viruslääkitys ja asianmukainen tukihoito aloitettava.
Neurologiset tapahtumat
TNF-antigonisteihin, kuten adalimumabiin, on harvinaisissa tapauksissa liittynyt keskushermoston demyelinoivan sairauden (mukaan lukien MS-tauti ja optikusneuriitti) ja ääreishermoston demyelinoivan sairauden (mukaan lukien Guillain–Barrén oireyhtymä) kliinisten oireiden ja/tai röntgenlöydösten ilmeneminen tai paheneminen. Varovaisuutta tulee siis noudattaa määrättäessä Yuflymaa potilaille, joilla on joko aiemmin tai hiljattain alkanut keskus- tai ääreishermoston demyelinoiva sairaus. Yuflyma-hoidon keskeytystä on harkittava, jos potilaalle kehittyy jokin näistä sairauksista. Intermediaarisen uveiitin ja keskushermoston demyelinoivien sairauksien välillä on tunnettu yhteys. Potilaille, joilla on ei-infektioperäinen intermediaarinen uveiitti, on ennen Yuflyma-hoidon aloitusta sekä säännöllisesti hoidon aikana tehtävä neurologinen arvio, jossa arvioidaan aiemmin alkaneita tai kehittymässä olevia keskushermoston demyelinoivia sairauksia.
Allergiset reaktiot
Kliinisissä tutkimuksissa adalimumabihoitoon liittyvät vakavat allergiset reaktiot olivat harvinaisia. Adalimumabiin liitetyt lievät allergiset reaktiot olivat kliinisissä tutkimuksissa melko harvinaisia. Adalimumabin annon yhteydessä on raportoitu vakavia allergisia reaktioita, mukaan lukien anafylaksia. Jos anafylaktinen tai muu vakava allerginen reaktio ilmenee, tulee Yuflyman antaminen keskeyttää välittömästi ja aloittaa asianmukainen hoito.
Immunosuppressio
Tutkimuksessa, jossa 64 nivelreumapotilasta sai adalimumabihoitoa, ei havaittu viivästyneen yliherkkyysreaktion heikkenemistä, immunoglobuliinipitoisuuden pienenemistä eikä muutoksia efektori T- tai B-solujen, luonnollisten tappajasolujen, monosyyttien/makrofagien eikä neutrofiilien määrässä.
Maligniteetit ja lymfoproliferatiiviset häiriöt
TNF-salpaajilla tehtyjen kliinisten tutkimusten kontrolloiduissa osioissa TNF-salpaajaa saaneilla potilailla on havaittu enemmän maligniteetteja, mukaan lukien lymfoomia, kuin verrokkipotilailla. Niitä esiintyi kuitenkin harvoin. Leukemiaa on raportoitu markkinoilletulon jälkeen potilailla, joita hoidettiin TNF-salpaajilla. Lymfooman ja leukemian taustariski on suurentunut nivelreumapotilailla, joilla on hyvin aktiivinen, pitkään kestänyt infektiosairaus, mikä vaikeuttaa riskin arviointia. Tämänhetkisten tietojen perusteella lymfoomien, leukemian ja muiden maligniteettien kehittymisriskiä ei voida sulkea pois TNF-salpaajahoitoa saavien potilaiden kohdalla.
Maligniteetteja, myös kuolemaan johtaneita, on ilmoitettu lapsilla, nuorilla ja nuorilla aikuisilla (alle 22-vuotiailla), jotka ovat saaneet TNF-salpaajahoitoa (hoidon aloitusikä ≤ 18 vuotta), markkinoilletulon jälkeinen adalimumabihoito mukaan lukien. Noin puolet tapauksista oli lymfoomia. Muut tapaukset olivat erilaisia maligniteetteja, ja mukana oli harvinaisia, yleensä immunosuppressioon liittyviä muotoja. Maligniteettiriskiä ei voida sulkea pois lapsilla ja nuorilla, jotka saavat TNF-salpaajahoitoa.
Adalimumabilla hoidetuilla potilailla on markkinoilletulon jälkeen raportoitu harvoin hepatospleenistä T-solulymfoomaa. Tämä harvinainen T-solulymfooma on taudinkuvaltaan aggressiivinen ja tavallisesti fataali. Osa adalimumabihoidon aikana ilmenneistä hepatospleenisistä T-solulymfoomista on ilmennyt nuorilla aikuisilla, joilla on hoidettu tulehduksellista suolistotautia samanaikaisesti atsatiopriinilla tai 6-merkaptopuriinilla. Atsatiopriinin tai 6-merkaptopuriinin ja Yuflyman yhdistelmähoitoon liittyvä mahdollinen riski on huomioitava. Hepatospleenisen T-solulymfooman kehittymisen riskiä ei voida sulkea pois potilailla, joita hoidetaan Yuflymalla (ks.kohta 4.8).
Tutkimuksia ei ole tehty potilailla, joilla on ollut jokin maligniteetti ennen adalimumabihoitoa, tai joilla adalimumabihoitoa olisi jatkettu maligniteetin kehittymisen jälkeen. Siksi erityistä varovaisuutta tulee noudattaa harkittaessa Yuflyma-hoitoa näille potilaille (ks. kohta Haittavaikutukset).
Kaikki potilaat tulee tutkia muiden ihosyöpien kuin melanooman varalta ennen Yuflyma-hoitoa ja sen aikana. Tämä koskee etenkin potilaita, jotka ovat käyttäneet runsaasti immunosuppressiivisia hoitoja, sekä PUVA-hoitoa saaneita psoriaasipotilaita. TNF-salpaajia, kuten adalimumabia, saaneilla potilailla on ilmoitettu esiintyneen myös melanoomaa ja merkelinsolukarsinoomaa (ks. kohta Haittavaikutukset).
Eksploratiivisessa kliinisessä tutkimuksessa, jossa arvioitiin erään toisen TNF-salpaajan, infliksimabin, käyttöä potilailla, joilla oli keskivaikea tai vaikea keuhkoahtaumatauti, infliksimabihoitoa saaneilla potilailla ilmoitettiin enemmän maligniteetteja etenkin keuhkojen, pään ja kaulan alueella kuin verrokkipotilailla. Kaikki potilaat olivat aiemmin tupakoineet runsaasti. Tämän vuoksi varovaisuutta on noudatettava, kun keuhkoahtaumatautipotilaita hoidetaan millä tahansa TNF-salpaajalla, samoin kuin potilailla, joiden maligniteettiriski on suurentunut runsaan tupakoinnin vuoksi.
Tämänhetkisten tietojen perusteella ei tiedetä, vaikuttaako adalimumabihoito dysplasian tai paksusuolen syövän kehittymisen riskiin. Kaikki ulseratiivista koliittia sairastavat potilaat, joilla on lisääntynyt riski dysplasiaan tai paksusuolen syöpään (esimerkiksi potilaat, joilla on pitkäaikainen ulseratiivinen koliitti tai primaarinen sklerosoiva kolangiitti), tai potilaat, joilla on aiemmin ollut dysplasia tai paksusuolen syöpä, tulee seuloa dysplasian varalta säännöllisin väliajoin ennen hoidon aloitusta ja hoidon aikana. Seulonnan tulisi sisältää kolonoskopia ja biopsia paikallisten suositusten mukaisesti.
Verenkuvamuutokset
Pansytopeniaa, mukaan lukien aplastista anemiaa, on ilmoitettu harvinaisissa tapauksissa TNF-salpaajien käytön yhteydessä. Hematologiseen järjestelmään kohdistuvia haittavaikutuksia, kuten lääketieteellisesti merkitsevää sytopeniaa (esim. trombosytopenia, leukopenia), on ilmoitettu adalimumabihoidon yhteydessä. Kaikkia potilaita tulee kehottaa hakeutumaan välittömästi lääkärin hoitoon, jos heille kehittyy Yuflyma-hoidon aikana verenkuvamuutoksiin viittaavia merkkejä ja oireita (esim. sitkeä kuume, mustelmanmuodostus, verenvuoto, kalpeus). Yuflyma-hoidon keskeyttämistä tulee harkita, jos potilaalla todetaan merkitseviä hematologisia poikkeavuuksia.
Rokotteet
Kun 226 aikuista nivelreumapotilasta sai adalimumabi- tai pleasbohoitoa, havaitut vasta-ainevasteet tavanomaiselle 23-valentille pneumokokkirokotteelle ja trivalentille influenssavirusrokotteelle olivat samankaltaiset. Elävien rokotteiden aiheuttamista infektioiden sekundaarisista siirtymistä ei ole tietoa adalimumabihoitoa saaneilla potilailla.
Kaikkien lapsipotilaiden kohdalla on suositeltavaa varmistaa mahdollisuuksien mukaan, että potilas saa kaikki ajankohtaisten rokotussuositusten mukaiset rokotukset ennen Yuflyma-hoidon aloittamista.
Potilaille voidaan antaa rokotuksia Yuflyma-hoidon aikana eläviä rokotteita lukuun ottamatta. Elävien rokotteiden (esim. BCG-rokotteen) antamista imeväisille, jotka ovat altistuneet adalimumabille in utero, ei suositella 5 kuukauteen äidin viimeisestä raskaudenaikaisesta adalimumabi-injektiosta.
Kongestiivinen sydämen vajaatoiminta
Erästä toista TNF-salpaajaa koskevassa kliinisessä tutkimuksessa havaittiin kongestiivisen sydämen vajaatoiminnan pahenemista ja kongestiivisesta sydämen vajaatoiminnasta johtuvan kuolleisuuden lisääntymistä. Myös adalimumabihoidon aikana on raportoitu kongestiivisen sydämen vajaatoiminnan pahenemista. Yuflyman käytössä on noudatettava varovaisuutta potilailla, joilla on lievä sydämen vajaatoiminta (NYHA I/II). Keskivaikea ja vaikea sydämen vajaatoiminta ovat Yuflyman käytön vasta-aiheita (ks. kohta Vasta-aiheet). Yuflyma-hoito tulee keskeyttää, jos potilaalle tulee kongestiivisen sydämen vajaatoiminnan oireita tai jos oireet pahenevat.
Autoimmuuniprosessit
Yuflyma-hoito voi johtaa autovasta-aineiden muodostukseen. Pitkäaikaisen adalimumabihoidon vaikutusta autoimmuunisairauksien kehittymiseen ei tunneta. Jos potilaalle kehittyy lupuksen kaltaiseen oireyhtymään viittaavia oireita Yuflyma-hoidon jälkeen ja hänellä todetaan vasta-aineita kaksijuosteiselle DNA:lle, Yuflyma-hoitoa ei tule jatkaa (ks. kohta Haittavaikutukset).
Samanaikainen biologisten DMARDien tai TNF-salpaajien antaminen
Kliinisissä tutkimuksissa anakinran ja toisen TNF-salpaajan, etanerseptin, yhteiskäytössä
todettiin vakavia infektioita, eikä yhteiskäytöstä ollut lisääntynyttä kliinistä hyötyä verrattuna etanerseptin antamiseen yksinään. Etanerseptin ja anakinran yhteiskäytössä havaittujen haittatapahtumien luonteen vuoksi samankaltainen toksisuus on mahdollista myös anakinran ja muiden TNF-salpaajien yhteiskäytössä. Siksi adalimumabin ja anakinran yhteiskäyttöä ei suositella (ks. kohta Yhteisvaikutukset).
Adalimumabin ja muiden biologisten DMARDien (kuten anakinra ja abatasepti) tai muiden TNF-salpaajien samanaikaista antoa ei suositella perustuen infektioiden mahdollisesti lisääntyneeseen riskiin, mukaan lukien vakavat infektiot ja muut farmakologiset yhteisvaikutukset (ks. kohta Yhteisvaikutukset).
Leikkaus
Turvallisuustiedot adalimumabilla hoidettujen potilaiden leikkaushoidoista ovat rajalliset. Leikkausta suunniteltaessa on otettava huomioon adalimumabin pitkä puoliintumisaika. Leikkaushoitoa vaatineen Yuflyma-potilaan infektioita on tarkkaan seurattava, ja asianmukaisiin toimenpiteisiin on tarvittaessa ryhdyttävä. Turvallisuustiedot artroplastiahoitoa vaativien adalimumabipotilaiden hoidosta ovat rajalliset.
Ohutsuolitukos
Jos Crohnin tauti ei reagoi hoitoon, potilaalla saattaa olla kiinteä fibroottinen striktuura, joka saattaa vaatia leikkaushoitoa. Nykyisten tietojen perusteella adalimumabi ei pahenna striktuuroita eikä aiheuta niitä.
Iäkkäät potilaat
Vakavien infektioiden esiintyvyys oli korkeampi yli 65-vuotiailla potilailla (3,7 %), joita hoidettiin adalimumabilla, kuin alle 65-vuotiailla (1,5 %). Jotkin näistä infektioista olivat fataaleja. Iäkkäitä potilaita hoidettaessa tulee erityisesti ottaa huomioon infektioriski.
Lapsipotilaat
Katso yllä oleva Rokotukset-kohta.
Natriumpitoisuus
Tämä lääkevalmiste sisältää alle 1 mmol natriumia (23 mg) per 0,8 ml annos eli sen voidaan sanoa olevan ”natriumiton”.
Yhteisvaikutukset
Adalimumabia on tutkittu nivelreumaa, polyartikulaarista juveniilia idiopaattista artriittia ja nivelpsoriaasia sairastavilla potilailla sekä yksinään että metotreksaattiin yhdistettynä. Vasta-ainemuodostus oli vähäisempää metotreksaatin kanssa annettuna kuin yksinään. Adalimumabin käyttö ilman metotreksaattia lisäsi vasta-ainemuodostusta, tehosti adalimumabin puhdistumaa ja heikensi sen tehoa (ks. kohta Farmakodynamiikka).
Adalimumabin ja anakinran yhdistämistä ei suositella (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet "Samanaikainen biologisten DMARDien tai TNF-salpaajien antaminen").
Adalimumabin ja abataseptin yhdistämistä ei suositella (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet "Samanaikainen biologisten DMARDien tai TNF-salpaajien antaminen").
Raskaus ja imetys
Naiset, jotka voivat tulla raskaaksi
Naisten, jotka voivat tulla raskaaksi, on harkittava riittävää raskauden ehkäisyä Yuflyma-hoidon aikana ja vähintään viiden kuukauden ajan viimeisen Yuflyma-annoksen jälkeen.
Raskaus
Laajat tiedot eivät viittaa epämuodostumien lisääntymiseen vastasyntyneillä. Tiedot kerättiin prospektiivisesti noin 2 100 raskaudesta, joiden aikana oli tapahtunut adalimumabialtistus ja jotka olivat johtaneet elävän lapsen syntymään tiedossa olevin lopputuloksin (mukaan lukien tiedot yli 1 500:sta ensimmäisen raskauskolmanneksen aikana tapahtuneesta altistuksesta).
Prospektiivisessa kohorttirekisterissä oli mukana 257 naista, joilla oli nivelreuma tai Crohnin tauti ja jotka saivat adalimumabia vähintään ensimmäisellä raskauskolmanneksella, ja 120 naista, joilla oli nivelreuma tai Crohnin tauti ja jotka eivät saaneet adalimumabia. Ensisijainen päätetapahtuma oli merkittävien synnynnäisten kehityshäiriöiden esiintyvyys syntymähetkellä. Vähintään yhden elävän, merkittävästi kehityshäiriöisen lapsen syntymään johtaneiden raskauksien osuus oli adalimumabihoitoa saaneilla nivelreumaa sairastavilla naisilla 6/69 (8,7 %) ja hoitamattomilla nivelreumaa sairastavilla naisilla 5/74 (6,8 %) (korjaamaton vetosuhde 1,31; 95 % luottamusväli [lv] 0,38–4,52). Adalimumabihoitoa saaneilla Crohnin tautia sairastavilla naisilla vastaava osuus oli 16/152 (10,5 %) ja hoitamattomilla Crohnin tautia sairastavilla naisilla 3/32 (9,4 %) (korjaamaton vetosuhde 1,14; 95 % lv 0,31–4,16). Korjattu vetosuhde (lähtötilanteen eroja koskeva) oli 1,10 (95 % lv 0,45–2,73), kun nivelreumaa ja Crohnin tautia koskevat tiedot yhdistettiin. Selviä eroja adalimumabihoitoa saaneiden ja hoitamattomien naisten välillä ei todettu toissijaisten päätetapahtumien kohdalla. Näitä olivat keskenmenot, vähäiset synnynnäiset kehityshäiriöt, ennenaikaiset synnytykset, syntymäkoko ja vakavat infektiot tai opportunistiset infektiot. Kohtukuolemia ja maligniteetteja ei ilmoitettu. Tutkimuksen metodologiset rajoitukset, mm. pieni otoskoko ja satunnaistamaton tutkimusasetelma, saattavat vaikuttaa tietojen tulkintaan.
Apinoilla tehdyssä sikiökehityksen toksisuustutkimuksessa ei havaittu merkkejä emoon eikä alkioon kohdistuvasta toksisuudesta eikä teratogeenisuudesta. Adalimumabin postnataalitoksisista vaikutuksista ei ole prekliinistä tietoa (ks. kohta Prekliiniset tiedot turvallisuudesta).
Koska adalimumabi estää TNFα:aa, sen antaminen raskausaikana voi vaikuttaa vastasyntyneen normaaliin immuunivasteeseen. Adalimumabia saa käyttää raskausaikana vain, jos se on selvästi tarpeellista.
Adalimumabi voi läpäistä adalimumabihoitoa saavan naisen istukan ja päätyä sikiön verenkiertoon raskauden aikana. Tästä johtuen näillä imeväisillä voi olla syntymän jälkeen kohonnut infektioriski. Elävien rokotteiden (esim. BCG-rokotteen) antamista imeväisille, jotka ovat altistuneet adalimumabille in utero, ei suositella 5 kuukauteen äidin viimeisestä raskaudenaikaisesta adalimumabi-injektiosta.
Imetys
Julkaistusta kirjallisuudesta saadut suppeat tiedot viittaavat siihen, että adalimumabi erittyy hyvin pieninä pitoisuuksina ihmisen rintamaitoon ja sen pitoisuus ihmisen rintamaidossa on 0,1–1 % äidin seerumin adalimumabipitoisuudesta. Suun kautta annettuna immunoglobuliini G -proteiinit hajoavat suolistossa proteolyysin kautta, ja niiden biologinen hyötyosuus on pieni. Ei ole odotettavissa vaikutuksia vastasyntyneisiin/imeväisiin. Näin ollen Yuflymaa voi käyttää imetyksen aikana.
Hedelmällisyys
Prekliinistä tietoa adalimumabin vaikutuksista hedelmällisyyteen ei ole saatavilla.
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Yuflymalla saattaa olla vähäinen vaikutus ajokykyyn ja koneiden käyttökykyyn. Yuflyman ottamisen jälkeen saattaa esiintyä kiertohuimausta ja näön heikkenemistä (ks. kohta Haittavaikutukset).
Haittavaikutukset
Turvallisuusprofiilin yhteenveto
Adalimumabia on tutkittu tärkeimmissä kontrolloiduissa ja avoimissa tutkimuksissa 9 506 potilaalla jopa 60 kuukauden ajan tai yli. Näihin tutkimuksiin osallistui nivelreumapotilaita, joiden tauti oli kestänyt lyhyen tai pitkän aikaa, sekä juveniilia idiopaattista artriittia (polyartikulaarista juveniilia idiopaattista artriittia ja entesiitteihin liittyvää artriittia), aksiaalista spondylartriittia (selkärankareumaa ja aksiaalista spondylartriittia (ilman radiografista näyttöä selkärankareumasta)), nivelpsoriaasia, Crohnin tautia, ulseratiivista koliittia, psoriaasia, hidradenitis suppurativaa ja uveiittia sairastavia potilaita. Tärkeimmissä kontrolloiduissa tutkimuksissa 6 089 potilasta sai adalimumabia ja 3 801 potilasta sai plaseboa tai vaikuttavaa vertailuvalmistetta kontrolloidun vaiheen aikana.
Tärkeimmissä kontrolloiduissa kaksoissokkotutkimuksissa hoidon keskeytti haittatapahtumien vuoksi 5,9 % adalimumabia ja 5,4 % vertailuhoitoa saaneista potilaista.
Yleisimmin ilmoitettuja haittavaikutuksia ovat infektiot (esim. nenänielutulehdus, ylähengitystieinfektiot ja sinuiitti), pistoskohdan reaktiot (punoitus, kutina, verenvuoto, kipu tai turvotus), päänsärky ja tuki- ja liikuntaelimistön kipu.
Adalimumabihoidon yhteydessä on ilmoitettu vakavia haittavaikutuksia. TNF-salpaajat, kuten adalimumabi, vaikuttavat immuunijärjestelmään, ja niiden käyttö voi vaikuttaa elimistön kykyyn torjua infektioita ja syöpää.
Adalimumabin käytön yhteydessä on ilmoitettu kuolemaan johtaneita ja henkeä uhanneita infektioita (mm. sepsistä, opportunistisia infektioita ja tuberkuloosia), HBV-infektion reaktivaatiota ja eri syöpätauteja (mm. leukemiaa, lymfoomia ja hepatospleenistä T-solulymfoomaa).
Myös vakavia hematologisia, neurologisia ja autoimmuunireaktioita on ilmoitettu. Näistä pansytopeniaa, aplastista anemiaa ja keskus- ja ääreishermoston myeliinikatotapauksia on ilmoitettu harvoin. Myös lupusta, lupuksen kaltaisia oireistoja ja Stevens–Johnsonin oireyhtymää on ilmoitettu.
Lapsipotilaat
Lapsipotilailla todetut haittatapahtumat olivat yleisesti ottaen yleisyydeltään ja luonteeltaan samanlaisia kuin aikuispotilailla todetut haitat.
Haittavaikutustaulukko
Allaolevassa taulukossa 5 on lueteltu kliinisissä tutkimuksissa ja markkinoilletulon jälkeen esiintulleet haittatapahtumat, ja ne on jaoteltu elinryhmittäin ja esiintyvyyden perusteella: hyvin yleiset (≥ 1/10), yleiset (≥ 1/100 – < 1/10), melko harvinaiset (≥ 1/1 000 – < 1/100), harvinaiset (≥ 1/10 000 – < 1/1 000) sekä tuntematon (koska saatavissa oleva tieto ei riitä arviointiin). Kunkin yleisyysluokan haittavaikutukset on esitetty vakavuuden mukaisessa järjestyksessä vakavimmasta haittavaikutuksesta alkaen. Eri käyttöaiheiden tiedoista on valittu suurin yleisyysluku. Elinjärjestelmäsarakkeessa oleva tähti (*) tarkoittaa, että kohdissa Vasta-aiheet, Varoitukset ja käyttöön liittyvät varotoimet ja Haittavaikutukset on lisätietoa aiheesta.
Taulukko 5 Haittavaikutukset
Elinjärjestelmä | Yleisyys | Haittavaikutus |
Infektiot * | Hyvin yleiset | Hengitystieinfektiot (mm. ylä- ja alahengitystieinfektiot, keuhkokuume, sinuiitti, nielutulehdus, nenänielutulehdus ja herpesviruspneumonia) |
Yleiset | Systeemiset infektiot (mm. sepsis, kandidiaasi ja influenssa), suolistoinfektiot (mm. virusperäinen gastroenteriitti), iho- ja pehmytkudosinfektiot (mm. paronykia, selluliitti, märkärupi, nekrotisoiva faskiitti ja vyöruusu), korvainfektiot, suutulehdukset (mm. herpes simplex, huuliherpes ja hammasinfektiot), sukuelininfektiot (mm. vulvovaginan sieniinfektiot), virtsatieinfektiot (mukaan lukien pyelonefriitti), sieni-infektiot, nivelinfektiot | |
Melko harvinaiset | Hermostoinfektiot (mm. virusmeningiitti), opportunistiset infektiot ja tuberkuloosi (mm. koksidioidomykoosi, histoplasmoosi ja Mycobacterium avium -infektiot), bakteerien aiheuttamat infektiot, silmäinfektiot, divertikuliitti1) | |
Hyvän- ja pahanlaatuiset kasvaimet (mukaan lukien kystat ja polyypit)* | Yleiset | Ei-melanoomatyyppiset ihosyövät (mm. tyvisolusyöpä ja okasolusyöpä), hyvänlaatuinen kasvain |
Melko harvinaiset | Lymfooma**, kiinteät kasvaimet (mm. rintasyöpä, keuhkokasvaimet kilpirauhaskasvaimet), melanooma** | |
Harvinaiset | Leukemia1) | |
Tuntematon | Hepatospleeninen T- solulymfooma1), Merkelinsolukarsinooma (ihon neuroendokriininen karsinooma)1), Kaposin sarkooma | |
Veri ja imukudos* | Hyvin yleiset | Leukopenia (mukaan lukien neutropenia ja agranulosytoosi), anemia |
Yleiset | Leukosytoosi, trombosytopenia | |
Melko harvinaiset | Idiopaattinen trombosytopeeninen purppura | |
Harvinaiset | Pansytopenia | |
Immuunijärjestelmän häiriöt* | Yleiset | Yliherkkyys, allergiat (myös kausiallergiat) |
Melko harvinaiset | Sarkoidoosi1), vaskuliitti | |
Harvinaiset | Anafylaksia1) | |
Aineenvaihdunta ja ravitsemus | Hyvin yleiset | Kohonneet lipidiarvot |
Yleiset | Hypokalemia, kohonneet virtsahappoarvot, poikkeavat veren natriumarvot, hypokalsemia, hyperglykemia, hypofosfatemia, nestehukka | |
Psyykkiset häiriöt | Yleiset | Mielialanvaihtelut (mm. masennus), ahdistuneisuus, unettomuus |
Hermosto* | Erittäin yleiset | Päänsärky |
Yleiset | Parestesiat (mukaan lukien hypestesia), migreeni, hermojuuren kompressio | |
Melko harvinaiset | Aivohalvaus1), vapina, neuropatia | |
Harvinaiset | Multippeliskleroosi, myeliinikatohäiriöt (mm. optikusneuriitti, Guillain–Barrén oireyhymä)1) | |
Silmät | Yleiset | Näköhäiriö, sidekalvotulehdus, luomitulehdus, silmän turvotus |
Melko harvinaiset | Kaksoiskuvat | |
Kuulo- ja tasapainoelin | Yleiset | Kiertohuimaus |
Melko harvinaiset | Kuurous, tinnitus | |
Sydän* | Yleiset | Takykardia |
Melko harvinaiset | Sydäninfarkti1), rytmihäiriöt, kongestiivinen sydämen vajaatoiminta | |
Harvinaiset | Sydänpysähdys | |
Verisuonisto | Yleiset | Hypertensio, punastelu, hematooma |
Melko harvinaiset | Aortan aneurysma, valtimotukos, tromboflebiitti | |
Hengityselimet, rintakehä ja välikarsina* | Yleiset | Astma, hengenahdistus, yskä |
Melko harvinaiset | Keuhkoembolia1), interstitiaalinen keuhkosairaus, keuhkoahtaumatauti, pneumoniitti, pleuraeffuusio1) | |
Harvinaiset | Keuhkofibroosi1) | |
Ruoansulatuselimistö | Hyvin yleiset | Vatsakipu, pahoinvointi ja oksentelu |
Yleiset | Ruoansulatuskanavan verenvuoto, dyspepsia, ruokatorven refluksitauti, Sjögrenin oireyhtymä | |
Melko harvinaiset | Haimatulehdus, dysfagia, kasvojen turvotus | |
Harvinaiset | Suolen puhkeama1) | |
Maksa ja sappi* | Hyvin yleiset | Kohonneet maksaentsyymiarvot Kolekystiitti ja sappikivet, maksan rasvoittuminen, kohonneet bilirubiiniarvot |
Melko harvinaiset | ||
Harvinaiset | Hepatiitti, B-hepatiitin uudelleenaktivoituminen1) autoimmuunihepatiitti1) | |
Tuntematon | Maksan vajaatoiminta1) | |
Iho ja ihon alainen kudos | Hyvin yleiset | Ihottuma (mm. eksfoliatiivinen ihottuma) |
Yleiset | Psoriaasin paheneminen tai uusi puhkeaminen (mukaan lukien palmoplantaarinen pustulaarinen psoriaasi)1), nokkosihottuma, mustelmat (mm. purppura), ihotulehdus (mm. ekseema), kynsien murtuminen, voimakas hikoilu, alopesia 1), kutina | |
Melko harvinaiset | Öinen hikoilu, arpimuodostus | |
Harvinaiset | Erythema multiforme1), Stevens–Johnsonin oireyhtymä1), angioedeema1), ihon vaskuliitti1), likenoidi (punajäkälää muistuttava) ihoreaktio1) | |
Tuntematon | Dermatomyosiitin oireiden paheneminen1) | |
Luusto, lihakset ja sidekudos | Hyvin yleiset | Lihas- ja luukipu |
Yleiset | Lihasspasmit (mm. kohonneet veren kreatiini-fosfokinaasiarvot) | |
Melko harvinaiset | Rabdomyolyysi, systeeminen lupus erythematosus (SLE/LED) | |
Harvinaiset | Lupuksen kaltainen oireyhtymä1) | |
Munuaiset ja virtsatiet | Yleiset | Munuaisten vajaatoiminta, hematuria |
Melko harvinaiset | Nokturia | |
Sukupuolielimet ja rinnat | Melko harvinaiset | Erektiohäiriö |
Yleisoireet ja antopaikassa todettavat haitat* | Hyvin yleiset | Pistoskohdan reaktiot (mm. pistoskohdan punoitus) |
Yleiset | Rintakipu, turvotus, kuume1) | |
Melko harvinaiset | Inflammaatio | |
Tutkimukset* | Yleiset | Hyytymis- ja verenvuotohäiriöt (mm. APTT-ajan piteneminen), positiivinen tulos autovasta-ainetestissä (mm. kaksijuosteisen DNA:n vasta-aineet), kohonnut veren laktaattidehydrogenaasiarvot |
Tuntematon | Painonnousu2) | |
Vammat, myrkytykset ja toimenpidekomplikaatiot | Yleiset | Hidas paraneminen |
* lisätietoja on kohdissa Vasta-aiheet, Varoitukset ja käyttöön liittyvät varotoimet ja Haittavaikutukset
** mukaan lukien avoimet jatkotutkimukset
1) mukaan lukien spontaaniraportit
2) Adalimumabin yhteydessä keskimääräinen painon muutos lähtötilanteesta oli 0,3–1,0 kg aikuisten käyttöaiheissa, kun taas lumelääkettä käytettäessä paino laski tai nousi keskimäärin 0,4 kg 4–6 kuukauden pituisen hoitojakson aikana. Pitkäaikaisissa jatkotutkimuksissa, joissa ei ollut vertailuryhmää, on havaittu myös 5–6 kg:n painonnousua, kun potilaat ovat altistuneet lääkevalmisteelle noin 1–2 vuoden ajan. Tämä koskee erityisesti potilaita, joilla on Crohnin tauti ja haavainen paksusuolitulehdus. Mekanismi, johon tämä vaikutus perustuu, on epäselvä, mutta se voi liittyä adalimumabin tulehduksia estävään ja lievittävään vaikutukseen.
Hidradenitis suppurativa
Turvallisuusprofiili adalimumabia viikoittain saaneilla HS-potilailla oli yhdenmukainen adalimumabin tunnetun turvallisuusprofiilin kanssa.
Uveiitti
Turvallisuusprofiili adalimumabia joka toinen viikko saaneilla uveiittipotilailla oli yhdenmukainen adalimumabin tunnetun turvallisuusprofiilin kanssa.
Tiettyjen haittavaikutusten kuvaus
Pistoskohdan reaktiot
Tärkeimmissä kontrolloiduissa tutkimuksissa aikuisilla ja lapsilla pistoskohdan reaktioita (punoitus ja/tai kutina, verenvuoto, kipu tai turvotus) ilmeni 12,9 %:lla adalimumabia ja 7,2 %:lla plaseboa tai vaikuttavaa vertailuvalmistetta saaneista potilaista. Pistoskohdan reaktioiden yhteydessä ei lääkityksen keskeyttäminen yleensä ollut tarpeen.
Infektiot
Tärkeimmissä kontrolloiduissa tutkimuksissa aikuisilla ja lapsilla infektioiden esiintyvyys oli adalimumabia saaneilla 1,51 tapausta ja plaseboa tai vaikuttavaa vertailuvalmistetta saaneilla 1,46 tapausta potilasvuotta kohti. Valtaosa infektioista oli nenänielutulehduksia, ylähengitystieinfektioita ja nenän sivuontelotulehduksia (sinuiitti). Useimmat potilaat jatkoivat adalimumabilääkitystä infektion parannuttua.
Vakavien infektioiden esiintyvyys oli adalimumabia saaneilla 0,04 tapausta ja plaseboa tai vaikuttavaa vertailuvalmistetta saaneilla 0,03 tapausta potilasvuotta kohti.
Adalimumabilla tehdyissä kontrolloiduissa ja avoimissa tutkimuksissa aikuisilla ja lapsilla on ilmoitettu vakavia infektioita (myös kuolemaan johtaneita infektioita, joita esiintyi harvoin), esim. tuberkuloosia (esim. miliaarituberkuloosia ja keuhkojen ulkopuolella esiintyvää tuberkuloosia) ja invasiivisia opportunistisia infektioita (esim. disseminoitunutta tai keuhkojen ulkopuolella esiintyvää histoplasmoosia, blastomykoosia, koksidioidomykoosia, pneumokystoosia, kandidiaasia, aspergilloosia ja listerioosia). Valtaosa tuberkuloositapauksista kehittyi kahdeksan kuukauden kuluessa hoidon aloittamisesta, mikä saattaa viitata latentin sairauden uudelleenaktivoitumiseen.
Maligniteetit ja lymfoproliferatiiviset häiriöt
Juveniilia idiopaattista artriittiaa (polyartikulaarista juveniilia idiopaattista artriittia ja entesiitteihin liittyvää artriittia) koskeneissa adalimumabitutkimuksissa 249:llä lapsipotilaalla, joiden kokonaisaltistus oli 655,6 potilasvuotta, ei havaittu maligniteetteja. Maligniteetteja ei havaittu myöskään lasten Crohnin tautia koskeneissa adalimumabitutkimuksissa 192 lapsipotilaalla, joiden kokonaisaltistus oli 498,1 potilasvuotta. Maligniteetteja ei havaittu lasten kroonista läiskäpsoriaasia koskeneissa adalimumabitutkimuksissa 77 lapsipotilaalla, joiden kokonaisaltistus oli 80,0 potilasvuotta. Ulseratiivista koliittia koskeneessa adalimumabi-tutkimuksessa 93:lla pediatrisella potilaalla, joiden kokonaisaltistus oli 65,3 potilasvuotta, ei havaittu maligniteetteja. Maligniteetteja ei havaittu lasten uveiittia koskeneessa adalimumabitutkimuksessa 60 lapsipotilaalla, joiden kokonaisaltistus oli 58,4 potilasvuotta.
Tärkeimpiin vähintään 12 viikkoa kestäneisiin aikuisten adalimumabitutkimuksiin osallistui potilaita, joilla oli keskivaikea tai vaikea aktiivinen nivelreuma, selkärankareuma, aksiaalinen spondylartriitti (ilman radiografista näyttöä selkärankareumasta), nivelpsoriaasi, psoriaasi, hidradenitis suppurativa, Crohnin tauti, ulseratiivinen koliitti tai uveiitti. Näiden tutkimusten kontrolloiduissa osissa 5 291 adalimumabihoitoa saaneella potilaalla havaittiin 6,8 (95 % luottamusväli 4,4–10,5) maligniteettia (lukuun ottamatta lymfoomia ja muita ihosyöpiä kuin melanoomia) 1 000 potilasvuotta kohti, kun taas 3 444 verrokkipotilaalla todettiin 6,3 (95 % luottamusväli 3,4–11,8) tapausta 1 000 potilasvuotta kohti. Hoidon mediaanikesto oli 4,0 kk adalimumabiryhmässä ja 3,8 kk vertailuhoitoa saaneilla. Muiden ihosyöpien kuin melanooman esiintymistiheys oli adalimumabihoitoa saaneilla potilailla 8,8 (95 % luottamusväli 6,0–13,0) tapausta 1 000 potilasvuotta kohti ja verrokkipotilailla 3,2 (95 % luottamusväli 1,3–7,6) tapausta 1 000 potilasvuotta kohti. Näistä ihosyövistä levyepiteelikarsinoomien esiintymistiheys oli adalimumabihoitoa saaneilla potilailla 2,7 (95 % luottamusväli 1,4–5,4) tapausta 1 000 potilasvuotta kohti ja verrokkipotilailla 0,6 (95 % luottamusväli 0,1–4,5) tapausta 1 000 potilasvuotta kohti. Lymfoomien esiintymistiheys oli adalimumabihoitoa saaneilla potilailla 0,7 (95 % luottamusväli 0,2–2,7) tapausta 1 000 potilasvuotta kohti ja verrokkipotilailla 0,6 (95 % luottamusväli 0,1–4,5) tapausta 1 000 potilasvuotta kohti.
Näiden tutkimusten kontrolloitujen osien ja parhaillaan tehtävien sekä lopetettujen avointen jatkotutkimusten mediaanikesto on noin 3,3 vuotta, ja niihin on osallistunut 6 427 potilasta yhteensä yli 26 439 potilashoitovuoden ajan. Kun näiden tutkimusten tulokset yhdistetään, havaittujen maligniteettien esiintymistiheydeksi saadaan noin 8,5 tapausta 1 000 potilasvuotta kohti (lymfoomia ja muita ihosyöpiä kuin melanoomaa lukuun ottamatta). Muiden ihosyöpien kuin melanooman havaittu esiintymistiheys on noin 9,6 tapausta 1 000 potilasvuotta kohti, ja lymfoomien havaittu esiintymistiheys noin 1,3 tapausta 1 000 potilasvuotta kohti.
Markkinoille tulon jälkeen tammikuusta 2003 joulukuuhun 2010 pääasiassa nivelreumapotilailla ilmoitettujen maligniteettien esiintymistiheys on noin 2,7 tapausta 1 000 potilasvuotta kohti. Muiden ihosyöpien kuin melanooman ilmoitettu esiintymistiheys on noin 0,2 tapausta 1 000 potilasvuotta kohti, ja lymfoomien ilmoitettu esiintymistiheys noin 0,3 tapausta 1 000 potilashoitovuotta kohti (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Adalimumabilla hoidetuilla potilailla on markkinoille tulon jälkeen raportoitu harvoin hepatospleenistä T-solulymfoomaa (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Autovasta-aineet
Potilaiden seeruminäytteistä määritettiin nivelreumatutkimuksissa I–V autovasta-aineet useana ajankohtana. Näissä tutkimuksissa 11,9 %:lla adalimumabilla ja 8,1 %:lla plaseboa tai vaikuttavaa vertailuvalmistetta saaneista potilaista lähtötason negatiivinen tumavasta-ainetitteri muuttui positiiviseksi viikolla 24. Kaikissa nivelreuma- ja nivelpsoriaasitutkimuksissa kahdella 3 441:stä adalimumabia saaneesta potilaasta havaittiin kliinisiä merkkejä lupuksen kaltaisen oireiston uudesta kehittymisestä. Tila korjaantui hoidon keskeyttämisen jälkeen. Yhdellekään potilaalle ei kuitenkaan tullut lupuksesta johtuvaa nefriittiä eikä keskushermosto-oireita.
Maksa- ja sappitapahtumat
Nivelreuma- ja nivelpsoriaasipotilailla tehdyissä kontrolloiduissa vaiheen 3 adalimumabitutkimuksissa, joiden kontrolloidun osan kesto oli 4–104 viikkoa, ALAT-arvon suurenemista ≥ 3 kertaa viitevälin ylärajan (ULN) suuruisiksi esiintyi 3,7 %:lla adalimumabihoitoa saaneista ja 1,6 %:lla vertailuhoitoa saaneista.
Polyartikulaarista juveniilia idiopaattista artriittia sairastavilla 4–17-vuotiailla potilailla ja entesiitteihin liittyvää artriittia sairastavilla 6–17-vuotiailla potilailla tehdyissä kontrolloiduissa vaiheen 3 adalimumabitutkimuksissa ALAT-arvon suurenemista tasolle ≥ 3 x ULN esiintyi 6,1 %:lla adalimumabihoitoa saaneista ja 1,3 %:lla vertailuhoitoa saaneista. ALAT-tason suurenemisista useimmat havaittiin potilailla, jotka käyttivät samanaikaisesti myös metotreksaattia. Kenelläkään vaiheen 3 adalimumabitutkimukseen osallistuneista polyartikulaarista juveniilia idiopaattista artriittia sairastavista 2–<4 -vuotiaista potilaista ei esiintynyt ALAT-tason suurenemista tasolle ≥ 3 x ULN.
Crohnin tautia tai ulseratiivista koliittia sairastavilla potilailla tehdyissä kontrolloiduissa vaiheen 3 adalimumabitutkimuksissa, joiden kontrolloidun osan kesto oli 4–52 viikkoa. ALAT-tason suurenemista tasolle 3 x ULN esiintyi 0,9 %:lla adalimumabihoitoa saaneista ja 0,9 %:lla verrokkihoitoa saaneista.
Crohnin tautia sairastavilla lapsipotilailla tehdyssä vaiheen 3 adalimumabitutkimuksessa, jossa selvitettiin kahden painonmukaisen induktiohoidon jälkeisen ylläpitoannoksen tehoa ja turvallisuutta potilailla 52 viikkoa kestäneen hoidon ajan, ALAT-arvojen suurenemista tasolle ≥ 3 x ULN esiintyi 2,6 %:lla (5/192) potilaista. Näistä potilaista 4 oli saanut samanaikaista immonosupressiivista hoitoa lähtötilanteessa.
Läiskäpsoriaasipotilailla tehdyissä kontrolloiduissa vaiheen 3 alimumabitutkimuksissa, joiden kontrolloidun osan kesto oli 12–24 viikkoa, ALAT-arvon suurenemista tasolle ≥ 3 x ULN esiintyi 1,8 %:lla alimumabihoitoa saaneista ja 1,8 %:lla vertailuhoitoa saaneista.
Kenelläkään vaiheen 3 adalimumabitutkimukseen osallistuneista läiskäpsoriaasia sairastaneista lapsipotilaista ei havaittu ALAT-arvon suurenemista tasolle ≥ 3 x ULN.
Hidradenitis suppurativaa sairastavilla potilailla tehdyissä kontrolloiduissa adalimumabitutkimuksissa (aloitusannos 160 mg viikolla 0 ja 80 mg viikolla 2, minkä jälkeen 40 mg kerran viikossa alkaen viikolta 4), joiden kontrolloidun osan kesto oli 12–16 viikkoa, ALAT-arvon suurenemista tasolle ≥ 3 x ULN esiintyi 0,3 %:lla adalimumabihoitoa saaneista ja 0,6 %:lla vertailuhoitoa saaneista.
Uveiittia sairastavilla potilailla tehdyissä kontrolloiduissa adalimumabitutkimuksissa (aloitusannos 80 mg viikolla 0, minkä jälkeen 40 mg kerran viikossa alkaen viikolta 1), joissa altistumisajan mediaani adalimumabihoitoa saaneilla potilailla oli 166,5 vuorokautta ja vertailuhoitoa saaneilla potilailla 105,0 vuorokautta, ALAT-arvon suurenemista tasolle ≥ 3 x ULN esiintyi 2,4 %:lla adalimumabihoitoa saaneista ja 2,4 %:lla vertailuhoitoa saaneista.
Ulseratiivista koliittia sairastavilla pediatrisilla potilailla (N = 93) tehdyssä kontrolloidussa vaiheen 3 tutkimuksessa, jossa arvioitiin adalimumabin tehoa ja turvallisuutta ylläpitoannoksella 0,6 mg/kg (enintään 40 mg) joka toinen viikko (N = 31) ja ylläpitoannoksella 0,6 mg/kg (enintään 40 mg) viikossa (N = 32) sen jälkeen, kun potilaat olivat saaneet painonmukaista induktiohoitoa annoksella 2,4 mg/kg (enintään 160 mg) viikolla 0 ja viikolla 1 sekä annoksella 1,2 mg/kg (enintään 80 mg) viikolla 2 (N = 63) tai induktiohoitoa annoksella 2,4 mg/kg (enintään 160 mg) viikolla 0, lumelääkettä viikolla 1 ja induktiohoitoa annoksella 1,2 mg/kg (enintään 80 mg) viikolla 2 (N = 30), ALAT-arvojen suurenemista tasolle ≥ 3 x ULN esiintyi 1,1 %:lla (1/93) potilaista.
Potilaat, joiden ALAT-arvot olivat koholla, olivat oireettomia, ja useimmissa tapauksissa ALAT-arvojen nousut olivat ohimeneviä ja korjaantuivat hoidon jatkuessa. Adalimumabilla hoidetuilla potilailla on kuitenkin markkinoilletulon jälkeen raportoitu myös maksan vajaatoimintaa ja lievempiä maksan häiriöitä, jotka saattavat edeltää maksan vajaatoimintaa, mm. hepatiittia (myös autoimmuunihepatiittia).
Samanaikainen hoito atsatiopriinilla/6-merkaptopuriinilla
Aikuisten Crohnin tautia käsittelevissä tutkimuksissa pahanlaatuisten ja vakavien infektioihin liittyvien haittatapahtumien ilmaantuvuus oli suurempi käytettäessä adalimumabia ja atsatiopriinin/6-merkaptopuriinin yhdistelmähoitoa verrattuna pelkkään adalimumabiin.
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55 00034
FIMEA
Yliannostus
Annosta rajoittavaa toksisuutta ei havaittu kliinisissä tutkimuksissa. Suurin tutkittu annos on 10 mg/kg laskimonsisäisesti useana annoksena, mikä on noin 15 kertaa suositusannoksen verran.
Farmakologiset ominaisuudet
Farmakodynamiikka
5.1 Farmakologiset ominaisuudet
Farmakoterapeuttinen ryhmä: Immunosuppressantit, tuumorinekroositekijä alfan (TNF-α) estäjät. ATC-koodi: L04AB04
Yuflyma on biosimilaari lääkevalmiste. Yksityiskohtaisempaa tietoa on saatavilla Euroopan lääkeviraston kotisivuilta http://www.ema.europa.eu.
Vaikutusmekanismi
Adalimumabi sitoutuu spesifisesti tuumorinekroositekijään (TNF) ja neutraloi TNF:n biologisen toiminnan estämällä sen vaikutuksen solukalvon TNF-reseptoreihin (p55 ja p75).
Adalimumabi säätelee myös TNF:n indusoimia tai säätelemiä biologisia vasteita, mm. leukosyyttien migraatiosta vastaavien adheesiomolekyylien määrän muutoksia (ELAM-1, VCAM-1 ja ICAM-1, joilla IC50 on 0,1–0,2 nM).
Farmakodynaamiset vaikutukset
Adalimumabihoidon jälkeen todettiin, että nivelreumapotilailla tulehduksen akuutin vaiheen osoittajien (C-reaktiivinen proteiini ja lasko) ja seerumin sytokiinien (IL-6) määrät pienenivät lähtötasoon verrattuna nopeasti. Myös rustotuhoa aiheuttavaa kudosten uudismuodostusta tuottavien matriksin metalloproteinaasientsyymien (MMP-1 ja MMP-3) pitoisuudet seerumissa pienenivät adalimumabin antamisen jälkeen. Adalimumabia saaneilla potilailla havaittiin usein kroonisen tulehduksen hematologisten merkkien parantumista.
Adalimumabia käyttävillä polyartikulaarista juveniilia idiopaattista artriittia, Crohnin tautia, ulseratiivista koliittia ja hidradenitis suppurativaa sairastavilla potilailla todettiin myös CRP-arvojen pienenevän nopeasti. Crohnin tauti -potilailla havaittiin tulehdusmarkkereita ilmentävien solujen määrän väheneminen paksusuolessa, mukaan lukien TNFα:n ilmentymisen merkittävä väheneminen. Suolen limakalvon endoskooppiset tutkimukset ovat osoittaneet limakalvon paranemista tapahtuvan adalimumabilla hoidetuilla potilailla.
Kliininen teho ja turvallisuus
Nivelreuma
Adalimumabia on kliinisissä tutkimuksissa arvioitu yhteensä yli 3 000:lla nivelreumapotilaalla. Adalimumabin tehoa ja turvallisuutta nivelreuman hoidossa on arvioitu viidessä satunnaistetussa, hyvin kontrolloidussa kaksoissokkotutkimuksessa. Osa potilaista sai hoitoa 120 kuukauden ajan. Adalimumabi 40 mg / 0,4 ml -valmisteen aiheuttamaa pistoskohdan kipua arvioitiin kahdessa satunnaistetussa, yksöissokkoutetussa kaksijaksoisessa vaihtovuoroisessa tutkimuksessa, jossa käytettiin verrokkina vaikuttavaa valmistetta.
Nivelreumatutkimuksessa I arvioitiin 271 vähintään 18-vuotiasta kohtalaisen aktiivista tai hyvin aktiivista nivelreumaa sairastavaa potilasta, joilla hoito vähintään yhdellä taudin kulkuun vaikuttavalla reumalääkkeillä oli epäonnistunut ja joilla metotreksaatti ei ollut riittävän tehokas annostasolla 12,5–25 mg/ vko (10 mg/vko, jos potilas ei siedä metotreksaattia) annoksen pysyessä vakiona 10–25 mg/vko. Adalimumabia tai plaseboa annettiin 20, 40 tai 80 mg:n annoksina joka toinen viikko 24 viikon ajan.
Nivelreumatutkimuksessa II arvioitiin 544 vähintään 18-vuotiasta keskivaikeaa tai vaikeaa aktiivista nivelreumaa sairastavaa potilasta, joilla hoito vähintään yhdellä taudin kulkuun vaikuttavalla reumalääkkeellä oli epäonnistunut. Adalimumabia annettiin ihonalaisina injektioina 20 tai 40 mg:n annoksina siten, että adalimumabia annettiin yksinään joko viikoittain tai vuoroviikoin plasebon kanssa 26 viikon ajan; plaseboa annettiin viikoittain samanmittaisen ajanjakson verran. Muiden taudin kulkuun vaikuttavien reumalääkkeiden käyttö ei ollut sallittua.
Nivelreumatutkimuksessa III arvioitiin 619 vähintään 18-vuotiasta keskivaikeaa tai vaikeaa aktiivista nivelreumaa sairastavaa potilasta, joilla metotreksaattihoito ei ollut riittävän tehokas annostasolla 12,5–25 mg/vko tai jotka eivät sietäneet 10 mg/vko annoksia metotreksaattia. Tutkimuksessa oli kolme ryhmää. Ensimmäinen ryhmä sai plaseboa viikoittain pistoksena 52 viikon ajan. Toinen ryhmä sai 20 mg adalimumabia viikoittain 52 viikon ajan. Kolmas ryhmä sai vuoroviikoin 40 mg adalimumabia ja vuoroviikoin plaseboa. Ensimmäisen 52 viikon jälkeen 457 potilasta siirrettiin avoimeen jatkovaiheeseen, jossa annettiin 40 mg adalimumabia/metotreksaattia joka toinen viikko enintään 10 vuoden ajan.
Nivelreumatutkimuksessa IV arvioitiin ensisijaisesti turvallisuutta 636 vähintään 18-vuotiaalla keskivaikeaa tai vaikeaa aktiivista nivelreumaa sairastavalla potilaalla. Potilailla ei ollut aikaisempaa taudin kulkuun vaikuttavaa reumalääkitystä tai he saivat jatkaa nykyistä reumalääkitystään, kunhan hoito pysyi samana vähintään 28 päivän ajan. Lääkitys oli metotreksaatti, leflunomidi, hydroksiklorokiini, sulfasalatsiini ja/tai kultasuolat. Potilaat satunnaistettiin saamaan joko 40 mg adalimumabia tai plaseboa joka toinen viikko 24 viikon ajan.
Nivelreumatutkimuksessa V arvioitiin 799 aikuispotilasta, joilla oli keskivaikea tai vaikea aktiivinen varhaisvaiheen nivelreuma (taudin kesto keskimäärin alle 9 kuukautta) ja jotka eivät olleet saaneet aiemmin metotreksaattihoitoa. Tässä tutkimuksessa arvioitiin eri hoitojen tehoa nivelvaurioiden oireiden ja löydösten vähenemisen sekä nivelvaurioiden etenemisen hidastumisen suhteen nivelreumapotilailla 104 viikon aikana, ja tutkittavat hoidot olivat: adalimumabi 40 mg joka toinen viikko yhdistelmänä metotreksaatin kanssa, adalimumabi 40 mg joka toinen viikko monoterapiana ja metotreksaatti monoterapiana. Ensimmäisen 104 viikon jälkeen 497 potilasta siirrettiin avoimeen jatkovaiheeseen, jossa annettiin 40 mg adalimumabia/metotreksaattia joka toinen viikko enintään 10 vuoden ajan.
Nivelreumatutkimuksissa VI ja VII arvioitiin molemmissa 60 keskivaikeaa tai vaikeaa aktiivista nivelreumaa sairastavaa vähintään 18-vuotiasta potilasta. Tutkimukseen osallistuneet potilaat olivat joko nykyisiä 40 mg/0,8 ml adalimumabin käyttäjiä ja arvioivat keskimääräisen pistoskohdan kivun olevan vähintään 3 cm (0–10 cm VAS-asteikolla) tai he eivät olleet aiemmin saaneet biologista lääkitystä ja olivat aloittamassa adalimumabi 40 mg/0,8 ml -valmisteen käytön. Potilaat satunnaistettiin saamaan ensin kerta-annos joko adalimumabia 40 mg/0,8 ml tai adalimumabi 40 mg/0,4 ml -valmistetta. Seuraavalla pistoskerralla potilaalle annettiin toista valmistetta kuin mitä hän oli saanut ensimmäisellä kerralla.
Ensisijainen päätetapahtuma nivelreumatutkimuksissa I, II ja III ja toissijainen päätetapahtuma nivelreumatutkimuksessa IV oli niiden potilaiden prosentuaalinen osuus, jotka saavuttivat ACR 20-vasteen viikolla 24 tai 26. Ensisijainen päätetapahtuma nivelreumatutkimuksessa V oli niiden potilaiden prosentuaalinen osuus, jotka saavuttivat ACR 50-vasteen viikolla 52. Ensisijaisena päätetapahtumana nivelreumatutkimuksissa III ja V oli lisäksi viikolla 52 todettu taudin etenemisen hidastuminen (röntgentutkimuksella todettuna). Ensisijaisena päätetapahtumana nivelreumatutkimuksessa III oli lisäksi elämänlaadussa tapahtunut muutos. Ensisijainen päätetapahtuma nivelreumatutkimuksissa VI ja VII oli pistoskohdan kipu välittömästi lääkkeenannon jälkeen VAS-asteikolla (0–10 cm) mitattuna.
ACR-vaste
Prosentuaaliset osuudet niistä adalimumabia saaneista potilasta, jotka saavuttivat ACR 20, 50 ja 70 -vasteet, olivat yhdenmukaiset nivelreumatutkimuksissa I, II ja III. Yhteenveto annostasolla 40 mg joka toinen viikko saaduista tuloksista on esitetty taulukossa 6.
Taulukko 6
ACR-vasteet plasebokontrolloiduissa tutkimuksissa
(prosenttia potilaista)
Vaste | RA study Ia** | RA study IIa** | RA study IIIa** | |||
Placebo/ MTXc n = 60 | Adalimumabib/ MTXc n = 63 | Placebo n = 110 | Adalimumabib n = 113 | Placebo/ MTXc n = 200 | Adalimumabib/ MTXc n = 207 | |
ACR 20 | ||||||
6 kuukautta | 13,3 % | 65,1 % | 19,1 % | 46,0 % | 29,5 % | 63,3 % |
12 kuukautta | Ei saatavilla | Ei saatavilla | Ei saatavilla | Ei saatavilla | 24,0 % | 58,9 % |
ACR 50 | ||||||
6 kuukautta | 6,7 % | 52,4 % | 8,2 % | 22,1 % | 9,5 % | 39,1 % |
12 kuukautta | Ei saatavilla | Ei saatavilla | Ei saatavilla | Ei saatavilla | 9,5 % | 41,5 % |
ACR 70 | ||||||
6 kuukautta | 3,3 % | 23,8 % | 1,8 % | 12,4 % | 2,5 % | 20,8 % |
12 kuukautta | Ei saatavilla | Ei saatavilla | Ei saatavilla | Ei saatavilla | 4,5 % | 23,2 % |
a Nivelreumatutkimus I viikolla 24, nivelreumatutkimus II viikolla 26 ja nivelreumatutkimus III viikoilla 24 ja 52
b 40 mg adalimumabia joka toinen viikko
c MTX = metotreksaatti
** p < 0,01, adalimumabi vs. plasebo
Nivelreumatutkimuksissa I-IV viikon 24 tai 26 kohdalla mitattu paraneminen kaikkien yksittäisten ACR- vastekriteerien osalta [aristavien ja turvonneiden nivelten lukumäärä, lääkärin ja potilaan arvio sairauden aktiivisuudesta ja kivusta, toimintakyky-indeksin (HAQ) pisteet ja CRP (mg/dl)] oli huomattavampaa kuin plaseboryhmässä. Nivelreumatutkimuksessa III tulokset säilyivät koko 52 viikon jakson ajan.
Nivelreumatutkimuksen III avoimessa jatkovaiheessa useimpien potilaiden ACR-vasteet säilyivät enintään 10 vuoden seurannassa. 207 potilaasta, jotka satunnaistettiin saamaan 40 mg adalimumabia joka toinen viikko, 114 potilasta jatkoi 40 mg adalimumabi-annosten käyttöä joka toinen viikko 5 vuoden ajan. Näistä 86 potilasta (75,4 %) saavutti ACR 20 -vasteen; 72 potilasta (63,2 %) saavutti ACR 50 -vasteen; ja 41 potilasta (36 %) ACR 70 -vasteen. 207 potilaasta 81 jatkoi 40 mg adalimumabiannosten käyttöä joka toinen viikko 10 vuoden ajan. Näistä 64 potilasta (79,0 %) saavutti ACR 20 -vasteen; 56 potilasta (69,1 %) saavutti ACR 50 -vasteen; ja 43 potilasta (53,1 %) ACR 70 -vasteen.
Nivelreumatutkimuksessa IV adalimumabia ja standardihoitoa saaneiden potilaiden ACR 20 -vaste oli tilastollisesti merkitsevästi parempi kuin plaseboa ja standardihoitoa saaneiden potilaiden (p < 0,001).
Nivelreumatutkimuksissa I–IV adalimumabia saaneet potilaat saavuttivat plaseboon verrattuna tilastollisesti merkitsevät ACR 20 ja 50 -vasteet jopa 1–2 viikon kuluttua hoidon aloittamisesta.
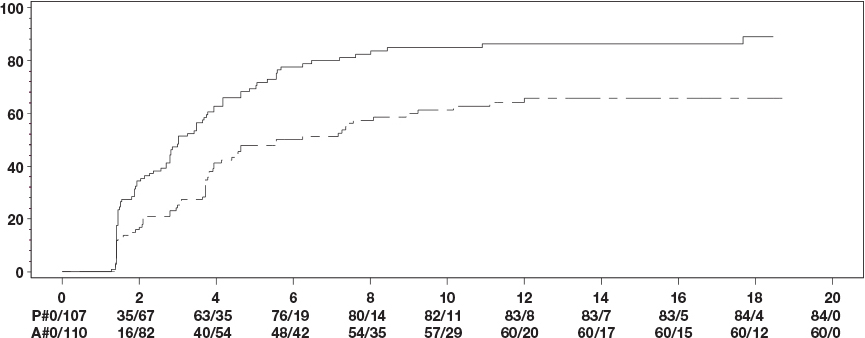
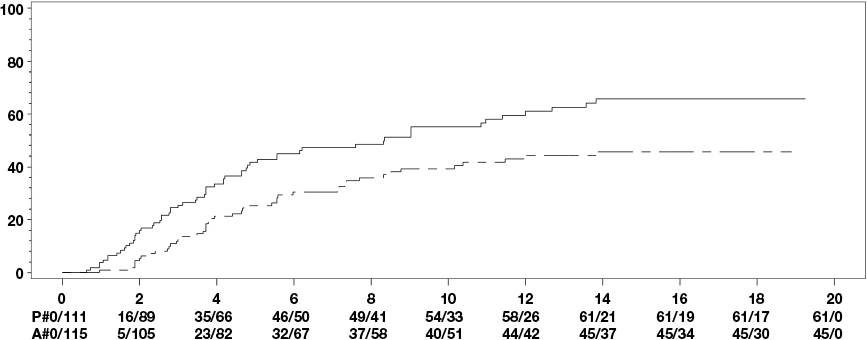
Nivelreumatutkimuksessa V varhaisilla nivelreumapotilailla, jotka eivät olleet aiemmin saaneet metotreksaattia, adalimumabin ja metotreksaatin yhdistelmähoito johti nopeampaan ja merkittävästi suurempaan ACR-vasteeseen kuin metotreksaatti- ja adalimumabimonoterapia viikolla 52 ja vasteet säilyivät viikolla 104 (katso taulukko 7).
Taulukko 7
ACR-vasteet nivelreumatutkimuksessa V
(prosenttia potilaista)
Vaste | Metotreksaatti n = 257 | Adalimumabi n = 274 | Adalimumabi/MTX n = 268 | p-arvo a | p-arvo b | p-arvo c |
ACR 20 | ||||||
Viikko 52 | 62,6 % | 54,4 % | 72,8 % | 0,013 | < 0,001 | 0,043 |
Viikko 104 | 56,0 % | 49,3 % | 69,4 % | 0,002 | < 0,001 | 0,140 |
ACR 50 | ||||||
Viikko 52 | 45,9 % | 41,2 % | 61,6 % | < 0,001 | < 0,001 | 0,317 |
Viikko 104 | 42,8 % | 36,9 % | 59,0 % | < 0,001 | < 0,001 | 0,162 |
ACR 70 | ||||||
Viikko 52 | 27,2 % | 25,9 % | 45,5 % | < 0,001 | < 0,001 | 0,656 |
Viikko 104 | 28,4 % | 28,1 % | 46,6 % | < 0,001 | < 0,001 | 0,864 |
a p-arvo on saatu metotreksaattimonoterapian ja adalimumabi/metotreksaattiyhdistelmähoidon parivertailusta Mann–Whitneyn U-testillä.
b p-arvo on saatu adalimumabimonoterapian ja adalimumabi/metotreksaattiyhdistelmähoidon parivertailusta Mann-Whitney U-testillä.
c p-arvo on saatu adalimumabimonoterapian ja metotreksaattimonoterapian parivertailusta Mann-Whitneyn U-testillä.
Nivelreumatutkimuksen V avoimessa jatkovaiheessa useimpien potilaiden ACR-vasteet säilyivät enintään 10 vuoden seurannassa. 542 potilaasta, jotka satunnaistettiin saamaan 40 mg adalimumabia joka toinen viikko, 170 potilasta jatkoi 40 mg adalimumabiannosten käyttöä joka toinen viikko 10 vuoden ajan. Näistä potilaista 154 (90,6 %) saavutti ACR 20 -vasteen, 127 potilasta (74,7 %) saavutti ACR 50 -vasteen ja 102 potilasta (60,0 %) ACR 70 -vasteen.
Viikolla 52 adalimumabin ja metotreksaatin yhdistelmähoitoa saaneista potilaista 42,9 %:llä saavutettiin kliininen remissio (DAS28 (CRP) < 2,6), kun vastaava luku oli pelkkää metotreksaattia saaneilla 20,6 % ja pelkkää adalimumabia saaneilla 23,4 %. Adalimumabin ja metotreksaatin yhdistelmähoito oli kliinisesti ja tilastollisesti parempi kuin pelkkä metotreksaatti (p<0,001) tai pelkkä adalimumabi (p 0,001) taudin lievittämisessä potilailla, joilla oli äskettäin diagnosoitu keskivaikea tai vaikea nivelreuma. Vasteet olivat samankaltaiset näissä kahdessa monoterapiaryhmässä (p = 0,447). 342:sta potilaasta, jotka oli alun perin satunnaistettu saamaan adalimumabia monoterapiana tai adalimumabin ja metotreksaatin yhdistelmähoitoa ja jotka jatkoivat avoimessa jatkotutkimuksessa, 171 jatkoi adalimumabihoitoa 10 vuotta. Heistä 109:n (63,7 %) raportoitiin olevan remissiossa 10 vuoden kohdalla.
Radiologinen vaste
Nivelreumatutkimuksessa III, jossa adalimumabia saavilla potilailla oli ollut nivelreuma noin 11 vuotta, rakenteelliset nivelvauriot arvioitiin röntgenkuvista ja ilmaistiin muutoksina modifioiduissa Sharpin (TSS) kokonaispisteissä ja sen komponenteissa, eroosiopisteissä ja nivelraon madaltumispisteissä. Adalimumabi/metotreksaattipotilailla todettiin 6 ja 12 kuukauden kohdalla merkitsevästi vähemmän etenemistä kuin pelkkää metotreksaattia saavilla potilailla (ks. taulukko 8).
Avoimen nivelreumatutkimuksen III jatkotutkimuksessa rakenteellisten vaurioiden etenemisnopeuden hidastuminen säilyy 8 ja 10 vuotta osalla potilaista. 8 vuoden kohdalla arvioitiin röntgenkuvista 81 potilasta 207 potilaasta, joita alun perin hoidettiin adalimumabilla (40 mg joka toinen viikko). 48 potilaalla näistä ei havaittu rakenteellisten vaurioiden etenemistä (määritelmä: mTSS arvon muutokset lähtötilanteesta 0,5 tai vähemmän). 10 vuoden kohdalla arvioitiin röntgenkuvista 79 potilasta 207 potilaasta, joita alun perin hoidettiin adalimumabilla (40 mg joka toinen viikko). 40:llä näistä potilaista ei todettu rakenteellisten vaurioiden etenemistä (määritelmä: mTSS-arvon muutos lähtötilanteesta enintään 0,5 pistettä).
Taulukko 8
Radiologiset keskiarvomuutokset 12 kuukauden aikana nivelreumatutkimuksessa III
Plasebo/ MTXa | Adalimumabi/MTX 40 mg joka toinen viikko | Plasebo/MTX-adalimumabi/MTX (95 % luottamusväli b) | p-arvo | |
Sharpen kokonaispisteet | 2,7 | 0,1 | 2,6 (1,4 ja 3,8) | < 0,001c |
Eroosioaste | 1,6 | 0,0 | 1,6 (0,9 ja 2,2) | < 0,001 |
JSNd-pisteet | 1,0 | 0,1 | 0,9 (0,3 ja 1,4) | 0,002 |
a metotreksaatti
b 95 % luottamusväli muutosasteen eroissa metotreksaatin ja adalimumabin välillä.
c Perustuu arviointianalyysiin
d Nivelraon kaventuminen
Nivelreumatutkimuksessa V rakenteelliset nivelvauriot arvioitiin röntgenkuvista ja ilmaistiin muutoksina modifioiduissa Sharpin kokonaispisteissä (ks. taulukko 9).
Taulukko 9
Radiologiset keskiarvomuutokset viikolla 52 nivelreumatutkimuksessa V
MTX n = 257 (95 % luottamusväli) | Adalimumabi n = 274 (95 % luottamusväli) | Adalimumabi/MTX n = 268 (95 % luottamusväli) | p-arvo a | p-arvo b | p-arvo c | |
Sharpen kokonaispisteet | 5,7 (4,2–7,3) | 3,0 (1,7–4,3) | 1,3 (0,5–2,1) | < 0,001 | 0,0020 | < 0,001 |
Eroosioaste | 3,7 (2,7–4,7) | 1,7 (1,0–2,4) | 0,8 (0,4–1,2) | < 0,001 | 0,0082 | < 0,001 |
JSN-pisteet | 2,0 (1,2–2,8) | 1,3 (0,5–2,1) | 0,5 (0–1,0) | < 0,001 | 0,0037 | 0,151 |
a p-arvo on saatu metotreksaattimonoterapian ja adalimumabi/metotreksaattiyhdistelmähoidon parivertailusta Mann–Whitneyn U-testillä.
b p-arvo on saatu adalimumabimonoterapian ja adalimumabi/metotreksaattiyhdistelmähoidon parivertailusta Mann-Whitney U-testillä.
c p-arvo on saatu adalimumabimonoterapian ja metotreksaattimonoterapian parivertailusta Mann-Whitneyn U-testillä.
52 ja 104 viikon hoidon jälkeen niiden potilaiden prosentuaalinen osuus, joilla tauti ei ollut edennyt (muutos lähtötilanteesta modifioiduissa Sharpin kokonaispisteissä vähintään 0,5) oli merkitsevästi suurempi potilailla, jotka olivat saaneet adalimumabi/metotreksaattiyhdistelmähoitoa (63,8 % ja 61,2 %) kuin potilailla, jotka olivat saaneet pelkkää metotreksaattia (37,4 % ja 33,5 %) tai pelkkää adalimumabia (50,7 %, p 0,002 ja 44,5 %, p 0,001).
Avoimessa nivelreuman jatkotutkimuksessa V keskimääräinen muutos lähtötilanteesta 10 vuoden kohdalla modifioiduissa Sharpin kokonaispisteissä oli alun perin metotreksaattimonoterapiaan satunnaistetuilla potilailla 10,8, adalimumabimonoterapiaan satunnaistetuilla potilailla 9,2 ja adalimumabi/metoreksaatti- yhdistelmähoitoon satunnaistetuilla potilailla 3,9. Vastaavat osuudet potilaista, joilla ei tapahtunut radiologista etenemistä, olivat 31,3 %, 23,7 % ja 36,7 %.
Elämänlaatu ja fyysinen toimintakyky
Terveyteen liittyvää elämänlaatua ja fyysistä toimintakykyä arvioitiin kaikissa neljässä asianmukaisessa ja hyvin kontrolloidussa tutkimuksessa toimintakykyindeksillä (HAQ), joka oli nivelreumatutkimuksessa III ennaltamääritelty ensisijainen päätetapahtuma viikolla 52. Kaikki adalimumabiannokset/-annostusohjelmat kaikissa neljässä tutkimuksessa osoittivat, että paraneminen mitattuna HAQ toimintakykyindeksillä lähtötasolta kuukaudelle 6 oli plaseboon verrattuna tilastollisesti merkitsevästi parempaa, ja nivelreumatutkimuksessa III havaittiin samaa viikolla 52. Short Form Health Survey (SF 36) -kyselyn tulokset adalimumabin kaikkien annosten/annostusohjelmien osalta tukevat näitä löydöksiä (mm. PCS-pisteet ja kipu- ja vitaliteettiosioiden pisteet annokselle 40 mg joka toinen viikko olivat tilastollisesti merkitseviä). FACIT-pisteet osoittavat, että väsymys väheni tilastollisesti merkitsevästi kaikissa niissä kolmessa tutkimuksessa, joissa sitä arvioitiin (nivelreumatutkimukset I, III ja IV).
Nivelreumatutkimuksessa III useimmilla potilailla, joiden fyysinen toimintakyky parani ja jotka jatkoivat hoitoa, paraneminen säilyi avoimen tutkimuksen viikkoon 520 asti (120 kuukautta). Elämänlaadun paraneminen mitattiin viikolle 156 (36 kuukautta) asti. Elämänlaadun paraneminen pysyi samalla tasolla koko tämän ajan.
Nivelreumatutkimuksessa V toimintakykyindeksin (HAQ) ja SF 36 -kyselyn fyysisen komponentin paraneminen oli merkittävämpää (p < 0,001) adalimumabi/metotreksaattiyhdistelmähoidon kuin pelkän metotreksaattihoidon tai pelkän adalimumabihoidon yhteydessä viikolla 52, ja vaikutus säilyi viikolle 104. Niillä 250:llä potilaalla, jotka olivat avoimessa jatkotutkimuksessa loppuun asti, fyysisessä toimintakyvyssä havaitut paranemiset säilyivät 10 hoitovuoden ajan.
Pistoskohdan kipu
Nivelreuman yhdistetyissä vaihtovuoroisissa tutkimuksissa VI ja VII havaittiin tilastollisesti merkitsevä ero välittömästi lääkkeenannon jälkeen havaitussa pistoskohdan kivussa valmisteiden adalimumabi 40 mg/0,8 ml ja adalimumabi 40 mg/0,4 ml välillä (VAS-keskiarvo 3,7 cm vs. 1,2 cm, asteikolla 0–10 cm, P < 0,001). Tämä vastasi 84 % mediaanivähenemää pistoskohdan kivussa.
Psoriaasi
Adalimumabin turvallisuutta ja tehoa tutkittiin aikuisilla potilailla, joilla oli krooninen läiskäpsoriaasi (≥ 10 % kehon pinta-alasta ja Psoriasis-alue ja vakavuusindeksi (PASI) ≥ 12 tai ≥ 10), jotka olivat ehdolla systeemiseen hoitoon tai valohoitoon satunnaistetussa, kaksoissokkoutetussa opinnot. 73 % psoriaasitutkimuksiin I ja II osallistuneista potilaista oli käyttänyt aiemmin systeemistä hoitoa tai valohoitoa. Adalimumabin turvallisuutta ja tehoa tutkittiin myös aikuisilla potilailla, joilla oli kohtalainen tai vaikea krooninen läiskäpsoriaasi ja samanaikainen käsi- ja/tai jalkapsoriaasi ja jotka olivat ehdolla systeemiselle hoidolle satunnaistetussa kaksoissokkoutetussa tutkimuksessa (Psoriaasitutkimus III).
Psoriaasitutkimuksessa I (REVEAL) arvioitiin 1 212 potilasta kolmen hoitojakson aikana. Potilaat saivat joko plaseboa tai adalimumabia (80 mg:n aloitusannos, jonka jälkeen 40 mg joka toinen viikko; ensimmäinen 40 mg:n annos otettiin viikon kuluttua aloitusannoksesta). 16 viikon hoidon jälkeen potilaat, jotka saavuttivat vähintään PASI 75 -vasteen (PASI-pistemäärän paraneminen vähintään 75 % lähtötasoon nähden), siirtyivät jaksoon B ja saivat avointa 40 mg adalimumabia joka toinen viikko. Potilaat, joiden ≥PASI 75 -vaste säilyi viikolla 33 ja satunnaistettiin alun perin aktiiviseen hoitoon jaksolla A, satunnaistettiin uudelleen jaksolla C saamaan 40 mg adalimumabia joka toinen viikko tai plaseboa vielä 19 viikon ajan. Kaikissa hoitoryhmissä lähtötilanteen PASI-indeksi oli keskimäärin 18,9 ja lääkärin yleisarvio (PGA) potilaan sairaudesta oli lähtötilanteessa “keskivaikea” (53 % tutkimushenkilöistä), “vaikea” (41 %) tai “hyvin vaikea” (6 %).
Psoriaasitutkimuksessa II (CHAMPION) adalimumabin tehoa ja turvallisuutta verrattiin metotreksaattiin ja plaseboon 271 potilaalla. Potilaat saivat plaseboa, metotreksaatin aloitusannos oli 7,5 mg ja sen jälkeen annosta nostetaan viikkoon 12 asti, maksimiannos oli 25 mg tai 80 mg:n aloitusannos adalimumabia ja sen jälkeen 40 mg joka toinen viikko (aloitettiin viikon kuluttua aloitusannoksesta) 16 viikon ajan. Adalimumabia ja metotreksaattia vertailevia tietoja 16 hoitoviikkoa pidemmältä ajalta ei ole. Metotreksaattiryhmässä potilaiden annosta ei enää nostettu, jos he saavutettivat ≥ PASI 50 - vasteen viikolla 8 ja/tai viikolla 12. Kaikissa hoitoryhmissä keskimääräinen lähtötason PASI-pistemäärä oli 19,7 ja lähtötilanteen PGA-pistemäärä vaihteli "lievästä" (<1 %) "kohtalaiseen" (48 %) "vakavaan" (46 %) "erittäin vakavaan" (6 %).
Kaikkiin vaiheen 2 ja vaiheen 3 psoriaasitutkimuksiin osallistuneet potilaat soveltuivat avoimeen jatkotutkimukseen, jossa adalimumabia annettiin vielä vähintään 108 viikon ajan.
Psoriaasitutkimusten I ja II ensisijainen päätetapahtuma oli niiden potilaiden osuus, jotka saavuttivat viikolla 16 PASI 75 -vasteen lähtötilanteeseen nähden (ks. taulukot 10 ja 11).
Taulukko 10
Psoriaasitutkimus I (REVEAL) – tehokkuustulokset 16 viikon kohdalla
Plasebo N = 398 n (%) | Adalimumabi 40 mg joka toinen viikko N = 814 n (%) | ||
≥ PASI 75a | 26 (6,5) | 578 (70,9) b | |
PASI 100 | 3 (0,8) | 163 (20,0) b | |
Lääkärin yleisarvio, PGA: Puhdas/melkein puhdas | 17 (4,3) | 506 (62,2) b | |
a PASI 75 -vasteen saavuttaneiden potilaiden prosenttiosuus laskettiin keskusten mukaan vakioituna b p < 0,001, adalimumabi vs. plasebo | |||
Taulukko 11
Psoriaasitutkimus II (CHAMPION) – tehokkuustulokset 16 viikon kohdalla
Plasebo N = 53 n (%) | Metotreksaatti n = 110 n (%) | Adalimumabi 40 mg joka toinen viikko N = 108 n (%) | |
≥ PASI 75 | 10 (18,9) | 39 (35,5) | 86 (79,6) a, b |
PASI 100 | 1 (1,9) | 8 (7,3) | 18 (16,7) c, d |
Lääkärin yleisarvio, PGA: Puhdas/melkein puhdas | 6 (11,3) | 33 (30,0) | 79 (73,1) a, b |
a p < 0,001, adalimumabi vs. plasebo b p <0,001 adalimumabi vs. metotreksaatti c p <0,01 adalimumabi vs. plasebo d p <0,05 adalimumabi vs. metotreksaatti | |||
Psoriaasitutkimuksessa I 28 % potilaista, jotka olivat PASI 75 -hoitovastetta saaneita ja jotka satunnaistettiin uudelleen plaseboon viikolla 33, verrattuna 5 %:iin adalimumabihoitoa jatkaneisiin potilaisiin, p < 0,001, kokivat "riittävän vasteen menetyksen" (PASI-pisteet viikon 33 jälkeen ja viikolla 52 tai ennen sitä suhteessa PASI 50 -vasteeseen lähtötasoon nähden ja PASI-pistemäärän nousun vähintään 6 yksiköllä viikkoon 33 verrattuna). 38 % (25/66) ja 55 % (36/66) niistä potilaista, jotka menettivät riittävän vasteen plasebohoitoon satunnaistamisen jälkeen, saavutti jälleen PASI 75 -vasteen 12 ja 24 hoitoviikon jälkeen.
Yhteensä 233 potilasta, jotka saavuttivat PASI 75 -hoitovasteen viikolla 16 ja viikolla 33, saivat jatkuvaa adalimumabihoitoa 52 viikon ajan psoriaasitutkimuksessa I ja jatkoivat adalimumabia avoimessa jatkotutkimuksessa. Näiden potilaiden PASI 75 ja lääkärin yleisarvio puhdas tai melkein puhdas -vasteet olivat 74,7 % ja 59,0 % ylimääräisten 108 viikkoa kestäneenna avoimen lisähoidon jälkeen (yhteensä 160 viikkoa). Analyysissa, jossa kaikki potilaat, jotka keskeyttivät tutkimuksen haittatapahtumien tai riittämättömän tehon vuoksi tai joiden annosta suurennettiin, luokiteltiin ilman vastetta jääneiksi potilaiksi, PASI 75 -vasteen sai 69,6 % potilaista ja 55,7 %:lla lääkärin yleisarvio oli puhdas tai melkein puhdas 108 viikon avoimen lisähoidon jälkeen (yhteensä 160 viikkoa).
Yhteensä 347 pysyvän vasteen saanutta potilasta osallistui hoidon lopettamista ja uusintahoitoa arvioivaan avoimeen jatkotutkimukseen. Lopettamisjakson aikana psoriaasioireet uusiutuivat ajan myötä, ja relapsiin (lääkärin yleisarvio huononi ”keskivaikeaksi” tai huonommaksi) kuluneen ajan mediaani oli noin 5 kuukautta. Yhdelläkään potilaista ei esiintynyt rebound-ilmiötä lopettamisjakson aikana. Yhteensä 76,5 %:lla (218/285) uusintajakson aloittaneista potilaista lääkärin yleisarvio oli puhdas tai melkein puhdas 16 uusintahoitoviikon kuluttua riippumatta siitä, esiintyikö relapseja lopettamisjakson aikana (69,1 %[123/178] potilaista, joilla oli relapsi lopettamisjakson aikana ja 88,8 % [95/107] potilaista, joilla ei ollut relapsia lopettamisjakson aikana). Uusintahoidon aikana turvallisuusprofiili oli samankaltainen kuin ennen hoidon lopettamista.
DLQI-elämänlaatumittarilla (Dermatology Life Quality Index) mitattuna potilaiden vointi koheni merkitsevästi viikkoon 16 mennessä lähtötilanteeseen nähden, kun tuloksia verrattiin plaseboon (tutkimukset I ja II) ja metotreksaattiin (tutkimus II). Tutkimuksessa I myös SF-36-mittarin fyysisten ja psyykkisten osioiden yhteispisteet paranivat merkitsevästi verrattuna plasebohoitoon.
Avoimessa jatkotutkimuksessa potilaille, joiden annos nousi 40 mg:sta joka toinen viikko 40 mg:aan viikossa PASI-vasteen laskettua lle 50 %:n, 26,4 % (92/349) ja 37,8 % (132/349) potilaista saavutti PASI 75 -vasteen viikolla 12 ja 24.
Psoriaasitutkimus III (REACH) vertasi adalimumabi- ja plasebohoidon tehoa ja turvallisuutta 72 potilaalla, joilla oli keskivaikea tai vaikea krooninen läiskäpsoriaasi ja käsi- ja/tai jalkapsoriaasi. Potilaat saivat 16 viikon ajan joko plaseboa tai adalimumabia aloitusannoksena 80 mg ja tämän jälkeen 40 mg joka toinen viikko (alkaen yksi viikko aloitusannoksen jälkeen). Viikolla 16 tilastollisesti merkittävästi suurempi osa adalimumabia saaneista potilaista saavutti käsien ja/tai jalkojen PGA-arvon puhdas tai melkein puhdas verrattuna plaseboa saaneisiin potilaisiin (vastaavasti 30,6 % vs. 4,3 % [P = 0,014]).
Psoriaasitutkimus IV vertasi adalimumabin ja plasebon tehoa ja turvallisuutta 217 aikuispotilaalla, joilla oli vaikea tai keskivaikea kynsipsoriaasi. Potilaat saivat 80 mg:n aloitusannoksen adalimumabia ja sen jälkeen 40 mg joka toinen viikko (aloittaen viikon aloitusannoksen jälkeen) tai plaseboa 26 viikon ajan, jota seurasi avoin adalimumabihoito vielä 26 viikkoa. Kynsipsoriaasia arvioitiin mNAPSI (Modified Nail Psoriasis Severity Index)-, PGA-F (Physician’s Global Assessment of Fingernail Psoriasis)- ja NAPSI (Nail Psoriasis Severity Index) -indekseillä (ks. taulukko 12). Adalimumabi osoitti hoidon hyödyn kynsipsoriaasipotilailla, joilla oli erilainen osuus kehon pinta-alasta (BSA≥ 10 % (60 % potilaista) ja BSA< 10 % ja ≥ 5 % (40 % potilaista)).
Taulukko 12
Psoriaasitutkimus IV tehokkuustulokset 16, 26 ja 52 viikon kohdalla
Päätetapahtuma | Viikko 16 | Viikko 26 | Viikko 52 | ||
Plasebokontrolloitu | Plasebokontrolloitu | Avoin | |||
Plasebo N = 108 | adalimumabi 40 mg joka toinen viikko N = 109 | Plasebo N = 108 | adalimumabi 40 mg joka toinen viikko N = 109 | adalimumabi 40 mg joka toinen viikko N = 80 | |
≥ mNAPSI 75 (%) | 2,9 | 26,0 a | 3,4 | 46,6a | 65,0 |
PGA-F puhdas/melkein puhdas ja ≥ 2-asteen parannus (%) | 2,9 | 29,7 a | 6,9 | 48,9a | 61,3 |
Prosentuaalinen muutos sormenkynsien kokonais-NAPSI-pistemäärässä (%) | -7,8 | -44,2 a | -11,5 | -56,2a | -72,2 |
a p < 0,001, adalimumabi vs.plasebo | |||||
Adalimumabihoitoa saaneilla potilailla elämänlaatu parani tilastollisesti merkitsevästi verrattuna plaseboa saaneisiin potilaisiin DLQI-elämänlaatumittarilla mitattuna 26 hoitoviikon kohdalla.
Hidradenitis suppurativa
Adalimumabin turvallisuutta ja tehoa arvioitiin satunnaistetuissa, kaksoissokkoutetuissa, plasebokontrolloiduissa tutkimuksissa ja avoimessa jatkotutkimuksessa keskivaikeaa tai vaikeaa hidradenitis suppurativaa (HS-tautia) sairastavilla aikuispotilailla, kun potilas ei sietänyt systeemistä antibioottihoitoa, kyseinen hoito oli vasta-aiheinen tai kyseisellä hoidolla ei saatu riittävää vastetta vähintään 3 kuukaudessa. HS‑I- ja HS-II-tutkimuksien potilailla oli Hurley-asteen II tai III tauti, johon liittyi vähintään 3 absessia tai tulehduksellista kyhmyä.
HS‑I-tutkimuksessa (PIONEER I) arvioitiin 307 potilasta kahden hoitojakson puitteissa. Kaudella A potilaat saivat plaseboa tai adalimumabia aloitusannoksena 160 mg viikolla 0, 80 mg viikolla 2 ja 40 mg joka viikko alkaen viikosta 4 viikkoon 11. Samanaikainen antibioottien käyttö ei ollut sallittua tutkimuksen aikana. 12 viikon hoidon jälkeen potilaat, jotka olivat saaneet adalimumabia jaksolla A, satunnaistettiin jaksolla B uudelleen yhteen kolmesta hoitoryhmästä (adalimumabi 40 mg joka viikko, adalimumabi 40 mg joka toinen viikko tai plasebo viikosta 12 viikkoon 35). Hoitojaksolla A plaseboryhmään satunnaistetut potilaat saivat hoitojaksolla B 40 mg adalimumabia kerran viikossa.
HS-II-tutkimuksessa (PIONEER II) arvioitiin 326 potilasta kahden hoitojakson puitteissa. Kaudella A potilaat saivat plaseboa tai adalimumabia aloitusannoksena 160 mg viikolla 0 ja 80 mg viikolla 2 ja 40 mg joka viikko viikosta 4 viikkoon 11 alkaen. 19,3 % potilaista jatkoi suun kautta otettavaa antibioottihoitoa tutkimuksen aikana. 12 viikon hoidon jälkeen potilaat, jotka olivat saaneet adalimumabia jaksolla A, satunnaistettiin jaksolla B uudelleen yhteen kolmesta hoitoryhmästä (adalimumabi 40 mg joka viikko, adalimumabi 40 mg joka toinen viikko tai plasebo viikosta 12 viikkoon 35). Hoitojaksolla A plaseboryhmään satunnaistetut potilaat saivat plasebohoitoa hoitojaksolla B.
HS-I- ja HS-II-tutkimuksiin osallistuneet potilaat soveltuivat avoimeen jatkotutkimukseen, jossa adalimumabia annettiin 40 mg kerran viikossa. Keskimääräinen altistumisaika kaikilla adalimumabia saaneilla oli 762 päivää. Potilaat käyttivät paikallisesti antiseptista ihohuuhdetta päivittäin kaikkien kolmen tutkimuksen ajan.
Kliininen vaste
Tulehduksellisten leesioiden vähenemistä ja absessien ja vuotavien fistelien pahenemisen ehkäisemistä arvioitiin HiSCR-vasteen avulla (Hidradenitis Suppurativa Clinical Response; absessien ja tulehduksellisten kyhmyjen kokonaismäärän pieneneminen vähintään 50 %:lla ilman absessien ja vuotavien fistelien määrän lisääntymistä suhteessa lähtötilanteeseen). HS-tautiin liittyvän ihokivun vähenemistä arvioitiin numeerisella arviointiasteikolla potilailla, joilla lähtötilanteen aloituspistemäärä oli tutkimukseenottohetkellä vähintään kolme (3) 11-portaisella asteikolla.
Merkitsevästi suurempi osuus adalimumabia saaneista potilaista saavutti HiSCR-vasteen viikon 12 kohdalla verrattuna plasebohoitoa saaneisiin. HS-II-tutkimuksessa merkitsevästi suuremmalla osalla potilaista HS-tautiin liittyvä ihokipu väheni kliinisesti merkitsevästi viikon 12 kohdalla (ks. taulukko 13). Adalimumabia saaneilla potilailla taudin pahenemisvaiheen riski oli merkitsevästi pienempi ensimmäisten 12 hoitoviikon aikana.
Taulukko 13
Tehokkuustulokset 12 viikon kohdalla, HS-tutkimukset I ja II
HS-tutkimus I | HS-tutkimus II | |||
Plasebo | Adalimumabi 40 mg viikoittain | Plasebo | Adalimumabi 40 mg viikoittain | |
HiSCR-vaste (Hidradenitis Suppurativa Clinical Response)a | N = 154 | N = 153 | N = 163 | N = 163 |
40 (26,0 %) | 64 (41,8 %)* | 45 (27,6 %) | 96 (58,9 %)*** | |
≥ 30 % ihokivun väheneminenb | N = 109 | N = 122 | N = 111 | N = 105 |
27 (24,8 %) | 34 (27,9 %) | 23 (20,7 %) | 48 (45,7 %)*** | |
*P <0,05, ***P 0,001, adalimumabi vs. plasebo a Kaikkien satunnaistettujen potilaiden joukossa. b Potilaidenjoukossa, joiden lähtötilanteessa HS-arvoon liittyvä ihokivun arvio oli ≥ 3, numeerisen luokitusasteikon 0–10 perusteella; 0 = ei ihokipua, 10 = niin kova ihokipu kuin voit kuvitella. | ||||
Adalimumabihoito (40 mg kerran viikossa) pienensi merkitsevästi absessien ja vuotavien fistelien pahenemisen riskiä. Noin kaksinkertainen osuus potilaista plaseboryhmässä HS-I- ja HS-II-tutkimusten ensimmäisen 12 viikon aikana verrattuna adalimumabiryhmän potilaisiin pahensi absesseja (23,0 % ja vastaavasti 11,4 %) ja vuotavia fisteleitä (30,0 % ja vastaavasti 13,9 %).
Viikon 12 kohdalla seuraavilla osa-alueilla tapahtui lähtötilanteeseen verrattuna enemmän kohentumista kuin plasebohoidossa: ihospesifinen terveyteen liittyvä elämänlaatu DLQI-elämänlaatumittarilla mitattuna (HS-I- ja HS-II-tutkimus), potilaan yleinen tyytyväisyys lääkehoitoon TSQM-kyselylomakkeella mitattuna (HS-I- ja HS-II-tutkimus) ja fyysinen terveys SF-36-mittarin fyysisen osion yhteispisteillä mitattuna (HS-I-tutkimus).
Vähintään osittaisen vasteen adalimumabihoitoon (40 mg kerran viikossa) viikon 12 kohdalla saaneilla potilailla HiSCR-prosentti viikon 36 kohdalla oli adalimumabihoitoa viikoittain jatkaneilla potilailla suurempi kuin potilailla, joilla annostelutiheyttä harvennettiin joka toiseen viikkoon tai joilla hoito keskeytettiin (ks. taulukko 14).
Taulukko 14
Niiden potilaiden osuusa, jotka saavuttivat HiSCR:nb viikoilla 24 ja 36 hoidon uudelleensijoittamisen jälkeen viikoittaiselta adalimumabilta viikolla 12
Plasebo (hoidon lopettaminen) N = 73 | Adalimumabi 40 mg joka toinen viikko N = 70 | Adalimumabi 40 mg viikoittain N = 70 | |
Viikko 24 | 24 (32,9 %) | 36 (51,4 %) | 40 (57,1 %) |
Viikko 36 | 22 (30,1 %) | 28 (40,0 %) | 39 (55,7 %) |
a Potilaat, joilla vähintään osittainen vaste 40 mg adalimumabille viikottain 12 viikon hoidon jälkeen. b Jos tutkimussuunnitelmassa nimetyt kriteerit täyttyivät eli vaste menetettiin tai tila ei kohentunut, potilaan oli keskeytettävä osallistuminen tutkimukseen ja potilas tulkittiin ei vastetta saaneeksi. | |||
Potilailla, jotka olivat saavuttaneet vähintään osittaisia vasteita viikolla 12 ja jotka saivat jatkuvaa viikoittaista adalimumabihoitoa, HiSCR-prosentti viikolla 48 oli 68,3 % ja viikolla 96 65,1 %. Pidempään, 96 viikon ajan jatkuneen adalimumabihoidon (40 mg kerran viikossa) aikana ei ilmennyt uusia turvallisuuslöydöksiä.
Potilailla, joiden adalimumabihoito lopetettiin viikolla 12 tutkimuksissa HS-I ja HS-II, HiSCR-määrä 12 viikkoa adalimumabin 40 mg viikoittaisen uudelleen käyttöönoton jälkeen palasi tasolle, joka oli samanlainen kuin ennen lopettamista (56,0 %).
Nuorten hidradenitis suppurativa
Nuorilla HS-tautia sairastavilla potilailla ei ole tehty kliinisiä adalimumabitutkimuksia. Adalimumabin teho nuorten HS-tautia sairastavien potilaiden hoidossa on arvioitu perustuen aikuisilla HS-tautia sairastavilla potilailla osoitettuun tehoon ja altistus-vastesuhteeseen sekä siihen todennäköisyyteen, että taudin kulku, patofysiologia ja lääkkeen vaikutukset ovat olennaisesti samanlaiset kuin aikuisilla samoilla altistumistasoilla. Suositellun adalimumabiannoksen turvallisuus nuorille HS-tautia sairastaville potilaille perustuu adalimumabin turvallisuusprofiiliin muissa käyttöaiheissa sekä aikuis- että lapsipotilailla samoilla tai tiheämmillä annoksilla (ks. kohta Farmakokinetiikka).
Crohnin tauti
Yuflyman tehoa ja turvallisuutta arvioitiin satunnaistetuissa, kaksoissokkoutetuissa ja plasebokontrolloiduissa tutkimuksissa yli 1 500 potilaalla, joilla oli keskivaikea tai vaikea aktiivinen Crohnin tauti (pisteet taudin aktiivisuutta mittaavalla CDAI-indeksillä ≥ 220 ja ≤ 450). Aminosalisylaatit, kortikosteroidit ja/tai immunomodulaattorit muuttumattomina annoksina olivat tutkimuksen aikana sallittuja, ja 80 % potilaista sai ainakin yhtä näistä lääkityksistä.
Kliinisen remission (määritelmän mukaan CDAI < 150) induktiota arvioitiin Crohn-tutkimuksessa I (CLASSIC I) ja Crohn-tutkimuksessa II (GAIN). Crohn-tutkimuksessa I 299 TNF-salpaajaa aiemmin käyttämätöntä potilasta sijoitettiin satunnaisesti yhteen neljästä hoitoryhmästä: plasebo viikoilla 0 ja 2, 160 mg adalimumabia viikolla 0 ja 80 mg viikolla 2, 80 mg viikolla 0 ja 40 mg viikolla 2 ja 40 mg viikolla 0 ja 20 mg viikolla 2. Crohn-tutkimuksessa II 325 potilasta, jotka olivat menettäneet vasteen tai olivat intolerantteja infliksimabille, satunnaistettiin saamaan joko 160 mg adalimumabia viikolla 0 ja 80 mg viikolla 2 tai plaseboa viikoilla 0 ja 2. Potilaat, joilla ei saavutettu primaarista hoitovastetta, suljettiin pois tutkimuksista, eikä heitä arvioitu pidempään.
Crohn-tutkimuksessa III (CHARM) arvioitiin kliinisen remission pysyvyyttä. Crohn-tutkimuksessa III 854 potilasta sai avoimesti 80 mg adalimumabia viikolla 0 ja 40 mg adalimumabia viikolla 2. Viikolla 4 potilaat satunnaistettiin saamaan joko 40 mg joka toinen viikko, 40 mg kerran viikossa tai plaseboa. Tutkimuksen kokonaiskesto oli 56 viikkoa. Potilaat, joilla todettiin kliininen hoitovaste (CDAI-pisteiden väheneminen ≥ 70:lla) viikolla 4, stratifioitiin ja analysoitiin erillään potilaista, joilla ei todettu kliinistä hoitovastetta viikolla 4. Kortikosteroidin vähentäminen sallittiin viikon 8 jälkeen.
Crohn-tutkimuksissa I ja II saavutetut remissio- ja vasteprosentit on esitetty taulukossa 15.
Taulukko 15
Kliinisen remission ja vasteen aikaansaaminen (% potilaista)
Crohn-tutkimus I: Infliksimabia aiemmin saamattomat potilaat | Crohn-tutkimus II: Infliksimabia aiemmin saaneet potilaat | ||||
Plasebo N = 74 | Adalimumabi 80/40 mg N = 75 | Adalimumabi 160/80 mg N = 76 | Plasebo N = 166 | Adalimumabi 160/80 mg N = 159 | |
Viikko 4 | |||||
Kliininen remissio | 12 % | 24 % | 36 %* | 7 % | 21 %* |
Kliininen vaste (CR-100) | 24 % | 37 % | 49 %** | 25 % | 38 %** |
Kaikki p-arvot on saatu adalimumabin ja plasebon osuuksien parivertailuista
*p < 0,001
**p < 0,01
Remissioprosentit olivat viikon 8 kohdalla samankaltaiset riippumatta siitä, saivatko potilaat hoidon alussa 160/80 mg vai 80/40 mg, mutta 160/80 mg saaneilla potilailla haittatapahtumien esiintymistiheys oli suurempi.
Crohn-tutkimuksessa III 58 %:lla potilaista (499/854) todettiin kliininen vaste viikolla 4, ja nämä potilaat otettiin mukaan päävasteanalyysiin. Viikkoon 4 mennessä kliinisen hoitovasteen saavuttaneista potilaista 4,48 % oli saanut aiemmin jotain muuta TNF-salpaajahoitoa. Remission ja vasteiden pysyvyys on esitetty taulukossa 16. Kliinisen remission ylläpidon suhteen tulokset pysyivät melko muuttumattomina aiemmista TNF-salpaajahoidoista riippumatta.
Sairauteen liittyvien sairaalahoitojaksojen ja leikkausten määrä väheni adalimumabihoidolla plasebohoitoon verrattuna tilastollisesti merkitsevästi viikolla 56.
Taulukko 16
Kliinisen remission ja vasteen ylläpitäminen (% potilaista)
Plasebo | 40 mg adalimumabia joka toinen viikko | 40 mg adalimumabia joka viikko | |
Viikko 26 | N = 170 | N = 172 | N = 157 |
Kliininen remissio | 17 % | 40 %* | 47 %* |
Kliininen vaste (CR-100) | 27 % | 52 %* | 52 %* |
Remissiossa ilman steroidihoitoa ≥ 90 vrk ajana | 3 % (2/66) | 19 % (11/58)** | 15 % (11/74)** |
Viikko 56 | N = 170 | N = 172 | N = 157 |
Kliininen remissio | 12 % | 36 %* | 41 %* |
Kliininen vaste (CR-100) | 17 % | 41 %* | 48 %* |
Remissiossa ilman steroidihoitoa ≥ 90 vrk ajana | 5 % (3/66) | 29 % (17/58)* | 20 % (15/74)** |
*p < 0,001 saatu adalimumabin ja plasebon osuuksien parivertailusta
**p < 0,02 saatu adalimumabin ja plasebon osuuksien parivertailusta
a Potilaista, jotka saivat kortikosteroidihoitoa lähtötilanteessa
Potilaista, joille ei saatu vastetta viikolla 4, 43 % adalimumabia ylläpitohoitona saaneista ja 30 % plaseboa ylläpitohoitona saaneista saavutti hoitovasteen viikkoon 12 mennessä. Näiden tulosten perusteella ylläpitohoidon jatkamisesta viikolle 12 voi olla hyötyä joillekin potilaille, joilla ei saavuteta hoitovastetta viikkoon 4 mennessä. Hoidon jatkaminen yli 12 viikon ajan ei lisännyt merkitsevästi vasteen saavuttaneiden lukumäärää (ks. kohta Annostus ja antotapa).
117/276 potilasta Crohn-tutkimuksesta I ja 272/777 potilasta Crohn-tutkimuksista II ja III seurattiin vähintään 3 vuoden ajan avoimessa adalimumabihoidossa. 88 (tutkimuksessa I) ja 189 (tutkimuksissa II ja III) potilasta pysyi kliinisessä remissiossa. Kliininen vaste (CR-100) säilyi 102 (tutkimuksessa I) ja 233 (tutkimuksissa II ja III) potilaalla.
Elämänlaatu
Crohn-tutkimuksissa I ja II potilailla, jotka oli satunnaistettu saamaan joko 80/40 mg tai 160/80 mg adalimumabia, todettiin plaseboa saaneisiin potilaisiin verrattuna tilastollisesti merkitsevää paranemista tulehduksellisia suolistosairauksia spesifisesti arvioivan IBDQ-kyselylomakkeen kokonaispisteissä viikolla 4, samoin kuin Crohn-tutkimuksessa III adalimumabihoitoa saaneilla plaseboryhmään verrattuna viikoilla 26 ja 56.
Lasten Crohnin tauti
Adalimumabihoitoa arvioitiin satunnaistetussa, kaksoissokkoutetussa kliinisessä monikeskustutkimuksessa, jossa arvioitiin induktio- ja ylläpitohoidon tehoa ja turvallisuutta painon (< 40 kg tai ≥ 40 kg) mukaisina annoksina 192 lapsipotilaalla, joiden ikä oli 6–17 vuotta ja joilla oli keskivaikea tai vaikea Crohnin tauti (määritelmä: Paediatric Crohn’s Disease Activity Index -pisteet [PCDAI] > 30). Mukaan otettiin vain potilaita, joilla Crohnin taudin tavanomainen hoito (mm. kortikosteroidi- ja/tai immunomodulanttihoito) oli epäonnistunut. Myös aiemman infliksimabihoitovasteen menettäminen tai infliksimabihoitoon liittyneet siedettävyysongelmat olivat hyväksyttäviä mukaanottoperusteita.
Kaikki potilaat saivat avointa induktiohoitoa, jonka annos riippui heidän painostaan lähtötilanteessa. 160 mg viikolla 0 ja 80 mg viikolla 2 ≥ 40 kg painoisilla potilailla ja vastaavasti 80 mg ja 40 mg potilailla, joiden paino on < 40 kg.
Viikolla 4 potilaat satunnaistettiin senhetkisen painon mukaan suhteessa 1:1 käyttämään joko pieniä tai tavanomaisia annoksia ylläpitohoitona (ks. taulukko 17).
Taulukko 17 Ylläpitohoito
Potilaan paino | Pieni annos | Tavanomainen annos |
< 40 kg | 10 mg joka 2. viikko | 20 mg joka 2. viikko |
≥ 40 kg | 20 mg joka 2. viikko | 40 mg joka 2. viikko |
Tehoa koskevat tulokset
Tutkimuksen ensisijainen päätetapahtuma oli kliininen remissio viikolla 26 (määritelmä: PCDAI- pisteet ≤ 10).
Kliiniset remissio- ja vasteprosentit esitetään taulukossa 18 (Kliinisen vasteen määritelmä: PCDAI-pisteet pienenivät vähintään 15 p lähtöarvoihin nähden). Kortikosteroidi- tai immunomodulaattorihoidon lopettamisprosentit esitetään taulukossa 19.
Taulukko 18
Tutkimus lasten Crohnin taudista
Kliininen PCDAI-remissio ja vaste
Tavanomainen annos 40/20 mg joka 2. viikko N = 93 | Pieni annos 20/10 mg joka 2. viikko N = 95 | P-arvo* | |
Viikko 26 | |||
Kliininen remissio | 38,7 % | 28,4 % | 0,075 |
Kliininen vaste | 59,1 % | 48,4 % | 0,073 |
Viikko 52 | |||
Kliininen remissio | 33,3 % | 23,2 % | 0,100 |
Kliininen vaste | 41,9 % | 28,4 % | 0,038 |
* Tavanomaisen ja pienen annoksen vertailun p-arvo. | |||
Taulukko 19
Tutkimus lasten Crohnin taudista
Kortikosteroidien tai immunomodulaattorien lopettaminen ja fistelien remissio
Tavanomainen annos 40/20 mg joka 2. viikko | Pieni annos 20/10 mg joka 2. viikko | P-arvo1 | |
Kortikosteroidien keskeyttäminen | N = 33 | N = 38 | |
Viikko 26 | 84,8 % | 65,8 % | 0,066 |
Viikko 52 | 69,7 % | 60,5 % | 0,420 |
Immunomodulaattorien keskeyttäminen2 | N = 60 | N = 57 | |
Viikko 52 | 30,0 % | 29,8 % | 0,983 |
Fistelien remissio3 | N = 15 | N = 21 | |
Viikko 26 | 46,7 % | 38,1 % | 0,608 |
Viikko 52 | 40,0 % | 23,8 % | 0,303 |
1 p-arvo tavanomaisen ja pienenannoksen vertailuun.
2 Immunosuppressanttihoito voitiin lopettaa aikaisintaan viikolla 26 tutkijan arvion mukaan, jos kliinisen vasteen kriteerit täyttyivät.
3 Määritelmä: kaikki lähtötilanteessa vuotaneet fistelit sulkeutuneina vähintään kahdella peräkkäisellä käynnillä lähtötasokäynnin jälkeen.
Molemmissa hoitoryhmissä todettiin, että painoindeksi ja pituuskasvunopeus suurenivat (paranivat) tilastollisesti merkitsevästi lähtötilanteen ja viikkojen 26 ja 52 välillä.
Molemmissa hoitoryhmissä todettiin myös elämänlaatuparametrien (mm. IMPACT III) parantuneen tilastollisesti ja kliinisesti merkitsevästi lähtötilanteeseen nähden.
Lasten Crohnin tauti -tutkimukseen osallistuneista potilaista sata (n = 100) jatkoi avoimeen pitkäkestoiseen jatkotutkimukseen. 5 vuoden adalimumabihoidon jälkeen 74,0 % (37/50) 50:stä tutkimuksessa jäljellä olevasta potilaasta pysyi kliinisessä remissiossa, ja 92,0 %:lla (46/50) potilaista säilyi kliininen vaste PCDAI:n mukaan.
Ulseratiivinen koliitti
Toistuvien adalimumabiannosten turvallisuutta ja tehoa arvioitiin satunnaistetuissa, kaksoissokkoutetuissa, plasebokontrolloiduissa tutkimuksissa aikuispotilailla, joiden ulseratiivinen koliitti oli aktiivisuudeltaan keskivaikea tai vaikea (Mayo-pisteet 6–12, endoskopiaosion pisteet 2–3).
UC-I-tutkimuksessa 390 potilasta, jotka eivät olleet saaneet aiemmin TNF-salpaajia, satunnaistettiin saamaan joko plaseboa viikoilla 0 ja 2 tai 160 mg adalimumabia viikolla 0 ja tämän jälkeen 80 mg viikolla 2 tai 80 mg adalimumabia viikolla 0 ja tämän jälkeen 40 mg viikolla 2. Viikon 2 jälkeen kummankin adalimumabiryhmän potilaat saivat 40 mg joka toinen viikko. Kliinisen remission saavuttaminen (määritelmänä Mayo-pisteet < 2, kunkin osion pisteet < 1) arvioitiin viikon 8 kohdalla.
UC-II-tutkimuksessa 248 potilasta sai 160 mg adalimumabia viikolla 0, 80 mg viikolla 2 ja tämän jälkeen 40 mg kahden viikon välein, ja 246 potilasta sai plaseboa. Kliinisiä tuloksia arvioitiin remission induktion osalta viikon 8 kohdalla ja remission ylläpidon osalta viikon 52 kohdalla.
8 viikon kohdalla todettu kliinisen remission saavuttaneiden osuus oli tilastollisesti merkitsevästi suurempi 160/80 mg adalimumabia saaneilla potilailla kuin plaseboa saaneilla UC-I-tutkimuksessa (18 % vs. plasebo 9 %, p = 0,031) ja UC-II-tutkimuksessa (17 % vs. plasebo 9 %, p = 0,019). UC-II-tutkimuksessa niistä adalimumabia saneista potilaista, jotka saavuttivat remission viikon 8 kohdalla, 21/41 (51 %) oli edelleen remissiossa viikon 52 kohdalla.
Taulukossa 20 esitetään koko UC-II-tutkimuspopulaation tulokset.
Taulukko 20
Hoitovaste, remissio ja limakalvon paraneminen UC-II-tutkimuksessa
(prosenttia potilaista)
Plasebo | Adalimumabi 40 mg joka toinen viikko | |
Viikko 52 | N = 246 | N = 248 |
Kliininen vaste | 18 % | 30 %* |
Kliininen remissio | 9 % | 17 %* |
Limakalvon paraneminen | 15 % | 25 %* |
steroidivapaa remissio ≥ 90 päivän ajan | 6 % (N = 140) | 13 %* (N = 150) |
Viikot 8 ja 52 | ||
Pitkäkestoinen vaste | 12 % | 24 %** |
Pitkäkestoinen remissio | 4 % | 8 %* |
Pitkäkestoinen limakalvon paraneminen | 11 % | 19 %* |
Kliininen remissio: Mayo-pisteet < 2, kunkin osion pisteet < 1
Kliininen vaste: Mayo-pisteiden lasku ≥ 3 pistettä ja ≥ 30 % lähtötilanteesta; lisäksi rektaaliverenvuotoa kuvaavan RBS-pistearvon tulee laskea ≥ 1 tai olla 0 tai 1.
*p < 0,05, adalimumabi vs. plasebo, osuuksien pareittainen vertailu
**p < 0,001 adalimumabi vs. plasebo, osuuksien pareittainen vertailu
a Potilaista, jotka saivat kortikosteroidihoitoa lähtötilanteessa
Niistä potilaista, jotka saivat vasteen viikolla 8, viikon 52 kohdalla 47 % oli säilyttänyt vasteen, 29 % oli remissiossa, 41 %:lla havaittiin limakalvon paranemista ja 20 % oli ollut steroidivapaassa remissiossa ≥ 90 vuorokautta.
Aiempi infliksimabilla toteutettu TNF-salpaajahoito oli epäonnistunut noin 40 prosentilla UC-II-tutkimuksen potilaista. Näillä potilailla adalimumabin teho oli heikompi kuin potilailla, jotka eivät olleet saaneet aiempaa TNF-salpaajahoitoa. Potilaista, joiden aiempi TNF-salpaajahoito oli epäonnistunut, viikon 52 kohdalla remission saavutti 3 % plasebohoitoa saaneista ja 10 % adalimumabihoitoa saaneista.
UC-I ja -II -tutkimusten potilailla oli mahdollisuus siirtyä avoimeen, pitkäkestoiseen jatkotutkimukseen (UC-III). Seuraavan kolmen vuoden adalimumabihoidon jälkeen 75 % (301/402) oli edelleen kliinisessä remissiossa osittaisen Mayo-pisteytyksen mukaan.
Sairaalahoitoon joutuminen
Adalimumab-tutkimushaarassa hoidetut potilaat tarvitsivat vähemmän sekä kaikista syistä johtuvaa että ulseratiiviseen koliittiin liittyvää sairaalahoitoa 52 viikkoa kestäneiden UC-I ja UC-II -tutkimusten aikana kuin plasebotutkimushaarassa hoidetut potilaat. Kun huomioon otettiin kaikki sairaalahoitoon johtaneet syyt, adalimumabihoitoa saaneista 0,18 vs. plasebohoitoa saaneista 0,26 tapausta/potilasvuosi tarvitsi sairaalahoitoa. Vastaavasti ulseratiivisen koliitin vuoksi sairaalahoitoon joutui adalimumabihoitoa saaneista 0,12 vs. plasebohoitoa saaneista 0,22 tapausta/potilasvuosi.
Elämänlaatu
UC-II –tutkimuksessa Inflammatory Bowel Disease Questionaire (IBDQ)-pisteet paranivat adalimumabihoitoa saaneilla.
Ulseratiivinen koliitti lapsilla
Adalimumabin turvallisuutta ja tehoa arvioitiin satunnaistetussa, kaksoissokkoutetussa monikeskustutkimuksessa, johon osallistui 93 pediatrista potilasta (5–17-vuotiaita), joilla oli keskivaikea tai vaikea ulseratiivinen koliitti (Mayo-pisteet 6–12, endoskopiaosion pisteet 2–3, vahvistettu keskitetysti arvioidulla endoskopialla) ja joiden kohdalla tavanomaisilla hoidoilla ei ollut saatu riittävää vastetta tai ne olivat olleet huonosti siedettyjä. Aiempi TNF-antagonistihoito oli epäonnistunut noin 16 %:lla tutkimukseen osallistuneista potilaista. Kortikosteroideja tutkimukseenottovaiheessa saaneiden potilaiden kortikosteroidiannoksen pienentäminen sallittiin viikon 4 jälkeen.
Tutkimuksen aloitusvaiheessa 77 potilasta satunnaistettiin suhteessa 3:2 saamaan kaksoissokkoutettua adalimumabi-hoitoa induktioannoksella 2,4 mg/kg (enintään 160 mg) viikolla 0 ja viikolla 1 sekä 1,2 mg/kg (enintään 80 mg) viikolla 2 tai induktioannoksella 2,4 mg/kg (enintään 160 mg) viikolla 0, lumelääkettä viikolla 1 sekä annoksella 1,2 mg/kg (enintään 80 mg) viikolla 2. Molemmat ryhmät saivat annoksena 0,6 mg/kg (enintään 40 mg) viikolla 4 ja viikolla 6. Tutkimusasetelmaan tehdyn muutoksen jälkeen loput 16 aloitusvaiheeseen osallistunutta potilasta saivat avoimesti adalimumab-hoitoa induktioannoksella 2,4 mg/kg (enintään 160 mg) viikolla 0 ja viikolla 1 sekä annoksella 1,2 mg/kg (enintään 80 mg) viikolla 2.
Viikolla 8 62 potilasta, joilla todettiin kliininen vaste osittaisen Mayo-pisteytyksen mukaan (määritelmä: osittaisten Mayo-pisteiden lasku ≥ 2 pistettä ja ≥ 30 % lähtötilanteesta), satunnaistettiin yhtäläisessä suhteessa saamaan joko kaksoissokkoutettua adalimumab-ylläpitohoitoa annoksella 0,6 mg/kg (enintään 40 mg) viikossa tai ylläpitoannoksella 0,6 mg/kg (enintään 40 mg) joka toinen viikko. Lisäksi 12 potilasta, joilla todettiin kliininen vaste osittaisen Mayo-pisteytyksen mukaan, satunnaistettiin saamaan lumelääkettä ennen tutkimusasetelman muuttamista, mutta heitä ei otettu mukaan tehon varmistamiseksi tehtyyn analyysiin.
Taudin pahenemisvaihe määriteltiin osittaisten Mayo-pisteiden nousuksi vähintään 3 pisteellä (potilaat, joiden osittaiset Mayo-pisteet olivat 0–2 viikolla 8), vähintään 2 pisteellä (potilaat, joiden osittaiset Mayo-pisteet olivat 3–4 viikolla 8) tai vähintään 1 pisteellä (potilaat, joiden osittaiset Mayo-pisteet olivat 5–6 viikolla 8).
Potilaat, jotka täyttivät taudin pahenemisvaiheen kriteerit viikolla 12 tai sen jälkeen, satunnaistettiin saamaan uutena induktioannoksena 2,4 mg/kg (enintään 160 mg) tai annoksena 0,6 mg/kg (enintään 40 mg), minkä jälkeen he jatkoivat hoitoa omalla ylläpitoannoksellaan.
Tehotulokset
Tutkimuksen ensisijaisia yhdistettyjä päätetapahtumia olivat kliininen remissio osittaisen Mayo-pisteytyksen mukaan (määritelmä: osittaiset Mayo-pisteet ≤ 2 eikä yhdenkään osion pisteet > 1) viikolla 8 ja kliininen remissio Mayo-kokonaispisteiden mukaan (määritelmä: Mayo-pisteet ≤ 2 eikä yhdenkään osion pisteet > 1) viikolla 52 niiden potilaiden osalta, jotka saavuttivat kliinisen vasteen osittaisen Mayo-pisteytyksen mukaan viikolla 8.
Kliiniset remissioprosentit osittaisen Mayo-pisteytyksen mukaan viikolla 8 kaksoissokkoutettua adalimumab-induktiohoitoa saaneisiin ryhmiin kuuluneilla potilailla esitetään taulukossa 21.
Taulukko 21: Kliininen remissio osittaisen Mayo-pisteytyksen mukaan viikolla 8
Adalimumabia Enintään 160 mg viikolla 0 / lumelääkettä viikolla 1 N = 30 | Adalimumabib, c Enintään 160 mg viikolla 0 ja viikolla 1 N = 47 | |
Kliininen remissio | 13/30 (43,3 %) | 28/47 (59,6 %) |
a Adalimumabi 2,4 mg/kg (enintään 160 mg) viikolla 0, lumelääkettä viikolla 1 ja 1,2 mg/kg (enintään 80 mg) viikolla 2 b Adalimumabi 2,4 mg/kg (enintään 160 mg) viikolla 0 ja viikolla 1 sekä 1,2 mg/kg (enintään 80 mg) viikolla 2 c Ei sisällä avointa adalimumabi-induktioannosta 2,4 mg/kg (enintään 160 mg) viikolla 0 ja viikolla 1 sekä 1,2 mg/kg (enintään 80 mg) viikolla 2 Huomautus 1: Molemmat induktioryhmät saivat annoksena 0,6 mg/kg (enintään 40 mg) viikolla 4 ja viikolla 6 Huomautus 2: Potilaiden, joilta puuttui arvoja viikolla 8, ei katsottu saavuttaneen päätetapahtumaa | ||
Viikolla 8 hoitoon vastanneiden kliinistä remissiota Mayo-kokonaispisteiden mukaan, viikolla 8 hoitoon vastanneiden kliinistä vastetta Mayo-kokonaispisteiden mukaan (määritelmä: Mayo-pisteiden lasku ≥ 3 pistettä ja ≥ 30 % lähtötilanteesta), viikolla 8 hoitoon vastanneiden limakalvojen paranemista Mayo-kokonaispisteiden mukaan (määritelmä: Mayo-endoskopiaosion pisteet ≤ 1), viikolla 8 remissiossa olleiden kliinistä remissiota Mayo-kokonaispisteiden mukaan sekä niiden viikolla 8 hoitoon vastanneiden tutkittavien osuutta, jotka olivat remissiossa ilman kortikosteroidihoitoa Mayo-kokonaispisteiden mukaan, arvioitiin viikolla 52 niiden potilaiden osalta, jotka saivat kaksoissokkoutettua adalimumabi-ylläpitohoitoa enintään 40 mg joka toinen viikko (0,6 mg/kg) ja enintään 40 mg viikossa (0,6 mg/kg) (taulukko 22).
Taulukko 22: Tehotulokset viikolla 52
Adalimumabia Enintään 40 mg joka toinen viikko N = 31 | Adalimumabib Enintään 40 mg viikossa N = 31 | |
Kliininen remissio potilailla, jotka vastasivat hoitoon viikolla 8 osittaisen Mayo-pisteytyksen mukaan | 9/31 (29,0 %) | 14/31 (45,2 %) |
Kliininen vaste potilailla, jotka vastasivat hoitoon viikolla 8 osittaisen Mayo-pisteytyksen mukaan | 19/31 (61,3 %) | 21/31 (67,7 %) |
Limakalvojen paraneminen potilailla, jotka vastasivat hoitoon viikolla 8 osittaisen Mayo-pisteytyksen mukaan | 12/31 (38,7 %) | 16/31 (51,6 %) |
Kliininen remissio potilailla, joiden tauti oli remissiossa viikolla 8 osittaisen Mayo-pisteytyksen mukaan | 9/21 (42,9 %) | 10/22 (45,5 %) |
Remissio ilman kortikosteroideja potilailla, jotka vastasivat hoitoon viikolla 8 osittaisen Mayo-pisteytyksen mukaanc | 4/13 (30,8 %) | 5/16 (31,3 %) |
a Adalimumabi 0,6 mg/kg (enintään 40 mg) joka toinen viikko b Adalimumabi 0,6 mg/kg (enintään 40 mg) viikossa c Potilailla, jotka saivat samanaikaista kortikosteroidihoitoa lähtötilanteessa Huom: Potilaiden, joilta puuttui arvoja viikolla 52 tai jotka satunnaistettiin saamaan uutta induktiohoitoa tai ylläpitohoitoa, ei katsottu vastanneen hoitoon viikon 52 päätetapahtumien osalta. | ||
Muita eksploratiivisia tehon päätetapahtumia olivat kliininen vaste pediatrisen ulseratiivisen koliitin aktiivisuusindeksin (PUCAI) mukaan (määritelmä: PUCAI-pisteiden lasku ≥ 20 pistettä lähtötilanteesta) ja kliininen remissio PUCAI-pisteiden mukaan (määritelmä: PUCAI-pisteet < 10) viikolla 8 ja viikolla 52 (taulukko 23).
Taulukko 23: Eksploratiivisten päätetapahtumien tulokset PUCAI-pisteiden mukaan | ||
Viikko 8 | ||
Adalimumabia Enintään 160 mg viikolla 0 / lumelääkettä viikolla 1 N = 30 | Adalimumabib,c Enintään 160 mg viikolla 0 ja viikolla 1 N = 47 | |
Kliininen remissio PUCAI-pisteiden mukaan | 10/30 (33,3 %) | 22/47 (46,8 %) |
Kliininen vaste PUCAI-pisteiden mukaan | 15/30 (50,0 %) | 32/47 (68,1 %) |
Viikko 52 | ||
Adalimumabid Enintään 40 mg joka toinen viikko N = 31 | Adalimumabie Enintään 40 mg viikossa N = 31 | |
Kliininen remissio PUCAI-pisteiden mukaan potilailla, jotka vastasivat hoitoon viikolla 8 osittaisen Mayo-pisteytyksen mukaan | 14/31 (45,2 %) | 18/31 (58,1 %) |
Kliininen vaste PUCAI-pisteiden mukaan potilailla, jotka vastasivat hoitoon viikolla 8 osittaisen Mayo-pisteytyksen mukaan | 18/31 (58,1 %) | 16/31 (51,6 %) |
a Adalimumabi 2,4 mg/kg (enintään 160 mg) viikolla 0, lumelääkettä viikolla 1 ja 1,2 mg/kg (enintään 80 mg) viikolla 2 b Adalimumabi 2,4 mg/kg (enintään 160 mg) viikolla 0 ja viikolla 1 sekä 1,2 mg/kg (enintään 80 mg) viikolla 2 c Ei sisällä avointa adalimumabi-induktioannosta 2,4 mg/kg (enintään 160 mg) viikolla 0 ja viikolla 1 sekä 1,2 mg/kg (enintään 80 mg) viikolla 2 d Adalimumabi 0,6 mg/kg (enintään 40 mg) joka toinen viikko e Adalimumabi 0,6 mg/kg (enintään 40 mg) viikossa Huomautus 1: Molemmat induktioryhmät saivat annoksena 0,6 mg/kg (enintään 40 mg) viikolla 4 ja viikolla 6 Huomautus 2: Potilaiden, joilta puuttui arvoja viikolla 8, ei katsottu saavuttaneen päätetapahtumia Huomautus 3: Potilaiden, joilta puuttui arvoja viikolla 52 tai jotka satunnaistettiin saamaan uutta induktiohoitoa tai ylläpitohoitoa, ei katsottu vastanneen hoitoon viikon 52 päätetapahtumien osalta. | ||
Niistä Adalimumabi-hoitoa saaneista potilaista, jotka saivat uuden induktiohoidon ylläpitovaiheessa, 2/6 (33 %) saavutti kliinisen vasteen Mayo-kokonaispisteiden mukaan viikolla 52.
Elämänlaatu
Adalimumabi-hoitoa saaneissa ryhmissä todettiin IMPACT III- pisteiden sekä huoltajan tuottavuuden ja aktiivisuuden heikentymistä mittaavien WPAI-pisteiden parantuneen kliinisesti merkitsevästi lähtötilanteeseen nähden.
Pituuskasvunopeuden kliinisesti merkittävää lisääntymistä (paranemista) lähtötilanteeseen nähden todettiin adalimumabia saaneissa ryhmissä, ja painoindeksin kliinisesti merkittävää nousua (paranemista) lähtötilanteeseen nähden todettiin niillä tutkittavilla, jotka saivat suurena ylläpitoannoksena enintään 40 mg (0,6 mg/kg) viikossa.
Uveiitti
Adalimumabin turvallisuutta ja tehoa arvioitiin kahdessa satunnaistetussa, kaksoissokkoutetussa, plasebokontrolloidussa tutkimuksessa (UV I ja II) aikuispotilailla, joilla oli ei-infektioperäinen intermediaarinen uveiitti, posteriorinen uveiitti tai panuveiitti. Pois suljettiin potilaat, joilla oli isoloitu anteriorinen uveiitti. Potilaat saivat joko plasebohoitoa tai adalimumabihoitoa (80 mg:n aloitusannos, jonka jälkeen 40 mg joka toinen viikko; ensimmäinen 40 mg:n annos otettiin viikon kuluttua aloitusannoksesta). Samanaikainen hoito yhdellä vakaa-annoksisella ei-biologisella immunosuppressantilla sallittiin.
UV I -tutkimuksessa arvioitiin 217 potilasta, joilla oli aktiivinen uveiitti kortikosteroidihoidosta huolimatta (peroraalinen prednisoni annoksella 10–60 mg/vrk). Kaikki potilaat saivat 2 viikon ajan prednisonihoitoa standardiannoksella 60 mg/vrk tutkimukseenottovaiheessa, minkä jälkeen oli pakollinen annoksen pienentämisvaihe, ja kortikosteroidihoito lopetettiin kokonaan viikkoon 15 mennessä.
UV II -tutkimuksessa arvioitiin 226 potilasta, joiden inaktiivinen uveiitti vaati lähtötilanteessa pitkäaikaista kortikosteroidihoitoa (peroraalinen prednisoni 10–35 mg/vrk) taudin hallitsemiseksi. Tämän jälkeen oli pakollinen annoksen pienentämisvaihe, ja kortikosteroidihoito lopetettiin kokonaan viikkoon 19 mennessä.
Ensisijainen tehon päätetapahtuma oli kummassakin tutkimuksessa ”hoidon epäonnistumiseen kuluva aika”. Hoidon epäonnistumisen määritelmänä oli monitekijäinen vastemuuttuja, joka perustui inflammatorisiin suoni- ja verkkokalvon ja/tai inflammatorisiin verkkokalvon verisuonien leesioihin, etukammion solujen määrään, lasiaissamentumien asteeseen ja parhaaseen lasikorjattuun näöntarkkuuteen (BCVA).
Potilaat, jotka olivat mukana UV I ja UV II -tutkimuksissa, olivat oikeutettuja osallistumaan kontrolloimattomaan pitkäkestoiseen jatkotutkimukseen, jonka alkuperäinen suunniteltu kesto oli 78 viikkoa. Potilaat saivat jatkaa tutkimuslääkkeellä viikon 78 jälkeen siihen saakka, kunnes adalimumabia oli heidän saatavillaan.
Kliininen vaste
Kummassakin tutkimuksessa havaittiin adalimumabiryhmässä tilastollisesti merkittävä hoidon epäonnistumisriskin pienentyminen plaseboa saaneeseen ryhmään verrattuna (ks. taulukko 24). Kummassakin tutkimuksessa adalimumabihoidolla havaittiin varhainen ja pitkäkestoinen vaikutus hoidon epäonnistumisosuuteen plaseboon verrattuna (ks. kuva 1).
Taulukko 24
Hoidon epäonnistumiseen kulunut aika UV I- ja UV II -tutkimuksissa
Analyysikäsittely | N | Epäonnistuminen N (%) | Mediaaniaika epäonnistumiseen (kk) | HRa | CI 95 % HR:llea | p Arvob |
Hoidon epäonnistumiseen kulunut aika viikon 6 kohdalla tai sen jälkeen UV I -tutkimuksessa | ||||||
Ensisijainen analyysi (ITT) | ||||||
plasebo | 107 | 84 (78,5) | 3,0 | -- | -- | -- |
adalimumabi | 110 | 60 (54,5) | 5,6 | 0,50 | 0,36, 0,70 | < 0,001 |
Hoidon epäonnistumiseen kulunut aika viikon 2 kohdalla tai sen jälkeen UV II -tutkimuksessa | ||||||
Ensisijainen analyysi (ITT) | ||||||
plasebo | 111 | 61 (55,0) | 8,3 | -- | -- | -- |
adalimumabi | 115 | 45 (39,1) | NEc | 0,57 | 0,39, 0,84 | 0,004 |
Huomio: Hoidon epäonnistuminen viikon 6 kohdalla tai sen jälkeen (UV I -tutkimus) tai viikon 2 kohdalla tai sen jälkeen (UV II -tutkimus) laskettiin tapahtumaksi. Muusta syystä kuin hoidon epäonnistumisesta johtuneet keskeytykset tutkimuksessa rajattiin keskeytyshetken kohdalta.
a Adalimumabin vs. plasebon riskisuhde (HR) laskettiin suhteellisen riskin regressiolla, jossa tekijänä oli hoito.
b 2-puolinen P-arvo log rank -testistä.
c NE = ei voida arvioida. Alle puolella riskille alttiista potilaista esiintyi tapahtuma.
Kuva 1: Hoidon epäonnistumiseen kulunut aika yhteenvetona Kaplan–Meier-käyrinä viikon 6 kohdalla tai sen jälkeen (UV I -tutkimus) tai viikon 2 kohdalla tai sen jälkeen (UV II -tutkimus)
HOIDON EPÄONNISTUMISOSUUS (%) |
| ||||||
AIKA (KUUKAUTTA) | |||||||
UV I -tutkimus | Hoito | _________ Plasebo | ••••••••• Adalimumabi | ||||
HOIDON EPÄONNISTUMISOSUUS (%) |
| ||||||
AIKA (KUUKAUTTA) | |||||
UV II -tutkimus | Hoito | _________ Plasebo | ••••••••• Adalimumabi | ||
Huomio: P# = plasebo (tapahtumien määrä/riskille alttiiden määrä); A# = adalimumabi (tapahtumien määrä /riskille alttiiden määrä).
UV I -tutkimuksessa havaittiin tilastollisesti merkitseviä eroja adalimumabin hyväksi plaseboon verrattuna kunkin hoidon epäonnistumisen osatekijän osalta. UV II -tutkimuksessa havaittiin tilastollisesti merkitseviä eroja vain näöntarkkuuden osalta, mutta muutkin osatekijät olivat adalimumabilla numeerisesti paremmat.
Tutkimusten UV I ja UV II kontrolloimattomaan pitkäkestoiseen jatkotutkimukseen otettiin 424 tutkittavaa. Heistä 60 tutkittavan ei katsottu soveltuvan analyysiin (esim. poikkeamien, diabeettisen retinopatian sekundaaristen komplikaatioiden, kaihileikkauksen tai vitrektomian vuoksi), ja heidät suljettiin pois ensisijaisesta tehoanalyysistä. Jäljelle jääneistä 364 tutkittavasta 269 arviointikelpoista tutkittavaa (74 %) sai avointa adalimumabihoitoa 78 viikon ajan. Havaintotietojen perusteella 216 tutkittavan (80,3 %) tilanne oli rauhallinen (ei aktiivisia tulehdusmuutoksia, etukammion solujen aste ≤ 0,5+, lasiaissamentumien aste ≤ 0,5+) ja samanaikaisesti käytössä ollut steroidiannos oli ≤ 7,5 mg/vrk. 178 tutkittavalla (66,2 %) tilanne oli rauhallinen, eikä käytössä ollut steroidilääkitystä. Paras lasikorjattu näöntarkkuus (BCVA) oli joko aiempaa parempi tai ennallaan (huonontunut < 5 kirjaimen verran) 88,6 %:ssa silmistä viikolla 78. Viikon 78 jälkeiset tiedot olivat yleisesti yhdenmukaisia näiden tulosten kanssa, mutta tutkimukseen osaa ottaneiden henkilöiden määrä väheni tämän ajan jälkeen. Kaiken kaikkiaan tutkimuksen keskeyttäneistä tutkittavista 18 % keskeytti osallistumisensa haittatapahtumien vuoksi ja 8 % siksi, että adalimumabihoidolla saavutettu vaste oli riittämätön.
Elämänlaatu
Kummassakin kliinisessä tutkimuksessa arvioitiin potilaiden ilmoittamia lopputulemia näköön liittyvästä toimintakyvystä NEI VFQ-25-kyselyllä. Adalimumabi oli numeerisesti parempi valtaosassa alaosioista, ja tilastollisesti merkitsevät keskimääräiset erot saavutettiin UV I -tutkimuksessa yleisen näkökyvyn, silmäkivun, lähinäön, mielenterveyden ja kokonaispisteiden alaosioissa sekä UV II - tutkimuksessa yleisen näkökyvyn ja mielenterveyden alaosioissa. Näkökykyyn liittyvät vaikutukset eivät olleet adalimumabihoidolla numeerisesti parempia UV I -tutkimuksessa värinäön osalta ja UV II - tutkimuksessa värinäön, perifeerisen näön ja lähinäön osalta.
Lasten uveiitti
Adalimumabin turvallisuutta ja tehoa arvioitiin satunnaistetussa, kaksoissokkoutetussa, kontrolloidussa tutkimuksessa, johon osallistui 90 2 – < 18-vuotiasta lapsipotilasta, joilla oli aktiivinen JIA:han liittyvä ei-infektioperäinen anteriorinen uveiitti, ja joilla tauti oli refraktaarinen vähintään 12 viikkoa kestäneestä metotreksaattihoidosta huolimatta. Potilaat saivat joko plaseboa tai 20 mg adalimumabia (paino < 30 kg) tai 40 mg adalimumabia (paino ≥ 30 kg) joka toinen viikko yhdessä lähtötilanteen metotreksaattiannoksensa kanssa.
Ensisijainen päätetapahtuma oli "hoidon epäonnistumiseen kuluva aika". Hoidon epäonnistumisen määritelmänä oli silmätulehduksen pahentuminen tai pysyvä ei-paraneminen, osittainen paraneminen, johon liittyi muiden samanaikaisten pysyvien silmäsairauksien kehittyminen tai paheneminen, muun samanaikaisen lääkityksen luvaton käyttö ja hoidon keskeytys pidemmäksi ajaksi.
Kliininen vaste
Adalimumabi viivästytti merkitsevästi hoidon epäonnistumiseen kuluvaa aikaa verrattuna plaseboon (ks. kuva 2, p < 0,0001 log-rank-testillä). Mediaaniaika hoidon epäonnistumiseen oli 24,1 viikkoa plaseboa saaneilla potilailla. Adalimumabihoitoa saaneiden potilaiden mediaaniaikaa hoidon epäonnistumiseen ei voitu arvioida, koska alle puolella heistä hoito epäonnistui. Adalimumabi pienensi merkitsevästi hoidon epäonnistumisen riskiä 75 %:lla verrattuna plaseboon, kuten riskisuhde osoittaa (HR = 0,25 [95 % luottamusväli: 0,12, 0,49]).
Kuva 2: Hoidon epäonnistumiseen kulunut aika yhteenvetona Kaplan-Meier-käyrinä lasten uveiittitutkimuksessa
|
Immunogeenisuus
Anti-adalimumabivasta-aineita voi kehittyä adalimumabihoidon aikana. Anti-adalimumabivasta-aineiden muodostus tehostaa adalimumabin puhdistumaa ja heikentää sen tehoa.
Anti-adalimumabivasta-aineiden muodostuksen ja haittatapahtumien esiintymistiheyden välillä ei ole mitään selkeää yhteyttä.
Farmakokinetiikka
5.2 Farmakokineettiset ominaisuudet
Imeytyminen ja jakautuminen
Ihonalaisen 40 mg:n kerta-annoksen jälkeen adalimumabin imeytyminen ja jakautuminen oli hidasta, huippupitoisuus seerumissa saavutettiin n. 5 päivän kuluttua lääkkeen antamisesta. Kolmesta tutkimuksesta saatujen tulosten perusteella adalimumabin absoluuttisen biologisen hyötyosuuden arvioidaan olevan keskimäärin 64 % 40 mg:n ihonalaisen kerta-annoksen jälkeen. Laskimonsisäisten kerta-annosten (0,25-10 mg/kg) jälkeen pitoisuudet olivat annoksesta riippuvaisia. Puhdistuma 0,5 mg/kg:n annosten (~40 mg) jälkeen oli 11–15 ml/h, jakautumistilavuus (Vss) vaihteli 5–6 litran välillä ja terminaalivaiheen puoliintumisajan keskiarvo oli noin kaksi viikkoa. Useilla nivelreumapotilailla adalimumabin pitoisuudet nivelnesteessä olivat 31–96 % seerumista mitattaviin pitoisuuksiin verrattuna.
Ihonalaisen joka toinen viikko annetun 40 mg:n adalimumabikerta-annoksen jälkeen vakaan tilan pienin pitoisuus aikuisilla nivelreumapotilailla oli keskimäärin n. 5 µg/ml (jos samanaikaisesti ei käytetty metotreksaattia) tai 8–9 µg/ml (jos samanaikaisesti käytettiin metotreksaattia). Vakaassa tilassa seerumin pienin adalimumabipitoisuus suureni lähes annoksesta riippuvaisesti, kun valmistetta annettiin ihonalaisesti 20, 40 ja 80 mg joka toinen viikko tai viikoittain.
Aikuisilla psoriaasipotilailla vakaan tilan minimipitoisuuksien keskiarvo oli 5 μg/ml adalimumabimonoterapian aikana (40 mg joka toinen viikko).
Kun hidradenitis suppurativaa sairastaville aikuispotilaille annettiin 160 mg:n adalimumabiannos viikolla 0 ja sen jälkeen 80 mg viikolla 2, seerumin pienin adalimumabipitoisuus oli noin 7–8 μg/ml viikolla 2 ja viikolla 4. Vakaan tilan pienimpien pitoisuuksien keskiarvo (arvot viikoilta 12–36) oli noin 8–10 μg/ml, kun adalimumabia annettiin 40 mg kerran viikossa.
Adalimumabialtistus nuorilla HS-tautia sairastavilla potilailla arvioitiin käyttämällä populaatiofarmakokineettistä mallinnusta ja simulaatiota, jotka perustuivat muiden käyttöaiheiden farmakokinetiikkaan muilla lapsipotilailla (psoriaasi lapsilla, juveniili idiopaattinen artriitti, Crohnin tauti lapsilla ja entesiitteihin liittyvä artriitti). Nuorille HS-tautia sairastaville potilaille suositeltava annostus on 40 mg joka toinen viikko. Koska elimistön koko voi vaikuttaa adalimumabialtistukseen, nuoret, jotka painavat enemmän ja joiden vaste ei ole riittävä, saattavat hyötyä aikuisille suositellusta annoksesta 40 mg joka viikko.
Kun Crohnin tautia sairastaville potilaille annettiin 80 mg:n latausannos adalimumabia viikolla 0 ja sen jälkeen 40 mg viikolla 2, seerumin pienimmät adalimumabipitoisuudet olivat hoidon aloitusvaiheen aikana noin 5,5 µg/ml. Kun potilaille annettiin 160 mg:n latausannos adalimumabia viikolla 0 ja sen jälkeen 80 mg viikolla 2, seerumin pienimmät adalimumabipitoisuudet olivat hoidon aloitusvaiheen aikana noin 12 μg/ml. Vakaassa tilassa pienimmät pitoisuudet Crohnin tautia sairastavilla potilailla olivat keskimäärin noin 7 μg/ml, kun potilaat saivat 40 mg adalimumabia ylläpitoannoksena joka toinen viikko.
Keskivaikeaa tai vaikeaa Crohnin tautia sairastavien lapsipotilaiden avoin adalimumabiannos oli induktiohoidon viikoilla 0 ja 2 joko 160/80 mg (vähintään 40 kg painoiset) tai 80/40 mg (alle 40 kg painoiset). Viikolla 4 potilaat satunnaistettiin suhteessa 1:1 käyttämään ylläpitohoitoa painon mukaan joko tavanomaisina annoksina (40/20 mg joka toinen viikko) tai pieninä annoksina (20/10 mg joka toinen viikko). Seerumin pienimpien adalimumabipitoisuuksien keskiarvo (± keskihajonta) viikolla 4 oli 15,7 ± 6,6 µg/ml, jos potilas painoi ≥ 40 kg (160/80 mg), ja 10,6 ± 6,1 µg/ml, jos potilas painoi < 40 kg (80/40 mg).
Satunnaistettua hoitoaan jatkaneilla potilailla pienimpien adalimumabipitoisuuksien keskiarvo (± keskihajonta) viikolla 52 oli tavanomaisen annoksen ryhmässä 9,5 ± 5,6 µg/ml ja pienen annoksen ryhmässä 3,5 ± 2,2 µg/ml. Pienimpien pitoisuuksien keskiarvo pysyi ennallaan, kun potilaat jatkoivat adalimumabihoidon käyttöä joka toinen viikko 52 viikon ajan. Jos hoitoa tehostettiin ottamalla lääke joka viikko, seerumin adalimumabipitoisuuksien keskiarvo (± keskihajonta) oli viikolla 52 joko 15,3 ± 11,4 μg/ml (40/20 mg joka viikko) tai 6,7 ± 3,5 μg/ml (20/10 mg joka viikko).
Kun ulseratiivista koliittia sairastaville potilaille annettiin 160 mg:n latausannos adalimumabia viikolla 0 ja sen jälkeen 80 mg viikolla 2, seerumin pienimmät adalimumabipitoisuudet olivat hoidon aloitusvaiheen aikana noin 12 μg/ml. Vakaassa tilassa pienimmät pitoisuudet ulseratiivista koliittia sairastavilla potilailla olivat keskimäärin noin 8 μg/ml, kun potilaat saivat 40 mg adalimumabia ylläpitoannoksena joka toinen viikko.
Kun uveiittia sairastaville aikuispotilaille annettiin 80 mg:n latausannos adalimumabia viikolla 0 ja sen jälkeen 40 mg adalimumabia joka toinen viikko viikosta 1 alkaen, vakaan tilan pitoisuuden keskiarvo oli noin 8–10 μg/ml.
Adalimumabialtistus uveiittia sairastavilla lapsipotilaille arvioitiin käyttämällä populaatiofarmakokineettistä mallinnusta ja simulaatiota, jotka perustuivat muiden käyttöaiheiden farmakokinetiikkaan muilla lapsipotilailla (psoriaasi lapsilla, juveniili idiopaattinen artriitti, Crohnin tauti lapsilla ja entesiitteihin liittyvä artriitti). Kliinistä tietoa altistumisesta latausannokselle alle 6-vuotiailla lapsilla ei ole saatavilla. Ennustetut altistukset viittaavat siihen, että ilman metotreksaattia latausannos voi johtaa aluksi systeemisen altistuksen nousuun.
Populaatiofarmakokineettinen ja farmakokineettinen/farmakodynaaminen mallinnus ja simulaatio ennustivat adalimumabialtistuksen ja tehon olevan samaa luokkaa annoksella 40 mg kerran viikossa ja 80 mg joka toinen viikko (potilaina aikuisia, joilla oli nivelreuma, HS-tauti, ulseratiivinen koliitti, Crohnin tauti tai läiskäpsoriaasi, nuoria, joilla oli HS-tauti, sekä ≥ 40 kg painavia lapsipotilaita, joilla oli Crohnin tauti ja ulseratiivinen koliitti).
Altistus-vastesuhde lapsipotilailla
JIA-potilailla (pJIA ja ERA) saatujen kliinisten tutkimusten perusteella altistumis-vastesuhde todettiin plasmapitoisuuksien ja PedACR 50 -vasteen välillä. Havaittava adalimumabin pitoisuus plasmassa, joka aiheuttaa puolet todennäköisestä PedACR 50 - vasteiden enimmäismäärästä (EC50), oli 3 μg/ml (95 % luottamusväli 1-6 μg/ml).
Adalimumabipitoisuuden ja tehon välinen altistus-vastesuhde lapsipotilailla, joilla oli vaikea krooninen läiskäpsoriaasi, arvioitiin PASI 75 -vasteelle ja PGA puhdas/melkein puhdas -vasteelle. PASI 75 ja PGA puhdas/melkein puhdas -vasteet paranivat, kun adalimumabipitoisuus nousi. Havaittu EC50 oli sama, noin 4,5 μg/ml (95 % luottamusväli 0,4-47,6 [PASI 75] ja 1,9-10,5 [PGA]).
Eliminaatio
Farmakokineettisissä yli 1 300 nivelreumapotilasta käsittävissä väestötutkimuksissa havaittiin adalimumabin näennäisen puhdistuman lisääntyvän ruumiinpainon mukaan. Kun tulokset vakioitiin painoerojen suhteen, havaittiin sukupuolella ja iällä olevan ainoastaan minimaalinen vaikutus adalimumabin puhdistumaan. Vapaan adalimumabin (adalimumabin, joka ei ole sitoutunut adalimumabin vasta-aineisiin) pitoisuudet seerumissa todettiin pienemmiksi niillä potilailla, joilla oli mitattavissa olevat määrät adalimumabin vasta-aineita.
Maksan tai munuaisten vajaatoiminta
Adalimumabia ei ole tutkittu maksan tai munuaisten vajaatoimintaa sairastavilla potilailla.
Prekliiniset tiedot turvallisuudesta
Kerta-altistuksen aiheuttamaa toksisuutta, toistuvan altistuksen aiheuttamaa toksisuutta ja geenitoksisuutta koskevien tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille.
Makakiapinoilla tehdyssä alkion/sikiön kehitykseen kohdistuvaa toksisuutta/postnataalia kehitystä koskevassa tutkimuksessa ei havaittu adalimumabin aiheuttavan haittaa sikiölle annostasolla 0, 30 ja 100 mg/kg (9-17 apinaa/ryhmä). Adalimumabilla ei ole tehty karsinogeenisuustutkimuksia eikä fertiliteettiä tai postnataalitoksisuutta koskevia standardiarviointeja, koska ei ole saatavilla sopivia malleja, joissa vasta-aine reagoisi rajoitetusti ristiin jyrsijän TNF:n kanssa, ja koska jyrsijöissä kehittyy neutraloivia vasta-aineita.
Farmaseuttiset tiedot
Apuaineet
Etikkahappo
Natriumasetaattitrihydraatti
Glysiini
Polysorbaatti 80
Injektionesteisiin käytettävä vesi
Yhteensopimattomuudet
Koska yhteensopivuustutkimuksia ei ole tehty, tätä lääkevalmistetta ei saa sekoittaa muiden lääkevalmisteiden kanssa.
Kestoaika
3 vuotta
Säilytys
Säilytä jääkaapissa (2 °C – 8 °C). Ei saa jäätyä.
Pidä esitäytetty kynä ulkopakkauksessa valolta suojattuna.
Yksi esitäytetty Yuflyma-kynä voidaan säilyttää korkeintaan 25 °C:n lämpötilassa enintään 31 päivän ajan. Esitäytetty kynä tulee suojata valolta, ja se on hävitettävä, jos sitä ei käytetä 31 päivän aikana.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
YUFLYMA injektioneste, liuos, esitäytetty kynä
80 mg (L:ei) 0,8 ml (80 mg/0,8 ml) (101,29 €)
PF-selosteen tieto
Yuflyma 80 mg injektioneste, liuos esitäytetty kynä
Injektioneste, liuos esitäytetyssä kynässä (sisältäen esitäytetyn ruiskun) potilaan käyttöön. Kynän sisällä oleva ruisku on valmistettu tyypin 1 lasista, männän tulppa on bromibutyylikumia ja neulansuojus termoplastista elastomeeria.
Pakkaukset:
1 esitäytetty kynä (0,8 ml steriiliä liuosta) ja 2 alkoholityynyä.
Valmisteen kuvaus:
Kirkas tai hieman opalisoiva, väritön tai vaaleanruskea liuos.
Käyttö- ja käsittelyohjeet
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
YUFLYMA injektioneste, liuos, esitäytetty kynä
80 mg 0,8 ml
- Alempi erityiskorvaus (65 %). Abatasepti, adalimumabi, bimekitsumabi, etanersepti, golimumabi, guselkumabi, iksekitsumabi, infliksimabi, risankitsumabi, sarilumabi, sekukinumabi, sertolitsumabipegoli ja tosilitsumabi (tulehdukselliset reumasairaudet): Nivelreuman, juveniilin polyartriitin, psoriaasiin liittyvän niveltulehduksen, selkärankareuman tai edellä mainittuja niveltulehduksia läheisesti muistuttavan niveltulehduksen hoito erityisin edellytyksin / Tosilitsumabi: Aktiivisen yleisoireisen lastenreuman hoito erityisin edellytyksin (281).
- Rajoitettu peruskorvaus lääkärin lausunnolla (40 %). Abatasepti, adalimumabi, bimekitsumabi, etanersepti, golimumabi, guselkumabi, iksekitsumabi, infliksimabi, risankitsumabi, sarilumabi, sekukinumabi, sertolitsumabipegoli, tosilitsumabi ja ustekinumabi (tulehdukselliset reumasairaudet): Eräiden reumasairauksien hoito erityisin edellytyksin / Adalimumabi: Uveiitin hoito erityisin edellytyksin / Tosilitsumabi: Aktiivisen yleisoireisen lastenreuman ja jättisoluarteriitin hoito erityisin edellytyksin (313), Adalimumabi, bimekitsumabi, brodalumabi, etanersepti, guselkumabi, iksekitsumabi, infliksimabi, risankitsumabi, sekukinumabi, sertolitsumabipegoli, tildrakitsumabi ja ustekinumabi (ihopsoriaasi): Vaikean kroonisen ihopsoriaasin hoito erityisin edellytyksin (319), Adalimumabi, golimumabi, infliksimabi, risankitsumabi, ustekinumabi ja vedolitsumabi (tulehdukselliset suolistosairaudet): Eräiden suolistosairauksien hoito erityisin edellytyksin (326), Adalimumabi ja sekukinumabi: Keskivaikean ja vaikean aktiivisen hidradenitis suppurativan hoito erityisin edellytyksin (380).
- Oikeus käyttää samaa biologista lääkettä (sama kauppanimi) 6 kk ajan.
ATC-koodi
L04AB04
Valmisteyhteenvedon muuttamispäivämäärä
29.09.2025
Yhteystiedot
Energiakatu 4
00180 Helsinki
Suomi
+358 (0)29 170 7755
https://celltrionhealthcare.fi/
contact_fi@celltrionhc.com