GRASUSTEK injektioneste, liuos, esitäytetty ruisku 6 mg
Huomioitavaa
▼ Tähän lääkevalmisteeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan epäillyistä lääkkeen haittavaikutuksista. Ks. kohdasta Haittavaikutukset, miten haittavaikutuksista ilmoitetaan.
Vaikuttavat aineet ja niiden määrät
Yksi esitäytetty ruisku sisältää 6 mg pegfilgrastiimia* 0,6 ml:ssa injektionestettä liuosta varten. Pelkkään proteiiniin perustuva pitoisuus on 10 mg/ml.**
*Tuotettu Escherichia coli -soluissa yhdistelmä-DNA-tekniikalla ja konjugoitu sen jälkeen polyetyleeniglykoliin (PEG).
** Pitoisuus on 20 mg/ml, jos PEG-osa lasketaan mukaan.
Tämän valmisteen vahvuutta ei pidä verrata minkään muun samaan lääkeaineryhmään kuuluvan pegyloidun tai pegyloimattoman proteiinin vahvuuteen. Lisätietoja, ks. kohta Farmakodynamiikka.
Apuaineet, joiden vaikutus tunnetaan
Yksi esitäytetty ruisku sisältää 30 mg sorbitolia (E420) (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Injektioneste, liuos.
Kliiniset tiedot
Käyttöaiheet
Neutropenian keston lyhentäminen ja kuumeisen neutropenian ilmaantuvuuden vähentäminen aikuisilla potilailla, jotka saavat solunsalpaajia syövän hoitoon (lukuun ottamatta kroonista myelooista leukemiaa ja myelodysplastisia oireyhtymiä).
Ehto
Hoidon aloittavat onkologiaan ja/tai hematologiaan perehtyneet lääkärit ja hoito toteutetaan heidän valvonnassaan.
Annostus ja antotapa
Onkologiaan ja/tai hematologiaan perehtyneiden lääkäreiden pitää aloittaa pegfilgrastiimi-hoito ja valvoa sen toteutumista.
Annostus
Pegfilgrastiimin suositeltu annostus on 6 mg (yksi esitäytetty ruisku) kutakin solunsalpaajasykliä kohti vähintään 24 tuntia solunsalpaajalääkityksen jälkeen.
Erityisryhmät
Pediatriset potilaat
Pegfilgrastiimin turvallisuutta ja tehoa lasten hoidossa ei ole vielä varmistettu. Kohdissa Haittavaikutukset, Farmakodynamiikka ja Farmakokinetiikka kuvatun saatavilla olevan tiedon perusteella ei voida antaa suosituksia annostuksesta.
Potilaat, joilla on munuaisten vajaatoiminta
Annosta ei tarvitse muuttaa munuaisten vajaatoimintaa sairastaville potilaille, ei myöskään potilaille, joilla on loppuvaiheen munuaissairaus.
Antotapa
Grasustek annetaan injektiona ihon alle. Injektiot annetaan reiteen, vatsaan tai olkavarteen.
Ks. kohdasta Käyttö- ja käsittelyohjeet ohjeet lääkevalmisteen käsittelystä ennen lääkkeen antoa.
Vasta-aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille.
Varoitukset ja käyttöön liittyvät varotoimet
Jäljitettävyys
Biologisten lääkevalmisteiden jäljitettävyyden parantamiseksi on annetun valmisteen nimi ja eränumero dokumentoitava selkeästi.
Rajalliset kliiniset tutkimustulokset viittaavat siihen, että pegfilgrastiimilla on vastaavanlainen vaikutus potilaiden toipumisaikaan vaikeasta neutropeniasta kuin filgrastiimilla de novo akuutissa myelooisessa leukemiassa (ks. kohta Farmakodynamiikka). Pegfilgrastiimin pitkäaikaisvaikutuksia ei kuitenkaan ole vahvistettu akuutin myelooisen leukemian hoidossa, joten sen käytössä on noudatettava varovaisuutta tässä potilasryhmässä.
Granulosyyttikasvutekijä (G-CSF) voi edistää myeloidisten solujen kasvua in vitro, ja samankaltaisia vaikutuksia voi esiintyä myös joissakin ei-myeloidisissa soluissa in vitro.
Pegfilgrastiimin tehoa ja turvallisuutta ei ole tutkittu myelodysplastista oireyhtymää, kroonista myelogeenista leukemiaa eikä sekundaarista akuuttia myelooista leukemiaa (AML) sairastavien potilaiden hoidossa, eikä sitä pidä antaa näille potilaille. Erityistä huomiota on kiinnitettävä kroonisen myelooisen leukemian blastitransformaation erottamiseen akuutista myelooisesta leukemiasta.
Pegfilgrastiimin tehoa ja turvallisuutta ei ole osoitettu alle 55-vuotiaiden potilaiden hoidossa de novo akuutissa myelooisessa leukemiassa, johon liittyy sytogenetiikka t(15;17).
Pegfilgrastiimin tehoa ja turvallisuutta ei ole tutkittu suuriannoksista solunsalpaajahoitoa saavilla potilailla. Tätä lääkevalmistetta ei saa käyttää solunsalpaajien vakiintuneiden annostussuositusten ylittämiseen.
Keuhkoihin liittyvät haittatapahtumat
Keuhkoihin kohdistuneita haittavaikutuksia, erityisesti interstitiaalista pneumoniaa, on raportoitu G-CSF antamisen jälkeen. Näiden vaikutusten vaara voi olla suurempi potilailla, joilla on äskettäin ollut keuhkoinfiltraatteja tai keuhkokuume (ks. kohta Haittavaikutukset).
Keuhko-oireiden, kuten yskän, kuumeen ja hengenahdistuksen ilmaantuminen radiologisten keuhkoinfiltraattilöydösten yhteydessä sekä keuhkofunktion heikkeneminen samalla kun neutrofiilien määrä lisääntyy, voivat olla äkillisen hengitysvajausoireyhtymän (ARDS) esioireita. Tällaisessa tilanteessa pegfilgrastiimin käyttö pitää keskeyttää lääkärin harkinnan mukaan ja antaa asianmukaista hoitoa (ks. kohta Haittavaikutukset).
Glomerulonefriitti
Filgrastiimia ja pegfilgrastiimia saavilla potilailla on raportoitu glomerulonefriittiä. Yleensä glomerulonefriitti parani filgrastiimin tai pegfilgrastiimin annoksen pienentämisen tai hoidon lopettamisen jälkeen. Virtsatutkimuksia suositellaan tehtäväksi säännöllisin välein.
Kapillaarivuoto-oireyhtymä
Kapillaarivuoto-oireyhtymää on raportoitu granulosyyttikasvutekijöiden (G-CSF) antamisen jälkeen. Sen tyypillisiä oireita ovat hypotensio, hypoalbuminemia, turvotus ja hemokonsentraatio. Potilaita, joille kehittyy kapillaarivuoto-oireyhtymän oireita, on seurattava tarkoin ja annettava oireenmukaista hoitoa, tarvittaessa myös tehohoitoa (ks. kohta Haittavaikutukset).
Splenomegalia ja pernan repeämä
Pegfilgrastiimin antamisen jälkeen on esiintynyt yleensä oireetonta splenomegaliaa, ja pernan repeämiä, jotka ovat joissakin tapauksissa johtaneet kuolemaan (ks. kohta Haittavaikutukset). Pernan kokoa on sen vuoksi seurattava tarkoin (esim. tunnustelu, ultraäänitutkimus). Pernan repeämän mahdollisuus on otettava huomioon, jos potilaalla esiintyy kipua vasemmalla ylävatsassa tai olkapään yläosassa.
Trombosytopenia ja anemia
Pegfilgrastiimi-hoito yksinään ei estä trombosytopeniaa ja anemiaa, koska luuydintä lamaavaa solunsalpaajahoitoa jatketaan täysin annoksin määrätyn hoito-ohjelman mukaisesti. Trombosyytti- ja hematokriittiarvoja on seurattava säännöllisin välein. Erityistä varovaisuutta on noudatettava käytettäessä vaikeaa trombosytopeniaa aiheuttavia yksittäisiä solunsalpaajia tai niiden yhdistelmiä.
Myelodysplastinen oireyhtymä ja akuutti myelooinen leukemia rinta- ja keuhkosyöpäpotilailla
Markkinoille tulon jälkeisessä havainnoivassa tutkimuksessa pegfilgrastiimi annettuna samanaikaisesti
solunsalpaajien ja/tai sädehoidon kanssa on yhdistetty myelodysplastisen oireyhtymän (MDS) ja
akuutin myelooisen leukemian (AML) kehittymiseen rinta- ja keuhkosyöpäpotilailla (katso kohta Haittavaikutukset).
Rinta- ja keuhkosyöpä potilaita on seurattava myelodysplastisen oireyhtymän ja akuutin myelooisen leukemian merkkien ja oireiden varalta.
Sirppisoluanemia
Sirppisolukriisejä on esiintynyt pegfilgrastiimin käytön aikana potilailla, joilla on alttius sirppisolutautiin tai sirppisolutauti (ks. kohta Haittavaikutukset). Sen vuoksi on oltava varovainen, jos määrätään pegfilgrastiimia potilaille, joilla on alttius sirppisolutautiin tai sirppisolutauti, ja asianmukaisia kliinisiä parametrejä ja laboratorioarvoja on seurattava tarkoin, huomioiden erityisesti tämän lääkkeen mahdollinen yhteys pernan suurentumiseen ja vaso-okklusiiviseen kriisiin.
Leukosytoosi
Alle 1 %:lla pegfilgrastiimia saaneista potilaista on havaittu valkosoluarvoja, jotka ovat 100 ×109/l tai suurempia. Tämänasteiseen leukosytoosiin suoranaisesti liittyviä haittatapahtumia ei ole raportoitu. Tällainen valkosoluarvon nousu on ohimenevä, se todetaan yleensä 24–48 tunnin kuluttua lääkkeen antamisesta ja se on tämän lääkkeen farmakodynaamisten vaikutusten mukainen. Kliinisten vaikutusten ja mahdollisen leukosytoosin vuoksi valkosoluarvoa on seurattava säännöllisin välein hoidon aikana. Jos valkosoluarvo ylittää tason 50 × 109/l sen jälkeen, kun odotettu pohjalukema on saavutettu, tämän lääkkeen käyttö on lopetettava heti.
Yliherkkyys
Pegfilgrastiimia saavilla potilailla on raportoitu yliherkkyysoireita, myös anafylaktisia reaktioita, ensimmäisen tai myöhempien hoitojaksojen yhteydessä. pegfilgrastiimi-hoito on lopetettava pysyvästi, jos potilaalla havaitaan kliinisesti merkittävää yliherkkyyttä. Pegfilgrastiimia ei pidä antaa potilaille, joilla on aikaisemmin esiintynyt pegfilgrastiimi- tai filgrastiimiyliherkkyyttä. Mahdolliset vakavat allergiset reaktiot on hoidettava asianmukaisesti, ja potilaan tilaa on seurattava tarkoin useiden vuorokausien ajan.
Stevens–Johnsonin oireyhtymä
Stevens–Johnsonin oireyhtymää, joka voi olla hengenvaarallinen tai johtaa kuolemaan, on raportoitu pegfilgrastiimihoidon yhteydessä harvoin. Jos potilaalle on kehittynyt Stevens–Johnsonin oireyhtymä pegfilgrastiimin käytön yhteydessä, potilaalle ei saa enää koskaan antaa pegfilgrastiimihoitoa.
Immunogeenisuus
Immunogeenisuuden mahdollisuus on olemassa, kuten kaikkia proteiinilääkkeitä käytettäessä. Pegfilgrastiimin vasta-aineiden muodostuminen on yleensä vähäistä. Sitoutuvia vasta-aineita esiintyy, kuten on odotettavissa kaikkia biologisia lääkkeitä käytettäessä, mutta toistaiseksi niillä ei ole havaittu olevan neutraloivaa vaikutusta.
Aortan tulehdus
Aortan tulehdusta on raportoitu terveillä henkilöillä ja syöpäpotilailla G-CSF-annon jälkeen. Oireita voivat olla kuume, vastakipu, huonovointisuus, selkäkipu ja tulehdusmarkkereiden (esim. c-reaktiivinen proteiini ja valkosolujen määrä) kohoaminen. Useimmissa tapauksissa aortan tulehdus diagnosoitiin tietokonetomografialla ja se korjautui yleisesti itsestään G-CSF:n lopettamisen jälkeen. Ks. myös kohta Haittavaikutukset.
Muut varoitukset
Pegfilgrastiimin tehoa ja turvallisuutta veren kantasolujen mobilisaatiossa ei ole tutkittu riittävästi potilailla eikä terveillä luovuttajilla.
Kasvutekijähoidosta aiheutuvaan luuytimen hematopoieettisen aktiivisuuden lisääntymiseen on liittynyt ohimeneviä positiivisia löydöksiä luuston kuvantamistutkimuksissa. Tämä on otettava huomioon luuston kuvantamistuloksia tulkittaessa.
Apuaineet
Sorbitoli
Sorbitolia (tai fruktoosia) sisältävien muiden valmisteiden samanaikaisen annon sekä ravinnosta
saatavan sorbitolin (tai fruktoosin) additiivinen vaikutus on huomioitava.
Natrium
Tämä lääkevalmiste sisältää alle 1 mmol (23 mg) natriumia 6 mg:n annosta kohti eli käytännössä sen voidaan sanoa olevan ”natriumiton”.
Yhteisvaikutukset
Koska nopeasti jakautuvat myeloidiset solut saattavat olla herkkiä solunsalpaajille, Pegfilgrastiimi pitää antaa vähintään 24 tuntia solunsalpaajien antamisen jälkeen. Kliinisissä tutkimuksissa pegfilgratiimia on annettu turvallisesti 14 päivää ennen solunsalpaajalääkitystä. Pegfilgrastiimin samanaikaista käyttöä minkään solunsalpaajan kanssa ei ole tutkittu potilailla. Eläinkoemalleissa pegfilgrastiimin ja 5- fluorourasiilin (5‑FU) tai muiden antimetaboliittien samanaikaisen käytön on todettu voimistavan luuydinlamaa.
Mahdollisia yhteisvaikutuksia muiden hematopoieettisten kasvutekijöiden ja sytokiinien kanssa ei ole erityisesti tutkittu kliinisissä tutkimuksissa.
Yhteisvaikutuksen mahdollisuutta litiumin kanssa, joka myös edistää neutrofiilien vapautumista, ei ole erityisesti tutkittu. Ei ole osoitettu, että tämänkaltainen yhteisvaikutus olisi haitallinen.
Grasustekin tehoa ja turvallisuutta ei ole tutkittu potilailla, jotka saavat viivästynyttä luuydinlamaa aiheuttavia solunsalpaajia, esimerkiksi nitrosoureoita.
Erityisiä interaktio- tai metaboliatutkimuksia ei ole tehty; kliinisissä tutkimuksissa Grasustekilla ei kuitenkaan ole havaittu yhteisvaikutuksia minkään muun lääkevalmisteen kanssa.
Raskaus ja imetys
Raskaus
Ei ole olemassa tietoja tai on vain vähän tietoja pegfilgrastiimin käytöstä raskaana oleville naisille. Eläinkokeissa on havaittu lisääntymistoksisuutta (ks. kohta Prekliiniset tiedot turvallisuudesta). Grasustekin käyttöä ei suositella raskauden aikana eikä sellaisten naisten hoitoon, jotka voivat tulla raskaaksi ja jotka eivät käytä ehkäisyä.
Imetys
Ei ole riittävästi tietoa pegfilgrastiimin/metaboliittien erittymisestä ihmisen rintamaitoon. Vastasyntyneeseen/imeväiseen kohdistuvia riskejä ei voida poissulkea. On päätettävä, lopetetaanko rintaruokinta vai lopetetaanko Grasustek-hoito ottaen huomioon rintaruokinnasta aiheutuvat hyödyt lapselle ja hoidosta koituvat hyödyt äidille.
Hedelmällisyys
Pegfilgrastiimi ei vaikuttanut uros- eikä naarasrottien lisääntymistoimintoihin eikä hedelmällisyyteen kerran viikossa annettuina kumulatiivisina annoksina, jotka olivat noin 6–9 kertaa suurempia kuin ihmisille suositeltu annos (kehon pinta-alan perusteella) (ks. kohta Prekliiniset tiedot turvallisuudesta).
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Pegfilgrastiimilla ei ole haitallista vaikutusta tai sillä on vähäinen vaikutus ajokykyyn ja koneidenkäyttökykyyn.
Haittavaikutukset
Tiivistelmä turvallisuustiedoista
Useimmin raportoidut haittavaikutukset olivat luukipu (hyvin yleinen [≥ 1/10]) ja lihas- ja luustokipu (yleinen [≥ 1/100, < 1/10]). Luukipu oli yleensä lievää tai kohtalaista ja ohimenevää, ja se saatiin useimmiten hallintaan tavallisilla kipulääkkeillä.
Yliherkkyysreaktion tyyppisiä oireita, kuten ihottumaa, nokkosihottumaa, angioedeemaa, hengenahdistusta, ihon punoitusta, kasvojen ja kaulan punoitusta ja hypotensiota, on esiintynyt ensimmäisellä tai myöhemmillä hoitokerroilla pegfilgrastiimin yhteydessä (melko harvinainen [≥ 1/1 000, < 1/100]). Pegfilgrastiimia saavilla potilailla voi esiintyä vakavia allergisia reaktioita, myös anafylaksiaa (melko harvinainen) (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Solunsalpaajahoidossa olevilla syöpäpotilailla on raportoitu G-CSF:ien antamisen jälkeen melko harvoin (≥ 1/1 000, < 1/100) kapillaarivuoto-oireyhtymää, joka voi olla hengenvaarallinen, jos hoito viivästyy; ks. kohta Varoitukset ja käyttöön liittyvät varotoimet ja jäljempänä oleva kappale Tärkeimpien haittavaikutusten kuvaus.
Splenomegalia, yleensä oireeton, on melko harvinainen haittavaikutus.
Pegfilgrastiimin antamisen jälkeen on raportoitu melko harvoin pernan repeämiä, jotka ovat joissakin tapauksissa johtaneet kuolemaan (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Keuhkoihin kohdistuneita haittavaikutuksia, kuten interstitiaalista pneumoniaa, keuhkoedeemaa, keuhkoinfiltraatteja ja keuhkofibroosia, on raportoitu melko harvoin. Nämä ovat johtaneet melko harvoin hengitysvajaukseen tai ARD:hen, jotka voivat johtaa kuolemaan (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Yksittäisiä sirppisolukriisitapauksia on ilmoitettu potilailla, joilla on sirppisolupoikkeavuus tai sirppisolutauti (melko harvinainen haittavaikutus sirppisolupotilailla) (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Haittavaikutustaulukko
Alla olevan taulukon tiedot perustuvat kliinisissä tutkimuksissa raportoituihin haittavaikutuksiin ja spontaaneihin haittavaikutusilmoituksiin. Haittavaikutukset on esitetty kussakin yleisyysluokassa haittavaikutuksen vakavuuden mukaan alenevassa järjestyksessä.
Elinjärjestelmä MedDRA
| Haittavaikutukset | ||||
Hyvin yleinen (≥ 1/10) | Yleinen (≥ 1/100, < 1/10) | Melko harvinainen (≥ 1/1 000,< 1/100) | Harvinainen (≥1/10 000, < 1/1 000) | Hyvin harvinainen (< 1/10 000) | |
Hyvän- ja pahanlaatuiset kasvaimet (mukaan lukien kystat ja polyypit) | Myelodysplastinen oireyhtymä1 Akuutti myelooinen leukemia1 | ||||
Veri ja imukudos | Trombosytopenia1; Leukosytoosi1 | Sirppisoluanemiaan liittyvä kriisi2 ; Splenomegalia2; Pernan repeämä2 | |||
Immuunijärjestelmä | Yliherkkyysreaktiot; Anafylaksia | ||||
Aineenvaihdunta ja ravitsemus | Virtsahappoarvon kohoaminen | ||||
Hermosto | Päänsärky1 | ||||
Verisuonisto | Kapillaarivuoto-oireyhtymä1 | Aortiitti | |||
Hengityselimet, rintakehä ja välikarsina | Äkillinen hengitysvajausoire-yhtymä2 Keuhkoihin kohdistuvat haittavaikutukset (interstitiaalinen pneumonia, keuhkoedeema, keuhkoinfiltraatit ja keuhkofibroosi) Veriyskä | Keuhkoverenvuoto | |||
Ruoansulatus-elimistö | Pahoinvointi1 | ||||
Iho ja ihonalainen kudos | Sweetin oireyhtymä (akuutti kuumeinen neutrofiilinen dermatoosi)1,2; Ihon vaskuliitti1,2 | Stevens–Johnsonin oireyhtymä | |||
Luusto, lihakset ja sidekudos | Luukipu | Lihas- ja luustokipu (lihaskipu, nivelkipu, raajakipu, selkäkipu, lihas- ja luustokipu, niskakipu) | |||
Munuaiset ja virtsatiet | Glomerulonefriitti2 | ||||
Yleisoireet ja antopaikassa todettavat haitat | Injektiokohdan kipu1 Muu kuin sydänperäinen rintakipu | Injektiokohdan reaktiot2 | |||
Tutkimukset | Laktaattidehydrogenaasiarvon ja alkalisen fosfataasiarvon kohoaminen1 ALAT- tai ASAT- arvon ohimenevä kohoaminen maksan toimintakokeissa1 | ||||
1 Ks. jäljempänä oleva kappale Tärkeimpien haittavaikutusten kuvaus.
2 Tämä haittavaikutus todettiin markkinoille tulon jälkeisessä seurannassa, mutta sitä ei havaittu satunnaistetuissa kliinisissä vertailututkimuksissa aikuisilla. Yleisyysluokitus arvioitiin tilastollisella laskelmalla, joka perustui yhdeksässä satunnaistetussa kliinisessä tutkimuksessa pegfilgrastiimia saaneiden 1 576 potilaan tietoihin.
Tärkeimpien haittavaikutusten kuvaus
Sweetin oireyhtymää on raportoitu melko harvoin, ja joissakin tapauksissa taustalla olevat pahanlaatuiset verisairaudet ovat voineet vaikuttaa sen kehittymiseen.
Pegfilgrastiimilla hoidetuilla potilailla on raportoitu melko harvoin ihon vaskuliittia. Vaskuliitin syntymekanismia pegfilgrastiimia saaneilla potilailla ei tunneta.
Injektiokohdan reaktioita, kuten injektiokohdan punoitusta (melko harvinainen) sekä injektiokohdan kipua (yleinen), on esiintynyt ensimmäisen tai myöhempien pegfilgrastiimi-hoitokertojen yhteydessä.
Leukosytoosia (valkosoluarvo > 100 ×109/l) on raportoitu yleisesti (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet)
Melko harvoin esiintyi korjautuvaa lievää tai kohtalaista virtsahappoarvon ja alkalisen fosfataasiarvon nousua ja korjautuvaa lievää tai kohtalaista laktaattidehydrogenaasiarvon nousua, kun pegfilgrastiimia annettiin solunsalpaajalääkityksen jälkeen. Arvojen kohoamiseen ei liittynyt kliinisiä oireita.
Pahoinvointia ja päänsärkyä esiintyi hyvin yleisesti solunsalpaajahoitoa saaneilla potilailla.
Maksan toimintakokeissa on todettu melko harvoin kohonneita alaniiniaminotransferaasiarvoja (ALAT) tai aspartaattiaminotransferaasiarvoja (ASAT), kun potilaat ovat saaneet pegfilgrastiimia solunsalpaajahoidon jälkeen. Nämä ovat ohimeneviä muutoksia, ja arvot palautuvat lähtötasolle.
Rinta- ja keuhkosyöpäpotilailla tehdyssä epidemiologisessa tutkimuksessa on havaittu lisääntynyt myelodysplastisen oireyhtymän ja akuutin myelooisen leukemian riski pegfilgrastiimi-hoidon ja samanaikaisesti annettujen solunsalpaajien ja/tai sädehoidon jälkeen (katso kohta Varoitukset ja käyttöön liittyvät varotoimet).
Trombosytopeniaa on raportoitu yleisesti.
Kapillaarivuoto-oireyhtymää on raportoitu G-CSF käytön yhteydessä niiden markkinoille tulon jälkeen. Tapaukset on yleensä todettu potilailla, joilla on pitkälle edennyt pahanlaatuinen sairaus tai sepsis tai jotka saavat useita solunsalpaajia tai joille on tehty afereesi (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Pediatriset potilaat
Lääkkeen käytöstä lapsipotilaiden hoidossa on vain vähän kokemuksia. Vakavia haittavaikutuksia on todettu useammin nuoremmilla 0–5-vuotiailla lapsilla (92 %) kuin 6–11-vuotiailla (80 %) ja 12–21- vuotiailla (67 %) vanhemmilla lapsilla ja aikuisilla. Yleisin raportoitu haittavaikutus oli luukipu (ks. kohdat Farmakodynamiikka ja Farmakokinetiikka).
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Vakavia haittavaikutuksia ei havaittu, kun muutamille terveille tutkittaville ja ei-pienisoluista keuhkosyöpää sairastaville potilaille annettiin ihonalaisina kerta-annoksina 300 µg/kg. Haittatapahtumat olivat samanlaisia kuin pienempiä pegfilgrastiimiannoksia saaneilla potilailla.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: immunostimulantit, kasvutekijät; ATC-koodi: L03AA13.
Grasustek on ns. biosimilaari lääkevalmiste. Yksityiskohtaisempaa tietoa on saatavilla Euroopan lääkeviraston verkkosivulta http://www.ema.europa.eu.
Ihmisen granulosyyttiryhmiä stimuloiva kasvutekijä (G-CSF) on glykoproteiini, joka säätelee neutrofiilien muodostumista ja vapautumista luuytimestä. Pegfilgrastiimissa rekombinantti ihmisen G-CSF (r-metHuG-CSF) on kovalenttisesti konjugoitunut yhteen 20 kilodaltonin kokoiseen polyetyleeniglykolimolekyyliin (PEG). Pegfilgrastiimi on filgrastiimin pitkävaikutteinen muoto, jonka pitempi vaikutuksen kesto perustuu vähäisempään munuaispuhdistumaan. Pegfilgrastiimilla ja filgrastiimilla on osoitettu olevan samanlainen vaikutusmekanismi, joka suurentaa huomattavasti perifeerisen veren neutrofiilien määrää 24 tunnin kuluessa ja hieman monosyyttien ja/tai lymfosyyttien määrää. Kuten filgrastiimin, myös pegfilgrastiimin avulla muodostuneet neutrofiilit toimivat normaalisti tai normaalia tehokkaammin, mikä on osoitettu kemotaksista ja fagosytoosia mittaavilla testeillä. Muiden hematopoeettisten kasvutekijöiden tavoin G-CSF:lla on ihmisen endoteelisoluja stimuloivia ominaisuuksia in vitro. G-CSF voi edistää myeloidisten, myös pahanlaatuisten, solujen kasvua in vitro, ja samankaltaisia vaikutuksia saattaa esiintyä myös joissakin ei-myeloidisissa soluissa in vitro.
Kahdessa satunnaistetussa kaksoissokkoutetussa avaintutkimuksessa, jossa suuren riskin II–IV asteen rintasyöpää sairastavat potilaat saivat doksorubisiinia ja doketakselia sisältävää luuydintä lamaavaa solunsalpaajahoitoa, yksi pegfilgrastiimiannos solunsalpaajasykliä kohti lyhensi neutropenian kestoa ja vähensi kuumeisen neutropenian esiintymistä samassa määrin kuin todettiin annettaessa filgrastiimia päivittäin (kerran päivässä annettujen annosten lukumäärä 11 [mediaani]). Ilman kasvutekijätukea tämän hoito-ohjelman yhteydessä raportoidun 4. asteen neutropenian kesto on ollut 5–7 vuorokautta ja kuumeisen neutropenian ilmaantuvuus 30–40 %. Tutkimuksessa (n = 157), jossa käytettiin pegfilgrastiimia 6 mg:n vakioannoksena, 4. asteen neutropenian kesto (keskiarvo) oli pegfilgrastiimiryhmässä 1,8 vuorokautta ja filgrastiimiryhmässä 1,6 vuorokautta (ero 0,23 vuorokautta, 95 %:n luottamusväli –0,15, 0,63). Kuumeista neutropeniaa esiintyi koko tutkimusjakson aikana pegfilgrastiimia saaneessa ryhmässä 13 %:lla ja filgrastiimia saaneessa ryhmässä 20 %:lla potilaista (ero 7 %, 95 %:n luottamusväli –19 %, 5 %). Toisessa tutkimuksessa (n = 310), jossa käytettiin painonmukaista annosta (100 μg/kg), 4. asteen neutropenian kesto (keskiarvo) oli pegfilgrastiimiryhmässä 1,7 vuorokautta ja filgrastiimiryhmässä 1,8 vuorokautta (ero 0,03 vuorokautta, 95 %:n luottamusväli –0,36, 0,30).
Kuumeisen neutropenian kokonaisesiintyvyys oli pegfilgrastiimia saaneiden potilaiden ryhmässä 9 % ja filgrastiimia saaneiden ryhmässä 18 % (ero 9 %, 95 %:n luottamusväli –16,8 %, –1,1 %).
Rintasyöpäpotilaiden lumekontrolloidussa kaksoissokkotutkimuksessa arvioitiin pegfilgrastiimin vaikutusta kuumeisen neutropenian ilmaantuvuuteen sellaisen solunsalpaajahoidon jälkeen, jossa kuumeisen neutropenian esiintyvyys on yleensä 10–20 % (doketakseli 100 mg/m2 3 viikon välein 4 syklin ajan). Yhteensä 928 potilasta sai satunnaistetusti joko pegfilgrastiimia tai lumevalmistetta kerta-annoksena noin 24 tunnin kuluttua (2. päivänä) solunsalpaaja-annoksesta jokaisen syklin aikana. Kuumeista neutropeniaa esiintyi pegfilgrastiimiryhmään satunnaistetuilla potilailla vähemmän (1 %) kuin lumeryhmän potilailla (17 %, p < 0,001). Kliinisesti diagnosoituun kuumeiseen neutropeniaan liittyvä sairaalahoidon ja laskimonsisäisen infektiolääkityksen tarve oli pegfilgrastiimiryhmässä vähäisempi kuin lumeryhmässä (1 % ja 14 %, p < 0,001; ja 2 % ja 10 %, p < 0,001).
Pienessä (n = 83) 2. vaiheen satunnaistetussa kaksoissokkotutkimuksessa, jossa potilaat saivat solunsalpaajahoitoa de novo akuuttiin myelooiseen leukemiaan, induktiohoidon aikana annettua pegfilgrastiimia (6 mg kerta-annos) verrattiin filgrastiimiin. Toipumisajan vaikeasta neutropeniasta arvioitiin olevan molemmissa hoitoryhmissä 22 vuorokautta (mediaani). Pitkäaikaista hoitotulosta ei tutkittu (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Sarkoomaa sairastavien lapsipotilaiden 2. vaiheen (n = 37) satunnaistetussa avoimessa monikeskustutkimuksessa, jossa pegfilgrastiimia (100 μg/kg) annettiin vinkristiiniä, doksorubisiinia ja syklofosfamidia (VAdriaC/IE) sisältävän solunsalpaajahoidon 1. syklin jälkeen, vaikean neutropenian (neutrofiilimäärä < 0,5 × 109/l) kesto oli pitempi 0–5-vuotiailla nuoremmilla lapsilla (8,9 vrk) kuin 6–11-vuotiailla (6 vrk) ja 12–21-vuotiailla (3,7 vrk) vanhemmilla lapsilla ja aikuisilla. Lisäksi kuumeista neutropeniaa esiintyi enemmän nuoremmilla 0–5-vuotiailla lapsilla (75 %) kuin 6–11-vuotiailla (70 %) ja 12–21-vuotiailla (33 %) vanhemmilla lapsilla ja aikuisilla (ks. kohdat Haittavaikutukset ja Farmakokinetiikka).
Farmakokinetiikka
Ihonalaisen kerta-annoksen jälkeen pegfilgrastiimin huippupitoisuus seerumissa saavutetaan 16–120 tunnin kuluttua annoksesta, ja pegfilgrastiimin pitoisuudet seerumissa säilyvät luuydintä lamaavan solunsalpaajahoidon jälkeisen neutropenian keston ajan. Pegfilgrastiimi eliminoituu epälineaarisesti suhteessa annokseen; pegfilgrastiimin seerumipuhdistuma vähenee annoksen suurentuessa. Pegfilgrastiimi näyttää eliminoituvan pääasiassa neutrofiilivälitteisen puhdistuman kautta, mikä saturoituu suurempia annoksia käytettäessä. Itsesäätelevän puhdistumamekanismin mukaisesti pegfilgrastiimin pitoisuus seerumissa pienenee nopeasti neutrofiilimäärän alkaessa suurentua (ks. kuva 1).
Kuva 1. Seerumin pegfilgrastiimipitoisuuden ja absoluuttisen neutrofiilimäärän (ANC) mediaaniarvot 6 mg:n kertainjektion jälkeen potilailla, jotka ovat saaneet solunsalpaajahoitoa
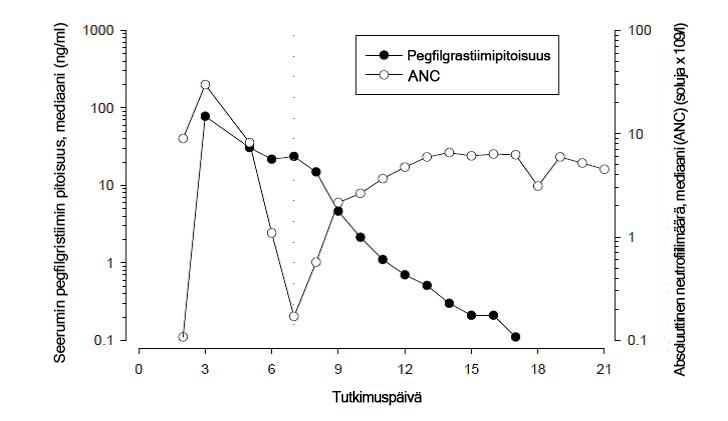
Neutrofiilivälitteisen puhdistumamekanismin vuoksi munuaisten tai maksan vajaatoiminnan ei odoteta vaikuttavan pegfilgrastiimin farmakokinetiikkaan. Eriasteinen munuaisten vajaatoiminta, mukaan lukien loppuvaiheen munuaissairaus, ei vaikuttanut pegfilgrastiimin farmakokinetiikkaan avoimessa kerta-annostutkimuksessa (n = 31).
Iäkkäät
Rajalliset tutkimustulokset osoittavat, että pegfilgrastiimin farmakokinetiikka on iäkkäillä (> 65‑ vuotiailla) samanlainen kuin muillakin aikuisilla.
Pediatriset potilaat
Pegfilgrastiimin farmakokinetiikkaa tutkittiin 37:llä sarkoomaa sairastavalla lapsipotilaalla, jotka saivat pegfilgrastiimia 100 μg/kg VAdriaC/IE-solunsalpaajahoidon päättymisen jälkeen. Pegfilgrastiimialtistuksen (AUC) keskiarvo (± keskihajonta) oli nuorimmassa ikäryhmässä (0–5‑ vuotiailla) suurempi (47,9 ± 22,5 μg·hr/ml) kuin 6–11-vuotiailla (22,0 ± 13,1 μg·hr/ml) ja 12–21‑ vuotiailla (29,3 ± 23,2 μg·hr/ml) vanhemmilla lapsilla (ks. kohta Farmakodynamiikka). Nuorinta ikäryhmää (0–5‑vuotiaita) lukuun ottamatta AUC:n keskiarvo näytti olevan lapsilla samanlainen kuin suuren riskin II–IV asteen rintasyöpää sairastavilla aikuisilla, jotka saivat pegfilgrastiimia 100 μg/kg doksorubisiini-/doketakselihoidon päättymisen jälkeen (ks. kohdat Haittavaikutukset ja Farmakodynamiikka).
Prekliiniset tiedot turvallisuudesta
Tavanomaisista toistuvilla annoksilla tehdyistä toksisuustutkimuksista saadut prekliiniset tiedot toivat esiin odotettuja farmakologisia vaikutuksia, joita olivat valkosolumäärän suureneminen, myeloidinen hyperplasia luuytimessä, ekstramedullaarinen hematopoieesi ja pernan suureneminen.
Jälkeläisillä ei havaittu haittavaikutuksia, kun tiineille rotille annettiin pegfilgrastiimia ihon alle, mutta kaniineilla pegfilgrastiimin on havaittu aiheuttavan alkio-/sikiötoksisuutta (alkionmenetyksiä), kun kumulatiiviset annokset olivat noin 4-kertaisia verrattuna ihmisille suositeltuun annokseen. Näitä vaikutuksia ei havaittu, kun tiineille kaniineille annettiin annoksia, jotka vastasivat ihmisille suositeltua annosta. Rotilla tehdyt tutkimukset ovat osoittaneet, että pegfilgrastiimi voi läpäistä istukan. Tutkimukset rotilla osoittivat, ettei ihon alle annettu pegfilgrastiimi vaikuttanut lisääntymistoimintoihin, hedelmällisyyteen, kiimakiertoon, pariuttamisen ja parittelun väliseen aikaan eikä sikiön elossaoloaikaan kohdussa. Näiden löydösten merkitystä ihmisen kannalta ei tunneta.
Farmaseuttiset tiedot
Apuaineet
Natriumasetaatti*
Sorbitoli (E420)
Polysorbaatti 20
Injektionesteisiin käytettävä vesi
*Natriumasetaatti on muodostunut väkevästä etikkahaposta ja natriumhydroksidista.
Yhteensopimattomuudet
Lääkevalmistetta ei saa sekoittaa muiden lääkevalmisteiden, varsinkaan natriumkloridiliuosten, kanssa.
Kestoaika
3 vuotta.
Säilytys
Säilytä jääkaapissa (2°C - 8°C).
Grasustek voidaan pitää huoneenlämmössä (ei yli 30°C) yhden kerran enintään 72 tunnin ajan.
Grasustek on hävitettävä, jos se on ollut huoneenlämmössä kauemmin kuin 72 tuntia.
Ei saa jäätyä. Alle 24 tuntia kestänyt, yhden kerran tapahtunut jäätyminen ei vaikuta haitallisesti Grasustekin säilyvyyteen.
Pidä pakkaus ulkopakkauksessa. Herkkä valolle.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
GRASUSTEK injektioneste, liuos, esitäytetty ruisku
6 mg 0,6 ml (444,05 €)
PF-selosteen tieto
Esitäytetty ruisku (tyypin I lasia), jossa on (butyyli)kumitulppa sekä ruostumattomasta teräksestä valmistettu neula, jossa on automaattinen turvamekanismi. Neulassa on joustava peräänantamaton neulansuojus.
Yksi esitäytetty ruisku sisältää 6 mg pegfilgrastiimia 0,6 ml:ssa injektionestettä liuosta varten. Pakkauksessa on 1 esitäytetty ruisku, jossa on automaattinen turvamekanismi (0,6 ml).
Valmisteen kuvaus:
Kirkas, väritön injektioneste, liuos.
Käyttö- ja käsittelyohjeet
Ennen Grasutekin antamista on tarkastettava silmämääräisesti, ettei liuoksessa ole hiukkasia. Vain kirkasta ja väritöntä liuosta saa antaa injektiona.
Voimakas ravistaminen voi aiheuttaa pegfilgrastiimin sakkautumisen, jolloin se muuttuu biologisesti tehottomaksi.
Anna esitäytetyn ruiskun manuaalista antoa varten lämmetä huoneenlämpötilaan 30 minuutin ajan ennen ruiskun käyttöä.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
GRASUSTEK injektioneste, liuos, esitäytetty ruisku
6 mg 0,6 ml
- Ei korvausta.
ATC-koodi
L03AA13
Valmisteyhteenvedon muuttamispäivämäärä
01.08.2022
Yhteystiedot
Spektri Business Park, Metsänneidonkuja 4
02130 Espoo
010 420 4000
www.medac.fi
info@medac.fi
