ILUVIEN implantaatti silmän lasiaiseen, asetin 190 mikrog
 Lääketurva
Lääketurva
Riskienminimointimateriaalit
Lääkäri
Hoito-opas sisältää ohjeet ILUVIEN-implantaatin käyttöön ja asettamiseen potilaalle sekä keskeiset turvallisuutta koskevat tiedot. Opastusvideo implantaatin oikeasta asettamistavasta on katsottavissa skannaamalla Hoito-oppaan kannessa oleva QR-koodi.
Potilas
Potilaan koulutusmateriaalissa kerrotaan hoidon riskeistä potilaalle, opastetaan potilasta tunnistamaan endoftalmiitin oireet ja muistutetaan seurantakäyntien tärkeydestä. Materiaalin sisältämät tiedot ovat kuunneltavissa äänitallenteena skannaamalla materiaalissa oleva QR-koodi.
Vaikuttavat aineet ja niiden määrät
Yksi implantaatti sisältää 190 mikrogrammaa fluosinoloniasetonidia.
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Implantaatti silmän lasiaiseen, asetin.
Kliiniset tiedot
Käyttöaiheet
Iluvien on tarkoitettu krooniseen diabeettiseen makulaturvotukseen liittyvän näön heikkenemisen hoitoon, kun vasteen muihin saatavilla oleviin hoitomuotoihin ei katsota olevan riittävä (ks. kohta Farmakodynamiikka).
Iluvien on tarkoitettu silmän takaosaan vaikuttavan toistuvan ei-infektiivisen uveiitin uusiutumisen estohoitoon (ks. kohta Farmakodynamiikka).
Annostus ja antotapa
Annostus
Suositeltu annos on yksi Iluvien-implantaatti hoidettavaan silmään. Implantaatin asettamista kumpaankin silmään samalla kertaa ei suositella (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Iluvien-implantaatista vapautuu fluosinoloniasetonidia jopa 36 kuukauden ajan.
Diabeettinen makulaturvotus
Lisäimplantaatti voidaan asettaa 12 kuukauden kuluttua, jos potilaan näkö on heikentynyt tai verkkokalvo on paksuuntunut diabeettisen makulaturvotuksen uusiutumisen tai pahenemisen seurauksena (ks. kohta Farmakodynamiikka).
Uutta implantaattia ei pidä asettaa, elleivät mahdolliset hyödyt ole riskejä suuremmat.
Iluvien-implantaatin saa asettaa vain, jos potilaan vaste aiempaan valopolttohoitoon tai diabeettisen makulaturvotuksen muihin saatavilla oleviin hoitoihin on ollut riittämätön.
Silmän takaosaan vaikuttava ei-infektiivinen uveiitti
Käytettäessä implantaatteja silmän takaosaan vaikuttavan toistuvan ei-infektiivisen uveiitin uusiutumisen estohoitoon lisäimplantaatilla toteutettavan uusintahoidon tueksi ei ole tietoja saatavissa.
Pediatriset potilaat
Ei ole asianmukaista käyttää silmän lasiaiseen annosteltavaa fluosinoloniasetonidia lasten diabeettisen makulaturvotuksen hoitoon.
Turvallisuutta ja tehoa lasten uveiitin hoidossa ei ole varmistettu.
Erityisryhmät
Iäkkäiden potilaiden ja potilaiden, joilla on munuaisten tai maksan vajaatoimintaa, annostusta ei tarvitse muuttaa.
Antotapa
VAIN SILMÄN LASIAISEEN.
Iluvien on tarkoitettu vain asetettavaksi silmän lasiaiseen, ja sen saa asettaa vain silmälääkäri, jolla on kokemusta silmän lasiaiseen annettavista injektioista. Valmiste on injisoitava silmän lasiaiseen kontrolloiduissa aseptisissa olosuhteissa, ja käytössä on oltava myös steriilit käsineet, steriili leikkausliina ja steriili luomenlevitin (tai vastaava). Potilaalle pitää antaa ennen injektiota riittävä puudutus ja laajakirjoista mikrobilääkettä.
Iluvien-valmiste injisoidaan seuraavasti:
- Silmään voidaan hoitavan silmälääkärin harkinnan mukaan tiputtaa ennen toimenpidettä antibioottitippoja.
- Tiputa injektiokohtaan (suositeltu injektiokohta inferotemporaalinen neljännes) juuri ennen injektiota yksi tippa paikallispuudutetta ja varmista sen jälkeen riittävä puudutus puuduteaineella kostutetun vanupuikon avulla tai antamalla puudutetta sidekalvon alle.
- Tiputa 2–3 tippaa sopivaa paikallisesti käytettävää antiseptista ainetta alaluomen pohjukkaan. Luomet voi puhdistaa paikallisesti käytettävällä antiseptisella aineella kostutetuilla vanupuikoilla. Aseta steriili luomenlevitin. Pyydä potilasta katsomaan ylöspäin ja aseta sopivalla antiseptisella aineella kostutettu vanupuikko injektiokohtaa vasten. Anna paikallisesti käytettävän antiseptisen aineen kuivua 30–60 sekunnin ajan ennen Iluvien-injektiota.
- Alustan ulkopintaa ei tarvitse pitää steriilinä pintana. Avustajan (ei-steriili) pitää poistaa alusta ulkopakkauksesta ja tarkastaa alusta ja sen kansi vaurioiden varalta. Jos vaurioita on, älä käytä kyseistä laitetta. Jos pakkaus on kunnossa, avustaja vetää alustan kannen pois koskettamatta sisäpintaa.
- Varmista esiladatun asettimen tarkistusikkunasta, että asettimen sisällä on lääkeimplantaatti.
- Ota asetin steriilein käsinein suojatuin käsin alustasta vain steriiliä pintaa ja asetinta koskettaen. Poista neulan suojakorkki vasta kun Iluvien on valmis injisoitavaksi. Pidä asettimen kärki ennen injektiota vaakatasoa ylempänä, jotta implantaatti pysyy asettimessa varmasti oikeassa asennossa.
- Implantaatti pitää asettaa kaksivaiheisesti, jotta voidaan vähentää implantaatin mukana kulkeutuvaa ilmamäärää. Ennen kuin pistät neulan silmään, paina painike alas ja liu’uta se ensimmäiseen pysäytyskohtaan (painikeuran kaarevien mustien merkkien kohdalle). Vapauta painike ensimmäisessä pysäytyskohdassa, jolloin se nousee YLÄasentoon. Jos painike ei nouse YLÄasentoon, älä käytä kyseistä laitetta.
- Implantaatin optimaalinen asetuskohta on näköhermon nystyn alapuolella ja silmän keskiviivan takana. Mittaa mittalaitteen avulla neljä millimetriä inferotemporaalisesti limbuksesta.
- Poista neulan suojakorkki varovasti ja tarkista, että neulankärki on suora.
- Siirrä sidekalvoa varovasti niin, että neulan sisäänvientikohdat sidekalvossa ja kovakalvossa eivät neulan poiston jälkeen ole enää samassa linjassa. Neulalla luomen reunaan tai silmäripsiin koskettamista on varottava tarkoin. Pistä neula silmään. Kun painike on YLÄasennossa, vapauta implantaatti liu’uttamalla painike eteenpäin painikeuran päähän asti ja vedä neula pois. Tärkeää: Varmista, että painike on painikeuran päässä ennen kuin vedät neulan pois.
- Poista luomenlevitin ja varmista epäsuoralla silmäntähystyksellä, että implantaatti on asettunut oikein, verkkokalvon keskusvaltimon perfuusio on riittävä ja ettei ole muita komplikaatioita. Implantaatti saattaa näkyä paremmin, jos kovakalvoa painetaan. Heti implantaatin injisoinnin jälkeen tehtävän tutkimuksen yhteydessä pitää tarkistaa näköhermon pään perfuusio. Silmänpaine voidaan mitata heti silmälääkärin harkinnan mukaan.
Potilasta pitää tarkkailla toimenpiteen jälkeen mahdollisten komplikaatioiden, kuten endoftalmiitin, kohonneen silmänpaineen, verkkokalvon irtoamisen ja lasiaisverenvuodon tai lasiaisen irtoamisen sekä matalan silmänpaineen (havaitaan 8 päivän kuluessa hoidon jälkeen), havaitsemiseksi. Toisen ja seitsemännen päivän välillä implantaatin injisoinnin jälkeen on tehtävä mittaus biomikroskooppiin kiinnitetyllä tonometrilla.
Potilasta suositellaan seuraamaan tämän jälkeen vähintään neljännesvuosittain mahdollisten komplikaatioiden havaitsemiseksi, koska fluosinoloniasetonidia vapautuu pitkään, noin 36 kuukauden ajan (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Vasta-aiheet
Iluvien-implantaatin asettaminen silmän lasiaiseen on vasta-aiheista, jos potilaalla on ennestään glaukooma tai aktiivinen tai epäilty silmän tai silmää ympäröivän alueen infektio, mukaan lukien useimmat sarveiskalvon ja sidekalvon virussairaudet, kuten aktiivinen epiteliaalinen herpes simplex ‑keratiitti (sarveiskalvon haarova pintatulehdus), lehmärokko, vesirokko, mykobakteeri-infektiot ja sienitaudit.
Iluvien on vasta-aiheista
- jos potilas on yliherkkä vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille
- jos potilaalla on infektiivinen uveiitti.
Varoitukset ja käyttöön liittyvät varotoimet
Silmän lasiaiseen annettaviin injektioihin on liittynyt endoftalmiittia, kohonnutta tai alentunutta silmänpainetta, verkkokalvon irtoaminen ja lasiaisverenvuotoa tai lasiaisen irtoaminen. Potilasta pitää kehottaa ilmoittamaan viipymättä kaikista endoftalmiittiin viittaavista oireista. Kun potilaan vointi tarkistetaan 2–8 päivän kuluttua injektiosta, silmäinfektio, kohonnut tai alentunut silmänpaine tai muu komplikaatio voidaan tunnistaa ja hoitaa varhaisvaiheessa. Silmänpainetta suositellaan seuraamaan tämän jälkeen vähintään neljännesvuosittain.
Silmän lasiaiseen annettavat kortikosteroidit saattavat aiheuttaa kaihia, kohonnutta silmänpainetta tai glaukooman ja saattavat lisätä hoidosta aiheutuvien infektioiden riskiä.
Iluvien-implantaatin turvallisuutta ja tehoa kumpaankin silmään samalla kertaa asetettuna ei ole tutkittu. Implantaatin asettamista kumpaankin silmään samalla kertaa ei suositella. Kummankin silmän samanaikaista hoitoa ei suositella ennen kuin potilaan systeeminen ja silmässä todettava vaste ensimmäiseen implantaattiin on tiedossa (ks. kohta Annostus ja antotapa).
Näköhäiriö
Systeemisesti tai topikaalisesti käytettävien kortikosteroidien käytön yhteydessä saatetaan ilmoittaa näköhäiriöistä. Jos potilaalla esiintyy oireita, kuten näön hämärtymistä tai muita näköhäiriöitä, potilas on ohjattava silmälääkärille, joka arvioi oireiden mahdolliset syyt. Niitä voivat olla kaihi, glaukooma tai harvinaiset sairaudet, kuten sentraalinen seroosi korioretinopatia, joista on ilmoitettu systeemisten tai topikaalisten kortikosteroidien käytön jälkeen.
Diabeettista makulaturvotusta koskevat vaiheen 3 tutkimukset (FAME)
80 %:lle fluosinoloniasetonidilla hoidetuista faakkisista potilaista tehtiin kaihileikkaus (ks. kohta Haittavaikutukset). Faakkista potilasta on hoidon jälkeen seurattava tarkoin kaihen merkkien varalta.
38 % fluosinoloniasetonidilla hoidetuista potilaista tarvitsi silmänpainetta alentavaa lääkitystä (ks. kohta Haittavaikutukset). Fluosinoloniasetonidin käytössä pitää olla varovainen, jos potilaan silmänpaine on korkea ennen hoitoa, ja silmänpainetta pitää seurata tarkasti. Jos silmänpaine nousee eikä reagoi silmänpainetta alentaviin lääkkeisiin tai silmänpainetta alentaviin toimenpiteisiin, Iluvien-implantaatti voidaan poistaa vitrektomialla.
24 % lumehoitoryhmän tutkittavista sai jossakin vaiheessa hoitoa joko antikoagulantilla tai trombosyyttien toimintaa estävillä lääkeaineilla verrattuna 27 %:iin Iluvien-hoitoa saaneen ryhmän tutkittavista. Jos tutkittavalle asetettiin Iluvien-implantaatti antikoagulantin tai trombosyyttien toimintaa estävien lääkkeiden käytön aikana tai 30 päivän kuluessa tällaisen lääkehoidon lopettamisesta, tutkittavilla esiintyi hieman yleisemmin sidekalvon verenvuotoa verrattuna lumehoitoa saaneisiin tutkittaviin (0,5 % lumehoitoa saaneilla ja 2,7 % Iluvien-hoitoa saaneilla). Ainoa muu Iluvien-hoitoa saaneilla potilailla yleisemmin raportoitu tapahtuma oli silmäleikkauskomplikaatiot (0 % lumehoitoa saaneilla ja 0,3 % Iluvien-hoitoa saaneilla).
Fluosinoloniasetonidin vaikutuksesta silmiin lasiaisen poiston jälkeen on vähän kokemusta. Lasiaisen poiston jälkeen lääkkeen puhdistuma todennäköisesti nopeutuu, mutta vakaan tilan pitoisuuksiin se ei oletettavasti vaikuta. Tämä voi lyhentää implantaatin vaikutuksen kestoa.
Uveiittia koskevat vaiheen 3 tutkimukset
Fluosinoloniasetonidihoitoa lasiaiseen asetettavalla implantaatilla hoitoa uveiittitutkimuksissa saaneille potilaille tehtiin kaihileikkaus. Faakkisia potilaita pitää seurata tarkoin kaihin oireiden havaitsemiseksi hoidon jälkeen.
Lisäksi joidenkin potilaiden silmänpaine kohosi ja vaati silmänpainetta alentavaa lääkehoitoa.
Tutkimuksissa fluosinoloniasetonidihoitoa saaneille potilaille kehittyi hypotonia, joka ilmeni hoidon jälkeisinä päivinä, monilla 1. päivänä ja hävisi useimmiten 1 viikon kuluessa ilmenemisestä. Potilaan silmänpaineen kohoamista tai alenemista suositellaan seuraamaan heti injektion jälkeen sekä 2.–8. päivänä injektion jälkeen.
Uveiittipotilaiden hoidossa on erittäin tärkeää sulkea pois uveitiin mahdollinen infektiivinen syy ennen Iluvien-hoidon aloittamista.
Implantaatti voi kulkeutua silmän etukammioon, etenkin jos potilaalla ei ole mykiön takakoteloa tai takakotelo on viallinen tai siinä on repeämä silmäleikkausten jälkeen. Hoitamattomasta implantaatin siirtymisestä voi aiheutua sarveiskalvoturvotusta, ja vaikea-asteisissa tapauksissa se voi johtaa sarveiskalvosiirteen vaativaan sarveiskalvovaurioon. Jos potilaalla on näköhäiriöitä, hänet on tutkittava implantaatin siirtymisen toteamiseksi ja hoitamiseksi varhaisvaiheessa.
Yhteisvaikutukset
Yhteisvaikutustutkimuksia ei ole tehty.
Raskaus ja imetys
Raskaus
Silmän lasiaiseen annetun fluosinoloniasetonidin käytöstä raskaana oleville naisille on vähän tietoja. Ei ole tehty riittäviä eläinkokeita silmän lasiaiseen annetun fluosinoloniasetonidin aiheuttaman lisääntymistoksisuuden selvittämiseksi (ks. kohta Prekliiniset tiedot turvallisuudesta). Vaikka silmään paikallisesti annettu fluosinoloniasetonidi ei ole todettavissa isossa verenkierrossa hoidon jälkeen, se on silti vahva kortikosteroidi, ja jo hyvin pieni systeeminen altistus voi olla jonkinasteinen riski kehittyvälle sikiölle. Varotoimena suositellaan Iluvien-valmisteen käytön välttämistä raskaana olevalle potilaalle.
Imetys
Systeemisesti annettu fluosinoloniasetonidi erittyy rintamaitoon. Vaikka fluosinoloniasetonidin anto silmän lasiaiseen aiheuttaa imettävässä naisessa odotettavasti vain hyvin vähäisen systeemisen altistuksen, on joko keskeytettävä rintaruokinta tai pidättäydyttävä Iluvien-hoidosta sen mukaan, mikä on lapsen rintaruokinnasta saama hyöty ja naisen hoidosta saama hyöty.
Hedelmällisyys
Hedelmällisyyteen liittyviä tietoja ei ole saatavilla. Valmiste ei todennäköisesti vaikuta kummankaan sukupuolen hedelmällisyyteen, koska fluosinoloniasetonidin silmän lasiaiseen annosta aiheutuva systeeminen altistus on hyvin vähäinen.
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Iluvien-valmisteella on vähäinen vaikutus ajokykyyn ja koneiden käyttökykyyn. Potilailla saattaa esiintyä tilapäistä näön heikkenemistä Iluvien-implantaatin asettamisen jälkeen, joten potilaan pitää olla ajamatta autoa ja käyttämättä koneita, kunnes näkökyky on palautunut.
Haittavaikutukset
Turvallisuusprofiilin yhteenveto
Diabeettinen makulaturvotus
Silmän lasiaiseen annettavaa fluosinoloniasetonidia tutkittiin kliinisten FAME-tutkimusten aikana 768 tutkittavalla (375:llä ryhmässä, jossa Iluvien-annos oli 0,2 mikrog/vrk, ja 393:lla ryhmässä, jossa Iluvien-annos oli 0,5 mikrog/vrk), joilla oli diabeettista makulaturvotusta. Yleisimmin raportoidut haittavaikutukset olivat kaihileikkaus, kaihi ja kohonnut silmänpaine.
Vaiheen 3 tutkimuksissa 38,4 % Iluvien-hoitoa saaneista tutkittavista tarvitsi silmänpainetta alentavaa lääkitystä ja 4,8 % tarvitsi silmänpainetta alentavan leikkauksen. Silmänpainetta alentavan lääkehoidon käytössä ei ollut eroja niiden tutkittavien välillä, jotka olivat saaneet vähintään kaksi Iluvien-hoitoa.
Iluvien-hoitoa saaneilla tutkittavilla raportoitiin vaiheen 3 tutkimusten aikana kaksi endoftalmiittitapausta. Ilmaantuvuus on tällöin 0,2 % (2 tapausta 1022 injektiota kohden).
Koska suurin osa kliinisten FAME-tutkimusten tutkittavista sai vain yhden implantaatin (ks. kohta Farmakodynamiikka), silmän sisälle jääneiden biohajoamattomien implantaattien pitkän aikavälin turvallisuutta koskevia vaikutuksia ei tunneta. Kliinisten FAME-tutkimusten kolme vuotta kattavat tiedot osoittavat, että kaihia, kohonnutta silmänpainetta ja lasiaiskellujia esiintyi vain hieman yleisemmin tutkittavilla, jotka saivat vähintään kaksi implantaattia. Tämän katsotaan johtuvan pikemminkin lisääntyneestä altistuksesta lääkkeelle kuin itse implantaatin vaikutuksesta. Ei-kliinisissä tutkimuksissa ei todettu muita viitteitä turvallisuutta koskevien ongelmien lisääntymisestä kuin mykiömuutokset kaniinien silmissä, kun niillä oli 2–4 implantaattia 24 kuukauden aikana. Implantaatti on valmistettu polyimidistä, ja se on oleellisesti samankaltainen kuin tekomykiön haptiikkaosa, minkä vuoksi siitä ei oleteta aiheutuvan reaktioita silmän sisällä.
Silmän takaosaan vaikuttava ei-infektiivinen uveiitti
Silmän takaosaan vaikuttavan ei-infektiivisen uveiitin turvallisuusprofiili perustuu kahteen 36 kuukautta kestäneeseen uveiittia koskeneeseen pivotaalitutkimukseen (PSV-FAI-001 ja PSV-FAI-005). Tietoja on tällä hetkellä saatavana 36 kuukauden ajanjaksolta tutkimuksesta PSV-FAI-001 ja 12 kuukauden ajanjaksolta tutkimuksesta PSV-FAI-005. Yleisimmin raportoituja haittavaikutuksia olivat kohonnut silmänpaine, kaihi ja sidekalvon verenvuoto. Harvemmin raportoituja, mutta vakavampia, haittavaikutuksia olivat näköhermon nystyn verenvuoto ja verkkokalvon irtauma.
Haittavaikutusluettelo
Seuraavien vaiheen III kliinisissä tutkimuksissa (diabeettinen makulaturvotus ja uveiitti) ja spontaanisti raportoitujen haittavaikutusten arvioitiin liittyvän hoitoon, ja ne on luokiteltu seuraavasti: hyvin yleinen (≥ 1/10), yleinen (≥ 1/100, < 1/10), melko harvinainen (≥ 1/1 000, < 1/100), harvinainen (≥ 1/10 000, < 1/1 000) ja hyvin harvinainen (< 1/10 000). Haittavaikutukset on esitetty kussakin yleisyysluokassa haittavaikutuksen vakavuuden mukaan alenevassa järjestyksessä.
Infektiot | Melko harvinainen: endoftalmiitti |
Hermosto | Melko harvinainen: päänsärky |
Silmät | Hyvin yleinen: kaihi1, kohonnut silmänpaine2 Yleinen: glaukooma3, verkkokalvon irtauma, näköhermon nystyn verenvuoto*, lasiaisverenvuoto, heikentynyt näöntarkkuus, skotooma*, makulan fibroosi*, sidekalvon verenvuoto4, näön hämärtyminen (ks. myös kohta Varoitukset ja käyttöön liittyvät varotoimet)5, matala silmänpaine6, lasiaiskellujat7, silmän etukammion solut*, lasiaissamentuma*, rikantunne silmässä*, kuivat silmät*, fotopsia*, silmäkipu8 Melko harvinainen: verkkokalvon suonitukos9, näköhermon häiriö, makulopatia, näköhermon surkastuma, sidekalvon haavauma, iiriksen uudissuonittuminen, tulehdusnesteen tihkuminen verkkokalvosta, lasiaisen rappeuma, lasiaisen irtauma, suonikalvon irtauma*, sarveiskalvon eroosio*, kertymät sarveiskalvossa, mykiönkotelon samentuminen, iiriksen kiinnikkeet, blefarospasmi*, silmän turvotus*10, silmän hyperemia, kovakalvon oheneminen, silmän eritevuoto, silmän kutina |
Vammat ja myrkytykset | Melko harvinainen: implantaatin työntyminen ulos silmästä, implantaatti näkökentässä, toimenpiteestä aiheutuva komplikaatio, toimenpiteeseen liittyvä kipu |
Kirurgiset ja lääketieteelliset toimenpiteet | Hyvin yleinen: kaihileikkaus Yleinen: trabekulektomia, glaukoomaleikkaus, vitrektomia, trabekuloplastia Melko harvinainen: ulos työntyneen implantaatin poisto kovakalvosta |
Yleisoireet ja antopaikassa todettavat haitat | Melko harvinainen: laitteen siirtyminen pois paikoiltaan (implantaatin siirtyminen), josta voi aiheutua sarveiskalvoturvotusta |
* Havaittu vain uveiittipotilailla
1 Sisältää MedDRA-termit kaihi (määrittämätön), subkapsulaarinen kaihi, kuorikaihi, tumakaihi ja diabeteskaihi.
2 Sisältää MedDRA-termit kohonnut silmänsisäinen paine ja okulaarinen hypertensio
3 Sisältää MedDRA-termit glaukooma, avokulmaglaukooma, rajalaatuinen glaukooma, näköhermon nystyn kovertuminen ja suurentunut näköhermon nystyn kuopan ja näköhermon nystyn suhde.
4 Sisältää MedDRA-termit sidekalvon verenvuoto, sidekalvon hyperemia.
5 Sisältää MedDRA-termit sumentunut näkö ja näkökyvyn heikentyminen.
6 Sisältää MedDRA-termit alentunut silmänpaine.
7 Sisältää MedDRA-termit myiodesopsia.
8 Sisältää MedDRA-termit silmäkipu, silmän ärsytys ja epämukava tunne silmässä.
9 Sisältää MedDRA-termit verkkokalvon laskimotukos, verkkokalvon valtimotukos ja verkkokalvon verisuonitukos.
10 Sisältää MedDRA-termit silmän turvotus, sidekalvon turvotus, sarveiskalvon turvotus.
Valittujen haittavaikutusten kuvaus
Kortikosteroidien pitkäaikainen käyttö voi aiheuttaa kaihia ja kohonnutta silmänpainetta. Seuraavassa esitetyt yleisyydet kuvastavat kaikkien FAME-tutkimuksissa mukana olleiden potilaiden löydöksiä. Havaitut yleisyydet potilailla, joilla on kroonista diabeettista makulaturvotusta, eivät eronneet merkittävästi koko potilasjoukon löydöksistä.
Diabeettista makulaturvotusta koskevat vaiheen 3 tutkimukset
Kaihin ilmaantuvuus faakkisille potilaille oli vaiheen 3 kliinisissä lääketutkimuksissa Iluvien-hoitoa saaneilla tutkittavilla noin 82 % ja lumehoitoa saaneilla tutkittavilla 50 %. Iluvien-hoitoa saaneista faakkisista potilaista 80 % tarvitsi kaihileikkauksen 3. vuoteen mennessä. Lumehoitoa saaneiden tutkittavien vastaava osuus oli 27 %, joista useimmat potilaat tarvitsivat leikkauksen 21. kuukauteen mennessä. Posteriorinen subkapsulaarinen kaihi on yleisin kortikosteroidihoitoon liittyvä kaihityyppi. Tämän tyyppisen kaihin leikkaus on vaikeampi, ja siihen voi liittyä suurempi leikkauskomplikaatioiden riski.
Diabeettista makulaturvotusta koskeneisiin -tutkimuksiin ei otettu mukaan tutkittavia, joiden silmänpaine oli lähtötilanteessa > 21 mmHg. Kohonnutta silmänpainetta esiintyi 37 %:lla tutkittavista, ja 38 % tutkittavista tarvitsi silmänpainetta alentavaa lääkitystä, ja puolet näistä tarvitsi ainakin kahta lääkettä silmänpaineen saamiseksi hallintaan. Silmänpainetta alentavan lääkehoidon käyttö oli samankaltaista tutkittavilla, joille asetettiin tutkimuksen aikana uusintahoitona lisäimplantaatti. Lisäksi 5,6 % (21/375) tutkittavista, joille implantaatti asetettiin, tarvitsi kirurgisen tai lasertoimenpiteen silmänpaineen saamiseksi hallintaan (trabekuloplastia 5 [1,3 %], trabekulektomia 10 [2,7 %], endosykloablaatio 2 [0,5 %] ja muut kirurgiset toimenpiteet 6 [1,6 %]).
Niiden potilaiden osajoukossa, joiden silmänpaine oli lähtötilanteessa mediaania korkeampi (≥ 15 mmHg), 47 % tarvitsi silmänpainetta alentavaa lääkehoitoa, ja kirurgisten tai lasertoimenpiteiden osuus nousi 7,1 %:iin. Tässä osajoukossa 5 (2,2 %) tutkittavaa hoidettiin trabekuloplastialla, 7 (3,1 %) trabekulektomialla, 2 (0,9 %) endosykloablaatiolla ja 4 (1,8 %) muilla glaukooman kirurgisilla toimenpiteillä.
Uveiittia koskevat vaiheen 3 tutkimukset
Taulukko 1. Silmänpainetta, kaihia ja hypotoniaa koskevat haittavaikutukset tutkimusten PSV-FAI-001 ja PSV-FAI-005 hoitoaikeen mukaisissa (intention-to-treat, ITT) potilasjoukoissa
Hoitoaikeen mukainen potilasjoukko | ||||
| PSV-FAI-001 (36 kuukautta) | PSV-FAI-005 (12 kuukautta) | ||
| Fluosinoloniasetonidi-implantaatti | Lumeinjektio | Fluosinoloniasetonidi-implantaatti | Lumeinjektio |
Satunnaistettujen tutkittavien lukumäärä | 87 | 42 | 101 | 52 |
Altistuksen kesto (vrk), keskiarvo (keskihajonta) | 1055 (139,47) | 1029 (191,09) | 354 (37,56) | 354 (37,56) |
Silmänpainetta alentava lääkitys, n (%) | 37 (42,5) | 14 (33,3) | 51 (50,5) | 27 (51,9) |
Silmänpaine > 25 mmHg, n (%) | 21 (24,1) | 10 (23,8) | 22 (21,8) | 2 (3,8) |
Silmänpaine > 30 mmHg, n (%) | 14 (16,1) | 5 (11,9) | 15 (14,9) | 1 (1,9) |
Silmänpainetta alentava leikkaus, n (%) | 5 (5,7) | 5 (11,9) | 1 (1,0) | 0 |
Silmänpainetta koskeva haittavaikutus, n (%) | 28 (32,2) | 13 (31,0) | 30 (29,7) | 1 (1,9) |
Kaihileikkaus, n (% perustuu faakkisiin potilaisiin) | 31 (73,8) | 5 (23,8) | 11 (18) | 4 (11,4) |
Kaihia koskeva haittavaikutus, n (%) | 37 (42,5) | 10 (23,8) | 29 (47,5) | 11 (31,4) |
Hypotonia, n (%) | 9 (10,3) | 5 (11,9) | 13 (12,9) | 0 (0,0) |
Uveiittia koskeneiden vaiheen 3 tutkimusten fluosinoloniasetonidia saaneessa ryhmässä ei esiintynyt endoftalmiittia.
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty‐haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www‐sivusto: www.fimea.fi
Lääkealan turvallisuus‐ ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Yliannostustapauksia ei ole raportoitu.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Tulehduslääkkeet, kortikosteroidit
ATC-koodi: S01BA15
Kortikosteroidit estävät inflammatorista vastetta moniin erilaisiin tulehduksenaiheuttajiin. Ne estävät tulehdukseen liittyvää turvotusta, fibriinin kertymistä, hiussuonten laajenemista, leukosyyttien migraatiota, hiussuonten proliferaatiota, fibroblastien proliferaatiota, kollageenin kertymistä ja arpeutumista.
Kortikosteroidien oletetaan vaikuttavan indusoimalla fosfolipaasi A:ta estäviä proteiineja, joita kutsutaan yhteisnimellä lipokortiinit. Näiden proteiinien oletetaan säätelevän voimakkaiden tulehduksenvälittäjäaineiden, kuten prostaglandiinien ja leukotrieenien, biosynteesiä estämällä niiden yhteisen esiasteen, arakidonihapon, vapautumista. Arakidonihappo vapautuu fosfolipaasi A2:n vaikutuksesta solukalvon fosfolipideistä. Kortikosteroidien on osoitettu myös pienentävän verisuonten läpäisevyyttä lisäävän ja turvotusta aiheuttavan proteiinin endoteelikasvutekijän pitoisuutta.
Diabeettinen makulaturvotus
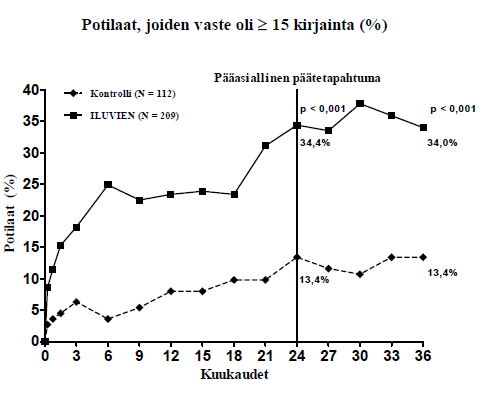
Iluvienin tehoa on arvioitu kahdessa satunnaistetussa, kaksoissokkoutetussa rinnakkaisryhmillä toteutetussa monikeskustutkimuksessa, joihin osallistuneilla potilailla oli diabeettista makulaturvotusta ja joita oli vähintään kerran aiemmin hoidettu valopolttohoidolla. Potilaita seurattiin kummassakin tutkimuksessa kolmen vuoden ajan. 74,4 % tutkittavista sai hoitona yhden implantaatin, 21,6 % sai kaksi implantaattia, 3,5 % sai kolme implantaattia ja 0,5 % sai neljä implantaattia (ja 0 % sai yli neljä implantaattia). Tehon ensisijainen päätetapahtuma oli kummassakin tutkimuksessa niiden potilaiden osuus, joiden näkö parani 24 kuukauden jälkeen 15 kirjainta tai enemmän. Iluvien-hoidolla saavutettiin kummassakin tutkimuksessa ensisijainen päätetapahtuma (ks. kuvasta 1 tehon ensisijaisen päätetapahtuman yhdistetyt tulokset).
Kuva 1: Niiden potilaiden osuus, joiden näöntarkkuus parani lähtötilanteesta ≥ 15 kirjainta (FAME-tutkimusten yhdistetyt tulokset)
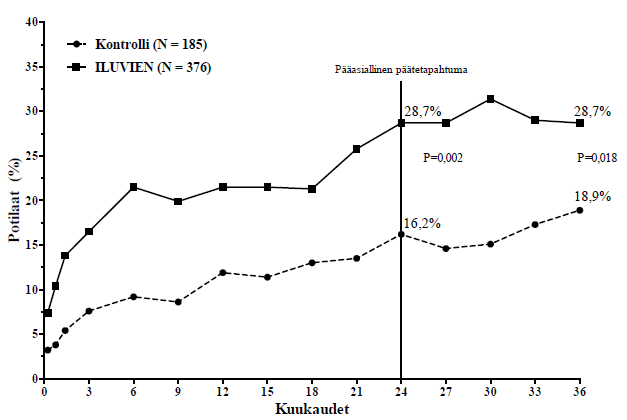
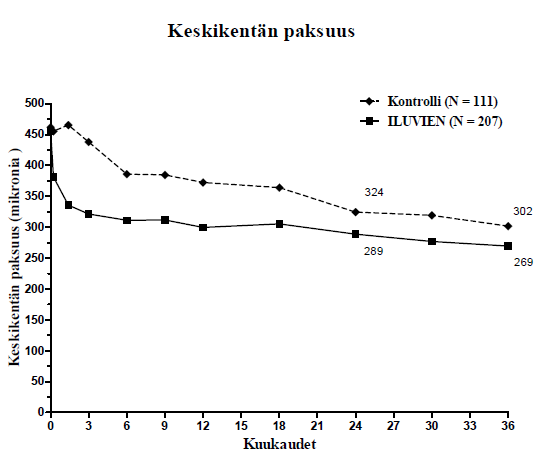
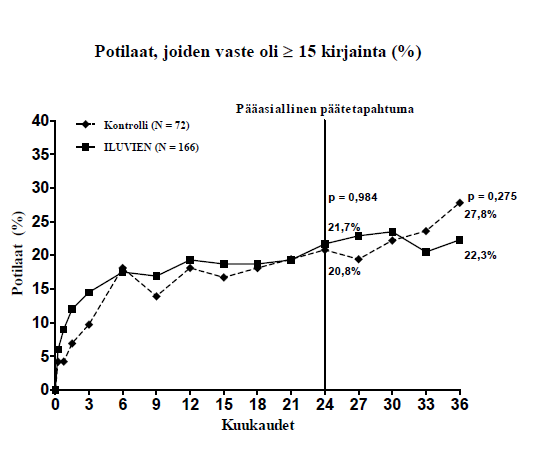
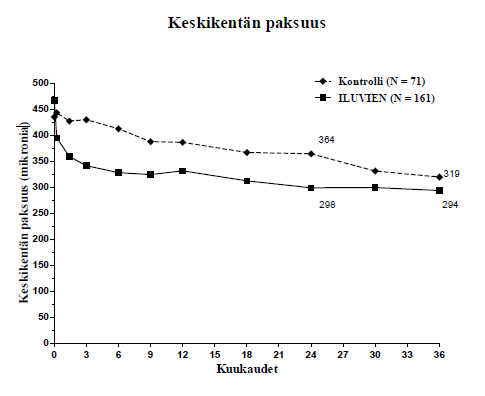
Kun tehoa arvioitiin taudin keston funktiona, potilailla, joiden diabeettisen makulaturvotuksen kesto oli yli mediaanin (≥ 3 vuotta), oli merkittävän suotuisa vaste Iluvieniin, kun taas potilailla, joiden diabeettinen makulaturvotus oli kestänyt lyhyemmän aikaa, näön paraneminen ei osoittautunut verrokkiryhmää paremmaksi (kuvat 2 ja 3). Nämä alaryhmätiedot tukevat kohdan Käyttöaiheet käyttöaihetta hoidon käytöstä kroonista diabeettista makulaturvotusta sairastavilla potilailla (kesto vähintään 3 vuotta).
Kuva 2: Vertailu niiden potilaiden prosenttiosuuksista, joiden näkökyky parani ≥ 15 kirjainta lähtötilanteen laseilla korjatusta näöntarkkuudesta (BCVA), ja keskikentän paksuuden keskimääräisestä muutoksesta lähtötilanteeseen nähden potilaiden osajoukossa, jossa diabeettisen makulaturvotuksen (DMO) kestoaika ≥ 3 vuotta
DMO ≥ 3 vuotta |
|
|
Kuva 3: Vertailu keskikentän paksuuden keskimääräisestä muutoksesta lähtötilanteeseen nähden ja niiden potilaiden prosenttiosuudesta, joiden näkökyky parani ≥ 15 kirjainta lähtötilanteen laseilla korjatusta näöntarkkuudesta (BCVA) potilaiden osajoukossa, jonka diabeettisen makulaturvotuksen (DMO) kestoaika < 3 vuotta
DMO < 3 vuotta |
|
|
6-vuotinen myyntiluvan myöntämisen jälkeen tehty turvallisuutta koskenut IRISS-rekisteritutkimus (M-01-12-001) päättyi. Tutkimuksessa oli mukana 556 potilaasta (695 silmästä) saadut tiedot, eikä siinä todettu turvallisuutta koskevia riskejä niiden lisäksi, jotka tunnistettiin jo FAME-tutkimuksissa.
Silmän takaosan ei-infektiivinen uveiitti
Silmän takaosaan vaikuttavan ei-infektiivisen uveiitin Iluvien-hoitoa koskeva kehitysohjelma koostuu kahdesta vaiheen 3 tutkimuksesta, joissa arvioidaan fluosinoloniasetonidiannosten 0,2 mikrog/vrk turvallisuutta ja tehoa lumeinjektioihin verrattuna 36 kuukauden pituisen ajanjakson aikana. Kumpikin tutkimus on prospektiivinen, satunnaistettu, kaksoissokkoutettu lumeinjektiokontrolloitu monikeskustutkimus, ja niissä oli mukana yhteensä 282 potilasta, jotka saivat kertahoitona joko fluosinoloniasetonidia (188 tutkittavaa) tai lumeinjektion (94 tutkittavaa). Soveltuvuuskriteerit oli määritelty siten, että tutkimuksiin otettiin mukaan vain tutkittavia, joilla oli uusiutunut tai pitkittynyt tauti. Tutkimuksiin mukaan otettujen potilaiden silmien ominaisuudet lähtötilanteessa esitetään taulukossa 2.
Taulukko 2. Tutkimuksessa hoidettavien silmien ominaisuudet lähtötilanteessa (hoitoaikeen mukainen potilasjoukko, ITT): PSV-FAI-001 ja PSV-FAI-005
Hoitoaikeen mukainen potilasjoukko | |||||
| PSV-FAI-001 | PSV-FAI-005 | |||
| Fluosinoloni-asetonidi-implantaatti (N = 87) | Lumeinjektio (N = 42) | Fluosinoloni-asetonidi-implantaatti (N = 101) | Lumeinjektio (N = 52) | |
Laseilla korjattu näöntarkkuus, kirjainta, keskiarvo (keskihajonta) | 66,9 (15,49) | 64.9 (15,53) | 66,4 (15,85) | 63,6 (16,82) | |
Lasiaissamentuman vaikeusaste 0/0.5+ | 48 (55,2) | 21 (50,0) | 37 (36,6) | 14 (27,0) | |
1/2+ | 39 (44,8) | 21 (50,0) | 64 (63,3) | 38 (73,1) | |
3/4+ | 0 | 0 | 0 | 0 | |
Etukammion soluja 0/0.5+ | 77 (88,5) | 33 (78,6) | 93 (92,0) | 49 (94,3) | |
1/2+ | 10 (11,5) | 9 (21,4) | 8 (7,9) | 3 (5,8) | |
3/4+ | 0 | 0 | 0 | 0 | |
Silmänpaine, keskiarvo (keskihajonta) | 13,9 (3,12) | 13,6 (3,15) | 13,3 (3,07) | 13,1 (2,60) | |
Makulaturvotuksen vaikeusaste (mikrom) CST < 300 | 37 (42,5) | 14 (33,3) | 70 (69,3) | 36 (69,2) | |
CST ≥ 300 | 48 (55,2) | 27 (64,3) | 30 (29,7) | 14 (26,9) | |
CST = verkkokalvon keskikuopan (keskikentän) paksuus
Tiedot ovat lkm (%), ellei muuta ole mainittu.
Ensisijainen tehon päätetapahtuma perustui niiden tutkittavien osuuteen, joiden uveiitti ei uusiutunut satunnaistamisen ja 6. hoitokuukauden välisenä aikana, kun uusiutumiseksi määriteltiin:
a) ≥ 2 yksikön lisäys solumäärässä per HPF-kenttä (high powered field) verrattuna lähtötilanteeseen tai mihinkään käyntiajankohtaan ennen 6. hoitokuukautta tai
b) lasiaissamentuman lisäys ≥ 2 yksikköä verrattuna lähtötilanteeseen tai mihinkään käyntiajankohtaan ennen 6. hoitokuukautta tai
c) laseilla korjatun näöntarkkuuden heikentyminen ≥ 15 kirjainta verrattuna lähtötilanteeseen tai mihinkään käyntiajankohtaan ennen 6. hoitokuukautta.
Kaikkien uusiutumisen määrittämiseen käytettyjen kriteerien piti liittyä vain ei-infektiiviseen uveiittiin. Jos tutkittavalla ei aiemmin ollut kohdissa a, b tai c määriteltyä uusiutumista, mutta tutkittava käytti tutkimuksessa hoidettavan silmän hoitoon jotakin systeemistä kortikosteroidia tai immunosuppressiivista lääkeainetta tai silmän sisään / silmää ympäröivään kudokseen annosteltavaa tai paikallisesti käytettävää kortikosteroidia milloin tahansa tutkimuksen aikana ennen 6. hoitokuukautta, taudin katsottiin uusiutuneen. Uusiutuminen voitiin hoitaa tutkimussuunnitelmassa määriteltyjen kriteerien mukaan tavanomaista hoitokäytäntöä noudattaen.
Kummassakin vaiheen 3 kliinisessä tutkimuksessa saavutettiin ensisijainen päätetapahtuma (ks. taulukot 3 ja 4) ensisijaisen tehoa koskevan päätetapahtuman tulosten osalta, kun tutkimuksessa hoidettavan silmän uveiitin uusiutumisen osuutta verrattiin lumeinjektion saaneeseen vertailuryhmään.
Taulukko 3. Niiden tutkittavien osuus, joilla uveiitti uusiutui tutkimuksessa hoidettavassa silmässä 6 kuukauden kuluessa (hoitoaikeen mukainen potilasjoukko, ITT): PSV-FAI-001 ja PSV-FAI-005
Hoitoaikeen mukainen potilasjoukko | ||||
PSV-FAI-001 | PSV-FAI-005 | |||
Fluosinoloni-asetonidi-implantaatti (N = 87) | Lumeinjektio (N = 42) | Fluosinoloni-asetonidi-implantaatti (N = 101) | Lumeinjektio (N = 52) | |
Uusiutuminen 6 kuukauden kuluessa, n (%) | 24 (27,6) | 38 (90,5) | 26 (25,7 %) | 31 (59,6 %) |
Ei uusiutumista 6 kuukauden kuluessa, n (%) | 63 (72,4) | 4 (9,5) | 75 (74,3 %) | 21 (40,4 %) |
Ero lumeinjektioon verrattuna 1 | ||||
Kerroinsuhde | 24,94 | 4,26 | ||
95 %:n luottamusväli | 8,04; 77,39 | 2,09; 8,67 | ||
p-arvo | < 0,001 | < 0,001 | ||
Ero lumeinjektioon verrattuna 2 | ||||
Prosentuaalinen ero | 62,9 % | 33,9 % | ||
95 %:n luottamusväli | (50,0 %; 75,8 %) | (18,0 %; 49,7 %) | ||
p-arvo | < 0,001 | < 0,001 | ||
1 Kerroinsuhde ja 95 %:n luottamusväli perustuvat Mantel-Haenszelin testiin. p-arvo on saatu jatkuvuuskorjatusta khiin neliö ‑testistä, jossa tutkimusryhmien välillä verrattiin niiden tutkittavien lukumäärää, joilla uveiitti oli tai ei ollut uusiutunut 6. hoitokuukauden jälkeen.
2 p-arvo perustuu yleistä yhteyttä selvittäneeseen Cochran-Mantel-Haenszelin khiin neliö ‑testiin, jossa hoitoryhmien välillä verrattiin niiden tutkittavien lukumäärää, joilla uveiitti oli tai ei ollut uusiutunut 6. hoitokuukauden jälkeen.
Taulukko 4. Niiden tutkittavien osuus, joilla uveiitti uusiutui tutkimuksessa hoidettavassa silmässä 6 kuukauden kuluessa (hoitoaikeen mukainen potilasjoukko, ITT): yhdistetyt uveiittitutkimukset
Hoitoaikeen mukainen potilasjoukko | ||
Fluosinoloniasetonidi-implantaatti (N = 188) | Lumeinjektio (N = 94) | |
Uusiutuminen 6 kuukauden kuluessa, n (%) | 50 (26,6) | 69 (73,4) |
Ei uusiutumista 6 kuukauden kuluessa, n (%) | 138 (73,4) | 25 (26,6) |
Ero lumeinjektioon verrattuna1 | ||
Kerroinsuhde | 7,62 | |
95 %:n luottamusväli | (4,35; 13,34) | |
p-arvo | < 0,001 | |
Ero lumeinjektioon verrattuna2 | ||
Prosentuaalinen ero | 46,8 % | |
95 %:n luottamusväli | (35,9 %; 57,8 %) | |
p-arvo | < 0,001 | |
1 Kerroinsuhde ja 95 %:n luottamusväli perustuvat Mantel-Haenszelin testiin. p-arvo on saatu jatkuvuuskorjatusta khiin neliö ‑testistä, jossa tutkimusryhmien välillä verrattiin niiden tutkittavien lukumäärää, joilla uveiitti oli tai ei ollut uusiutunut 6. hoitokuukauden jälkeen.
2 p-arvo perustuu yleistä yhteyttä selvittäneeseen Cochran-Mantel-Haenszelin khiin neliö ‑testiin, jossa hoitoryhmien välillä verrattiin niiden tutkittavien lukumäärää, joilla uveiitti oli tai ei ollut uusiutunut 6. hoitokuukauden jälkeen.
Kuva 4. Kaplan-Meierin kuvaaja ajasta uveiitin ensimmäiseen uusiutumiseen tutkimuksessa hoidettavassa silmässä 6. hoitokuukauden jälkeen (ITT): yhdistetyt uveiittitutkimukset
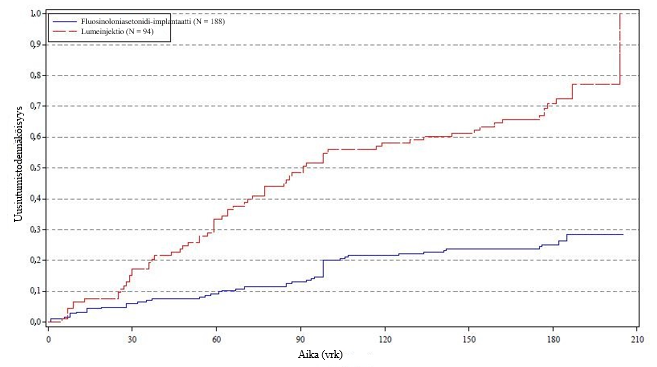
Uveiitin uusiutumiseen kuluneen ajan kahta jakaumaa vertaileva p-arvo (p < 0,001) perustuu log-rank-testiin. Tutkimuksessa hoidetun silmän uveiitin uusiutumisen 6. hoitokuukauden jälkeen raportoitiin olleen hoitoaikeen mukaisessa potilasjoukossa huomattavasti (p < 0,001) harvinaisempaa Iluvien-ryhmässä (37,9 %) verrattuna lumeinjektioita saaneeseen ryhmään (97,6 %); lumeinjektioiden suhteen todetun eron kerroinsuhde oli 67,09 (95 %:n luottamusväli: 8,81, 511,06).
Ensimmäiseksi käynnistyneen vaiheen 3 tutkimuksen (PSV-FAI-001) 36 kuukauden tulokset osoittivat tehon säilyneen (ks. taulukosta tutkimuksen PSV-FAI-001 ensisijaista tehon päätetapahtumaa koskevat tulokset, joissa niiden potilaiden osuutta, joiden tutkimuksessa hoidetussa silmässä uveiitti uusiutui, verrataan lumevalmistetta saaneeseen vertailuryhmään sekä kuva, jossa esitetään vertailu ajasta uveiitin uusiutumiseen näissä hoitoryhmissä).
Taulukko 5. Niiden tutkittavien osuus, joiden tutkimuksessa hoidettavassa silmässä uveiitti uusiutui 36 kuukauden kuluessa (hoitoaikeen mukainen potilasjoukko, ITT) PSV-FAI-001
Hoitoaikeen mukainen potilasjoukko | ||
Fluosinoloniasetonidi-implantaatti (N = 87) | Lumeinjektio (N = 42) | |
Uusiutuminen 36 kuukauden kuluessa, n (%) | 57 (65,5 %) | 41 (97,6 %) |
Ei uusiutumista 36 kuukauden kuluessa, n (%) | 30 (34,5 %) | 1 (2,4 %) |
Ero lumeinjektioon verrattuna1 | ||
Kerroinsuhde | 21,58 | |
95 %:n luottamusväli | (2,83; 164,70) | |
p-arvo | < 0,001 | |
Ero lumeinjektioon verrattuna2 | ||
Prosentuaalinen ero | 32,1 % | |
95 %:n luottamusväli | (21,1 %; 43,1 %) | |
p-arvo | < 0,001 | |
1 Kerroinsuhde ja 95 %:n luottamusväli perustuvat Mantel-Haenszelin testiin. p-arvo on saatu jatkuvuuskorjatusta khiin neliö ‑testistä, jossa tutkimusryhmien välillä verrattiin niiden tutkittavien lukumäärää, joilla uveiitti oli tai ei ollut uusiutunut 36 kuukauden jälkeen.
2 p-arvo perustuu yleistä yhteyttä selvittäneeseen Cochran-Mantel-Haenszelin khiin neliö ‑testiin, jossa hoitoryhmien välillä verrattiin niiden tutkittavien lukumäärää, joilla uveiitti oli tai ei ollut uusiutunut 36 kuukauden jälkeen.
Kuva 5. Kaplan-Meierin kuvaaja ajasta uveiitin ensimmäiseen uusiutumiseen tutkimuksessa hoidettavassa silmässä 36 kuukauden jälkeen (hoitoaikeen mukainen potilasjoukko, ITT): PSV-FAI-001
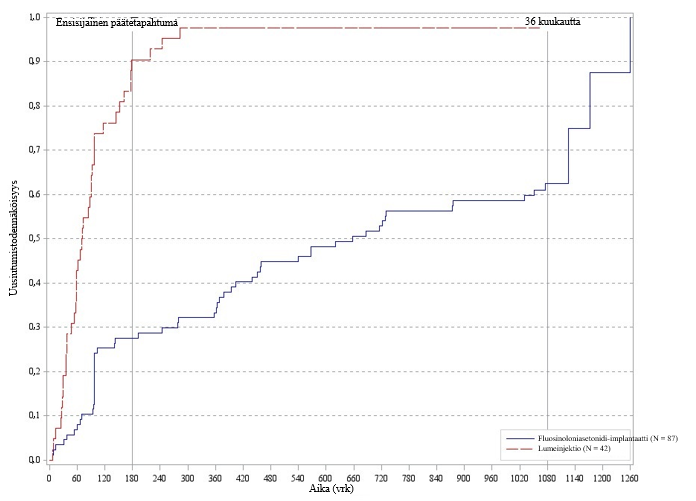
Hoitoaikeen mukaisessa (ITT) potilasjoukossa tutkimuksessa hoidetun silmän uveiitin uusiutumisen 36 kuukauden kuluessa raportoitiin olleen huomattavasti harvinaisempaa (p < 0,001) Iluvien-ryhmässä verrattuna lumeinjektioita saaneeseen ryhmään.
Taulukko 6. Tutkimuksessa hoidettavassa silmässä 6 kuukauden kuluessa tapahtuneiden uveiitin uusiutumisten lukumäärä (hoitoaikeen mukainen potilasjoukko, ITT): PSV-FAI-001 ja PSV-FAI-005
Hoitoaikeen mukainen potilasjoukko | ||||
PSV-FAI-001 | PSV-FAI-005 | |||
Fluosinoloniasetonidi-implantaatti (N = 87) | Lumeinjektio (N = 42) | Fluosinoloniasetonidi-implantaatti (N = 101) | Lumeinjektio (N = 52) | |
Uusiutumisten kokonaislukumäärä | 36 | 70 | 59 | 53 |
Niiden potilaiden lukumäärä, joilla vähintään yksi uusiutumiskerta | 24 | 38 | 26 | 31 |
Uusiutumiskertojen lukumäärä potilasta kohden | ||||
N | 87 | 42 | 101 | 52 |
Keskiarvo (keskihajonta) | 0,4 (0,76) | 1,7 (1,07) | 0,6 (1,34) | 1,0 (1,21) |
Mediaani | 0,0 | 1,0 | 0,0 | 1,0 |
Minimi, maksimi | (0; 3) | (0; 5) | (0; 9) | (0; 6) |
0 | 63 (72,4 %) | 4 (9,5 %) | 75 (74,3 %) | 21 (40,4 %) |
1 | 14 (16,1 %) | 18 (42,9 %) | 12 (11,9 %) | 18 (34,6 %) |
2 | 8 (9,2 %) | 10 (23,8 %) | 4 (4,0 %) | 8 (15,4 %) |
3 | 2 (2,3 %) | 9 (21,4 %) | 7 (6,9 %) | 3 (5,8 %) |
4 | 0 (0,0 %) | 0 (0,0 %) | 1 (1,0 %) | 1 (1,9 %) |
5 | 0 (0,0 %) | 1 (2,4 %) | 1 (1,0 %) | 0 (0,0 %) |
> 5 | 0 (0,0 %) | 0 (0,0 %) | 1 (1,0 %) | 1 (1,9 %) |
Ero lumeinjektioon verrattuna1 | ||||
Estimaatti | -1,3 | -0,4 | ||
95 %:n luottamusväli | (-1,62; -0,88) | (-0,87; 0,00) | ||
p-arvo | < 0,001 | 0,051 | ||
1 p-arvo perustuu yhden näytteen varianssianalyysiin, jossa hoitoryhmä on kiinteä vaikutus verrattaessa uveiitin uusiutumiskertojen lukumäärää 36 kuukauden aikana.
Taulukko 7. Tutkimuksessa hoidettavassa silmässä 36 kuukauden kuluessa tapahtuneiden uveiitin uusiutumisten lukumäärä (hoitoaikeen mukainen potilasjoukko, ITT): PSV-FAI-001
Hoitoaikeen mukainen potilasjoukko | |||
Fluosinoloniasetonidi-implantaatti (N = 87) | Lumeinjektio (N = 42) | ||
Uusiutumisten kokonaislukumäärä | 149 | 223 | |
Niiden potilaiden lukumäärä, joilla vähintään yksi uusiutumiskerta | 57 | 41 | |
Uusiutumiskertojen lukumäärä potilasta kohden | |||
N | 87 | 42 | |
Keskiarvo (keskihajonta) | 1,7 (2,42) | 5,3 (3,84) | |
Mediaani | 1,0 | 5,0 | |
Minimi, maksimi | (0, 15) | (0, 15) | |
0 | 30 (34,5 %) | 1 (2,4 %) | |
1 | 29 (33,3 %) | 5 (11,9 %) | |
2 | 7 (8,0 %) | 7 (16,7 %) | |
3 | 8 (9,2 %) | 4 (9,5 %) | |
4 | 4 (4,6 %) | 3 (7,1 %) | |
5 | 2 (2,3 %) | 5 (11,9 %) | |
> 5 | 7 (8,0 %) | 17 (40,5 %) | |
Ero lumeinjektioon verrattuna1 | |||
Estimaatti | -3,6 | ||
95 %:n luottamusväli | (-4,89, -2,30) | ||
p-arvo | < 0,001 | ||
1 p-arvo perustuu yhden näytteen varianssianalyysiin, jossa hoitoryhmä on kiinteä vaikutus verrattaessa uveiitin uusiutumiskertojen lukumäärää 36 kuukauden aikana.
Iluvien-hoitoa saaneilla potilailla oli merkittävästi vähemmän uusiutumiskertoja 36 kuukauden aikana verrattuna lumehoitoa saaneisiin (1,7 uusiutumiskertaa vs. 5,3 uusiutumiskertaa, p < 0,001).
Taulukko 8. Tutkimuksessa hoidettavaan silmään uveiitin vuoksi annettujen lisähoitokertojen lukumäärä 6 kuukauden kuluessa (hoitoaikeen mukainen potilasjoukko, ITT): PSV-FAI-001 ja PSV-FAI-005
Hoitoaikeen mukainen potilasjoukko | ||||
PSV-FAI-001 | PSV-FAI-005 | |||
Fluosinoloniasetonidi-implantaatti (N = 87) | Lumeinjektio (N = 42) | Fluosinoloniasetonidi-implantaatti (N = 101) | Lumeinjektio (N = 52) | |
Systeemisesti käytettävät steroidit tai immunosuppressiiviset lääkkeet | ||||
Uusiutumiskertojen kokonaislukumäärä | 21 | 24 | 25 | 14 |
Niiden tutkittavien lukumäärä, joilla vähintään yksi uusiutumiskerta | 13 (14,9 %) | 16 (38,1 %) | 14 (13,9 %) | 11 (21,2 %) |
Ero lumeinjektioon verrattuna 1 | ||||
Prosentuaalinen ero | 23,2 % | 7,3 % | ||
95 %:n luottamusväli | (6,7 %; 39,6 %) | (-5,7 %; 20,3 %) | ||
p-arvo | 0,003 | 0,249 | ||
Silmän sisään / silmää ympäröivään kudokseen annettavat steroidit | ||||
Uusiutumiskertojen kokonaislukumäärä | 5 | 35 | 2 | 19 |
Niiden tutkittavien lukumäärä, joilla vähintään yksi uusiutumiskerta | 5 (5,7 %) | 24 (57,1 %) | 2 (2 %) | 19 (36,5 %) |
Ero lumeinjektioon verrattuna1 | ||||
Prosentuaalinen ero | 51,4 % | 34,6 % | ||
95 %:n luottamusväli | (35,7 %; 67,1 %) | (21,2 %; 47,9 %) | ||
p-arvo | < 0,001 | < 0,001 | ||
Paikallisesti käytettävät steroidit | ||||
Uusiutumiskertojen kokonaislukumäärä | 17 | 22 | 11 | 17 |
Niiden tutkittavien lukumäärä, joilla vähintään yksi uusiutumiskerta | 15 (17,2 %) | 18 (42,9 %) | 10 (9,9 %) | 12 (23,1 %) |
Ero lumeinjektioon verrattuna1 | ||||
Prosentuaalinen ero | 25,6 % | 13,2 % | ||
95 %:n luottamusväli | (8,7 %; 42,6 %) | (0,3 %, 26,0 %) | ||
p-arvo | 0,002 | 0,028 | ||
1 p-arvo perustuu yleistä yhteyttä selvittäneeseen Cochran-Mantel-Haenszelin khiin neliö ‑testiin, jossa hoitoryhmien välillä verrattiin niiden tutkittavien lukumäärää, jotka olivat tai eivät olleet saaneet lisähoitoa.
Taulukko 9. Tutkimuksessa hoidettavaan silmään uveiitin vuoksi annettujen lisähoitokertojen lukumäärä 36 kuukauden kuluessa (hoitoaikeen mukainen potilasjoukko, ITT): PSV-FAI-001
Hoitoaikeen mukainen potilasjoukko | |||
Fluosinoloniasetonidi-implantaatti (N = 87) | Lumeinjektio (N = 42) | ||
Systeemisesti käytettävät steroidit tai immunosuppressiiviset lääkkeet | |||
Uusiutumiskertojen kokonaislukumäärä | 61 | 45 | |
Niiden tutkittavien lukumäärä, joilla vähintään yksi uusiutumiskerta | 30 (34,5 %) | 21 (50,0 %) | |
Ero lumeinjektioon verrattuna1 | |||
Prosentuaalinen ero | 15,5 % | ||
95 %:n luottamusväli | (-2,6 %, 33,6 %) | ||
p-arvo | 0,092 | ||
silmän sisään / silmää ympäröivään kudokseen annettavat steroidit | |||
Uusiutumiskertojen kokonaislukumäärä | 23 | 99 | |
Niiden tutkittavien lukumäärä, joilla vähintään yksi uusiutumiskerta | 17 (19,5 %) | 29 (69,0 %) | |
Ero lumeinjektioon verrattuna1 | |||
Prosentuaalinen ero | 49,5 % | ||
95 %:n luottamusväli | (33,2 %, 65,8 %) | ||
p-arvo | < 0,001 | ||
Paikallisesti käytettävät steroidit | |||
Uusiutumiskertojen kokonaislukumäärä | 40 | 47 | |
Niiden tutkittavien lukumäärä, joilla vähintään yksi uusiutumiskerta | 24 (27,6 %) | 24 (57,1 %) | |
Ero lumeinjektioon verrattuna1 | |||
Prosentuaalinen ero | 29,6 % | ||
95 %:n luottamusväli | (11,9 %, 47,2 %) | ||
p-arvo | 0,001 | ||
1 p-arvo perustuu yleistä yhteyttä selvittäneeseen Cochran-Mantel-Haenszelin khiin neliö ‑testiin, jossa hoitoryhmien välillä verrattiin niiden tutkittavien lukumäärää, jotka olivat tai eivät olleet saaneet lisähoitoa.
Merkittävästi harvemmat Iluvien-hoitoa saaneet potilaat verrattuna lumeinjektion saaneisiin potilaisiin tarvitsivat lisähoitoa silmän sisään / silmää ympäröivään kudokseen annettavilla steroideilla (19,5 % vs 69,0 %, < 0,001) tai paikallisesti käytettävillä steroideilla (27,6 % vs 57,1 %, p = 0,001). Harvemmat potilaat tarvitsivat lisähoitoa systeemisillä steroideilla tai immunosuppressiivista hoitoa (34,5 % vs 50,0 %, p = 0,092),
Euroopan lääkevirasto on myöntänyt vapautuksen velvoitteesta toimittaa tutkimustulokset lasiaiseen annettavan fluosinoloniasetonidin käytöstä kaikkien pediatristen potilasryhmien diabeettisen makulaturvotuksen hoidossa (ks. kohta Annostus ja antotapa ohjeet käytöstä pediatristen potilaiden hoidossa).
Farmakokinetiikka
Ihmisellä tehdyssä farmakokineettisessä tutkimuksessa (C-01-06-002, FAMOUS-tutkimus) plasman fluosinoloniasetonidipitoisuudet olivat kaikkina ajankohtina päivästä 1 kuukauteen 36 kvantitatiivisen määrityksen alarajan (100 pg/ml) alapuolella. Kammiovedessä maksimaaliset fluosinoloniasetonidipitoisuudet havaittiin useimmilla tutkittavilla päivänä 7. Kammioveden fluosinoloniasetonidipitoisuudet laskivat ensimmäisten 3−6 kuukauden aikana ja pysyivät oleellisesti samoina kuukauden 36 loppuun asti, jos tutkittavan hoitoa ei uusittu. Jos tutkittavan hoito uusittiin, esiintyi toinen fluosinoloniasetonidin pitoisuushuippu, joka oli samankaltainen kuin ensimmäisen annoksen jälkeen. Kammioveden fluosinoloniasetonidipitoisuudet palasivat uuden hoidon jälkeen suunnilleen samankaltaiselle tasolle kuin ensimmäisen hoidon aikana havaittiin.
Kuva 6. Kammioveden fluosinoloniasetonidipitoisuudet tutkittavilla, jotka saivat yhden Iluvien-implantaatin (FAMOUS-tutkimus)
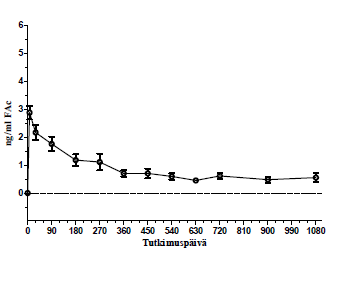
Prekliiniset tiedot turvallisuudesta
Systeemisesti annetun fluosinoloniasetonidin on osoitettu olevan teratogeeninen hiirille ja kaniineille. Silmän lasiaiseen annettavaa fluosinoloniasetonidia koskevia mutageenisuus-, karsinogeenisuus-, lisääntymis- tai kehitystoksisuustietoja ei ole saatavilla. Silmän lasiaiseen annettava fluosinoloniasetonidi ei ollut kuitenkaan systeemisesti mitattavissa, joten systeemisiä vaikutuksia ei odoteta ilmenevän.
Kun kaniinien silmän lasiaiseen annettiin suurempi fluosinoloniasetonidiannos kuin käytännön hoitotyössä, havaittiin, paikallisia vaikutuksia (fokaalisia rappeumavaurioita mykiön takaosan polaaristen ja kortikaalisten osien säikeissä). Paikallisia vaikutuksia (fokaalista arpimuodostusta verkkokalvossa) todettiin myös kaniineilla, joita hoidettiin sekä lumelääkettä että fluosinoloniasetonidia sisältävällä laitteella. Tämäntyyppistä arpimuodostusta ei todettu kliinisesti ihmisellä, ja sen oletetaan johtuvan kaniinin ja ihmisen silmien anatomisista eroista.
Farmaseuttiset tiedot
Apuaineet
Polyvinyylialkoholi
Polyimidiputki
Silikoniliima
Yhteensopimattomuudet
Ei oleellinen.
Kestoaika
2 vuotta.
Käytä välittömästi sen jälkeen, kun kansi on avattu.
Säilytys
Säilytä alle 30 °C. Älä säilytä kylmässä. Ei saa jäätyä.
Avaa sinetöity pakkausalusta vasta juuri ennen käyttöä.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
ILUVIEN implantaatti silmän lasiaiseen, asetin
190 mikrog (L:ei) 1 kpl (11330,84 €)
PF-selosteen tieto
Implantaatti toimitetaan kertakäyttöisessä 25 gaugen neulalla varustetussa asettimessa. Yksi steriili asetin sisältää vaaleanruskean 3,5 mm pituisen lieriön muotoisen implantaatin. Asetin on pakattu muoviseen pakkausalustaan, joka on suljettu kannella.
Valmisteen kuvaus:
Vaaleanruskea lieriö, kooltaan noin 3,5 mm x 0,37 mm.
Implantaattiasetin, jossa 25 gaugen neula.
Käyttö- ja käsittelyohjeet
Hävitä asetin turvallisesti viiltävälle ja pistävälle tartuntavaaralliselle jätteelle tarkoitetussa säiliössä.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
ILUVIEN implantaatti silmän lasiaiseen, asetin
190 mikrog 1 kpl
- Ei korvausta.
ATC-koodi
S01BA15
Valmisteyhteenvedon muuttamispäivämäärä
25.08.2023
Yhteystiedot
c/o Franska Handelskammaren, Waterfront Building, Box 190
10123 Stockholm
Sweden
www.horus-pharma.fi
contact-nordics@horus-pharma.com