INSULIN ASPART SANOFI injektioneste, liuos, esitäytetty kynä 100 U/ml
Vaikuttavat aineet ja niiden määrät
1 ml liuosta sisältää 100 yksikköä aspartinsuliinia* (vastaa 3,5 mg:aa).
Insulin aspart Sanofi 100 yksikköä/ml injektioneste, liuos, esitäytetty kynä
Yksi esitäytetty kynä sisältää 3 ml liuosta, mikä vastaa 300:aa yksikköä aspartinsuliinia.
Yhdestä esitäytetystä kynästä saa 1–80 yksikköä yhden yksikön tarkkuudella.
* tuotettu Escherichia coli -bakteerissa yhdistelmä-DNA-tekniikalla.
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Injektioneste, liuos (injektioneste).
Kliiniset tiedot
Käyttöaiheet
Insulin aspart Sanofi on tarkoitettu aikuisten, nuorten ja vähintään 1-vuotiaiden lasten diabetes mellituksen hoitoon.
Annostus ja antotapa
Annostus
Insuliinianalogien, kuten aspartinsuliinin, vahvuus ilmoitetaan yksikköinä, kun taas ihmisinsuliinin vahvuus ilmaistaan kansainvälisinä yksikköinä.
Insulin aspart Sanofi -insuliinin annostus on yksilöllinen ja se määritetään potilaan tarpeiden mukaisesti. Insulin aspart Sanofi -insuliinia käytetään yleensä yhdessä keskipitkä- tai pitkävaikutteisen insuliinin kanssa.
Verenglukoosin seurantaa ja insuliinin annoksen säätämistä suositellaan optimaalisen glukoositasapainon saavuttamiseksi.
Yksilöllinen insuliinin tarve aikuisilla ja lapsilla on yleensä 0,5–1,0 yksikköä/kg/vrk. Perusinsuliini-ateriainsuliinihoitomallissa 50–70 % insuliinin kokonaistarpeesta voidaan kattaa Insulin aspart Sanofi -insuliinilla. Loput insuliinin tarpeesta katetaan keskipitkä- tai pitkävaikutteisella insuliinilla.
Annoksen säätäminen voi olla tarpeen, jos potilaan fyysinen rasitus lisääntyy, tavanomainen ruokavalio muuttuu tai hänellä on muu samanaikainen sairaus.
Siirtyminen muista insuliinivalmisteista
Toisista insuliinivalmisteista siirryttäessä Insulin aspart Sanofi -insuliinin ja perusinsuliinin annoksia voidaan joutua säätämään. Insulin aspart Sanofi -insuliinin vaikutus alkaa nopeammin ja sen vaikutusaika on lyhyempi kuin lyhytvaikutteisen (liukenevan) ihmisinsuliinin. Vatsan alueelle ihonalaisesti annetun injektion vaikutus alkaa 10–20 minuutin kuluessa pistämisestä. Vaikutus on voimakkaimmillaan 1–3 tunnin välillä injektion antamisesta. Vaikutus kestää 3–5 tuntia.
Verenglukoosin tarkka seuranta on suositeltavaa siirtymisvaiheen aikana ja sitä seuraavina ensimmäisinä viikkoina (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Erityisryhmät
Iäkkäät (≥ 65-vuotiaat)
Insulin aspart Sanofi -insuliinia voidaan käyttää iäkkäiden potilaiden hoitoon.
Verenglukoosin seurantaa on tehostettava ja aspartinsuliinin annos on säädettävä yksilöllisesti, jos potilas on iäkäs.
Munuaisten vajaatoiminta
Munuaisten vajaatoiminta saattaa vähentää potilaan insuliinin tarvetta.
Verenglukoosin seurantaa on tehostettava ja aspartinsuliinin annos on säädettävä yksilöllisesti, jos potilaalla on munuaisten vajaatoiminta.
Maksan vajaatoiminta
Maksan vajaatoiminta saattaa vähentää potilaan insuliinin tarvetta.
Verenglukoosin seurantaa on tehostettava ja aspartinsuliinin annos on säädettävä yksilöllisesti, jos potilaalla on maksan vajaatoiminta.
Pediatriset potilaat
Insulin aspart Sanofi -insuliinia voidaan antaa nuorille sekä vähintään 1-vuotiaille lapsille lyhytvaikutteisen (liukenevan) ihmisinsuliinin sijaan, kun vaikutuksen nopeasta alkamisesta saattaa olla hyötyä, esimerkiksi kun pistos halutaan ajoittaa oikein aterioihin nähden (ks. kohdat Farmakodynamiikka ja Farmakokinetiikka).
Insulin aspart Sanofi -valmisteen turvallisuutta ja tehoa alle 1-vuotiaiden lasten hoidossa ei ole varmistettu. Tietoja ei ole saatavilla.
Antotapa
Aspartinsuliini on pikavaikutteinen insuliinianalogi.
Insulin aspart Sanofi annetaan ihonalaisena pistoksena olkavarteen, reiteen, pakaraan tai vatsaan. Pistoskohtia on vaihdeltava saman alueen sisällä lipodystrofian ja ihoamyloidoosin vaaran pienentämiseksi (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet ja Haittavaikutukset). Ihonalainen pistos vatsan alueelle varmistaa nopeamman imeytymisen verrattuna pistoksiin muille pistosalueille. Pistoskohdasta riippumatta aspartinsuliini alkaa vaikuttaa lyhytvaikutteista ihmisinsuliinia nopeammin. Vaikutusaika vaihtelee annoksen, pistoskohdan, verenkierron, lämpötilan ja fyysisen rasituksen mukaan.
Vaikutuksen nopeammasta alkamisesta johtuen aspartinsuliini annetaan yleensä välittömästi ennen ateriaa. Tarpeen vaatiessa aspartinsuliinin voi pistää heti aterian jälkeen.
Insulin aspart Sanofi 100 yksikköä/ml injektioneste, liuos, esitäytetty kynä
Insulin aspart Sanofi 100 yksikköä/ml esitäytetty kynä sopii vain ihon alle annettaviin pistoksiin. Jos antaminen ruiskulla, pistoksena laskimoon tai infuusiopumpulla on tarpeen, on käytettävä injektiopulloa, jolloin käytetään muita tällaisen vaihtoehdon tarjoavia aspartinsuliinivalmisteita. Insulin aspart Sanofi esitäytetystä kynästä saa 1–80 yksikköä yhden yksikön tarkkuudella.
Potilaan on varmistettava valittujen yksiköiden määrä kynän annosikkunasta. Siksi edellytyksenä sille, että potilas voi itse antaa pistoksen, on, että hän pystyy näkemään kynän annosikkunan lukeman. Sokeita tai heikkonäköisiä potilaita on neuvottava käyttämään aina apuna toista henkilöä, jolla on hyvä näkö ja joka on koulutettu käyttämään kyseistä insuliinilaitetta.
Katso yksityiskohtaiset käyttöohjeet pakkausselosteesta.
Vasta-aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille.
Varoitukset ja käyttöön liittyvät varotoimet
Jäljitettävyys
Biologisten lääkevalmisteiden jäljitettävyyden parantamiseksi on annetun valmisteen nimi ja eränumero dokumentoitava selkeästi.
Potilaita on ohjeistettava vuorottelemaan pistoskohtaa jatkuvasti lipodystrofian ja ihoamyloidoosin kehittymisen vaaran vähentämiseksi. Jos insuliinin pistämistä jatketaan niihin kohtiin, joilla esiintyy näitä muutoksia, on olemassa mahdollinen vaara, että insuliinin imeytyminen hidastuu ja verensokerin hallinta heikentyy. Injektiokohdan äkillisestä vaihtamisesta terveelle alueelle on ilmoitettu aiheutuvan hypoglykemiaa. Verensokerin seurantaa suositellaan pistoskohdan vaihtamisen jälkeen, ja diabeteslääkevalmisteiden annoksen muuttamista voidaan harkita.
Hyperglykemia
Riittämätön annostus tai hoidon keskeytyminen saattavat johtaa hyperglykemiaan ja diabeettiseen ketoasidoosiin erityisesti tyypin 1 diabeteksessa. Hyperglykemian ensimmäiset oireet ilmaantuvat yleensä vähitellen tuntien tai päivien kuluessa. Oireita ovat jano, tihentynyt virtsaaminen, pahoinvointi, oksentelu, uneliaisuus, ihon punoitus ja kuivuminen, suun kuivuminen, ruokahaluttomuus sekä asetonin haju hengityksessä. Tyypin 1 diabeteksessa hoitamaton hyperglykemia johtaa lopulta diabeettiseen ketoasidoosiin, joka saattaa johtaa kuolemaan.
Hypoglykemia
Aterian laiminlyöminen tai suunnittelematon, voimakas fyysinen rasitus voi johtaa hypoglykemiaan.
Erityisesti lapsilla on hypoglykemiariskin minimoimiseksi noudatettava huolellisuutta insuliiniannosten (etenkin käytettäessä perus- ja ateriainsuliinin yhdistelmiä) sovittamisessa ruokailuun, fyysiseen aktiivisuuteen ja sen hetkiseen verenglukoosipitoisuuteen.
Hypoglykemiaa saattaa ilmetä, jos insuliiniannos on liian suuri suhteessa insuliinin tarpeeseen. Hypoglykemian yhteydessä tai hypoglykemiaa epäiltäessä aspartinsuliinia ei saa pistää. Kun potilaan verenglukoosi on saatu tasapainoon, annoksen säätämistä on harkittava (ks. kohdat Haittavaikutukset ja Yliannostus).
Potilailla, joiden verenglukoositasapaino paranee huomattavasti, esim. tehostetun insuliinihoidon ansiosta, tavanomaiset hypoglykemiasta varoittavat oireet saattavat muuttua. Potilaille on kerrottava asiasta ja annettava asianmukaista ohjausta. Tavanomaiset varoittavat oireet saattavat hävitä diabetesta pitkään sairastaneilta potilailta.
Pikavaikutteisten insuliinianalogien farmakodynamiikasta johtuen mahdollinen hypoglykemia saattaa niitä käytettäessä ilmetä pistämisen jälkeen nopeammin kuin lyhytvaikutteista (liukenevaa) ihmisinsuliinia käytettäessä.
Koska aspartinsuliini annostellaan aterian välittömässä yhteydessä, sen vaikutuksen nopea alkaminen on otettava huomioon potilailla, joilla on muita sairauksia tai jotka saavat muita hoitoja, joiden odotetaan hidastavan ruuan imeytymistä.
Muut sairaudet, varsinkin tulehdukset ja kuumetilat, yleensä lisäävät potilaan insuliinin tarvetta. Munuais- tai maksasairaus tai lisämunuaisen, aivolisäkkeen tai kilpirauhasen toimintaan vaikuttavat sairaudet voivat edellyttää insuliiniannoksen muuttamista.
Kun potilaat siirtyvät käyttämään erityyppistä insuliinivalmistetta, hypoglykemiasta varoittavat oireet voivat muuttua tai tulla vaikeammin havaittaviksi kuin aikaisempaa insuliinia käytettäessä.
Siirtyminen muista insuliinivalmisteista
Kun potilas siirtyy käyttämään toisentyyppistä tai toisen valmistajan insuliinia, on siirtyminen toteutettava lääkärin tarkassa valvonnassa. Kun muutetaan insuliinin vahvuutta, tavaramerkkiä (valmistajaa), tyyppiä, alkuperää (eläininsuliini, ihmisinsuliini tai ihmisinsuliinianalogi) ja/tai valmistusmenetelmää (yhdistelmä-DNA-tekniikalla valmistettu insuliini vs. eläinperäinen insuliini), annoksen muuttaminen saattaa olla tarpeen. Toisentyyppisestä insuliinista Insulin aspart Sanofi -insuliiniin siirtyvien potilaiden päivittäisiä pistoskertoja saatetaan joutua lisäämään tai annosta saatetaan joutua muuttamaan verrattuna potilaan tavallisesti käyttämän insuliinivalmisteen annokseen. Jos annoksen säätäminen on tarpeen, tarkistuksen tarve voi ilmaantua ensimmäisen annoksen antamisen yhteydessä tai muutamien ensimmäisten viikkojen tai kuukausien aikana.
Pistoskohdan reaktiot
Kuten mitä tahansa insuliinihoitoa käytettäessä, pistoskohdan reaktioita (kipu, punoitus, nokkosihottuma, tulehdus, mustelmat, turvotus ja kutina) saattaa ilmetä. Pistoskohdan jatkuva vaihtaminen pistosalueella vähentää tällaisten reaktioiden riskiä. Reaktiot yleensä häviävät muutaman päivän tai muutaman viikon aikana. Harvoissa tapauksissa aspartinsuliinihoito saattaa olla tarpeen lopettaa pistoskohdan reaktioiden vuoksi.
Aspartinsuliinin yhdistelmähoito pioglitatsonin kanssa
Sydämen vajaatoimintatapauksia on raportoitu esiintyneen, kun pioglitatsonia oli käytetty yhdistelmänä insuliinin kanssa, erityisesti potilailla, joilla oli riskitekijöitä sydämen vajaatoiminnan kehittymiselle. Tämä on pidettävä mielessä, jos harkitaan yhdistelmähoitoa pioglitatsonilla ja aspartinsuliinilla. Jos valmisteita käytetään yhdessä, potilaita on seurattava sydämen vajaatoiminnan, painonnousun ja turvotuksen merkkien ja oireiden varalta. Pioglitatsonihoito on lopetettava, jos sydänoireet pahenevat.
Vahingossa tapahtuvien sekaannusten/lääkitysvirheiden välttäminen
Potilaat täytyy ohjeistaa aina tarkistamaan insuliinin etiketti ennen jokaista pistosta, jotta vältetään vahingossa tapahtuvat sekaannukset Insulin aspart Sanofi -insuliinin ja muiden insuliinilääkevalmisteiden välillä.
Insuliinin vasta-aineet
Insuliinin antaminen saattaa aiheuttaa vasta-aineiden muodostumista. Tällaisten insuliinin vasta-aineiden kehittyminen saattaa harvinaisissa tapauksissa edellyttää insuliiniannoksen säätämistä hyper- tai hypoglykemiataipumuksen korjaamiseksi.
Matkustaminen
Potilaan on kysyttävä neuvoa lääkäriltä ennen matkustamista aikavyöhykkeeltä toiselle, sillä insuliinin ottamisen ja aterioiden ajankohtia voidaan joutua muuttamaan.
Natrium
Tämä lääkevalmiste sisältää alle 1 mmol (23 mg) natriumia per annos eli sen voidaan sanoa olevan ”natriumiton”.
Yhteisvaikutukset
Useiden lääkkeiden tiedetään vaikuttavan glukoosiaineenvaihduntaan.
Seuraavat lääkeaineet saattavat vähentää potilaan insuliinin tarvetta:
Suun kautta otettavat diabeteslääkkeet, monoamiinioksidaasin (MAO:n) estäjät, beetasalpaajat, angiotensiinikonvertaasin (ACE:n) estäjät, salisylaatit, anaboliset steroidit ja sulfonamidit.
Seuraavat lääkeaineet saattavat lisätä potilaan insuliinin tarvetta:
Suun kautta otettavat ehkäisyvalmisteet, tiatsidit, glukokortikoidit, kilpirauhashormonit, sympatomimeetit, kasvuhormoni ja danatsoli.
Beetasalpaajat saattavat peittää hypoglykemian oireet.
Oktreotidi ja lanreotidi voivat joko lisätä tai vähentää insuliinin tarvetta.
Alkoholi saattaa tehostaa tai heikentää insuliinin verenglukoosia alentavaa vaikutusta.
Raskaus ja imetys
Raskaus
Insulin aspart Sanofi -insuliinia (aspartinsuliinia) voidaan käyttää raskauden aikana. Tiedot kahdesta satunnaistetusta, kontrolloidusta kliinisestä tutkimuksesta (toisessa 322 ja toisessa 27 raskautta) eivät viittaa siihen, että aspartinsuliinilla olisi raskauteen tai sikiön/vastasyntyneen terveyteen kohdistuvia haittavaikutuksia verrattuna ihmisinsuliiniin (ks. kohta Farmakodynamiikka).
Raskaana olevien diabetesta (tyypin 1 diabetesta, tyypin 2 diabetesta tai raskausajan diabetesta) sairastavien naisten tehostettua verenglukoositasapainon hallintaa ja hoidon seurantaa suositellaan raskautta suunniteltaessa ja koko raskauden ajan. Insuliinin tarve yleensä vähenee raskauden ensimmäisen raskauskolmanneksen aikana ja lisääntyy tämän jälkeen toisen ja kolmannen raskauskolmanneksen aikana. Synnytyksen jälkeen insuliinin tarve tavallisesti palautuu nopeasti raskautta edeltäneisiin arvoihin.
Imetys
Insulin aspart Sanofi -insuliinin käyttöön ei liity rajoituksia rintaruokinnan aikana. Imettävän äidin insuliinihoito ei aiheuta vaaraa lapselle. Insulin aspart Sanofi -insuliinin annosta saatetaan kuitenkin joutua tarkistamaan.
Hedelmällisyys
Eläimillä tehdyissä hedelmällisyyttä koskevissa lisääntymistutkimuksissa ei ole havaittu hedelmällisyyteen liittyviä eroja aspartinsuliinin ja ihmisinsuliinin välillä (ks. kohta Prekliiniset tiedot turvallisuudesta).
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Potilaan keskittymis- ja reaktiokyky saattavat heikentyä hypoglykemian seurauksena. Tämä voi aiheuttaa vaaraa tilanteissa, joissa näillä taidoilla on suuri merkitys (esim. autolla ajo tai koneiden käyttö).
Potilaita on neuvottava ryhtymään varotoimiin hypoglykemian välttämiseksi ajon aikana. Tämä on erityisen tärkeää niille potilaille, joiden kyky tunnistaa hypoglykemiasta varoittavia oireita on huonontunut tai puuttuu tai joilla on toistuvia hypoglykemioita. Tällaisissa tapauksissa on harkittava, onko ajaminen suositeltavaa.
Haittavaikutukset
Turvallisuusprofiilin yhteenveto
Aspartinsuliinia käyttävillä potilailla havaitut haittavaikutukset johtuvat pääasiassa insuliinin farmakologisesta vaikutuksesta.
Hoidon aikana yleisimmin raportoitu haittavaikutus on hypoglykemia. Hypoglykemian esiintymistiheys vaihtelee potilasryhmän, annoksen ja glukoositasapainon mukaan (ks. kohta Haittavaikutukset, valikoitujen haittavaikutusten kuvaus).
Insuliinihoidon alkuvaiheessa saattaa ilmetä poikkeavuuksia silmien taittokyvyssä, turvotusta ja pistoskohdan reaktioita (kipu, punoitus, nokkosihottuma, tulehdus, mustelmat, turvotus ja kutina pistoskohdassa). Nämä oireet ovat yleensä ohimeneviä. Verenglukoositasapainon nopeaan paranemiseen saattaa liittyä akuutti kivulias neuropatia, joka on yleensä korjautuva. Insuliinihoidon tehostamisella aikaansaatuun äkilliseen glukoositasapainon paranemiseen saattaa liittyä diabeettisen retinopatian tilapäinen vaikeutuminen, kun taas pitkäaikainen glukoositasapainon paraneminen pienentää diabeettisen retinopatian etenemisriskiä.
Haittavaikutustaulukko
Alla olevassa luettelossa esitetyt haittavaikutukset perustuvat kliinisistä tutkimuksista saatuihin tietoihin, ja ne on luokiteltu elinjärjestelmän mukaan. Esiintymistiheydet on määritelty seuraavasti: Hyvin yleinen (≥ 1/10); yleinen (≥ 1/100, < 1/10); melko harvinainen (≥ 1/1 000, < 1/100); harvinainen (≥ 1/10 000, < 1/1 000); hyvin harvinainen (< 1/10 000), tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin).
MedDRA-elinjärjestelmä | Hyvin yleinen | Melko harvinainen | Harvinainen | Hyvin harvinainen | Tuntematon |
Immuunijärjestelmä | Nokkosihottuma, ihottuma, iho-oireiden puhkeaminen | Anafylaktiset reaktiot* | |||
Aineenvaihdunta ja ravitsemus | Hypoglykemia* | ||||
Hermosto | Perifeerinen neuropatia (kivulias neuropatia) | ||||
Silmät | Taittovirheet, diabeettinen retinopatia | ||||
Iho ja ihonalainen kudos | Lipodystrofia* | Ihoamyloidoosi* | |||
Yleisoireet ja antopaikassa todettavat haitat | Pistoskohdan reaktiot, turvotus |
*Ks. kohta Haittavaikutukset, Valikoitujen haittavaikutusten kuvaus
Valikoitujen haittavaikutusten kuvaus
Anafylaktiset reaktiot
Yleistyneet yliherkkyysreaktiot (joiden oireita ovat yleistynyt ihottuma, kutina, hikoilu, ruuansulatusvaivat, angioedeema, hengitysvaikeudet, sydämentykytys ja verenpaineen lasku) ovat hyvin harvinaisia, mutta ne saattavat olla hengenvaarallisia.
Hypoglykemia
Yleisimmin raportoitu haittavaikutus on hypoglykemia. Sitä saattaa ilmetä, jos insuliiniannos on liian suuri suhteessa insuliinin tarpeeseen. Vaikea hypoglykemia saattaa johtaa tajuttomuuteen ja/tai aiheuttaa kouristuksia, tilapäisen tai pysyvän aivojen toimintahäiriön tai jopa kuoleman. Hypoglykemian oireet ilmaantuvat yleensä yllättäen. Oireita voivat olla kylmänhikisyys, kalpea ja viileä iho, uupumus, hermostuneisuus tai vapina, ahdistus, epätavallinen väsymys tai heikkous, sekavuus, keskittymisvaikeudet, uneliaisuus, voimakas näläntunne, näköhäiriöt, päänsärky, pahoinvointi ja sydämentykytys.
Kliinisissä tutkimuksissa hypoglykemian esiintymistiheys on vaihdellut potilasryhmän, annoksen ja glukoositasapainon mukaan. Kliinisten tutkimusten aikana hypoglykemioiden kokonaismäärässä ei ollut eroa aspartinsuliinia tai ihmisinsuliinia saaneiden potilaiden välillä.
Iho ja ihonalainen kudos
Pistoskohdassa saattaa ilmetä lipodystrofiaa (mukaan lukien lipohypertrofiaa ja lipoatrofiaa) ja ihoamyloidoosia. Ne viivästyttävät insuliinin paikallista imeytymistä. Pistoskohdan jatkuva vuorottelu sovitulla pistosalueella saattaa vähentää tai ehkäistä näitä muutoksia (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Pediatriset potilaat
Myyntiintulon jälkeen julkaistujen tietojen ja aspartinsuliinilla tehtyjen kliinisten tutkimusten perusteella lapsilla havaittujen haittavaikutusten esiintymistiheys, tyyppi ja vaikeusaste eivät viittaa eroihin verrattuna koko väestöstä saatuun laajempaan kokemukseen.
Muut erityiset potilasryhmät
Myyntiintulon jälkeen julkaistujen tietojen ja aspartinsuliinilla tehtyjen kliinisten tutkimusten perusteella iäkkäillä potilailla ja munuaisten tai maksan vajaatoimintaa sairastavilla potilailla havaittujen haittavaikutusten esiintymistiheys, tyyppi ja vaikeusaste eivät viittaa eroihin verrattuna koko väestöstä saatuun laajempaan kokemukseen.
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Insuliinin yliannostukselle ei ole olemassa erityistä määritelmää. Hypoglykemia saattaa kuitenkin kehittyä vaiheittain, jos potilaan saamat insuliiniannokset ovat liian suuria insuliinin tarpeeseen nähden:
- Lievät hypoglykemiakohtaukset voidaan hoitaa antamalla suun kautta glukoosia tai sokeria sisältäviä tuotteita. Siksi on suositeltavaa, että diabeetikko pitää aina mukanaan sokeripitoisia tuotteita.
- Vaikeat hypoglykemiakohtaukset, jolloin potilas menettää tajuntansa, voidaan hoitaa antamalla glukagonia (0,5–1 mg) lihakseen tai ihon alle tai antamalla glukoosia laskimoon. Lihaksensisäisen tai ihonalaisen glukagoni-injektion voi antaa riittävän koulutuksen saanut henkilö. Laskimonsisäisen glukoosin antaa lääkäri tai muu terveydenhuollon ammattilainen. Jos glukagoniin ei saada vastetta 10–15 minuutin kuluessa, potilaalle täytyy antaa glukoosia laskimoon. Kun potilas palaa tajuihinsa, hänelle kannattaa antaa hiilihydraatteja suun kautta hypoglykemian uusiutumisen estämiseksi.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Diabeteslääkkeet. Insuliinit ja insuliinijohdokset, lyhytvaikutteiset.
ATC-koodi: A10AB05
Insulin aspart Sanofi on biosimilaari lääkevalmiste. Yksityiskohtaisempaa tietoa on saatavilla Euroopan lääkeviraston verkkosivulta http://www.ema.europa.eu.
Vaikutusmekanismi ja farmakodynaamiset vaikutukset
Aspartinsuliinin verenglukoosipitoisuutta alentava vaikutus perustuu glukoosin soluunoton helpottumiseen, kun insuliini sitoutuu lihas- ja rasvasolujen insuliinireseptoreihin, ja samanaikaiseen maksan glukoosin tuotannon estymiseen.
Aterianjälkeisten neljän ensimmäisen tunnin kuluessa on voitu määrittää, että aspartinsuliinin vaikutus alkaa nopeammin kuin lyhytvaikutteisen (liukenevan) ihmisinsuliinin ja lisäksi se laskee veren glukoosipitoisuutta enemmän. Ihon alle annetun aspartinsuliinin vaikutusaika on lyhyempi kuin lyhytvaikutteisen ihmisinsuliinin.
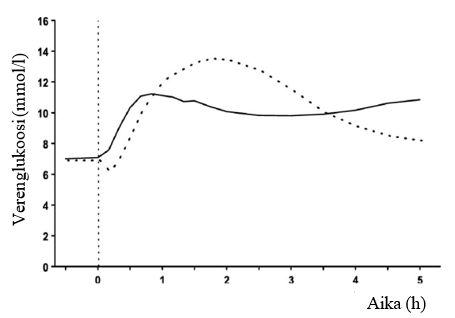
Kuva I. Yhden, ateriaa edeltävän insuliiniannoksen vaikutus veren glukoosipitoisuuteen välittömästi ennen ateriaa pistetyn aspartinsuliiniannoksen (yhtenäinen viiva) tai 30 minuuttia ennen ateriaa annetun lyhytvaikutteisen ihmisinsuliiniannoksen (katkoviiva) jälkeen potilailla, joilla on tyypin 1 diabetes.
Ihon alle annetun aspartinsuliini-injektion vaikutus alkaa 10–20 minuutin kuluttua pistämisestä. Vaikutus on voimakkaimmillaan 1–3 tunnin välillä injektion antamisesta. Vaikutus kestää 3–5 tuntia.
Kliininen teho
Tyypin 1 diabetesta sairastavilla potilailla tehdyt kliiniset tutkimukset ovat osoittaneet, että aterianjälkeiset verenglukoosiarvot ovat matalammat aspartinsuliinilla kuin lyhytvaikutteisella ihmisinsuliinilla (kuva I). Kahdessa avoimessa tyypin 1 diabetesta sairastavilla potilailla tehdyssä pitkäaikaistutkimuksessa (tutkimuksista ensimmäiseen osallistui 1 070 potilasta ja toiseen 884) aspartinsuliini laski glykohemoglobiinin arvoja: ensimmäisessä tutkimuksessa 0,12 [95 %:n luottamusväli 0,03; 0,22] prosenttiyksiköllä ja toisessa 0,15 [95 %:n luottamusväli 0,05; 0,26] prosenttiyksiköllä ihmisinsuliinin käyttöön verrattuna; tämän eron kliininen merkitys on vähäinen.
Tyypin 1 diabetesta sairastavilla potilailla tehdyt kliiniset tutkimukset ovat osoittaneet, että yöllisen hypoglykemian riski on aspartinsuliinia käytettäessä pienempi kuin lyhytvaikutteista (liukenevaa) ihmisinsuliinia käytettäessä. Päivällä ilmenevän hypoglykemian riski ei ollut merkitsevästi suurempi.
Aspartinsuliini on moolitasolla yhtä tehokas kuin lyhytvaikutteinen ihmisinsuliini.
Erityisryhmät
Iäkkäät (≥ 65-vuotiaat)
Satunnaistetussa, kaksoissokkoutetussa, vaihtovuoroisessa tutkimuksessa verrattiin aspartinsuliinin ja lyhytvaikutteisen (liukenevan) ihmisinsuliinin farmakokinetiikkaa ja farmakodynamiikkaa tyypin 2 diabetesta sairastavilla iäkkäillä potilailla (19 potilasta iältään 65–83 vuotta, iän keskiarvo 70 vuotta). Suhteelliset erot aspartinsuliinin ja ihmisinsuliinin farmakodynaamisissa ominaisuuksissa (GIRmax, AUCGIR, 0–120 min) iäkkäillä olivat samanlaisia kuin terveillä tutkittavilla ja nuoremmilla diabeetikoilla.
Pediatriset potilaat
Pienillä lapsilla (20 lasta, joiden ikä oli 2 vuodesta alle 6 vuoteen ja joista neljä oli alle 4-vuotiaita) tehdyssä, 12 viikkoa kestäneessä kliinisessä tutkimuksessa verrattiin ennen ateriaa annettua liukenevaa ihmisinsuliinia ja aterian jälkeen annettua aspartinsuliinia. Kerta-annoksen farmakokinetiikkaa ja farmakodynamiikkaa tutkittiin lapsilla (6–12-vuotiailla) ja nuorilla (13–17-vuotiailla). Aspartinsuliinin farmakodynaaminen profiili lapsilla oli samanlainen kuin aikuisilla.
Aspartinsuliinin tehoa ja turvallisuutta ateriainsuliinina yhdistettynä perusinsuliineista joko detemir- tai degludekinsuliiniin on tutkittu 12 kuukauden ajan kahdessa satunnaistetussa, kontrolloidussa kliinisessä tutkimuksessa nuorilla ja lapsilla, jotka olivat vähintään 1- ja alle 18-vuotiaita (n = 712). Tutkimuksissa oli mukana 167 iältään 1–5-vuotiasta, 260 iältään 6–11-vuotiasta ja 285 iältään 12–17-vuotiasta lasta. Havaitut parannukset HbA1c-arvoissa ja turvallisuusprofiilit olivat vastaavanlaiset kaikissa ikäryhmissä.
Raskaus
Kliinisessä tutkimuksessa, jossa verrattiin aspartinsuliinin ja ihmisinsuliinin turvallisuutta ja tehoa raskaana olevilla tyypin 1 diabetesta sairastavilla naisilla (322 raskautta (aspartinsuliini: 157; ihmisinsuliini: 165)), ei havaittu, että aspartinsuliinilla olisi raskauteen tai sikiön/vastasyntyneen terveyteen kohdistuvia haittavaikutuksia.
Lisäksi tulokset kliinisestä tutkimuksesta, jossa oli mukana 27 raskausdiabetesta sairastavaa naista, osoittivat turvallisuusprofiilin olevan samanlainen verrattaessa aspartinsuliini- ja ihmisinsuliinihoitoa keskenään. Tutkimuksessa naiset satunnaistettiin saamaan joko aspartinsuliinia (14) tai ihmisinsuliinia (13).
Farmakokinetiikka
Imeytyminen, jakautuminen ja eliminaatio
Aspartinsuliinissa proliiniaminohapon korvaaminen asparagiinihapolla asemassa B28 vähentää lyhytvaikutteisella (liukenevalla) ihmisinsuliinilla havaittua heksameerien muodostustaipumusta. Tästä syystä aspartinsuliini imeytyy ihonalaiskudoksesta lyhytvaikutteista ihmisinsuliinia nopeammin.
Aspartinsuliinin huippupitoisuus saavutetaan keskimäärin puolet lyhyemmässä ajassa kuin lyhytvaikutteisen ihmisinsuliinin. Tyypin 1 diabetesta sairastavilla potilailla aspartinsuliinin keskimääräinen huippupitoisuus plasmassa, 492 ± 256 pmol/l, saavutettiin 40 (kvartiiliväli: 30–40) minuutin kuluttua ihon alle annetusta pistoksesta annoksen ollessa 0,15 yksikköä painokiloa kohden. Veren insuliinipitoisuus palautui lähtötasolle noin 4–6 tunnin kuluttua pistoksesta. Tyypin 2 diabetesta sairastavilla potilailla imeytyminen tapahtui jonkin verran hitaammin, minkä seurauksena huippupitoisuus oli pienempi (Cmax 352 ± 240 pmol/l), ja se saavutettiin myöhemmin, tmax 60 (kvartiiliväli: 50–90) minuuttia. Aspartinsuliinin huippupitoisuuden saavuttamiseen kuluva aika vaihtelee yksilökohtaisesti huomattavasti vähemmän kuin lyhytvaikutteisen ihmisinsuliinin vastaava aika, mutta aspartinsuliinin huippupitoisuus vaihtelee yksilökohtaisesti enemmän.
Erityisryhmät
Iäkkäät (≥ 65-vuotiaat)
Suhteelliset erot aspartinsuliinin ja lyhytvaikutteisen (liukenevan) ihmisinsuliinin farmakokineettisissä ominaisuuksissa tyypin 2 diabetesta sairastavilla iäkkäillä potilailla (65–83 vuotta, iän keskiarvo 70 vuotta) olivat samankaltaisia kuin on havaittu terveillä tutkittavilla ja nuoremmilla diabeetikoilla. Iäkkäillä potilailla imeytyminen oli hidastunut, minkä vuoksi tmax oli pidentynyt (82 (kvartiiliväli: 60‑120) minuuttia), kun taas Cmax oli samaa luokkaa kuin oli havaittu nuoremmilla tyypin 2 diabetesta sairastavilla potilailla ja hieman pienempi kuin tyypin 1 diabetesta sairastavilla potilailla.
Maksan vajaatoiminta
Aspartinsuliinin kerta-annoksen farmakokinetiikkaa arvioitiin 24 tutkittavalla, joilla maksan toiminta oli normaali tai joilla oli lievä, kohtalainen tai vaikea maksan vajaatoiminta. Maksan vajaatoimintaa sairastavilla imeytymisnopeus oli pienentynyt ja vaihtelevampi, minkä vuoksi tmax oli pidentynyt noin 50 minuutista tutkittavilla, joilla oli normaali maksan toiminta, noin 85 minuuttiin potilailla, joilla oli kohtalainen tai vaikea maksan vajaatoiminta. AUC-, Cmax- ja CL/F-arvot olivat samankaltaisia potilailla, joilla maksan toiminta oli heikentynyt, kuin tutkittavilla, joilla maksan toiminta oli normaali.
Munuaisten vajaatoiminta
Aspartinsuliinin kerta-annoksen farmakokinetiikkaa arvioitiin 18 tutkittavalla, joilla munuaisten toiminta oli normaali tai joilla oli lievä, kohtalainen tai vaikea munuaisten vajaatoiminta. Kreatiniinipuhdistuman arvoilla ei ollut selvää vaikutusta aspartinsuliinin AUC-, Cmax-, CL/F- ja tmax-arvoihin. Tietoa oli vain vähän potilaista, joilla oli kohtalainen tai vaikea munuaisten vajaatoiminta. Potilaita, joilla munuaisten vajaatoiminta vaati dialyysihoitoa, ei tutkittu.
Pediatriset potilaat
Aspartinsuliinin farmakokineettisiä ja farmakodynaamisia ominaisuuksia tutkittiin tyypin 1 diabetesta sairastavilla lapsilla (6–12-vuotiailla) ja nuorilla (13–17-vuotiailla). Aspartinsuliini imeytyi molemmissa ikäryhmissä nopeasti, ja tmax oli samansuuruinen kuin aikuisilla. Cmax kuitenkin vaihteli ikäryhmien välillä, ja tässä korostuukin aspartinsuliinin yksilöllisen annostitrauksen merkitys.
Prekliiniset tiedot turvallisuudesta
Farmakologista turvallisuutta, toistuvan altistuksen aiheuttamaa toksisuutta, genotoksisuutta sekä lisääntymis- ja kehitystoksisuutta koskevien konventionaalisten tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille.
In vitro -kokeissa, joissa tutkittiin myös sitoutumista insuliini- ja IGF-1-reseptoreihin sekä vaikutuksia solun kasvuun, aspartinsuliini käyttäytyi lähes samoin kuin ihmisinsuliini. Tutkimukset osoittavat myös, että aspartinsuliini irtoaa insuliinireseptorista kuten ihmisinsuliini.
Farmaseuttiset tiedot
Apuaineet
Fenoli
Metakresoli
Sinkkikloridi
Polysorbaatti 20
Natriumkloridi
Kloorivetyhappo (pH:n säätämiseen)
Natriumhydroksidi (pH:n säätämiseen)
Injektionesteisiin käytettävä vesi
Yhteensopimattomuudet
Insulin aspart Sanofi -valmisteeseen lisätyt aineet saattavat aiheuttaa aspartinsuliinin hajoamista.
Tätä lääkevalmistetta ei saa laimentaa tai sekoittaa muiden lääkevalmisteiden kanssa.
Insulin aspart Sanofi ‑insuliinin sekoittaminen NPH-insuliinin kanssa ei ole suositeltavaa, koska yhteensopivuustutkimuksia ei ole tehty.
Kestoaika
Ennen ensimmäistä käyttökertaa:
30 kuukautta.
Ensimmäisen käyttökerran jälkeen:
4 viikkoa.
Säilytys
Insulin aspart Sanofi 100 yksikköä/ml injektioneste, liuos, esitäytetty kynä
Ennen ensimmäistä käyttökertaa
Säilytä jääkaapissa (2–8 °C). Ei saa jäätyä.
Pidä esitäytetty kynä ulkopakkauksessa. Herkkä valolle.
Ensimmäisen käyttökerran jälkeen
Säilytä alle 30 °C. Älä säilytä kylmässä. Ei saa jäätyä.
Pidä kynänsuojus paikallaan. Herkkä valolle.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
INSULIN ASPART SANOFI injektioneste, liuos, esitäytetty kynä
100 U/ml (L:ei) 5 x 3 ml (SoloStar) (30,77 €)
PF-selosteen tieto
Insulin aspart Sanofi 100 yksikköä/ml injektioneste, liuos, esitäytetty kynä
Tyypin 1 värittömästä lasista valmistettu sylinteriampulli, jossa harmaa mäntä (bromibutyylikumia) ja suljin (alumiinia), jossa tiivistelevy (isopreenistä ja bromibutyylikumista valmistettua laminaattia) kertakäyttöisessä injektiokynässä (SoloStar).
Yksi esitäytetty kynä sisältää 3 ml liuosta.
Pakkauskoot: 1, 5 tai 10 esitäytettyä kynää.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Valmisteen kuvaus:
Kirkas, väritön vesiliuos.
Käyttö- ja käsittelyohjeet
Tarkista Insulin aspart Sanofi ‑liuos. Tätä lääkevalmistetta ei saa käyttää, jos liuos ei ole kirkasta, väritöntä ja veden kaltaista.
Insulin aspart Sanofi ‑valmistetta ei saa käyttää, jos se on jäätynyt.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Insulin aspart Sanofi 100 yksikköä/ml injektioneste, liuos, esitäytetty kynä
Mahdollisten sairauksien leviämisen ehkäisemiseksi samaa kynää saa käyttää vain yhdelle potilaalle, vaikka neula vaihdettaisiinkin.
Älä säilytä esitäytettyä kynää neula kiinnitettynä.
Käytä aina uutta neulaa jokaista pistosta varten.
Pakkauksessa ei ole mukana neuloja.
Korvattavuus
INSULIN ASPART SANOFI injektioneste, liuos, esitäytetty kynä
100 U/ml 5 x 3 ml
- Ylempi erityiskorvaus (100 %). Diabetes, insuliinihoito (103).
- Peruskorvaus (40 %).
ATC-koodi
A10AB05
Valmisteyhteenvedon muuttamispäivämäärä
05.02.2026
Yhteystiedot
Revontulenkuja 1
02100 Espoo
0201 200 300
www.sanofi.fi

 SANOFI OY
SANOFI OY