ENERZAIR BREEZHALER inhalaatiojauhe, kapseli, kova 114/46/136 mikrog
Vaikuttavat aineet ja niiden määrät
Yksi kapseli sisältää 150 mikrog indakaterolia (asetaattina), 63 mikrog glykopyrroniumbromidia, joka vastaa 50 mikrog glykopyrroniumia, ja 160 mikrog mometasonifuroaattia (indacaterol./glycopyrron./mometason. fur.).
Jokainen inhalaattorista saatava annos (annos, joka vapautuu inhalaattorin suukappaleesta) sisältää 114 mikrog indakaterolia (asetaattina), 58 mikrog glykopyrroniumbromidia, joka vastaa 46 mikrog glykopyrroniumia, ja 136 mikrog mometasonifuroaattia.
Apuaine, jonka vaikutus tunnetaan
Yksi kapseli sisältää 25 mg laktoosia (monohydraattina).
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Inhalaatiojauhe, kapseli, kova (inhalaatiojauhe)
Kliiniset tiedot
Käyttöaiheet
Enerzair Breezhaler on tarkoitettu astman ylläpitohoitoon aikuisille, joiden ylläpitohoidossa oireita ei saada riittävästi hallintaan pitkävaikutteisen beeta2‑agonistin ja suuriannoksisen inhaloitavan kortikosteroidin yhdistelmällä ja joilla on ollut edeltävänä vuonna vähintään yksi astman pahenemisvaihe.
Annostus ja antotapa
Annostus
Suositusannos on yhden kapselin sisältö inhaloituna kerran vuorokaudessa.
Suurin suositeltu annos on 114 mikrog/46 mikrog/136 mikrog kerran vuorokaudessa.
Hoito otetaan samaan aikaan päivästä joka päivä. Se voidaan ottaa mihin aikaan päivästä hyvänsä. Jos annos jää väliin, se on otettava mahdollisimman pian. Potilaille on kerrottava, ettei yhden vuorokauden aikana saa ottaa enempää kuin yhden annoksen.
Erityisryhmät
Iäkkäät potilaat
Iäkkäiden potilaiden (65 vuotta täyttäneiden) annosta ei tarvitse muuttaa (ks. kohta Farmakokinetiikka).
Munuaisten vajaatoiminta
Annosta ei tarvitse muuttaa, jos potilaalla on lievä tai keskivaikea munuaisten vajaatoiminta. Jos potilaalla on vaikea tai loppuvaiheen munuaisten vajaatoiminta, joka vaatii dialyysihoitoa, varovaisuutta on noudatettava (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Farmakokinetiikka).
Maksan vajaatoiminta
Annosta ei tarvitse muuttaa, jos potilaalla on lievä tai keskivaikea maksan vajaatoiminta. Tietoja lääkevalmisteen käytöstä vaikeaa maksan vajaatoimintaa sairastavilla potilailla ei ole saatavilla, joten sitä tulee käyttää näillä potilailla ainoastaan, mikäli odotettu hyöty on suurempi kuin mahdollinen riski (ks. kohta Farmakokinetiikka).
Pediatriset potilaat
Enerzair Breezhaler -valmisteen turvallisuutta ja tehoa alle 18-vuotiaiden lasten hoidossa ei ole varmistettu. Tietoja ei ole saatavilla.
Antotapa
Vain inhalaatioon. Kapseleita ei saa niellä.
Kapselit pitää aina ottaa jokaisen uuden pakkauksen mukana toimitettavaa inhalaattoria käyttäen (ks. kohta Käyttö- ja käsittelyohjeet).
Potilaita pitää neuvoa lääkevalmisteen oikeasta käyttötavasta. Jos potilaan hengittäminen ei helpotu, häneltä on varmistettava, ettei hän niele lääkevalmistetta inhaloinnin sijaan.
Kapselit saa ottaa repäisypakkauksesta vasta juuri ennen käyttöä.
Inhalaation jälkeen potilaan on huuhdeltava suunsa vedellä nielaisematta vettä (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Käyttö- ja käsittelyohjeet).
Ks. kohdasta Käyttö- ja käsittelyohjeet ohjeet lääkevalmisteen käytöstä ennen lääkkeen antoa.
Vasta-aiheet
Yliherkkyys vaikuttaville aineille tai kohdassa Apuaineet mainituille apuaineille.
Varoitukset ja käyttöön liittyvät varotoimet
Taudin paheneminen
Tätä lääkevalmistetta ei saa käyttää akuuttien astmaoireiden hoitoon, mukaan lukien akuutit bronkospasmijaksot. Tässä tapauksessa on käytettävä lyhytvaikutteista keuhkoputkia laajentavaa valmistetta. Oireiden lievittämiseen käytettävien lyhytvaikutteisten keuhkoputkia laajentavien valmisteiden käytön lisääntyminen viittaa hoitotasapainon huononemiseen, jolloin lääkärin on tutkittava tilanne.
Potilaiden ei pidä lopettaa hoitoa ilman lääkärin valvontaa, sillä oireet voivat uusiutua lopettamisen jälkeen.
Hoitoa tällä lääkevalmisteella ei ole suositeltavaa lopettaa äkillisesti. Jos potilas kokee hoidon tehottomaksi, hoitoa on jatkettava, mutta potilaan on käännyttävä lääkärin puoleen. Oireiden lievittämiseen käytettävien keuhkoputkia laajentavien valmisteiden käytön lisääntyminen viittaa perussairauden pahenemiseen, jolloin hoidon uudelleenarviointi on tarpeen. Astmaoireiden äkillinen, etenevä paheneminen voi olla henkeä uhkaavaa, ja lääkärin on arvioitava tilanne pikaisesti.
Yliherkkyys
Tämän lääkevalmisteen annostelun jälkeen on havaittu välittömiä yliherkkyysreaktioita. Jos allergiseen reaktioon viittaavia merkkejä ilmenee, etenkin angioedeemaa (hengitys- tai nielemisvaikeuksia; kielen, huulten tai kasvojen turpoamista), urtikariaa tai ihottumaa, hoito on välittömästi lopetettava ja muu, vaihtoehtoinen lääkitys aloitettava.
Paradoksaalinen bronkospasmi
Kuten muidenkin inhalaatiovalmisteiden anto, myös tämän lääkevalmisteen anto voi johtaa paradoksaaliseen bronkospasmiin, joka voi olla hengenvaarallinen. Tässä tapauksessa hoito on lopetettava heti ja sen sijasta on aloitettava muu hoito.
Kardiovaskulaariset vaikutukset
Kuten muutkin beeta2-agonisteja sisältävät valmisteet, tämä lääkevalmiste voi aiheuttaa joillekin potilaille kliinisesti merkittäviä kardiovaskulaarivaikutuksia, jotka ilmenevät syketaajuuden tihenemisenä, verenpaineen kohoamisena ja/tai muina oireina. Tällaisessa tilanteessa hoito saatetaan joutua lopettamaan.
Tämän lääkevalmisteen käytössä tulee noudattaa varovaisuutta, jos potilaalla on jokin kardiovaskulaarisairaus (sepelvaltimotauti, akuutti sydäninfarkti, rytmihäiriöitä, hypertensio), kouristuksia aiheuttava sairaus tai tyreotoksikoosi, sekä jos potilas on tavallista herkempi beeta2-agonisteille.
Indakateroli/glykopyrronium/mometasonifuroaattivalmisteen kliinisen tutkimusohjelman tutkimuksista suljettiin pois potilaat, joilla oli epästabiili iskeeminen sydänsairaus, anamneesissa sydäninfarkti edeltäneiden 12 kk aikana, NYHA-luokituksen (New York Heart Association) luokan III/IV vasemman kammion vajaatoiminta, rytmihäiriö, kontrolloimaton hypertensio, aivoverisuonisairaus tai anamneesissa pitkän QT-ajan oireyhtymä sekä tunnetusti QTc-aikaa pidentäviä lääkevalmisteita käyttäneet potilaat. Näiden potilasryhmien turvallisuustuloksia pidetään tuntemattomina.
Beeta2‑agonistit ovat aiheuttaneet myös EKG-muutoksia kuten T-aallon madaltumista, QT-ajan pitenemistä ja ST-laskua. Havaintojen kliinisestä merkityksestä ei kuitenkaan ole tietoa.
Pitkävaikutteisten beeta2-agonistien (LABA) tai LABA-valmistetta sisältävien yhdistelmävalmisteiden kuten Enerzair Breezhalerin käytössä on siis noudatettava varovaisuutta, jos potilaalla on tunnettu tai epäilty QT-välin piteneminen tai jos potilas saa jotakin QT-väliin vaikuttavaa lääkevalmistetta.
Beeta-agonistien käyttöön liittyvä hypokalemia
Joillekin potilaille beeta2-agonistit saattavat aiheuttaa merkittävää hypokalemiaa, joka altistaa kardiovaskulaarihaitoille. Seerumin kaliumpitoisuuksien pieneneminen on yleensä ohimenevää eikä vaadi kaliumlisän käyttöä. Vaikeaa astmaa sairastavilla hypoksia ja samanaikainen hoito saattavat pahentaa hypokalemiaa, mikä voi suurentaa rytmihäiriöherkkyyttä (ks. kohta Yhteisvaikutukset).
Kliinisesti merkittäviä hypokaleemisia vaikutuksia ei ole havaittu suositellulla terapeuttisella indakateroli/glykopyrronium/mometasonifuroaattiannoksella suoritetuissa kliinisissä tutkimuksissa.
Hyperglykemia
Suurten beeta2-agonistiannosten inhaloiminen saattaa suurentaa plasman glukoosipitoisuuksia. Diabeetikkojen plasman glukoosipitoisuuksia tulee seurata tavanomaista tarkemmin hoidon aloittamisen yhteydessä.
Tätä lääkevalmistetta ei ole tutkittu potilailla, joilla on tyypin I diabetes tai huonossa hoitotasapainossa oleva tyypin II diabetes.
Glykopyrroniumiin liittyvät antikolinergiset vaikutukset
Kuten muidenkin antikolinergisten lääkevalmisteiden kohdalla, tämän lääkevalmisteen käytössä on noudatettava varovaisuutta, jos potilaalla on ahdaskulmaglaukooma tai virtsaumpi.
Potilaille on kerrottava akuutin ahdaskulmaglaukooman merkeistä ja oireista, ja heitä on kehotettava lopettamaan hoitoa ja ottamaan heti yhteys lääkäriin, jos heille kehittyy joitakin näistä merkeistä tai oireista.
Potilaat, joilla on vaikea munuaisten vajaatoiminta
Jos potilaalla on vaikea munuaisten vajaatoiminta (glomerulusten laskennallinen suodatusnopeus alle 30 ml/min/1,73 m2), mukaan lukien dialyysihoitoa vaativa loppuvaiheen munuaissairaus, varovaisuutta on noudatettava (ks. kohdat Annostus ja antotapa ja Farmakokinetiikka).
Suunielutulehdusten ehkäisy
Potilaita tulee kehottaa huuhtelemaan suuta tai kurlaamaan vedellä, ilman nielemistä, tai harjaamaan hampaat määrätyn annoksen inhaloinnin jälkeen, suunielun candida-infektion riskin vähentämiseksi.
Kortikosteroidien systeemiset vaikutukset
Inhaloitavat kortikosteroidit voivat aiheuttaa systeemisiä vaikutuksia etenkin, jos niitä käytetään suurina annoksina pitkiä aikoja. Tällaisten vaikutusten todennäköisyys on kuitenkin huomattavasti pienempi kuin peroraalisia kortikosteroideja käytettäessä.
Myös potilaskohtaisia ja kortikosteroidivalmistekohtaisia eroja voi esiintyä. Mahdollisia systeemisiä vaikutuksia voivat olla Cushingin oireyhtymä, Cushingin oireyhtymän kaltaiset piirteet, lisämunuaistoiminnan lamaantuminen, kasvun hidastuminen lapsilla ja nuorilla, luuntiheyden pieneneminen, kaihi, glaukooma ja harvinaisemmissa tapauksissa myös monenlaiset psyykeen/käyttäytymiseen kohdistuvat vaikutukset kuten psykomotorinen yliaktiivisuus, unihäiriöt, ahdistuneisuus, masennus tai aggressiivisuus (erityisesti lapsilla). Tästä syystä on tärkeää titrata inhaloitava kortikosteroidiannos pienimmälle tehokkaalle tasolle, jolla astman hoitotasapaino pysyy hyvänä.
Systeemisten ja paikallisten (ml. intranasaaliset, inhaloitavat ja intraokulaariset) kortikosteroidien käytön yhteydessä voidaan ilmoittaa näköhäiriöitä. Potilailla, joilla on esimerkiksi näön hämärtymistä tai muita näköhäiriöitä, on harkittava lähetettä silmälääkärille näköhäiriöiden mahdollisten aiheuttajien arvioimiseksi. Näitä voivat olla kaihi, glaukooma tai harvinaissairaudet kuten sentraalinen seroosi korioretinopatia (CSCR), joita on ilmoitettu systeemisesti ja paikallisesti käytettävien kortikosteroidien käytön jälkeen.
Tämän lääkevalmisteen käytössä on noudatettava varovaisuutta, jos potilaalla on keuhkotuberkuloosi tai krooninen tai hoitamaton infektio.
Apuaineet
Tämä lääkevalmiste sisältää laktoosia. Potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, täydellinen laktaasinpuutos tai glukoosi‑galaktoosi-imeytymishäiriö, ei pidä käyttää tätä lääkettä.
Yhteisvaikutukset
Indakateroli/glykopyrronium/mometasonifuroaattivalmisteella ei ole tehty erityisiä yhteisvaikutustutkimuksia. Tiedot mahdollisista yhteisvaikutuksista perustuvat kunkin vaikuttavan aineen yhteisvaikutuspotentiaalia koskeviin tietoihin.
QTc-aikaa tunnetusti pidentävät lääkevalmisteet
Kuten muitakin beeta2-agonisteja sisältäviä lääkevalmisteita, myös tämä lääkevalmiste tulee käyttää varoen potilailla, joita hoidetaan monoamiinioksidaasin estäjillä, trisyklisillä masennuslääkkeillä tai tunnetusti QT-aikaa pidentävillä lääkevalmisteilla, sillä niiden mahdollinen vaikutus QT-aikaan voi voimistua. QT-aikaa tunnetusti pidentävien lääkevalmisteiden käyttö voi suurentaa kammioperäisten rytmihäiriöiden riskiä (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Farmakodynamiikka).
Hypokaleemisesti vaikuttavat hoidot
Samanaikainen hoito hypokalemiaa aiheuttavilla lääkkeillä (metyyliksantiinijohdokset, steroidit tai kaliumia säästämättömät diureetit) saattaa tehostaa beeta2-agonistien mahdollista hypokaleemista vaikutusta (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Beetasalpaajat
Beetasalpaajat saattavat heikentää tai estää beeta2-agonistien vaikutusta. Näin ollen tätä lääkevalmistetta ei pidä käyttää yhdessä beetasalpaajien kanssa, ellei niiden käyttöön ole painavaa syytä. Jos beetasalpaajan käyttö on tarpeen, tulee ensisijaisesti valita kardioselektiivinen beetasalpaaja, mutta niidenkin käytössä on noudatettava varovaisuutta.
Yhteisvaikutukset CYP3A4:n ja P-glykoproteiinin estäjien kanssa
CYP3A4:n ja P-glykoproteiinin (P-gp) esto ei vaikuta hoitoannoksilla käytettävän Enerzair Breezhaler valmisteen turvallisuuteen.
Indakaterolipuhdistuman kannalta keskeisten tekijöiden (CYP3A4:n ja P-gp:n) tai mometasonifuroaattipuhdistuman kannalta keskeisten tekijöiden (CYP3A4:n) toiminnan estyminen suurentaa systeemisen indakateroli- tai mometasonifuroaattialtistuksen jopa kaksinkertaiseksi.
Inhaloituna annetun mometasonifuroaatin pitoisuudet plasmassa ovat hyvin pienet, joten kliinisesti merkittävät interaktiot eivät ole todennäköisiä. Systeeminen altistus mometasonifuroaatille saattaa kuitenkin mahdollisesti suurentua, kun samanaikaisesti käytetään voimakkaita CYP3A4:n estäjiä (esim. ketokonatsoli, itrakonatsoli, nelfinaviiri, ritonaviiri, kobisistaatti).
Simetidiini tai muut orgaanisten kationien kuljetusta estävät aineet
Terveille vapaaehtoisille tehdyssä kliinisessä tutkimuksessa glykopyrroniumin kokonaisaltistus (AUC) suureni 22 % ja munuaispuhdistuma pieneni 23 %, kun potilaille annettiin simetidiiniä, joka estää orgaanisten kationien kuljetusta ja jonka arvellaan vaikuttavan glykopyrroniumin munuaiseritykseen. Näiden muutosten suuruusluokan perusteella kliinisesti merkittäviä yhteisvaikutuksia ei ole odotettavissa, kun glykopyrroniumia annetaan samanaikaisesti simetidiinin tai muiden orgaanisten kationien kuljetuksen estäjien kanssa.
Muut pitkävaikutteiset antikolinergit ja pitkävaikutteiset beeta2-agonistit
Tämän lääkevalmisteen käyttöä muiden pitkävaikutteisia antikolinergisiä lääkeaineita tai pitkävaikutteisia beeta2-agonisteja sisältävien valmisteiden kanssa ei ole tutkittu. Yhteiskäyttöä ei suositella, sillä se voi voimistaa haittavaikutuksia (ks. kohdat Haittavaikutukset ja Yliannostus).
Raskaus ja imetys
Raskaus
Enerzair Breezhaler valmisteen tai yksittäisten vaikuttavien aineiden (indakateroli, glykopyrronium ja mometasonifuroaatti) käytöstä raskauden aikana ei ole riittävästi tietoa mahdollisen riskin määrittämiseksi.
Ihon alle annettu indakateroli ja inhalaationa annettu glykopyrronium eivät olleet teratogeenisia rotalla eivätkä kanilla (ks. kohta Prekliiniset tiedot turvallisuudesta). Eläintutkimuksissa kantavilla hiirillä, rotilla ja kaneilla mometasonifuroaatti suurensi sikiöepämuodostumien esiintyvyyttä ja heikensi sikiöiden eloonjäämistä ja kasvua.
Kuten muutkin beeta2-agonistit, indakateroli saattaa vaikeuttaa synnytystä relaksoimalla kohdun sileää lihasta.
Tätä lääkevalmistetta ei pidä käyttää raskauden aikana, ellei hoidon odotettavissa oleva hyöty potilaalle oikeuta sikiöön mahdollisesti kohdistuvaa riskiä.
Imetys
Indakaterolin, glykopyrroniumin tai mometasonifuroaatin esiintymisestä rintamaidossa, hoidon vaikutuksesta imetettävään lapseen ja hoidon vaikutuksesta maidoneritykseen ei ole tietoa. Muut inhaloitavat kortikosteroidit, jotka ovat samantapaisia kuin mometasonifuroaatti, siirtyvät ihmisen rintamaitoon. Imettävien rottien maidossa on havaittu indakaterolia, glykopyrroniumia ja mometasonifuroaattia. Kun glykopyrroniumia annettiin laskimoon imettäville rotille, pitoisuudet maidossa nousivat jopa 10‑kertaisiksi verrattuna pitoisuuksiin emon veressä.
On päätettävä lopetetaanko imetys vai pidättäydytäänkö hoidosta ottaen huomioon imetyksen hyödyt lapselle ja hoidosta koituvat hyödyt äidille.
Hedelmällisyys
Eläimillä tehdyt lisääntymistutkimukset ja muut tiedot eivät viittaa miehen tai naisen hedelmällisyyteen kohdistuviin huolenaiheisiin.
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Tällä lääkevalmisteella ei ole haitallista vaikutusta ajokykyyn ja koneidenkäyttökykyyn.
Haittavaikutukset
Yhteenveto turvallisuusprofiilista
Yleisimmät haittavaikutukset 52 viikon aikana olivat astma (pahenemisvaihe) (41,8 %), nenänielun tulehdus (10,9 %), ylähengitystieinfektio (5,6 %) ja päänsärky (4,2 %).
Haittavaikutustaulukko
Haittavaikutukset on lueteltu MedDRA-elinjärjestelmäluokituksen mukaisesti (taulukko 1). Haittavaikutusten yleisyys perustuu IRIDIUM-tutkimukseen. Kunkin elinjärjestelmäluokan haittavaikutukset on järjestetty yleisyysjärjestykseen yleisimmästä alkaen. Haittavaikutukset on esitetty kussakin yleisyysluokassa haittavaikutuksen vakavuuden mukaan alenevassa järjestyksessä. Kunkin haittavaikutuksen kohdalla mainittava yleisyysluokka perustuu seuraavaan käytäntöön (CIOMS III): hyvin yleinen (≥ 1/10), yleinen (≥1/100, <1/10), melko harvinainen (≥1/1 000, <1/100), harvinainen (≥1/10 000, <1/1 000), hyvin harvinainen (<1/10 000).
Taulukko 1 Haittavaikutukset
| Elinjärjestelmä | Haittavaikutukset | Yleisyysluokka |
| Infektiot | Nenänielun tulehdus | Hyvin yleinen |
| Ylähengitystieinfektiot | Yleinen | |
| Kandidiaasi*1 | Yleinen | |
| Virtsatieinfektio*2 | Yleinen | |
| Immuunijärjestelmä | Yliherkkyys*3 | Yleinen |
| Aineenvaihdunta ja ravitsemus | Hyperglykemia*4 | Melko harvinainen |
| Hermosto | Päänsärky*5 | Yleinen |
| Silmät | Kaihi | Melko harvinainen |
| Sydän | Takykardia*6 | Yleinen |
| Hengityselimet, rintakehä ja välikarsina | Astma (pahenemisvaihe) | Hyvin yleinen |
| Suun ja nielun alueen kipu*7 | Yleinen | |
| Yskä | Yleinen | |
| Dysfonia | Yleinen | |
| Ruoansulatuselimistö | Gastroenteriitti*8 | Yleinen |
| Suun kuivuus*9 | Melko harvinainen | |
| Iho ja ihonalainen kudos | Ihottuma*10 | Melko harvinainen |
| Kutina*11 | Melko harvinainen | |
| Luusto, lihakset ja sidekudos | Tuki- ja liikuntaelimistön kipu*12 | Yleinen |
| Lihasspasmit | Yleinen | |
| Munuaiset ja virtsatiet | Dysuria | Melko harvinainen |
| Yleisoireet ja antopaikassa todettavat haitat | Kuume | Yleinen |
* Viittaa haittavaikutustermien ryhmittelyyn seuraavasti: 1 Suun kandidiaasi, suun ja nielun kandidiaasi. 2 Oireeton bakteerivirtsaisuus, bakteerivirtsaisuus, kystiitti, virtsaputkitulehdus, virtsatieinfektio, virusperäinen virtsatieinfektio. 3 Lääkeihottuma, lääkeyliherkkyys, yliherkkyys, ihottuma, kutiava ihottuma, nokkosihottuma. 4 Veren glukoosipitoisuuden suureneminen, hyperglykemia. 5 Päänsärky, jännityspäänsärky. 6 Sinustakykardia, supraventrikulaarinen takykardia, takykardia. 7 Nielemiskipu, epämukava tunne suunielussa, suunielun kipu, nielun ärsytys. 8 Krooninen mahakatarri, enteriitti, gastriitti, gastroenteriitti, ruoansulatuskanavan tulehdus. 9 Suun kuivuus, nielun kuivuus. 10 Lääkeihottuma, ihottuma, papulaarinen ihottuma, kutiava ihottuma. 11 Silmien kutina, kutina, sukuelinten kutina. 12 Selkäkipu, tuki- ja liikuntaelinperäinen rintakipu, tuki- ja liikuntaelimistön kipu, lihaskipu, niskakipu. | ||
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Yliannostusta epäiltäessä on aloitettava yleiset tukitoimet ja oireenmukainen hoito.
Yliannostus aiheuttaa todennäköisesti yksittäisten vaikuttavien aineiden farmakologisiin vaikutuksiin liittyviä oireita, löydöksiä tai haittavaikutuksia (esim. takykardia, vapina, sydämentykytys, päänsärky, pahoinvointi, oksentelu, uneliaisuus, kammioperäiset rytmihäiriöt, metabolinen asidoosi, hypokalemia, hyperglykemia, silmänpaineen nousu [aiheuttaen silmäkipua, näköhäiriöitä tai silmän punoitusta], ummetus tai virtsaamisvaikeudet, hypotalamus-aivolisäke-lisämunuaisakselin toiminnan suppressio).
Kardioselektiivisten beetasalpaajien käyttöä voidaan harkita beeta2-adrenergisten vaikutusten hoitoon, mutta sen tulee aina tapahtua lääkärin valvonnassa ja äärimmäistä varovaisuutta noudattaen, sillä beetasalpaajien käyttö voi johtaa bronkospasmiin. Vakavissa tapauksissa potilaat pitää ottaa sairaalahoitoon.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Obstruktiivisten hengitystiesairauksien lääkkeet, adrenergisten lääkeaineiden ja antikolinergien yhd. valm. sis. kolm. yhd. kortikosteroidien kanssa, ATC-koodi: R03AL12
Vaikutusmekanismi
Tämä lääkevalmiste sisältää yhdistelmänä indakaterolia, joka on pitkävaikutteinen beeta2‑agonisti (LABA), glykopyrroniumia, joka on pitkävaikutteinen antikolinergi (LAMA), sekä mometasonifuroaattia, joka on inhaloitava synteettinen kortikosteroidi (ICS).
Indakateroli
Beeta2‑agonistien (indakateroli mukaan lukien) farmakologiset vaikutukset johtuvat ainakin osittain syklisen 3’, 5’‑adenosiinimonofosfaatin (syklinen AMP) pitoisuuden suurenemisesta, joka johtaa keuhkoputkien sileän lihaksen relaksoitumiseen.
Inhaloidulla indakaterolilla on keuhkoissa paikallinen bronkodilatoiva vaikutus. Indakateroli on ihmisen beeta2‑adrenoreseptorin osittainen agonisti, jonka teho ilmenee jo nanomolaarisilla pitoisuuksilla. Eristetyissä ihmisen keuhkoputkissa indakaterolin vaikutus alkaa nopeasti ja kestää pitkään.
Vaikka beeta2‑adrenergiset reseptorit ovat vallitsevia adrenergisia reseptoreja keuhkoputkien sileässä lihaksessa ja beeta1‑adrenergiset reseptorit sydämessä, on ihmisen sydämessä silti myös beeta2‑adrenergisia reseptoreja, joiden osuus kaikista adrenergisista reseptoreista on 10–50 %.
Glykopyrronium
Glykopyrronium vaikuttaa estämällä asetyylikoliinin keuhkoputkia supistavaa vaikutusta hengitysteiden sileissä lihassoluissa ja sitä kautta laajentamalla hengitysteitä. Glykopyrroniumbromidi on muskariinireseptorin antagonisti, jolla on suuri affiniteetti. Kilpailevaa sitoutumista koskeneissa tutkimuksissa on osoitettu, että sen selektiivisyys ihmisen M3- ja M1-reseptoreihin on 4–5-kertainen ihmisen M2-reseptoreihin verrattuna. Glykopyrroniumbromidin vaikutus alkaa nopeasti, mikä havaitaan reseptoriin sitoutumisen ja vapautumisen kinetiikan parametreista sekä kliinisissä tutkimuksissa havaitusta vaikutuksen alkamisesta inhalaation jälkeen. Pitkäkestoisen tehon voidaan katsoa johtuvan osittain keuhkoissa pitkään pysyvistä lääkeainepitoisuuksista. Tätä kuvastaa se, että glykopyrroniumin terminaalinen eliminaation puoliintumisaika on inhalaation jälkeen pidempi kuin laskimoon annon jälkeen (ks. kohta Farmakokinetiikka).
Mometasonifuroaatti
Mometasonifuroaatti on synteettinen kortikosteroidi, joka sitoutuu suurella affiniteetilla glukokortikoidireseptoreihin ja jolla on paikallisia tulehdusta hillitseviä ominaisuuksia. In vitro mometasonifuroaatti estää leukotrieenien vapautumista allergisten potilaiden leukosyyteistä. Soluviljelmissä mometasonifuroaatti esti hyvin tehokkaasti IL‑1:n, IL‑5:n, IL‑6:n ja TNF‑alfan synteesiä ja vapautumista. Se myös estää tehokkaasti leukotrieenien muodostumista ja IL‑4:n ja IL‑5:n (Th2-tyypin sytokiinien) muodostumista ihmisen CD4+ T‑soluissa.
Farmakodynaamiset vaikutukset
Tämän lääkevalmisteen farmakodynaamista vasteprofiilia luonnehtii nopeasti alkava vaikutus 5 minuutin kuluessa lääkkeenannon jälkeen ja pitkäkestoinen teho koko 24 tunnin annosteluvälin ajan.
Farmakodynaamista vasteprofiilia luonnehtii myös uloshengityksen sekuntikapasiteetin (FEV1) suureneminen: indakateroli/glykopyrronium/mometasonifuroaatti 114 mikrog/46 mikrog/136 mikrog x 1 hoidolla 172 ml verrattuna salmeteroli/flutikasonihoitoon 50 mikrog/500 mikrog x 2.
Enerzair Breezhaler valmisteella ei havaittu viitteitä ajan myötä kehittyvästä takyfylaksiasta keuhkotoiminnan kohenemiseen liittyen.
QTc-aika
Tämän lääkevalmisteen vaikutusta QT-aikaan ei ole arvioitu perusteellisessa QT-ajan tutkimuksessa (TQT). Mometasonifuroaatilla ei tiedetä olevan QTc-aikaa pidentäviä vaikutuksia.
Kliininen teho ja turvallisuus
Enerzair Breezhaler -valmisteen ja kiinteiden LABA/ICS yhdistelmävalmisteiden vertailu
Enerzair Breezhaler valmisteen turvallisuutta ja tehoa pitkittynyttä astmaa sairastavilla aikuispotilailla arvioitiin vaiheen III satunnaistetussa, kaksoissokkoutetussa tutkimuksessa (IRIDIUM). IRIDIUM oli 52 viikon pituinen tutkimus, jossa arvioitiin Enerzair Breezhaler 114 mikrog/46 mikrog/68 mikrog x 1 hoitoa (N = 620) ja 114 mikrog/46 mikrog/136 mikrog x 1 hoitoa (N = 619) verrattuna indakateroli/mometasonifuroaatti 125 mikrog/127,5 mikrog x 1 hoitoon (N = 617) ja 125 mikrog/260 mikrog x 1 hoitoon (N = 618). Kolmannen aktiivisen vertailuhoidon ryhmässä tutkimushenkilöt saivat salmeteroli/flutikasonipropionaattihoitoa 50 mikrog/500 mikrog kahdesti vuorokaudessa (N = 618). Kaikkien tutkimushenkilöiden tuli sairastaa oireista astmaa (ACQ 7 pistemäärä ≥ 1,5) ja olla käyttänyt astman ylläpitohoitona keskisuuri tai suuriannoksisen inhaloitavan synteettisen kortikosteroidin (ICS) ja pitkävaikutteisen beeta2-agonistin (LABA) yhdistelmää vähintään 3 kk ajan ennen tutkimukseenottoa. Tutkittavien ikäkeskiarvo oli 52,2 vuotta. Seulontavaiheessa 99,9 % potilaista ilmoitti sairastaneensa pahenemisvaiheen edellisenä vuonna. Tutkimukseenottovaiheessa yleisimmin ilmoitettuja astmalääkkeitä olivat keskisuurella annoksella käytetty inhaloitava kortikosteroidi yhdistelmänä pitkävaikutteisen beeta2-agonistin kanssa (62,6 %) ja suuriannoksinen inhaloitava kortikosteroidi yhdistelmänä pitkävaikutteisen beeta2-agonistin kanssa (36,7 %).
Tutkimuksen ensisijainen tavoite oli osoittaa joko Enerzair Breezhaler 114 mikrog/46 mikrog/ 68 mikrog x 1 hoidon paremmuus suhteessa indakateroli/mometasonifuroaatti 125 mikrog/ 127,5 mikrog x 1 hoitoon tai Enerzair Breezhaler 114 mikrog/46 mikrog/136 mikrog x 1 hoidon paremmuus suhteessa indakateroli/mometasonifuroaatti 125 mikrog/260 mikrog x 1 hoitoon, mitattuna alhaisimmalla FEV1-arvolla viikon 26 kohdalla.
Enerzair Breezhaler 114 mikrog/46 mikrog/136 mikrog x 1 hoidolla havaittiin alhaisimman FEV1-arvon kohenevan tilastollisesti merkitsevästi viikon 26 kohdalla verrattuna vastaavalla annoksella käytettyyn indakateroli/mometasonifuroaattihoitoon. Kliinisesti merkittävää keuhkotoiminnan kohenemista (alhaisimman FEV1-arvon muutos lähtötilanteesta viikon 26 kohdalla, aamulla ja illalla mitattu uloshengityksen huippuvirtausarvo) havaittiin myös verrattuna salmeteroli/flutikasonipropionaatti 50 mikrog/500 mikrog x 2 hoitoon. Viikon 52 kohdalla löydökset olivat yhteneväiset viikon 26 löydöksiin nähden (ks. taulukko 2).
Kaikissa hoitoryhmissä ACQ‑7-mittarilla havaittiin kliinisesti merkittävää kohenemista lähtötilanteesta viikon 26 kohdalla, mutta ryhmien välillä ei havaittu tilastollisesti merkitsevää eroa. ACQ‑7-mittarin keskimuutos lähtötilanteesta viikon 26 kohdalla (tärkeä toissijainen päätetapahtuma) ja viikon 52 kohdalla oli noin ‑1 kaikissa hoitoryhmissä. Taulukossa 2 esitetään ACQ‑vasteprosentit (määritelmänä pistemäärän pieneneminen ≥ 0,5 pisteellä) eri ajankohtina.
Pahenemisvaiheet olivat toissijainen päätetapahtuma (ne eivät kuuluneet vahvistavaan tutkimusmenettelyyn). Enerzair Breezhaler 114 mikrog/46 mikrog/136 mikrog x 1 hoidolla pahenemisvaiheiden vuotuinen määrä pieneni verrattuna salmeteroli/ flutikasonipropionaatti 50 mikrog/500 mikrog x 2 hoitoon sekä indakateroli/mometasonifuroaatti 125 mikrog/260 mikrog x 1 hoitoon (ks. taulukko 2).
Kliinisesti oleellisimpien päätetapahtumien tulokset kuvataan taulukossa 2.
Taulukko 2 Ensi- ja toissijaisten päätetapahtumien tulokset IRIDIUM-tutkimuksessa viikoilla 26 ja 52
| Päätetapahtuma | Ajankohta/ Kesto | Enerzair Breezhaler1 vs. IND/MF2 | Enerzair Breezhaler1 vs. SAL/FP3 |
| Keuhkotoiminta | |||
| Alhaisin FEV14 | |||
Hoitojen ero p-arvo (95 % lv) | Viikko 26 (ensisijainen päätetapahtuma) | 65 ml < 0,001 (31; 99) | 119 ml < 0,001 (85; 154) |
| Viikko 52 | 86 ml < 0,001 (51; 120) | 145 ml < 0,001 (111; 180) | |
| Aamulla mitattu uloshengityksen huippuvirtaus (PEF), keskiarvo | |||
Hoitojen ero (95 % lv) | Viikko 52* | 18,7 l/min (13,4; 24,1) | 34,8 l/min (29,5; 40,1) |
| Illalla mitattu uloshengityksen huippuvirtaus (PEF), keskiarvo | |||
Hoitojen ero (95 % lv) | Viikko 52* | 17,5 l/min (12,3; 22,8) | 29,5 l/min (24,2; 34,7) |
| Oireet | |||
| ACQ-vasteen saaneet (pienimmän kliinisesti merkittävän muutoksen lähtötilanteesta (MCID) saavuttaneet, ACQ ≥ 0,5) | |||
| Prosenttiosuus | Viikko 4 | 66 % vs. 63 % | 66 % vs. 53 % |
Vetosuhde (95 % lv) | 1,21 (0,94; 1,54) | 1,72 (1,35; 2,20) | |
| Prosenttiosuus | Viikko 12 | 68 % vs. 67 % | 68 % vs. 61 % |
Vetosuhde (95 % lv) | 1,11 (0,86; 1,42) | 1,35 (1,05; 1,73) | |
| Prosenttiosuus | Viikko 26 | 71% vs. 74% | 71% vs. 67% |
Vetosuhde (95 % lv) | 0,92 (0,70; 1,20) | 1,21 (0,93; 1,57) | |
| Prosenttiosuus | Viikko 52 | 79 % vs. 78 % | 79 % vs. 73 % |
Vetosuhde (95 % lv) | 1,10 (0,83; 1,47) | 1,41 (1,06; 1,86) | |
| Astman pahenemisvaiheiden vuotuinen määrä | |||
| Keskivaikeat tai vaikeat pahenemisvaiheet | |||
| AR | Viikko 52 | 0,46 vs. 0,54 | 0,46 vs. 0,72 |
RR** (95 % lv) | Viikko 52 | 0,85 (0,68; 1,04) | 0,64 (0,52; 0,78) |
| Vaikeat pahenemisvaiheet | |||
| AR | Viikko 52 | 0,26 vs. 0,33 | 0,26 vs. 0,45 |
RR** (95 % lv) | Viikko 52 | 0,78 (0,61; 1,00) | 0,58 (0,45; 0,73) |
* Hoidon keston keskiarvo. ** Jos RR oli < 1,00, indakateroli/glykopyrronium/mometasonifuroaatti tuotti paremmat tulokset. 1 Enerzair Breezhaler annos 114 mikrog/46 mikrog/136 mikrog x 1. 2 IND/MF: indakateroli/mometasonifuroaatti,; suuri annos: 125 mikrog/260 mikrog x 1. Enerzair Breezhaler valmisteen sisältämä 136 mikrog mometasonifuroaattiannos on verrattavissa indakateroli/mometasonifuroaattivalmisteen sisältämään 260 mikrog mometasonifuroaattiannokseen. 3 SAL/FP: salmeteroli/flutikasonipropionaatti; suuri annos: 50 mikrog/500 mikrog x 2 (sisällön määrä). 4 Alhaisin FEV1: 23 h 15 min kuluttua ja 23 h 45 min kuluttua ilta-annoksen jälkeen mitattujen kahden FEV1-arvon keskiarvo. Ensisijainen päätetapahtuma (alhaisin FEV1 viikon 26 kohdalla) ja tärkeä toissijainen päätetapahtuma (ACQ‑7 -pistemäärä viikon 26 kohdalla) kuuluivat vahvistavaan tutkimusmenettelyyn, joten päätetapahtumat oli kontrolloitu multiplisiteetin suhteen. Mitkään muut päätetapahtumat eivät kuuluneet vahvistavaan tutkimusmenettelyyn. RR = esiintyvyyssuhde, AR = vuotuinen määrä x 1 = kerran vuorokaudessa, x 2 = kahdesti vuorokaudessa | |||
Enerzair Breezhaler-valmisteen ja samanaikaisesti avoimesti annetun salmeteroli/flutikasoni +tiotropium-yhdistelmän vertailu
Satunnaistetussa, osittain sokkoutetussa, aktiivihoitokontrolloidussa, non‑inferiority-tutkimuksessa (ARGON) verrattiin Enerzair Breezhaler-annosta 114 mikrog/46 mikrog/136 mikrog kerran vuorokaudessa (N=476) ja annosta 114 mikrog/46 mikrog/68 mikrog kerran vuorokaudessa (N=474) samanaikaiseen salmeteroli/flutikasonipropionaatti 50 mikrog/500 mikrog annokseen kahdesti vuorokaudessa + 5 mg tiotropium kerran vuorokaudessa (N=475) 24 viikon hoidon ajan.
Enerzair Breezhaler osoittautui vähintään yhdenveroiseksi (non-inferior) salmeteroli/flutikasoni + tiotropium -yhdistelmään nähden ensisijaisen päätetapahtuman osalta (muutos astman elämänlaatukyselyn lähtötasosta [AQLQ-S]) aiemmin oireellisilla ICS- ja LABA-hoitoa saaneilla potilailla eron ollessa 0,073 (yksisuuntainen alempi 97,5 %:n luottamusväli [CL]: -0,027).
Pediatriset potilaat
Euroopan lääkevirasto on myöntänyt lykkäyksen velvoitteelle toimittaa tutkimustulokset indakateroli/glykopyrronium/mometasonifuroaattivalmisteen käytöstä astman hoidossa yhdessä tai useammassa pediatrisessa potilasryhmässä (ks. kohdasta Annostus ja antotapa ohjeet käytöstä pediatristen potilaiden hoidossa).
Farmakokinetiikka
Imeytyminen
Enerzair Breezhaler -inhalaation jälkeen mediaaniaika indakaterolihuippupitoisuuden saavuttamiseen plasmassa on noin 15 minuuttia, glykopyrroniumhuippupitoisuuden saavuttamiseen noin 5 minuuttia ja mometasonifuroaattihuippupitoisuuden saavuttamiseen noin 1 tunti.
In vitro -tutkimuksista kerättyjen tietojen perusteella kunkin yksittäisen vaikuttavan aineen keuhkoihin jakautuvan annoksen oletetaan olevan indakateroli/glykopyrronium/mometasonifuroaatti -yhdistelmävalmisteella samankaltainen kuin kullakin monoterapiana käytetyllä valmisteella. Vakaassa tilassa yhdistelmävalmisteen inhalaation jälkeen saavutettu indakateroli-, glykopyrronium- ja mometasonifuroaattialtistus plasmassa oli vastaava kuin systeeminen altistus pelkkää indakaterolimaleaattia, glykopyrroniumia tai mometasonifuroaattia sisältävän valmisteen inhaloinnin jälkeen.
Yhdistelmävalmisteen inhaloinnin jälkeen indakaterolin absoluuttisen biologisen hyötyosuuden on arvioitu olevan noin 45 %, glykopyrroniumin noin 40 % ja mometasonifuroaatin alle 10 %.
Indakateroli
Indakaterolipitoisuudet suurenivat, kun lääke otettiin toistuvasti kerran vuorokaudessa. Vakaa tila saavutettiin 12–14 päivässä. Kun 60–480 mikrogramman annoksia (inhalaattorista saatava annos) inhaloitiin kerran vuorokaudessa, indakaterolin keskimääräinen kumuloitumissuhde (24 tunnin AUC-arvo päivänä 14 verrattuna päivään 1) oli 2,9–3,8. Systeeminen altistus johtuu sekä keuhkoista että ruoansulatuskanavasta tapahtuvasta imeytymisestä. Noin 75 % systeemisestä altistuksesta oli peräisin keuhkoista tapahtuvasta imeytymisestä ja noin 25 % suolistosta tapahtuvasta imeytymisestä.
Glykopyrronium
Inhalaation jälkeen noin 90 % systeemisestä altistuksesta on peräisin keuhkoista tapahtuvasta imeytymisestä ja 10 % suolistosta tapahtuvasta imeytymisestä. Suun kautta annetun glykopyrroniumin absoluuttisen biologisen hyötyosuuden arvioitiin olevan noin 5 %.
Mometasonifuroaatti
Mometasonifuroaattipitoisuudet suurenivat, kun lääke otettiin Breezhaler-inhalaattorilla toistuvasti kerran vuorokaudessa. Vakaa tila saavutettiin 12 päivän kuluttua. Kun 68–136 mikrogramman annoksia (indakateroli/glykopyrronium/mometasonifuroaatti yhdistelmävalmisteen hoidon osana) inhaloitiin kerran vuorokaudessa, mometasonifuroaatin keskimääräinen kumuloitumissuhde (24 tunnin AUC-arvo päivänä 14 verrattuna päivään 1) oli 1,28–1,40.
Suun kautta annetun mometasonifuroaatin absoluuttinen systeeminen biologinen hyötyosuus arvioitiin hyvin pieneksi (< 2 %).
Jakautuminen
Indakateroli
Laskimoinfuusion jälkeen indakaterolin jakautumistilavuus (Vz) oli 2 361–2 557 litraa, mikä viittaa siihen, että lääkeaine jakautuu voimakkaasti kudoksiin. In vitro kokeissa 94,1–95,3 % sitoutui ihmisen seerumin proteiineihin ja 95,1–96,2 % plasman proteiineihin.
Glykopyrronium
Kun glykopyrroniumia annettiin laskimoon, vakaan tilan jakautumistilavuus (Vss) oli 83 litraa ja terminaalivaiheen jakautumistilavuus (Vz) oli 376 litraa. Terminaalivaiheen näennäinen jakaantumistilavuus inhalaation jälkeen (Vz/F) oli 7 310 litraa, mikä kuvastaa paljon hitaampaa eliminaatiota inhalaation jälkeen. Glykopyrroniumin sitoutuminen ihmisen plasman proteiineihin in vitro oli 38–41 %, kun pitoisuudet olivat 1–10 nanogrammaa/ml. Nämä pitoisuudet olivat vähintään 6 kertaa suuremmat kuin 44 mikrog x 1 antoprotokollaa noudatettaessa saavutettava vakaan tilan huippupitoisuuksien keskiarvo plasmassa.
Mometasonifuroaatti
Laskimoon annetun bolusannoksen jälkeen Vd on 332 litraa. Mometasonifuroaatti sitoutuu voimakkaasti proteiineihin in vitro: 5–500 ng/ml pitoisuusalueella sitoutuminen on 98–99-prosenttista.
Biotransformaatio
Indakateroli
Kun radioaktiivisesti leimattua indakaterolia annettiin suun kautta ihmisellä tehdyssä imeytymis-, jakautumis-, metabolia- ja eliminaatiotutkimuksessa, seerumissa tavattiin lähinnä muuttumatonta indakaterolia, joka selitti noin kolmanneksen lääkkeen vuorokausialtistuksesta (24 tunnin AUC). Runsaimmin seerumissa tavattu metaboliitti oli indakaterolin hydroksyloitunut johdannainen. Muita runsaina esiintyneitä metaboliitteja olivat indakaterolin ja hydroksyloituneen indakaterolin fenoli-O-glukuronidit. Lisäksi tavattiin hydroksyloituneen metaboliitin diastereomeeriä, indakaterolin N-glukuronidia ja C- ja N-dealkylaation kautta muodostuneita metaboliitteja.
In vitro tutkimukset viittasivat siihen, että ainoa indakaterolia fenoli-O-glukuronidiksi metaboloiva UGT-isoentsyymi oli UGT1A1. Kun indakaterolia inkuboitiin rekombinanttien CYP1A1-, CYP2D6- ja CYP3A4-entsyymien kanssa, havaittiin oksidaatiotuotteita. CYP3A4:n todettiin olevan tärkein indakaterolia hydroksyloiva isoentsyymi. In vitro tutkimukset viittasivat myös siihen, että indakateroli on P-gp-ulosvirtauspumpun substraatti. Sen P-gp-affiniteetti on kuitenkin pieni.
UGT1A1-isoformi on tärkeä indakaterolin metaboliseen puhdistumaan vaikuttava isoentsyymi in vitro. Kliinisessä tutkimuksessa, johon osallistui eri UGT1A1-genotyyppejä edustavia henkilöitä, UGT1A1-genotyypeillä ei kuitenkaan todettu olevan merkittävää vaikutusta systeemiseen indakaterolialtistukseen.
Glykopyrronium
Metaboliatutkimukset in vitro osoittivat glykopyrroniumbromidin metaboliareittien olevan samat eläimissä ja ihmisissä. Ihmiselle spesifisiä metaboliitteja ei havaittu. Havaittiin hydroksylaatiota, josta syntyi erilaisia mono- ja bishydroksyloituja metaboliitteja, samoin kuin suoraa hydrolyysia, josta muodostui karboksyylihappojohdosta (M9).
In vitro tutkimusten mukaan useat CYP-isoentsyymit osallistuvat glykopyrroniumin oksidatiiviseen biotransformaatioon. On todennäköistä, että koliiniesteraasiperheen jäsenet katalysoivat hydrolyysia M9-johdokseksi.
Inhalaation jälkeen systeeminen altistus M9-johdokselle oli keskimäärin samaa luokkaa kuin altistus kanta-aineelle. In vitro tutkimuksissa ei havaittu keuhkoissa tapahtuvaa metaboliaa, ja M9:n osuus verenkierrossa oli laskimoon tapahtuneen lääkkeenannon jälkeen vähäinen (noin 4 % kanta-aineen Cmax ja AUC-arvoista). Näin ollen oletetaan, että M9 muodostuu inhaloidun glykopyrroniumbromidiannoksen niellystä osuudesta pre‑systeemisen hydrolyysin ja/tai ensikierron metabolian kautta. Sekä inhalaation että laskimoon tapahtuneen lääkkeenannon jälkeen M9-johdosta havaittiin virtsassa vain minimaalisina määrinä (≤ 0,5 % annoksesta). Glukuronidia ja/tai glykopyrroniumin sulfaattikonjugaatteja havaittiin ihmisen virtsassa toistuvien inhalaatioiden jälkeen, ja niiden osuus oli noin 3 % annoksesta.
Inhibitiotutkimukset in vitro osoittivat, että glykopyrroniumbromidi ei estä merkitsevästi CYP1A2-, CYP2A6-, CYP2C8-, CYP2C9-, CYP2C19-, CYP2D6-, CYP2E1- tai CYP3A4/5-isoentsyymeitä, effluksikuljettajaproteiineja MDR1, MRP2 tai MXR eikä soluunoton kuljettajaproteiineja OATP1B1, OATP1B3, OAT1, OAT3, OCT1 tai OCT2. Entsyymi-induktiotutkimukset in vitro eivät viitanneet glykopyrroniumbromidin indusoivan kliinisesti merkittävästi mitään tutkituista P450-isoentsyymeistä eikä myöskään UGT1A1-entsyymiä tai MDR1- ja MRP2-kuljettajia.
Mometasonifuroaatti
Se osuus inhaloidusta mometasonifuroaattiannoksesta, joka nielaistaan ja joka imeytyy ruoansulatuskanavasta, käy läpi laajan metabolian useiksi eri metaboliiteiksi. Plasmassa ei havaita päämetaboliitteja. Ihmisen maksan mikrosomeissa mometasonifuroaatti metaboloituu CYP3A4:n välityksellä.
Eliminaatio
Indakateroli
Kliinisissä tutkimuksissa, joissa virtsaa kerättiin talteen, todettiin, että yleensä alle 2 % annoksesta erittyi muuttumattomana indakaterolina virtsaan. Indakaterolin munuaispuhdistuma oli keskimäärin 0,46–1,20 l/h. Kun tätä verrataan indakaterolin puhdistumaan seerumista, joka on 18,8–23,3 l/h, on selvää, että munuaispuhdistumalla on vähäinen merkitys systeemiseen verenkiertoon päässeen indakaterolin eliminaation kannalta (noin 2–6 % systeemisestä puhdistumasta).
Ihmisen imeytymis-, jakautumis-, metabolia- ja eliminaatiotutkimuksessa, jossa indakaterolia annettiin suun kautta, lääkettä erittyi ulosteeseen enemmän kuin virtsaan. Indakateroli erittyi ihmisen ulosteeseen lähinnä muuttumattoman kanta-aineen muodossa (54 % annoksesta) ja vähäisemmässä määrin myös indakaterolin hydroksyloituneina metaboliitteina (23 % annoksesta). Massatasapaino oli täydellinen, ja ≥ 90 % annoksesta erittyi ulosteeseen.
Seerumin indakaterolipitoisuudet pienenivät monivaiheisesti, ja terminaalinen puoliintumisaika oli keskimäärin 45,5–126 tuntia. Toistuvan indakateroliannostelun yhteydessä tapahtuvasta kumuloitumisesta laskettu efektiivinen puoliintumisaika oli 40–52 tuntia. Tämä on yhtäpitävää sen kanssa, että vakaan tilan saavuttamiseen kuluva aika on havaintojen mukaan noin 12–14 vrk.
Glykopyrronium
Kun [3H]-merkittyä glykopyrroniumbromidia annettiin laskimoon, keskimääräinen virtsaan erittynyt radioaktiivisuus 48 tunnin aikana oli 85 % annoksesta. Lisäksi sappinesteessä havaittiin 5 % annoksesta. Massatasapaino oli siis lähes täydellinen.
Kanta-aineen eliminaatio munuaisten kautta muodostaa noin 60–70 % systeemisen glykopyrroniumin kokonaispuhdistumasta, kun taas ei-renaalisen puhdistuman osuus on noin 30–40 %. Biliaarinen puhdistuma on osa ei-renaalista puhdistumaa, mutta arvellaan, että suurin osa ei-renaalisesta puhdistumasta tapahtuu metaboloitumalla.
Glykopyrroniumin munuaispuhdistuman keskiarvo oli 17,4–24,4 litraa/h. Aktiivinen tubulaarinen eritys myötävaikuttaa glykopyrroniumin eliminaatioon munuaisten kautta. Jopa 20 % annoksesta havaittiin virtsassa kanta-aineena.
Glykopyrroniumin pitoisuudet plasmassa pienenivät monivaiheisesti. Keskimääräinen terminaalinen eliminaation puoliintumisaika oli paljon pidempi inhalaation jälkeen (33–57 tuntia) verrattuna laskimonsisäiseen (6,2 tuntia) ja suun kautta (2,8 tuntia) tapahtuneeseen annosteluun. Eliminaatiotapa viittaa pitkäkestoiseen imeytymiseen keuhkoista ja/tai glykopyrroniumin siirtymiseen systeemiseen verenkiertoon 24 tunnin kuluttua tai myöhemmin inhalaation jälkeen.
Mometasonifuroaatti
Laskimoon annetun bolusannoksen jälkeen mometasonifuroaatin terminaalinen eliminaation T½-aika on noin 4,5 tuntia. Radioaktiivisesti merkitty, suun kautta inhaloitu annos erittyy lähinnä ulosteeseen (74 %) ja vähemmässä määrin virtsaan (8 %).
Yhteisvaikutukset
Vakaassa tilassa indakaterolin, glykopyrroniumin ja mometasonifuroaatin samanaikainen suun kautta tapahtuva inhalaatio ei vaikuta minkään vaikuttavan aineen farmakokinetiikkaan.
Erityisryhmät
Enerzair Breezhaler -inhalaation jälkeen astmapotilailta kerättyjen populaatiofarmakokineettisten tietojen analyysissä ei havaittu viitteitä siitä, että ikä, sukupuoli, paino, tupakointistatus, lähtötilanteen glomerulusten laskennallinen suodatusnopeus (eGFR) tai lähtötilanteen FEV1-arvo vaikuttaisivat merkitsevästi systeemiseen indakateroli-, glykopyrronium- tai mometasonifuroaattialtistukseen.
Potilaat, joilla on munuaisten vajaatoiminta
Munuaisten vajaatoiminnan vaikutusta indakaterolin, glykopyrroniumin ja mometasonifuroaatin farmakokinetiikkaan ei ole arvioitu erityisissä Enerzair Breezhaler valmisteella suoritetuissa tutkimuksissa. Populaatiofarmakokinetiikan analyysissa glomerulusten laskennallinen suodatusnopeus (eGFR) ei ollut tilastollisesti merkitsevä kovariaatti indakaterolin, glykopyrroniumin tai mometasonifuroaatin systeemiselle altistukselle, kun Enerzair Breezhaler valmistetta annettiin astmapotilaille.
Koska hyvin pieni osa indakaterolista ja mometasonifuroaatista eliminoituu virtsan kautta, munuaisten vajaatoiminnan vaikutusta systeemiseen altistukseen näille lääkeaineille ei ole tutkittu (ks. kohdat Annostus ja antotapa ja Varoitukset ja käyttöön liittyvät varotoimet).
Munuaisten vajaatoiminta vaikuttaa systeemiseen altistukseen glykopyrroniumille, kun lääkeainetta käytetään ainoana lääkkeenä. Potilailla, joilla oli lievä tai kohtalainen munuaisten vajaatoiminta, todettiin kohtalainen systeemisen kokonaisaltistuksen (AUClast) suurentuminen enimmillään keskimäärin 1,4-kertaiseksi. Potilailla, joilla oli vaikea munuaisen vajaatoiminta tai loppuvaiheen munuaissairaus, kokonaisaltistus suureni enimmillään keskimäärin 2,2-kertaiseksi. Astmapotilailla toteutetun glykopyrroniumin populaatiofarmakokinetiikan analyysin perusteella Enerzair Breezhaler valmisteen annon jälkeen AUC0–24h suureni 27 % potilailla, joiden absoluuttinen GFR oli 58 ml/min, ja pieneni 19 % potilailla, joiden absoluuttinen GFR oli 143 ml/min, verrattuna potilaisiin, joiden absoluuttinen GFR-arvo oli 93 ml/min. Populaatiofarmakokinetiikan analyysin perusteella lääkittäessä keuhkoahtaumatautipotilaita, joilla on lievä tai kohtalainen munuaisten vajaatoiminta (eGFR ≥ 30 ml/min/1,73 m2), glykopyrroniumbromidia voidaan käyttää suositusannoksella.
Potilaat, joilla on maksan vajaatoiminta
Maksan vajaatoiminnan vaikutusta indakaterolin, glykopyrroniumin ja mometasonifuroaatin farmakokinetiikkaan ei ole arvioitu maksan vajaatoimintaa sairastavilla potilailla Enerzair Breezhaler valmisteen annon jälkeen. Valmisteen vaikuttavista aineista indakaterolia ja mometasonifuroaattia on kuitenkin tutkittu ainoana lääkkeenä (ks. kohta Annostus ja antotapa).
Indakateroli
Indakaterolin Cmax- ja AUC-arvoissa ei havaittu oleellisia muutoksia lievää tai keskivaikeaa maksan vajaatoimintaa sairastavilla potilailla, eivätkä nämä potilaat eronneet terveistä verrokeista myöskään proteiineihin sitoutumisen suhteen. Vaikeaa maksan vajaatoimintaa sairastavilla ei ole tehty tutkimuksia.
Glykopyrronium
Maksan vajaatoimintaa sairastaville potilaille ei ole tehty kliinisiä tutkimuksia. Glykopyrronium poistuu systeemisestä verenkierrosta pääosin erittymällä munuaisten kautta. Glykopyrroniumin maksametabolian heikkenemisen ei oleteta aiheuttavan kliinisesti merkittävää systeemisen altistuksen suurentumista.
Mometasonifuroaatti
Tutkimuksessa arvioitiin 400 mikrog mometasonifuroaattikerta-annoksen inhalaatiota jauheinhalaattorista tutkimushenkilöille, joilla oli lievä (n = 4), keskivaikea (n = 4) tai vaikea (n = 4) maksan vajaatoiminta. Kussakin näistä ryhmistä mometasonifuroaatin huippupitoisuudet plasmassa olivat havaittavissa (vaihteluväli 50–105 pikogrammaa/ml) vain 1 tai 2 tutkittavalla. Havaitut huippupitoisuudet plasmassa ilmeisesti suurenevat maksan vajaatoiminnan vaikeusasteen myötä. Havaittavia pitoisuuksia kuitenkin todettiin vain harvoin (määrityksen kvantifikaatioalaraja oli 50 pikogrammaa/ml).
Muut erityisryhmät
Systeemisessä kokonaisaltistuksessa (AUC) ei havaittu huomattavia eroja japanilaisten ja valkoihoisten välillä indakaterolin, glykopyrroniumin eikä mometasonifuroaatin osalta. Muiden etnisten ryhmien osalta ei ole riittävästi farmakokineettistä tietoa saatavilla. Glykopyrroniumin systeeminen kokonaisaltistus (AUC) voi olla jopa 1,8-kertaisesti suurentunut kevyillä (35 kg) astmapotilailla ja jopa 2,5-kertaisesti suurentunut kevyillä (35 kg) astmapotilailla, joilla on pieni absoluuttinen GFR (45 ml/min).
Prekliiniset tiedot turvallisuudesta
Indakaterolin, glykopyrroniumin ja mometasonifuroaatin yhdistelmällä ei ole tehty eläintutkimuksia. Seuraavassa esitetään kunkin monoterapian sekä indakateroli/mometasoniyhdistelmähoidon ja indakateroli/glykopyrroniumyhdistelmähoidon ei-kliiniset arvioinnit:
Indakateroli
Indakaterolin beeta2-agonistisesta vaikutuksesta johtuvia kardiovaskulaarisia vaikutuksia olivat koirilla havaitut takykardia, rytmihäiriöt ja sydänlihasvauriot. Jyrsijöillä todettiin lievää nenäontelon ja kurkunpään ärsytystä.
Geenitoksisuustutkimuksissa ei havaittu mutageenisuutta eikä klastogeenisuutta.
Karsinogeenisuutta arvioitiin kaksivuotisessa tutkimuksessa rotalla ja 6 kk pituisessa tutkimuksessa siirtogeenisellä hiirellä. Rotalla havaittiin munasarjojen hyvänlaatuisten leiomyoomien ja munasarjojen sileän lihaksen paikallisen hyperplasian yleistymistä. Tämä vastasi muilla beeta2-agonisteilla ilmoitettuja samankaltaisia havaintoja. Hiirellä ei todettu viitteitä karsinogeenisuudesta.
Kaikki nämä löydökset havaittiin altistuksilla, jotka olivat riittävästi ihmisen odotettavissa olevaa altistusta suuremmat.
Kun indakaterolia annettiin kaneille ihon alle, tiineyteen ja alkion-/sikiönkehitykseen liittyviä haittavaikutuksia havaittiin vasta yli 500‑kertaisilla annoksilla verrattuna altistuksiin, joita saavutetaan ihmisellä päivittäisen 150 mikrog annoksen inhalaation jälkeen (AUC0–24 h-arvon perusteella).
Vaikka indakateroli ei vaikuttanut rottien tavallisiin lisääntymistoimintoihin rotilla tehdyssä hedelmällisyystutkimuksessa, pieneni tiineeksi tulleiden F1-jälkeläisten osuus tehdyssä peri- ja postnataalisen kehityksen rottatutkimuksessa, jossa altistus oli 14-kertainen verrattuna indakaterolilla hoidettuihin ihmisiin. Indakateroli ei ollut alkiotoksinen eikä teratogeeninen rotalla eikä kanilla.
Glykopyrronium
Glykopyrroniumin muskariinireseptoriantagonistisista ominaisuuksista johtuviin vaikutuksiin sisältyivät lievä tai kohtalainen syketaajuuden kiihtyminen koirilla, mykiön samentumat rotilla sekä korjautuvat rauhaserityksen vähenemiseen liittyvät muutokset rotilla ja koirilla. Rotilla todettiin lievää ärsytystä tai adaptiivisia muutoksia hengitysteissä. Kaikki nämä löydökset havaittiin altistuksilla, jotka olivat riittävästi ihmisen odotettavissa olevaa altistusta suuremmat.
Genotoksisuustutkimuksissa ei havaittu merkkejä glykopyrroniumin mahdollisista mutageenisistä tai klastogeenisista vaikutuksista. Karsinogeenisuustutkimuksissa transgeenisillä hiirillä suun kautta annettuna ja rotilla inhalaationa annettuna ei ilmennyt viitteitä karsinogeenisuudesta.
Glykopyrronium ei ollut teratogeeninen rotalla eikä kanilla inhalaation jälkeen. Glykopyrronium ja sen metaboliitit eivät merkittävässä määrin läpäisseet istukkaa tiineillä hiirillä, kaneilla ja koirilla. Glykopyrroniumin eläintutkimuksista julkaistut tiedot eivät viittaa lisääntymistoksisuuteen liittyviin huolenaiheisiin. Rotilla ei todettu hedelmällisyyteen eikä jälkeläisten pre- ja postnataaliseen kehitykseen kohdistuvia vaikutuksia.
Mometasonifuroaatti
Kaikki havaitut vaikutukset ovat tyypillisiä glukokortikoidien luokkavaikutuksia, ja ne liittyvät glukokortikoidien farmakologisten vaikutusten korostumiseen.
Mometasonifuroaatilla ei osoitettu geenitoksisia vaikutuksia tavanomaisissa in vitro- ja in vivo kokeissa.
Karsinogeenisuustutkimuksissa hiirellä ja rotalla inhaloidun mometasonifuroaatin ei osoitettu suurentavan kasvainten ilmaantuvuutta tilastollisesti merkitsevästi.
Kuten muutkin glukokortikoidit, mometasonifuroaatti on teratogeeninen jyrsijöillä ja kaneilla. Havaittuja vaikutuksia olivat napatyrä rotalla, suulakihalkio hiirellä sekä sappirakon ageneesi, napatyrä ja etukäpälien koukkuasento kanilla. Rotalla, kanilla ja hiirellä havaittiin myös emon painonnousun hidastumista, vaikutuksia sikiön kasvuun (sikiöiden painon pienenemistä ja/tai luutumisen viivästymistä), ja hiirellä havaittiin poikasten eloonjäämisprosentin pienenemistä. Lisääntymistoimintojen tutkimuksissa ihon alle annettu mometasonifuroaatti annoksella 15 mikrog/kg johti tiineyden pitkittymiseen ja vaikeisiin synnytyksiin sekä poikasten eloonjäämisprosentin ja painon pienenemiseen.
Ympäristöön kohdistuvien riskien arviointi
Ympäristöön kohdistuvia riskejä arvioivissa tutkimuksissa on ilmennyt, että mometasoni voi olla haitallista pintavesille (ks. kohta Käyttö- ja käsittelyohjeet).
Indakaterolin ja glykopyrroniumin yhdistelmä
Indakateroli/glykopyrroniumvalmisteen ei-kliinisten turvallisuustutkimusten löydökset olivat johdonmukaiset ainoana lääkkeenä käytettyjen indakateroli- ja glykopyrroniumkomponenttien tunnettujen farmakologisten vaikutusten kanssa.
Indakateroli/glykopyrroniumvalmisteen aiheuttamat sykkeenmuutokset olivat huomattavammat ja pitkäkestoisemmat kuin ainoana lääkkeenä käytettyjen vaikuttavien aineiden aiheuttamat muutokset.
EKG-käyrässä näkyvien välien lyhentymistä ja systolisen sekä diastolisen verenpaineen laskua todettiin myös. Indakaterolin antoon koirille yksinään tai indakateroli/glykopyrroniumyhdistelmän osana liittyi samankaltainen sydänlihasvaurioiden esiintyvyys ja vaikeusaste.
Indakaterolin ja mometasonifuroaatin yhdistelmä
13 viikon pituisten inhalaatiotoksisuustutkimusten löydökset johtuivat pääasiassa mometasonifuroaattikomponentista, ja ne olivat glukokortikoidien tyypillisiä farmakologisia vaikutuksia. Indakateroliin liittyvää sykkeen nopeutumista havaittiin koirilla indakateroli/mometasonifuroaatin tai pelkän indakaterolin annon jälkeen.
Farmaseuttiset tiedot
Apuaineet
Kapselin sisältö
Laktoosimonohydraatti
Magnesiumstearaatti
Kapselin kuori
Hypromelloosi
Karrageeni
Kaliumkloridi
Rautaoksidi, keltainen (E172)
Indigokarmiini (E132)
Vesi, puhdistettu
Painomuste
Vesi, puhdistettu
Rautaoksidi, musta (E172)
Isopropyylialkoholi
Propyleeniglykoli (E1520)
Hypromelloosi (E464)
Yhteensopimattomuudet
Ei oleellinen.
Kestoaika
3 vuotta.
Säilytys
Säilytä alle 30 °C.
Säilytä alkuperäispakkauksessa. Herkkä valolle. Herkkä kosteudelle.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
ENERZAIR BREEZHALER inhalaatiojauhe, kapseli, kova
114/46/136 mikrog (L:kyllä) 30 x 1 fol (inhalaattori) (73,14 €), 90 x 1 fol (inhalaattori) (199,36 €)
PF-selosteen tieto
Inhalaattorin runko-osa ja suojus on valmistettu akryylinitriilibutadieenistyreenistä (ABS), ja painikkeet on valmistettu metyylimetakrylaatti-ABS:stä. Neulat ja jouset ovat ruostumatonta terästä.
Yksittäispakattu PA/Alu/PVC//Alu-repäisypakkaus. Yksi repäisypakkaus sisältää 10 kovaa kapselia.
Yksittäispakkaus sisältää 10 x 1, 30 x 1 tai 90 x 1 kovaa kapselia sekä 1 inhalaattorin.
Monipakkaus sisältää 150 (15 pakkausta, joissa 10 x 1) kovaa kapselia ja 15 inhalaattoria.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Valmisteen kuvaus:
Kapseli, jossa on vihreä, läpinäkyvä kansiosa ja väritön, läpinäkyvä runko ja joka sisältää valkoista jauhetta. Runko-osaan on mustalla painettu tuotekoodi ”IGM150‑50‑160” kahden mustan viivan ylle, ja kansiosaan on mustalla painettu valmisteen logo, jota ympäröi musta viiva.
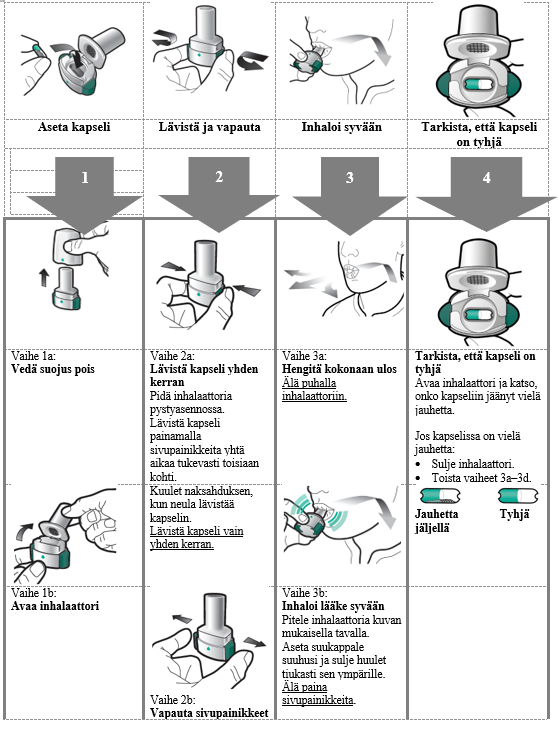
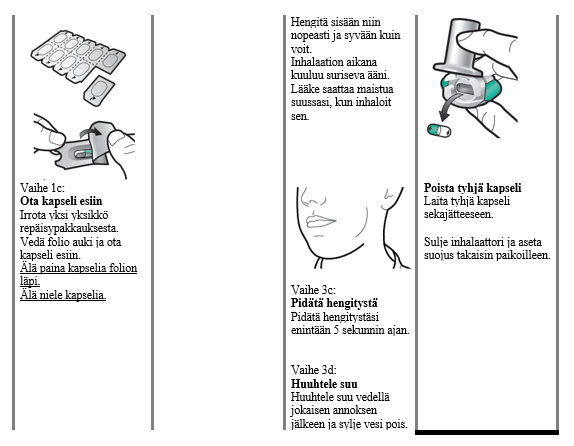
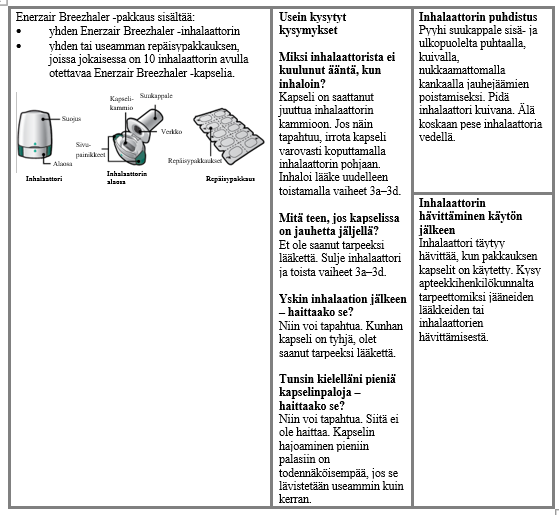
Käyttö- ja käsittelyohjeet
Potilaan tulee käyttää kunkin pakkauksen mukana toimitettavaa inhalaattoria. Jokaisen pakkauksen inhalaattori on hävitettävä, kun kaikki pakkauksen kapselit on käytetty.
Tämä lääkevalmiste voi aiheuttaa riskin ympäristölle (ks. kohta Prekliiniset tiedot turvallisuudesta).
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Käsittely- ja käyttöohjeet
Lue Käyttöohjeet kokonaan ennen kuin käytät Enerzair Breezhaler -valmistetta.

Korvattavuus
ENERZAIR BREEZHALER inhalaatiojauhe, kapseli, kova
114/46/136 mikrog 30 x 1 fol, 90 x 1 fol
- Alempi erityiskorvaus (65 %). Krooninen keuhkoastma ja sitä läheisesti muistuttavat krooniset obstruktiiviset keuhkosairaudet (203).
- Peruskorvaus (40 %).
ATC-koodi
R03AL12
Valmisteyhteenvedon muuttamispäivämäärä
20.11.2025
Yhteystiedot
Revontulenkuja 1
02100 Espoo
010 613 3200
www.novartis.fi
Lääkeinformaatiopalvelu 010 6133 210,
medinfo.nordics@novartis.com

 NOVARTIS FINLAND OY
NOVARTIS FINLAND OY