NUCALA injektionsvätska, lösning i förfylld injektionspenna 100 mg, injektionsvätska, lösning i förfylld spruta 40 mg, 100 mg
Kvalitativ och kvantitativ sammansättning
Nucala 100 mg injektionsvätska, lösning, i förfylld injektionspenna
Varje 1 ml innehåller 100 mg mepolizumab.
Nucala 100 mg injektionsvätska, lösning, i förfylld spruta
Varje 1 ml innehåller 100 mg mepolizumab.
Nucala 40 mg injektionsvätska, lösning, i förfylld spruta
Varje 0,4 ml innehåller 40 mg mepolizumab.
Mepolizumab är en humaniserad monoklonal antikropp framställd i ovarieceller från kinesisk hamster med rekombinant DNA-teknik.
Hjälpämne med känd effekt
Nucala 100 mg injektionsvätska, lösning, i förfylld injektionspenna
Varje 1 ml-förfylld injektionspenna innehåller 0,2 mg polysorbat 80.
Nucala 100 mg injektionsvätska, lösning, i förfylld spruta
Varje 1 ml-förfylld spruta innehåller 0,2 mg polysorbat 80.
Nucala 40 mg injektionsvätska, lösning, i förfylld spruta
Varje 0,4 ml-förfylld spruta innehåller 0,08 mg polysorbat 80.
För fullständig förteckning över hjälpämnen, se avsnitt Förteckning över hjälpämnen.
Läkemedelsform
Injektionsvätska, lösning
Kliniska uppgifter
Terapeutiska indikationer
Svår eosinofil astma
Nucala är avsett som tilläggsbehandling vid svår refraktär eosinofil astma hos vuxna, ungdomar och barn från 6 års ålder (se avsnitt Farmakodynamiska egenskaper).
Kronisk rinosinuit med näspolyper (CRSwNP)
Nucala är avsett som tilläggsbehandling till intranasala kortikosteroider för behandling av vuxna patienter med svår CRSwNP, som inte uppnår tillräcklig sjukdomskontroll med systemiska kortikosteroider och/eller kirurgi.
Kroniskt obstruktiv lungsjukdom (KOL)
Nucala är avsett som underhållsbehandling för vuxna med okontrollerad kroniskt obstruktiv lungsjukdom (KOL) som karakteriseras av ökat antal eosinofiler i blodet, i tillägg till en kombination av inhalationssteroider (ICS), en långverkande beta2-agonist (LABA) och en långverkande muskarinantagonist (LAMA) (se avsnitt Farmakodynamiska egenskaper).
Eosinofil granulomatös polyangit (EGPA)
Nucala är avsett som tilläggsbehandling till patienter från 6 års ålder med remitterande eller refraktär eosinofil granulomatös polyangit (EGPA).
Hypereosinofilt syndrom (HES)
Nucala är avsett som tilläggsbehandling för vuxna patienter med otillräckligt kontrollerat hypereosinofilt syndrom utan identifierbar icke-hematologisk sekundär orsak (se avsnitt Farmakodynamiska egenskaper).
Villkor
Valmistetta saavat määrätä vain käyttöaiheessa mainitun sairauden diagnosointiin ja hoitoon perehtyneet lääkärit.
Dosering och administreringssätt
Det rekommenderas att Nucala förskrivs av läkare med erfarenhet av diagnos och behandling av allvarlig refraktär eosinofil astma, CRSwNP, KOL, EGPA eller HES.
Dosering
Svår eosinofil astma
Vuxna och ungdomar från 12 års ålder
Rekommenderad dos mepolizumab är 100 mg administrerat subkutant en gång var fjärde vecka.
Barn 6 till 11 år
Rekommenderad dos mepolizumab är 40 mg administrerat subkutant en gång var fjärde vecka.
Nucala är avsett för långtidsbehandling. Behovet av fortsatt behandling ska omprövas minst en gång om året baserat på läkarens bedömning av sjukdomens svårighetsgrad och patientens kontroll över exacerbationer.
CRSwNP
Vuxna
Rekommenderad dos mepolizumab är 100 mg administrerat subkutant en gång var fjärde vecka.
Nucala är avsett för långtidsbehandling. Alternativa behandlingar kan övervägas till patienter med
CRSwNP som inte visat någon behandlingsrespons efter 24 veckor. Vissa patienter med initial partiell respons kan eventuellt förbättras vid fortsatt behandling längre än 24 veckor.
KOL
Vuxna
Rekommenderad dos mepolizumab är 100 mg administrerat subkutant en gång var fjärde vecka.
Nucala är avsett för långtidsbehandling. Behovet av fortsatt behandling ska utvärderas minst en gång om året baserat på läkarens bedömning av sjukdomens svårighetsgrad och nivå av exacerbationskontroll.
EGPA
Vuxna och ungdomar från 12 års ålder
Rekommenderad dos mepolizumab är 300 mg administrerat subkutant en gång var fjärde vecka.
Dosen av mepolizumab till barn och ungdomar 6 till 17 år med EGPA stöds av modellerings- och simuleringsdata (se avsnitt Farmakokinetiska egenskaper).
Barn 6 till 11 år som väger ≥40 kg
Rekommenderad dos mepolizumab är 200 mg administrerat subkutant en gång var fjärde vecka.
Barn 6 till 11 år som väger <40 kg
Rekommenderad dos mepolizumab är 100 mg administrerat subkutant en gång var fjärde vecka.
Nucala är avsett för långtidsbehandling. Behovet av fortsatt behandling ska utvärderas minst en gång om året baserat på läkarens bedömning av sjukdomens svårighetsgrad och förbättrad symtomkontroll.
Patienter som utvecklar livshotande symtom av EGPA måste också utvärderas avseende behovet av fortsatt behandling eftersom Nucala inte har studerats i denna population.
HES
Vuxna
Rekommenderad dos för mepolizumab är 300 mg administrerat subkutant en gång var fjärde vecka.
Nucala är avsett för långtidsbehandling. Behovet av fortsatt behandling ska utvärderas minst en gång om året baserat på läkarens bedömning av sjukdomens svårighetsgrad och patientens symtomkontroll.
Patienter som utvecklar livshotande manifestationer av HES måste också utvärderas avseende behovet av fortsatt behandling eftersom Nucala inte har studerats hos denna population.
Speciella populationer
Äldre
Ingen dosjustering krävs för äldre patienter i åldern ≥ 65 år (se avsnitt Farmakokinetiska egenskaper).
Nedsatt njur- och leverfunktion
Ingen dosjustering krävs för patienter med nedsatt njur- eller leverfunktion (se avsnitt Farmakokinetiska egenskaper).
Pediatrisk population
Svår eosinofil astma
Barn 6 till 11 år
Nucala 100 mg pulver till injektionsvätska, lösning, och 40 mg injektionsvätska, lösning, i förfylld spruta är lämpliga för administrering i denna åldersgrupp.
Nucala 100 mg injektionsvätska, lösning, i förfylld injektionspenna och 100 mg injektionsvätska, lösning, i förfylld spruta är inte indicerade för administrering i denna åldersgrupp.
Barn yngre än 6 år
Säkerhet och effekt för mepolizumab för barn under 6 år har ännu inte fastställts. Inga data finns tillgängliga.
CRSwNP
Barn under 18 år
Säkerhet och effekt för mepolizumab för barn yngre än 18 år med CRSwNP har ännu inte fastställts. Inga data finns tillgängliga.
KOL
Barn under 18 år
Det finns ingen relevant användning av mepolizumab för en pediatrisk population (yngre än 18 år) för indikationen KOL.
EGPA
Barn under 6 år
Säkerhet och effekt för mepolizumab för barn yngre än 6 år har ännu inte fastställts. Inga data finns tillgängliga.
HES
Barn yngre än 18 år
Säkerhet och effekt för mepolizumab hos barn och ungdomar yngre än 18 år har ännu inte fastställts.
Tillgänglig information finns i avsnitten Biverkningar, Farmakodynamiska egenskaper och Farmakokinetiska egenskaper men ingen doseringsrekommendation kan fastställas.
Administreringssätt
Nucala 100 mg injektionsvätska, lösning, i förfylld injektionspenna eller förfylld spruta
Den förfyllda injektionspennan eller förfyllda sprutan får endast användas för subkutan injektion.
Nucala kan administreras av patienten själv eller administreras av en vårdare om hälso- och sjukvårdpersonal anser det lämpligt och patienten eller vårdaren har utbildats i injektionsteknik.
För barn mellan 6 till11 år måste Nucala administreras av hälso- och sjukvårdspersonal eller en utbildad vårdare.
Vid själv-administrering rekommenderas magen eller låret som injektionsställe. Vårdare kan även injicera Nucala i överarmen.
Vid doser som kräver fler än en injektion rekommenderas att varje injektion administreras med minst 5 cm mellanrum.
Utförliga instruktioner för subkutan administrering med Nucala förfylld injektionspenna eller förfylld spruta ges i steg-för-steg-anvisningarna i slutet av bipacksedeln.
Nucala 40 mg injektionsvätska, lösning, i förfylld spruta
Den förfyllda sprutan får endast användas för subkutan injektion.
Nucala måste administreras av hälso- och sjukvårdspersonal eller en vårdare. Det kan administreras av en vårdare om hälso- och sjukvårdspersonal anser det lämpligt och vårdaren har utbildats i injektionsteknik.
Rekommenderade injektionsställen är överarmen, magen eller låret.
Utförliga instruktioner för subkutan administrering med Nucala i förfylld spruta ges i steg-för-steg-anvisningarna i slutet av bipacksedeln.
Kontraindikationer
Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt Förteckning över hjälpämnen.
Varningar och försiktighet
Spårbarhet
För att underlätta spårbarhet av biologiska läkemedel ska läkemedlets namn och tillverkningssatsnummer dokumenteras.
Exacerbationer av astma eller KOL
Mepolizumab får inte användas för att behandla akuta astma- eller KOL-exacerbationer.
Astmarelaterade eller KOL-relaterade biverkningar eller exacerbationer kan förekomma under behandling. Patienten måste instrueras att söka läkarvård om astman eller KOL kvarstår utom kontroll eller förvärras efter behandlingsstart.
Kortikosteroider
Abrupt utsättning av kortikosteroider efter behandlingsstart med mepolizumab rekommenderas ej. Vid behov måste kortikosteroiddosen sänkas stegvis under överinseende av läkare.
Överkänslighet och reaktioner i samband med administrering
Akuta och fördröjda systemiska reaktioner, inklusive överkänslighetsreaktioner (t.ex. anafylaxi, urtikaria, angioödem, hudutslag, bronkospasm, hypotoni), har förekommit efter administrering av mepolizumab. Sådana reaktioner uppstår vanligen inom några timmar efter administrering men kan i vissa fall vara fördröjda (dvs. normalt inom flera dagar). Dessa reaktioner kan uppstå för första gången efter att behandlingen har pågått under lång tid (se avsnitt Biverkningar). I händelse av en överkänslighetsreaktion måste lämplig behandling baserat på klinisk status inledas.
Parasitinfektioner
Eosinofiler kan vara involverade i det immunologiska svaret på vissa maskinfektioner. Patienter med befintliga maskinfektioner ska behandlas innan behandling med mepolizumab påbörjas. Om patienten blir infekterad under behandling med Nucala och inte svarar på maskmedel ska temporär utsättning av Nucala övervägas.
KOL-patienter med lågt blodeosinofilvärde
Data stödjer inte användningen av Nucala i patienter med KOL med ett blodeosinofilvärde <150 celler/µl eller utan dokumenterat blodeosinofilvärde ≥300 celler/µl under de senaste 12 månaderna.
EGPA som är organ- eller livshotande
Nucala har inte studerats hos patienter med organ- eller livshotande symtom på EGPA (se avsnitt Dosering och administreringssätt).
Livshotande HES
Nucala har inte studerats hos patienter med livshotande manifestationer av HES (se avsnitt Dosering och administreringssätt).
Hjälpämnen
Detta läkemedel innehåller polysorbat 80 (se avsnitt KVALITATIV OCH KVANTITATIV SAMMANSÄTTNING), som kan orsaka allergiska reaktioner.
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per 100 mg dosering, d.v.s. är näst intill ”natriumfritt”.
Interaktioner
Inga interaktionsstudier har utförts.
Cytokrom P450-enzymer, effluxpumpar och proteinbindningsmekanismer deltar inte i clearance av mepolizumab. Ökade nivåer av proinflammatoriska cytokiner (t.ex. IL-6), via interaktion med deras besläktade receptorer på hepatocyter, har visat sig undertrycka bildningen av CYP450-enzymer och läkemedelstransportörer men förhöjningen av systemiska proinflammatoriska markörer vid svår refraktär eosinofil astma är minimal och det finns inga belägg för uttryck av IL-5-receptor-alfa på hepatocyter. Potentialen för interaktioner med mepolizumab anses därför låg.
Fertilitet, graviditet och amning
Graviditet
Det finns begränsad mängd data (färre än 300 graviditeter) från användningen av mepolizumab hos gravida kvinnor.
Mepolizumab passerar placentabarriären hos apor. Djurstudier tyder inte på reproduktionstoxikologiska effekter (se avsnitt Prekliniska säkerhetsuppgifter). Den potentiella risken för human fosterskada är okänd.
Som en försiktighetsåtgärd bör man undvika användningen av Nucala under graviditet. Administrering av Nucala till gravida kvinnor ska endast övervägas om den förväntade fördelen för modern är större än den eventuella risken för fostret.
Amning
Det finns inga data vad avser utsöndring av mepolizumab i bröstmjölk. Mepolizumab utsöndrades emellertid i mjölken hos cynomolgusapor i lägre koncentrationer än 0,5 % av den påvisade koncentrationen i plasma.
Ett beslut måste fattas om man ska avbryta amningen eller avbryta behandling med Nucala efter att man tagit hänsyn till fördelen med amning för barnet och fördelen med behandling för kvinnan.
Fertilitet
Det finns inga fertilitetsdata för människa. Djurstudier visade inte några negativa effekter på fertiliteten av läkemedel riktade mot IL‑5 (se avsnitt Prekliniska säkerhetsuppgifter).
Effekter på förmågan att framföra fordon och använda maskiner
Nucala har ingen eller försumbar effekt på förmågan att framföra fordon och använda maskiner.
Biverkningar
Sammanfattning av säkerhetsprofilen
Svår eosinofil astma
I placebokontrollerade studier på vuxna och ungdomar med svår refraktär eosinofil astma var huvudvärk (20 %), reaktioner vid injektionsstället (8 %) och ryggvärk (6 %) de oftast rapporterade biverkningarna under behandling.
CRSwNP
I en placebokontrollerad studie på patienter med CRSwNP var huvudvärk (18 %) och ryggvärk (7 %) de oftast rapporterade biverkningarna under behandling.
KOL
I tre placebokontrollerade studier på patienter med KOL var huvudvärk (10 %), ryggvärk (7 %) och artralgi (5 %) de vanligast rapporterade biverkningarna under behandling.
EGPA
I en placebokontrollerad studie på patienter med EGPA var huvudvärk (32 %), reaktioner vid injektionsstället (15%) och ryggvärk (13 %) de oftast rapporterade biverkningarna under behandling. Systemiska allergiska/överkänslighetsreaktioner rapporterades av 4 % av EGPA patienterna.
HES
I en placebokontrollerad studie på patienter med HES var huvudvärk (13 %), urinvägsinfektion (9 %), reaktioner vid injektionsstället och feber (7 % vardera) de oftast rapporterade biverkningarna under behandling.
Tabell över biverkningar
Tabellen nedan presenterar biverkningarna från placebokontrollerade studierna för svår eosinofil astma från de patienter som fick mepolizumab 100 mg subkutant (s.c.) (n=263), en randomiserad, dubbelblind placebokontrollerad 52-veckorsstudie på patienter med CRSwNP som fick mepolizumab 100 mg s.c. (n=206), tre dubbelblinda, placebokontrollerade 52 till 104 veckor långa studier på patienter med KOL som fick mepolizumab 100 mg s.c. (n=1 043), patienter med EGPA som fick mepolizumab 300 mg s.c. (n=68), en dubbelblind placebokontrollerad 32-veckorsstudie på patienter med HES som fick mepolizumab 300 mg s.c. (n=54) och från spontana rapporter efter marknadsföring.
Säkerhetsdata är också tillgänglig från öppna förlängningsstudier hos patienter med svår refraktär eosinofil astma (n=998) behandlade under, i medeltal 2,8 år (intervall 4 veckor till 4,5 år).
Säkerhetsprofilen för mepolizumab hos patienter med HES (n=102) som rekryterades till en öppen förlängningsstudie under 20 veckor liknade säkerhetsprofilen hos de patienter som ingick i den pivotala placebokontrollerade studien.
Biverkningsfrekvensen definieras enligt följande: mycket vanliga (≥1/10), vanliga (≥1/100, <1/10), mindre vanliga (≥1/1 000, <1/100), sällsynta (≥1/10 000, <1/1 000), mycket sällsynta (<1/10 000) och ingen känd frekvens (kan inte beräknas från tillgängliga data). Biverkningarna presenteras inom varje frekvensområde efter fallande allvarlighetsgrad.
| Organsystem | Biverkning | Frekvens |
| Infektioner och infestationer | Nedre luftvägsinfektion Urinvägsinfektion Faryngit Herpes zoster** | Vanliga |
| Immunsystemet | Överkänslighetsreaktioner (systemallergiska)* | Vanliga |
| Anafylaxi** | Sällsynta | |
| Centrala och perifera nervsystemet | Huvudvärk | Mycket vanliga |
| Andningsvägar, bröstkorg och mediastinum | Nästäppa | Vanliga |
| Magtarmkanalen | Övre buksmärta | Vanliga |
| Hud och subkutan vävnad | Eksem | Vanliga |
| Muskuloskeletala systemet och bindväv | Ryggvärk Artralgi** | Vanliga |
| Allmänna symtom och/eller symtom vid administreringsstället | Administreringsrelaterade reaktioner (systemiska icke-allergiska)*** Lokala reaktioner vid injektionsstället Feber | Vanliga |
* Systemiska reaktioner inklusive överkänslighet har rapporterats med en samlad incidens som är jämförbar med den för placebo i studierna av svår eosinofil astma och KOL. Se avsnitt Varningar och försiktighet för exempel på rapporterade manifestationer och beskrivning av tid till debut.
** Från spontanrapportering efter marknadsföring. Herpes zoster rapporterades som mindre vanligt i studier på svår astma.
*** De vanligaste manifestationerna i samband med rapporter av systemiska, icke-allergiska administreringsrelaterade reaktioner hos patienter i studierna av svår eosinofil astma och KOL var hudutslag, värmevallningar, myalgi och trötthet. Dessa manifestationer var mindre vanliga och rapporterades av <1 % av patienterna som fick 100 mg mepolizumab subkutant.
Beskrivning av valda biverkningar
Systemiska reaktioner, inklusive överkänslighetsreaktioner, vid CRSwNP
I den 52 veckor långa placebokontrollerade studien rapporterades systemiska allergiska reaktioner (typ I-överkänslighet) hos 2 patienter (<1 %) i gruppen som fick 100 mg mepolizumab och inte hos någon patient i placebogruppen. Andra systemiska reaktioner rapporterades inte hos någon patient i gruppen som fick 100 mg mepolizumab och hos 1 patient (<1 %) i placebogruppen.
Systemiska reaktioner, inklusive överkänslighetsreaktioner, vid KOL
I den 52 till 104 veckor långa placebokontrollerade studien rapporterades systemiska allergiska reaktioner (typ I-överkänslighet) hos 1 patient (<1 %) i gruppen som fick 100 mg mepolizumab och inte hos någon patient i placebogruppen. Andra systemiska reaktioner rapporterades av 4 patienter (<1 %) i gruppen som fick 100 mg mepolizumab och hos 4 patienter (<1 %) i placebogruppen.
I de två 52 veckor långa placebokontrollerade studierna rapporterades systemiska allergiska reaktioner hos 4 patienter (<1 %) i grupperna som fick 100 mg mepolizumab och hos 3 patienter (<1 %) i placebogrupperna. Andra systemiska reaktioner rapporterades av 7 patienter (1 %) i grupperna som fick 100 mg mepolizumab och hos 10 patienter (2 %) i placebogrupperna.
Systemiska reaktioner, inklusive överkänslighetsreaktioner, vid EGPA
I den 52 veckor långa placebokontrollerade studien var andelen patienter som fick systemiska (allergiska och icke-allergiska) reaktioner 6 % i gruppen som fick 300 mg mepolizumab och 1 % i placebogruppen. Systemiska allergiska/överkänslighetsreaktioner rapporterades hos 4 % av patienterna i gruppen som fick 300 mg mepolizumab och 1 % av patienterna i placebogruppen. Systemiska icke-allergiska reaktioner (angioödem) rapporterades hos 1 patient (1 %) i gruppen som fick 300 mg mepolizumab och inte hos någon patient i placebogruppen.
Systemiska reaktioner, inklusive överkänslighet, vid HES
I den placebokontrollerade 32-veckorsstudien rapporterades en systemisk (övrig) reaktion hos 1 patient (2 %) i gruppen som fick 300 mg mepolizumab (multifokal hudreaktion) och inte hos någon patient i placebogruppen.
Lokala reaktioner vid injektionsstället
Svår eosinofil astma
I placebokontrollerade studier var incidensen av lokala reaktioner vid injektionsstället med 100 mg mepolizumab subkutant och placebo 8 % respektive 3 %. Dessa händelser var samtliga icke allvarliga, lindriga till måttliga i intensitet och flertalet försvann inom några dagar. Lokala reaktioner vid injektionsstället förekom främst i början av behandlingen och inom de första 3 injektionerna, med färre rapporter vid efterföljande injektioner. De vanligaste manifestationer som rapporterades för dessa händelser var smärta, hudrodnad, svullnad, klåda och sveda.
CRSwNP
I den placebokontrollerade studien inträffade lokala reaktioner vid injektionsstället (t.ex. hudrodnad, klåda) hos 2 % av patienterna som fick 100 mg mepolizumab jämfört med hos <1 % av patienterna som fick placebo.
KOL
I de placebokontrollerade studierna inträffade lokala reaktioner vid injektionsstället hos 2 % av patienterna som fick 100 mg mepolizumab jämfört med hos 2 % av patienterna som fick placebo. De vanligaste manifestationer som rapporterades var smärta, svullnad, klåda och erytem.
EGPA
I den placebokontrollerade studien inträffade lokala reaktioner vid injektionsstället (t.ex. smärta, hudrodnad, svullnad) hos 15 % av patienterna som fick 300 mg mepolizumab jämfört med hos 13 % av patienterna som fick placebo.
HES
I den placebokontrollerade studien inträffade lokala reaktioner vid injektionsstället (t.ex. sveda och klåda) hos 7 % av patienterna som fick 300 mg mepolizumab jämfört med 4 % av patienterna som fick placebo.
Pediatrisk population
Svår eosinofil astma
Trettiosju ungdomar (i åldern 12 till 17 år) rekryterades till fyra placebokontrollerade studier (25 behandlade med mepolizumab intravenöst eller subkutant) som pågick i 24 eller 52 veckor. Trettiosex pediatriska patienter (i åldern 6 till 11 år) fick mepolizumab subkutant i i en öppen studie under 12 veckor. Efter behandlingsavbrott i 8 veckor fick 30 av dessa patienter mepolizumab under ytterligare 52 veckor. Biverkningsprofilen var likartad den som sågs hos vuxna. Inga ytterligare biverkningar identifierades.
Den långsiktiga säkerheten för mepolizumab utvärderades dessutom hos 9 ungdomar (i åldern 12‑17 år) och 15 pediatriska patienter (i åldern 6‑11 år) som rekryterades till en öppen förlängningsstudie (201956). I denna studie fick patienterna mepolizumab subkutant under i genomsnitt 21,5 månader. Inga ytterligare biverkningar identifierades.
HES
Fyra ungdomar i åldern 12 till 17 år rekryterades till den placebokontrollerade studien 200622. En ungdom fick 300 mg mepolizumab och tre ungdomar fick placebo under 32 veckor. Alla fyra ungdomarna deltog därefter i den öppna förlängningsstudien 205203 under 20 veckor (se avsnitt Farmakodynamiska egenskaper).
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta-riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning via
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Överdosering
Engångsdoser på upp till 1500 mg administrerades intravenöst utan tecken på dosrelaterad toxicitet i en klinisk studie på patienter med eosinofil sjukdom.
Det finns ingen specifik behandling vid överdosering av mepolizumab. Vid överdosering rekommenderas att patienten ges understödjande behandling med lämplig övervakning efter behov.
Fortsatt behandling ska ges enligt kliniska indikationer eller enligt rekommendation från nationell giftinformationscentral, där sådan finns.
Farmakologiska egenskaper
Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: Medel vid obstruktiva luftvägssjukdomar, övriga systemiska medel för obstruktiva lungsjukdomar, ATC-kod: R03DX09.
Verkningsmekanism
Mepolizumab är en IL-5-antagonist (IgG1 kappa) som binder till IL-5 och hämmar dess biologiska aktivitet med nanomolär potens genom att blockera dess bindning till IL‑5R-alfakomplexet på cellytan. IL‑5 är det cytokin som spelar den viktigaste rollen för eosinofilers tillväxt och differentiering, rekrytering, aktivering och överlevnad. Hos patienter vars sjukdom drivs av typ 2-inflammation är IL-5 en viktig komponent i processerna som ligger bakom patogenesen för astma, CRSwNP, KOL, EGPA och HES. Även andra strukturella och inflammatoriska celltyper uttrycker IL-5R alfa t.ex. epitelialceller, mastceller, plasmaceller, basofiler, ILC-2-celler, T-celler, glatta muskelceller, neutrofiler och fibroblaster. Vid svår astma och CRSwNP har hämning av IL-5 förknippats med en förbättring av aspekter av luftvägsremodellering. Verkningsmekanismen i dessa celler och vid olika sjukdomar har dock inte fastställts definitivt.
Farmakodynamisk effekt
Svår eosinofil astma
Efter en dos om 100 mg administrerad subkutant var 4:e vecka i 32 veckor till patienter med svår refraktär eosinofil astma (vuxna/ungdomar) minskade eosinofilantalet i blodet från ett geometriskt medelvärde vid baslinjen på 290 till 40 celler/µl vecka 32 (N=182), en minskning med 84 % jämfört med placebo. Magnituden av minskningen av eosinofilantalet i blodet upprätthölls i patienter med svår refraktär eosinofil astma (n = 998) behandlade under, i medeltal, 2,8 år (intervall 4 veckor till 4,5 år) i öppna förlängningsstudier.
Hos barn i åldern 6 till 11 år med svår refraktär eosinofil astma som fick mepolizumab subkutant var 4:e vecka i 52 veckor hade eosinofilantalet i blodet vecka 52 minskat från ett geometriskt medelvärde vid baslinjen på 306 (n=16) till 48 celler/µl (n=15) efter 40 mg (för en vikt <40kg) och på 331 till 44 celler/µl (n=10) efter 100 mg (för en vikt ≥40 kg), en minskning från baslinjen med 85 % respektive 87 %.
Minskningar i denna storleksordning observerades hos vuxna, ungdomar och barn inom 4 veckors behandling.
CRSwNP
Efter en dos om 100 mg mepolizumab administrerat subkutant var 4:e vecka i 52 veckor till patienter med CRSwNP hade eosinofilantalet i blodet minskat från ett geometriskt medelvärde vid baslinjen på 390 (n=206) till 60 celler/µl (n=126) vecka 52, en minskning med 83 % jämfört med placebo. Minskningar i denna storleksordning observerades inom 4 veckors behandling och kvarstod under hela behandlingsperioden om 52 veckor.
KOL
Efter en dos om 100 mg mepolizumab administrerat subkutant var 4:e vecka i 52 veckor (och upp till 104 veckor) till patienter med KOL, hade antalet eosinofiler i blodet minskat från ett geometriskt medelvärde vid baslinjen på 480 (n=403) till 60 celler/µl vecka 52 (n=257) och vecka 104 (n=61), vilket motsvarar en minskning med 79 % vecka 52 och 80 % vecka 104 jämfört med placebo. Minskningar i denna storleksordning observerades inom 4 veckors behandling.
EGPA
Efter en dos om 300 mg mepolizumab administrerat subkutant till patienter med EGPA var 4:e vecka i 52 veckor hade eosinofilantalet i blodet vecka 52 minskat från ett geometriskt medelvärde vid baslinjen på 177 (n=68) till 38 celler/µl (n=64). Minskningen jämfört med placebo var 83 % och observerades inom 4 veckors behandling.
HES
Efter en dos om 300 mg mepolizumab administrerat subkutant var 4:e vecka i 32 veckor till patienter (vuxna/ungdomar) med HES observerades en minskning av antalet eosinofiler i blodet efter 2 veckors behandling. Vecka 32 hade antalet eosinofiler i blodet minskat från ett geometriskt medelvärde vid baslinjen på 1 460 (n=54) till 70 celler/µl (n=48) och en minskning av det geometriska medelvärdet på 92 % jämfört med placebo observerades. Minskningar i denna storleksordning bibehölls under ytterligare 20 veckor hos de patienter som fick fortsatt behandling med mepolizumab i den öppna förlängningsstudien.
Immunogenicitet
Svår eosinofil astma, CRSwNP, KOL, EGPA och HES
Som förväntat med tanke på de potentiellt immunogena egenskaperna hos protein- och peptidläkemedel kan patienter utveckla antikroppar mot mepolizumab efter behandling. I de placebokontrollerade studierna hade 15/260 (6 %) av vuxna och ungdomar med svår refraktär eosinofil astma som behandlades med dosen 100 mg, 6/196 (3 %) av vuxna med CRSwNP som behandlades med dosen 100 mg, 9/381 (2 %) av vuxna patienter med KOL som behandlades med dosen 100 mg, 1/68 (<2%) av vuxna med EGPA som behandlades med dosen 300 mg och 1/53 (2 %) vuxna och ungdomar med HES som behandlades med dosen 300 mg mepolizumab subkutant påvisbara antikroppar mot mepolizumab efter att ha fått minst en dos mepolizumab.
Immunogenicitetsprofilen för mepolizumab hos patienter med svår refraktär eosinofil astma (n=998) behandlade under, i medeltal, 2,8 år (intervall mellan 4 veckor till 4,5 år) eller hos patienter med HES (n=102) behandlade under 20 veckor i öppna förlängningsstudier var liknande det som observerats i de placebokontrollerade studierna. Immunogenicitetsdata samlades in från patienter med CRSwNP under 68 veckor (n=68), från patienter med KOL under 104 veckor (n=127) och från patienter med EGPA under 60 veckor (n=65).
Efter att ha fått minst en dos mepolizumab under den första korta fasen av studien hade 2/35 (6 %) barn i åldern 6 till 11 år med svår refraktär eosinofil astma behandlade med antingen 40 mg subkutant (för en vikt <40 kg) eller 100 mg subkutant (för en vikt ≥40 kg) påvisbara antikroppar mot mepolizumab. Inga barn hade påvisbara antikroppar mot mepolizumab under den långsiktiga fasen av studien.
Neutraliserande antikroppar påvisades hos en vuxen patient med svår refraktär eosinofil astma och inte hos någon patient med CRSwNP, KOL, EGPA eller HES. Antikroppar mot mepolizumab påverkade inte märkbart farmakokinetiken och farmakodynamiken för mepolizumab hos majoriteten av patienterna och det fanns inga tecken på ett samband mellan antikroppstitrar och förändring av eosinofilantalet i blodet.
Klinisk effekt
Svår eosinofil astma
Effekten av mepolizumab vid behandling av en selekterad grupp patienter med svår refraktär eosinofil astma utvärderades i 3 randomiserade, dubbelblinda, kliniska parallellgruppsstudier som pågick i 24‑52 veckor på patienter i åldern 12 år och äldre. Antingen förblev dessa patienter okontrollerade (minst två svåra exacerbationer under de senaste 12 månaderna) på sin aktuella standardbehandling som minst inkluderade högdosbehandling med inhalerade kortikosteroider (ICS) plus ytterligare underhållsbehandling(ar) eller så var de beroende av systemiska kortikosteroider. Ytterligare underhållsbehandlingar inkluderade långverkande beta2-adrenerga agonister (LABA), leukotrienmodifierare, långverkande muskarinantagonister (LAMA), teofyllin och orala kortikosteroider (OCS).
De två exacerbationsstudierna MEA1122997 och MEA115588 rekryterade totalt 1 192 patienter, 60 % kvinnor med en genomsnittlig ålder på 49 år (intervall 12‑82). Andelen patienter på underhålls-OCS var 31 % respektive 24 %. Patienterna måste ha haft minst två eller fler svåra astmaexacerbationer som krävde oral eller systemisk kortikosteroidbehandling under de senaste 12 månaderna och nedsatt lungfunktion vid baslinjen (FEV1 <80 % före bronkvidgare hos vuxna och <90 % hos ungdomar) Genomsnittligt antal exacerbationer under föregående år var 3,6 och genomsnittlig förväntad FEV1 före bronkvidgare var 60 %. Under dessa studiers gång fortsatte patienterna med sina astmaläkemedel.
Studien MEA115575, som undersökte möjligheten att minska användningen av orala kortikosteroider, rekryterade totalt 135 patienter (55 % var kvinnor, genomsnittlig ålder 50 år) som behandlades dagligen med OCS (5‑35 mg per dag) och högdos-ICS plus ett ytterligare underhållsläkemedel.
Dos-effektstudie MEA112997 (DREAM)
I MEA112997, en randomiserad, dubbelblind, placebokontrollerad, 52-veckors multicenterstudie med parallella grupper på 616 patienter med svår refraktär eosinofil astma, minskade mepolizumab signifikant kliniskt signifikanta astmaexacerbationer (definierade som försämring av astma som kräver användning av orala/systemiska kortikosteroider och/eller sjukhusinläggning och/eller besök på akutmottagning) jämfört med placebo när det administrerades i doser om 75 mg, 250 mg eller 750 mg intravenöst (se tabell 1).
Tabell 1: Frekvens av kliniskt signifikanta exacerbationer vecka 52 i intent-to-treat-populationen
| Intravenöst mepolizumab | Placebo | |||
75 mg n=153 | 250 mg n=152 | 750 mg n=156 | n=155 | |
| Exacerbationsfrekvens/år | 1,24 | 1,46 | 1,15 | 2,40 |
| Procentuell minskning | 48 % | 39 % | 52 % | |
| Frekvenskvot (95 % CI) | 0,52 (0,39, 0,69) | 0,61 (0,46, 0,81) | 0,48 (0,36, 0,64) | |
| p-värde | <0,001 | <0,001 | <0,001 | - |
Exacerbationsminskningsstudien MEA115588 (MENSA)
MEA115588 var en randomiserad, dubbelblind, placebokontrollerad multicenterstudie med parallella grupper som utvärderade effekt och säkerhet för mepolizumab som tilläggsbehandling hos 576 patienter med svår refraktär eosinofil astma definierad som ett eosinofilantal i perifert blod på minst 150 celler/μl vid behandlingsstart eller minst 300 celler/μl under de senaste 12 månaderna.
Patienterna fick 100 mg mepolizumab administrerat subkutant, 75 mg mepolizumab administrerat intravenöst eller placebo en gång var 4:e vecka under 32 veckor. Det primära effektmåttet var frekvensen av kliniskt signifikanta astmaexacerbationer. Sänkningarna för de båda mepolizumab-behandlingsarmarna var statistiskt signifikant jämfört med placebo (p<0,001). Tabell 2 visar resultaten för det primära effektmåttet och de sekundära effektmåtten för patienter behandlade med subkutant mepolizumab eller placebo.
Tabell 2: Resultat för primärt och sekundära effektmått vecka 32 i intent-to-treat-populationen (MEA115588)
Mepolizumab (100 mg s.c.) N=194 | Placebo N=191 | |
| Primärt effektmått | ||
| Frekvens av kliniskt signifikanta exacerbationer | ||
| Exacerbationsfrekvens per år | 0,83 | 1,74 |
Procentuell minskning Frekvenskvot (95 % CI) | 53 % 0,47 (0,35, 0,64) | - |
| p-värde | <0,001 | |
| Sekundära effektmått | ||
| Frekvens av exacerbationer som kräver sjukhusinläggning/besök på akutmottagning | ||
| Exacerbationsfrekvens per år | 0,08 | 0,20 |
Procentuell minskning Frekvenskvot (95 % CI) | 61 % 0,39 (0,18, 0,83) | _ |
| p-värde | 0,015 | |
| Frekvens av exacerbationer som kräver sjukhusinläggning | ||
| Exacerbationsfrekvens per år | 0,03 | 0,10 |
Procentuell minskning Frekvenskvot (95 % CI) | 69 % 0,31 (0,11, 0,91) | _ |
| p-värde | 0,034 | |
| FEV1(ml) före bronkvidgare vecka 32 | ||
| Baslinje | 1 730 (659) | 1 860 (631) |
| Genomsnittlig förändring från baslinjen (SE) | 183 (31) | 86 (31) |
| Skillnad (mepolizumab mot placebo) | 98 | |
| 95 % CI | (11, 184) | |
| p-värde | 0,028 | |
| St. George’s Respiratory Questionnaire (SGRQ) vecka 32 | ||
| Baslinje (SD) | 47,9 (19,5) | 46,9 (19,8) |
| Genomsnittlig förändring från baslinjen (SE) | -16,0 (1,1) | -9,0 (1,2) |
| Skillnad (mepolizumab mot placebo) | -7,0 | |
| 95 % CI | (-10,2, -3,8) | |
| p-värde | <0,001 | |
Minskning av exacerbationsfrekvens per eosinofilantal i blodet vid baslinjen
Tabell 3 visar resultaten av en kombinerad analys av de två exacerbationsstudierna (MEA112997 och MEA115588) per eosinofilantal i blodet vid baslinjen. Exacerbationsfrekvensen i placeboarmen ökade med stigande eosinofilantal i blodet vid baslinjen. Sänkningen av frekvensen med mepolizumab var större hos patienter med högre eosinofilantal i blodet.
Tabell 3: Kombinerad analys av frekvensen av klinisk signifikanta exacerbationer per eosinofilantal i blodet vid baslinjen hos patienter med svår refraktär eosinofil astma
Mepolizumab 75 mg i.v./100 mg s.c. N=538 | Placebo N=346 | |
| MEA112997+MEA115588 | ||
| <150 celler/μl | ||
| n | 123 | 66 |
| Exacerbationsfrekvens per år | 1,16 | 1,73 |
| Mepolizumab jämfört med placebo | ||
| Frekvenskvot (95 % CI) | 0,67 (0,46;0,98) | --- |
| 150 till <300 celler/μl | ||
| n | 139 | 86 |
| Exacerbationsfrekvens per år | 1,01 | 1,41 |
| Mepolizumab jämfört med placebo | ||
| Frekvenskvot (95 % CI) | 0,72 (0,47;1,10) | --- |
| 300 till <500 celler/μl | ||
| n | 109 | 76 |
| Exacerbationsfrekvens per år | 1,02 | 1,64 |
| Mepolizumab jämfört med placebo | ||
| Frekvenskvot (95 % CI) | 0,62 (0,41;0,93) | --- |
| ≥500 celler/μl | ||
| n | 162 | 116 |
| Exacerbationsfrekvens per år | 0,67 | 2,49 |
| Mepolizumab jämfört med placebo | ||
| Frekvenskvot (95 % CI) | 0,27 (0,19;0,37) | --- |
Studie av minskning av orala kortikosteroider MEA115575 (SIRIUS)
MEA115575 utvärderade effekten av mepolizumab 100 mg administrerat subkutant avseende minskning av behovet av underhållsbehandling med orala kortikosteroider (OCS) med bibehållen astmakontroll hos försökspersoner med svår refraktär eosinofil astma. Patienterna hade ett eosinofilantal i blod på ≥150/μl vid baslinjen eller ett eosinofilantal i perifert blod på ≥300/μl under de senaste 12 månaderna före screening. Patienterna gavs behandling med mepolizumab eller placebo en gång var 4:e vecka under behandlingsperioden. Patienterna fortsatte med sitt befintliga astmaläkemedel under studien med undantag av OCS-dosen som minskades var 4:e vecka under OCS-minskningsfasen (vecka 4‑20) så länge som astmakontrollen bibehölls.
Totalt 135 patienter rekryterades: genomsnittlig ålder var 50 år, 55 % var kvinnor, 48 % hade fått oral steroidbehandling i minst 5 år. Genomsnittlig dos vid baslinjen motsvarade cirka 13 mg prednison per dag.
Det primära effektmåttet var procentuell minskning av daglig OCS-dos (vecka 20‑24) med bibehållen astmakontroll per definierade dosminskningskategorier (se tabell 4). Fördefinierade kategorier var procentuell minskning från 90‑100 % ned till ingen minskning av prednisondosen i slutet av optimeringsfasen. Jämförelsen mellan mepolizumab och placebo var statistiskt signifikant (p=0,008).
Tabell 4: Resultat för primärt och sekundära effektmått i MEA115575
| ITT-population | ||
Mepolizumab 100 mg (subkutant) N=69 | Placebo N=66 | |
| Primärt effektmått | ||
| Procentuell minskning av OCS från baslinjen (vecka 20‑24) | ||
90‑100 % 75‑<90 % 50‑<75 % >0‑<50 % Ingen minskning av OCS/bristande astmakontroll/behandlingsavbrott | 16 (23 %) 12 (17 %) 9 (13 %) 7 (10 %) 25 (36 %) | 7 (11 %) 5 (8 %) 10 (15 %) 7 (11 %) 37 (56 %) |
| Oddskvot (95 % CI) | 2,39 (1,25, 4,56) | |
| p-värde | 0,008 | |
| Sekundära effektmått (vecka 20‑24) | ||
| Minskning av daglig OCS-dos till 0 mg/d | 10 (14 %) | 5 (8 %) |
| Oddskvot (95 % CI) | 1,67 (0,49, 5,75) | |
| p-värde | 0,414 | |
| Minskning av daglig OCS-dos till ≤5 mg/dag | 37 (54 %) | 21 (32 %) |
| Oddskvot (95 % CI) | 2,45 (1,12, 5,37) | |
| p-värde | 0,025 | |
| Medianvärde för % minskning av daglig OCS-dos från baslinjen (95 % CI) | 50,0 (20,0, 75,0) | 0,0 (-20,0, 33,3) |
| Medianskillnad (95 % CI) | -30,0 (-66,7, 0,0) | |
| p-värde | 0,007 | |
Öppna förlängningsstudier av svår refraktär eosinofil astma MEA115666 (COLOMBA), MEA115661 (COSMOS) och 201312 (COSMEX)
Den långsiktiga effektmåttsprofilen för mepolizumab hos patienter med svår refraktär eosinofil astma (n=998) behandlade under, i medeltal, 2,8 år (intervall mellan 4 veckor till 4,5 år) i öppna förlängningsstudier MEA115666, MEA115661 och 201312 var generellt överensstämmande med de 3 placebokontrollerade studierna.
Kronisk rinosinuit med näspolyper (CRSwNP)
Studie 205687 (SYNAPSE) var en randomiserad, dubbelblind, placebokontrollerad 52-veckorsstudie där man utvärderade 407 patienter från 18 års ålder med CRSwNP.
Patienterna som rekryterades till studien skulle ha nästäppa med symtompoäng enligt VAS (visuell analog skala) på >5 av 10 möjliga, totalpoäng för symtom enligt VAS på >7 av 10 möjliga, samt en poäng för endoskopiska bilaterala näspolyper på ≥5 av 8 möjliga (minimipoäng 2 i vardera näshåla). Patienterna skulle dessutom ha genomgått minst en operation av näspolyper under de senaste 10 åren.
Huvudbaslinjekaraktäristika inkluderade total NP-poäng (summan av poängen för båda näsborrarna) vid endoskopi; medelvärde (SD) 5,5 (1,29), VAS-poäng för nästäppa; medelvärde (SD) 9,0 (0,83), total VAS-poäng för symtom; medelvärde (SD) 9,1 (0,74), VAS-poäng för förlorat luktsinne; medelvärde (SD) 9,7 (0,72) och sinonasalt resultattest (SNOT-22); medelvärde (SD) 64,1 (18,32). Det geometriska medelvärdet för eosinofiltal var 390 celler/µl (95 % CI: 360; 420). I tillägg hade 27 % av patienterna aspirinförvärrad andningssjukdom (AERD) och 48 % av patienterna använt minst 1 behandlingskur orala kortikosteroider (OCS) mot CRSwNP de senaste 12 mån.
Patienterna fick en 100 mg-dos mepolizumab eller placebo, administrerad subkutant en gång var fjärde vecka, förutom bakgrundsbehandlingen med intranasala kortikosteroider.
De koprimära effektmåtten var förändring från baslinjen av total NP-poäng vid endoskopi vecka 52 samt förändring från baslinjen av genomsnittlig VAS-poäng för nästäppa under veckorna 49‑52. Det viktigaste sekundära effektmåttet var tid till första operation av näspolyper fram till vecka 52 (operation definierades som någon procedur där instrument var involverade som ledde till snitt och borttagning av vävnad [dvs. polypektomi] i näshålan). Patienterna som fick mepolizumab hade en signifikant större förbättring (minskning) av total NP-poäng vid endoskopi vecka 52 och av VAS-poäng för nästäppa under veckorna 49‑52, jämfört med placebo. Dessutom visade samtliga sekundära effektmått statistiskt signifikanta bättre resultat för mepolizumab (se tabell 5 och figur 1).
Tabell 5: Sammanfattning av resultaten för primära och sekundära effektmått (intent to treat-population)
Placebo (N=201) | Mepolizumab 100 mg s.c. (N=206) | |
| Koprimära effektmått | ||
| Total endoskopipoäng vecka 52 a | ||
| Medianpoäng vid baslinjen (min, max) | 6,0 (0;8) | 5,0 (2;8) |
| Medianförändring från baslinjen | 0,0 | -1,0 |
| p-värde b | <0,001 | |
| Skillnad i medianvärden (95 % CI) c | -0,73 (-1,11; -0,34) | |
| Förbättring ≥1 poäng, n (%) | 57 (28) | 104 (50) |
| Förbättring ≥2 poäng, n (%) | 26 (13) | 74 (36) |
| VAS-poäng för nästäppa (vecka 49 till 52)a | ||
| Medianpoäng vid baslinjen (min, max) | 9,14 (5,31; 10,00) | 9,01 (6,54; 10,00) |
| Medianförändring från baslinjen | -0,82 | -4,41 |
| p-värde b | <0,001 | |
| Skillnad i medianvärden (95 % CI) c | -3,14 (-4,09; -2,18) | |
| Förbättring ≥1 poäng, n (%) | 100 (50) | 146 (71) |
| Förbättring ≥3 poäng, n (%) | 73 (36) | 124 (60) |
| Viktigt sekundärt effektmått | ||
| Tid till första operation av näspolyper | ||
| Deltagare som opererats | 46 (23) | 18 (9) |
| Riskkvot (mepolizumab/placebo) (95 % CI) e | 0,43 (0,25; 0,76) | |
| p-värde e | 0,003 | |
| Andra sekundära effektmått | ||
| Total VAS-poäng (vecka 49-52) a | ||
| Medianpoäng vid baslinjen (min, max) | 9,20 (7,21; 10,00) | 9,12 (7,17; 10,00) |
| Medianförändring från baslinjen | -0,90 | -4,48 |
| p-värde b | <0,001 | |
| Skillnad i medianvärden (95 % CI) c | -3,18 (-4,10; -2,26) | |
| Förbättring ≥2,5 poäng (%)f | 40 | 64 |
| Totalpoäng på SNOT-22 vecka 52 a,g | ||
| n | 198 | 205 |
| Medianpoäng vid baslinjen (min, max) | 64,0 (19; 110) | 64,0 (17; 105) |
| Medianförändring från baslinjen | -14,0 | -30,0 |
| p-värde b | <0,001 | |
| Skillnad i medianvärden (95 % CI) c | -16,49 (-23,57; -9,42) | |
| Förbättring ≥28 poäng (%)f | 32 | 54 |
| Patienter som behövde systemiska kortikosteroider mot näspolyper fram till vecka 52 | ||
| Antal patienter med ≥1 behandlingskur | 74 (37) | 52 (25) |
| Oddskvot jämfört med placebo (95 % CI)h | 0,58 (0,36; 0,92) | |
| p-värdeh | 0,020 | |
| Kombinerad VAS-poäng för nasala symtom (vecka 49-52) a,i | ||
| Medianpoäng vid baslinjen (min, max) | 9,18 (6,03; 10,00) | 9,11 (4,91; 10,00) |
| Medianförändring från baslinjen | -0,89 | -3,96 |
| p-värde b | <0,001 | |
| Skillnad i medianvärden (95 % CI) c | -2,68 (-3,44; -1,91) | |
| Förbättring ≥2 poäng (%)f | 40 | 66 |
| VAS-poäng för förlorat luktsinne (vecka 49-52) a | ||
| Medianpoäng vid baslinjen (min, max) | 9,97 (6,69; 10,00) | 9,97 (0,94; 10,00) |
| Medianförändring från baslinjen | 0,00 | -0,53 |
| p-värde b | <0,001 | |
| Skillnad i medianvärden (95 % CI) c | -0,37 (-0,65; -0,08) | |
| Förbättring ≥3 poäng (%) f | 19 | 36 |
a För patienter som genomgått näsoperation eller sinuskirurgi före besöket rapporterades poäng som motsvarade deras värsta besvär före ingreppet. För patienter som avbröt studien utan att ha genomgått näsoperation eller sinuskirurgi rapporterades poäng som motsvarade deras värsta besvär innan de avbröt studien.
b Baserat på Wilcoxons ranksummetest.
c Kvantil regression med kovariat för behandlingsgrupp, geografisk region, poäng vid baslinjen och log(e) för eosinofilantal i blodet vid baslinjen.
d En förbättring med 3 VAS-poäng för nästäppa har visats vara en meningsfull förändring för en individ när det gäller denna bedömning.
e Beräknat med Cox proportionella hazardmodell med kovariat för behandlingsgrupp, geografisk region, total endoskopisk poäng vid baslinjen (central bedömning), VAS-poäng för nästäppa vid baslinjen, log(e) för eosinofilantal i blodet vid baslinjen, samt antal tidigare operationer (1, 2, >2 i ordningsföljd).
f Tröskelvärde för förbättring har visats vara en meningsfull förändring hos en individ när det gäller denna bedömning.
g Förbättring sågs på samtliga 6 domäner för symtom och inverkan av CRSwNP.
h Analys med logistisk regressionsmodell med kovariat för behandlingsgrupp, geografisk region, antal OCS-kurer för näspolyper under de senaste 12 månaderna (0, 1, >1 i ordningsföljd), total endoskopisk poäng för näspolyper vid baslinjen (central bedömning), VAS-poäng för nästäppa vid baslinjen samt log(e) för eosinofilantal i blodet vid baslinjen.
i Kombinerad VAS-poäng för nästäppa, snuva, slembildning i svalget och förlorat luktsinne.
Tid till första operation av näspolyper
Under den 52 veckor långa behandlingsperioden var sannolikheten mindre för patienterna i mepolizumabgruppen att genomgå operation av näspolyper än för patienterna i placebogruppen. Risken för att behöva operation var signifikant lägre, 57 %, för patienterna som behandlades med mepolizumab än för dem som fick placebo (riskkvot: 0,43; 95 % CI 0,25; 0,76; p=0,003).
Figur 1: Kaplan Meier-diagram över tid till första operation av näspolyper
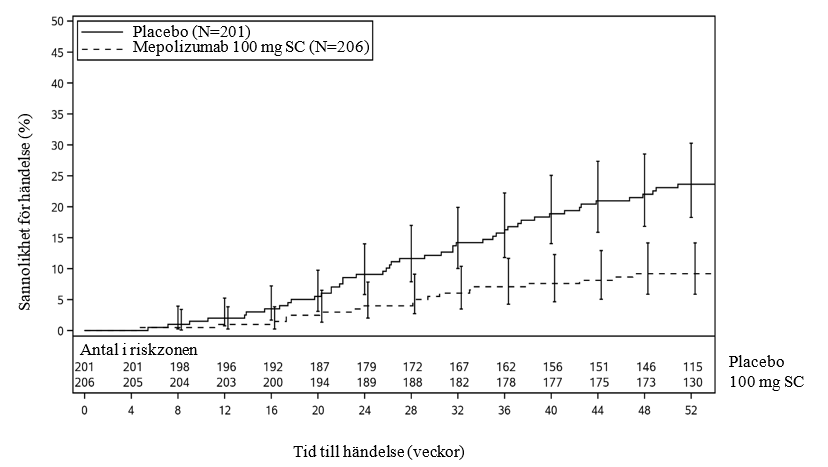
En post-hoc-analys av andelen patienter som opererades visade på en 61 % lägre sannolikhet för operation jämfört med vid behandling med placebo (OR: 0,39; 95 % CI: 0,21; 0,72; p=0,003).
CRSwNP med samtidig astma
Hos 289 (71 %) patienter med samtidig astma visade förspecificerade analyser förbättring av de koprimära effektmåtten som överensstämde med dem som sågs i den totala populationen hos de patienter som fick mepolizumab 100 mg jämfört med hos dem som fick placebo. Dessa patienter hade också en större förbättring vecka 52 jämfört med vid baslinjen av sin astmakontroll, uppmätt med hjälp av Asthma Control Questionnaire (ACQ‑5) för mepolizumab 100 mg jämfört med placebo (medianförändring [Q1, Q3] på -0,80 [-2,20; 0,00] respektive 0,00 [-1,10;, 0,20]).
Kroniskt obstruktiv lungsjukdom (KOL)
Studie 208657 (MATINEE)
Effekten av mepolizumab (100 mg s.c. var 4:e vecka) som tillägg till standardbehandling utvärderades hos 804 vuxna patienter i åldern 40 år eller äldre med KOL med eosinofil fenotyp i en 52‑104 veckor lång randomiserad, placebokontrollerad, multicenterstudie (208657, MATINEE). Patienterna måste ha ett eosinofiltal i blodet (BEC) på ≥300 celler/µl vid screening och ett BEC på ≥150 celler/µl under de senaste 12 månaderna. Samtliga patienter stod på inhalerad trippelbehandling (ICS, långverkande beta2-agonist och långverkande muskarinantagonist) under studien. Rekryterade patienter hade måttligt till mycket svår lungfunktionsnedsättning (FEV1 20‑80 % av förväntat värde efter bronkvidgare), ingen tidigare eller pågående historik med astma, och en historik med exacerbationer (minst 1 svår exacerbation som krävde sjukhusinläggning eller 2 måttliga exacerbationer som krävde behandling med systemiska kortikosteroider med eller utan antibiotika) under de senaste 12 månaderna trots regelbunden användning av inhalerade kortikosteroider samt 2 ytterligare underhållsbehandlingar i minst 3 månader före screening.
Det primära syftet med studien var att utvärdera effekten av mepolizumab på den annualiserade frekvensen av måttliga (definierade som försämring av KOL-symtom som kräver behandling med orala/systemiska kortikosteroider och/eller antibiotika) eller svåra (definierade som kräver sjukhusinläggning eller med dödligt utfall) exacerbationer. Symtom och hälsorelaterad livskvalitet utvärderades med en analys av behandlingssvar enligt CAT-(COPD Assessment Test) (definierat som en minskning med minst 2 poäng från baslinjen); enligt SGRQ (St. George’s Respiratory Questionnaire) (definierat som en minskning med minst 4 poäng från baslinjen); och enligt E-RS: COPD (Evaluating Respiratory Symptoms in Chronic Obstructive Pulmonary Disease) (definierat som en minskning med minst 2 poäng från baslinjen).
Patienternas demografi och karakteristika vid baslinjen visas i tabell 6.
Tabell 6: Demografi och karakteristika vid baslinjen i MATINEE (mITT-population)
| (N=804) | |
| Patienternas ålder (år), genomsnitt (SD) | 66 (8,0) |
| Kvinnor, n (%) | 253 (31) |
| Vita, n (%) | 673 (84) |
| Nuvarande rökare, n (%) | 222 (28) |
| Genomsnittlig rökhistorik (paket-år), genomsnitt (SD) | 43,0 (24,88) |
| Varaktighet av KOL (år), genomsnitt (SD) | 10,0 (6,28) |
| mMRC-poäng ≥2 (intervall 0‑4), n (%) | 611 (76) |
| Endast emfysema, n (%) | 252 (31) |
| Endast kronisk bronkita, n (%) | 338 (42) |
| Emfysem och kronisk bronkita, n (%) | 143 (18) |
| Måttlig lungfunktionsnedsättning: ≥50 % till <80 % av förväntad FEV1, n (%) | 349 (43) |
| Svår lungfunktionsnedsättning: ≥30 % till <50 % av förväntad FEV1, n (%) | 340 (42) |
| Mycket svår lungfunktionsnedsättning:<30 % av förväntad FEV1, n (%) | 110 (14) |
| % av förväntad FEV1 efter bronkvidgare, genomsnitt (SD) | 48,2 (15,77) |
| FEV1/FVC-kvot efter bronkvidgare, genomsnitt (SD) | 0,49 (0,124) |
| Antal måttliga eller svåra exacerbationer under föregående år, genomsnitt (SD) | 2,3 (0,94) |
| En eller flera svåra exacerbationer under föregående år, n (%) | 165 (21) |
| CAT-poäng, genomsnitt (SD) | 19,2 (6,85) |
| SGRQ-poäng, genomsnitt (SD) | 54,6 (17,80) |
| E-RS: KOL-poäng, genomsnitt (SD) | 13,05 (6,790) |
| Geometriskt genomsnitt för blodeosinofilvärdet vid screening, celler/µl (95 % CI) | 480 (470, 490) |
mITT = modifierad Intent-to-Treat, SD = standardavvikelse, mMRC = modifierad Medical Research Council, FEV1 = forcerad exspiratorisk volym under 1 sekund, FVC = forcerad vitalkapacitet, CAT = COPD Assessment Test, SGRQ = St. George’s Respiratory Questionnaire, E-RS: COPD = Evaluating Respiratory Symptoms in COPD
a KOL-typ baserad på prövarens bedömning. 544 (68 %) patienter rapporterade symtom på kronisk bronkit baserat på SGRQ.
Exacerbationer
Hos patienter som fick 100 mg mepolizumab sågs en statistiskt signifikant minskning av den annualiserade frekvensen av måttliga/svåra exacerbationer och längre tid till första måttlig/svår exacerbation jämfört med placebo och dessutom sågs en minskning av den annualiserade frekvensen av svåra exacerbationer (se tabell 7).
Tabell 7: Effektmått avseende KOL-exacerbationer i MATINEE (mITT population)
Mepolizumab 100 mg s.c. N=403 | Placebo N=401 | |
| Frekvens av måttligaa eller svårab exacerbationer | ||
| Exacerbationsfrekvens per år | 0,80 | 1.01 |
Procentuell frekvensminskning Frekvenskvot jämfört med placebo (95 % CI) | 21% 0,79 (0,66, 0,94) | |
| p-värde | 0,011 | |
| Tid till första måttliga eller svårb exacerbation | ||
| Mediantid till första exacerbation c (dagar) | 419 | 321 |
Procentuell riskminskning Hazardkvot jämfört med. placebo (95 % CI) | 23% 0,77 (0,64, 0,93) | |
| p-värde | 0,009 | |
| Frekvens av svårab exacerbationerd | ||
| Exacerbationsfrekvens per år | 0,10 | 0,15 |
Procentuell frekvensminskning Frekvenskvot jämfört med placebo (95 % CI) | 34% 0,66 (0,43, 1,01) | |
a Måttliga exacerbationer definerade som försämring av KOL-symtom som kräver behandling med orala/systemiska kortikosteroider och /eller antibiotika.
b Svåra exacerbationer definierade som kräver sjukhusinläggning eller med dödligt utfall
c Kaplan-Meier-estimat
d Del av det primära effektmåttet, analys är inte justerad för multiplicitet.
Lungfunktion
Ingen direkt effekt på lungfunktion (FEV1 före bronkvidgare) hos patienter som fick 100 mg mepolizumab s.c. jämfört med placebo sågs vid 52 veckor med en genomsnittlig förändring från baslinjen på 30,2 ml för mepolizumab och 35,6 ml för placebo (differens -5,4 ml; 95% KI: -56,2; 45,4).
Bedömning av hälsorelaterad livskvalitet
Resultaten för effektmåtten avseende symtom och hälsorelaterad livskvalitet (CAT, SGRQ och E-RS: COPD) var inte statistiskt signifikanta. Procentandelen patienter med förbättring enligt SGRQ (definierat som en minskning av minst 4 poäng från baslinjen) vecka 52 var 50 % för 100 mg mepolizumab jämfört med 46 % för placebo (oddskvot 1,17; 95 % CI: 0,87; 1,57).
Eosinofil granulomatös polyangit (EGPA)
MEA115921 var en randomiserad, dubbelblind, placebokontrollerad 52-veckorsstudie där man utvärderade 136 vuxna patienter med EGPA, med anamnes på remitterande eller refraktär sjukdom och som stod på en stabil behandling med orala kortikosteroider (OCS; ≥7,5 till ≤50 mg/dag prednisolon/prednison), med eller utan stabil behandling med immunsuppressiva (undantaget cyklofosfamid). Annan rutinmässig bakgrundsbehandling var tillåten under studien. 53 % (n=72) stod även på samtidig stabil behandling med immunsuppressiva läkemedel. Patienter med organ- eller livshotande EGPA var exkluderade från studien MEA115921. Patienterna fick antingen en 300 mg-dos mepolizumab eller placebo subkutant var 4:e vecka förutom sin bakgrundsbehandling med prednisolon/prednison, med eller utan immunsupprimerande behandling. OCS-dosen kunde trappas ner enligt beslut av prövaren.
Remission
Koprimära effektmått var total ackumulerad tid i remission, definierat som 0 poäng på Birmingham Vasculitis Activity Score (BVAS) plus en prednisolon-/prednisondos på ≤4 mg/dag, och andelen patienter i remission såväl behandlingsvecka 36 som vecka 48. BVAS=0 innebär ingen aktiv vaskulit.
I jämförelse med placebo fick patienterna som behandlades med mepolizumab 300 mg en signifikant längre ackumulerad tid i remission. Dessutom var en signifikant större andel av patienterna som fick mepolizumab 300 mg i remission såväl vecka 36 som vecka 48 (tabell 8).
I jämförelse med placebo var behandling med mepolizumab 300 mg till nytta oavsett om patienterna fick immunsupprimerande behandling eller inte i tillägg till bakgrundsbehandling med kortikosteroider, för båda de koprimära effektmåtten.
Baserat på definitionen av det sekundära effektmåttet remission, d.v.s. BVAS=0 plus prednisolon/prednison ≤7,5 mg/dag, uppnådde patienterna som fick mepolizumab 300 mg även en signifikant längre ackumulerad tid i remission (p<0,001) och en större andel av patienterna var i remission såväl vecka 36 som vecka 48 (p<0,001) jämfört med placebo.
Tabell 8: Analys av koprimära effektmått
| Antal (%) av patienterna | ||
Placebo N=68 | Mepolizumab 300 mg N=68 | |
| Ackumulerad tid i remission under 52 veckor | ||
| 0 | 55 (81) | 32 (47) |
| >0 till <12 veckor | 8 (12) | 8 (12) |
| 12 till <24 veckor | 3 (4) | 9 (13) |
| 24 till <36 veckor | 0 | 10 (15) |
| ≥36 veckor | 2 (3) | 9 (13) |
| Oddskvot (mepolizumab/placebo) | 5,91 | |
| 95 % CI | --- | 2,68; 13,03 |
| p-värde | --- | <0,001 |
| Patienter i remission vecka 36 och 48 | 2 (3) | 22 (32) |
| Oddskvot (mepolizumab/placebo) | 16,74 | |
| 95 % CI | --- | 3,61; 77,56 |
| p-värde | --- | <0,001 |
| En oddskvot på >1 innebär fördel för mepolizumab. Remission: BVAS=0 och OCS-dos ≤4 mg/dag. | ||
Recidiv
I jämförelse med placebo var tiden till första recidiv signifikant längre för patienterna som fick mepolizumab 300 mg (p<0,001). Patienterna som fick mepolizumab hade dessutom en 50-procentig minskning av annualiserad recidivfrekvens jämfört med placebo: 1,14 respektive 2,27.
Minskning av orala kortikosteroider
Försökspersoner som behandlades med mepolizumab använde en signifikant lägre genomsnittlig daglig dos av OCS under veckorna 48‑52, jämfört med försökspersonerna som fick placebo. Under veckorna 48‑52 använde 59 % respektive 44 % av patienterna som behandlades med mepolizumab en genomsnittlig daglig OCS-dos på ≤7,5 mg respektive ≤4 mg, jämfört med 33 % och 7 % i placebogruppen. I mepolizumabgruppen kunde 18 % av försökspersonerna trappa ner sin OCS-användning helt, jämfört med 3 % i placebogruppen.
Asthma Control Questionnaire – 6 (ACQ-6)
Patienterna som behandlades med mepolizumab uppvisade signifikanta förbättringar av genomsnittlig ACQ 6-poäng under veckorna 49‑52 jämfört med patienterna som fick placebo.
Hypereosinofilt syndrom (HES)
Studie 200622 var en randomiserad, dubbelblind, placebokontrollerad 32-veckorsstudie som utvärderade 108 patienter med HES i åldern ≥ 12 år. Patienterna fick 300 mg mepolizumab eller placebo administrerat subkutant en gång var 4:e vecka som tillägg till pågående behandling av HES. Behandling av HES i studie 200622 omfattade, men var inte begränsad till, OCS, immunsuppressiv, cytotoxisk behandling och andra symtomatiska behandlingar som kan tillämpas vid HES, till exempel omeprazol.
Patienterna i studien hade haft minst två skov av HES under de senaste 12 månaderna och hade ett eosinofilantal i blodet på ≥ 1 000 celler/μl vid screening. Patienter som var positiva för FIP1L1-PDGFRα-kinas uteslöts från studien.
Det primära effektmåttet i studie 200622 var andelen patienten som skov av HES under den 32 veckor långa behandlingsperioden. Ett skov av HES definierades som förvärrade kliniska tecken och symtom på HES som ledde till att behandling med OCS måste utökas, cytotoxisk eller immunsuppressiv behandling av HES måste utökas/läggas till eller aktiv blindad behandling med OCS måste sättas in på grund av förhöjt eosinofilantal i blodet (vid ≥ 2 tillfällen).
I den primära analysen jämfördes de patienter som fick ett skov av HES eller avbröt studien i behandlingsgrupperna som fick mepolizumab och placebo. Under den 32 veckor långa behandlingsperioden fick 50 % färre patienter ett skov av HES eller avbröt studien vid behandling med 300 mg mepolizumab jämfört med placebo; 28 % respektive 56 % (OR 0,28, 95 % CI: 0,12, 0,64) (se tabell 9).
Sekundära effektmått var tid till det första skovet av HES, andelen patienter som fick ett skov av HES under vecka 20 till och med vecka 32, frekvensen av skov av HES och förändring från baslinjen av svårighetsgraden av trötthet. Alla sekundära effektmått var statistiskt signifikanta och stödde det primära effektmåttet (se figur 2 och tabell 10).
Tabell 9: Resultat för primärt effektmått/analys i intent-to-treat-populationen (studie 200622)
Mepolizumab 300 mg N=54 | Placebo N=54 | |
| Andel patienter som fick ett skov av HES | ||
| Patienter med ≥ 1 skov av HES eller som avbröt studien (%) | 15 (28) | 30 (56) |
| Patienter med ≥ 1 skov av HES (%) | 14 (26) | 28 (52) |
| Patienter utan skov av HES som avbröt studien (%) | 1 (2) | 2 (4) |
| Oddskvot (95 % CI) | 0,28 (0,12, 0,64) | |
| CMH p-värde | 0,002 | |
CMH = Cochran-Mantel-Haenszel
Tid till första skov
Patienter som fick 300 mg mepolizumab uppvisade en tydlig ökning av tiden till första skov av HES jämfört med de som fick placebo. Risken för ett första skov av HES under behandlingsperioden var 66 % lägre hos de patienter som behandlades med mepolizumab jämfört med de som fick placebo (riskkvot: 0,34; 95 % CI 0,18, 0,67; p=0,002).
Figur 2: Kaplan-Meier-kurva över tid till första skov av HES
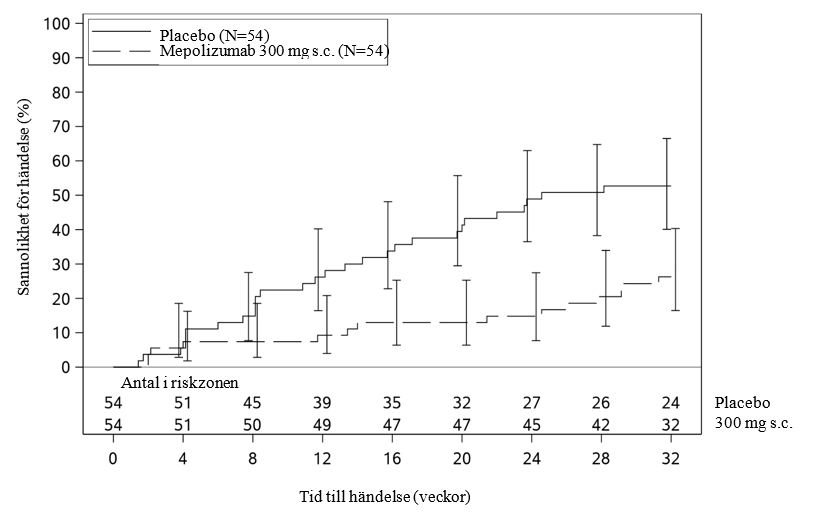
Tabell 10: Resultat för övriga sekundära effektmått i intent-to-treat-populationen (studie 200622)
Mepolizumab 300 mg N=54 | Placebo N=54 | |
| Skov av HES under vecka 20 till och med vecka 32 | ||
| Patienter med ≥ 1 skov av HES eller som avbröt studien (%) | 9 (17) | 19 (35) |
| Oddskvot (95 % CI) | 0,33 (0,13, 0,85) | |
| CMH p-värde | 0,02 | |
| Frekvens av skov av HES | ||
| Beräknad genomsnittlig frekvens/år | 0,50 | 1,46 |
| Frekvenskvot (95 % CI)a | 0,34 (0,19, 0,63) | |
| p-värde från Wilcoxons rangsummetest | 0,002 | |
| Förändring från baslinjen av svårighetsgrad av trötthet baserad på Brief Fatigue Inventory (BFI), fråga 3 (högsta nivån av trötthet under de senaste 24 timmarna) vecka 32b | ||
| Medianförändring enligt BFI fråga 3 | -0,66 | 0,32 |
| Jämförelse (mepolizumab jämfört med placebo) av p-värde från Wilcoxons ranksummetest | 0,036 | |
a frekvenskvot < 1 till fördel för mepolizumab.
b patienter för vilka data saknades ingick i sämsta observerade värde. BFI fråga 3, skala: 0 = ingen trötthet till 10 = värsta tänkbara
CMH = Cochran-Mantel-Haenszel
Öppen förlängningsstudie
Studie 205203 var en 20-veckors öppen förlängning av studie 200622. Behandlingen av HES kunde anpassas efter lokal vårdpraxis medan behandlingen med mepolizumab 300 mg var oförändrad och påbörjades vecka 4. I denna studie bibehölls behandlingseffekten av mepolizumab avseende minskning av antalet HES-skov som rapporterades under studie 200622 hos de patienter som fortsatte behandlingen med mepolizumab i studie 205203, i vilken 94% (47/50) av patienterna inte upplevde något skov.
Av de 72 patienter som behövde behandling med OCS under vecka 0 till 4 i den öppna förlängningsstudien minskade 28% av patienterna den genomsnittliga dagliga OCS-dosen med ≥50% under vecka 16 till 20.
Pediatrisk population
Svår refraktär eosinofil astma
I MEA 115588 och i den dubbelblinda placebokontrollerade studien 200862 deltog 34 ungdomar (12 till 17 år). Av dessa 34 försökspersoner fick 12 placebo, 9 fick mepolizumab 75 mg intravenöst och 13 fick 100 mg subkutant . I en kombinerad analys av dessa studier observerades en 40-procentig minskning av kliniskt signifikanta exacerbationer hos ungdomar efter behandling med mepolizumab jämfört med placebo (frekvenskvot 0,60; 95 % CI 0,17 till 2,10).
Eosinofil granulomatös polyangit (EGPA)
Inga kliniska data finns tillgängliga för barn och ungdomar i åldern 6 till 17 år.
HES
Fyra ungdomar (12 till 17 år) rekryterades till studie 200622. En ungdom fick 300 mg mepolizumab och 3 ungdomar fick placebo i 32 veckor. Den enda ungdom som behandlades med mepolizumab under 32-veckorsstudien 200622 fick inget skov av HES. Alla 4 ungdomar som fullföljde studie 200622 deltog därefter i den öppna förlängningsstudien 205203 under 20 veckor, under vilken en av de 4 ungdomarna fick ett skov av HES.
Farmakokinetiska egenskaper
Efter subkutan dosering till patienter med astma eller CRSwNP uppvisade mepolizumab en ungefärligt dosproportionell farmakokinetik i dosintervallet 12,5 mg till 250 mg. Vid subkutan administrering av 300 mg mepolizumab var den systemiska exponeringen cirka tre gånger högre jämfört med 100 mg mepolizumab. Mepolizumabs farmakokinetik var konsekvent hos patienter med astma, CRSwNP, KOL, EGPA eller HES. Efter administrering av en 100 mg subkutan engångsdos till friska försökspersoner var systemisk exponering av mepolizumab jämförbar mellan formuleringarna.
Absorption
Efter subkutan administrering till friska försökspersoner eller patienter med astma absorberades mepolizumab långsamt med en mediantid till maximal plasmakoncentration (Tmax) i intervallet 4 till 8 dagar.
Efter subkutan administrering av en engångsdos i buken, låret eller armen på friska försökspersoner var mepolizumabs biotillgänglighet 64 %, 71 % respektive 75 %. Hos patienter med astma låg den absoluta biotillgängligheten för mepolizumab administrerat subkutant i armen i intervallet 74‑80 %. Efter upprepad subkutan administrering var 4:e vecka föreligger en ungefär tvåfaldig ackumulering vid steady state.
Distribution
Efter intravenös administrering av en engångsdos till patienter med astma distribueras mepolizumab till en genomsnittlig distributionsvolym på 55 till 85 ml/kg.
Metabolism
Mepolizumab är en humaniserad IgG1 monoklonal antikropp som bryts ned av proteolytiska enzymer som finns i många kroppsvävnader och är inte begränsade till levervävnad.
Eliminering
Efter intravenös administrering av en engångsdos till patienter med astma låg genomsnittligt systemiskt clearance (CL) i intervallet 1,9 till 3,3 ml/dag/kg med en genomsnittlig terminal halveringstid på cirka 20 dagar. Efter subkutan administrering av mepolizumab låg den genomsnittliga terminala halveringstiden (t1/2) i intervallet 16 till 22 dagar. I den populationsfarmakokinetiska analysen var beräknat systemiskt clearance för mepolizumab 3,1 ml/dag/kg.
Särskilda populationer
Äldre patienter (≥65 år)
Det finns begränsade farmakokinetiska data tillgängliga för äldre patienter (≥65 år) från samtliga kliniska studier (N=90). I den populationsfarmakokinetiska analysen fanns det emellertid ingenting som tydde på att åldern har någon effekt på farmakokinetiken för mepolizumab i åldersintervallet 12 till 82 år.
Nedsatt njurfunktion
Inga formella studier har utförts för att undersöka effekten av nedsatt njurfunktion på farmakokinetiken för mepolizumab. Baserat på populationsfarmakokinetiska analyser behövs ingen dosjustering hos patienter med kreatininclearance mellan 50 och 80 ml/min. Det finns begränsade data tillgängliga för patienter med kreatininclearance <50 ml/min.
Nedsatt leverfunktion
Inga formella studier har utförts för att undersöka effekten av nedsatt leverfunktion på farmakokinetiken för mepolizumab. Eftersom mepolizumab bryts ned av proteolytiska enzymer som finns i många kroppsvävnader och inte är begränsade till levervävnad, är det inte sannolikt att förändrad leverfunktion har någon effekt på elimineringen av mepolizumab.
Pediatrisk population
Svår refraktär eosinofil astma och HES
Det finns begränsade farmakokinetiska data tillgängliga för den pediatriska populationen (59 patienter med eosinofil esofagit, 55 patienter med svår refraktär eosinofil astma och en patient med HES). Farmakokinetiken för intravenöst mepolizumab utvärderades i en populationsfarmakokinetisk analys i en pediatrisk studie som utfördes på patienter i åldern 2‑17 år med eosinofil esofagit. Pediatrisk farmakokinetik kunde i stort sett predikteras från vuxna efter att hänsyn tagits till kroppsvikten. Mepolizumabs farmakokinetik hos tonåriga patienter med svår refraktär eosinofil astma eller HES som deltog i fas 3-studierna överensstämde med den för vuxna (se avsnitt Dosering och administreringssätt).
Pediatrisk farmakokinetik efter subkutan administrering till patienter i åldern 6 till 11 år med svår refraktär eosinofil astma undersöktes i en öppen icke-kontrollerad studie som pågick i 12 veckor. Farmakokinetiken hos barn överensstämde i stort sett med den hos vuxna och ungdomar efter att hänsyn tagits till kroppsvikt och biotillgänglighet. Den absoluta subkutana biotillgängligheten förefaller vara fullständig jämfört med den på 76 % som observeras hos vuxna och ungdomar. Exponeringen efter subkutan administrering av antingen 40 mg (för en vikt <40 kg) eller 100 mg (för en vikt ≥40 kg) var 1,32 respektive 1,97 gånger den som observerades hos vuxna vid 100 mg.
Undersökning av en doseringsregim med 40 mg subkutant var 4:e vecka till barn i åldern 6 till 11 år över ett viktintervall på 15–70 kg med farmakokinetisk modellering och simulering predikterar att exponeringen med denna doseringsregim i genomsnitt skulle ligga inom 38 % av den för vuxna vid 100 mg. Denna doseringsregim anses acceptabel på grund av mepolizumabs breda terapeutiska index.
EGPA
Farmakokinetiken för mepolizumab hos barn (6 till 17 år) med EGPA har beräknats med hjälp av modellering och simulering baserat på farmakokinetiken vid andra eosinofila sjukdomar, och förväntas vara densamma som hos barn med svår eosinofil astma. Vid den rekommenderade dosen till barn 6 till 11 år som väger 15‑70 kg förutspås exponeringen ligga på i genomsnitt 26 % av exponeringen hos vuxna som får 300 mg.
Prekliniska säkerhetsuppgifter
Eftersom mepolizumab är en monoklonal antikropp har inga gentoxicitets- eller karcinogenicitetsstudier utförts.
Toxikologi och/eller farmakologi hos djur
Gängse studier avseende säkerhetsfarmakologi och allmäntoxicitet på apor visade inte några särskilda risker för människa. Intravenös och subkutan administrering till apor var förenad med minskningar av eosinofilantalet i perifert blod och lungor utan några toxikologiska fynd.
Eosinofiler anses delta i immunsystemsvaret på vissa parasitinfektioner. Studier som utförts på mus behandlade med anti‑IL‑5‑antikroppar eller med genetisk brist på IL‑5 eller eosinofiler har inte visat nedsatt förmåga att övervinna parasitinfektioner. Betydelsen av dessa fynd för människan är okänd.
Fertilitet
Ingen nedsättning av fertiliteten observerades i en studie av fertilitets- och allmän reproduktionstoxicitet på mus utförd med en analog antikropp som hämmar IL‑5 hos mus. Denna studie inkluderade inte någon utvärdering av kullarna eller funktionell bedömning av avkomman.
Graviditet
Hos apor hade mepolizumab ingen effekt på dräktighet eller på embryonal/fetal eller postnatal utveckling (inklusive immunfunktionen) hos avkomman. Inga undersökningar av förekomsten av invärtes missbildningar eller skelettmissbildningar utfördes. Data för cynomolgusapa visar att mepolizumab passerade placenta. Koncentrationerna av mepolizumab var cirka 1,2‑2,4 gånger högre hos ungarna än hos moderdjuren under flera månader post partum och påverkade inte ungarnas immunsystem.
Farmaceutiska uppgifter
Förteckning över hjälpämnen
Sackaros
Dibasiskt natriumfosfatheptahydrat
Citronsyramonohydrat
Polysorbat 80 (E 433)
Dinatriumedetat
Vatten för injektionsvätskor
Inkompatibiliteter
Då blandbarhetsstudier saknas får detta läkemedel inte blandas med andra läkemedel.
Hållbarhet
3 år.
Särskilda förvaringsanvisningar
Förvaras i kylskåp (2°C-8°C).
Får inte frysas.
Förvaras i originalkartongen. Ljuskänsligt.
Om nödvändigt så kan förfylld(a) injektionspenna(or) och förfylld(a) spruta(or) tas ut från kylen och förvaras i oöppnad förpackning i upp till 7 dagar i rumstemperatur (högst 30°C) och i skydd mot ljus. Förpackningen måste kasseras om den har varit utanför kylen i mer än 7 dagar.
Förfylld(a) injektionspenna(or) eller förfylld(a) spruta(or) måste administreras inom 8 timmar efter öppnandet av förpackningen. Förpackningen måste kasseras om administrering inte har skett inom 8 timmar.
Förpackningstyp och innehåll
Markkinoilla olevat pakkaukset
Resepti
NUCALA injektioneste, liuos, esitäytetty kynä
100 mg (L:ei) 1 kpl (1 ml, kiinteä neula) (1117,73 €)
NUCALA injektioneste, liuos, esitäytetty ruisku
40 mg (L:ei) 1 kpl (0,4 ml, kiinteä neula, turvasuojus) (465,23 €)
100 mg (L:ei) 1 kpl (1 ml, kiinteä neula, turvasuojus) (1117,73 €)
PF-selosteen tieto
Nucala 100 mg injektionsvätska, lösning, i förfylld injektionspenna
1 ml lösning i en spruta av typ 1-glas med fast nål (rostfritt stål) i en förfylld injektionspenna.
Förpackningsstorlekar:
1 förfylld injektionspenna
Flerpack innehållande 3 (3 förpackningar om 1) förfyllda injektionspennor.
Flerpack innehållande 9 (9 förpackningar om 1) förfyllda injektionspennor.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Nucala 100 mg injektionsvätska, lösning, i förfylld spruta
1 ml lösning i en spruta av typ 1-glas med fast nål (rostfritt stål) och passivt nålskydd.
Förpackningsstorlekar:
1 förfylld spruta
Flerpack innehållande 3 (3 förpackningar om 1) förfyllda sprutor.
Flerpack innehållande 9 (9 förpackningar om 1) förfyllda sprutor.
Nucala 40 mg injektionsvätska, lösning, i förfylld spruta
0,4 ml lösning i en spruta av typ 1-glas med fast nål (rostfritt stål) och passivt nålskydd.
Förpackningsstorlekar:
1 förfylld spruta
Flerpack innehållande 3 (3 förpackningar om 1) förfyllda sprutor.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Läkemedlets utseende:
En klar till opaliserande, färglös till svagt gul till svagt brun lösning, med ett pH-värde på 6,0‑6,6 och en osmolalitet på 415‑615 mOsm/kg.
Särskilda anvisningar för destruktion och övrig hantering
Före administrering måste lösningen inspekteras visuellt. Lösningen måste vara klar till opaliserande, färglös till svagt gul till svagt brun lösning. Om lösningen är grumlig, missfärgad eller innehåller partiklar får lösningen inte användas.
Låt den förfyllda injektionspennan eller förfyllda sprutan(orna) anta rumtemperatur i minst 30 minuter före injektion av Nucala efter att injektionspennan eller sprutan(orna) tagits ut från kylen.
Utförliga instruktioner för subkutan administrering med Nucala förfylld injektionspenna eller förfylld(a) spruta(or) ges i slutet av bipacksedeln (se steg-för-steg-anvisningarna).
Destruktion
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.
Ersättning
NUCALA injektioneste, liuos, esitäytetty kynä
100 mg 1 kpl
NUCALA injektioneste, liuos, esitäytetty ruisku
40 mg 1 kpl
100 mg 1 kpl
- Alempi erityiskorvaus (65 %). Mepolitsumabi: Vaikean eosinofiilisen astman hoito aikuisille ja 6 vuotta täyttäneille lapsille ja nuorille erityisin edellytyksin (297).
- Rajoitettu peruskorvaus lääkärin lausunnolla (40 %). Mepolitsumabi: Aikuisten ja 6 vuotta täyttäneiden lasten ja nuorten vaikean eosinofiilisen astman sekä aikuisten vaikean kroonisen polypoottisen rinosinuiitin hoito erityisin edellytyksin (3028).
Atc-kod
R03DX09
Datum för översyn av produktresumén
04.02.2026
Yhteystiedot
Porkkalankatu 20 A
00180 Helsinki
010 303 030
www.glaxosmithkline.fi

 GLAXOSMITHKLINE OY
GLAXOSMITHKLINE OY