LUMIVELA tabletti, kalvopäällysteinen 150/20 mikrog
 Lääketurva
Lääketurva
Riskienminimointimateriaalit
Potilas
Kysymyksiä ja vastauksia yhdistelmäehkäisyvalmisteista
Terveydenhuollon ammattilainen
Tärkeää tietoa yhdistelmäehkäisyvalmisteesta ja veritulppariskistä
Tarkistuslista yhdistelmäehkäisyvalmisteiden määrääjille
Yksilöllisten veritulppariskitekijöiden arviointiin, keskustelun tueksi ja sopivimman valmisteen valitsemiseksi
Vaikuttavat aineet ja niiden määrät
21 valkoista kalvopäällysteistä tablettia (vaikuttavaa tablettia):
Jokainen kalvopäällysteinen tabletti sisältää:
Desogestreeli 150 mikrogrammaa
Etinyyliestradioli 20 mikrogrammaa
Apuaineet, joiden vaikutus tunnetaan: laktoosimonohydraatti 55 mg, soijaöljy (enintään 0,026 mg).
7 vihreää kalvopäällysteistä lumetablettia (vaikuttavia aineita sisältämätöntä tablettia):
Tabletti ei sisällä vaikuttavia aineita.
Apuaine, jonka vaikutus tunnetaan: laktoosimonohydraatti 55 mg.
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Tabletti, kalvopäällysteinen.
Kliiniset tiedot
Käyttöaiheet
Raskauden ehkäisy.
Lumivela-valmisteen määräämistä koskevassa päätöksessä on otettava huomioon valmisteen käyttäjän nykyiset riskitekijät, erityisesti laskimotromboembolian (VTE) riskitekijät, ja millainen Lumivela-käytön VTE:n riski on verrattuna muiden yhdistelmäehkäisyvalmisteiden riskeihin (ks. kohdat Vasta-aiheet ja Varoitukset ja käyttöön liittyvät varotoimet).
Annostus ja antotapa
Miten Lumivela-tabletteja otetaan
Tabletit otetaan pakkaukseen merkityssä järjestyksessä päivittäin suunnilleen samaan aikaan, tarvittaessa pienen nestemäärän kanssa. Tablettien otossa ei pidetä taukoa. Yksi tabletti otetaan kerran vuorokaudessa 28 perättäisen päivän ajan. Uusi läpipainopakkaus aloitetaan edellisen läpipainopakkauksen viimeisen tabletin ottopäivää seuraavana päivänä. Tyhjennysvuoto alkaa yleensä 2–3 päivän kuluttua lumetablettien (viimeinen rivi) ottamisen aloittamisesta ja saattaa kestää seuraavan läpipainopakkauksen aloittamiseen saakka.
Lumivela-tablettien käytön aloittaminen
- Ei edeltävää hormonaalista ehkäisyä (kuluneen kuukauden aikana)
Tablettien käyttö aloitetaan luonnollisen kuukautiskierron ensimmäisenä päivänä (kuukautisten ensimmäisenä päivänä). Tablettien käyttö voidaan aloittaa myös 2.–5. vuotopäivänä, mutta tällöin on käytettävä lisäehkäisyä 7 ensimmäisen tablettipäivän ajan.
- Vaihto Lumivela-valmisteeseen toisesta yhdistelmäehkäisyvalmisteesta (yhdistelmäehkäisytabletista, emätinrenkaasta tai ehkäisylaastarista)
Lumivela-tablettien käyttö aloitetaan mieluiten aiemman yhdistelmäehkäisyvalmisteen viimeisen vaikuttavan tabletin (vaikuttavia aineita sisältävän tabletin) ottoa seuraavana päivänä, mutta viimeistään aiemman yhdistelmäehkäisyvalmisteen tavanomaista tablettitaukoa (tai viimeisen lumetabletin ottoa) seuraavana päivänä.
Kun yhdistelmäehkäisyvalmisteena on käytetty emätinrengasta tai ehkäisylaastaria, Lumivela-tablettien ottaminen aloitetaan mieluiten poistamispäivänä, mutta viimeistään sinä päivänä, jona seuraava emätinrengas tai ehkäisylaastari olisi asetettu paikoilleen. Hormonittoman jakson kesto ei saa missään tapauksessa ylittää aiemmalle ehkäisymenetelmälle suositeltua hormonittoman jakson kestoa.
Jos aiempaa yhdistelmäehkäisyvalmistetta on käytetty jatkuvasti ja oikein edeltävien 7 vuorokauden ajan ja on kohtuullisen varmaa, ettei käyttäjä ole raskaana, aiemmasta yhdistelmäehkäisyvalmisteesta voidaan siirtyä Lumivela-valmisteeseen minä tahansa kuukautiskierron päivänä.
Kaikkia kuvattuja ehkäisymenetelmiä (ehkäisyrengas, ehkäisylaastari) ei välttämättä ole saatavilla kaikissa EU‑maissa.
- Vaihto Lumivela-valmisteeseen pelkkää progestiinia sisältävästä ehkäisyvalmisteesta (minipilleri, injektio, implantaatti) tai progestiinia vapauttavasta kohdunsisäisestä ehkäisimestä (IUS)
Minipillereistä voidaan siirtyä käyttämään Lumivela-tabletteja koska tahansa (implantaatista tai IUS:stä sen poistopäivänä ja injektiosta seuraavana suunniteltuna injektiopäivänä), mutta kaikissa näissä tapauksissa on käytettävä lisäehkäisyä 7 ensimmäisen tablettipäivän ajan.
- Käyttö ensimmäisellä raskauskolmanneksella tapahtuneen raskauden keskeytymisen jälkeen
Tablettien käyttö voidaan aloittaa heti. Muita ehkäisymenetelmiä ei tällöin tarvita.
- Käyttö synnytyksen tai toisella raskauskolmanneksella tapahtuneen raskauden keskeytymisen jälkeen
Tablettien käyttö aloitetaan 21–28 vuorokautta synnytyksen tai toisella raskauskolmanneksella tapahtuneen raskauden keskeytymisen jälkeen.
Jos tablettien käyttö aloitetaan myöhemmin, 7 ensimmäisen tablettipäivän aikana on käytettävä lisäehkäisyä. Jos nainen on jo ollut yhdynnässä, raskauden mahdollisuus on suljettava pois tai yhdistelmäehkäisytablettien käyttö on aloitettava vasta seuraavien kuukautisten alkamisen jälkeen.
Imetys, ks. kohta Raskaus ja imetys.
Tablettien unohtaminen
Läpipainopakkauksen viimeisellä rivillä olevien lumetablettien unohtaminen voidaan jättää huomioimatta. Ne tulee kuitenkin hävittää, jotta lumetablettijakso ei pitkity tarpeettomasti.
Seuraavat ohjeet koskevat ainoastaan unohdettuja vaikuttavia tabletteja (läpipainopakkauksen 1.–3. rivillä):
Jos unohtunut tabletti otetaan 12 tunnin kuluessa, valmisteen ehkäisyteho ei ole heikentynyt.
Unohtunut tabletti tulee ottaa heti muistettaessa ja seuraavat tabletit tavanomaiseen aikaan.
Jos tabletin unohtamisesta on kulunut yli 12 tuntia, valmisteen ehkäisyteho saattaa olla heikentynyt.
Seuraavat kaksi perussääntöä pätevät tapauksissa, joissa tablettien ottaminen on unohtunut:
- Tablettien ottamista ei saa koskaan keskeyttää yli 7 peräkkäisen päivän ajaksi.
- Hypotalamus-aivolisäke-munasarja-akseli riittävän suppression saavuttaminen edellyttää tablettien ottamista yhtäjaksoisesti 7 päivän ajan.
Täten voidaan antaa seuraavat käytännön ohjeet:
- Viikko 1
Viimeinen unohtunut tabletti otetaan heti muistettaessa, vaikka tällöin olisikin otettava kaksi tablettia samalla kertaa. Tämän jälkeen seuraavat tabletit otetaan tavanomaiseen aikaan. Lisäksi seuraavien 7 päivän ajan on käytettävä lisäehkäisyä. Raskaus on mahdollinen, jos nainen on ollut yhdynnässä edeltävien 7 päivän aikana. Raskauden mahdollisuus on sitä suurempi, mitä useampi tabletti on unohtunut ja mitä lähempänä lumetablettijaksoa unohtuminen on tapahtunut.
- Viikko 2
Viimeinen unohtunut tabletti otetaan heti muistettaessa, vaikka tällöin olisikin otettava kaksi tablettia samalla kertaa. Tämän jälkeen seuraavat tabletit otetaan tavanomaiseen aikaan. Jos tabletteja on otettu ohjeen mukaan 7 päivän ajan ennen ensimmäistä unohtunutta tablettia, lisäehkäisyä ei tarvita. Jos näin ei ole tai jos käyttäjä on unohtanut useamman kuin yhden tabletin, häntä on neuvottava käyttämään lisäehkäisyä seuraavien 7 päivän ajan.
- Viikko 3
Ehkäisytehon heikkenemisen riski on suuri, koska 7 päivän lumetablettijakso on lähellä. Ehkäisytehon heikkeneminen voidaan kuitenkin estää muuttamalla tablettien ottamisen aikataulua. Jompaakumpaa alla olevista ohjeista noudattamalla lisäehkäisyä ei tarvita, jos tabletteja on otettu säännöllisesti ohjeen mukaan 7 päivän ajan ennen ensimmäistä unohtunutta tablettia. Jos tabletteja ei ole otettu ohjeiden mukaan, käyttäjän on toimittava alla olevan ensimmäisen ohjeen mukaan ja käytettävä lisäehkäisyä seuraavien 7 päivän ajan.
- Viimeinen unohtunut tabletti otetaan heti muistettaessa, vaikka tällöin olisikin otettava kaksi tablettia samalla kertaa. Tämän jälkeen tablettien ottoa jatketaan tavanomaisen aikataulun mukaisesti, kunnes kaikki vaikuttavat tabletit on otettu. Viimeisen rivin 7 tablettia (lumetabletit) on hävitettävä. Seuraava pakkaus aloitetaan heti, kun edellisen pakkauksen vaikuttavat tabletit on otettu. Tyhjennysvuotoa ei todennäköisesti tule ennen uuden pakkauksen vaikuttavien tablettien loppumista, mutta tablettien käyttöpäivinä voi esiintyä tiputtelu- tai läpäisyvuotoa.
- Vaikuttavien tablettien ottaminen käytössä olleesta pakkauksesta voidaan myös lopettaa. Tällöin voidaan ottaa tabletteja viimeiseltä riviltä (lumetabletteja) enintään 7 päivän ajan, mukaan lukien päivät, jolloin vaikuttavat tabletit on unohdettu ottaa. Sen jälkeen aloitetaan tablettien ottaminen uudesta läpipainopakkauksesta.
Jos nainen on unohtanut ottaa tabletteja eikä tyhjennysvuotoa tule lumetablettijakson aikana, raskauden mahdollisuus on otettava huomioon.
Ohjeet ruuansulatuselimistön häiriöiden varalle
Jos esiintyy vaikeita ruuansulatuselimistön häiriöitä (esim. oksentelua tai ripulia), imeytyminen saattaa olla epätäydellistä ja lisäehkäisyä on käytettävä. Jos käyttäjä oksentaa 3–4 tunnin kuluessa vaikuttavan tabletin ottamisesta, noudatetaan tabletin unohtamista koskevia ohjeita kohdasta Annostus ja antotapa ”Tablettien unohtaminen”. Jos käyttäjä ei halua muuttaa tavanomaista tablettien ottoaikataulua, hänen on otettava tarvittava ylimääräinen tabletti tai tabletit toisesta pakkauksesta.
Kuukautisten siirtäminen myöhemmäksi tai alkamispäivän muuttaminen pysyvästi
Kuukautisten siirtäminen ei ole tämän valmisteen käyttöaihe. Poikkeustapauksissa kuukautisia voidaan siirtää myöhemmäksi aloittamalla uusi Lumivela-läpipainopakkaus heti edellisen loputtua ilman lumetablettien ottamista. Kuukautisia voidaan siirtää niin pitkälle kuin halutaan, kuitenkin enintään toisen pakkauksen vaikuttavien tablettien loppumiseen saakka. Toisen pakkauksen käytön aikana voi esiintyä läpäisy- tai tiputteluvuotoa. Lumivela-valmisteen käyttöä jatketaan normaalisti lumetablettijakson jälkeen.
Jos käyttäjä haluaa muuttaa kuukautisten alkamispäivää nykyisestä joksikin toiseksi viikonpäiväksi, häntä voidaan neuvoa lyhentämään seuraavaa lumetablettijaksoa niin monella päivällä kuin hän haluaa. Mitä lyhyempi jakso, sitä suurempi riski, että tyhjennysvuotoa ei tule ja että toisen pakkauksen käytön aikana esiintyy läpäisy- tai tiputteluvuotoa (verrattavissa kuukautisia siirrettäessä esiintyviin).
Pediatriset potilaat
Lumivela-valmisteen turvallisuutta ja tehoa alle 18 vuoden ikäisten nuorten hoidossa ei ole vielä tutkittu.
Vasta-aiheet
Yhdistelmäehkäisyvalmistetta ei pidä käyttää seuraavien tilojen yhteydessä. Jos jokin näistä tiloista ilmenee ensimmäistä kertaa yhdistelmäehkäisytablettien käytön aikana, valmisteen käyttö on lopetettava heti.
-
Laskimotromboembolia (VTE) tai sen riski
- laskimotromboembolia – tällä hetkellä esiintyvä VTE (potilas antikoagulanttilääkityksellä) tai anamneesissa VTE (esim. syvä laskimotromboosi [SLT] tai keuhkoembolia)
- tiedossa oleva perinnöllinen tai hankittu laskimotromboembolia-alttius, kuten APC-resistenssi (mukaan lukien Faktori V Leiden), antitrombiini III:n puutos, C-proteiinin puutos, S-proteiinin puutos
- suuri leikkaus ja siihen liittyvä pitkittynyt immobilisaatio (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet)
- useiden riskitekijöiden aiheuttama suuri laskimotromboembolian riski (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet)
-
Valtimotromboembolia tai sen riski
- valtimotromboembolia – tällä hetkellä esiintyvä tai aiemmin esiintynyt valtimotromboembolia (esim. sydäninfarkti) tai sitä ennakoiva tila (esim. angina pectoris)
- aivoverisuonisairaus – tällä hetkellä esiintyvä tai aiemmin esiintynyt aivohalvaus tai sitä ennakoiva tila (esim. ohimenevä aivoverenkiertohäiriö, TIA)
- tiedossa oleva perinnöllinen tai hankittu valtimotromboembolia-alttius, kuten hyperhomokystinemia ja fosfolipidivasta-aineet (kardiolipiinivasta-aineet, lupusantikoagulantti)
- anamneesissa migreeni, johon liittyy fokaalisia neurologisia oireita
- monista riskitekijöistä (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet) tai yhden vakavan riskitekijän esiintymisestä johtuva suuri valtimotromboemboliariski. Näitä riskitekijöitä voivat olla:
- diabetes, jossa esiintyy verisuonioireita
- vaikea hypertensio
- vaikea dyslipoproteinemia.
- Nykyinen tai aiemmin ilmennyt haimatulehdus, jos siihen liittyy/liittyi vaikea hypertriglyseridemia.
- Nykyinen tai aiemmin ilmennyt vaikea maksasairaus, niin kauan kuin maksa-arvot eivät ole palautuneet normaaleiksi.
- Nykyinen tai aiemmin ilmennyt hyvän- tai pahanlaatuinen maksakasvain.
- Todetut tai epäillyt sukupuolihormoneista riippuvaiset kasvaimet (esim. sukupuolielinten tai rintojen maligniteetit).
- Kohdun limakalvon hyperplasia.
- Vaginaverenvuoto, jonka syytä ei ole selvitetty.
- Yliherkkyys vaikuttaville aineille tai kohdassa Apuaineet mainituille apuaineille.
- Allergia maapähkinälle tai soijalle.
- Lumivela on vasta-aiheinen käytettäessä samanaikaisesti ombitasviirin, paritapreviirin ja ritonaviirin yhdistelmää ja dasabuviiria, glekapreviirin ja pibrentasviirin yhdistelmää tai sofosbuviirin, velpatasviirin ja voksilapreviirin yhdistelmää sisältäviä lääkkeitä (ks. kohta Yhteisvaikutukset).
Varoitukset ja käyttöön liittyvät varotoimet
Varoitukset
Lumivela-valmisteen soveltuvuudesta on keskusteltava naisen kanssa, jos hänellä esiintyy mikä tahansa alla mainituista tiloista tai riskitekijöistä.
Jos jokin näistä tiloista tai riskitekijöistä pahenee tai ilmenee ensimmäisen kerran, käyttäjää on kehotettava ottamaan yhteys lääkäriin, joka päättää, pitääkö Lumivela-valmisteen käyttö keskeyttää.
Verenkiertohäiriöt
Laskimotromboembolian (VTE) riski
Minkä tahansa yhdistelmäehkäisyvalmisteen käyttö lisää laskimotromboembolian (VTE) riskiä verrattuna siihen, että tällaista valmistetta ei käytetä lainkaan. Levonorgestreelia, norgestimaattia tai noretisteronia sisältäviin valmisteisiin liittyy pienin VTE:n riski. Tämä riski voi olla jopa kaksinkertainen muilla valmisteilla, kuten esimerkiksi Lumivela-valmisteella. Päätöksen muun kuin VTE:n riskiltään pienimmän valmisteen käyttämisestä saa tehdä vain sen jälkeen, kun ehkäisyä harkitsevan naisen kanssa on keskusteltu. Keskustelussa on varmistettava, että hän ymmärtää Lumivela-valmisteen käyttöön liittyvän VTE:n riskin, miten hänen nykyiset riskitekijänsä vaikuttavat tähän riskiin ja että hänen VTE:n riskinsä on suurimmillaan ensimmäisen vuoden aikana, jona hän käyttää yhdistelmäehkäisyvalmistetta ensimmäistä kertaa elämässään. On myös jonkin verran näyttöä siitä, että riski suurenee, kun yhdistelmäehkäisyvalmisteen käyttö aloitetaan uudelleen vähintään 4 viikon tauon jälkeen.
Noin kahdelle naiselle 10 000:sta, jotka eivät käytä yhdistelmäehkäisyvalmistetta eivätkä ole raskaana, kehittyy VTE yhden vuoden aikana. Yksittäisellä naisella tämä riski voi kuitenkin olla suurempi riippuen hänen omista, taustalla vaikuttavista riskitekijöistään (ks. jäljempänä).
Arviolta 9–12 naiselle1 10 000:sta, jotka käyttävät desogestreelia sisältävää yhdistelmäehkäisyvalmistetta, kehittyy VTE yhden vuoden aikana. Levonorgestreelia sisältävää yhdistelmäehkäisyvalmistetta käyttävillä naisilla vastaava luku on 62.
1 Ilmaantuvuus arvioitiin kaikista epidemiologisista tutkimustuloksista vertaamalla eri valmisteiden suhteellisia riskejä levonorgestreelia sisältäviin yhdistelmäehkäisyvalmisteisiin.
2 Vaihteluvälin 5–7 keskipiste 10 000 naisvuotta kohden, mikä perustuu levonorgestreelia sisältävien yhdistelmäehkäisyvalmisteiden käytön suhteelliseen riskiin verrattuna käyttämättömyyteen, jolloin riski on noin 2,3–3,6.
Molemmissa tapauksissa VTE-tapausten määrä vuotta kohti on pienempi kuin määrä, joka on odotettavissa raskauden aikana tai synnytyksen jälkeisenä aikana.
VTE saattaa aiheuttaa kuoleman 1–2 %:ssa tapauksista.
VTE-tapausten määrä 10 000 naista kohti yhden vuoden aikana
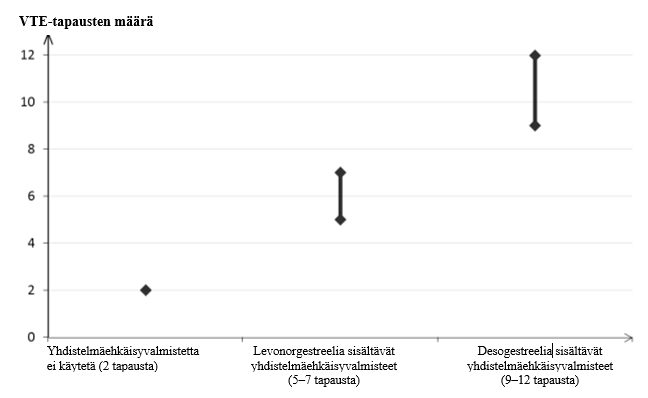
Yhdistelmäehkäisyvalmisteiden käyttäjillä tromboosia on erittäin harvoin raportoitu esiintyneen muissa verisuonissa (esim. maksan, suoliliepeen, munuaisten tai verkkokalvon laskimoissa ja valtimoissa).
Laskimotromboembolian riskitekijät
Yhdistelmäehkäisyvalmisteiden käyttäjillä esiintyvien laskimotromboembolisten komplikaatioiden riski voi suurentua huomattavasti, jos naisella on muita riskitekijöitä, erityisesti jos riskitekijöitä on useita (ks. taulukko).
Lumivela-valmiste on vasta-aiheinen naisella, jolla on useita riskitekijöitä, jotka aiheuttavat suuren VTE:n riskin (ks. kohta Vasta-aiheet). Jos naisella on useampia kuin yksi riskitekijä, nämä yhdessä voivat muodostaa yksittäisten tekijöiden summaa suuremman riskin – tässä tapauksessa VTE:n kokonaisriski on otettava huomioon. Jos hyöty-riski-suhteen katsotaan olevan negatiivinen, yhdistelmäehkäisyvalmistetta ei pidä määrätä (ks. kohta Vasta-aiheet).
Taulukko: Laskimotromboembolian (VTE) riskitekijät
| Riskitekijä | Kommentti |
| Ylipaino (painoindeksi yli 30 kg/m2) | Riski suurenee huomattavasti painoindeksin noustessa. Huomioitava erityisesti silloin, jos muita riskitekijöitä on myös olemassa. |
Pitkittynyt immobilisaatio, suuri leikkaus, kaikki jalkojen tai lantion alueen leikkaukset, neurokirurgia tai merkittävä trauma Huomioitavaa: väliaikainen immobilisaatio, mukaan lukien > 4 tunnin lentomatka, voi myös olla VTE:n riskitekijä, erityisesti naisilla, joilla on myös muita riskitekijöitä | Näissä tilanteissa on suositeltavaa lopettaa laastarin/tabletin/renkaan käyttö (elektiivisen leikkauksen kohdalla vähintään neljä viikkoa etukäteen), eikä sitä pidä jatkaa ennen kuin käyttäjä on ollut kaksi viikkoa täysin liikuntakykyinen. Jotain muuta raskaudenehkäisymenetelmää on käytettävä ei-toivotun raskauden ehkäisemiseksi. Antitromboottista hoitoa on harkittava, ellei Lumivela-valmisteen käyttöä ole lopetettu etukäteen. |
| Positiivinen sukuanamneesi (tämänhetkinen tai aikaisempi VTE sisaruksella tai vanhemmalla, etenkin suhteellisen nuorella iällä, esim. alle 50-vuotiaana) | Jos perinnöllistä alttiutta epäillään, potilas on syytä ohjata erikoislääkärin tutkimuksiin ennen kuin minkään yhdistelmäehkäisyvalmisteen käytöstä päätetään. |
| Muut laskimotromboemboliaan liitetyt sairaudet | Syöpä, systeeminen lupus erythematosus, hemolyyttis-ureeminen oireyhtymä, krooninen tulehduksellinen suolistosairaus (Crohnin tauti tai haavainen koliitti) ja sirppisoluanemia |
| Ikääntyminen | Erityisesti yli 35 vuoden ikä |
Suonikohjujen ja pinnallisen laskimontukkotulehduksen mahdollisesta yhteydestä laskimotromboosin alkamiseen tai etenemiseen ei ole yksimielisyyttä.
Tromboembolian suurempi riski raskauden ja erityisesti synnytyksen jälkeisten noin 6 viikon aikana on otettava huomioon (ks. lisätiedot kohdasta Raskaus ja imetys).
Laskimotromboembolian oireet (syvä laskimotromboosi ja keuhkoembolia)
Jos oireita ilmaantuu, naisia on neuvottava hakeutumaan välittömästi lääkärin hoitoon ja kertomaan, että he käyttävät yhdistelmäehkäisyvalmistetta.
Syvän laskimotromboosin (SLT) oireita voivat olla:
- toisen jalan ja/tai jalkaterän turvotus tai turvotus jalan laskimon kohdalla
- jalan kipu tai arkuus, joka saattaa tuntua vain seistessä tai kävellessä
- jalan lisääntynyt lämmöntunne, jalan ihon värin muutos tai punoitus.
Keuhkoembolian oireita voivat olla:
- äkillisesti alkanut, selittämätön hengenahdistus tai nopeutunut hengitys
- äkillinen yskä, johon saattaa liittyä veriysköksiä
- pistävä rintakipu
- vaikea pyörrytys tai huimaus
- nopea tai epäsäännöllinen sydämen syke.
Jotkut näistä oireista (esim. hengenahdistus, yskä) ovat epäspesifisiä, ja ne voidaan tulkita virheellisesti yleisluontoisemmiksi tai vähemmän vaikeiksi tapahtumiksi (esim. hengitystieinfektioksi).
Muita verisuonitukoksen merkkejä voivat olla mm.: äkillinen kipu, turvotus ja sinertävä värimuutos raajassa.
Jos tukos tulee silmään, oireena voi olla esim. kivuton näön hämärtyminen, joka voi edetä näön menetykseen. Joskus näön menetys voi tapahtua lähes välittömästi.
Valtimotromboembolian (ATE) riski
Epidemiologisissa tutkimuksissa on osoitettu, että yhdistelmäehkäisyvalmisteiden käyttöön liittyy suurentunut valtimotromboembolian (sydäninfarkti) tai aivoverisuonitapahtuman (esim. aivojen ohimenevä verenkiertohäiriö [TIA], aivohalvaus) riski. Valtimotromboemboliset tapahtumat voivat johtaa kuolemaan.
Valtimotromboembolian (ATE) riskitekijät
Valtimotromboembolisten komplikaatioiden tai aivoverisuonitapahtuman riski yhdistelmäehkäisyvalmisteen käyttäjillä on korkeampi niillä naisilla, joilla on riskitekijöitä (ks. taulukko). Lumivela-valmiste on vasta-aiheinen, jos naisella on joko yksi vakava tai useampia ATE:n riskitekijöitä, mikä aiheuttaa suuren valtimotromboemboliariskin (ks. kohta Vasta-aiheet). Jos naisella on useampi kuin yksi riskitekijä, nämä yhdessä voivat muodostaa yksittäisten tekijöiden summaa suuremman riskin – tässä tapauksessa kokonaisriski on otettava huomioon. Jos hyöty-riski-suhteen katsotaan olevan negatiivinen, yhdistelmäehkäisyvalmistetta ei pidä määrätä (ks. kohta Vasta-aiheet).
Taulukko: Valtimotromboembolian (ATE) riskitekijät
| Riskitekijä | Kommentti |
| Ikääntyminen | Erityisesti yli 35 vuoden ikä |
| Tupakointi | Yhdistelmäehkäisyvalmistetta käyttäviä naisia on neuvottava olemaan tupakoimatta. Yli 35-vuotiaita, tupakoimista jatkavia naisia on vakavasti kehotettava käyttämään jotakin muuta ehkäisymenetelmää. |
| Korkea verenpaine | |
| Ylipaino (painoindeksi yli 30 kg/m2) | Riski kasvaa huomattavasti painoindeksin noustessa. Erityisen tärkeää naisilla, joilla on muitakin riskitekijöitä. |
| Positiivinen sukuanamneesi (tämänhetkinen tai aikaisempi valtimotromboembolia sisaruksella tai vanhemmalla, etenkin suhteellisen nuorella iällä, alle 50-vuotiaana). | Jos perinnöllistä alttiutta epäillään, potilas on syytä ohjata erikoislääkärin tutkimuksiin ennen kuin minkään yhdistelmäehkäisyvalmisteen käytöstä päätetään. |
| Migreeni | Migreenin esiintymistiheyden kasvu tai vaikeusasteen lisääntyminen (mikä saattaa olla aivoverisuonitapahtumaa ennakoiva oire) yhdistelmäehkäisyvalmisteen käytön aikana voi olla syy yhdistelmäehkäisyvalmisteen käytön välittömään keskeyttämiseen. |
| Muut verisuoniston haittatapahtumiin liitetyt sairaudet | Diabetes, hyperhomokystinemia, sydämen läppävika ja eteisvärinä, dyslipoproteinemia ja systeeminen lupus erythematosus (SLE). |
Valtimotromboembolian (ATE) oireet
Jos oireita ilmaantuu, naisia on neuvottava hakeutumaan välittömästi lääkärin hoitoon ja kertomaan, että he käyttävät yhdistelmäehkäisyvalmistetta.
Aivoverisuonitapahtuman oireita voivat olla:
- kasvojen, käsivarren tai jalan äkillinen tunnottomuus tai heikkous (varsinkin vain yhdellä puolella vartaloa esiintyvä)
- äkillinen kävelyn vaikeutuminen, huimaus, tasapainon tai koordinaation menetys
- äkillinen sekavuus, puhe- tai ymmärtämisvaikeudet
- äkillinen näön heikentyminen yhdessä tai molemmissa silmissä
- äkillinen, voimakas tai pitkittynyt päänsärky, jonka syytä ei tiedetä
- tajunnan menetys tai pyörtyminen, johon saattaa liittyä kouristuskohtaus.
Ohimenevät oireet viittaavat siihen, että tapahtuma on ohimenevä aivoverenkiertohäiriö (TIA).
Sydäninfarktin oireita voivat olla:
- kipu, epämiellyttävä tunne, paineen tunne, painon tunne, puristuksen tai täysinäisyyden tunne rinnassa, käsivarressa tai rintalastan takana
- selkään, leukaan, kurkkuun, käsivarteen ja/tai vatsaan säteilevä epämiellyttävä tunne
- täysinäisyyden, ruoansulatushäiriöiden tai tukehtumisen tunne
- hikoilu, pahoinvointi, oksentelu tai huimaus
- erittäin voimakas heikkouden tunne, ahdistuneisuus tai hengenahdistus
- nopea tai epäsäännöllinen sydämen syke.
Kasvaimet
- Epidemiologiset tutkimukset ovat osoittaneet, että pitkäaikainen (> 5 vuoden) ehkäisytablettien käyttö lisää kohdunkaulan syövän riskiä potilailla, joilla on ihmisen papilloomavirus (HPV) ‑infektio. Kuitenkin on vielä epäselvää, missä määrin tähän havaintoon vaikuttavat sekoittavat tekijät (esim. erot sukupuolikumppanien määrissä tai estemenetelmien käytössä).
- Meta-analyysi 54 epidemiologisesta tutkimuksesta osoitti, että yhdistelmäehkäisytablettien tämänhetkisten käyttäjien suhteellinen rintasyöpäriski on hieman suurentunut (suhteellinen riskikerroin 1,24) ja että tämä suurentunut riski häviää vähitellen 10 vuoden kuluessa yhdistelmäehkäisytablettien käytön loputtua. Koska rintasyöpä on harvinainen alle 40-vuotiailla naisilla, tällä hetkellä yhdistelmäehkäisytabletteja käyttävillä tai hiljattain niitä käyttäneillä havaittu rintasyöpädiagnoosien ylimäärä on pieni verrattuna rintasyövän kokonaisriskiin. Nämä tutkimukset eivät anna näyttöä kausaalisuhteesta. Havaittu riskin suureneminen voi johtua rintasyövän varhaisesta toteamisesta yhdistelmäehkäisytablettien käyttäjillä, yhdistelmäehkäisytablettien biologisista vaikutuksista tai molemmista. Yhdistelmäehkäisytabletteja joskus käyttäneillä naisilla diagnosoidut rintasyövät ovat tendenssinomaisesti varhaisemmassa vaiheessa kuin ehkäisytabletteja käyttämättömillä diagnosoidut rintasyövät.
- Yhdistelmäehkäisytablettien käyttäjillä on raportoitu harvoin hyvänlaatuisia ja vielä harvemmin pahanlaatuisia maksakasvaimia. Yksittäistapauksissa nämä kasvaimet ovat aiheuttaneet hengenvaarallisia vatsaontelon sisäisiä verenvuotoja. Erotusdiagnostisesti maksakasvaimen mahdollisuutta tulisi harkita, kun yhdistelmäehkäisytablettien käyttäjällä on voimakasta ylävatsakipua, suurentunut maksa tai merkkejä vatsaontelonsisäisestä verenvuodosta.
Muut tilat
- Hypertriglyseridemia tai sen esiintyminen suvussa voi suurentaa haimatulehduksen riskiä yhdistelmäehkäisytablettien käyttäjillä.
- Vähäistä verenpaineen kohoamista on raportoitu monilla yhdistelmäehkäisytablettien käyttäjillä, mutta kliinisesti merkittävä verenpaineen kohoaminen on harvinaista. Yhdistelmäehkäisytablettien käytön ja kliinisen hypertension välistä yhteyttä ei ole vahvistettu. Jos verenpaine kuitenkin kohoaa pitkäkestoisesti ja kliinisesti merkittävästi yhdistelmäehkäisytablettien käytön aikana, lääkärin tulisi keskeyttää valmisteen käyttö ja hoitaa hypertensiota. Valmisteen käyttöä voidaan jatkaa, jos verenpainelääkityksellä saadaan aikaan normotensio.
- Seuraavia sairaustiloja tai niiden pahenemista on raportoitu sekä raskauden että yhdistelmäehkäisytablettien käytön yhteydessä, mutta niiden yhteydestä yhdistelmäehkäisytablettien käyttöön ei ole vakuuttavaa näyttöä: kolestaasiin liittyvä keltaisuus ja/tai kutina, sappikivimuodostus, porfyria, SLE, hemolyyttis-ureeminen oireyhtymä, Sydenhamin korea, herpes gestationis, otoskleroosiin liittyvä kuulonalenema.
- Estrogeenien käyttö saattaa aiheuttaa tai pahentaa perinnöllisen ja hankinnaisen angioedeeman oireita.
- Yhdistelmäehkäisytablettien käytön keskeyttäminen saattaa olla tarpeen akuuteissa tai kroonisissa maksan toimintahäiriöissä, kunnes maksafunktioarvot ovat normalisoituneet. Yhdistelmäehkäisytablettien käyttö on lopetettava, jos raskausaikana ensi kertaa ilmennyt tai aiempaan sukupuolihormonien käyttöön liittynyt kolestaattinen keltaisuus ja/tai kolestaasiin liittyvä kutina uusiutuu.
- Vaikka yhdistelmäehkäisytabletit voivat vaikuttaa perifeeriseen insuliiniresistenssiin tai glukoosinsietoon, yhdistelmäehkäisytabletteja (< 0,05 mg etinyyliestradiolia sisältäviä) käyttävien naisten diabeteshoidon muuttamistarpeesta ei ole näyttöä. Yhdistelmäehkäisytabletteja käyttäviä diabeetikkoja tulee kuitenkin seurata huolellisesti.
- Yhdistelmäehkäisytablettien käytön yhteydessä on esiintynyt Crohnin tautia ja haavaista koliittia.
- Maksaläiskiä voi joskus esiintyä, erityisesti jos niitä on esiintynyt raskausaikana. Maksaläiskiin taipuvaisten naisten tulisi välttää aurinkoa ja ultraviolettisäteilyaltistusta yhdistelmäehkäisytablettien käytön aikana.
- Masentunut mieliala ja masennus ovat tunnettuja hormonaalisten ehkäisyvalmisteiden käyttöön liittyviä haittavaikutuksia (ks. kohta Haittavaikutukset). Masennus voi olla vakavaa, ja se on itsetuhoisen käyttäytymisen ja itsemurhan tunnettu riskitekijä. Naisia on kehotettava ottamaan yhteyttä lääkäriinsä, jos heillä esiintyy mielialan muutoksia ja masennuksen oireita, myös pian hoidon aloittamisen jälkeen.
Tämä lääkevalmiste sisältää 55 mg laktoosia per valkoinen tabletti ja 55 mg laktoosia per vihreä tabletti. Laktoositonta ruokavaliota noudattavien potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, täydellinen laktaasinpuutos tai glukoosi-galaktoosi-imeytymishäiriö, ei tule käyttää tätä lääkettä.
Edellä mainitut tiedot on otettava huomioon, kun päätetään ehkäisymenetelmästä tai -menetelmistä.
Lääkärintarkastus
Ennen Lumivela-valmisteen käytön aloittamista tai uudelleen aloittamista potilaan sairaushistoria on selvitettävä täydellisesti (mukaan lukien sukuanamneesi), ja raskaus on suljettava pois. Naisen verenpaine on mitattava ja hänelle on tehtävä lääkärintarkastus ottaen huomioon vasta-aiheet (ks. kohta Vasta-aiheet) ja varoitukset (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet). On tärkeää kiinnittää naisen huomiota laskimo- ja valtimoveritulppia koskeviin tietoihin, kuten Lumivela-valmisteen käyttöön liittyvään riskiin verrattuna muihin yhdistelmäehkäisyvalmisteisiin, laskimo- ja valtimoveritulppien oireisiin, tiedossa oleviin riskitekijöihin sekä siihen, mitä tehdä, jos epäilee veritulppaa.
Naista on myös neuvottava lukemaan pakkausseloste huolellisesti ja noudattamaan siinä annettuja ohjeita. Tarkastuskäyntien tiheyden ja luonteen pitää perustua vakiintuneisiin hoitosuosituksiin, ja ne on toteutettava kunkin naisen kliinisten tarpeiden mukaisesti.
Naisia on varoitettava siitä, että hormonaaliset ehkäisymenetelmät eivät suojaa HIV-infektiolta (AIDS) tai muilta sukupuoliteitse tarttuvilta taudeilta.
Tehon heikkeneminen
Lumivela-valmisteen tehoa voivat heikentää tablettien unohtaminen (ks. kohta Annostus ja antotapa, Tablettien unohtaminen), ruoansulatuskanavan häiriöt (ks. kohta Annostus ja antotapa, Ohjeet ruuansulatuselimistön häiriöiden varalle) tai se, että samanaikaisesti käytetään lääkevalmisteita, jotka pienentävät etinyyliestradiolin ja/tai etonogestreelin (desogestreelin aktiivisen metaboliitin) pitoisuuksia plasmassa (ks. kohta Yhteisvaikutukset).
Mäkikuismaa (Hypericum perforatum) sisältäviä kasvirohdosvalmisteita ei pidä käyttää samanaikaisesti Lumivela-valmisteen kanssa, sillä ne voivat aiheuttaa vaikuttavien aineiden plasmapitoisuuksien pienenemistä ja Lumivela-valmisteen tehon heikentymistä (ks. kohta Yhteisvaikutukset).
Syklikontrollin heikentyminen
Kaikki yhdistelmäehkäisyvalmisteet voivat aiheuttaa epäsäännöllisiä vuotoja (tiputtelu- tai läpäisyvuotoa) etenkin ensimmäisten käyttökuukausien aikana. Siksi epäsäännöllistä vuotoa kannattaa alkaa tutkia vasta noin kolme kiertoa kestävän sopeutumisvaiheen jälkeen.
Jos vuotohäiriöt jatkuvat tai niitä ilmaantuu kiertojen oltua aiemmin säännölliset, ei-hormonaaliset syyt on syytä ottaa huomioon. Asianmukaiset diagnostiset toimenpiteet (mahdollisesti kohdun kaavinta) ovat indisoituja maligniteetin tai raskauden poissulkemiseksi.
Joskus lumetablettijakson aikana ei tule tyhjennysvuotoa. Jos yhdistelmäehkäisytabletteja on käytetty kohdassa Annostus ja antotapa annettujen ohjeiden mukaan, nainen ei todennäköisesti ole raskaana. Jos valmistetta ei kuitenkaan ole käytetty ohjeiden mukaan ennen tyhjennysvuodon ensimmäistä poisjääntiä tai jos jo kaksi tyhjennysvuotoa on jäänyt tulematta, raskauden mahdollisuus on suljettava pois ennen yhdistelmäehkäisytablettien käytön jatkamista.
Yhteisvaikutukset
Yhteisvaikutukset
Huom.: Samanaikaisesti käytettävien lääkevalmisteiden valmisteyhteenvetoihin tulee tutustua mahdollisten yhteisvaikutusten selvittämiseksi.
Farmakodynaamiset yhteisvaikutukset
Kun kliinisissä tutkimuksissa hoidettiin hepatiitti C -virusinfektiota (HCV) ombitasviirin, paritapreviirin ja ritonaviirin yhdistelmällä ja dasabuviirilla ribaviriinin kanssa tai ilman, transaminaasiarvon (ALAT) kohoamista yli 5 x ULN (viitealueen yläraja) esiintyi merkitsevästi useammin naisilla, jotka käyttivät etinyyliestradiolia sisältävää valmistetta, kuten yhdistelmäehkäisyvalmistetta. Myös glekapreviirin ja pibrentasviirin yhdistelmää tai sofosbuviirin, velpatasviirin ja voksilapreviirin yhdistelmää käyttävillä potilailla ALAT-arvojen kohoamista havaittiin etinyyliestradiolia sisältävää valmistetta (kuten yhdistelmäehkäisyvalmistetta) käyttävillä naisilla (ks. kohta Vasta-aiheet). Tästä syystä Lumivela-käyttäjien on vaihdettava muuhun ehkäisymenetelmään (esim. pelkkää progestiinia sisältävään ehkäisyyn tai ei-hormonaalisiin menetelmiin) ennen kyseisten yhdistelmähoitojen aloittamista. Lumivela-valmisteen käyttö voidaan aloittaa uudelleen 2 viikon kuluttua näiden yhdistelmähoitojen lopettamisesta.
Muiden lääkkeiden vaikutukset Lumivela-valmisteeseen
Yhteisvaikutuksia saattaa ilmetä mikrosomaalisia entsyymejä (sytokromi P450 ‑entsyymejä [CYP]) indusoivien lääke- tai rohdosvalmisteiden kanssa, jotka voivat lisätä sukupuolihormonien puhdistumaa, mikä voi johtaa läpäisyvuotoihin ja/tai raskauteen.
Hoito
Entsyymi-induktio voidaan havaita jo muutaman hoitopäivän jälkeen. Maksimaalinen entsyymi-induktio ilmenee yleensä muutaman viikon kuluessa. Lääkehoidon lopettamisen jälkeen entsyymi-induktio voi jatkua noin neljän viikon ajan.
Lyhytaikainen hoito
Entsyymejä indusoivia lääke- tai rohdosvalmisteita saavien naisten tulee väliaikaisesti käyttää jotakin estemenetelmää tai valita yhdistelmäehkäisytablettien sijasta jokin muu ehkäisykeino. Estemenetelmää on käytettävä samanaikaisen lääkehoidon ajan sekä lisäksi 28 päivää hoidon lopettamisen jälkeen.
Jos lääkitys jatkuu vielä yhdistelmäehkäisytabletti-läpipainopakkauksen vaikuttavien tablettien loppumisen jälkeen, lumetabletit on hävitettävä ja siirryttävä heti seuraavaan läpipainopakkaukseen.
Pitkäaikainen hoito
Naisille, jotka saavat pitkäaikaista hoitoa entsyymejä indusoivilla lääkevalmisteilla, on harkittava sellaista toista luotettavaa, ei‑hormonaalista ehkäisymenetelmää, johon entsyymejä indusoivilla lääkevalmisteilla ei ole vaikutusta.
Kirjallisuudessa on ilmoitettu seuraavia yhteisvaikutuksia:
Lumivela-valmisteen puhdistumaa lisäävät aineet (entsyymi-induktio heikentää yhdistelmäehkäisytablettien tehoa), esimerkiksi:
Fenytoiini, fenobarbitaali, primidoni, bosentaani, karbamatsepiini, rifampisiini, jotkin HIV‑proteaasinestäjät (esim. ritonaviiri) ja ei‑nukleosidirakenteiset käänteiskopioijaentsyymin estäjät (esim. nevirapiini, efavirentsi) sekä mahdollisesti myös felbamaatti, griseofulviini, okskarbatsepiini, topiramaatti, rifabutiini ja mäkikuismaa (Hypericum perforatum) sisältävät kasvirohdosvalmisteet.
Aineet, joilla on vaihtelevia vaikutuksia Lumivela-valmisteen puhdistumaan
Yhtäaikaisesti hormonaalisten ehkäisyvalmisteiden kanssa käytettynä monet HIV-proteaasinestäjiä (esim. nelfinaviiri) ja ei-nukleosidirakenteisia käänteiskopioijaentsyymin estäjiä (esim. nevirapiini) sisältävät lääkeyhdistelmät ja/tai hepatiitti C ‑viruksen (HCV:n) estäjiä (esim. bosepreviiri, telapreviiri) sisältävät yhdistelmät voivat suurentaa tai pienentää progestageenien, myös etonogestreelin, tai estrogeenien pitoisuutta plasmassa. Näiden muutosten kokonaisvaikutus voi joissakin tapauksissa olla kliinisesti merkittävä.
Tämän vuoksi samanaikaisen HIV/HCV-lääkityksen valmisteyhteenveto pitää tarkastaa potentiaalisten yhteisvaikutusten varalta ja niiden suhteen annettujen lisäohjeiden osalta. Naisen, joka käyttää proteaasinestäjää tai ei-nukleosidirakenteista käänteiskopioijaentsyymin estäjää, tulee käyttää lisäehkäisyä, jos yhteisvaikutuksen mahdollisuutta epäillään.
Lumivela-valmisteen puhdistumaa pienentävät lääkeaineet (entsyymitoiminnan estäjät)
Entsyymitoiminnan estäjien kanssa mahdollisesti esiintyvien yhteisvaikutusten kliinistä merkitystä ei tunneta.
Estrogeenien tai progestageenien (myös etonogestreelin) pitoisuudet seerumissa saattavat suurentua, jos samanaikaisesti käytetään vahvoja (esim. ketokonatsoli, itrakonatsoli, klaritromysiini) tai keskivahvoja (esim. flukonatsoli, diltiatseemi, erytromysiini) CYP3A4:n estäjiä.
Etorikoksibin 60 mg:n vuorokausiannosten on todettu suurentavan plasman etinyyliestradiolipitoisuutta 1,4‑kertaiseksi ja 120 mg:n vuorokausiannosten 1,6‑kertaiseksi, kun etorikoksibia käytetään yhdessä 0,035 mg etinyyliestradiolia sisältävän yhdistelmäehkäisyvalmisteen kanssa.
Lumivela-valmisteen vaikutus muihin lääkevalmisteisiin
Ehkäisytabletit saattavat vaikuttaa muiden lääkkeiden metaboliaan, jolloin niiden pitoisuus plasmassa ja kudoksessa voi joko nousta (esim. siklosporiini) tai laskea (esim. lamotrigiini).
Kliiniset tiedot viittaavat siihen, että etinyyliestradioli estää CYP1A2:n substraattien puhdistumaa, mikä johtaa niiden pitoisuuden vähäiseen (esim. teofylliini) tai kohtalaiseen (esim. titsanidiini) suurenemiseen plasmassa.
Laboratorioarvot
Steroidiehkäisyn käyttö voi vaikuttaa eräisiin laboratorioarvoihin, kuten maksan, kilpirauhasen, lisämunuaisen ja munuaisten toimintakokeiden biokemiallisiin parametreihin, (kantaja)proteiinien (esimerkiksi kortikosteroideja sitovan globuliinin ja lipidi/lipoproteiinifraktioiden) pitoisuuksiin plasmassa, hiilihydraattiaineenvaihdunnan parametreihin ja veren hyytymis- ja fibrinolyysiparametreihin. Muutokset pysyvät yleensä normaalialueella.
Raskaus ja imetys
Raskaus
Lumivela-tabletteja ei ole tarkoitettu käytettäväksi raskauden aikana. Jos Lumivela-tabletteja käyttävä nainen tulee raskaaksi, tablettien käyttö on lopetettava välittömästi. Useimpien epidemiologisten tutkimusten mukaan synnynnäisten kehityshäiriöiden riski ei kuitenkaan ole suurentunut ennen raskautta yhdistelmäehkäisytabletteja käyttäneiden naisten lapsilla, kuten ei myöskään teratogeenisten vaikutusten riski silloin, kun yhdistelmäehkäisytabletteja on käytetty raskauden varhaisvaiheessa.
Kun Lumivela-valmisteen käyttö aloitetaan uudelleen, on huomioitava, että laskimotromboembolian riski on suurentunut synnytyksen jälkeisenä aikana (ks. kohdat Annostus ja antotapa ja Varoitukset ja käyttöön liittyvät varotoimet).
Imetys
Yhdistelmäehkäisytabletit voivat vaikuttaa imetykseen, sillä ne voivat vähentää rintamaidon määrää ja muuttaa sen koostumusta. Siksi yhdistelmäehkäisytabletteja tulisi suosituksen mukaan yleensä käyttää vasta, kun lapsi on vieroitettu rintamaidosta. Pieniä määriä kontraseptiivisiä steroideja ja/tai niiden metaboliitteja voi erittyä rintamaitoon. Haitallisista vaikutuksista imeväisterveyteen ei kuitenkaan ole näyttöä.
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Vaikutusta ajokykyyn tai koneidenkäyttökykyyn ei ole havaittu.
Haittavaikutukset
Tiettyjen haittavaikutusten kuvaus
Yhdistelmäehkäisyvalmisteita käyttävillä naisilla on havaittu valtimoiden ja laskimoiden tromboottisten ja tromboembolisten tapahtumien lisääntynyt riski. Näitä tapahtumia ovat mm. sydäninfarkti, aivohalvaus, ohimenevät aivoverenkiertohäiriöt (TIA), laskimoveritulppa ja keuhkoembolia. Tapahtumia kuvataan tarkemmin kohdassa Varoitukset ja käyttöön liittyvät varotoimet.
Kuten kaikkien yhdistelmäehkäisytablettien käytön yhteydessä, tämänkin valmisteen käytön yhteydessä voi esiintyä kuukautisvuodon muutoksia etenkin ensimmäisten käyttökuukausien aikana. Muutokset voivat koskea esimerkiksi vuototiheyttä (poisjääminen, harventuminen, tihentyminen tai jatkuvaksi muuttuminen), vuodon runsautta (väheneminen tai lisääntyminen) tai vuodon kestoa.
Lumivela-valmisteen käyttäjillä tai yleisesti yhdistelmäehkäisytablettien käyttäjillä ilmoitetut mahdollisesti käyttöön liittyvät haittavaikutukset on lueteltu seuraavassa taulukossa1. Kaikki haittavaikutukset on lueteltu niiden elinjärjestelmäluokituksen ja yleisyyden mukaan. Yleisyysluokittelu on seuraava: yleiset (≥ 1/100), melko harvinaiset (≥ 1/1 000, < 1/100), harvinaiset (< 1/1 000) ja yleisyys tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin).
| Elinjärjestelmä | Yleiset
| Melko harvinaiset
| Harvinaiset
| Yleisyys tuntematon |
|---|---|---|---|---|
| Immuunijärjestelmä | Yliherkkyysreaktiot | Perinnöllisen ja hankinnaisen angioedeeman oireiden paheneminen | ||
| Aineenvaihdunta ja ravitsemus | Nesteretentio | |||
| Psyykkiset häiriöt | Masentuneisuus Mielialan vaihtelut | Libidon heikkeneminen | Libidon voimistuminen | |
| Hermosto | Päänsärky | Migreeni | ||
| Silmät | Piilolinssien huono sieto | |||
| Verisuonisto | Valtimotromboembolia (VTE) Laskimotromboembolia (ATE) | |||
| Ruoansulatuselimistö | Pahoinvointi Vatsakipu | Oksentelu, ripuli | ||
| Iho ja ihonalainen kudos | Ihottuma Urtikaria | Erythema nodosum Erythema multiforme
| ||
| Sukupuolielimet ja rinnat | Rintojen aristus Rintojen kipu | Rintojen suureneminen
| Vuoto emättimestä Vuoto rinnoista | |
| Tutkimukset | Painon nousu | Painon lasku |
1 Luettelossa esitetään yleisin asianmukainen haittavaikutusta kuvaava MedDRA‑termi. Synonyymejä tai samankaltaisia tiloja ei luetella, mutta nekin on aiheellista ottaa huomioon.
Joitakin yhdistelmäehkäisytablettien käyttäjien ilmoittamia haittavaikutuksia on kuvattu tarkemmin kohdassa Varoitukset ja käyttöön liittyvät varotoimet. Näitä ovat mm. hypertensio, hormoniriippuvaiset kasvaimet (esim. maksa- tai rintakasvaimet) ja maksaläiskät.
Yhteisvaikutukset
Muiden lääkevalmisteiden (entsyymitoiminnan indusorien) ja ehkäisytablettien yhteisvaikutukset voivat aiheuttaa läpäisyvuotoa ja/tai ehkäisytehon heikkenemistä (ks. kohta Yhteisvaikutukset).
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haitta-tasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Yliannostuksen ei ole raportoitu aiheuttavan vakavia haittavaikutuksia.
Mahdollisia yliannostusoireita ovat pahoinvointi, oksentelu ja nuorilla tytöillä vähäinen verenvuoto emättimestä. Antidoottia ei ole, ja jatkohoito on oireenmukaista.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: progestageenit ja estrogeenit, kiinteät yhdistelmävalmisteet, ATC-koodi: G03AA09
Yhdistelmäehkäisyvalmisteiden ehkäisyteho perustuu monen eri tekijän yhteisvaikutukseen. Näistä tärkeimpiä ovat ovulaation estyminen ja kohdunkaulan limakalvon koostumuksen muuttuminen. Raskauden ehkäisyn lisäksi yhdistelmäehkäisyvalmisteiden käyttöön liittyy monia muitakin hyötyjä, jotka, kuten haitatkin (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Haittavaikutukset), on tärkeää ottaa huomioon sopivaa ehkäisymenetelmää valittaessa. Kuukautiskierto on säännöllisempi, ja kuukautiskivut ovat yleensä lievemmät ja kuukautisvuoto vähäisempää. Tämän vuoksi raudanpuuteanemian ilmaantuvuus on pienempi. Lisäksi on viitteitä siitä, että suuriannoksisten (50 mikrog etinyyliestradiolia) yhdistelmäehkäisytablettien käyttö olisi yhteydessä seuraavien tilojen pienempään todennäköisyyteen: fibrokystiset rintakasvaimet, munasarjakystat, sisäsynnytintulehdus, kohdunulkoinen raskaus, kohdun limakalvon syöpä ja munasarjasyöpä. Vielä ei ole varmistettu, koskeeko tämä myös pieniannoksisten yhdistelmäehkäisytablettien käyttöä.
Pediatriset potilaat
Kliinisiä tietoja turvallisuudesta ja tehosta alle 18-vuotiailla nuorilla ei ole saatavilla.
Farmakokinetiikka
Desogestreeli
Imeytyminen
Lumivela-valmisteen peroraalisen annon jälkeen desogestreeli imeytyy nopeasti ja muuttuu etonogestreeliksi. Huippupitoisuus plasmassa, n. 2 ng/ml, saavutetaan noin 1,5 tunnin kuluttua annoksen ottamisesta. 3-keto-desogestreelin absoluuttinen biologinen hyötyosuus on 62–81 %.
Jakautuminen
Etonogestreeli sitoutuu seerumin albumiiniin ja sukupuolihormoneja sitovaan globuliiniin (SHBG). Vain 2–4 % lääkkeen kokonaispitoisuudesta seerumissa on vapaassa steroidimuodossa, ja 40–70 % on sitoutuneena spesifisesti SHBG:hen. Etinyyliestradiolin aiheuttama SHBG:n nousu vaikuttaa jakautumiseen seerumin proteiineissa, jolloin SHBG:hen sitoutumisen osuus suurenee ja albumiiniin sitoutumisen osuus pienenee. Desogestreelin jakautumistilavuus on 1,5 l/kg.
Biotransformaatio
Etonogestreeli metaboloituu täydellisesti steroidien tunnettujen metaboliareittien välityksellä. Metabolinen puhdistuma seerumista on noin 2 ml/min/kg. Yhteisvaikutuksia samanaikaisesti annetun etinyyliestradiolin kanssa ei todettu.
Eliminaatio
Etonogestreelin pitoisuudet seerumissa pienenevät kahdessa vaiheessa. Terminaalisen vaiheen puoliintumisaika on noin 30 tuntia. Desogestreeli ja sen metaboliitit erittyvät virtsaan ja sappeen noin suhteessa 6:4.
Vakaa tila
Etonogestreelin farmakokinetiikkaan vaikuttaa SHBG:n pitoisuus, joka suurenee kolminkertaiseksi etinyyliestradiolin vaikutuksesta. Päivittäisen oton jälkeen lääkkeen pitoisuus seerumissa suurenee kaksin- tai kolminkertaiseksi, ja vakaa tila saavutetaan hoitojakson jälkimmäisellä puoliskolla.
Etinyyliestradioli
Imeytyminen
Suun kautta annettu etinyyliestradioli imeytyy nopeasti ja täydellisesti. Huippupitoisuus seerumissa, n. 80 pg/ml, saavutetaan 1-2 tunnin kuluessa kerta-annoksen ottamisesta. Absoluuttinen biologinen hyötyosuus on presysteemisen konjugaation ja alkureitin metabolian seurauksena 60 %.
Jakautuminen
Etinyyliestradioli sitoutuu voimakkaasti (noin 98,5‑prosenttisesti) mutta epäspesifisesti seerumin albumiiniin ja suurentaa SHBG:n pitoisuutta seerumissa. Näennäiseksi jakautumistilavuudeksi määritettiin noin 5 l/kg.
Biotransformaatio
Etinyyliestradioliin kohdistuu presysteeminen konjugaatio sekä ohutsuolen limakalvolla että maksassa.
Etinyyliestradioli metaboloituu pääasiassa aromaattisen hydroksylaation kautta, mutta reaktiossa muodostuu laajasti erilaisia hydroksyloituneita ja metyloituneita metaboliitteja, jotka esiintyvät seerumissa vapaina metaboliitteina tai konjugoituneina glukuronidien tai sulfaattien kanssa. Metabolinen puhdistuma on noin 5 ml/min/kg.
In vitro etinyyliestradioli on CYP2C19:n, CYP1A1:n ja CYP1A2:n reversiibeli estäjä sekä CYP3A4/5:n, CYP2C8:n ja CYP2J2:n mekanistinen estäjä.
Eliminaatio
Etinyyliestradiolin pitoisuus seerumissa pienenee kahdessa vaiheessa; terminaalisen vaiheen puoliintumisaika on noin 24 tuntia. Etinyyliestradioli ei erity muuttumattomassa muodossa. Sen metaboliitit erittyvät virtsaan ja sappeen suhteessa 4:6. Metaboliittien erityksen puoliintumisaika on noin 1 vrk.
Vakaa tila
Vakaan tilan pitoisuudet saavutetaan 3–4 vrk:n kuluttua, jolloin lääkkeen pitoisuus seerumissa on 30–40 % suurempi kuin kerta-annoksen jälkeen.
Prekliiniset tiedot turvallisuudesta
Etinyyliestradiolia ja desogestreelia koskeneiden prekliinisten tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille, kun yhdistelmäehkäisytabletteja käytetään ohjeiden mukaan. Tämä päätelmä perustuu toistuvan altistuksen aiheuttamaa toksisuutta, genotoksisuutta, karsinogeenisuutta sekä lisääntymistoksisuutta koskeviin konventionaalisiin tutkimuksiin. On kuitenkin muistettava, että sukupuolihormonit voivat edistää tiettyjen hormoniriippuvaisten kudosten ja kasvainten kasvua.
Farmaseuttiset tiedot
Apuaineet
Vaikuttavat kalvopäällysteiset tabletit (valkoiset):
-
Tabletin ydin:
Laktoosimonohydraatti
Maissitärkkelys
Povidoni K-30 (E1201)
RRR-α-tokoferoli (E307)
Soijaöljy
Piidioksidi, kolloidinen, hydratoitu (E551)
Piidioksidi, kolloidinen, vedetön (E551)
Steariinihappo (E570) -
Tabletin kalvopäällyste:
Hypromelloosi 2910 (E464)
Makrogoli 400
Titaanidioksidi (E171)
Kalvopäällysteiset lumetabletit (vihreät):
-
Tabletin ydin:
Laktoosimonohydraatti
Maissitärkkelys
Povidoni K-30 (E1201)
Piidioksidi, kolloidinen, vedetön (E551)
Magnesiumstearaatti (E572) -
Tabletin kalvopäällyste:
Hypromelloosi 2910 (E464)
Triasetiini (E1518)
Polysorbaatti 80
Titaanidioksidi (E171)
Indigokarmiinin alumiinilakka (E132)
Keltainen rautaoksidi (E172)
Yhteensopimattomuudet
Ei oleellinen.
Kestoaika
2 vuotta
Säilytys
Säilytä alle 30 ºC. Säilytä alkuperäispakkauksessa. Herkkä valolle.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
LUMIVELA tabletti, kalvopäällysteinen
150/20 mikrog (L:kyllä) 3 x 28 fol (14,45 €)
PF-selosteen tieto
Läpipainopakkaus, jossa alumiinitaustakalvo ja kirkas tai hieman samea PVC/PVDC-kalvo.
Pakkauskoot:
1 x 21 + 7 kalvopäällysteistä tablettia (21 vaikuttavaa tablettia ja 7 lumetablettia)
3 x 21 + 7 kalvopäällysteistä tablettia (21 vaikuttavaa tablettia ja 7 lumetablettia)
6 x 21 + 7 kalvopäällysteistä tablettia (21 vaikuttavaa tablettia ja 7 lumetablettia)
13 x 21 + 7 kalvopäällysteistä tablettia (21 vaikuttavaa tablettia ja 7 lumetablettia)
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Valmisteen kuvaus:
Vaikuttavat tabletit: valkoinen, pyöreä, kalvopäällysteinen tabletti, jonka läpimitta on 5 mm. Toisella puolella on merkintä ”C” ja toisella puolella ”5”.
Lumetabletit: vihreä, pyöreä, kalvopäällysteinen tabletti, jonka läpimitta on 5 mm.
Käyttö- ja käsittelyohjeet
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
LUMIVELA tabletti, kalvopäällysteinen
150/20 mikrog 3 x 28 fol
- Ei korvausta.
ATC-koodi
G03AA09
Valmisteyhteenvedon muuttamispäivämäärä
04.11.2024
Yhteystiedot
Arenagatan 35
215 32 Malmö
Sweden
www.exeltis.fi
nordics@exeltis.com
