MULTAQ tabletti, kalvopäällysteinen 400 mg
 Lääketurva
Lääketurva
Riskienminimointimateriaalit
Lääkäri
Vaikuttavat aineet ja niiden määrät
Yksi tabletti sisältää 400 mg dronedaronia (hydrokloridimuodossa).
Apuaine, jonka vaikutus tunnetaan:
Yksi tabletti sisältää lisäksi 41,65 mg laktoosia (monohydraattimuodossa).
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Tabletti, kalvopäällysteinen.
Kliiniset tiedot
Käyttöaiheet
Multaq on tarkoitettu sinusrytmin ylläpitämiseen rytmin onnistuneen kääntymisen jälkeen aikuisille, kliinisesti vakaille potilaille, joilla ilmenee kohtauksittaista tai jatkuvaa eteisvärinää.Turvallisuusprofiilin vuoksi (ks. kohdat Vasta-aiheet ja Varoitukset ja käyttöön liittyvät varotoimet) Multaq-valmistetta tulee määrätä vasta, kun muita hoitovaihtoehtoja on harkittu.
Multaq-valmistetta ei saa antaa potilaille, joilla on vasemman kammion systolinen toimintahäiriö tai potilaille, joilla on ilmennyt tai ilmenee parhaillaan sydämen vajaatoiminta.
Ehto
Valmistetta saavat määrätä vain hyväksytyn käyttöaiheen hoitoon perehtyneet erikoislääkärit tai heidän valvonnassaan toimivat lääkärit.
Annostus ja antotapa
Hoito tulee aloittaa ja sitä on seurattava vain erikoislääkärin valvonnassa (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Dronedaronihoito voidaan aloittaa avohoidossa.
Ryhmän I tai III rytmihäiriölääkkeiden (esim. flekainidi, propafenoni, kinidiini, disopyramidi, dofetilidi, sotaloli, amiodaroni) käyttö on lopetettava ennen dronedaronihoidon aloittamista.
Sopivasta ajankohdasta aloittaa dronedaronilääkitys amiodaronin lopettamisen jälkeen on vain vähän tietoa. On otettava huomioon, että amiodaronin vaikutus voi jatkua pitkään sen lopettamisen jälkeen johtuen sen pitkästä puoliintumisajasta. Jos vaihtoon ryhdytään, se pitäisi tehdä erikoislääkärin valvonnassa (ks. kohdat Vasta-aiheet ja Farmakodynamiikka).
Annostus
Aikuisten suositusannos on 400 mg kahdesti vuorokaudessa. Annos tulee ottaa seuraavasti:
- yksi tabletti aamuaterian yhteydessä ja
- yksi tabletti ilta-aterian yhteydessä.
Greippimehua ei pidä ottaa samanaikaisesti dronedaronin kanssa (ks. kohta Yhteisvaikutukset).
Jos potilaalta jää annos ottamatta, seuraava annos tulee ottaa normaalin aikataulun mukaan, eikä kaksinkertaista annosta pidä ottaa.
Erityispotilasryhmät
Iäkkäät potilaat
Teho ja turvallisuus olivat samankaltaiset iäkkäillä potilailla, joilla ei ollut muita sydänsairauksia, ja nuoremmilla potilailla. Vähintään 75-vuotiaita, monisairaita potilaita on seurattava sydämen vajaatoiminnan kliinisten merkkien varalta ja EKG-tutkimus on tehtävä säännöllisesti (ks. kohdat Vasta-aiheet, Varoitukset ja käyttöön liittyvät varotoimet ja Farmakodynamiikka). Iäkkäiden naisten plasman lääkeainealtistus suureni terveillä tutkimushenkilöillä tehdyssä farmakokineettisessä tutkimuksessa, mutta annoksen muuttamista ei pidetä tarpeellisena (ks. kohdat Farmakodynamiikka ja Farmakokinetiikka).
Maksan vajaatoiminta
Dronedaroni on vasta-aiheista potilailla, joilla on vaikea maksan vajaatoiminta, koska tällaisesta käytöstä ei ole tutkimustietoa (ks. kohdat Vasta-aiheet ja Varoitukset ja käyttöön liittyvät varotoimet). Annosta ei tarvitse muuttaa, jos potilaalla on lievä tai keskivaikea maksan vajaatoiminta (ks. kohta Farmakokinetiikka).
Munuaisten vajaatoiminta
Dronedaroni on vasta-aiheista potilailla, joilla on vaikea munuaisten vajaatoiminta (kreatiniinipuhdistuma on < 30 ml/min) (ks. kohta Vasta-aiheet). Annosta ei tarvitse muuttaa muilla munuaisten vajaatoimintaa sairastavilla potilailla (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet sekä Farmakokinetiikka).
Pediatriset potilaat
MULTAQ-valmisteen turvallisuutta ja tehoa alle 18‑vuotiaiden lasten hoidossa ei ole vielä varmistettu. Tietoja ei ole saatavilla.
Antotapa
Suun kautta.
On suositeltavaa niellä tabletti kokonaisena veden kera aterian yhteydessä. Tablettia ei voi jakaa yhtä suuriin annoksiin.
Vasta-aiheet
- Yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille
- Toisen tai kolmannen asteen eteis-kammiokatkos, täydellinen haarakatkos, distaalinen katkos, sinussolmukkeen toimintahäiriö, eteisten johtumishäiriö tai sairas sinus -oireyhtymä (paitsi jos samaan aikaan käytetään toimivaa sydämentahdistinta)
- Bradykardia < 50 lyöntiä/min
- Pysyvä eteisvärinä, jossa eteisvärinä on jatkunut vähintään 6 kk (tai kestoa ei tiedetä) ja sinusrytmin palauttamista ei enää yritetä lääkärin harkinnan mukaan.
- Potilaat, joilla on epävakaa hemodynaaminen tila
- Aiemmin ilmennyt tai parhaillaan ilmenevä sydämen vajaatoiminta tai vasemman kammion systolinen toimintahäiriö
- Aiemmin amiodaronin käytöstä aiheutunut maksa- tai keuhkotoksisuus
- Samanaikainen potenttien sytokromi P450 (CYP) 3A4:n estäjien, kuten ketokonatsolin, itrakonatsolin, vorikonatsolin, posakonatsolin, telitromysiinin, klaritromysiinin, nefatsodonin tai ritonaviirin, käyttö (ks. kohta Yhteisvaikutukset)
- Kääntyvien kärkien takykardiaa (torsades de pointes) aiheuttavat lääkkeet, esim. fentiatsiinit, sisapridi, bepridiili, trisykliset masennuslääkkeet, terfenadiini, eräät suun kautta otettavat makrolidit (kuten erytromysiini) sekä ryhmän I tai III rytmihäiriölääkkeet (ks. kohta Yhteisvaikutukset)
- QTc-aika (Bazett) ≥ 500 millisekuntia
- Vaikea maksan vajaatoiminta
- Vaikea munuaisten vajaatoiminta (CrCl < 30 ml/min)
- Yhteiskäyttö dabigatraanin kanssa.
Varoitukset ja käyttöön liittyvät varotoimet
Dronedaronin käytön aikana suositellaan huolellista seurantaa sisältäen sydämen, maksan ja keuhkojen toiminnan säännöllisen arvioinnin (ks. alla). Jos eteisvärinä ilmenee uudelleen, dronedaronin lopettamista tulee harkita.
Dronedaronihoito pitää lopettaa kesken hoitojakson, jos potilaalla ilmenee jokin tila, joka voi johtaa kohdassa Vasta-aiheet mainittuun vasta-aiheeseen.
Samanaikaisten lääkitysten, kuten digoksiinin ja antikoagulanttien seuranta on tarpeen.
Potilaat, joille kehittyy pysyvä eteisvärinä hoidon aikana
Kliininen tutkimus potilaille, joilla oli pysyvä eteisvärinä (eteisvärinä oli jatkunut vähintään 6 kk) ja sydän- ja verisuonisairauksien riskitekijöitä, lopetettiin ennenaikaisesti, koska dronedaronia saaneilla potilailla todettiin enemmän kardiovaskulaarisia kuolemia, aivohalvauksia ja sydämen vajaatoimintaa (ks. kohta Farmakodynamiikka). Jatkuvaa EKG-seurantaa suositellaan vähintään 6 kuukauden välein. Jos dronedaronihoitoa saaneelle potilaalle kehittyy pysyvä eteisvärinä, dronedaronihoito tulee lopettaa.
Potilaat, joilla on ilmennyt tai ilmenee parhaillaan sydämen vajaatoiminta tai vasemman kammion systolinen toimintahäiriö
Dronedaroni on vasta-aiheista potilaille, joilla on epävakaa hemodynaaminen tila, johon liittyy aiemmin ilmennyt tai parhallaan ilmenevä sydämen vajaatoiminta tai vasemman kammion systolinen toimintahäiriö (ks. kohta Vasta-aiheet).
Potilaita tulee seurata tarkkaan kongestiivisen sydämen vajaatoiminnan oireiden varalta. Uusia sydämen vajaatoimintatapauksia ja sydämen vajaatoiminnan pahenemista dronedaronihoidon aikana on raportoitu spontaanisti. Potilaita on neuvottava ottamaan yhteyttä lääkäriin, jos heille kehittyy tai he tuntevat sydämen vajaatoiminnan merkkejä tai oireita, kuten painon nousua, siihen liittyvää turvotusta tai lisääntyvää hengenahdistusta. Jos sydämen vajaatoiminta kehittyy, dronedaronihoito tulee lopettaa. Potilaita on seurattava vasemman kammion systolisen toimintahäiriön kehittymisen varalta hoidon aikana. Jos vasemman kammion systolinen toimintahäiriö kehittyy, dronedaronihoito tulee lopettaa.
Potilaat, joilla on sepelvaltimotauti
Potilaita, joilla on sepelvaltimotauti, on seurattava sydämen vajaatoiminnan kliinisten merkkien varalta ja heille on tehtävä säännöllisesti EKG-tutkimus sydämen vajaatoiminnan varhaisten merkkien havaitsemiseksi. ESC:n ja ACC/AHA/HRS:n hoitosuosituksissa dronedaronia koskevat ryhmän IA suositukset potilailla, joilla ilmenee kohtauksittaista tai jatkuvaa eteisvärinää tai joilla on sepelvaltimotauti.
Iäkkäät potilaat
Iäkkäitä vähintään 75-vuotiaita, monisairaita potilaita on seurattava sydämen vajaatoiminnan kliinisten merkkien varalta ja heille on tehtävä säännöllisesti EKG-tutkimus (ks. kohdat Annostus ja antotapa ja Farmakodynamiikka).
Naiset, jotka voivat tulla raskaaksi, ja raskaus
Dronedaronin käyttöä ei suositella raskauden aikana eikä sellaisten naisten hoitoon, jotka voivat tulla raskaaksi mutta eivät käytä ehkäisyä. Naisten, jotka voivat tulla raskaaksi, on käytettävä tehokasta ehkäisyä dronedaronihoidon aikana ja 7 päivän ajan viimeisen annoksen saamisen jälkeen. Jos potilas on nainen, joka voi tulla raskaaksi, lääkärin on varmistettava ennen dronedaronin käytön aloittamista, että potilas ei ole raskaana (ks. kohta Raskaus ja imetys).
Maksavaurio
Maksasolujen vaurioita mukaan lukien henkeäuhkaavaa akuuttia maksan vajaatoimintaa on raportoitu ilmenneen dronedaronia käyttäville potilaille myyntiluvan myöntämisen jälkeisessä seurannassa. Maksan toimintakokeet on tehtävä ennen dronedaronihoidon aloittamista sekä yhden viikon ja yhden kuukauden kuluttua hoidon aloittamisen jälkeen ja sen jälkeen joka kuukausi kuuden kuukauden ajan ja sitten kuukausien 9 ja 12 kohdalla, jonka jälkeen ajoittain.
Jos ALAT-arvo (alaniiniaminotransferaasi) on koholla ≥ 3 × normaalin ylärajan (ULN), ALAT-arvo on mitattava uudelleen 48–72 tunnin sisällä. Jos ALAT-arvon todetaan uudelleen olevan ≥ 3 × ULN, dronedaronihoito on lopetettava. Potilaalle on tehtävä asianmukaiset tutkimukset ja seurattava tarkkaan kunnes ALAT-arvo on palautunut normaaliksi.
Potilaita on neuvottava kertomaan välittömästi lääkärille kaikki mahdolliseen maksavaurioon liittyvät oireet (kuten jatkuva vatsakipu uutena oireena, ruokahaluttomuus, pahoinvointi, oksentelu, kuume, huonovointisuus, väsymys, ihon/silmien keltaisuus, tumma virtsa tai kutina).
Suurentunut plasman kreatiniinipitoisuus
Plasman kreatiniinipitoisuuden on havaittu suurentuneen (keskimääräinen nousu 10 mikromol/l), kun terveet tutkimushenkilöt ja potilaat ovat saaneet dronedaronia 400 mg kahdesti vuorokaudessa. Useimmilla potilailla tämä suureneminen tapahtuu pian hoidon aloittamisen jälkeen ja tasaantuu 7 päivän kuluttua. Plasman kreatiniinipitoisuuden mittaamista suositellaan ennen dronedaronihoidon aloittamista ja 7 päivän kuluttua hoidon aloittamisen jälkeen. Jos veren kreatiniinipitoisuuden suurenemista havaitaan, seerumin kreatiniinipitoisuus tulee mitata uudelleen 7 päivän kuluttua. Jos kreatiniinipitoisuus ei ole enää noussut, tätä arvoa tulee käyttää uutena lähtötilanteen viitearvona, koska tällainen voi olla odotettavissa dronedaronia käytettäessä. Jos seerumin kreatiniinipitoisuus nousee edelleen, tulee lisätutkimuksia ja hoidon lopettamista harkita.
Veren kreatiniinipitoisuuden suureneminen ei välttämättä edellytä ACE:n estäjien tai angiotensiini II-reseptorin salpaajien (AIIRAs) käytön lopettamista.
Myyntiluvan myöntämisen jälkeisessä käytössä on raportoitu suurempia kreatiniinipitoisuuksien nousuja dronedaronihoidon aloittamisen jälkeen. Joissain tapauksissa raportoitiin myös veren ureapitoisuuden nousua, joka johtui mahdollisesti sydämen vajaatoiminnan aiheuttamasta sekundaarisesta hypoperfuusiosta (prerenaalinen atsotemia). Tällaisissa tapauksissa dronedaronin käyttö on lopetettava (ks. kohdat Vasta-aiheet ja Varoitukset ja käyttöön liittyvät varotoimet). On suositeltavaa seurata munuaisten toimintaa säännöllisesti ja harkita jatkotutkimuksia tarpeen mukaan.
Elektrolyyttiepätasapaino
Rytmihäiriölääkkeet voivat olla tehottomia tai aiheuttaa rytmihäiriöitä hypokaleemisilla potilailla, ja siksi kaliumin tai magnesiumin puutos on korjattava ennen dronedaronihoitoa ja sen aikana.
QT-ajan piteneminen
Dronedaronin farmakologinen vaikutusmekanismi voi aiheuttaa keskivaikeaa QTc-ajan pitenemistä (Bazettin kaavalla laskettuna noin 10 ms), joka liittyy repolarisaation pidentymiseen. Nämä muutokset liittyvät dronedaronin hoitovaikutukseen, eivätkä ne ole merkkejä toksisuudesta. Hoidonaikaista seurantaa mm. EKG:n (elektrokardiografian) avulla suositellaan. Jos QTc-aika (Bazett) ≥ 500 millisekuntia, dronedaronin käyttö tulee lopettaa (ks. kohta Vasta-aiheet).
Kliinisen kokemuksen perusteella dronedaronin proarytminen vaikutus on heikko, ja dronedaronin osoitettiin ATHENA-tutkimuksessa vähentävän rytmihäiriöihin liittyviä kuolemia (ks. kohta Farmakodynamiikka).
Proarytmisiä vaikutuksia voi kuitenkin ilmetä tietyissä tilanteissa, kuten rytmihäiriöille altistavien lääkkeiden käytön ja/tai elektrolyyttihäiriöiden yhteydessä (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet sekä Yhteisvaikutukset).
Hengityselimet, rintakehä ja välikarsina
Interstitiaalia keuhkosairautta kuten pneumoniittia ja keuhkofibroosia on raportoitu myyntiluvan myöntämisen jälkeisessä seurannassa. Hengenahdistuksen tai ärsytysyskän ilmeneminen voi liittyä keuhkotoksisuuteen ja potilaiden kliininen arvio tulee tehdä huolella. Jos keuhkotoksisuutta todetaan, hoito tulee lopettaa.
Yhteisvaikutukset (ks. kohta Yhteisvaikutukset)
Digoksiini
Dronedaronin antaminen digoksiinia saaville potilaille aiheuttaa plasman digoksiinipitoisuuden suurenemista ja sen seurauksena jouduttaa digoksiinimyrkytyksen löydöksiä ja oireita. Kliinistä ja biologista seurantaa sekä EKG-seurantaa suositellaan, ja digoksiiniannos tulee puolittaa. Synergistinen vaikutus syketiheyteen ja eteis-kammiojohtumiseen on myös mahdollinen.
Beetasalpaajat ja kalsiuminestäjät
Sinussolmukkeeseen ja eteis-kammiosolmukkeeseen lamaavasti vaikuttavien beetasalpaajien tai kalsiuminestäjien samanaikaisessa käytössä on noudatettava varovaisuutta. Näiden lääkkeiden käyttö tulee aloittaa pieninä annoksina, ja annosta tulee suurentaa vasta EKG-tutkimuksen jälkeen. Jos potilas käyttää kalsiuminestäjiä tai beetasalpaajia dronedaronihoitoa aloitettaessa, potilaalle on tehtävä EKG-tutkimus ja annosta on muutettava tarvittaessa.
K-vitamiiniantagonistit
Potilaille tulee antaa sopivasti antikoagulantteja eteisvärinän kliinisten ohjeiden mukaan. K-vitamiiniantagonistia käyttävien potilaiden INR-arvoa (International Normalized Ratio) tulee seurata tarkkaan dronedaronin aloittamisen jälkeen.
Potentit CYP3A4:n indusoijat
Potenttien CYP3A4:n indusoijien, kuten rifampisiinin, fenobarbitaalin, karbamatsepiinin, fenytoiinin ja mäkikuisman, käyttöä ei suositella.
Statiinit
Statiinien käytössä on noudatettava varovaisuutta. Tavallista pienemmän statiinialoitusannoksen ja -ylläpitoannosten käyttöä tulee harkita, ja potilaan tilaa tulee seurata lihastoksisuuden kliinisten merkkien varalta.
Greippimehu
Potilaita tulee kehottaa välttämään greippimehua sisältäviä juomia dronedaronihoidon aikana.
Laktoosi
Tämä lääkevalmiste sisältää laktoosia. Potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, täydellinen laktaasinpuutos tai glukoosi-galaktoosi-imeytymishäiriö, ei pidä käyttää tätä lääkettä.
Yhteisvaikutukset
Dronedaroni metaboloituu pääasiassa CYP3A4:n kautta (ks. kohta Farmakokinetiikka). Siksi CYP3A4:n estäjät ja indusoijat voivat aiheuttaa yhteisvaikutuksia dronedaronin kanssa. Dronedaroni on kohtalaisen voimakas CYP3A4:n estäjä, heikko CYP2D6:n estäjä ja voimakas P-glykoproteiinien estäjä. Siksi dronedaroni voi aiheuttaa yhteisvaikutuksia P-glykoproteiinien, CYP3A4:n ja CYP2D6:n substraattien kanssa. Dronedaronin ja/tai sen metaboliittien on osoitettu in vitro estävän kuljettajaproteiineja, jotka kuuluvat orgaanisten anionien kuljettajiin (OAT, Organic Anion Transporter), orgaanisten anionien kuljettajapolypeptideihin (OATP, Organic Anion Transporting Polypeptide) ja orgaanisten kationien kuljettajiin (OCT, Organic Cation Transporter). Dronedaroni ei estä merkitsevästi CYP1A2:ta, CYP2C9:ä, CYP2C19:ä, CYP2C8:a eikä CYP2B6:ta.
Myös farmakodynaaminen yhteisvaikutus on mahdollinen beetasalpaajien, kalsiuminestäjien ja digitaliksen kanssa.
Kääntyvien kärkien takykardiaa aiheuttavat lääkkeet
Kääntyvien kärkien takykardiaa (torsades de pointes) aiheuttavat lääkkeet, esim. fentiatsiinit, sisapridi, bepridiili, trisykliset masennuslääkkeet, eräät suun kautta otettavat makrolidit (kuten erytromysiini), terfenadiini sekä ryhmän I tai III rytmihäiriölääkkeet ovat vasta-aiheisia mahdollisen proarytmiariskin vuoksi (ks. kohta Vasta-aiheet).
Jos potilas käyttää beetasalpaajia dronedaronihoitoa aloitettaessa, potilaalle on tehtävä EKG-tutkimus ja beetasalpaajan annosta on tarvittaessa muutettava (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Kliinistä ja biologista seurantaa sekä EKG-seurantaa suositellaan, ja digoksiiniannos tulee puolittaa (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Muiden lääkkeiden vaikutus dronedaroniin
Voimakkaat CYP3A4:n estäjät
Dronedaronialtistus suurentui 17-kertaiseksi, kun samanaikaisesti annettiin toistuvasti 200 mg:n ketokonatsoliannoksia. Siksi ketokonatsolin ja muiden voimakkaiden CYP3A4:n estäjien, kuten itrakonatsolin, vorikonatsolin, posakonatsolin, ritonaviirin, telitromysiinin, klaritromysiinin tai nefatsodonin, samanaikainen käyttö on vasta-aiheista (ks. kohta Vasta-aiheet).
Kohtalaisen voimakkaat / heikot CYP3A4:n estäjät:
Erytromysiini
Erytromysiini, suun kautta otettava makrolidi, voi aiheuttaa kääntyvien kärkien takykardiaa ja on siksi vasta-aiheinen (ks. kohta Vasta-aiheet). Toistuvat erytromysiiniannokset (500 mg kolme kertaa vuorokaudessa 10 päivää) nostivat dronedaronille altistumisen 3,8-kertaiseksi vakaassa tilassa.
Kalsiuminestäjät
Kalsiuminestäjät diltiatseemi ja verapamiili ovat CYP3A4:n substraatteja ja/tai kohtalaisen voimakkaita estäjiä. Syketiheyttä pienentävien ominaisuuksiensa vuoksi verapamiililla ja diltiatseemilla voi lisäksi olla farmakodynaamisia yhteisvaikutuksia dronedaronin kanssa. Dronedaronialtistus suurentui 1,7-kertaiseksi, kun samanaikaisesti annettiin toistuvasti diltiatseemia (240 mg kahdesti vuorokaudessa), 1,4-kertaiseksi, kun samanaikaisesti annettiin toistuvasti verapamiilia (240 mg kerran vuorokaudessa), ja 1,2-kertaiseksi, kun samanaikaisesti annettiin toistuvasti nifedipiiniä (20 mg kahdesti vuorokaudessa). Dronedaroni (400 mg kahdesti vuorokaudessa) suurentaa myös kalsiuminestäjäaltistusta (verapamiili 1,4-kertaiseksi ja nisoldipiini 1,5-kertaiseksi). Kliinisissä tutkimuksissa 13 % potilaista sai kalsiuminestäjiä samanaikaisesti dronedaronin kanssa. Hypotension, bradykardian ja sydämen vajaatoiminnan riski ei suurentunut.
Yleisesti voidaan todeta, että farmakokineettisen yhteisvaikutuksen ja mahdollisen farmakodynaamisen yhteisvaikutuksen vuoksi sinussolmukkeeseen ja eteis-kammiosolmukkeeseen lamaavasti vaikuttavia kalsiuminestäjiä, kuten verapamiilia ja diltiatseemia, tulee käyttää varoen yhdessä dronedaronin kanssa. Näiden lääkkeiden käyttö tulee aloittaa pieninä annoksina, ja annosta tulee suurentaa vasta EKG-tutkimuksen jälkeen. Jos potilaalla on jo käytössä kalsiuminestäjä dronedaronihoidon aloittamisen aikaan, potilaalle on tehtävä EKG-tutkimus ja kalsiuminestäjän annosta on tarvittaessa muutettava (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Muut keskivahvat/heikot CYP 3A4:n estäjät
Myös muut kohtalaisen voimakkaat CYP3A4:n estäjät lisäävät todennäköisesti dronedaronialtistusta.
CYP3A4:n indusoijat
Rifampisiini (600 mg kerran vuorokaudessa) pienensi dronedaronialtistusta 80 %, mutta se ei vaikuttanut merkittävästi dronedaronin aktiivisten metaboliittien altistukseen. Rifampisiinin ja muiden voimakkaiden CYP3A4:n indusoijien, kuten fenobarbitaalin, karbamatsepiinin, fenytoiinin tai mäkikuisman, samanaikaista käyttöä ei suositella, koska ne pienentävät dronedaronialtistusta.
MAO:n estäjät
MAO osallistui dronedaronin aktiivisen metaboliitin metaboliaan in vitro tutkimuksessa. Tämän havainnon kliinistä merkitystä ei tunneta (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Farmakokinetiikka).
Dronedaronin vaikutus muihin lääkkeisiin
Yhteisvaikutukset CYP3A4:n kautta metaboloituvien lääkeaineiden kanssa
Dabigatraani
Kun dabigatraanieteksilaattia annettiin annoksella 150 mg kerran vuorokaudessa samanaikaisesti dronedaronin kanssa, jonka annos oli 400 mg kahdesti vuorokaudessa, dabigatraanin AUC0-24 lisääntyi 100 %:lla ja Cmax lisääntyi 70 %:lla. Kliinistä tietoa näiden lääkevalmisteiden yhteiskäytöstä eteisvärinäpotilailla ei ole. Näiden valmisteiden yhteiskäyttö on vasta-aiheista (ks. kohta Vasta-aiheet).
Statiinit
Dronedaroni voi suurentaa sellaisten statiinien altistusta, jotka ovat CYP3A4:n tai P-glykoproteiinin substraatteja. Dronedaroni (400 mg kahdesti vuorokaudessa) suurensi simvastatiinialtistuksen 4-kertaiseksi ja simvastatiinihappoaltistuksen 2-kertaiseksi. Oletettavasti dronedaroni voi suurentaa myös lovastatiinialtistusta samantyyppisesti kuin simvastatiinihappoaltistuksen. Dronedaronin ja atorvastatiinin välillä oli heikko yhteisvaikutus (josta seurasi keskimäärin 1,7-kertainen lisäaltistuminen atorvastatiinille). Dronedaronin ja OATP:n kuljettamien statiinien, kuten rosuvastatiinin, välillä oli heikko yhteisvaikutus (josta seurasi keskimäärin 1,4-kertainen lisäaltistuminen rosuvastatiinille).
Kliinisissä tutkimuksissa ei ilmennyt turvallisuusongelmia, kun dronedaronia annettiin samanaikaisesti sellaisten statiinien kanssa, jotka metaboloituvat CYP3A4:n välityksellä. Spontaaneja rabdomyolyysitapauksia on kuitenkin raportoitu, kun dronedaronia on käytetty yhdessä statiinien (erityisesti simvastatiinin) kanssa, ja sen vuoksi statiinien samanaikainen käyttö edellyttää varovaisuutta.
Tavallista pienemmän statiinialoitusannoksen ja ylläpitoannosten käyttöä tulee harkita kyseisen statiinin valmisteyhteenvedon suositusten mukaisesti, ja potilaan tilaa tulee seurata lihastoksisuuden kliinisten merkkien varalta (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Kalsiuminestäjät
Dronedaronin ja kalsiuminestäjien yhteisvaikutus on kuvattu edellä (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Immunosuppressantit
Dronedaroni saattaa suurentaa immunosuppressanttien (takrolimuusi, sirolimuusi, everolimuusi ja siklosporiini) pitoisuutta plasmassa. Sirolimuusin ja takrolimuusin pitoisuuksia plasmassa tulee seurata ja annoksia muuttaa tarvittaessa, jos niitä käytetään samanaikaisesti dronedaronin kanssa.
Ehkäisytabletit
Dronedaronia (800 mg kahdesti vuorokaudessa) ja ehkäisytabletteja samanaikaisesti käyttäneillä terveillä tutkimushenkilöillä ei havaittu etinyyliestradiolin eikä levonorgestreelin pitoisuuden pienenemistä.
Yhteisvaikutukset CYP2D6:n kautta metaboloituvien lääkeaineiden kanssa
Beetasalpaajat
Sotalolihoito on lopetettava ennen dronedaronihoidon aloittamista (ks. kohdat Annostus ja antotapa ja Vasta-aiheet). Dronedaroni saattaa suurentaa CYP2D6:n kautta metaboloituvien beetasalpaajien altistusta. Beetasalpaajilla voi lisäksi olla farmakodynaamisia yhteisvaikutuksia dronedaronin kanssa. Dronedaroni (800 mg vuorokaudessa) suurensi metoprololialtistuksen 1,6-kertaiseksi ja propranololialtistuksen 1,3-kertaiseksi (eli muutos oli paljon pienempi kuin hitaiden ja nopeiden CYP2D6-metaboloijien välillä, jolloin ero voi olla 6-kertainen). Kliinisissä tutkimuksissa bradykardiaa havaittiin useammin, kun dronedaronia annettiin samanaikaisesti beetasalpaajien kanssa.
Farmakokineettisen yhteisvaikutuksen ja mahdollisen farmakodynaamisen yhteisvaikutuksen vuoksi beetasalpaajia tulee käyttää varoen yhdessä dronedaronin kanssa. Näiden lääkkeiden käyttö tulee aloittaa pieninä annoksina, ja annosta tulee suurentaa vasta EKG-tutkimuksen jälkeen. Jos potilas käyttää beetasalpaajia dronedaronihoitoa aloitettaessa, potilaalle on tehtävä EKG-tutkimus ja beetasalpaajan annosta on tarvittaessa muutettava (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Masennuslääkkeet
Dronedaroni on ihmisellä heikko CYP2D6:n estäjä, joten sen oletetaan aiheuttavan vain vähän yhteisvaikutuksia CYP2D6:n kautta metaboloituvien masennuslääkkeiden kanssa.
Yhteisvaikutukset P-glykoproteiinin substraattien kanssa
Digoksiini
Dronedaroni (400 mg kahdesti vuorokaudessa) suurensi digoksiinialtistuksen 2,5-kertaiseksi estämällä P-glykoproteiinipumppua. Digitaliksella voi lisäksi olla farmakodynaamisia yhteisvaikutuksia dronedaronin kanssa. Synergistinen vaikutus syketiheyteen ja eteis-kammiojohtumiseen on mahdollinen. Kliinisissä tutkimuksissa havaittiin suurentuneita digitalispitoisuuksia ja/tai digitalismyrkytykseen viittaavia maha-suolikanavan häiriöitä, kun dronedaronia annettiin samanaikaisesti digitaliksen kanssa.
Digoksiiniannosta on pienennettävä noin 50 % ja seerumin digoksiinipitoisuutta on seurattava tarkasti. Lisäksi suositellaan kliinistä seurantaa ja EKG-seurantaa.
Yhteisvaikutukset CYP3A4:n ja P-glykoproteiinin välityksellä metaboloituvien lääkeaineiden kanssa
Rivaroksabaani
Dronedaroni todennäköisesti suurentaa rivaroksabaanialtistusta (rivaroksabaani on CYP3A4:n ja P‑glykoproteiinin substraatti), joten niiden samanaikainen käyttö saattaa suurentaa verenvuotojen riskiä. Rivaroksabaanin ja dronedaronin samanaikaista käyttöä ei suositella.
Apiksabaani
Dronedaroni saattaa suurentaa apiksabaanialtistusta (apiksabaani on CYP3A4:n ja P-glykoproteiinin substraatti). Apiksabaaniannoksen muuttaminen ei kuitenkaan ole tarpeen samanaikaisessa käytössä lääkeaineiden kanssa, jotka eivät ole voimakkaita sekä CYP3A4:n että P-glykoproteiinin estäjiä, kuten dronedaroni.
Edoksabaani
In vivo -tutkimuksissa edoksabaanialtistus (edoksabaani on CYP3A4:n ja P-glykoproteiinin substraatti) suureni, kun sitä annettiin dronedaronin kanssa. Edoksabaaniannosta on pienennettävä edoksabaanin valmisteyhteenvedon suositusten mukaisesti.
Yhteisvaikutukset varfariinin ja losartaanin (CYP2C9:n substraatteja) kanssa
Varfariini ja muut K-vitamiiniantagonistit
Dronedaroni (600 mg kahdesti vuorokaudessa) suurensi S-varfariinin pitoisuuden 1,2-kertaiseksi. R-varfariinin pitoisuus ei muuttunut, ja INR-arvo (International Normalized Ratio) suureni vain 1,07-kertaiseksi.
Kliinisesti merkittäviä INR-arvon nousuja (>5) raportoitiin kuitenkin oraalisia antikoagulantteja käyttävillä potilailla yleensä viikon sisällä dronedaronihoidon aloittamisen jälkeen. Tämän vuoksi K-vitamiiniantagonistia käyttävien potilaiden INR-arvoa tulee seurata tarkkaan dronedaronin aloittamisen jälkeen.
Losartaani ja muut angiotensiini II-reseptorin salpaajat (AIIRAs)
Dronedaronin ja losartaanin välillä ei havaittu yhteisvaikutuksia, ja dronedaronin ja muiden angiotensiini II-reseptorin salpaajien välillä ei odoteta esiintyvän yhteisvaikutuksia.
Yhteisvaikutukset teofylliinin (CYP1A2:n substraatti) kanssa
Dronedaroni annoksena 400 mg kahdesti vuorokaudessa ei suurenna vakaan tilan teofylliinialtistusta.
Yhteisvaikutus metformiinin kanssa (OCT1:n ja OCT2:n substraatti)
Dronedaronin ja metformiinin, OCT1:n ja OCT2:n substraatin, välillä ei havaittu yhteisvaikutusta.
Yhteisvaikutus omepratsolin kanssa (CYP 2C19:n substraatti)
Dronedaroni ei vaikuta omepratsolin, CYP 2C19:n substraatin, farmakokinetiikkaan.
Yhteisvaikutus klopidogreelin kanssa
Dronedaroni ei vaikuta klopidogreelin eikä sen aktiivisen metaboliitin farmakokinetiikkaan.
Muuta tietoa
Pantopratsoli (40 mg kerran vuorokaudessa) – lääkeaine, joka suurentaa mahan pH-arvoa vaikuttamatta mitenkään sytokromi P450 -järjestelmään – ei vaikuttanut merkitsevästi dronedaronin farmakokinetiikkaan.
Greippimehu (CYP3A4:n estäjä)
Dronedaronialtistus suurentui 3-kertaiseksi, kun samanaikaisesti annettiin toistuvasti 300 ml greippimehua kolmesti vuorokaudessa. Potilaita tulee siksi kehottaa välttämään greippimehua sisältäviä juomia dronedaronihoidon aikana (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Raskaus ja imetys
Naiset, jotka voivat tulla raskaaksi, ja raskaus
MULTAQ-valmisteen käyttöä ei suositella raskauden aikana eikä sellaisten naisten hoitoon, jotka voivat tulla raskaaksi mutta eivät käytä ehkäisyä. Dronedaronin käytöstä raskaana oleville naisille ei ole olemassa tietoja tai on vain vähän tietoja. Eläinkokeissa on havaittu lisääntymistoksisuutta (ks. kohta Prekliiniset tiedot turvallisuudesta).
Naisten, jotka voivat tulla raskaaksi, on käytettävä tehokasta ehkäisyä MULTAQ-hoidon aikana ja 7 päivän ajan viimeisen annoksen saamisen jälkeen.
Jos potilas on nainen, joka voi tulla raskaaksi, lääkärin on varmistettava ennen MULTAQ-valmisteen käytön aloittamista, että potilas ei ole raskaana.
Imetys
Ei tiedetä, erittyvätkö dronedaroni ja sen metaboliitit ihmisen rintamaitoon. Olemassa olevat farmakokineettiset/toksikologiset tiedot koe-eläimistä ovat osoittaneet dronedaronin ja sen metaboliittien erittyvän rintamaitoon. Vastasyntyneeseen/imeväiseen kohdistuvia riskejä ei voida poissulkea. Naisia on kehotettava olemaan imettämättä MULTAQ-hoidon aikana ja 7 päivän ajan (noin 5 puoliintumisaikaa) viimeisen annoksen saamisen jälkeen.
On päätettävä, lopetetaanko rintaruokinta vai lopetetaanko Multaq-hoito ottaen huomioon rintaruokinnasta aiheutuvat hyödyt lapselle ja hoidosta koituvat hyödyt äidille.
Hedelmällisyys
Dronedaronin ei ole todettu vaikuttavan hedelmällisyyteen eläinkokeissa.
Vaikutus ajokykyyn ja koneiden käyttökykyyn
MULTAQ-valmisteella ei ole haitallista vaikutusta ajokykyyn ja koneidenkäyttökykyyn. Haittavaikutukset, kuten väsymys, voivat kuitenkin vaikuttaa ajokykyyn ja koneidenkäyttökykyyn.
Haittavaikutukset
Yhteenveto turvallisuusprofiilista
Kun arvioitiin sisäisten tekijöiden, kuten sukupuolen tai iän, vaikutusta hoidon aikana ilmenneisiin haittavaikutuksiin, havaittiin, että sukupuoli (naispotilaat) vaikutti haittavaikutusten ja vakavien haittavaikutusten ilmaantuvuuteen.
Kliinisissä tutkimuksissa dronedaronia saaneista potilaista 11,8 % ja lumelääkettä saaneista potilaista 7,7 % keskeytti osallistumisen etuajassa haittavaikutusten vuoksi. Yleisimmät syyt dronedaronihoidon keskeyttämiseen olivat ruoansulatuselimistön häiriöt (3,2 % dronedaroniryhmässä vs. 1,8 % lumelääkeryhmässä).
Yleisimmät dronedaronin (400 mg kahdesti vuorokaudessa) aiheuttamat haittavaikutukset näissä viidessä tutkimuksessa olivat ripuli (9 %), pahoinvointi (5 %) ja oksentelu (2 %) sekä väsymys ja heikkous (7 %).
Haittavaikutusluettelo taulukossa
Dronedaronin (400 mg kahdesti vuorokaudessa) turvallisuusprofiili potilailla, joilla on eteisvärinää tai eteislepatusta, perustuu viiteen lumekontrolloituun tutkimukseen, joihin satunnaistettiin yhteensä 6 285 potilasta (3 282 potilasta sai dronedaronia 400 mg kahdesti vuorokaudessa ja 2 875 sai lumelääkettä).
Keskimääräinen altistusaika näissä tutkimuksissa oli 13 kuukautta.
ATHENA-tutkimuksessa pisin seuranta-aika oli 30 kuukautta. Joitakin haittavaikutuksia havaittiin myös myyntiluvan myöntämisen jälkeisessä seurannassa.
Haittavaikutukset on esitetty elinjärjestelmittäin.
Haittavaikutusten esiintymistiheydet on määritelty seuraavasti: hyvin yleinen (≥ 1/10), yleinen (≥ 1/100, < 1/10), melko harvinainen (≥ 1/1 000, < 1/100), harvinainen (≥ 1/10 000, < 1/1 000), hyvin harvinainen (< 1/10 000), tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin).
Haittavaikutukset on esitetty kussakin yleisyysluokassa haittavaikutuksen vakavuuden mukaan alenevassa järjestyksessä.
Taulukko 1: Haittavaikutukset
| Elinjärjestelmä | Hyvin yleiset (≥ 1/10) | Yleiset (≥ 1/100, < 1/10) | Melko harvinaiset (≥ 1/1 000, < 1/100) | Harvinaiset (≥ 1/10 000, < 1/1 000) |
| Immuunijärjestelmä | - | - | - | Anafylaktiset reaktiot mukaan lukien angioedeema |
| Hermosto | - | - | Makuhäiriöt | Makuaistin puute |
| Sydän | Kongestiivinen sydämen vajaatoiminta (ks. alla) | Bradykardia (ks. kohdat Vasta-aiheet ja Varoitukset ja käyttöön liittyvät varotoimet) | - | - |
| Verisuonisto | - | - | - | Vaskuliitti, esim. leukosytoklastinen vaskuliitti |
Hengityselimet, rintakehä ja välikarsina | - | - | Interstitiaalinen keuhkosairaus mukaan lukien pneumoniitti ja keuhkofibroosi (ks. alla) | - |
| Ruoansulatuselimistö | - | Ripuli Oksentelu Pahoinvointi Vatsakipu Dyspepsia | - | - |
| Maksa ja sappi | - | Poikkeavat maksan toimintakokeiden tulokset | - | Maksasolujen vaurio, mukaan lukien henkeä uhkaava akuutti maksan vajaatoiminta (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet) |
| Iho ja ihonalainen kudos | - | Ihottuma (esim. yleistynyt, makulaarinen tai makulopapulaarinen ihottuma) Kutina | Eryteema (esim. punoitus tai punoittava ihottuma) Ekseema Valoherkkyysreaktio Allerginen dermatiitti Dermatiitti | - |
| Yleisoireet ja antopaikassa todettavat haitat | - | Väsymys Heikkous | - | - |
| Tutkimukset | Veren kreatiniinin lisääntyminen* QTc-ajan (Bazett) piteneminen# | - | - | - |
* ≥ 10 % viiden päivän kuluttua hoidon aloittamisesta (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet)
# > 450 ms miehillä ja > 470 ms naisilla (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet)
Valikoituja haittavaikutuskuvauksia
Kongestiivinen sydämen vajaatoiminta
Viidessä lumekontrolloidussa tutkimuksessa kongestiivista sydämen vajaatoimintaa ilmeni yhtä paljon dronedaroniryhmässä kuin lumelääkeryhmässä (hyvin yleisesti, 11,2 % vs. 10,9 %). Tämän yleisyyden arvioinnissa olisi huomioitava kongestiivisen sydämen vajaatoiminnan ilmeneminen eteisvärinäpotilailla yleensä. Kongestiivista sydämen vajaatoimintaa on raportoitu ilmenneen myös myyntiluvan myöntämisen jälkeisessä seurannassa (yleisyys tuntematon) (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Interstitiaalinen keuhkosairaus, mukaan lukien pneumoniitti ja keuhkofibroosi
Viidessä lumekontrolloidussa tutkimuksessa 0,6 % dronedaroniryhmän potilaista sai keuhkohaittoja, kun lumeryhmän potilaista niitä sai 0,8 %. Interstitiaalista keuhkosairautta mukaan lukien pneumoniittia ja keuhkofibroosia on raportoitu myyntiluvan myöntämisen jälkeisessä seurannassa (yleisyys tuntematon). Monien potilaiden kohdalla tätä on edeltänyt altistuminen amiodaronille (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Yliannostustapauksessa on tarkkailtava potilaan sydämen rytmiä ja verenpainetta. Potilaalle annetaan tukihoitoa oireiden perusteella.
Ei tiedetä, voidaanko dronedaroni ja/tai sen metaboliitit poistaa dialyysin (hemodialyysin, peritoneaalidialyysin tai hemofiltraation) avulla.
Erityistä vastalääkettä ei ole. Yliannostustapauksessa on syytä keskittyä tukemaan peruselintoimintoja ja lievittämään oireita.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: sydänlääkkeet, rytmihäiriölääkkeet, ryhmä III, ATC-koodi: C01BD07
Vaikutusmekanismi
Eläinmalleissa dronedaroni estää eteisvärinää tai palauttaa normaalin sinusrytmin mallista riippuen. Se estää myös kammiotakykardiaa ja kammiovärinää useissa eläinmalleissa. Nämä vaikutukset johtuvat todennäköisesti dronedaronin elektrofysiologisista ominaisuuksista, jotka kuuluvat kaikkiin neljään Vaughan-Williamsin ryhmään. Dronedaroni estää kaliumin virtausta salpaamalla useita kanavia (esim. IKAch, IKur, IKr, IKs) sekä pidentää siten sydämen aktiopotentiaalia ja refraktaariaikaa (ryhmä III). Se estää myös natriumin (ryhmä Ib) ja kalsiumin virtausta (ryhmä IV). Se estää adrenergista toimintaa ei-kilpailevasti (ryhmä II).
Farmakodynaamiset vaikutukset
Dronedaroni hidastaa syketiheyttä eläinmalleissa. Se pidentää Wenckebachin syklin pituutta sekä AH- , PQ- ja QT-aikaa. QTc-aika ei joko pitene ollenkaan tai vain hyvin vähän, ja HV- ja QRS-ajat säilyvät muuttumattomina. Dronedaroni pidentää eteisten ja eteis-kammiosolmukkeen efektiivistä refraktaariaikaa (ERP). Kammioiden ERP pitenee hiukan, mutta käänteinen riippuvuus syketaajuudesta on hyvin pieni.
Dronedaroni alentaa valtimoverenpainetta ja vähentää sydänlihaksen kontraktiliteettia (dP/dt max) vaikuttamatta vasemman kammion ejektiofraktioon sekä vähentää sydänlihaksen hapenkulutusta.
Dronedaronilla on verisuonia laajentavia ominaisuuksia sepelvaltimoissa (tämä liittyy typpioksidiradan aktivaatioon) ja ääreisvaltimoissa.
Dronedaronilla on epäsuoria antiadrenergisiä vaikutuksia ja osittaisantagonistinen vaikutus adrenergiseen stimulaatioon. Se heikentää adrenaliinin aiheuttamaa alfa-adrenergistä verenpainevastetta sekä isoprenaliinin aiheuttamaa beeta1- ja beeta2-vastetta.
Kliininen teho ja turvallisuus
Eteisvärinään liittyvän sairaalahoidon riskin pieneneminen
Dronedaronin tehokkuus eteisvärinään liittyvien sairaalahoitojaksojen riskin pienentämisessä potilailla, joilla esiintyi tai oli esiintynyt eteisvärinää ja joilla oli muita riskitekijöitä, osoitettiin ATHENA-tutkimuksessa, joka oli kansainvälinen, kaksoissokkoutettu, satunnaistettu ja lumekontrolloitu monikeskustutkimus.
Potilailla oli oltava dokumentoidusti vähintään yksi riskitekijä (esim. ikä, hypertensio, diabetes, aiempi aivoverenkiertohäiriö, vasemman eteisen läpimitta ≥ 50 mm tai LVEF < 0,40) sekä eteisvärinä/eteislepatus että sinusrytmi tutkimusta edeltäneiden 6 kuukauden aikana. Potilaita, jotka olivat saaneet amiodaronia satunnaistamista edeltäneiden 4 viikon aikana, ei otettu tutkimukseen. Potilailla sai olla eteisvärinä, eteislepatus tai spontaanisti tai rytminsiirron avulla normaaliksi palautunut sinusrytmi.
Tutkimukseen satunnaistettiin 4 628 potilasta, joita hoidettiin enintään 30 kuukauden ajan (mediaaniseuranta-aika: 22 kuukautta) joko dronedaronilla 400 mg kahdesti vuorokaudessa (2 301 potilasta) tai lumelääkkeellä (2 327 potilasta). Potilaat saivat lisäksi tavanomaista hoitoa mm. beetasalpaajilla (71 %), ACE:n estäjillä tai AT1-salpaajilla (69 %), digitaliksella (14 %), kalsiuminestäjillä (14 %), statiineilla (39 %), suun kautta otettavilla antikoagulanteilla (60 %), verihiutaleiden toimintaa estävillä aineilla pitkäaikaisesti (6 %) ja/tai diureeteilla (54 %).
Tutkimuksen ensisijainen päätetapahtuma oli aika ensimmäiseen sairaalahoitojaksoon sydän- ja verisuonisyystä tai kuolema mistä tahansa syystä.
Potilaiden ikäjakauma oli 23–97 vuotta, ja 42 % oli yli 75-vuotiaita. Potilaista 47 % oli naisia, ja suurin osa (89 %) oli valkoihoisia.
Suurimmalla osalla (86 %) oli hypertensiota ja rakenteellinen sydänsairaus (60 %) (esim. sepelvaltimotauti: 30 %; sydämen vajaatoiminta: 30 %; LVEF < 45 %: 12 %).
Potilaista 25 prosentilla oli eteisvärinä lähtötilanteessa.
Dronedaroni pienensi sydän- ja verisuonisyistä johtuvan sairaalahoidon tai mistä tahansa syystä johtuvan kuoleman ilmaantuvuutta 24,2 % lumelääkkeeseen verrattuna (p < 0,0001).
Sydän- ja verisuonisyistä johtuvan sairaalahoidon tai mistä tahansa syystä johtuvan kuoleman ilmaantuvuuden pieneneminen oli samansuuruinen kaikissa alaryhmissä riippumatta lähtötilanteen ominaisuuksista tai lääkevalmisteista (ACE:n estäjät tai AT1-salpaajat, beetasalpaajat, digitalis, statiinit, kalsiuminestäjät, diureetit) (ks. kuva 1).
Kuva 1 -Suhteellinen riski (dronedaroni 400 mg kahdesti vuorokaudessa vs. lumelääke) – ensimmäinen sydän- ja verisuonisyistä johtuva sairaalahoitojakso tai mistä tahansa syystä johtuva kuolema.
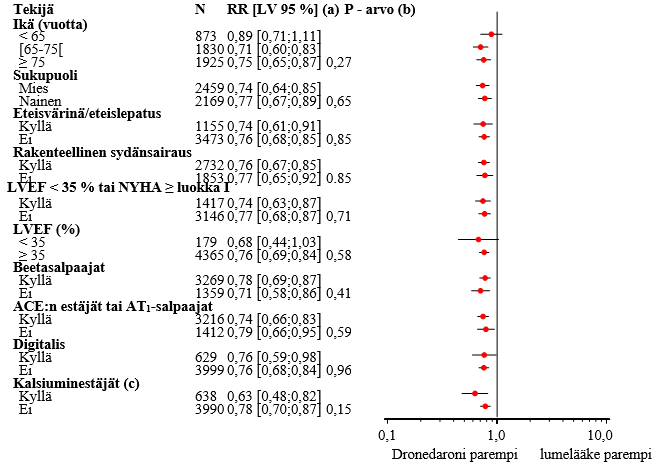
a Määritetty Coxin regressiomallin avulla
b Lähtötilanteen tekijöiden ja hoidon välisen interaktion P-arvo perustuu Coxin regressiomalliin
c Syketiheyttä pienentävät kalsiuminestäjät rajoitettu diltiatseemiin, verapamiiliin ja bepridiiliin
Tulokset olivat samantyyppisiä sydän- ja verisuonisyistä johtuvan sairaalahoidon ilmaantuvuuden osalta: riski pieneni 25,5 % (p < 0,0001).
Tutkimuksen aikana mistä tahansa syystä johtuneiden kuolemien määrä oli samaa luokkaa dronedaroniryhmässä (116 / 2 301) ja lumelääkeryhmässä (139 / 2 327).
Sinusrytmin säilyttäminen
EURIDIS- ja ADONIS-tutkimuksiin satunnaistettiin yhteensä 1 237 avohoitopotilasta, joilla oli ollut aiemmin eteisvärinä- tai eteislepatusjakso. Potilaat saivat hoidoksi joko dronedaronia 400 mg kahdesti vuorokaudessa (n = 828) tai lumelääkettä (n = 409) ja lisäksi tavanomaista hoitoa (esim. suun kautta otettavia antikoagulantteja, beetasalpaajia, ACE:n estäjiä tai AT1-salpaajia, verihiutaleiden toimintaa estäviä aineita pitkäaikaisesti, diureetteja, statiineja, digitalista tai kalsiuminestäjiä). Potilailla oli ollut vähintään yksi EKG:n avulla dokumentoitu eteisvärinä- tai eteislepatusjakso tutkimusta edeltäneiden 3 kuukauden aikana, heillä oli sinusrytmi vähintään yhden tunnin ajan, ja heitä seurattiin 12 kuukauden ajan. Amiodaronia saaneille potilaille tehtiin EKG-tutkimus noin 4 tunnin kuluttua ensimmäisestä lääkeannoksesta hyvän siedettävyyden varmistamiseksi. Muiden rytmihäiriölääkkeiden käyttö oli lopetettava vähintään viisi plasman puoliintumisaikaa ennen ensimmäistä lääkeannosta.
Potilaiden ikäjakauma oli 20–88 vuotta, ja suurin osa potilaista oli valkoihoisia (97 %) ja miehiä (69 %). Yleisimmät samanaikaiset sairaudet olivat hypertensio (56,8 %) ja rakenteellinen sydänsairaus (41,5 %), esim. sepelvaltimotauti (21,8 %).
EURIDIS- ja ADONIS-tutkimusten yhdistettyjen tulosten mukaan ja muissa yksittäisissä tutkimuksissa dronedaroni pidensi säännönmukaisesti eteisvärinän tai eteislepatuksen ensimmäiseen uusiutumiseen kulunutta aikaa (ensisijainen päätetapahtuma). Lumelääkkeeseen verrattuna dronedaroni pienensi 25 % (p = 0,00007) sitä riskiä, että eteisvärinä tai eteislepatus uusiutuisi ensimmäisen kerran 12 kuukauden tutkimusjakson aikana. Mediaaniaika satunnaistamisesta eteisvärinän tai eteislepatuksen ensimmäiseen uusiutumiseen oli dronedaroniryhmässä 116 päivää eli 2,2 kertaa niin pitkä kuin lumeryhmässä (53 päivää).
DIONYSOS-tutkimuksessa verrattiin dronedaronin (400 mg kahdesti vuorokaudessa) ja amiodaronin (600 mg vuorokaudessa 28 päivän ajan ja sen jälkeen 200 mg vuorokaudessa) tehokkuutta ja turvallisuutta 6 kuukauden ajan. Tutkimukseen satunnaistettiin 504 potilasta, joilla oli dokumentoitu eteisvärinä, ja heistä 249 sai dronedaronia ja 255 amiodaronia. Potilaiden ikäjakauma oli 28–90 vuotta ja 49 % oli yli 65-vuotiaita. Ensisijaisen tehokkuuspäätetapahtuman (eteisvärinän ensimmäinen uusiutuminen tai tutkimuslääkityksen ennenaikainen lopettaminen siedettävyysongelmien vuoksi tai lääkkeen tehottomuus) ilmaantuvuus 12 kuukauden kohdalla oli dronedaroniryhmässä 75 % ja amiodaroniryhmässä 59 % (riskisuhde = 1,59; log-rank, p-arvo < 0,0001). Eteisvärinä uusiutui dronedaroniryhmässä 63,5 prosentilla ja amiodaroniryhmässä 42 prosentilla potilaista. Eteisvärinän uusiutuminen (mukaan lukien normaalin sinusrytmin palautumisen puuttuminen) oli yleisempää dronedaroniryhmässä, mutta tutkimuslääkityksen ennenaikainen lopettaminen siedettävyysongelmien vuoksi oli yleisempää amiodaroniryhmässä. Pääasiallisen turvallisuuspäätetapahtuman (kilpirauhaseen, maksaan, keuhkoihin, hermostoon, ihoon, silmiin tai maha-suolikanavaan liittyvä haittatapahtuma tai tutkimuslääkityksen ennenaikainen lopettaminen minkä tahansa haittatapahtuman vuoksi) ilmaantuvuus oli dronedaroniryhmässä 20 % pienempi kuin amiodaroniryhmässä (p = 0,129). Tämä pienentyminen johtui siitä, että kilpirauhaseen ja hermostoon liittyviä tapahtumia ilmeni merkitsevästi vähemmän, ihoon ja silmiin liittyviä tapahtumia jonkin verran vähemmän, ja ennenaikaisia tutkimuslääkityksen lopettamisia vähemmän kuin amiodaroniryhmässä.
Dronedaroniryhmässä havaittiin enemmän ruoansulatuselimistön haittatapahtumia (12,9 % vs. 5,1 %), pääasiassa ripulia.
Potilaat, joilla on esiintynyt sydämen vajaatoiminnan oireita levossa tai lievässä rasituksessa edellisen kuukauden aikana tai jotka ovat olleet sairaalahoidossa sydämen vajaatoiminnan vuoksi edellisen kuukauden aikana
ANDROMEDA-tutkimukseen osallistui 627 potilasta, joilla oli vasemman kammion toimintahäiriöitä, jotka olivat olleet sairaalahoidossa sydämen vajaatoiminnan vuoksi (uusi diagnoosi tai pahenemisvaihe) ja joilla oli ollut vähintään yksi hengenahdistusjakso lievässä rasituksessa tai levossa (NYHA-luokka III tai IV) tai paroksysmaalinen yöllinen dyspnea osallistumista edeltäneen kuukauden aikana. Potilaiden ikäjakauma oli 27–96 vuotta ja 68 % oli yli 65-vuotiaita.
Tutkimus keskeytettiin ennenaikaisesti dronedaroniryhmässä havaitun kuolemien epätasapainon vuoksi (n = 25 dronedaroniryhmässä vs. 12 lumelääkeryhmässä, p = 0,027) (ks. kohdat Vasta-aiheet sekä Varoitukset ja käyttöön liittyvät varotoimet).
Potilaat, joilla on pysyvä eteisvärinä
PALLAS-tutkimus oli satunnaistettu, lumekontrolloitu tutkimus, jossa arvioitiin dronedaroniannoksen 400 mg x 2/vrk kliinistä hyötyä vakiintuneen hoidon lisänä potilaille, joilla oli pysyvä eteisvärinä ja sen lisäksi muita riskitekijöitä (potilailla oli kongestiivista sydämen vajaatoimintaa ~ 69 %, sepelvaltimotautia ~ 41 %, aiempi aivohalvaus tai TIA-kohtaus ~ 27 %; LVEF ≤ 40 % ~ 20.7 % tai potilaat olivat vähintään 75-vuotiaita verenpainetautia ja diabetestä sairastavia potilaita ~ 18 %). Tutkimus lopetettiin ennenaikaisesti sen jälkeen, kun siihen oli satunnaistettu 3 149 potilasta (lumelääke = 1 577; dronedaroni = 1 572), koska sydämen vajaatoimintatapausten (lumelääke = 33; dronedaroni = 80; HR = 2.49 (1.66-3.74)]; aivohalvausten [lumelääke = 8; dronedaroni = 17; HR = 2.14 (0.92-4.96)] ja kardiovaskulaaristen kuolemien [lumelääke = 6; dronedaroni = 15; HR = 2.53 (0.98-6.53)] määrät olivat merkitsevästi suurempia (ks. kohdat Vasta-aiheet ja Varoitukset ja käyttöön liittyvät varotoimet).
Farmakokinetiikka
Imeytyminen
Dronedaroni imeytyy hyvin (vähintään 70-prosenttisesti) suun kautta ruokailun yhteydessä otettuna. Alkureitin metabolian vuoksi dronedaronin absoluuttinen biologinen hyötyosuus (ruoan kanssa otettuna) on kuitenkin vain 15 %. Samanaikainen ruokailu suurentaa dronedaronin biologisen hyötyosuuden keskimäärin 2–4-kertaiseksi. Dronedaronin ja verenkierrossa tavattavan aktiivisen päämetaboliitin (N-debutyylimetaboliitti) huippupitoisuudet plasmassa saavutetaan suun kautta ruokailun yhteydessä otettuna 3–6 tunnissa. Kun dronedaronia annetaan toistuvasti 400 mg kahdesti vuorokaudessa, vakaa tila saavutetaan 4–8 hoitopäivässä ja dronedaronin keskimääräinen akkumulaatiosuhde on 2,6–4,5. Dronedaronin vakaan tilan keskimääräinen Cmax on 84–147 ng/ml, ja pääasiallisen N-debutyylimetaboliitin ja kantayhdisteen altistukset ovat keskenään samantyyppiset. Dronedaronin ja sen N-debutyylimetaboliitin farmakokinetiikka ei ole suoraan verrannollinen annoskokoon: kun annos suurennetaan 2-kertaiseksi, Cmax suurenee noin 2,5-kertaiseksi ja AUC noin 3-kertaiseksi.
Jakautuminen
Dronedaronista sitoutuu in vitro plasman proteiineihin 99,7 % ja sen N-debutyylimetaboliitista 98,5 %, eikä sitoutuminen ole saturoituvaa. Molemmat yhdisteet sitoutuvat pääasiassa albumiiniin. Laskimoon annetun annoksen jakautumistilavuus on vakaassa tilassa (Vss) 1 200–1 400 l.
Biotransformaatio
Dronedaroni metaboloituu laajasti pääasiassa CYP3A4:n kautta (ks. kohta Yhteisvaikutukset). Tärkeimpään metaboliareittiin kuuluu N-debutylaatio, jossa muodostuu pääasiallinen verenkierrossa tavattava aktiivinen metaboliitti. Tämän jälkeen metaboliitti hapettuu ja tapahtuu oksidatiivinen deaminaatio, jossa muodostuu inaktiivinen propionihappometaboliitti, mitä seuraa hapettuminen ja suora hapettuminen. Monoamiinioksidaasi osallistuu osittain dronedaronin aktiivisen metaboliitin metaboliaan (ks. kohta Yhteisvaikutukset).
N-debutyylimetaboliitti on farmakodynaamisesti aktiivinen, mutta se on 3–10 kertaa vähemmän potentti kuin dronedaroni. Tämä metaboliitti osallistuu dronedaronin farmakologiseen vaikutukseen ihmisellä.
Eliminaatio
Suun kautta otetusta merkitystä annoksesta noin 6 % erittyy virtsaan pääasiassa metaboliitteina (muuttumatonta yhdistettä ei erity virtsaan) ja 84 % erittyy ulosteeseen pääasiassa metaboliitteina. Laskimoon annetun dronedaronin plasmapuhdistuma on 130–150 l/h. Dronedaronin terminaalinen eliminaation puoliintumisaika on noin 25–30 tuntia ja sen N-debutyylimetaboliitin noin 20–25 tuntia. Potilailla dronedaroni ja sen metaboliitti eliminoituvat plasmasta täysin 2 viikon kuluessa hoidon päättymisestä, kun annostus on ollut 400 mg kahdesti vuorokaudessa.
Erityispotilasryhmät
Dronedaronin farmakokinetiikka eteisvärinäpotilailla on vastaava kuin terveillä tutkimushenkilöillä. Dronedaronin farmakokinetiikkaan vaikuttavia tekijöitä ovat sukupuoli, ikä ja paino. Kullakin näistä tekijöistä on rajallinen vaikutus dronedaroniin.
Sukupuoli
Naispotilailla dronedaronialtistus on keskimäärin 1,3-kertainen ja N-debutyylimetaboliittialtistus keskimäärin 1,9-kertainen miespotilaisiin verrattuna.
Iäkkäät potilaat
Kaikista dronedaronilla tehtyihin kliinisiin tutkimuksiin osallistuneista tutkimushenkilöistä 73 % oli vähintään 65-vuotiaita ja 34 % vähintään 75-vuotiaita. Vähintään 65-vuotiailla potilailla dronedaronialtistus on 23 % suurempi kuin alle 65-vuotiailla potilailla.
Maksan vajaatoiminta
Vapaan dronedaronin altistus suurenee 2-kertaiseksi henkilöillä, joilla on keskivaikea maksan vajaatoiminta. Keskimääräinen N-debutyylimetaboliitin altistus pienenee 47 % (ks. kohta Annostus ja antotapa).
Vaikean maksan vajaatoiminnan vaikutusta dronedaronin farmakokinetiikkaan ei ole arvioitu (ks. kohta Vasta-aiheet).
Munuaisten vajaatoiminta
Munuaisten vajaatoiminnan vaikutusta dronedaronin farmakokinetiikkaan ei ole tutkittu nimenomaisesti. Munuaisten vajaatoiminnan ei odoteta muuttavan dronedaronin farmakokinetiikkaa, koska virtsaan ei erity muuttumatonta yhdistettä ja vain noin 6 % annoksesta erittyy virtsaan metaboliitteina (ks. kohta Annostus ja antotapa).
Prekliiniset tiedot turvallisuudesta
Yhden hiirillä tehdyn in vivo -mikrotumatestin ja neljän in vitro -tutkimuksen perusteella dronedaronilla ei ole genotoksisia vaikutuksia.
Kaksi vuotta kestäneissä karsinogeenisuustutkimuksissa, joissa dronedaronia annettiin eläimille suun kautta, suurin 24 kuukauden ajan annettu dronedaroniannos oli 70 mg/kg/vrk rotille ja 300 mg/kg/vrk hiirille.
Pelkästään suurimman tutkitun annoksen (vastaa 5–10-kertaisesti ihmisen hoitoannoksen altistusta) yhteydessä havaittiin maitorauhaskasvainten lisääntymistä naarashiirillä, histiosyyttisarkoomien lisääntymistä hiirillä ja suoliliepeen imusolmukkeiden hemangioomien lisääntymistä rotilla. Hemangioomat eivät ole syövän esiasteita eivätkä ne muutu pahanlaatuisiksi hemangiosarkoomiksi eläimillä eivätkä ihmisellä. Näiden havaintojen ei katsota liittyvän ihmiseen.
Pitkäaikaistoksisuustutkimuksissa havaittiin lievää ja korjautuvaa fosfolipidoosia (vaahtosolu-makrofagien kertymistä) suoliliepeen imusolmukkeissa pääasiassa rotalla. Tämän vaikutuksen katsotaan liittyvän vain rottaan, eikä sen katsota koskevan ihmistä.
Dronedaroni vaikutti rotalla suurina annoksina huomattavasti alkion- ja sikiönkehitykseen ja aiheutti mm. alkionmenetyksiä munasolun kiinnittymisen jälkeen, sikiön ja istukan painon pienenemistä sekä ulkoisia epämuodostumia ja sisäelinten ja luuston epämuodostumia.
Farmaseuttiset tiedot
Apuaineet
Tablettiydin:
Hypromelloosi (E 464)
Maissitärkkelys
Krospovidoni (E 1202)
Poloksameeri 407
Laktoosimonohydraatti
Kolloidinen vedetön piidioksidi
Magnesiumstearaatti (E 572)
Tabletin päällyste:
Hypromelloosi (E 464)
Makrogoli 6000
Titaanidioksidi (E 171)
Karnaubavaha (E 903)
Yhteensopimattomuudet
Ei oleellinen.
Kestoaika
3 vuotta.
Säilytys
Tämä lääkevalmiste ei vaadi erityisiä säilytysolosuhteita.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
MULTAQ tabletti, kalvopäällysteinen
400 mg (L:kyllä) 100 x 1 fol (81,54 €)
PF-selosteen tieto
- Läpinäkymätön PVC/alumiiniläpipainopakkaus 20, 50 ja 60 kalvopäällysteisen tabletin pakkauksessa
- Läpinäkymätön, yksittäispakattu PVC/alumiiniläpipainopakkaus 100 x 1 kalvopäällysteisen tabletin pakkauksessa.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Valmisteen kuvaus:
Valkoinen, pitkänomainen tabletti, jonka toiselle puolelle on kaiverrettu kaksoisaalto ja toiselle puolelle koodi ”4142”.
Käyttö- ja käsittelyohjeet
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
MULTAQ tabletti, kalvopäällysteinen
400 mg 100 x 1 fol
- Rajoitettu peruskorvaus lääkärin lausunnolla (40 %). Dronedaroni: Eteisvärinän estohoito erityisin edellytyksin (342).
ATC-koodi
C01BD07
Valmisteyhteenvedon muuttamispäivämäärä
11.07.2024
Yhteystiedot
Revontulenkuja 1
02100 Espoo
0201 200 300
www.sanofi.fi

 SANOFI OY
SANOFI OY