SCOPODERM depotlaastari 1 mg/72 h
Vaikuttavat aineet ja niiden määrät
Yksi Scopoderm 1 mg/72 t depotlaastari sisältää 1,3 mg skopolamiinia 2,5 cm2:n kokoisessa laastarissa. Yksi laastari vapauttaa noin 1 mg skopolamiinia 72 tunnin kuluessa.
Hyoskiini on vaikuttavan aineen nimi Euroopan farmakopeassa (Ph.Eur.).
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Depotlaastari.
Kliiniset tiedot
Käyttöaiheet
Matkapahoinvoinnin ja merisairauden oireiden, kuten kiertohuimauksen, pahoinvoinnin ja oksentamisen esto.
Annostus ja antotapa
Annostus
Optimaalisen suojaavan vaikutuksen saamiseksi yksi Scopoderm-depotlaastari asetetaan noin 5–6 tuntia ennen matkan alkua (tai edellisenä iltana) puhtaalle, kuivalle, karvattomalle alueelle korvan taakse (ks. Käyttöohjeet). Yksi Scopoderm-depotlaastari tarjoaa riittävän suojan matkapahoinvointia vastaan 72 tunnin ajaksi. Jos laastaria tarvitaan tätä lyhyempi aika, se pitää poistaa matkan lopussa. Jos tarvitaan pitempiaikaista hoitoa, on laastari poistettava 72 tunnin kuluttua asettamisesta ja uusi laastari kiinnitettävä toisen korvan taakse.
Pediatriset potilaat
10‑vuotiaat ja sitä vanhemmat lapset voivat käyttää Scopoderm-depotlaastaria. Valmisteen turvallisuutta ja tehoa alle 10 vuoden ikäisten lasten hoidossa ei ole varmistettu.
Iäkkäät
Iäkkäät voivat käyttää Scopoderm-depotlaastaria (ks. aikuisia koskevat suositukset), tosin he saattavat olla muunikäisiä alttiimpia skopolamiinin haittavaikutuksille (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Potilaat, joilla on maksan tai munuaisten vajaatoiminta
Varovaisuutta on noudatettava käytettäessä Scoperm-depotlaastaria potilailla, joilla on maksan tai munuaisen vajaatoiminta (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet.)
Antotapa
Käyttöohjeet
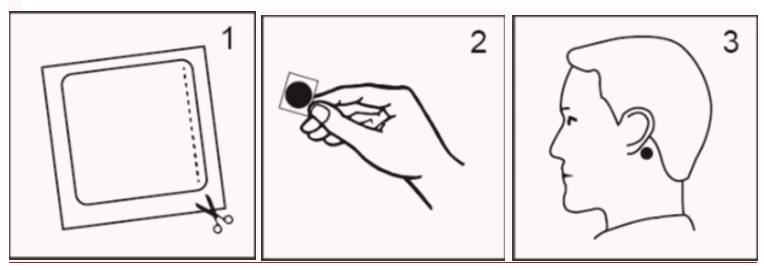
- Leikkaa katkoviivaa pitkin ja ota ulos kellanruskea laastari, jossa on päällä läpinäkyvä neliönmuotoinen suojakalvo (kuva 1).
- Pidä laastaria kiinni kulmasta ja poista neliönmuotoinen suojakalvo. Yritä olla koskematta keskellä olevaa hopeanväristä liimapintaa (kuva 2).
- Paina laastari (hopeanvärinen liimapinta alaspäin) tiiviisti vasten korvan takana olevaa puhdasta, kuivaa ja karvatonta ihoaluetta (kuva 3).
Iholle kiinnitetyn laastarin koskettelemista tulee välttää, koska siihen kohdistuva paine saattaa aiheuttaa vaikuttavan aineen tihkumisen laastarin reunoilta.
Jotta vältettäisiin vaikuttavan aineen jäämien joutuminen silmiin – tämä saattaa aiheuttaa lievää tilapäistä näön hämärtymistä ja pupillien laajenemista (joskus vain toisessa silmässä) – kädet on aina pestävä laastarin käsittelemisen jälkeen.
Myös laastarin kiinnityskohta iholla on hoidon jälkeen pestävä.
Scopoderm-depotlaastari kiinnittyy yleensä hyvin. Jos se irtoaa vahingossa, se on korvattava uudella. Scopoderm-depotlaastaria voidaan käyttää kylvyn ja suihkun aikana.
Käytetyt laastarit taitetaan kokoon ja hävitetään niin, etteivät lapset pääse niihin käsiksi.
Vasta-aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille. Glaukooma.
Varoitukset ja käyttöön liittyvät varotoimet
Scopoderm-depotlaastaria on käytettävä erityistä varovaisuutta noudattaen pylorusobstruktiopotilaille ja potilaille, joilla virtsan tulo on estynyt, esim. prostatan sairauksissa, tai joilla on suoliston obstruktio.
Varovaisuutta on noudatettava myös iäkkäiden potilaiden ja metaboliahäiriöistä tai maksan tai munuaisten vajaatoiminnasta kärsivien potilaiden hoidossa.
Jos potilaalla on aiemmin ilmennyt silmänpaineen kohoamista (painekipu, näön hämärtyminen, halo glaucomatosus), Scopoderm-depotlaastaria ei tule käyttää ennen kuin potilaalle on tehty oftalmologinen tutkimus.
Harvoin voi esiintyä sekavuustiloja ja/tai näköharhoja. Näissä tapauksissa Scopoderm-depotlaastari on heti poistettava. Jos oireet tästä huolimatta jatkuvat vaikeina, tarvittaviin hoitotoimenpiteisiin on ryhdyttävä esim. antamalla fysostigmiiniä hitaasti laskimoon 1–4 mg (lapsille 0,5 mg). Tämä voidaan tarvittaessa toistaa.
Yksittäisissä tapauksissa epileptikoilla on raportoitu kohtausten lisääntymistä.
Idiosynkraattisia reaktioita voi esiintyä tavanomaisilla terapeuttisilla skopolamiiniannoksilla.
Varovaisuutta on noudatettava laastarin poistamisen jälkeen, sillä haittavaikutukset voivat jatkua vielä yli 24 tunnin ajan laastarin poistamisen jälkeen.
Valmisteen sisältämän alumiinin vuoksi laastari poistetaan ennen lääketieteellistä kuvantamista.
Kädet on pestävä huolellisesti Scopoderm-depotlaastarin käsittelyn jälkeen. Myös laastarin kiinnityskohta iholla on pestävä huolellisesti laastarin poistamisen jälkeen.
Älä käytä useampaa kuin yhtä laastaria kerrallaan.
Yhteisvaikutukset
Skopolamiinia tulee antaa varoen potilaille, jotka saavat keskushermostoon vaikuttavia lääkkeitä. Tämä koskee erityisesti niitä potilaita, jotka saavat antikolinergistä lääkitystä, esim. muita belladonna-alkaloideja, antihistamiineja, trisyklisiä masennuslääkkeitä (kuten amitriptyliini tai imipramiini), amantadiinia tai kinidiiniä.
Alkoholin käytöstä pidättäytymistä suositellaan Scopoderm-depotlaastarin käytön ajaksi.
Raskaus ja imetys
Raskaus
Skopolamiinin mahdollisista vaikutuksista raskaus- tai imetysaikana ei ole kontrolloituja tutkimuksia. Hiirillä ja rotilla tehdyt non-kliiniset tutkimukset eivät ole osoittaneet lisääntymis- tai kehityshäiriöitä annoksilla, jotka ovat verrattavissa suositeltuun kliiniseen annokseen (ks. kohta Prekliiniset tiedot turvallisuudesta).
Vaikuttava aine, skopolamiini, läpäisee istukan helposti. Raskaana olevien on otettava yhteyttä lääkäriin ennen tämän lääkkeen käyttöä.
Imetys
Koska skopolamiini erittyy ihmisen rintamaitoon, vaikkakin vain erittäin pieninä määrinä, Scopoderm-depotlaastarin käytössä imettäville naisille tulee noudattaa varovaisuutta. Imettävien potilaiden on otettava yhteyttä lääkäriin ennen tämän lääkkeen käyttöä.
Hedelmällisyys
Hedelmällisyystutkimuksissa, joissa naarasrotille pistettiin päivittäin skopolamiinihydrobromidia nahan alle, ei ilmennyt hedelmällisyyden heikkenemistä eikä sikiöhaittoja. Emojen ruumiinpaino pieneni suurinta annosta saaneessa ryhmässä (pitoisuus plasmassa oli noin 500 kertaa suurempi kuin pitoisuus, joka saavutetaan ihmisellä skopolamiinidepotlaastaria käytettäessä).
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Scopoderm-depotlaastari voi aiheuttaa uneliaisuutta tai näköhäiriöitä ja harvoin myös muita keskushermostoperäisiä haittavaikutuksia (ks. kohta Haittavaikutukset), jotka voivat vaikuttaa haitallisesti potilaan reaktiokykyyn. Potilaita tulee varoittaa tästä mahdollisuudesta ja kehottaa heitä noudattamaan varovaisuutta tarkkuutta vaativissa tehtävissä, kuten autonajossa tai koneiden käytössä.
Haittavaikutukset
Scopodermin haittavaikutukset johtuvat pääasiassa skopolamiinin antikolinergisistä vaikutuksista.
Haittavaikutukset on ryhmitelty elinjärjestelmän ja yleisyyden mukaan seuraavaa luokittelua käyttäen:
hyvin yleiset (≥ 1/10), yleiset (≥ 1/100, < 1/10), melko harvinaiset (≥ 1/1 000, < 1/100), harvinaiset (≥ 1/10 000, < 1/1 000), hyvin harvinaiset (< 1/10 000), tuntematon (koska saatavissa oleva tieto ei riitä arviointiin). Yleisyysryhmissä haittavaikutukset on esitetty vakavuuden mukaisesti alenevassa järjestyksessä.
Taulukko 1 Luettelo haittavaikutuksista
| Elinryhmä | Haittavaikutus | Yleisyys |
| Psyykkiset häiriöt | Desorientaatio, sekavuus ja hallusinaatiot | Harvinaiset |
| Hermosto | Uneliaisuus, heitehuimaus | Hyvin yleiset |
| Muistihäiriöt, keskittymiskyvyn heikkeneminen, levottomuus | Harvinaiset | |
| Agitaatio, koordinaatiohäiriöt, päänsärky | Tuntematon | |
| Silmät | Akkommodaatiohäiriöt (sykloplegia), mukaan lukien näkökyvyn hämärtyminen, myopia ja mydriaasi (joskus vain toisessa silmässä) | Hyvin yleiset |
| Silmäluomien ärsytys | Yleiset | |
| Ahdaskulmaglaukooma | Hyvinharvinaiset | |
| Ruoansulatuselimistö | Suun kuivuminen | Hyvin yleiset |
| Iho ja ihonalainen kudos | Ihoärsytys | Yleiset |
| Yleistynyt ihottuma | Hyvin harvinaiset | |
| Kiinnityskohdan reaktiot, mukaan lukien ihottuma, kutina, punoitus ja polttelu | Tuntematon | |
| Munuaiset ja virtsatiet | Virtsaretentio | Harvinaiset |
Scopoderm-depotlaastarin käytön lopettamiseen liittyviä haittavaikutuksia
Hoidon keskeyttämisen jälkeen – tavallisesti useampia päiviä jatkuneen käytön yhteydessä – on harvinaisina raportoitu mm. heitehuimausta, pahoinvointia, oksentamista, päänsärkyä ja tasapainohäiriöitä.
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haitta-tasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Suurten skopolamiiniannosten keskeiset vaikutukset muistuttavat atropiinin vaikutuksia. Ne alkavat levottomuutena, kiihotustiloina ja sekavuutena. Suuremmilla annoksilla ilmenee äkillisiä sekavuustiloja (delirium), hallusinaatioita ja kouristuksia. Erittäin suurilla annoksilla kooma ja hengityshalvaus.
Hoito
Poista kaikki laastarit välittömästi, sillä jotkut yliannostusoireet voivat jatkua jopa yli 24 tuntia laastarin poistamisen jälkeenkin.
Tehokkain antidootti on fysostigmiini, jota injisoidaan hitaasti laskimoon, oireiden vaikeusasteesta riippuen aikuisille 1–4 mg (lapsille 0,5 mg). Koska fysostigmiini metaboloituu nopeasti, potilas saattaa vajota uudelleen koomaan 1–2 tunnin kuluessa, jolloin fysostigmiini-injektio tulee uusia. Kohtalaisen pienet diatsepaamiannokset voivat olla hyödyllisiä kiihotustiloissa ja kouristuksissa. Suurempia annoksia tulee välttää, koska hengitysdepressio voi lisääntyä. Vaikeissa tapauksissa tekohengitys voi olla tarpeen. Mikäli hypertermiaa esiintyy, liikalämpöä tulee kiireellisesti pyrkiä poistamaan (kylmät kylvyt).
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Pahoinvointilääkkeet, ATC-koodi: A04AD01
Vaikutusmekanismi
Skopolamiinin kyky estää matkapahoinvoinnista ja merisairaudesta johtuvaa pahoinvointia ja oksentamista saattaa olla yhteydessä siihen, että kolinergisen impulssin johtuminen vestibulaarisesta keskuksesta keskushermoston ylempiin keskuksiin sekä retikulaariformaatiosta oksetuskeskukseen estyy.
Farmakodynaamiset vaikutukset
Scopoderm-depotlaastarin vaikuttava aine on luonnossa esiintyvä belladonna-alkaloidi, skopolamiini, jonka farmakologiset vaikutukset tunnetaan hyvin. Parasympatolyyttinä skopolamiini kilpailevasti estää asetyylikoliinin (ja muiden suoraan vaikuttavien parasympatomimeettien) vaikutusta muskariinireseptoreissa, ja sen vaikutus voidaan kumota suurilla parasympatomimeettiannoksilla. Skopolamiinin vaikutus riippuu kohde-elinten herkkyydestä ja annoksen koosta. Terapeuttisina annoksina skopolamiini heikentää liiketoimintoja, aiheuttaa uneliaisuutta, estää syljeneritystä ja hikoilua sekä aiheuttaa pupillien laajenemista.
Farmakokinetiikka
Imeytyminen
Imeytyneen ja eliminoituneen vaikuttavan aineen välinen tasapaino saavutetaan noin 6 tunnin kuluttua Scopoderm-depotlaastarin kiinnittämisestä iholle. Depotlaastarista ihon läpi imeytyvän skopolamiinin vakaan tilan pitoisuus plasmassa on 0,17–0,33 nmol/l. Tasapaino säilyy 72 tuntia, ellei laastaria poisteta.
Jakautuminen
Skopolamiinin jakautumisesta on saatavilla vain vähän tietoa. Lääkeaine jakautuu kuitenkin hyvin ja pääsee keskushermostoon. Skopolamiini näyttäisi sitoutuvan plasman proteiineihin palautuvalla mekanismilla.
Biotransformaatio
Skopolamiinin metaboliaa ei ole täysin karakterisoitu. Lääkeaine vaikuttaisi metaboloituvan maksassa (glukuronidi- tai sulfaattikonjugaatiolla).
Eliminaatio
Laastarin poistamisen jälkeen elimistössä olevan vaikuttavan aineen määrä laskee seuraavan 24 tunnin aikana hitaasti noin yhteen kolmasosaan, koska ihossa vielä oleva skopolamiini siirtyy edelleen verenkiertoon. Skopolamiini erittyy virtsaan. Yhden skopolamiinidepotlaastarin käytön jälkeen virtsan mukana erittyvän vapaan skopolamiinin määrä on noin 0,7 mikrog/h ja erittyvän skopolamiinin kokonaismäärä (vapaa sekä konjugoitunut) on noin 3,8 mikrog/h. . Alle 10 % kokonaismäärästä erittyy virtsaan muuntumattomana lääkeaineena sekä lääkeaineen metaboliitteina 108 tunnin kuluessa. Kahden laastarin yksittäisen käytön jälkeen lääkeaineen (vapaan skopolamiinin) eliminaation puoliintumisaika oli 9,5 h.
Prekliiniset tiedot turvallisuudesta
Toistuvan altistuksen aiheuttamaa toksisuutta, ihoärsytystä, geenitoksisuutta, karsinogeenisuutta sekä lisääntymistoksisuutta koskevien konventionaalisten tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille. Marginaalinen embryotoksinen vaikutus havaittiin kaneilla skopolamiinihydrobromidin päivittäisen laskimonsisäisen annostelun jälkeen, annoksen ollessa noin satakertainen depotlaastareista saatuihin annostasoihin nähden. Rotilla ei kirjattu haittavaikutuksia lisääntymistoksisuustutkimuksissa laskimonsisäisen annostelun jälkeen.
Farmaseuttiset tiedot
Apuaineet
Laastarin ulkopinta
Aluminoitu polyesterikalvo
Lääkesäiliö ja laastarin liimapinta
Krospovidoni
Isopropyylipalmitaatti
Kevyt nestemäinen parafiini
Polyisobuteeni
Imeytymisnopeutta säätelevä kalvo
Etyleenivinyyliasetaattikopolymeeri
Liimapinnan suojakalvo
Polyesteri
Yhteensopimattomuudet
Ei oleellinen.
Kestoaika
3 vuotta.
Säilytys
Säilytä alle 25 °C.
Älä irrota laastarin suojakalvoa ennen kuin tarvitset laastaria.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
SCOPODERM depotlaastari
1 mg/72 h (L:ei) 5 kpl (48,59 €)
PF-selosteen tieto
Laastarit on pakattu litteään, suljettuun foliolla vuorattuun pussiin. Ulkopakkaus koostuu pahvista ja sisältää ohjeet.
Pussin materiaali on PET-muovin, matalatiheyksisen polyetyleenin, päällystetyn alumiinikalvon ja kuivausainekalvon laminaattia.
Valmisteen kuvaus:
Litteä, pyöreä säiliölaastari, jonka halkaisija on 1,8 cm. Laastarin toinen puoli on kellanruskea, toinen hopeanvärinen, ja sen päällä on suurempi neliönmuotoinen, läpinäkyvä suojakalvo.
Käyttö- ja käsittelyohjeet
Depotlaastarit tulee taittaa puoliksi (liimapinnat vastakkain) ennen hävittämistä. Käytetyt laastarit taitetaan kokoon ja hävitetään niin, etteivät lapset pääse niihin käsiksi. Laastaria ei saa leikata.
Depotlaastarien käsittelyn jälkeen kädet on pestävä huolellisesti. Myös laastarin irrottamisen jälkeen laastarin kiinnityskohta iholla on pestävä. Nämä varotoimet ovat välttämättömiä, jotta voidaan minimoida skopolamiinin joutuminen silmiin (ks. kohta Haittavaikutukset).
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
SCOPODERM depotlaastari
1 mg/72 h 5 kpl
- Ei korvausta.
ATC-koodi
A04AD01
Valmisteyhteenvedon muuttamispäivämäärä
01.10.2025
Yhteystiedot
Karhumäentie 3
01530 Vantaa
0800 144 233
