OCREVUS injektioneste, liuos 920 mg
Vaikuttavat aineet ja niiden määrät
Yksi injektiopullo sisältää 920 mg okrelitsumabia 23 ml:ssa (40 mg/ml).
Okrelitsumabi on kiinanhamsterin munasarjasoluissa yhdistelmä-DNA-tekniikalla tuotettu humanisoitu monoklonaalinen vasta-aine.
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Injektioneste, liuos.
Kliiniset tiedot
Käyttöaiheet
Ocrevus on tarkoitettu aaltomaisen MS-taudin (RMS) hoitoon aikuispotilailla, joilla on kliinisten piirteiden tai kuvantamislöydösten perusteella määriteltyä MS-taudin aktiivisuutta (ks. kohta Farmakodynamiikka).
Ocrevus on tarkoitettu varhaisvaiheen primaaristi etenevän MS-taudin (PPMS) hoitoon aikuispotilailla määriteltynä taudin keston ja toimintakykytason sekä tulehdusaktiivisuudelle tyypillisten kuvantamislöydösten perusteella (ks. kohta Farmakodynamiikka).
Ehto
Hoito aloitetaan ja toteutetaan neurologisten sairauksien diagnosointiin ja hoitoon perehtyneen erikoislääkärin valvonnassa. Ensimmäisellä antokerralla edellytetään asianmukaista kliinistä tarkkailua yksikössä, jossa on tarvittavat valmiudet vaikeiden haittavaikutusten, kuten vaikea-asteisten injektioreaktioiden, yliherkkyys- ja/tai anafylaktisten reaktioiden hoitamiseen.
Annostus ja antotapa
Hoito aloitetaan ja toteutetaan neurologisten sairauksien diagnosointiin ja hoitoon perehtyneen erikoislääkärin valvonnassa. Ensimmäisellä antokerralla edellytetään asianmukaista kliinistä tarkkailua yksikössä, jossa on tarvittavat valmiudet vaikeiden haittavaikutusten, kuten vaikea-asteisten injektioreaktioiden, yliherkkyys- ja/tai anafylaktisten reaktioiden hoitamiseen (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Esilääkitys injektioreaktioiden varalta
Potilaalle on annettava seuraavat kaksi esilääkitystä juuri ennen jokaista okrelitsumabi-injektiota vähentämään paikallisten ja systeemisten injektioreaktioiden riskiä:
- 20 mg deksametasonia suun kautta (tai vastaavaa)
- antihistamiinia suun kautta (esim. desloratadiinia tai vastaavaa).
Esilääkitykseksi voidaan lisäksi harkita jotakin kuumetta alentavaa lääkettä (esim. parasetamolia) juuri ennen jokaisen injektion antoa.
Annostus
Suositeltu annos on 920 mg kuuden kuukauden välein.
Alkuannosta tai seuraavia annoksia ei tarvitse jakaa erillisiin injektioihin.
Okrelitsumabiannosten välisen ajan pitää olla aina vähintään viisi kuukautta.
Injisoinnin tai hoidon lopettaminen injektioreaktion yhteydessä
Henkeä uhkaavat injektioreaktiot
Jos henkeä uhkaavan injektioreaktion oireita ilmenee, injektion antaminen on lopetettava välittömästi ja potilaalle on annettava asianmukaista hoitoa. Näiden potilaiden hoito on lopetettava pysyvästi (ks. kohta Vasta-aiheet).
Vaikea-asteiset injektioreaktiot
Jos potilaalle ilmaantuu vaikea-asteinen injektioreaktio, injektion antaminen on keskeytettävä välittömästi ja potilaalle on annettava oireenmukaista hoitoa. Injektio voidaan antaa loppuun vasta, kun kaikki oireet ovat hävinneet (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Annosten viivästyminen tai antamatta jääminen
Jos injektio jää antamatta, se on annettava mahdollisimman pian. Älä odota seuraavaa suunniteltua antoajankohtaa. Annosten välisen ajan tulisi olla kuusi kuukautta, kuitenkin vähintään viisi kuukautta.
Erityispotilasryhmät
Yli 55-vuotiaat aikuiset
Laskimoon annettavasta okrelitsumabista saatavissa olevien rajallisten tietojen perusteella (ks. kohdat Farmakodynamiikka ja Farmakokinetiikka) yli 55-vuotiaiden potilaiden annostusta ei tarvitse muuttaa. Käynnissä oleviin kliinisiin tutkimuksiin mukaan otetut potilaat jatkavat 55 vuotta täytettyään okrelitsumabihoitoa laskimoon annettavin 600 mg:n annoksin kuuden kuukauden välein. Ihon alle annettavaa okrelitsumabia ei ole tutkittu yli 65‑vuotiailla potilailla.
Munuaisten vajaatoiminta
Okrelitsumabin turvallisuutta ja tehoa ei ole virallisesti tutkittu potilailla, joilla on munuaisten vajaatoiminta. Kliinisissä tutkimuksissa oli mukana lievää munuaisten vajaatoimintaa sairastavia potilaita. Keskivaikeaa ja vaikeaa munuaisten vajaatoimintaa sairastavista potilaista ei ole kokemusta. Okrelitsumabi on monoklonaalinen vasta-aine, ja se poistuu elimistöstä kataboloitumalla (eli hajoamalla peptideiksi ja aminohapoiksi), joten annoksen säätäminen ei oletettavasti ole munuaisten vajaatoimintaa sairastaville potilaille tarpeen (ks. kohta Farmakokinetiikka).
Maksan vajaatoiminta
Okrelitsumabin turvallisuutta ja tehoa ei ole virallisesti tutkittu potilailla, joilla on maksan vajaatoiminta. Kliinisissä tutkimuksissa oli mukana lievää maksan vajaatoimintaa sairastavia potilaita. Keskivaikeaa ja vaikeaa maksan vajaatoimintaa sairastavista potilaista ei ole kokemusta. Okrelitsumabi on monoklonaalinen vasta-aine, ja se poistuu elimistöstä kataboloitumalla (ei niinkään maksan kautta metaboloitumalla), joten annoksen säätäminen ei oletettavasti ole maksan vajaatoimintaa sairastaville potilaille tarpeen (ks. kohta Farmakokinetiikka).
Pediatriset potilaat
Okrelitsumabin turvallisuutta ja tehoa 0–18 vuoden ikäisten lasten ja nuorten hoidossa ei ole vielä varmistettu. Tietoja ei ole saatavilla.
Antotapa
Ocrevus 920 mg injektioneste, liuos ei ole tarkoitettu annettavaksi laskimoon. Sitä pitää aina antaa injektiona ihon alle terveydenhuollon ammattilaisen toimesta.
On tärkeää varmistaa valmisteen etiketistä, että potilaalle annetaan lääkemääräyksen mukaista oikeaa lääkemuotoa oikean antoreitin kautta (laskimoon tai ihon alle).
Potilaan hoito voidaan aloittaa laskimoon annettavalla tai ihon alle annettavalla okrelitsumabilla. Okrelitsumabia laskimoon annettavana hoitona parhaillaan saavien potilaiden hoitoa voidaan jatkaa laskimoon annettavalla okrelitsumabilla tai heille voidaan vaihtaa ihon alle annettava Ocrevus 920 mg injektioneste -valmiste.
920 mg:n annos annetaan noin 10 minuutin kestoisena injektiona vatsan ihon alle. Ihonalaiseen antoon tarkoitettujen infuusiovälineiden (esim. siipi-/perhosneula) käyttöä suositellaan. Ihonalaiseen antoon tarkoitettuihin infuusiovälineisiin jäävää jäännöstilavuutta ei saa antaa potilaalle.
Injektio pitää antaa vatsan alueelle vähintään 5 cm:n etäisyydelle navasta. Injektioita ei saa koskaan antaa ihoalueille, joilla on punoitusta, mustelma, aristusta tai kovettuma, eikä alueille, joilla on luomia tai arpia.
Ocrevus injektioneste annostellaan aina terveydenhuollon ammattilaisen toimesta. Aloitusannoksen yhteydessä suositellaan potilaan seurantaa vähintään yhden tunnin ajan injektion jälkeen. Hoitopaikassa pitää olla tarvittavat valmiudet vaikeiden haittavaikutusten, kuten injektioreaktioiden hoitamiseen. Seuraavien annosten yhteydessä injektion jälkeinen seurannan tarve perustuu hoitavan lääkärin harkintaan (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Lääkevalmisteen käyttö- ja käsittelyohjeet ennen lääkkeen antoa, ks. kohta Käyttö- ja käsittelyohjeet.
Vasta-aiheet
- Yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille.
- Parhaillaan sairastettava aktiivinen infektio (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
- Potilaalla oleva vaikea-asteinen immuunipuutostila (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
- Tiedossa oleva aktiivinen syöpä (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Varoitukset ja käyttöön liittyvät varotoimet
Jäljitettävyys
Biologisten lääkevalmisteiden jäljitettävyyden parantamiseksi on annetun valmisteen nimi ja eränumero dokumentoitava selkeästi.
Injektioreaktiot
Ihon alle annettavaan okrelitsumabihoitoon liittyy injektioreaktioita, jotka saattavat olla yhteydessä sytokiinien vapautumiseen ja/tai muihin kemiallisiin välittäjäaineisiin. Lääkärin pitää kertoa potilaalle, että injektioreaktioita voi ilmetä injektion annon aikana tai sen jälkeen 24 tunnin kuluessa. Injektioreaktioiden oireita on raportoitu yleisemmin ensimmäisen injektion yhteydessä. Injektioreaktiot voivat olla paikallisia tai systeemisiä injektioreaktioita. Pistoskohdan paikallisten injektioreaktioiden yleisiä oireita ovat eryteema, kipu, turvotus ja kutina. Systeemisten injektioreaktioiden yleisiä oireita ovat päänsärky ja pahoinvointi (ks. kohta Haittavaikutukset).
Potilaille pitää antaa esilääkitys juuri ennen injektiota injektioreaktioiden riskin vähentämiseksi (ks. kohta Annostus ja antotapa). Potilaita pitää tarkkailla ensimmäisen lääkevalmisteannoksen jälkeen vähintään tunnin ajan vaikea-asteisen injektioreaktion oireiden havaitsemiseksi. Ensimmäistä lääkevalmisteannosta annettaessa on oltava saatavilla asianmukaiset edellytykset vaikea-asteisten injektioreaktioiden, yliherkkyysreaktioiden ja/tai anafylaktisten reaktioiden hoitoon. Seuraavien annosten yhteydessä soveltuva hoitopaikka (esim. klinikka tai koti) ja seuranta injektion jälkeen perustuvat hoitavan lääkärin harkintaan. Jos injektioreaktioita ilmaantuu, ne voidaan hoitaa oireenmukaisella hoidolla.
Henkeä uhkaavan injektioreaktion oireiden ilmetessä injektion antaminen pitää lopettaa välittömästi ja potilaalle pitää antaa asianmukaista hoitoa. Näiden potilaiden okrelitsumabihoito on lopetettava pysyvästi. Jos potilaalle ilmaantuu vaikea-asteinen injektioreaktio, injektion antaminen pitää keskeyttää välittömästi ja potilaalle pitää antaa oireenmukaista hoitoa. Injektio voidaan antaa loppuun vasta, kun kaikki oireet ovat hävinneet.
Laskimoon annettavaan okrelitsumabihoitoon liittyy infuusioreaktioita, jotka saattavat olla yhteydessä sytokiinien vapautumiseen ja/tai muihin kemiallisiin välittäjäaineisiin. Infuusioreaktiot saattavat ilmetä kutinana, ihottumana, urtikariana, eryteemana, kurkun ärsytyksenä, suunielun kipuna, hengenahdistuksena, nielun tai kurkunpään turvotuksena, kaulan ja kasvojen punoituksena, hypotensiona, kuumeena, uupumuksena, päänsärkynä, heitehuimauksena, pahoinvointina, takykardiana ja anafylaksiana. Laskimoon annettavan okrelitsumabin käytössä on raportoitu vakavia infuusioreaktioita, joista osa on vaatinut sairaalahoitoa.
Yliherkkyyttä saattaa olla mahdotonta erottaa kliinisesti injektioreaktiosta tai infuusioreaktiosta oireiden perusteella. Jos yliherkkyysreaktiota epäillään, injektion antaminen on lopetettava välittömästi pysyvästi (ks. jäljempänä Yliherkkyysreaktiot).
Yliherkkyysreaktiot
Yliherkkyysreaktioita (akuutti allerginen reaktio lääkevalmisteelle) voi myös ilmetä. Tyypin 1 (IgE‑välitteiset) akuutit yliherkkyysreaktiot eivät välttämättä ole kliinisesti erotettavissa injektioreaktioista.
Yliherkkyysreaktio voi ilmaantua minkä tahansa antokerran yhteydessä, mutta tyypillisesti niitä ei esiinny ensimmäisellä antokerralla. Seuraavilla antokerroilla aiempaa vaikeampiasteisten tai uudenlaisten vaikeiden oireiden ilmaantuessa on syytä huomioida yliherkkyysreaktion mahdollisuus. Potilasta, jolla tiedetään olevan IgE‑välitteinen yliherkkyys okrelitsumabille tai jollekin apuaineelle, ei saa hoitaa (ks. kohta Vasta-aiheet).
Infektiot
Jos potilaalla on aktiivinen infektio, okrelitsumabin antamista pitää siirtää myöhemmäksi, kunnes infektio on parantunut.
Potilaan immuniteetin tila suositellaan varmistamaan ennen infuusion antoa potilaalle, koska valmistetta ei tule antaa potilaille, joilla on vaikea-asteinen immuunipuutostila (esim. lymfopenia, neutropenia, hypogammaglobulinemia) (ks. kohdat Vasta-aiheet ja Haittavaikutukset).
Niiden potilaiden kokonaisosuus, joilla oli jokin vakava infektio, oli laskimoon annettavalla okrelitsumabilla tehdyissä tutkimuksissa samankaltainen kuin verrokeilla (ks. kohta Haittavaikutukset). Hengenvaarallisten (4. asteen) ja kuolemaan johtavien (5. asteen) infektioiden esiintyvyys oli kaikissa hoitoryhmissä pieni, mutta primaaristi etenevää MS-tautia sairastavilla potilailla hengenvaaralliset ja kuolemaan johtaneet infektiot olivat yleisempiä laskimoon annettavaa okrelitsumabihoitoa saaneilla kuin lumehoitoa saaneilla potilailla (hengenvaaralliset: 1,6 % [laskimoon annettava Ocrevus-hoito] vs 0,4 % [lumehoito], ja kuolemaan johtaneet: 0,6 % [laskimoon annettava Ocrevus-hoito] vs 0 % [lumehoito]). Kaikki hengenvaaralliset infektiot paranivat ilman okrelitsumabihoidon lopettamista.
Primaaristi etenevää MS-tautia sairastavilla potilailla, joilla on nielemisvaikeuksia, on tavanomaista suurempi aspiraatiopneumonian riski. Näillä potilailla okrelitsumabihoito saattaa entisestään lisätä vaikea-asteisen pneumonian riskiä. Lääkärin pitää ryhtyä nopeasti toimenpiteisiin, jos potilaalla on pneumonia.
Progressiivinen multifokaalinen leukoenkefalopatia (PML)
Progressiivisen multifokaalisen leukoenkefalopatian aiheuttavaa JC‑virusinfektiota on havaittu hyvin harvoin anti-CD20-vasta-aineilla, mukaan lukien okrelitsumabilla, hoidetuilla potilailla. Infektioon on tällöin liittynyt useimmiten riskitekijöitä (potilasryhmä, esim. lymfopenia, korkea ikä, usean immunosuppressiivisen lääkkeen käyttö).
Lääkärin pitää tarkkailla PML:n varhaisvaiheen oireita ja löydöksiä, joita voivat olla uudenlaisten neurologisten oireiden ilmaantuminen tai aiempien löydösten ilmaantuminen tai paheneminen, sillä ne voivat olla samankaltaisia kuin MS-taudissa.
Jos PML:a epäillään, okrelitsumabihoito pitää keskeyttää. Tutkimuksia, kuten magneettikuvaus (MK) mieluiten varjoainetehosteisena (vertailu ennen hoitoa tehtyyn MK:n), JCV-DNA-määritys aivo-selkäydinnesteestä sekä toistuvat neurologiset tutkimukset, on harkittava. Jos PML varmistuu, hoito on lopetettava pysyvästi.
B-hepatiitin uudelleen aktivoituminen
Anti-CD20-vasta-aineilla hoitoa saaneilla potilailla on raportoitu hepatiitti B ‑viruksen (HBV) uudelleen aktivoitumista, mikä on johtanut joissain tapauksissa fulminantin hepatiitin kehittymiseen, maksan vajaatoimintaan ja kuolemaan.
Kaikille potilaille pitää ennen hoidon aloittamista tehdä HBV-seulonta paikallisten ohjeistojen mukaisesti. Aktiivista HBV-infektiota (eli aktiivinen infektio varmistunut positiivisilla HBsAg- ja anti-HB-testituloksilla) sairastaville potilaille ei pitäisi antaa okrelitsumabihoitoa (ks. kohta Vasta-aiheet). Jos potilaan serologinen testitulos on positiivinen ([eli negatiivinen HbsAg ja positiivinen HB-c-antigeeni (HbcAB +]; HBV:n kantaja [pinta-antigeenipositiivinen, HbsAg+]), maksatautien erikoislääkäriä pitää konsultoida ennen hoidon aloittamista, ja potilasta pitää seurata ja hoitaa paikallisten hoitokäytäntöjen mukaisesti B-hepatiitin uudelleenaktivoitumisen estämiseksi.
Viivästynyt neutropenia
Viivästyneesti ilmenevää neutropeniaa on raportoitu aikaisintaan 4 viikkoa viimeisimmän laskimoon annetun okrelitsumabi-infuusion jälkeen (ks. kohta Haittavaikutukset). Vaikka jotkut tapaukset olivat vaikeusasteen 3. tai 4. tapauksia, oli valtaosa tapauksista vaikeusasteen 1. tai 2. asteen tapauksia. Jos potilaalla on infektion oireita ja löydöksiä, veren neutrofiilimäärä suositellaan määrittämään.
Syövät
Kliinisten pivotaalitutkimusten kontrolloidulla aikajaksolla on havaittu syöpien (mukaan lukien rintasyöpien) määrän lisääntymistä laskimoon annettavaa okrelitsumabihoitoa saaneilla potilailla vertailuryhmään verrattuna. Esiintyvyys oli MS-potilaiden oletetun taustaesiintyvyyden mukainen. Kliinisten pivotaalitutkimusten kontrolloidulla jaksolla ja avoimessa jatkovaiheessa annetun okrelitsumabihoidon jatkuttua yhtäjaksoisesti noin 10 vuotta syöpien ilmaantuvuus oli edelleen MS-potilaiden oletetun taustaesiintyvyyden mukainen. Jos potilaalla tiedetään olevan aktiivinen syöpä, okrelitsumabihoitoa ei saa antaa (ks. kohta Vasta-aiheet). Jos potilaalla tiedetään olevan syöpien riskitekijöitä tai potilaan sairastaman syövän uusiutumista seurataan aktiivisesti, potilaan hoidon yksilölliset hyödyt ja riskit pitää arvioida. Potilaan pitää noudattaa tavanomaisia paikallisia suosituksia rintasyöpäseulonnoista.
Vaikea-asteisesti immuunipuutteisten potilaiden hoito
Vaikea-asteisesti immuunipuutteisia potilaita ei saa hoitaa ennen kuin immuunipuutostila korjautuu (ks. kohta Vasta-aiheet).
Okrelitsumabin käyttö muiden autoimmuunisairauksien yhteydessä samanaikaisesti käytettävien immunosuppressiivisten lääkkeiden (esim. pitkäaikaisesti käytettävien kortikosteroidien, ei-biologisten ja biologisten taudinkulkua muuntavien reumalääkkeiden [DMARD], mykofenolaattimofetiilin, syklofosfamidin, atsatiopriinin) kanssa lisäsi vakavia infektioita, mukaan lukien opportunisti-infektioita. Infektioita olivat epätyypillinen keuhkokuume ja pneumocystis jirovecin aiheuttama keuhkokuume, vesirokkoviruksen aiheuttama keuhkokuume, tuberkuloosi ja histoplasmoosi näihin kuitenkaan rajoittumatta. Jotkut näistä infektioista johtivat harvinaisissa tapauksissa potilaan kuolemaan. Lisäanalyysissa todettiin seuraavien tekijöiden liittyvän vakavien infektioiden riskiin: MS-taudin hoitoon suositeltua suuremmat okrelitsumabiannokset, muut samanaikaiset sairaudet ja immunosuppressiivisten lääkkeiden/kortikosteroidien pitkäaikaiskäyttö.
Muiden immunosuppressiivisten lääkkeiden samanaikaista käyttöä okrelitsumabin kanssa ei suositella, lukuun ottamatta pahenemisvaiheiden oireenmukaiseen hoitoon käytettäviä kortikosteroideja. Tiedot siitä, liittyykö kliinisessä hoidossa pahenemisvaiheiden samanaikaiseen oireenmukaiseen steroidihoitoon lisääntynyt infektioriski, ovat suppeita. Laskimoon annettavalla okrelitsumabilla tehdyissä MS-tautia koskevissa pivotaalitutkimuksissa pahenemisvaiheiden kortikosteroidihoitoon ei liittynyt vakavien infektioiden riskin lisääntymistä.
Kun okrelitsumabihoito aloitetaan immunosuppressiivisen hoidon jälkeen tai kun immunosuppressiivista hoitoa aloitetaan okrelitsumabihoidon jälkeen, on otettava huomioon päällekkäisten farmakodynaamisten vaikutusten mahdollisuus (ks. kohta Farmakodynamiikka). Okrelitsumabin määräämisessä on oltava varovainen ja huomioitava muiden taudinkulkua muuntavien MS-lääkkeiden farmakodynamiikka.
Rokotukset
Eläviä tai heikennettyjä eläviä viruksia sisältävillä rokotteilla annettujen rokotusten turvallisuutta okrelitsumabihoidon jälkeen ei ole tutkittu, joten rokotuksia eläviä tai heikennettyjä eläviä taudinaiheuttajia sisältävillä rokotteilla ei suositella hoidon aikana eikä ennen kuin B-solut ovat palautuneet. Kliinisissä tutkimuksissa ajan mediaani B-solujen palautumiseen oli 72 viikkoa (ks. kohta Farmakodynamiikka).
Satunnaistetussa avoimessa tutkimuksessa aaltomaista MS-tautia sairastavia laskimoon annettavalla okrelitsumabilla hoitoa saaneita potilaita rokotettiin seuraavilla rokotteilla: tetanustoksoidi, 23-valenttinen pneumokokkipolysakkaridi (PPV23) ilman tehosteannosta tai tehosteannoksen kanssa, KLH (keyhole limpet haemocyanin) ‑neoantigeeni ja kausi-influenssarokote. Potilaat saivat humoraalisen, tosin alentuneen vasteen rokotteille (ks. kohdat Yhteisvaikutukset ja Farmakodynamiikka).
Okrelitsumabihoitoa saavien potilaiden kausi-influenssarokotukseen suositellaan käyttämään inaktivoitua virusta sisältävää rokotetta.
Lääkärin pitää tarkistaa potilaan rokotustilanne, kun potilaalle harkitaan okrelitsumabihoitoa. Jos potilas tarvitsee rokotuksia, ne pitää antaa viimeistään 6 viikkoa ennen okrelitsumabihoidon aloittamista.
Sikiöaikainen altistuminen okrelitsumabille sekä vastasyntyneiden ja imeväisikäisten rokottaminen eläviä tai heikennettyjä eläviä taudinaiheuttajia sisältävillä rokotteilla
Okrelitsumabille raskauden aikana altistuneen äidin imeväisikäisellä lapsella saattaa olla B‑solupuutos. Tästä syystä rokottamista eläviä tai heikennettyjä eläviä taudinaiheuttajia sisältävillä rokotteilla suositellaan siirtämään siihen asti, kunnes B‑solumäärä on korjautunut normaaliksi. Vastasyntyneiltä ja imeväisikäisiltä suositellaan tämän vuoksi mittaamaan CD19-positiivisten B‑solujen määrä ennen rokotuksen antamista.
Kaikki muut kuin eläviä tai heikennettyjä eläviä taudinaiheuttajia sisältävät rokotteet suositellaan antamaan paikallisen rokotusohjelman mukaisesti. Rokotteista saadun vasta-ainetiitterin mittaamista pitää harkita, jotta voidaan tarkistaa, onko henkilö saanut suojaavan immuunivasteen, sillä rokotuksen teho saattaa olla tavanomaista heikompi.
Rokotuksen turvallisuudesta ja ajoituksesta pitää keskustella lasta hoitavan lääkärin kanssa (ks. kohta Raskaus ja imetys).
Natrium
Tämä lääkevalmiste sisältää alle 1 mmol natriumia (23 mg) per annos eli se on olennaisesti natriumiton.
Yhteisvaikutukset
Yhteisvaikutustutkimuksia ei ole tehty, koska yhteisvaikutuksia sytokromi P450 ‑entsyymien, muiden metaboloivien entsyymien tai kuljettajaproteiinien kanssa ei oletettavasti esiinny.
Rokotukset
Eläviä tai heikennettyjä eläviä taudinaiheuttajia sisältävillä rokotteilla annettujen rokotusten turvallisuutta okrelitsumabihoidon jälkeen ei ole tutkittu.
Seuraavien rokotteiden vaikutuksista laskimoon annettavaa okrelitsumabihoitoa saavilla potilailla on olemassa tietoa: tetanustoksoidi-, 23-valenttinen pneumokokkipolysakkaridi- (PPV23), KLH (keyhole limpet haemocyanin) -neoantigeenia sisältävä rokote ja kausi-influenssarokote (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Farmakodynamiikka).
Laskimoon annettavalla okrelitsumabilla kahden vuoden ajan annetun hoidon jälkeen niiden potilaiden osuus, joiden vasta-ainetiitteri S. pneumoniae ‑bakteeria, sikotautia, vihurikokkoa ja vesirokkoa vastaan oli positiivinen, oli yleisesti samankaltainen kuin lähtötilanteessa.
Immunosuppressiiviset lääkkeet
Muiden immunosuppressiivisten lääkkeiden käyttöä samanaikaisesti okrelitsumabihoidon kanssa ei suositella, lukuun ottamatta pahenemisvaiheiden oireenmukaiseen hoitoon käytettäviä kortikosteroideja (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Raskaus ja imetys
Hedelmällisessä iässä olevat naiset
Hedelmällisessä iässä olevien naisten on käytettävä ehkäisyä okrelitsumabihoidon aikana ja 4 kuukauden ajan viimeisen okrelitsumabiannoksen jälkeen.
Raskaus
Okrelitsumabin käytöstä raskaana oleville naisille on vain vähän tietoja. Okrelitsumabi on immunoglobuliini G (IgG). IgG:n tiedetään läpäisevän istukkaesteen. Okrelitsumabille sikiöaikana altistuneiden vastasyntyneiden tai imeväisikäisten rokotus eläviä tai heikennettyjä eläviä taudinaiheuttajia sisältävillä rokotteilla pitää harkita siirrettäväksi myöhemmäksi. Okrelitsumabille kohdussa altistuneista vastasyntyneistä ja imeväisikäisistä ei ole kerätty B‑solumäärää koskevia tietoja, joten vastasyntyneen ja imeväisen B‑solupuutoksen mahdollista kestoaikaa ei tiedetä (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Muille anti-CD20-vasta-aineille raskauden aikana altistuneille äideille syntyneillä lapsilla on raportoitu ohimenevää perifeeristä B-solupuutosta ja lymfopeniaa. Myös eläimillä tehdyissä tutkimuksissa havaittiin in utero B‑solupuutosta.
Eläinkokeet (alkio- ja sikiötoksisuus) eivät osoittaneet teratogeenisia vaikutuksia. Pre- ja postnataalista kehitystä koskevissa tutkimuksissa havaittiin lisääntymistoksisuutta (ks. kohta Prekliiniset tiedot turvallisuudesta).
Okrelitsumabin käyttöä tulee välttää raskauden aikana elleivät mahdolliset hyödyt äidille ole sikiölle mahdollisesti aiheutuvia riskejä suuremmat.
Imetys
Ihmisen immunoglobuliinien G (IgG) tiedetään erittyvän äidinmaitoon muutaman päivän ajan synnytyksen jälkeen (ensimaitojakso). Pian sen jälkeen pitoisuudet laskevat mataliksi.
Prospektiivisessa, avoimessa MN42989-monikeskustutkimuksessa (SOPRANINO) 13 imettävää naista sai okrelitsumabia 2,0 kuukautta (mediaani) synnytyksen jälkeen (vaihteluväli 0,5–5,0 kuukautta). Äidinmaidossa havaittiin pieniä okrelitsumabipitoisuuksia 60 päivän ajan ensimmäisen infuusion jälkeen, jonka äiti sai synnytyksen jälkeen (vauvan suhteellisen annoksen mediaani 0,27 % [vaihteluväli 0,0–1,8 %]), mikä osoittaa okrelitsumabia siirtyvän minimaalisesti äidinmaitoon. 30 päivää ensimmäisen infuusion jälkeen, jonka äiti sai synnytyksen jälkeen, okrelitsumabia ei ollut enää havaittavissa imetettyjen vauvojen saatavissa olleissa seeruminäytteissä (n = 9) ja vauvojen B‑solumäärä oli kaikissa saatavissa olleissa verinäytteissä (n = 10) normaaliarvoissa. Okrelitsumabin ei havaittu vaikuttavan imetettyjen vauvojen terveyteen, kasvuun ja kehitykseen 44,6 viikon seurantajakson aikana (vaihteluväli 8,6–62,7 viikkoa).
Vaikka okrelitsumabille äidinmaidon kautta mahdollisesti altistuneista ja eläviä tai heikennettyjä eläviä rokotteita saaneista vauvoista ei ole saatavissa kliinisiä tietoja, riskejä ei oletettavasti ole, sillä näiden vauvojen B‑solupitoisuuksien havaittiin olevan normaalit eikä seerumissa ollut havaittavia okrelitsumabipitoisuuksia.
Erillisessä prospektiivisessa kliinisessä tutkimuksessa 29 imettävällä naisella, jotka saivat okrelitsumabia 4,3 kuukautta (mediaani) (vaihteluväli 0,1–36 kuukautta) synnytyksen jälkeen, havaittiin äidinmaidossa pieniä okrelitsumabipitoisuuksia (vauvan suhteellisen annoksen mediaani 0,1 % [vaihteluväli 0,07–0,7 %]) 90 päivän ajan ensimmäisen infuusion jälkeen, jonka äiti sai synnytyksen jälkeen. 21:n imetetyn vauvan vähintään kaksi viikkoa kestäneessä seurannassa todettiin normaali kasvu ja kehitys yhteen ikävuoteen saakka.
Okrelitsumabia voidaan käyttää imetyksen aikana aloittamalla sen käyttö muutama päivä synnytyksen jälkeen.
Hedelmällisyys
Okrelitsumabille altistuneilla Cynomolgus-apinauroksilla ja -naarailla tehtyjen hedelmällisyyttä koskevien prekliinisten tutkimusten tulokset eivät viittaa erityiseen haittaan ihmisille.
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Ocrevus-valmisteella ei ole haitallista vaikutusta ajokykyyn tai koneiden käyttökykyyn.
Haittavaikutukset
Turvallisuusprofiilin yhteenveto
Tärkeimmät ja yleisimmin raportoidut haittavaikutukset kliinisten pivotaalitutkimusten kontrolloidulla jaksolla olivat infuusioreaktiot (34,3 %:lla aaltomaista MS-tautia sairastavista ja 40,1 %:lla primaaristi etenevää MS‑tautia sairastavista) ja infektiot (58,5 %:lla aaltomaista MS-tautia sairastavista ja 72,2 %:lla primaaristi etenevää MS-tautia sairastavista) (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Kliinisten pivotaalitutkimusten kontrolloidulla jaksolla oli mukana yhteensä 2 376 potilasta, joista 1 852 potilasta osallistui avoimeen jatkovaiheeseen. Kaikki potilaat siirtyivät okrelitsumabihoitoon avoimen jatkovaiheen aikana. 1 155 potilasta oli mukana avoimen jatkovaiheen loppuun asti, jolloin kontrolloidun jakson ja avoimen jatkovaiheen aikana annettu okrelitsumabihoito kesti yhtäjaksoisesti noin 10 vuotta (15 515 potilasvuoden altistus). Kontrolloidulla jaksolla ja avoimessa jatkovaiheessa todettu turvallisuusprofiili oli yhdenmukainen kontrolloidulla jaksolla todetun yleisen turvallisuusprofiilin kanssa.
Ocrevus injektionesteen turvallisuusprofiilin havaittiin olleen yhdenmukainen laskimoon annettavan okrelitsumabin tunnetun turvallisuusprofiilin kanssa (taulukko 1 jäljempänä), lukuun ottamatta hyvin yleisenä haittavaikutuksena havaittuja injektioreaktioita.
Haittavaikutustaulukko
Laskimoon annettavaa okrelitsumabia koskeneiden kliinisten pivotaalitutkimusten kontrolloidulla jaksolla raportoidut ja spontaaniraportointiin perustuvat haittavaikutukset luetellaan jäljempänä taulukossa 1. Haittavaikutukset luetellaan MedDRA-elinjärjestelmäluokituksen ja esiintyvyysluokkien mukaan. Esiintymistiheydet on määritelty seuraavasti: hyvin yleinen (≥ 1/10), yleinen (≥ 1/100, < 1/10), melko harvinainen (≥ 1/1 000, < 1/100), harvinainen (≥ 1/10 000, < 1/1 000), hyvin harvinainen (< 1/10 000) ja tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin). Haittavaikutukset on esitetty kussakin elinjärjestelmäluokassa haittavaikutuksen yleisyyden mukaan alenevassa järjestyksessä.
Taulukko 1. Haittavaikutukset
MedDRA Elinjärjestelmäluokka | Hyvin yleiset | Yleiset | Tuntematon |
| Infektiot | Ylähengitysteiden infektio, nasofaryngiitti, influenssa | Sinuiitti, bronkiitti, huuliherpes, gastroenteriitti, hengitystie-infektio, virusinfektio, herpes zoster ‑infektio, konjunktiviitti, selluliitti | |
| Veri ja imukudos | Neutropenia | Viivästynyt neutropenia3 | |
| Hengityselimet, rintakehä ja välikarsina | Yskä, katarri | ||
| Tutkimukset | Veren pienentynyt immunoglobuliini M ‑pitoisuus | Veren pienentynyt immunoglobuliini G ‑pitoisuus | |
| Vammat, myrkytykset ja hoitokomplikaatiot | Infuusioon liittyvät reaktiot1, injektioreaktio2,3 |
1 Havaittu vain laskimoon annettavaa okrelitsumabia koskevassa yhdistetyssä tietoaineistossa.
2 Havaittu laskimoon annettavaa okrelitsumabia koskevan yhdistetyn tietoaineiston ulkopuolisessa tutkimuksessa (liittyy antoon ihon alle).
3 Havaittu valmisteen markkinoille tulon jälkeen.
Valikoitujen haittavaikutusten kuvaus
Injektioreaktiot
Injektioreaktiot luokitellaan havaittujen oireiden perusteella systeemisiksi injektioreaktioiksi ja paikallisiksi injektioreaktioiksi.
OCARINA II ‑tutkimuksessa 118 potilasta (okrelitsumabilla aiemmin hoitamattomia) sai ensimmäisen injektion valmistetta. Yleisimmin raportoituja systeemisten injektioreaktioiden ja paikallisten injektioreaktioiden oireita olivat päänsärky (2,5 %), pahoinvointi (1,7 %), injektiokohdan eryteema (29,7 %), injektiokohdan kipu (14,4 %), injektiokohdan turvotus (8,5 %) ja injektiokohdan kutina (6,8 %). Injektiokohdan reaktioita ilmaantui ensimmäisen injektion jälkeen 48,3 %:lle näistä potilaista. Näistä 118 tutkimuspotilaasta 11,0 %:lle ilmaantui vähintään yksi systeemistä injektioreaktiota koskeva tapahtuma ja 45,8 %:lle potilaista ilmaantui vähintään yksi paikallista injektioreaktiota koskeva tapahtuma. Niistä potilaista, joille injektioreaktio ilmaantui, injektioreaktiot ilmenivät valtaosalla (82,5 %) potilaista 24 tunnin kuluessa injektion annon päättymisestä eikä injektion annon aikana. Yksikään injektioreaktioista ei ollut vakava ja ne kaikki olivat vaikeusasteeltaan lieviä (71,9 %) tai keskivaikeita (28,1 %). Systeemisten injektioreaktioiden keston mediaani oli 3 päivää, ja paikallisten injektioreaktioiden keston mediaani oli 4 päivää. Kaikki potilaat toipuivat injektioreaktioista, ja heistä 26,3 % tarvitsi oireenmukaista hoitoa.
OCARINA I ‑tutkimuksessa 125 potilasta sai yhden tai useamman 1200 mg:n ihonalaisen okrelitsumabi-injektion. Näistä 125 potilaasta, jotka saivat ensimmäisen injektion, 16,0 %:lle potilaista ilmaantui vähintään yksi systeemistä injektioreaktiota koskeva tapahtuma ja 64,0 %:lle potilaista ilmaantui vähintään yksi paikallista injektioreaktiota koskeva tapahtuma. Niillä 104 potilaalla, jotka saivat toisen injektion, systeemisten injektioreaktioiden ilmaantuvuus väheni 7,7 %:iin ja paikallisten injektioreaktioiden ilmaantuvuus väheni 37,5 %:iin. Ensimmäisen injektion yhteydessä yksikään injektioreaktioista ei ollut vakava, ja yhtä injektioreaktiota lukuun ottamatta ne kaikki olivat vaikeusasteeltaan lieviä tai keskivaikeita. Toisen injektion yhteydessä yksikään injektioreaktioista ei ollut vakava ja ne kaikki olivat vaikeusasteeltaan lieviä tai keskivaikeita. Potilaista, joille ilmaantui injektioreaktio ensimmäisen injektion jälkeen, 21,2 % tarvitsi oireenmukaista hoitoa ja potilaista, joille ilmaantui injektioreaktio toisen injektion jälkeen, 17,9 % tarvitsi oireenmukaista hoitoa.
Laskimoon annettavaan okrelitsumabihoitoon liittyy infuusioreaktioita, jotka saattavat olla yhteydessä myös sytokiinien vapautumiseen ja/tai muihin kemiallisiin välittäjäaineisiin. Infuusioreaktiot saattavat ilmetä kutinana, ihottumana, urtikariana, eryteemana, kurkun ärsytyksenä, suunielun kipuna, hengenahdistuksena, nielun tai kurkunpään turvotuksena, kaulan ja kasvojen punoituksena, hypotensiona, kuumeena, uupumuksena, päänsärkynä, heitehuimauksena, pahoinvointina, takykardiana ja anafylaksiana. Laskimoon annettavan okrelitsumabin käytössä on raportoitu vakavia infuusioreaktioita, joista osa on vaatinut sairaalahoitoa.
Infektio
Aktiivisella vertailuvalmisteella kontrolloiduissa aaltomaista MS-tautia koskeneissa tutkimuksissa infektioita esiintyi 58,5 %:lla laskimoon annettavaa okrelitsumabihoitoa saaneista potilaista ja 52,5 %:lla interferonibeeta-1a:ta saaneista potilaista. Vakavia infektioita esiintyi 1,3 %:lla laskimoon annettavaa okrelitsumabihoitoa saaneista potilaista ja 2,9 %:lla interferonibeeta-1a:ta saaneista potilaista. Primaaristi etenevää MS-tautia koskeneessa lumekontrolloidussa tutkimuksessa infektioita esiintyi 72,2 %:lla laskimoon annettavaa okrelitsumabihoitoa saaneista potilaista ja 69,9 %:lla lumehoitoa saaneista potilaista. Vakavia infektioita esiintyi 6,2 %:lla laskimoon annettavaa okrelitsumabihoitoa saaneista potilaista ja 6,7 %:lla lumehoitoa saaneista potilaista.
Sekä aaltomaista MS-tautia että primaaristi etenevää MS-tautia koskeneissa laskimoon annettavalla okrelitsumabilla tehdyissä pivotaalitutkimuksissa kaikki potilaat siirtyivät laskimoon annettavaan okrelitsumabihoitoon tutkimuksen avoimen jakson aikana. Aaltomaista MS-tautia ja primaaristi etenevää MS-tautia sairastavilla potilailla vakavien infektioiden kokonaisriski ei ollut avoimen jatkovaiheen aikana suurempi kuin kontrolloidulla jaksolla havaittu riski. Kuten kontrolloidulla jaksolla havaittiin, vakavien infektioiden esiintyvyys primaaristi etenevää MS-tautia sairastavilla potilailla oli edelleen yleisempää kuin aaltomaista MS-tautia sairastavilla potilailla.
Muihin autoimmuunisairauksiin kuin MS-tautiin liittyvien vakavien infektioiden riskitekijöistä aiemmin tehdyn analyysin (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet) mukaisesti vakavien infektioiden riskitekijöistä tehtiin monen muuttujan analyysi noin 10 vuoden kumulatiivisista altistustiedoista, jotka oli saatu kliinisten pivotaalitutkimusten kontrolloidusta jaksosta ja avoimesta jatkovaiheesta. Vakavien infektioiden riskitekijöitä aaltomaista MS-tautia sairastavilla potilailla ovat vähintään yksi muu samanaikainen sairaus, äskettäinen kliininen pahenemisvaihe ja liikunta- ja toimintakyvyn heikentymistä osoittavat pisteet (Expanded Disability Status Scale (EDSS) ‑pisteet) ≥ 6,0. Vakavien infektioiden riskitekijöitä primaaristi etenevää MS-tautia sairastavilla potilailla ovat painoindeksi yli 25 kg/m2, vähintään kaksi muuta samanaikaista sairautta, EDSS-pisteet ≥ 6,0 ja IgM viitevälin alarajan alapuolella (< LLN). Muita samanaikaisia sairauksia olivat muun muassa sydän- ja verisuonitaudit, munuais- ja virtsatiesairaudet, aiemmat infektiot ja masennus.
Hengitystieinfektiot
Hengitystieinfektioiden osuus oli suurempi laskimoon annettavaa okrelitsumabihoitoa saaneilla potilailla verrattuna interferonibeeta-1a- ja lumehoitoa saaneisiin potilaisiin.
Aaltomaista MS-tautia koskeneissa tutkimuksissa ylähengitystieinfektioita esiintyi 39,9 %:lla laskimoon annettavaa okrelitsumabihoitoa saaneista potilaista ja 33,2 %:lla interferonibeeta-1a:ta saaneista potilaista, ja alahengitystieinfektioita esiintyi 7,5 %:lla laskimoon annettavaa okrelitsumabihoitoa saaneista potilaista ja 5,2 %:lla interferonibeeta-1a:ta saaneista potilaista.
Primaaristi etenevää MS-tautia koskeneessa tutkimuksessa ylähengitystieinfektioita esiintyi 48,8 %:lla laskimoon annettavaa okrelitsumabihoitoa saaneista potilaista ja 42,7 %:lla lumehoitoa saaneista potilaista, ja alahengitystieinfektioita esiintyi 9,9 %:lla laskimoon annettavaa okrelitsumabihoitoa saaneista potilaista ja 9,2 %:lla lumehoitoa saaneista potilaista.
Laskimoon annettavalla okrelitsumabilla hoitoa saaneilla potilailla raportoidut hengitystieinfektiot olivat pääasiassa lieviä tai keskivaikeita (80–90 %).
Herpes
Aktiivisella vertailuvalmisteella kontrolloiduissa (aaltomainen MS-tauti) kliinisissä tutkimuksissa herpesinfektioita raportoitiin yleisemmin laskimoon annettavaa okrelitsumabihoitoa saaneilla potilailla kuin interferonibeeta-1a:ta saaneilla potilailla, mukaan lukien herpes zoster (2,1 % vs 1,0 %), herpes simplex (0,7 % vs 0,1 %), huuliherpes (3,0 % vs 2,2 %), sukupuolielinherpes (0,1 % vs 0 %) ja herpesvirusinfektio (0,1 % vs 0 %). Kaikki infektiot olivat lieviä tai keskivaikeita, yhtä kolmannen asteen tapahtumaa lukuun ottamatta, ja potilaat paranivat normaalin hoitokäytännön mukaisella hoidolla.
Lumekontrolloidussa (primaaristi etenevä MS-tauti) kliinisessä tutkimuksessa suurempi osa huuliherpesinfektioista (2,7 % vs 0,8 %) todettiin laskimoon annettavaa okrelitsumabia saaneessa hoitoryhmässä.
Laboratorioarvojen poikkeavuudet
Immunoglobuliinit
Okrelitsumabihoito pienensi laskimoon annettavalla okrelitsumabilla tehtyjen kliinisten pivotaalitutkimusten kontrolloitujen jaksojen aikana immunoglobuliinien kokonaispitoisuutta siten, että IgM-pitoisuus pieneni voimakkaimmin.
Tiedot kliinisten pivotaalitutkimusten kontrolloidusta jaksosta ja avoimesta jatkovaiheesta ovat osoittaneet yhteyden IgG:n (ja harvemmin IgM:n tai IgA:n) pitoisuuksien pienenemisen ja vakavien infektioiden lisääntymisen välillä. Aaltomaista MS-tautia sairastavista potilaista 2,1 %:lla ja primaaristi etenevää MS-tautia sairastavista potilaista 2,3 %:lla ilmeni vakava infektio, kun IgG oli viitevälin alarajan alapuolella (< LLN). Ero vakavien infektioiden esiintyvyydessä potilailla, joilla IgG oli viitevälin alarajan alapuolella (< LLN), verrattuna potilaisiin, joilla IgG oli viitevälin alarajalla tai sen yläpuolella (≥ LLN), ei kasvanut ajan mittaan. Sellaisten jaksojen aikana, jolloin immunoglobuliinipitoisuus oli viitevälin alarajan alapuolella, todettujen vakavien infektioiden tyyppi, vaikeusaste, piilevyys, kesto ja lopputulos olivat yhdenmukaisia okrelitsumabihoitoa kontrolloidulla jaksolla ja avoimessa jatkovaiheessa saaneilla potilailla todettujen kaikkien vakavien infektioiden kanssa. Aaltomaista MS-tautia ja primaaristi etenevää MS-tautia sairastavien potilaiden keskimääräiset IgG-pitoisuudet pysyivät viitevälin alarajan yläpuolella koko 10 vuotta kestäneen yhtäjaksoisen okrelitsumabihoidon aikana.
Lymfosyytit
Aaltomaisen MS-taudin yhteydessä lymfosyyttien vähenemistä viitevälin alarajan alapuolelle (< LLN) havaittiin 20,7 %:lla laskimoon annettavalla okrelitsumabilla hoitoa saaneista potilaista ja 32,6 %:lla interferonibeeta-1a:ta saaneista potilaista. Primaaristi etenevän MS-taudin yhteydessä lymfosyyttien vähenemistä viitevälin alarajan alapuolelle (< LLN) havaittiin 26,3 %:lla laskimoon annettavaa okrelitsumabihoitoa saaneista potilaista ja 11,7 %:lla lumehoitoa saaneista potilaista.
Valtaosa raportoidusta lymfosyyttien vähenemisestä laskimoon annettavaa okrelitsumabihoitoa saaneilla potilailla oli vaikeusasteeltaan 1 (< LLN – 800 solua/mm3) ja 2 (500–800 solua/mm3). Laskimoon annettavaa okrelitsumabia saaneessa ryhmässä noin 1 %:lla potilaista oli 3. asteen lymfopenia (200–500 solua/mm3). Yhdelläkään potilaalla ei raportoitu 4. asteen lymfopeniaa (< 200 solua/mm3).
Laskimoon annettavaa okrelitsumabihoitoa saaneilla potilailla havaittiin vakavien infektioiden lisääntymistä sellaisten jaksojen aikana, jolloin lymfosyyttien kokonaismäärän väheneminen varmistui. Vakavia infektioita oli liian vähän, jotta siitä voitaisiin tehdä varmoja päätelmiä.
Neutrofiilit
Aktiivisella vertailuvalmisteella kontrolloidulla (aaltomainen MS-tauti) hoitojaksolla neutrofiilien vähenemistä normaaliarvojen alarajan alapuolelle (< LLN) havaittiin 14,7 %:lla laskimoon annettavalla okrelitsumabilla hoitoa saaneista potilaista ja 40,9 %:lla interferonibeeta-1a:ta saaneista potilaista. Lumekontrolloidussa (primaaristi etenevä MS-tauti) kliinisessä tutkimuksessa niiden laskimoon annettavaa okrelitsumabihoitoa saaneiden potilaiden osuus, joiden neutrofiilimäärä väheni, oli suurempi (12,9 %) kuin lumehoitoa saaneilla potilailla (10,0 %). Toisen asteen tai vaikeampiasteisen neutropenian osuus oli suurempi laskimoon annettavaa okrelitsumabia saaneessa ryhmässä (4,3 %) kuin lumeryhmässä (1,3 %). Neljännen asteen neutropeniaa oli laskimoon annettavaa okrelitsumabia saaneessa ryhmässä noin 1 %:lla potilaista ja 0 %:lla lumeryhmässä.
Valtaosa neutrofiilimäärän vähenemisistä oli ohimenevää (havaittiin tietyllä okrelitsumabihoitoa saavalla potilaalla vain kerran) ja vaikeusasteeltaan 1 (< LLN – 1500 solua/mm3) tai 2 (1000−1500 solua/mm3). Kolmannen tai neljännen asteen neutropeniaa oli kaikkiaan noin 1 %:lla laskimoon annettavaa okrelitsumabia saaneen ryhmän potilaista. Yksi potilas, jolla oli 3. asteen neutropenia (500−1000 solua/mm3) ja yksi potilas, jolla oli 4. asteen neutropenia (< 500 solua/mm3), tarvitsivat spesifistä hoitoa granulosyyttejä stimuloivilla kasvutekijöillä, minkä jälkeen potilaat jatkoivat okrelitsumabihoitoa. Neutropenia voi ilmetä useita kuukausia okrelitsumabin annon jälkeen (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Muuta
Yksi 2000 mg:n annoksen laskimoon annettavaa okrelitsumabia saanut potilas kuoli tuntemattomasta syystä kehittyneen tulehdusreaktio-oireyhtymän (SIRS) seurauksena 12 viikkoa viimeisestä infuusiosta tehdyn magneettikuvauksen jälkeen. Tulehdusreaktio-oireyhtymän kehittymiseen saattoi vaikuttaa anafylaktinen reaktio magneettikuvauksessa käytetylle gadoliniumia sisältäneelle varjoaineelle.
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Hyväksyttyä okrelitsumabiannosta suuremmista annoksista on vain vähän kliinistä kokemusta. Tähän mennessä suurin tutkittu annos MS-potilailla on 2000 mg annosteltuna kahtena 1000 mg:n infuusiona laskimoon kahden viikon välein (aaltomaista MS-tautia sairastavilla potilailla tehty vaiheen II annoshakututkimus) ja 1200 mg annosteltuna injektiona ihon alle (vaiheen Ib annoshakututkimus). Haittavaikutukset sopivat kliinisissä pivotaalitutkimuksissa todettuun turvallisuusprofiiliin.
Yliannokseen ei ole spesifistä vasta-ainetta. Injektion anto on keskeytettävä heti, ja potilasta on tarkkailtava injektioreaktioiden havaitsemiseksi (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: immunosuppressantit, monoklonaaliset vasta-aineet, ATC-koodi: L04AG08.
Vaikutusmekanismi
Okrelitsumabi on yhdistelmä-DNA-tekniikalla tuotettu humanisoitu monoklonaalinen vasta-aine, jonka vaikutus kohdistuu selektiivisesti CD20:ta ilmentäviin B-soluihin.
CD20 pinta-antigeenia esiintyy pre-B-solujen, kypsien ja B-muistisolujen pinnalla, mutta ei lymfoidisissa kantasoluissa tai plasmasoluissa.
Tarkkaa mekanismia, johon okrelitsumabin kliininen hoitovaikutus MS-taudissa perustuu, ei täysin tunneta, mutta sen oletetaan liittyvän CD20:ta ilmentävien B-solujen määrän ja toiminnan vähenemisestä aiheutuvaan immunomodulaatioon. Solun pintaan sitoutunut okrelitsumabi hävittää CD20:ta ilmentäviä B-soluja selektiivisesti vasta-aineriippuvaisen solujen fagosytoosin (antibody-dependent cellular phagocytosis, ADCP), vasta-aineriippuvaisen soluvälitteisen solutuhon (antibody-dependent cellular cytotoxicity, ADCC), komplementtivälitteisen solutuhon (complement-dependent cytotoxicity, CDC) ja ohjelmoidun solukuoleman välityksellä. B-solujen elpymiskyky ja aiempi humoraalinen immuunivaste säilyvät. Myöskään luonnollinen immuniteetti ja T-solujen kokonaismäärä eivät muutu.
Ihonalainen okrelitsumabi sisältää rekombinanttia ihmisen hyaluronidaasia (rHuPH20), joka on entsyymi, jota käytetään ihon alle annettaessa lisäämään lääkemuodon sisältämien lääkeaineiden dispersiota ja imeytymistä.
Farmakodynaamiset vaikutukset
Okrelitsumabihoito aiheuttaa oletettuna farmakologisena vaikutuksena veressä nopean CD19-positiivisten B-solujen vähenemisen 14. hoidon jälkeiseen päivään mennessä (ensimmäinen arviointiajankohta). Tämä säilyi laskimoon annettavalla okrelitsumabilla toteutetun koko hoitojakson ajan. B-solumäärän laskentaan käytetään CD19-positiivisia B-soluja, sillä okrelitsumabi häiritsee määrityksessä CD20-positiivisten B-solujen tunnistamista.
Vaiheen III tutkimuksissa enintään 5 %:lla potilaista todettiin laskimoon annettujen okrelitsumabiannosten välillä vähintään yhden kerran B-solujen palautumista yli viitevälin alarajan [LLN] tai lähtötilanteen. B-solujen vähenemisen laajuus ja kesto oli ensisijaisesti etenevää MS-tautia ja MS-tautia koskeneissa tutkimuksissa yhdenmukainen.
Pisin seuranta-aika viimeisen laskimoon annetun infuusion jälkeen (vaiheen II tutkimus WA21493, N = 51) osoittaa, että mediaaniaika B-solujen palautumiseen (takaisin lähtötasolle tai viitevälin alarajalle sen mukaan, kumpi näistä tapahtui ensin) oli 72 viikkoa (vaihteluväli 27–175 viikkoa). B-solut olivat palautuneet viitevälin alarajalle tai lähtötilanteeseen 90 %:lla kaikista potilaista noin kahden ja puolen vuoden kuluessa viimeisen infuusion jälkeen.
Kliininen teho ja turvallisuus
Ihon alle annettava lääkemuoto
OCARINA II
CN42097-tutkimus (OCARINA II) oli satunnaistettu, avoin, rinnakkaisryhmillä tehty monikeskustutkimus, joka tehtiin ihon alle annettavan okrelitsumabin farmakokinetiikan, farmakodynamiikan, turvallisuuden ja immunogeenisuuden sekä radiologisten ja kliinisten vaikutusten arvioimiseksi laskimoon annettavaan okrelitsumabiin verrattuna potilailla, jotka sairastivat joko aaltomaista MS-tautia tai primaaristi etenevää MS-tautia. OCARINA II ‑tutkimus oli suunniteltu osoittamaan ihon alle annettavan okrelitsumabin vähintään yhdenveroisuus (non-inferiority) laskimoon annettavaan okrelitsumabiin nähden ensisijaisen farmakokineettisen päätetapahtuman perusteella, joka oli pitoisuus-aikakuvaajan pinta-ala (AUC) viikkoon 12 saakka injektion/infuusion jälkeen (AUCw1-12).
Yhteensä 236 potilasta, jotka sairastivat aaltomaista MS-tautia tai primaaristi etenevää MS-tautia (213 potilasta sairasti aaltomaista MS-tautia, 23 potilasta sairasti primaaristi etenevää MS-tautia), satunnaistettiin suhteessa 1:1 valmistetta ihon alle saaneeseen haaraan tai valmistetta laskimoon saaneeseen haaraan. Kontrolloidun jakson aikana (päivästä 0 viikkoon 24) potilaat saivat joko yhden 920 mg:n ihonalaisen injektion tutkimuspäivänä 1 tai kaksi 300 mg:n infuusiota laskimoon tutkimuspäivinä 1 ja 14. Kontrolloidun jakson jälkeen kaikilla potilailla oli mahdollisuus saada 920 mg:n ihonalaisen injektion vielä viikoilla 24 ja 48 (vastaavasti annokset 2 ja 3). Potilaita ei otettu tutkimukseen mukaan, jos he olivat saaneet edeltävien 24 kuukauden aikana aiempaa hoitoa anti-CD20-vasta-aineilla, mukaan lukien okrelitsumabia.
Potilaat olivat iältään 18–65-vuotiaita, ja seulonnassa heidän EDSS-pisteensä olivat 0–6,5. Demografiset tiedot olivat samankaltaiset näiden kahden hoitoryhmän välillä ja lähtötilanteen ominaisuudet olivat niissä hyvin tasapainossa. Keskimääräinen ikä oli ihon alle annettavaa valmistetta saaneessa haarassa 39,9 vuotta ja laskimoon annettavaa valmistetta saaneessa haarassa 40,0 vuotta. Ihon alle annettavaa valmistetta saaneessa haarassa 34,7 % potilaista oli miehiä ja laskimoon annettavaa valmistetta saaneessa haarassa miehiä oli 40,7 % potilaista. MS-taudin diagnoosista kulunut aika oli ihon alle annettavaa valmistetta saaneessa haarassa 5,70 vuotta (keskiarvo) / 3,10 vuotta (mediaani) ja laskimoon annettavaa valmistetta saaneessa haarassa 4,78 vuotta (keskiarvo) / 2,35 vuotta (mediaani).
Okrelitsumabialtistuksen vähintään yhdenveroisuus (non-inferiority) ihonalaisen 920 mg:n okrelitsumabiannoksen jälkeen verrattuna laskimoon annettavan okrelitsumabin 600 mg:n annoksen jälkeen osoitettiin ensisijaisen farmakokineettisen päätetapahtuman perusteella, joka oli AUC-arvo viikkoon 12 saakka (AUCw1-12) injektion jälkeen (ks. kohta Farmakokinetiikka).
Laskimoon annettava lääkemuoto
Aaltomainen MS-tauti (RMS)
Okrelitsumabin tehoa ja turvallisuutta selvitettiin kahdessa satunnaistetussa, kaksoissokkoutetussa (double-blind, double-dummy), aktiivisella vertailuvalmisteella kontrolloidussa kliinisessä tutkimuksessa (WA21092 ja WA21093), joiden tutkimusasetelma oli identtinen ja joissa mukana olleet potilaat sairastivat aaltomaista MS-tautityyppiä (McDonaldin vuoden 2010 kriteerien mukaisesti) ja heillä oli näyttöä taudin aktiivisuudesta kliinisten piirteiden tai kuvantamislöydösten perusteella viimeisen kahden vuoden aikana. Tiivistelmä tutkimusasetelmasta ja tutkimuksen potilasjoukon lähtötilanteen ominaisuuksista on esitetty taulukossa 2.
Demografiset tiedot ja lähtötilanteen ominaisuudet olivat tasapainossa kahden hoitoryhmän välillä. Okrelitsumabihoitoa saaville potilaille (ryhmä A) annettiin 600 mg kuuden kuukauden välein (ensimmäinen annos kahtena 300 mg:n infuusiona laskimoon kahden viikon välein, jonka jälkeen seuraavat annokset 600 mg:n kertainfuusiona laskimoon). Ryhmän B potilaat saivat 44 mikrog interferonibeeta-1a:ta injektiona ihon alle kolme kertaa viikossa.
Taulukko 2. Tutkimusasetelma sekä demografiset ja lähtötilanteen tiedot
| Tutkimus 1 | Tutkimus 2 | |||
| Tutkimuksen nimi | WA21092 (OPERA I) (n = 821) | WA21093 (OPERA II) (n = 835) | ||
| Tutkimusasetelma | ||||
| Tutkimuksen potilasjoukko | Aaltomaista (RMS) MS-tautia sairastavat potilaat | |||
| Sairaushistoria seulonnassa | Vähintään kaksi pahenemisvaihetta edellisten kahden vuoden aikana tai yksi pahenemisvaihe edellisen vuoden aikana; EDSS* 0–5,5, raja-arvot mukaan lukien | |||
| Tutkimuksen kesto | 2 vuotta | |||
| Hoitoryhmät | Ryhmä A: 600 mg okrelitsumabia Ryhmä B: 44 mikrog interferonibeeta-1a s.c. (IFN) | |||
| Lähtötilanteen ominaisuudet | Okrelitsumabi 600 mg (n = 410) | IFN 44 mikrog (n = 411) | Okrelitsumabi 600 mg (n = 417) | IFN 44 mikrog (n = 418) |
| Keskimääräinen ikä (vuotta) | 37,1 | 36,9 | 37,2 | 37,4 |
| Iän vaihteluväli (vuotta) tutkimuksen sisäänottovaiheessa | 18–56 | 18–55 | 18–55 | 18–55 |
| Sukupuolijakauma (% miehiä/% naisia) | 34,1/65,9 | 33,8/66,2 | 35,0/65,0 | 33,0/67,0 |
| Sairauden kestoajan keskiarvo/mediaani diagnoosin jälkeen (vuotta) | 3,82/1,53 | 3,71/1,57 | 4,15/2,10 | 4,13/1,84 |
| Taudin kulkua muuntavilla lääkkeillä aiemmin hoitamattomia potilaita (%)** | 73,4 | 71,0 | 72,7 | 74,9 |
| Keskimääräinen pahenemisvaiheiden määrä kuluneena vuonna | 1,31 | 1,33 | 1,32 | 1,34 |
| Niiden potilaiden osuus, joilla gadoliniumilla tehostuvia T1-muutoksia | 42,5 | 38,1 | 39,0 | 41,4 |
| Keskimääräiset EDSS-pisteet* | 2,82 | 2,71 | 2,73 | 2,79 |
* Liikunta- ja toimintakyvyn heikentymistä osoittava pisteytys, Expanded Disability Status Scale
** Potilaat, jotka eivät olleet käyttäneet mitään taudinkulkua muuntavaa hoitoa 2 vuoden aikana ennen satunnaistamista.
Keskeiset kliiniset ja magneettikuvauksella todetut tehotulokset esitetään taulukossa 3 ja kuvassa 1.
Näiden tutkimusten tulokset osoittavat, että okrelitsumabi vähentää merkitsevästi pahenemisvaiheita, magneettikuvauksella mitattavaa subkliinistä tautiaktiivisuutta ja taudin etenemistä verrattuna ihon alle annettuun 44 mikrog:n interferonibeeta-1a-hoitoon.
Taulukko 3. Tutkimusten WA21092 ja WA21093 keskeiset kliiniset ja magneettikuvaukseen liittyvät päätetapahtumat (aaltomainen MS-tauti)
| Päätetapahtumat | Tutkimus 1: WA21092 (OPERA I) | Tutkimus 2: WA21093 (OPERA II) | ||
Okrelitsumabi 600 mg (n = 410) | IFN 44 mikrog (n = 411) | Okrelitsumabi 600 mg (n = 417) | IFN 44 mikrog (n = 418) | |
| Kliiniset päätetapahtumat | ||||
| Vuosittainen pahenemisvaiheiden määrä (ARR, ensisijainen päätetapahtuma) | 0,156 | 0,292 | 0,155 | 0,290 |
| Suhteellinen vähenemä | 46 % (p < 0,0001) | 47 % (p < 0,0001) | ||
Niiden potilaiden osuus, joilla oli 12 viikon vahvistettu toimintakyvyn heikkeneminen3 Riskin alenema (yhdistetty analyysi1) Riskin alenema (yksittäiset tutkimukset2) | 9,8 % okrelitsumabi vs 15,2 % IFN 40 % (p = 0,0006)7 | |||
| 43 % (p = 0,0139)7 | 37 % (p = 0,0169)7 | |||
Niiden potilaiden osuus, joilla oli 24 viikon vahvistettu toimintakyvyn heikkeneminen3 Riskin alenema (yhdistetty analyysi1) Riskin alenema (yksittäiset tutkimukset2) | 7,6 % okrelitsumabi vs 12,0 % IFN 40 % (p = 0,0025)7 | |||
| 43 % (p = 0,0278)7 | 37 % (p = 0,0370)7 | |||
| Niiden potilaiden osuus, joilla oli vähintään 12 viikon vahvistettu toimintakyvyn parannus4 | 20,7 % okrelitsumabi vs 15,6 % IFN | |||
Suhteellinen lisäys (yhdistetty analyysi1) Suhteellinen lisäys (yksittäiset tutkimukset2) | 33 % (p = 0,0194) | |||
| 61 % (p = 0,0106) | 14 % (p = 0,4019) | |||
| Niiden potilaiden osuus, joilla ei ollut pahenemisvaihetta hoitoviikkoon 96 mennessä2 | 80,4 % | 66,7 % | 78,9 % | 64,3 % |
| (p < 0,0001) | (p < 0,0001) | |||
| Niiden potilaiden osuus, joilla ei ollut näyttöä taudin aktiivisuudesta (NEDA)5 | 48 % | 29 % | 48 % | 25 % |
| Suhteellinen lisäys2 | 64 % (p < 0,0001) | 89 % (p < 0,0001) | ||
| Magneettikuvauksen (MKn) päätetapahtumat | ||||
| Gadoliniumilla tehostuvien T1-muutosten määrä (keskiarvo) magneettikuvauskertaa kohden | 0,016 | 0,286 | 0,021 | 0,416 |
| Suhteellinen vähenemä | 94 % (p < 0,0001) | 95 % (p < 0,0001) | ||
| Uusien ja/tai suurentuneiden T2-hyperintensiivisten muutosten määrä (keskiarvo) magneettikuvauskertaa kohden | 0,323 | 1,413 | 0,325 | 1,904 |
| Suhteellinen vähenemä | 77 % (p < 0,0001) | 83 % (p < 0,0001) | ||
| Aivojen tilavuuden prosentuaalinen muutos viikosta 24 viikkoon 96 | -0,572 | -0,741 | -0,638 | -0,750 |
| Aivojen tilavuuden menetyksen suhteellinen vähenemä | 22,8 % (p = 0,0042)6 | 14,9 % (p = 0,0900) | ||
1 Tutkimusten 1 ja 2 prospektiivisesti yhdistetyt tiedot
2 Ei-konfirmatorinen p-arvoanalyysi; ei osa ennalta määriteltyä testaushierarkiaa
3 Vahvistettu toimintakyvyn heikkeneminen (Confirmed Disability Progression, CDP) määritelty EDSS-pisteiden (Expanded Disability Status Scale) ≥ 1,0 pisteen suurenemiseksi lähtötilanteen pisteistä, jos potilaan lähtötilanteen pisteet ovat 5,5 tai vähemmän, tai ≥ 0,5 pisteen suurenemiseksi, kun lähtötilanteen pisteet ovat > 5,5; Kaplan–Meierin estimaatit viikolla 96
4 Määritelty EDSS-pisteiden ≥ 1,0 pisteen vähenemiseksi lähtötilanteesta, jos potilaan lähtötilanteen EDSS-pisteet ≥ 2 ja ≤ 5,5, tai ≥ 0,5 pisteen vähenemiseksi, kun lähtötilanteen pisteet ovat > 5,5. Potilaita, joiden lähtötilanteen pisteet olivat < 2, ei otettu mukaan analyysiin.
5 Tilanteeksi, jossa ei näyttöä taudin aktiivisuudesta (NEDA), on määritelty tutkimussuunnitelmassa määriteltyjen pahenemisvaiheiden puuttuminen, ei merkkiä 12 viikon vahvistetusta toimintakyvyn heikkenemisestä eikä mitään MK:ssa todettua aktiivisuutta (joko gadoliniumilla tehostuvia T1-muutoksia tai uusia tai laajenevia T2-muutoksia) koko 96 viikon hoidon aikana. Koko hoitoaikeen mukaiseen (ITT) potilasjoukkoon perustuvat eksploratiiviset tulokset.
6 Ei-konfirmatorinen p-arvo; hierarkkinen testaus lopetettu ennen päätetapahtuman saavuttamista.
7 Log-rank-testi
8 Varmistetut relapsit (joihin liittyy kliinisesti oleellinen EDSS-pisteiden muutos)
Kuva 1. Kaplan–Meier-kuvaaja ajankohtaan, jolloin todetaan toimintakyvyn heikkeneminen vähintään 12 viikon ajaksi ja jossa ensimmäinen havainto neurologisesta heikkenemisestä tehtiin kaksoissokkoutetun hoitojakson aikana (tutkimusten WA21092 ja WA21093 yhdistetty hoitoaikeen mukainen potilasjoukko)*
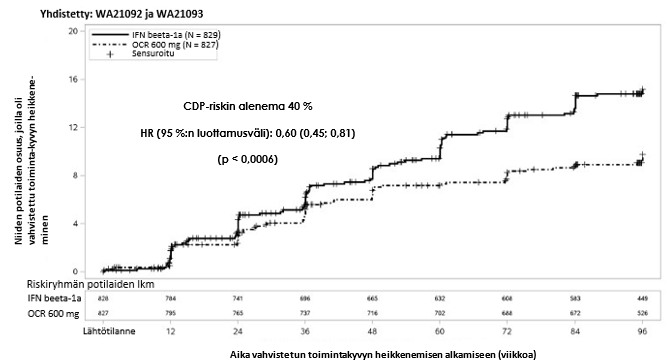
*Tutkimusten WA21092 ja WA21093 ennalta määritelty yhdistetty analyysi
Ennalta määritettyjen yhdistettyjen analyysien tulokset ajankohtaan, jolloin todetaan vähintään 12 viikkoa kestänyt vahvistettu toimintakyvyn heikkeneminen (riskin alenema okrelitsumabihoidossa 40 % verrattuna interferonibeeta-1a-hoitoon [p = 0,0006]) olivat erittäin yhdenmukaiset vähintään 24 viikon ajan kestäneen toimintakyvyn heikkenemisen tulosten kanssa (riskin alenema okrelitsumabihoidossa 40 % verrattuna interferonibeeta-1a-hoitoon, p = 0,0025).
Tutkimuksiin otettiin mukaan potilaita, joilla oli aktiivinen tauti. Potilaat eivät olleet aiemmin saaneet aktiivista hoitoa tai hoidon vaste oli ollut riittämätön kliinisten piirteiden tai kuvantamislöydösten perusteella. Analyysi potilasjoukoista, joissa taudin aktiivisuudessa oli lähtötilanteessa eroja, mukaan lukien aktiivinen tai erittäin aktiivinen tauti, osoitti okrelitsumabihoidon tehon vuosittaiseen pahenemisvaiheiden määrään ja 12 viikon vahvistettuun toimintakyvyn heikkenemiseen olevan yhdenmukainen koko potilasjoukossa.
Primaaristi etenevä MS-tauti
Okrelitsumabin tehoa ja turvallisuutta selvitettiin myös satunnaistetussa, kaksoissokkoutetussa, lumekontrolloidussa kliinisessä tutkimuksessa potilailla, jotka sairastavat primaaristi etenevää MS-tautia (tutkimus WA25046), joka oli tärkeimpien sisäänottokriteerien perusteella varhaisvaiheessa, eli potilaan ikä oli 18–55 vuotta, EDSS-pisteet olivat seulonnassa 3,0–6,5 pistettä, taudin kesto MS-oireiden alusta oli alle 10 vuotta, jos potilaan EDSS-pisteet olivat seulonnassa ≤ 5,0, tai alle 15 vuotta, jos potilaan EDSS-pisteet olivat seulonnassa > 5,0. Myös etenevässä MS-taudissa taudin aktiivisuudelle tyypillinen tulehdusaktiivisuus voi olla olla todettavissa kuvantamisella (eli Gd-tehosteiset T1‑muutokset ja/tai aktiiviset [uudet tai laajenevat] T2‑muutokset]). Tulehdusaktiivisuus pitäisi varmistaa kaikilla potilailla magneettikuvauksella. Yli 55-vuotiaita potilaita ei tutkittu. Tutkimusasetelma ja tutkimuksen potilasjoukon lähtötilanteen ominaisuudet esitetään taulukossa 4.
Demografiset tiedot ja lähtötilanteen ominaisuudet olivat hyvin tasapainossa näiden kahden hoitoryhmän välillä. Pään magneettikuvauksessa todettiin joko Gd-tehosteisten T1‑muutosten tai T2‑muutosten perusteella tulehdusaktiivisuudelle tyypillisiä piirteitä.
Primaaristi etenevää MS-tautia koskeneessa vaiheen III tutkimuksessa potilaat saivat 600 mg:n okrelitsumabiannoksen kuuden kuukauden välein kahtena kahden viikon välein annettuna 300 mg:n infuusiona koko hoitojakson ajan. Aaltomaista MS-tautia sairastaville potilaille annettujen 600 mg:n infuusioiden ja ensisijaisesti etenevää MS-tautia sairastaville potilaille kahtena 300 mg:n infuusiona annetun hoidon farmakokineettiset/farmakodynaamiset profiilit olivat yhdenmukaiset. Infuusioreaktiot olivat infuusiota kohden myös samankaltaiset riippumatta siitä, annettiinko 600 mg:n annos yhtenä 600 mg:n infuusiona vai kahtena 300 mg:n infuusiona kahden viikon välein (ks. kohdat Haittavaikutukset ja Farmakokinetiikka). Koska kahden 300 mg:n infuusion hoito-ohjelmassa annettiin kokonaisuudessaan enemmän infuusioita, infuusioreaktioiden kokonaismäärä oli kuitenkin suurempi. Näin ollen suositellaan, että 1. annoksen jälkeen okrelitsumabi annetaan 600 mg:n kertainfuusiona (ks. kohta Annostus ja antotapa) infuusioiden kokonaismäärän (sekä samanaikaisen altistuksen estohoitona annetulle metyyliprednisolonille ja antihistamiinille) sekä niihin liittyvien infuusioreaktioiden vähentämiseksi.
Taulukko 4. Tutkimuksen WA25046 tutkimusasetelma sekä demografiset ja lähtötilanteen tiedot
| Tutkimuksen nimi | Tutkimus WA25046 ORATORIO (n = 732) | |
| Tutkimusasetelma | ||
| Tutkimuksen potilasjoukko | Primaaristi etenevää MS-tautia sairastavat potilaat | |
| Tutkimuksen kesto | Tapahtumaperusteinen (vähintään 120 viikkoa ja 253 vahvistettua toimintakyvyn heikkenemiseen liittyvää tapahtumaa) (Seuranta-ajan mediaani: okrelitsumabi 3,0 vuotta, lumehoito 2,8 vuotta | |
| Sairaushistoria seulonnassa | Ikä 18–55 vuotta, EDSS-pisteet 3,0–6,5 | |
| Hoitoryhmät | Ryhmä A: okrelitsumabi 600 mg Ryhmä B: lumehoito, satunnaistettu suhteessa 2:1 | |
| Lähtötilanteen tiedot | Okrelitsumabi 600 mg (n = 488) | Lumehoito (n = 244) |
| Keskimääräinen ikä (vuotta) | 44,7 | 44,4 |
| Iän vaihteluväli (vuotta) tutkimuksen sisäänottovaiheessa | 20–56 | 18–56 |
| Sukupuolijakauma (% miehiä/% naisia) | 51,4/48,6 | 49,2/50,8 |
| Sairauden kestoajan keskiarvo/mediaani primaaristi etenevän MS-taudin diagnoosin jälkeen (vuotta) | 2,9/1,6 | 2,8/1,3 |
| Keskimääräiset EDSS-pisteet | 4,7 | 4,7 |
Keskeiset kliiniset ja magneettikuvauksella todetut tehon tulokset esitetään taulukossa 5 ja kuvassa 2.
Tämän tutkimuksen tulokset osoittavat, että okrelitsumabi hidastaa taudin etenemistä ja vähentää kävelynopeuden hidastumista merkitsevästi lumehoitoon verrattuna.
Taulukko 5. Tutkimuksen WA25046 (ensisijaisesti etenevä MS-tauti) keskeiset kliiniset ja magneettikuvauksen päätetapahtumat
| Tutkimus 3 | ||
| Päätetapahtumat | WA25046 (Oratorio) | |
Okrelitsumabi 600 mg (n = 488) | Lumehoito (n = 244) | |
| Kliiniset päätetapahtumat | ||
Ensisijainen tehon päätetapahtuma Niiden potilaiden osuus, joilla oli 12 viikon vahvistettu toimintakyvyn heikkeneminen (ensisijainen päätetapahtuma) Riskin alenema | 30,2 % | 34,0 % |
24 % (p = 0,0321) | ||
Niiden potilaiden osuus, joilla oli 24 viikon vahvistettu toimintakyvyn heikkeneminen1 Riskin alenema | 28,3 % | 32,7 % |
25 % (p = 0,0365) | ||
Kävelynopeustestin (Timed 25-Foot Walk) prosentuaalinen muutos lähtötilanteesta viikkoon 120 Kävelynopeuden hidastumisen suhteellinen vähenemä | 38,9 | 55,1 |
29,4 % (p = 0,0404) | ||
| Magneettikuvauksen päätetapahtumat | ||
| T2-hyperintensiivisten muutosten tilavuuden prosentuaalinen muutos lähtötilanteesta viikkoon 120 | -3,4 | 7,4 |
| (p < 0,0001) | ||
Aivojen tilavuuden prosentuaalinen muutos viikosta 24 viikkoon 120 Aivojen tilavuuden menetyksen suhteellinen vähenemä | -0,902 | -1,093 |
17,5 % (p = 0,0206) | ||
1 Määritelty EDSS-pisteiden (Expanded Disability Status Scale) ≥ 1,0 pisteen suurenemiseksi potilailla, joilla lähtötilanteen pisteet ≤ 5,5 tai ≥ 0,5 pisteen suurenemiseksi, kun lähtötilanteen pisteet ovat > 5,5; Kaplan–Meierin estimaatit viikolla 120
Kuva 2. Kaplan–Meier-kuvaaja* ajankohtaan, jolloin todetaan toimintakyvyn heikkeneminen vähintään 12 viikon ajaksi ja jossa ensimmäinen havainto neurologisesta heikkenemisestä tehtiin kaksoissokkoutetun hoitojakson aikana (tutkimuksen WA25046 hoitoaikeen mukainen potilasjoukko)*
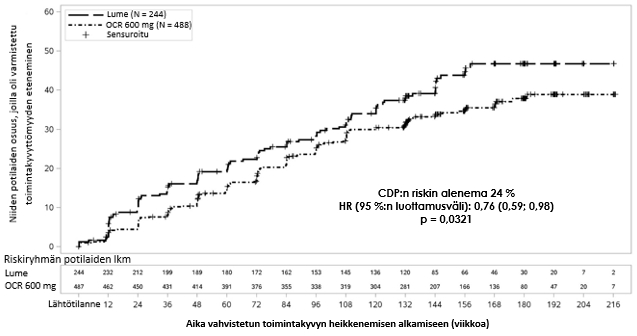
* Kaikkien tässä analyysissa mukana olevien potilaiden seuranta-aika oli vähintään 120 viikkoa. Ensisijainen analyysi perustuu kaikkiin kertyneisiin tapahtumiin.
Ennalta määritellyn, mutta tilastolliselta voimaltaan riittämättömän ensisijaisen päätetapahtuman alaryhmäanalyysi viittaa siihen, että nuoremmat potilaat tai potilaat, joilla oli lähtötilanteessa Gd‑tehosteisia T1‑muutoksia, saavat hoidosta suuremman hyödyn kuin iäkkäämmät potilaat tai potilaat, joilla ei ole Gd‑tehosteisia T1‑muutoksia (≤ 45 vuoden iässä: HR 0,64 [0,45, 0,92], > 45 vuoden iässä: HR 0,88 [0,62, 1,26]), joilla on Gd‑tehosteisia T1-muutoksia lähtötilanteessa (HR 0,65 [0,40–1,06]) tai joilla ei ole Gd‑tehosteisia T1‑muutoksia lähtötilanteessa (HR 0,84 [0,62–1,13]).
Post-hoc-analyysit viittasivat lisäksi siihen, että hoidon teho on parempi nuoremmilla potilailla, joilla on lähtötilanteessa Gd‑tehosteisia T1‑muutoksia (≤ 45 vuoden iässä: HR 0,52 [0,27–1,00], ≤ 46 vuoden iässä [iän mediaani tutkimuksessa WA25046]; HR 0,48 [0,25–0,92], < 51 vuoden iässä: HR 0,53 [0,31–0,89]).
Jatketun kontrolloidun jakson (Extended Controlled Period, ECP) osalta, joka käsitti kaksoissokkoutetun hoitojakson ja noin 9 lisäkuukauden pituisen kontrolloidun seurantajakson ennen siirtymistä avoimeen jatkovaiheeseen (Open-Label Extension, OLE) tai tutkimushoidosta vetäytymiseen saakka, tehtiin post-hoc-analyysit. Niiden potilaiden osuus, joilla 24 viikon vahvistettua toimintakyvyn heikkenemistä (24-week Confirmed Disease Progression, 24W-CDP) osoittavat EDSS-pisteet olivat ≥ 7,0 (EDSS 24W-CDP ≥ 7,0, pyörätuolin tarpeeseen kuluva aika), oli lumeryhmässä 9,1 % verrattuna 4,8 %:iin okrelitsumabiryhmässä viikolla 144, mikä tarkoittaa 47 % riskin alenemista (HR 0,53, [0,31–0,92]) pyörätuolin tarpeeseen kuluvan ajan osalta jatketun kontrolloidun jakson aikana. Nämä tulokset olivat luonteeltaan eksploratiivisia ja sisälsivät sokkouttamisen avaamisen jälkeiset tiedot, joten tuloksia pitää tulkita harkiten.
Immunogeenisuus
Ihon alle annettava lääkemuoto
OCARINA I- ja OCARINA II ‑tutkimuksissa yhdelläkään potilaalla ei todettu hoidon aikana ilmenneitä vasta-aineita okrelitsumabia kohtaan. OCARINA II -tutkimuksen potilaat testattiin vasta-aineiden varalta lähtötilanteessa ja kuuden kuukauden välein annetun hoidon jälkeen koko tutkimuksen keston ajan. Ohimeneviä vasta-aineita ei siksi välttämättä havaittu testausajankohtien välissä.
Hoidon aikana ilmenneiden anti-rHuPH20 (hyaluronidaasi) ‑vasta-aineiden ilmaantuvuus OCARINA I ‑tutkimuksessa ihon alle annettavaa okrelitsumabihoitoa saaneilla potilailla oli 2,3 % (3/132). OCARINA II ‑tutkimuksessa yhdelläkään potilaalla ei todettu hoidon aikana ilmenneitä anti-rHuPH20-vasta-aineita.
Laskimoon annettava lääkemuoto
MS-tutkimuksissa (WA21092, WA21093 ja WA25046) mukana olleilta potilailta testattiin useana ajankohtana (lähtötilanteessa ja kuuden kuukauden välein annetun hoidon jälkeen koko tutkimuksen keston ajan) vasta-aineet lääkevalmisteelle. Okrelitsumabihoitoa saaneista 1 311 potilaasta 12 potilasta (~1 %) kehitti vasta-aineita lääkettä kohtaan, ja näistä kahdella potilaalla oli neutraloivia vasta-aineita. Hoidosta aiheuttamien lääkevasta-aineiden vaikutusta turvallisuuteen ja tehoon ei voida arvioida, koska okrelitsumabihoitoon liittyneiden vasta-aineiden ilmaantuvuus on pieni.
Immunisaatio
Aaltomaista MS-tautia sairastavilla potilailla (N = 102) tehdyssä satunnaistetussa avoimessa tutkimuksessa niiden potilaiden prosenttiosuus, jotka saivat positiivisen vasteen tetanusrokotteeseen kahdeksan viikkoa rokotuksen jälkeen, oli laskimoon annettavaa okrelitsumabia saaneessa ryhmässä 23,9 % ja vertailuryhmässä 54,5 % (ei taudinkulkua muuntavaa hoitoa paitsi interferonibeeta). Antitetanustoksoidispesifisten vasta-ainetiitterien geometrinen keskiarvo viikolla kahdeksan oli okrelitsumabiryhmässä 3,74 IU/ml ja vertailuryhmässä 9,81 IU/ml. Positiivinen vaste vähintään viidelle PPV23-rokotteen sisältämälle serotyypille todettiin 71,6 %:lla potilaista laskimoon annettavaa okrelitsumabia saaneessa ryhmässä ja 100 %:lla potilaista vertailuryhmässä neljä viikkoa rokotuksen jälkeen. Laskimoon annettavalla okrelitsumabilla hoitoa saaneille potilaille neljä viikkoa PPV23-rokotuksen jälkeen annettu tehosterokotus (PCV13) ei lisännyt merkittävästi vastetta niille 12 serotyypille, jotka olivat samoja kuin PPV23-rokotteessa. Potilaiden prosenttiosuus, joilla oli suojaava serologinen tiitteri viittä influenssakantaa vastaan, oli ennen rokotusta laskimoon annettavaa okrelitsumabia saaneessa ryhmässä 20,0−60,0 % ja vertailuryhmässä 16,7−43,8 %. Neljä viikkoa rokotuksen jälkeen prosenttiosuus oli laskimoon annettavaa okrelitsumabia saaneessa ryhmässä 55,6−80,0 % ja vertailuryhmässä 75,0−97,0 %. Ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Yhteisvaikutukset.
Pediatriset potilaat
Euroopan lääkevirasto on myöntänyt lykkäyksen velvoitteelle toimittaa tutkimustulokset Ocrevus-valmisteen käytöstä yhden tai useamman pediatrisen potilasryhmän MS-taudin hoidossa. Ks. kohta Annostus ja antotapa ohjeet käytöstä pediatristen potilaiden hoidossa.
Farmakokinetiikka
Okrelitsumabin farmakokinetiikkaa MS-tutkimuksissa kuvasi kaksitilamalli, jossa puhdistuma on aikariippuvainen, ja jossa oli IgG1-monoklonaaliselle vasta-aineelle tyypilliset farmakokineettiset parametrit.
Ennustettu keskimääräinen altistus (AUC 24 viikon antovälin aikana) ihonalaisen 920 mg:n okrelitsumabiannoksen antamisen jälkeen oli 3730 mikrog/ml•vrk. OCARINA II ‑tutkimuksessa ensisijaisen farmakokineettisen päätetapahtuman eli 920 mg:n ihonalaisen okrelitsumabiannoksen antamisen jälkeisen AUCw1-12-arvon osoitettiin olevan vähintään yhdenveroinen (non-inferior) laskimoon annettavan okrelitsumabin 600 mg:n annoksen antamiseen nähden. AUCw1-12-arvon geometrisen keskiarvon suhde oli 1,29 (90 %:n luottamusväli: 1,23–1,35).
Imeytyminen
Arvioitu biologinen hyötyosuus ihon alle annetun 920 mg:n okrelitsumabiannoksen jälkeen oli 81 %. Cmax-arvon keskiarvo oli 132 mikrog/ml, ja tmax saavutettiin noin 4 vuorokauden kuluttua (vaihteluväli 2–13 vuorokautta).
Jakautuminen
Keskusjakautumistilavuuden populaatiofarmakokineettinen arvio oli 2,78 l. Perifeeriseksi tilavuudeksi arvioitiin 2,68 l, ja tilojen väliseksi puhdistumaksi arvioitiin 0,294 l/vrk.
Biotransformaatio
Okrelitsumabin metaboliaa ei ole tutkittu suoraan, sillä vasta-aineet puhdistuvat pääasiassa katabolian kautta (eli hajoavat peptideiksi ja aminohapoiksi).
Eliminaatio
Vakiopuhdistumaksi arvioitiin 0,17 l/vrk, ja alkuvaiheen aikariippuvaiseksi puhdistumaksi arvioitiin 0,0489 l/vrk, mikä väheni 33 viikon puoliintumisajan mukaan. Okrelitsumabin terminaalisen eliminaation puoliintumisaika oli 26 vuorokautta.
Erityisryhmät
Pediatriset potilaat
Okrelitsumabin farmakokinetiikkaa ei ole tutkittu alle 18-vuotiailla lapsilla ja nuorilla.
Iäkkäät
Okrelitsumabilla ei ole tehty erityisesti vähintään 55-vuotiaita potilaita koskevia farmakokineettisiä tutkimuksia, koska kliinistä kokemusta on vain vähän (ks. kohta Annostus ja antotapa).
Munuaisten vajaatoiminta
Varsinaisia farmakokineettisiä tutkimuksia ei ole tehty. Kliinisissä tutkimuksissa oli mukana lievää munuaisten vajaatoimintaa sairastavia potilaita eikä okrelitsumabin farmakokinetiikassa havaittu tässä potilasryhmässä muutoksia. Keskivaikeaa ja vaikeaa munuaisten vajaatoimintaa sairastavista potilaista ei ole farmakokineettisiä tietoja saatavissa.
Maksan vajaatoiminta
Varsinaisia farmakokineettisiä tutkimuksia ei ole tehty. Kliinisissä tutkimuksissa oli mukana lievää maksan vajaatoimintaa sairastavia potilaita eikä farmakokinetiikassa havaittu tässä potilasryhmässä muutoksia. Keskivaikeaa ja vaikeaa maksan vajaatoimintaa sairastavista potilaista ei ole farmakokineettisiä tietoja saatavissa.
Prekliiniset tiedot turvallisuudesta
Farmakologista turvallisuutta, toistuvan altistuksen aiheuttamaa toksisuutta sekä alkion ja sikiön kehitystä koskevien perinteisten ei-kliinisten tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille. Okrelitsumabilla ei ole tehty karsinogeenisuus- eikä mutageenisuustutkimuksia.
Kahdessa Cynomolgus-apinoilla tehdyssä pre- ja postnataalista kehitystä koskevassa tutkimuksessa laskimoon annettavan okrelitsumabin antoon tiineyspäivästä 20 vähintään synnytykseen saakka liittyi jälkeläisillä glomerulopatiaa, lymfoidisten follikkelien muodostumista luuytimeen, lymfoplasmasyyttistä munuaistulehdusta ja kivesten painon vähenemistä. Näissä tutkimuksissa emolle annetuista annoksista aiheutuneet suurimmat keskiarvopitoisuudet (Cmax) seerumissa olivat 4,5–21-kertaisia kliinisessä käytössä oletettaviin pitoisuuksiin nähden.
Viiteen tapaukseen liittyi neonataalikuolleisuutta. Yhdessä tapauksessa kyse oli keskosuuteen liittyvästä heikkoudesta, mihin liittyi opportunistinen bakteeri-infektio, yhdessä tapauksessa emon aktiivisesta bakteeri-infektiosta (mastiitti) aiheutui vastasyntyneelle jälkeläiselle pikkuaivojen infektiivinen meningoenkefaliitti ja kolmessa tapauksessa havaittiin ikterusta ja maksavaurio, joiden epäiltiin olleen virusperäisiä, mahdollisesti polyoomaviruksen aiheuttamia. B-solujen puutos on saattanut vaikuttaa näihin viiteen varmistettuun tai epäiltyyn infektioon. Okrelitsumabille altistuneiden emojen vastasyntyneillä jälkeläisillä havaittiin vähentyneitä B-solupopulaatioita heti syntymän jälkeen.
Hyaluronidaasi
Rekombinanttia ihmisen hyaluronidaasia koskevat konventionaalisten tutkimusten prekliiniset tiedot, mukaan lukien farmakologista turvallisuutta koskevat päätetapahtumat, eivät viittaa erityiseen vaaraan.
Hyaluronidaasia (rHuPH20) on useimmissa ihmisen elimistön kudoksissa. Kun okrelitsumabia annettiin ihon alle paikallista siedettävyyttä koskeneissa tutkimuksissa, rotat ja minisiat sietivät hyaluronidaasin hyvin.
rHuPH20:lla tehdyissä lisääntymistoksikologisissa tutkimuksissa hiirillä todettiin alkioon ja sikiöön kohdistuvaa toksisuutta vaikutuksettomalla altistustasolla (no effect level), joka oli > 1 100 kertaa ehdotettua kliinistä annosta suurempi, mutta teratogeenisuutta ei havaittu.
Farmaseuttiset tiedot
Apuaineet
Rekombinantti ihmisen hyaluronidaasi (rHuPH20)
Natriumasetaattitrihydraatti (E 262)
Väkevä etikkahappo
α,α-trehaloosidihydraatti
Polysorbaatti 20 (E 432)
L‑metioniini
Injektionesteisiin käytettävä vesi
Yhteensopimattomuudet
Koska yhteensopivuustutkimuksia ei ole tehty, tätä lääkevalmistetta ei saa sekoittaa muiden lääkevalmisteiden kanssa.
Kestoaika
Avaamaton injektiopullo
2 vuotta
Käyttöön valmisteltu ruisku
- Käytönaikaiseksi kemialliseksi ja fysikaaliseksi säilyvyydeksi on osoitettu 30 päivää 2–8 °C:ssa ja lisäksi 8 tuntia valolta suojaamattomana ≤ 30 °C:ssa.
- Mikrobiologiselta kannalta valmiste pitää käyttää välittömästi sen jälkeen, kun se on siirretty injektiopullosta ruiskuun. Jos valmistetta ei käytetä välittömästi, käytönaikaiset säilytysajat ja ‑olosuhteet ennen käyttöä ovat käyttäjän vastuulla eivätkä saa normaalisti ylittää 24 tuntia 2–8 °C:ssa, ellei valmistelua ole tehty kontrolloiduissa ja validoiduissa aseptisissa olosuhteissa.
Säilytys
Säilytä jääkaapissa (2 °C – 8 ºC).
Ei saa jäätyä. Ei saa ravistaa.
Pidä injektiopullot ulkopakkauksessa. Herkkä valolle.
Avaamatonta injektiopulloa voidaan tarvittaessa säilyttää poissa jääkaapista ≤ 25 °C:een lämpötilassa enintään 12 tuntia.
Injektiopullot voidaan ottaa jääkaapista ja palauttaa sinne takaisin siten, että avaamattoman injektiopullon yhdistetty kokonaisaika poissa jääkaapista ei saa ylittää 12 tuntia ≤ 25 °C:ssa.
Käyttöön valmistellun ruiskun säilytys, ks. kohta Kestoaika.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
OCREVUS injektioneste, liuos
920 mg (L:ei) 1 kpl (23 ml (40 mg/ml)) (12540,75 €)
PF-selosteen tieto
23 ml injektionestettä, liuosta, injektiopullossa (väritöntä tyypin I lasia).
Pakkauskoko: 1 injektiopullo.
Valmisteen kuvaus:
Kirkas tai hieman opaalinhohtoinen, ja väritön tai vaaleanruskehtava liuos.
Käyttö- ja käsittelyohjeet
Lääkevalmiste pitää tarkastaa ennen antoa silmämääräisesti sen varmistamiseksi, ettei siinä ole hiukkasia eikä värimuutoksia.
Lääkevalmiste on kertakäyttöinen, ja terveydenhuollon ammattilaisen pitää valmistella se aseptista tekniikkaa noudattaen.
Yhteensopimattomuuksia ei ole havaittu tämän lääkevalmisteen ja polypropeenin (PP), polykarbonaatin (PC), polyeteenin (PE), polyvinyylikloridin (PVC), polyuretaanin (PUR) ja ruostumattoman teräksen välillä.
Ruiskun valmistelu
- Ota injektiopullo jääkaapista ennen käyttöä ja anna liuoksen lämmetä huoneenlämpöiseksi.
- Vedä injektiopullon koko sisältö ihon alle annettavaa Ocrevus-liuosta ruiskuun siirtoneulaa (suositus 21G) käyttäen.
- Irrota siirtoneula ja kiinnitä ihon alle antoon tarkoitetut infuusiovälineet (esim. siipi-/perhosneula), joissa on 24–26G:n injektioneula. Käytä ihon alle antoon tarkoitettuja infuusiovälineitä, joihin annon yhteydessä jäävä jäännöstilavuus on ENINTÄÄN 0,8 ml.
- Esitäytä ihon alle antoon tarkoitettu infuusioletku lääkevalmisteliuoksella, jotta ilma poistuu infuusioletkusta. Lopeta esitäyttö ennen kuin nestettä pääsee neulaan.
- Varmista, että esitäytön ja mahdollisen ylimäärän ruiskusta poistamisen jälkeen ruisku sisältää tarkalleen 23 ml lääkevalmisteliuosta.
- Anna välittömästi, jotta vältät neulan tukkeutumisen. Käyttöön valmisteltua ruiskua, johon on kiinnitetty esitäytetyt ihon alle antoon tarkoitetut infuusiovälineet, ei saa säilyttää.
Jos annosta ei anneta välittömästi, katso jäljempänä kohta ”Ruiskun säilytys”.
Ruiskun säilytys
- Jos annosta ei ole tarkoitus antaa välittömästi, vedä injektiopullon koko sisältö ihon alle annettavaa Ocrevus-liuosta ruiskuun aseptista tekniikkaa noudattaen siten, että ruisku sisältää annoksen tilavuuden (23 ml) ja ihon alle antoon tarkoitettujen infuusiovälineiden esitäyttötilavuuden. Vaihda siirtoneulan tilalle ruiskun korkki. Ihon alle antoon tarkoitettuja infuusiovälineitä ei saa kiinnittää säilytyksen ajaksi.
- Jos ruiskua on säilytetty jääkaapissa, anna ruiskun lämmetä huoneenlämpöiseksi ennen valmisteen antamista.
Hävittäminen
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
OCREVUS injektioneste, liuos
920 mg 1 kpl
- Ei korvausta.
ATC-koodi
L04AG08
Valmisteyhteenvedon muuttamispäivämäärä
13.02.2025
Yhteystiedot
Revontulenpuisto 2 C, P.O. Box 112
02101 Espoo
010 554 500
www.roche.fi
etunimi.sukunimi@roche.com

 ROCHE OY
ROCHE OY