NEMLUVIO injektiokuiva-aine ja liuotin, liuosta varten, esitäytetty kynä 30 mg
Huomioitavaa
▼ Tähän lääkevalmisteeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan epäillyistä lääkkeen haittavaikutuksista. Ks. kohdasta Haittavaikutukset, miten haittavaikutuksista ilmoitetaan.
Vaikuttavat aineet ja niiden määrät
Nemluvio 30 mg injektiokuiva-aine ja liuotin, liuosta varten, esitäytetty kynä
Yksi kertakäyttöinen esitäytetty kynä sisältää 30 mg nemolitsumabia 0,49 ml:n annosta kohti käyttökuntoon saattamisen jälkeen.
Nemolitsumabi, humanisoitu monoklonaalinen modifioitu immunoglobuliini G (IgG) -vasta-aine, tuotetaan yhdistelmä-DNA-tekniikalla kiinanhamsterin munasarjasoluissa.
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Injektiokuiva-aine ja liuotin, liuosta varten
Kliiniset tiedot
Käyttöaiheet
Atooppinen ihottuma (AD)
Nemluvio on tarkoitettu keskivaikean tai vaikean atooppisen ihottuman hoitoon vähintään 12-vuotiaille potilaille, joille voidaan antaa systeemistä hoitoa.
Kyhmykutina (PN)
Nemluvio on tarkoitettu keskivaikean tai vaikean kyhmykutinan hoitoon aikuisille, joille voidaan antaa systeemistä hoitoa.
Ehto
Valmisteen käyttöaiheissa mainittujen sairauksien hoitoon perehtyneen lääkärin on aloitettava hoito ja valvottava sitä.
Annostus ja antotapa
Nemolitsumabihoidon aloittavat ja sitä valvovat terveydenhuollon ammattilaiset, jotka ovat perehtyneet nemolitsumabin käyttöaiheiden diagnosointiin ja hoitoon.
Annostus
Atooppinen ihottuma (AD)
Suositeltu annos on:
- 60 mg:n aloitusannos (kaksi 30 mg:n injektiota), jonka jälkeen annetaan 30 mg neljän (4) viikon välein
- 16 viikon hoidon jälkeen suositeltu ylläpitoannos kliinisen vasteen saavuttaneille potilaille on 30 mg kahdeksan (8) viikon välein
Nemolitsumabia voidaan käyttää paikalliskortikosteroidien (TCS) kanssa tai ilman niitä. Paikallisia kalsineuriinin estäjiä (TCI) voidaan käyttää, mutta niiden käytön on rajoituttava vain ongelma-alueille, kuten kasvojen ja kaulan alueelle, intertriginoosiselle alueelle ja genitaalialueille. Paikallishoitojen käyttöä on vähennettävä ja ne on lopetettava, kun sairaus on lievittynyt riittävästi.
Hoidon keskeyttämistä on harkittava potilailla, joilla ei ole ilmennyt vastetta 16 viikon pituisen atooppisen ihottuman hoidon jälkeen. Joidenkin alkuvaiheessa osittaisen vasteen saavuttaneiden potilaiden tila saattaa kohentua edelleen jatkettaessa hoitoa viikon 16 jälkeen.
Kun kliininen vaste on saavutettu, nemolitsumabin suositeltu ylläpitoannos on 30 mg kahdeksan (8) viikon välein.
Kyhmykutina (PN)
Suositeltu annos < 90 kg painaville potilaille on 60 mg:n aloitusannos (kaksi 30 mg:n injektiota), jonka jälkeen annetaan 30 mg neljän (4) viikon välein.
Suositeltu annos ≥ 90 kg painaville potilaille on 60 mg:n aloitusannos (kaksi 30 mg:n injektiota), jonka jälkeen annetaan 60 mg neljän (4) viikon välein.
Hoidon keskeyttämistä on harkittava potilailla, joilla ei ole ilmennyt vastetta kutinan osalta 16 viikon pituisen kyhmykutinan hoidon jälkeen.
Annoksen jääminen väliin
Jos annos jää väliin, se on annettava mahdollisimman pian. Tämän jälkeen annostusta on jatkettava normaalin aikataulun mukaisesti.
Erityisryhmät
Iäkkäät (≥ 65-vuotiaat)
Iäkkäiden potilaiden annoksen muuttamista ei suositella (ks. kohta Farmakokinetiikka).
Maksan ja munuaisten vajaatoiminta
Annosta ei tarvitse muuttaa potilaille, joilla on maksan tai munuaisten vajaatoiminta (ks. kohta Farmakokinetiikka).
Pediatriset potilaat
Atooppinen ihottuma
Nemolitsumabin turvallisuutta ja tehoa alle 12 vuoden ikäisten ja alle 30 kg painavien lasten hoidossa ei ole vielä varmistettu. Tietoja ei ole saatavilla.
Kyhmykutina
Nemolitsumabin turvallisuutta ja tehoa alle 18 vuoden ikäisten lasten hoidossa ei ole varmistettu. Tietoja ei ole saatavilla.
Antotapa
Ihon alle.
Ihonalainen injektio on annettava etureiteen tai vatsaan siten, että navan ympärillä olevaa 5 cm:n aluetta vältetään. Vain omaishoitaja tai terveydenhuollon ammattilainen saa antaa injektion olkavarteen.
Jokaisen seuraavan annoksen kohdalla on suositeltavaa kierrättää pistoskohtaa. Nemolitsumabia ei saa injisoida ihoon, joka on arka, tulehtunut, turvonnut tai vaurioitunut tai jossa on mustelmia, arpia tai avohaavoja.
Nemolitsumabi on tarkoitettu käytettäväksi terveydenhuollon ammattilaisen ohjauksessa. Potilas voi injisoida nemolitsumabin itse, tai potilaan omaishoitaja voi antaa nemolitsumabin, jos potilasta hoitava terveydenhuollon ammattilainen katsoo tämän olevan asianmukaista. Ennen ensimmäistä injektiota potilaille ja/tai omaishoitajille on annettava asianmukainen koulutus nemolitsumabin valmisteluun ja antamiseen pakkausselosteen lopussa olevien käyttöohjeiden mukaisesti.
Vasta-aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille.
Varoitukset ja käyttöön liittyvät varotoimet
Jäljitettävyys
Biologisten lääkevalmisteiden jäljitettävyyden parantamiseksi on annetun valmisteen nimi ja eränumero dokumentoitava selkeästi.
Yliherkkyys
Tyypin 1 yliherkkyyden tapauksia, mukaan lukien angioedeema, on raportoitu. Jos systeeminen yliherkkyysreaktio (välitön tai viiveellä tuleva) ilmenee, nemolitsumabin antaminen on keskeytettävä välittömästi ja asianmukainen hoito on aloitettava (ks. kohta Haittavaikutukset).
Astman paheneminen (mukaan lukien PEF-arvon heikkeneminen)
Kyhmykutinaa sairastavilla potilailla, joilla on olemassa oleva astma, astman lievää tai kohtalaista pahenemista on raportoitu nemolitsumabihoidon aloittamisen jälkeen. Tätä on havaittu yleisemmin > 90 kg painavilla potilailla, jotka saivat 60 mg nemolitsumabia neljän viikon välein, kuin < 90 kg painavilla potilailla, jotka saivat 30 mg nemolitsumabia neljän viikon välein (ks. kohta Haittavaikutukset).
Kliinisistä tutkimuksista suljettiin pois potilaat, joilla oli sairaalahoitoa edellyttänyt astman paheneminen edeltävien 12 kuukauden aikana; potilaat, joilla oli kontrolloimaton astma edeltävien kolmen kuukauden aikana sekä potilaat, joilla oli tämänhetkinen keuhkoahtaumataudin ja/tai kroonisen bronkiitin historia. Tietoa nemolitsumabin tehosta tai turvallisuudesta näillä potilailla ei ole saatavilla.
Rokotukset
On suositeltavaa, että potilaat ottavat kaikki iänmukaiset rokotukset voimassa olevien rokotusohjeiden mukaisesti ennen hoidon aloittamista. Eläviä taudinaiheuttajia sisältävien rokotteiden samanaikaista käyttöä nemolitsumabilla hoidetuille potilaille on vältettävä. Ei tiedetä, vaikuttaako eläviä taudinaiheuttajia sisältävien rokotteiden antaminen hoidon aikana näiden rokotteiden turvallisuuteen tai tehoon. Ei-eläviä taudinaiheuttajia sisältävien rokotteiden vasteesta ei ole saatavilla tietoja.
Yhteisvaikutukset
Eläviä taudinaiheuttajia sisältävät rokotteet
Nemolitsumabin ja eläviä heikennettyjä taudinaiheuttajia sisältävien rokotteiden samanaikaisen käytön turvallisuutta ja tehoa ei ole tutkittu. Eläviä taudinaiheuttajia sisältäviä rokotteita ei pidä antaa samanaikaisesti nemolitsumabin kanssa (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Ei-eläviä taudinaiheuttajia sisältävät rokotteet
Nemolitsumabin ja ei-eläviä taudinaiheuttajia sisältävien rokotteiden samanaikaisen käytön turvallisuutta ja tehoa ei ole tutkittu (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Yhteisvaikutukset sytokromi P450:n kanssa
Nemolitsumabin vaikutuksia midatsolaamin (CYP3A4/5:n substraatti), varfariinin (CYP2C9:n substraatti), omepratsolin (CYP2C19:n substraatti), metoprololin (CYP2D6:n substraatti) ja kofeiinin (CYP1A2:n substraatti) farmakokinetiikkaan arvioitiin tutkimuksessa, jossa oli mukana keskivaikeaa tai vaikeaa atooppista ihottumaa sairastavia tutkittavia. CYP450-substraattien altistuksessa ei havaittu kliinisesti merkittäviä muutoksia verrattuna tilanteeseen ennen nemolitsumabihoitoa. Annoksen muuttaminen ei ole tarpeen.
Raskaus ja imetys
Raskaus
Nemolitsumabin käytöstä raskaana oleville naisille on vain vähän tietoja. Eläimillä tehdyissä tutkimuksissa ei ole havaittu suoria tai epäsuoria lisääntymistoksisia vaikutuksia (ks. kohta Prekliiniset tiedot turvallisuudesta). Varmuuden vuoksi nemolitsumabin käyttöä on suositeltavaa välttää raskauden aikana.
Imetys
Ei tiedetä, erittyykö nemolitsumabi ihmisillä äidinmaitoon. Ihmisillä IgG-vasta-aineiden erittyminen äidinmaitoon tapahtuu ensimmäisinä päivinä syntymän jälkeen ja vähenee pian sen jälkeen pieniin pitoisuuksiin. Näin ollen IgG-vasta-aineiden siirtyminen vastasyntyneille voi tapahtua äidinmaidon välityksellä ensimmäisten päivien aikana. Tänä lyhyenä ajanjaksona imetettävään lapseen kohdistuvia riskejä ei voida sulkea pois. Tämän jälkeen nemolitsumabia voidaan käyttää imetyksen aikana, jos se on kliinisesti tarpeen.
Hedelmällisyys
Eläimillä tehdyissä tutkimuksissa ei ole havaittu hedelmällisyyden heikentymistä (ks. kohta Prekliiniset tiedot turvallisuudesta).
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Nemluvio-valmisteella ei ole haitallista vaikutusta ajokykyyn ja koneidenkäyttökykyyn.
Haittavaikutukset
Turvallisuusprofiilin yhteenveto
Yleisimmät haittavaikutukset atooppista ihottumaa ja kyhmykutinaa sairastavilla ovat tyypin I yliherkkyys (1,1%; sisältää urtikarian 1,0% ja angioedeeman 0,1%) ja injektiokohdan reaktiot (1,2%) (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet). Muita haittavaikutuksia, kuten päänsärkyä (7,0%), atooppista ihottumaa (4,6%), ekseemaa (3,8%), nummulaarista ekseemaa (3,5%), pinnallisia sieni-infektioita (3,0%) ja astman pahenemista (2,2%) raportoitiin kyhmykutinaa sairastavilla.
Taulukkomuotoinen luettelo haittavaikutuksista
Taulukko 1 sisältää kaikki kliinisissä tutkimuksissa havaitut haittavaikutukset elinjärjestelmäluokan ja esiintyvyyden mukaan jaoteltuina, seuraavia luokkia käyttäen: hyvin yleinen (≥ 1/10); yleinen (≥ 1/100, < 1/10); melko harvinainen (≥ 1/1 000, < 1/100); harvinainen (≥ 1/10 000, < 1/1 000); hyvin harvinainen (< 1/10 000). Haittavaikutukset esitetään kussakin esiintyvyysluokassa vakavuuden mukaan alenevassa järjestyksessä.
Taulukko 1: Luettelo haittavaikutuksista
| MedDRA-elinjärjestelmäluokka | Esiintyvyys | Haittavaikutukset |
| Infektiot | Yleinen | Pinnalliset sieni-infektiot*# |
| Veri ja imukudos | Melko harvinainen | Eosinofilia† |
| Immuunijärjestelmä | Yleinen | Tyypin I yliherkkyys (ml. urtikaria† ja angioedeema*) |
| Hermosto | Yleinen | Päänsärky* (ml. jännityspäänsärky) |
| Hengityselimet, rintakehä ja välikarsina | Yleinen | Astman paheneminen* (mukaan lukien astma, hengityksen vinkuminen, PEF-arvon heikkeneminen) |
| Iho ja ihonalainen kudos | Yleinen Melko harvinainen | Atooppinen ihottuma* Ekseema* Nummulaarinen ekseema* Rakkulainen pemfigoidi§ |
| Yleisoireet ja antopaikassa todettavat haitat | Yleinen | Injektiokohdan reaktiot (sis. seuraavat: eryteema, kutina, hematooma†, kipu†, ärsytys†, mustelmat* ja injektiokohdan edeema†) |
†Esiintyi atooppista ihottumaa koskevissa tutkimuksissa
*Esiintyi kyhmykutinaa koskevissa tutkimuksissa
#Pinnalliset sieni-infektiot sisältävät seuraavat: kehon silsa, jalkasilsa, kynsisieni, sieni-infektio, savipuoli, nivussilsa, ihon sieni-infektio ja jalan sieni-infektio
§Markkinoille saattamisen jälkeisestä raportoinnista
Valittujen haittavaikutusten kuvaus
Yliherkkyys
Tyypin 1 yliherkkyysreaktioita (Ig-E-välitteisiä reaktioita), mukaan lukien lievä urtikaria ja lievä kasvojen (periokulaarinen) angioedeema, havaittiin yleisesti nemolitsumabilla hoidetuilla tutkittavilla kliinisten tutkimusten aikana. Nämä reaktiot eivät johtaneet hoidon keskeyttämiseen (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Päänsärky
Kyhmykutinaa sairastavilla potilailla päänsärkyä raportoitiin useammin nemolitsumabihoitoa saaneilla potilailla (7,0 %) kuin lumelääkkeellä hoidetuilla potilailla. Päänsärkyä havaittiin useammin naispotilailla molemmissa ryhmissä. Nemolitsumabiryhmässä päänsärky oli voimakkuudeltaan yleensä lievää tai kohtalaista eikä johtanut hoidon keskeyttämiseen.
Astman paheneminen
Niistä kyhmykutinaa sairastavista potilaista, joilla oli olemassa oleva astma (n=51), kahdeksalla (15,7 %) potilaalla ilmeni astman paheneminen nemolitsumabihoidon aloittamisen jälkeen. Viidellä heistä paino oli > 90 kg ja he saivat 60 mg nemolitsumabia neljän viikon välein. Kyhmykutinaa sairastavilla potilailla, joilla oli olemassa oleva astma, astman paheneminen oli kolme kertaa yleisempää potilailla, joiden paino oli > 90 kg ja jotka saivat 60 mg nemolitsumabia neljän viikon välein, kuin potilailla, joiden paino oli < 90 kg ja jotka saivat 30 mg nemolitsumabia neljän viikon välein.
Suurin osa astman pahenemisen tapahtumista ilmeni ensimmäisten kahden kuukauden aikana hoidon aloittamisesta, ja kaikkien niiden vaikeusasteeksi raportoitiin lievä tai kohtalainen. Suurimmalle osalle potilaista tuli yksi astman pahenemisvaihe hoidon aikana, ja tämä tapahtuma lievittyi astman standardilääkityksellä (inhalaattoreilla) ilman systeemisten steroidien käyttöä. Yksikään astman pahenemisen tapahtuma ei johtanut hoidon pysyvään lopettamiseen. Astman pahenemisen esiintyvyys ei lisääntynyt pidempiaikaisen nemolitsumabille altistumisen (viikolle 52 saakka) myötä kyhmykutinan avoimessa pitkäkestoisessa jatkotutkimuksessa.
Eksematoottiset reaktiot
Kyhmykutinaa sairastavilla nemolitsumabihoitoa saaneilla potilailla raportoitiin useammin eksematoottisia reaktioita, kuten atooppista ihottumaa, nummulaarista ekseemaa tai ekseemaa, kuin lumelääkettä saaneilla potilailla: Atooppinen ihottuma (4,6 %), ekseema (3,8 %) ja nummulaarinen ekseema (3,5 %), eli eksematoottiset reaktiot, olivat vaikeusasteeltaan lieviä tai kohtalaisia. Atooppinen ihottuma johti nemolitsumabihoidon keskeyttämiseen kahdella (0,5%) potilaalla. Vähintään 65-vuotiailla potilailla oli enemmän eksematoottisia reaktioita.
Eosinofilia
Niiden potilaiden suhteellinen osuus, joilla oli kliinisesti merkittävästi koholla oleva eosinofiilien määrä (> 700 solua/mikrol) oli 10,2 % atooppista ihottumaa sairastavien populaatiossa (alkujakson aikana) ja 5,5 % kyhmykutinaa sairastavien populaatiossa. Vaikeaa eosinofiliaa (> 5 000 solua/mikrol) ei havaittu atooppista ihottumaa sairastavilla nemolitsumabihoitoa saaneilla potilailla ensimmäisen hoitojakson aikana viikolle 16 mennessä. Haittavaikutuksena eosinofiliaa raportoitiin 0,2 %:lla atooppista ihottumaa sairastavista potilaista, joita hoidettiin nemolitsumabilla alkuhoitojakson aikana. Kaikki atooppista ihottumaa sairastavien tutkittavien tapahtumat olivat voimakkuudeltaan lieviä, eikä niihin liittynyt kliinisiä oireita. Yksikään hoidon myötä ilmaantunut eosinofilian tapahtuma ei johtanut hoidon keskeyttämiseen. Lukuun ottamatta yhtä eosinofiilisen koliitin tapausta atooppista ihottumaa sairastavalla potilaalla, jolla oli muita atooppisia sairauksia, muita raportteja eosinofiilisistä häiriöistä ei ilmaantunut.
Pediatriset potilaat
Atooppinen ihottuma
Nuoret (12–17-vuotiaat)
Nemolitsumabin turvallisuutta arvioitiin 176:lla 12–17-vuotiaalla pediatrisella tutkittavalla, joilla oli keskivaikea tai vaikea atooppinen ihottuma ja jotka osallistuivat ARCADIA 1- ja ARCADIA 2 -tutkimuksiin. Nemolitsumabin turvallisuusprofiili oli näillä tutkittavilla viikkoon 16 asti samankaltainen kuin aikuisilla, joilla on atooppinen ihottuma.
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Nemolitsumabin yliannostukseen ei ole spesifistä hoitoa. Yliannostustapauksessa potilasta on tarkkailtava haittavaikutusten oireiden tai löydösten varalta ja asianmukainen oireenmukainen hoito on aloitettava välittömästi.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Muut ihotautien lääkkeet, ihottumalääkkeet, lukuun ottamatta kortikosteroideja, ATC-koodi: D11AH12
Vaikutusmekanismi
Nemolitsumabi on humanisoitu monoklonaalinen IgG2-vasta-aine, joka estää interleukiini-31 (IL-31) -signaalin sitoutumisen selektiivisesti interleukiini-31-reseptori alfaan (IL-31 RA). IL-31 on luonnollisesti esiintyvä sytokiini, joka liittyy kutinaan, tulehdukseen, epidermaaliseen dysregulaatioon ja fibroosiin. Nemolitsumabi esti IL-31:n indusoimia vasteita, mukaan lukien proinflammatoristen sytokiinien ja kemokiinien vapautuminen.
Atooppisen ihottuman kliinisissä tutkimuksissa nemolitsumabin havaittiin moduloivan atooppisen ihottuman patofysiologiaan liittyvää geeni-ilmentymistä, jolla oli ensisijainen vaikutus immuunijärjestelmän prosesseihin, vähentämällä tiettyjen immuunisolujen (T-solut ja monosyytit/makrofagit) tulehduksellista ja proliferatiivista profiilia ilman immunosuppressiota.
Kyhmykutinan kliinisissä tutkimuksissa nemolitsumabin havaittiin moduloivan kyhmykutinan patofysiologiaan liittyviä molekulaarisia prosesseja, mikä vaikuttaa kutinaan, tulehdukseen, epidermaaliseen erilaistumiseen ja fibroosiin.
Farmakodynaamiset vaikutukset
Immunogeenisuus
Lääkevasta-aineita havaittiin yleisesti. Lääkevasta-aineiden vaikutuksesta farmakokinetiikkaan, tehoon tai turvallisuuteen ei havaittu näyttöä.
Kliininen teho ja turvallisuus atooppisen ihottuman hoidossa
Atooppista ihottumaa sairastavat aikuiset ja nuoret
Nemolitsumabin tehoa ja turvallisuutta yhdessä paikallisen taustahoidon kanssa arvioitiin kahdessa satunnaistetussa, kaksoissokkoutetussa, lumelääkekontrolloidussa keskeisessä tutkimuksessa (ARCADIA 1 ja ARCADIA 2), joihin osallistui yhteensä 1 728 vähintään 12-vuotiasta tutkittavaa. Tutkittavilla oli keskivaikea tai vaikea atooppinen ihottuma, joka ei ollut riittävästi hallinnassa paikallishoidoilla. Taudin vaikeusaste määritettiin tutkijan tekemän atooppisen ihottuman yleisarvion (IGA) pistemääränä 3 (keskivaikea) ja 4 (vaikea), ihottuma-alueen ja vaikeusasteen indeksin (Eczema Area and Severity Index, EASI) pistemääränä ≥ 16, minimissään ≥ 10%:n alueena kehon pinta-alasta (BSA), ja kutinan huippuarvon numeerisen arviointiasteikon (Peak Pruritus Numeric Rating Scale, PP NRS) pistemääränä ≥ 4.
Tutkittaville annettiin aluksi injektioina ihon alle joko 60 mg nemolitsumabia, jonka jälkeen 30 mg:n injektioita neljän viikon välein, tai ulkoisesti vastaavaa lumelääkettä. Samanaikaista matalan ja/tai kohtalaisen tehon paikallista kortikosteroidi- ja/tai kalsineuriinin estäjähoitoa annettiin sekä nemolitsumabi- että lumelääkeryhmissä vähintään 14 päivän ajan ennen lähtötilannetta, ja tämä hoito jatkui tutkimuksen aikana. Taudin aktiivisuuden perusteella nämä samanaikaiset hoidot voitiin vähentää ja/tai lopettaa tutkijan harkinnan mukaan.
16 viikon jälkeen EASI-75- tai IGA-vasteen saaneet tutkittavat jatkoivat tutkimuksen ylläpitojaksoon 32 lisäviikon ajaksi, joiden aikana arvioitiin viikon 16 kohdalla saavutetun vasteen säilymistä. Nemolitsumabivasteen saaneet potilaat satunnaistettiin uudelleen saamaan joko 30 mg nemolitsumabia neljän viikon välein, nemolitsumabia 30 mg kahdeksan viikon välein tai lumelääkettä neljän viikon välein (kaikki ryhmät jatkoivat paikallista kortikosteroidi-/kalsineuriinin estäjähoitoa). Tutkittavat, jotka satunnaistettiin saamaan lumelääkettä ensimmäisen hoitojakson ajaksi ja saavuttivat saman kliinisen vasteen viikon 16 kohdalla, saivat edelleen lumelääkettä neljän viikon välein. Ilman vastetta viikon 16 kohdalla jääneillä tutkittavilla, kliinisen vasteen ylläpitojakson aikana menettäneillä tutkittavilla ja ylläpitojakson loppuun suorittaneilla tutkittavilla oli mahdollisuus osallistua avoimeen tutkimukseen (ARCADIA LTE) ja saada nemolitsumabia 30 mg neljän viikon välein enintään 200 viikon ajan.
Päätetapahtumat
Sekä ARCADIA 1- että ARCADIA 2 -tutkimuksessa arvioitiin ensisijaiset päätetapahtumat:
- niiden tutkittavien osuus, jotka saivat IGA-vasteen (määritelmänä IGA 0 [puhdas] tai 1 [lähes puhdas] ja ≥ 2 pisteellä kohentuminen lähtötilanteesta) viikon 16 kohdalla
- niiden tutkittavien osuus, joilla oli EASI-75-vaste (≥ 75%:n kohentuminen EASI-mittarissa lähtötilanteeseen verrattuna) viikon 16 kohdalla.
Tärkeimmät toissijaiset päätetapahtumat olivat PP NRS -mittarin tuloksen kohentuminen ≥ 4 pisteellä lähtötilanteeseen verrattuna viikkojen 1, 2, 4 ja 16 kohdalla, PP NRS -mittarin tulos < 2 pistettä viikon 4 ja viikon 16 kohdalla, unihäiriöiden numeerisen arviointiasteikon (Sleep Disturbance Numeric Rating Scale, SD NRS) tuloksen kohentuminen ≥ 4 pisteellä lähtötilanteeseen verrattuna viikon 16 kohdalla, tutkittavien määrä, joilla oli sekä EASI-75-vaste että PP NRS -pistemäärän kohentuminen ≥ 4 pisteellä lähtötilanteeseen verrattuna viikon 16 kohdalla, sekä tutkittavien määrä, joilla oli sekä IGA-vaste että PP NRS -pistemäärän kohentuminen ≥ 4 pisteellä lähtötilanteeseen verrattuna viikon 16 kohdalla.
Lähtötilanteen ominaisuudet
Näissä tutkimuksissa lähtötilanteessa 51,0 % tutkittavista oli miehiä, 79,9 % oli valkoihoisia ja keskimääräinen paino oli 75,0 kg. Keskimääräinen ikä oli 34,1 vuotta, 15,4 % tutkittavista oli nuoria (12–17-vuotiaita) ja 5,3 % oli vähintään 65-vuotiaita. 70 %:lla tutkittavista oli lähtötilanteen IGA-pistemäärä 3 (keskivaikea atooppinen ihottuma) ja 30 %:lla tutkittavista lähtötilanteen IGA-pistemäärä oli 4 (vaikea atooppinen ihottuma). Keskiarvoinen (SD) lähtötilanteen EASI-pistemäärä oli 27,5 (10,5), lähtötilanteen viikoittainen keskiarvoinen (SD) PP NRS -mittarin pistemäärä oli 7,1 (1,5) (vaikea kutina) ja lähtötilanteen viikoittainen keskiarvoinen (SD) SD NRS -mittarin pistemäärä oli 5,8 (2,2). Kaiken kaikkiaan 63,3 % tutkittavista sai muita aiempia systeemisiä hoitoja atooppiseen ihottumaan.
Kliininen vaste
ARCADIA 1 ja ARCADIA 2 – Aikuiset ja nuoret – aloitusjakso, viikosta 0 viikkoon 16
Nemolitsumabi oli tilastollisesti merkitsevästi parempi kuin lumelääke ihoon liittyvien ensisijaisten päätetapahtumien, IGA-vasteen ja EASI-75-vasteen, osalta 16 viikon aikana (taulukko 2). Molempien ensisijaisten päätetapahtumien tulokset olivat yhdenmukaisia vaikea-asteisesta kutinasta kärsivien potilasjoukossa (lähtötilanteen PP NRS -mittarin pistemäärä ≥ 7).
Taulukko 2 – Tehoa koskevat tulokset nemolitsumabin (30 mg neljän viikon välein) ja samanaikaisen paikallisen kortikosteroidi-/kalsineuriinin estäjähoidon (TCS/TCI) yhdistelmästä ARCADIA 1- ja ARCADIA 2 -tutkimuksissa viikon 16 kohdalla
| ARCADIA 1 | ARCADIA 2 | |||
| Nemolitsumabi + TCS/TCI | Lumelääke + TCS/TCI | Nemolitsumabi + TCS/TCI | Lumelääke + TCS/TCI | |
| Satunnaistettujen ja annoksen saaneiden tutkittavien määrä (lähtötilanteen PP NRS -mittarin pistemäärä ≥ 4) | 620 | 321 | 522 | 265 |
| % tutkittavista, joilla oli IGA 0- tai 1-vastea | 35,6# | 24,6 | 37,7# | 26,0 |
| % tutkittavista, joilla oli EASI-75-vastea | 43,5* | 29,0 | 42,1# | 30,2 |
a Tutkittavien, jotka saivat kohtaushoitoa (rescue-lääke) tai joiden kohdalla oli puuttuvia tietoja, katsottiin jääneen ilman vastetta.
*p-arvo < 0,0001, #p-arvo < 0,001
Ositekorjattu p-arvo perustuu CMH-testiin, joka on ositettu PP NRS- ja IGA-pistemäärän perusteella lähtötilanteessa.
Kuva 1 – Niiden tutkittavien osuus, joilla oli IGA-vaste ja EASI-75-vaste, lähtötilanteesta viikolle 16 ARCADIA 1- ja ARCADIA 2 -tutkimuksissa
| Kuva 1a. IGA-vaste | Kuva 1b. EASI-75-vaste |
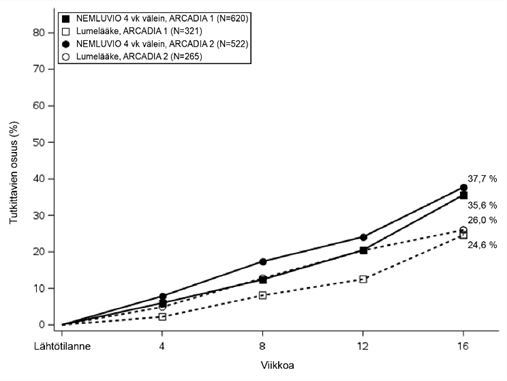 | 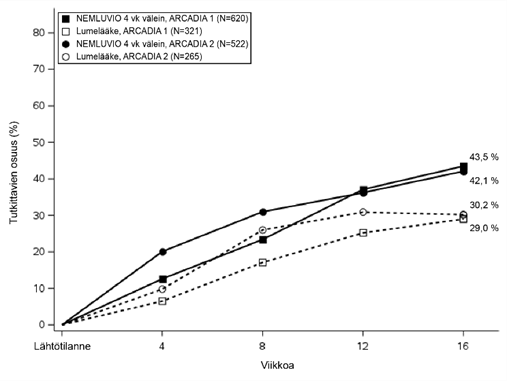 |
Nemolitsumabilla hoidetuilla tutkittavilla havaittiin merkitsevää kutinan lievittymistä ARCADIA 1- ja ARCADIA 2 -tutkimuksissa lumelääkkeeseen verrattuna PP NRS -mittarissa ≥ 4 pisteen kohentumisena ja PP NRS -mittarin prosentuaalisena muutoksena lähtötilanteeseen verrattuna viikosta 1 alkaen. Muutos säilyi viikolle 16 asti (taulukko 3, kuva 2). Tulokset olivat yhdenmukaisia vaikeasta kutinasta kärsineessä potilasjoukossa (lähtötilanteen PP NRS -mittarin pistemäärä ≥ 7).
Taulukko 3 –Tehoa koskevat tulokset nemolitsumabin ja samanaikaisen paikallisen kortikosteroidi-/kalsineuriinin estäjähoidon (TCS/TCI) yhdistelmästä ARCADIA 1- ja ARCADIA 2 -tutkimuksissa viikkoon 16 asti
| ARCADIA 1 | ARCADIA 2 | |||
| Nemolitsumabi + TCS/TCI | Lumelääke + TCS/TCI | Nemolitsumabi + TCS/TCI | Lumelääke + TCS/TCI | |
| Satunnaistettujen ja annoksen saaneiden tutkittavien määrä (lähtötilanteen PP NRS -mittarin pistemäärä ≥ 4)a | 620 | 321 | 522 | 265 |
| % tutkittavista, joiden PP NRS -mittarin pistemäärä kohentui ≥ 4 pisteelläa | ||||
| Viikon 1 kohdalla | 4,7§ | 1,2 | 6,7* | 0,4 |
| Viikon 2 kohdalla | 17,7* | 3,1 | 16,9* | 1,9 |
| Viikon 4 kohdalla | 27,4* | 6,5 | 26,1* | 5,3 |
| Viikon 16 kohdalla | 42,7* | 17,8 | 41,0* | 18,1 |
| % tutkittavista, joiden PP NRS -mittarin pistemäärä < 2a | ||||
| Viikon 4 kohdalla | 16,0* | 3,7 | 15,9* | 2,6 |
| Viikon 16 kohdalla | 30,6* | 11,2 | 28,4* | 11,3 |
| Keskimääräinen muutos lähtötilanteesta (%) | ||||
| Viikon 16 kohdalla | -56,1* | -30,6 | -55,6* | -30,3 |
a Tutkittavien, jotka saivat kohtaushoitoa (rescue-lääke) tai joiden kohdalla oli puuttuvia tietoja, katsottiin jääneen ilman vastetta.
*p-arvo < 0,0001; §p-arvo < 0,05 Ositekorjattu p-arvo perustuu CMH-testiin, joka on ositettu PP NRS- ja IGA-pistemäärän perusteella lähtötilanteessa.
Kuva 2 – Niiden tutkittavien osuus, joilla PP NRS -mittarin pistemäärä kohentui ≥ 4 pisteellä lähtötilanteesta viikolle 16 asti ARCADIA 1- ja ARCADIA 2 -tutkimuksissa
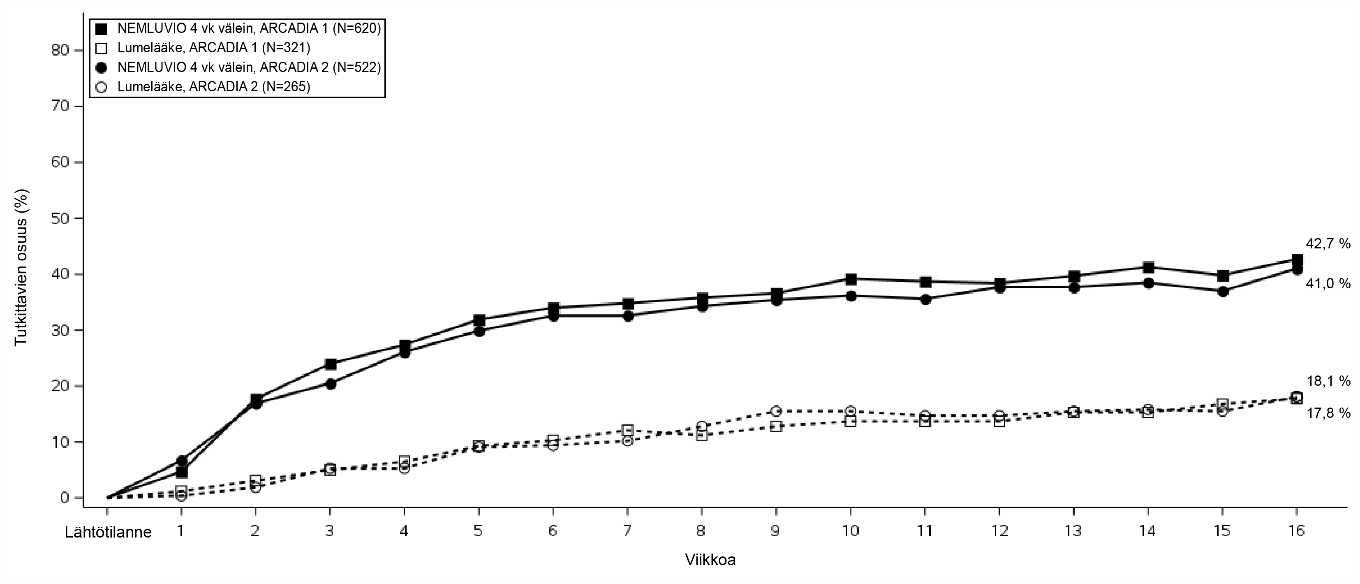
Kussakin keskeisessä tutkimuksessa tehdyssä post-hoc-analyysissä potilailla, joiden paino oli ≥ 90 kg, ei ollut eroa anti-inflammatorisessa vasteessa (IGA 0 tai 1 ja EASI 75) viikolla 16 nemolitsumabi- ja lumelääkeryhmissä. Tämä vaikutus havaittiin tosin kutinan vähentymisessä (PP NRS -mittari).
Unihäiriöiden numeerinen arviointiasteikko (Sleep Disturbance Numeric Rating Scale, SD NRS) on päivittäin täytettävä asteikko, jota tutkittavat käyttävät atooppiseen ihottumaan liittyvän unettomuuden määrän raportoimiseen. Unihäiriöissä havaittiin merkitsevää lievittymistä viikon 16 kohdalla lumelääkkeeseen verrattuna (taulukko 4). Tulokset olivat yhdenmukaisia vaikeasta kutinasta kärsineessä potilasjoukossa (lähtötilanteen PP NRS -mittarin pistemäärä ≥ 7).
Taulukko 4 –Unihäiriöihin kohdistuva teho nemolitsumabin ja samanaikaisen paikallisen kortikosteroidi-/kalsineuriinin estäjähoidon (TCS/TCI) yhdistelmää käytettäessä ARCADIA 1- ja ARCADIA 2 -tutkimuksissa viikon 16 kohdalla
| ARCADIA 1 | ARCADIA 2 | |||
| Nemolitsumabi + TCS/TCI | Lumelääke + TCS/TCI | Nemolitsumabi + TCS/TCI | Lumelääke + TCS/TCI | |
| Satunnaistettujen ja annoksen saaneiden tutkittavien määrä (lähtötilanteen PP NRS -mittarin pistemäärä ≥ 4)a | 620 | 321 | 522 | 265 |
% tutkittavista, joiden SD NRS -mittarin pistemäärä kohentui ≥ 4 pisteelläa Keskimääräinen muutos lähtötilanteesta (%) | 37,9* -64,6 | 19,9 -38,1 | 33,5* -59,7 | 16,2 -35,4 |
a Tutkittavien, jotka saivat kohtaushoitoa (rescue-lääke) tai joiden kohdalla oli puuttuvia tietoja, katsottiin jääneen ilman vastetta.
*p-arvo < 0,0001 Ositekorjattu p-arvo perustuu CMH-testiin, joka on ositettu PP NRS- ja IGA-pistemäärän perusteella lähtötilanteessa.
Atooppista ihottumaa sairastavat nuoret (12–17-vuotiaat)
ARCADIA 1- ja ARCADIA 2 -tutkimusten tehoa koskevat tulokset viikon 16 kohdalla 12–17-vuotiailla pediatrisilla tutkittavilla on esitetty taulukossa 5. Pediatristen tutkittavien tulokset olivat yleisesti ottaen yhdenmukaisia aikuispotilaiden tulosten kanssa. Ensisijaisten päätetapahtumien ja keskeisten toissijaisten päätetapahtumien tulokset olivat yhdenmukaisia vaikea-asteisesta kutinasta kärsivien potilasjoukossa (lähtötilanteen PP NRS -mittarin pistemäärä ≥ 7).
Taulukko 5 – Tehoa koskevat tulokset nemolitsumabin (30 mg neljän viikon välein) ja samanaikaisen paikallisen kortikosteroidi-/kalsineuriinin estäjähoidon (TCS/TCI) yhdistelmästä ARCADIA 1- ja ARCADIA 2 -tutkimuksissa viikon 16 kohdalla 12–17-vuotiailla pediatrisilla tutkittavilla
| ARCADIA 1 JA ARCADIA 2 | ||
| Nemolitsumabi + TCS/TCI | Lumelääke + TCS/TCI | |
| Satunnaistettujen ja annoksen saaneiden tutkittavien määrä (lähtötilanteen PP NRS -mittarin pistemäärä ≥ 4) | 179 | 90 |
| % tutkittavista, joilla oli IGA 0- tai 1-vaste a | 48,9* | 34,4 |
| % tutkittavista, joilla oli EASI-75-vaste a | 53,4§ | 43,3 |
| % tutkittavista, joiden PP NRS -mittarin pistemäärä kohentui ≥ 4 pisteellä a | 40,9# | 17,8 |
| % tutkittavista, joiden PP NRS -mittarin pistemäärä < 2 a | 30,1≠ | 6,7 |
| % tutkittavista, joiden SD NRS -mittarin pistemäärä kohentui ≥ 4 pisteellä a | 31,8∞ | 20,0 |
a Tutkittavien, jotka saivat kohtaushoitoa (rescue-lääke) tai joiden kohdalla oli puuttuvia tietoja, katsottiin jääneen ilman vastetta.
≠p-arvo < 0,0001; #p-arvo < 0,001; *p-arvo < 0,05; ∞p-arvo=0,0591; §p-arvo=0,1824
Ositekorjattu p-arvo perustuu CMH-testiin, joka on ositettu PP NRS- ja IGA-pistemäärän perusteella lähtötilanteessa.
ARCADIA 1 ja ARCADIA 2 – Aikuiset ja nuoret – ylläpitojakso, viikosta 16 viikkoon 48
Kliinistä vastetta nemolitsumabivasteen saaneilla (IGA 0/1-vaste tai EASI-75-vaste viikon 16 kohdalla) arvioitiin viikkojen 16 ja 48 välillä ARCADIA 1- ja ARCADIA 2 -tutkimuksissa. Ylläpitohoitojaksoa varten 507 nemolitsumabille vasteen saanutta potilasta satunnaistettiin uudelleen saamaan nemolitsumabia 30 mg neljän viikon välein, nemolitsumabia 30 mg kahdeksan viikon välein tai lumelääkettä neljän viikon välein (nemolitsumabin käytön keskeyttäminen) samanaikaisen paikallisen kortikosteroidi-/kalsineuriinin estäjähoidon kanssa. Taulukossa 6 on esitetty yhdistetyt nemolitsumabin tehoa koskevat tulokset viikon 48 kohdalla keskeisissä tutkimuksissa (ARCADIA 1 ja ARCADIA 2). Tuloksissa on vain kuvaava analyysi tämän jakson osalta.
Taulukko 6 – Ylläpitojakson yhdistetyt tehoa koskevat tulokset nemolitsumabin ja samanaikaisen paikallisen kortikosteroidi-/kalsineuriinin estäjähoidon (TCS/TCI) yhdistelmästä ARCADIA 1- ja ARCADIA 2 -tutkimuksissa viikon 48 kohdalla
| Nemolitsumabi + TCS/TCI 4 vk välein N=169 | Nemolitsumabi + TCS/TCI 8 vk välein N=169 | Lumelääke + TCS/TCI 4 vk välein (nemolitsumabin käytön keskeyttäminen) N=169 | |
| % tutkittavista, joilla oli IGA 0- tai 1-vastea | |||
| Viikko 16 (ylläpitojakson lähtötilanne) | 84,0 | 84,0 | 77,5 |
| Viikko 48 Ositekorjattu osuusero (%) Ositekorjattu 95 %:n luottamusväli | 61,5 11,8 (1,3; 22,3) | 60,4 10,7 (0,3; 21,0) | 49,7 |
| % tutkittavista, joilla oli EASI-75-vastea (95 %:n luottamusväli) | |||
| Viikko 16 (ylläpitojakso/lähtötilanne) | 96,4 | 96,4 | 92,9 |
| Viikko 48 Ositekorjattu osuusero (%) Ositekorjattu 95 %:n luottamusväli | 76,3 12,4 (2,7; 22,0) | 75,7 11,8 (2,1; 21,5) | 63,9 |
a Tutkittavien, jotka saivat kohtaushoitoa (rescue-lääke) tai joiden kohdalla oli puuttuvia tietoja, katsottiin jääneen ilman vastetta.
Kliininen teho ja turvallisuus aikuisilla, joilla on kyhmykutina
Nemolitsumabin tehoa ja turvallisuutta monoterapiana arvioitiin kahdessa satunnaistetussa, kaksoissokkoutetussa, lumelääkekontrolloidussa keskeisessä tutkimuksessa (OLYMPIA 1 ja OLYMPIA 2), joihin osallistui yhteensä 560 vähintään 18-vuotiasta tutkittavaa, joilla oli keskivaikea tai vaikea kyhmykutina. Taudin vaikeusaste määritettiin käyttämällä tutkijan tekemää kyhmykutinan kyhmyjen yleisarviointia (Global Assessment, IGA) asteikolla 0–4. Näihin kahteen tutkimukseen mukaan otetuilla tutkittavilla oli IGA-pistemäärä ≥ 3, vaikeaa kutinaa, jonka määritelmänä oli suurimman kutinan numeerisen arviointiasteikon (peak pruritus numeric rating scale, PP-NRS) viikoittainen keskiarvo ≥ 7 asteikolla 0–10, ja tutkittavilla oli vähintään 20 nodulaarista leesiota. OLYMPIA 1- ja OLYMPIA 2 -tutkimuksissa arvioitiin nemolitsumabimonoterapian vaikutusta kyhmykutinan oireisiin ja löydöksiin. Arviointi kohdistui ihomuutosten ja kutinan lievittymiseen 16 viikon aikana. OLYMPIA 1-tutkimuksessa oli 24 viikon hoitojakso ja OLYMPIA 2-tutkimuksessa oli 16 viikon hoitojakso.
Nemolitsumabihoitoryhmässä alle 90 kg painavat tutkittavat saivat 60 mg nemolitsumabia ihon alle (kaksi 30 mg:n injektiota) viikolla 0 ja sen jälkeen 30 mg:n injektioita neljän viikon välein. Vähintään 90 kg painavat tutkittavat saivat 60 mg nemolitsumabia ihon alle (kaksi 30 mg:n injektiota) viikolla 0 ja neljän viikon välein.
Päätetapahtumat
Sekä OLYMPIA 1- että OLYMPIA 2 -tutkimus arvioivat samoja kahta ensisijaista päätetapahtumaa:
- niiden tutkittavien osuus, joiden suurimman kutinan numeerisen arviointiasteikon (Pruritus Numeric Rating Scale, PP NRS) pistemäärä oli kohentunut lähtötilanteesta ≥ 4 pisteellä viikon 16 kohdalla
- niiden tutkittavien osuus, jotka saivat IGA-vasteen (määritelmänä IGA 0 [puhdas] tai 1 [lähes puhdas] ja ≥ 2 pisteellä kohentuminen lähtötilanteesta) viikon 16 kohdalla.
Keskeisiä toissijaisia päätetapahtumia olivat PP NRS -mittarin pistemäärän kohentuminen ≥ 4 pisteellä lähtötilanteeseen verrattuna viikon 4 kohdalla, PP NRS -mittarin pistemäärä < 2 viikon 4 ja viikon 16 kohdalla sekä unihäiriöiden numeerisen arviointiasteikon (Sleep Disturbance Numeric Rating Scale, SD NRS) pistemäärän kohentuminen ≥ 4 pisteellä lähtötilanteeseen verrattuna viikkojen 4 ja 16 kohdalla.
Lähtötilanteen ominaisuudet
Näissä tutkimuksissa lähtötilanteessa 59,6 % tutkittavista oli naisia, 81,4 % oli valkoihoisia, keskimääräinen paino oli 82,6 kg, keskimääräinen ikä oli 55,2 vuotta ja 25,4 % tutkittavista oli yli 65-vuotiaita. Lähtötilanteen viikoittainen keskiarvoinen PP NRS -mittarin pistemäärä (SD) oli 8,4 (0,9). 58 %:lla tutkittavista lähtötilanteen IGA-pistemäärä oli 3 (keskivaikea kyhmykutina) ja 42 %:lla tutkittavista lähtötilanteen IGA-pistemäärä oli 4 (vaikea kyhmykutina).
Kliininen vaste
Keskeiset tutkimukset (OLYMPIA 1 ja OLYMPIA 2) – viikosta 0 viikkoon 16
Taulukossa 7 on esitetty keskeisten tutkimusten (OLYMPIA 1 ja OLYMPIA 2) tulokset, joissa arvioitiin nemolitsumabihoitoa. Nemolitsumabilla hoidetuilla tutkittavilla havaittiin merkitsevää kohentumista lumelääkkeeseen verrattuna ensisijaisten päätetapahtumien (kuva 3 ja kuva 4).
Taulukko 7 – Tehoa koskevat tulokset neljän viikon välein annetusta nemolitsumabimonoterapiasta OLYMPIA 1- ja OLYMPIA 2 -tutkimuksissa
| OLYMPIA 1 | OLYMPIA 2 | |||
| Nemolitsumabi | Lumelääke | Nemolitsumabi | Lumelääke | |
| Satunnaistettujen tutkittavien määrä | 190 | 96 | 183 | 91 |
| % tutkittavista, joiden PP NRS -mittarin pistemäärä oli kohentunut ≥ 4 pisteellä lähtötilanteestaa | ||||
| Viikko 4 | 41,1* | 6,3 | 41,0* | 7,7 |
| Viikko 16 | 58,4* | 16,7 | 56,3* | 20,9 |
| % tutkittavista, joilla oli IGA 0- tai 1-vaste viikon 16 kohdallaa | 26,3# | 7,3 | 37,7* | 11 |
| % tutkittavista, joiden PP NRS -mittarin pistemäärä < 2 a | ||||
| Viikko 4 | 21,6* | 1,0 | 19,7* | 2,2 |
| Viikko 16 | 34,2* | 4,2 | 35,0* | 7,7 |
| % tutkittavista, joiden SD NRS -mittarin pistemäärä oli kohentunut ≥ 4 pisteellä lähtötilanteestaa | ||||
| Viikko 4 | 31,1* | 5,2 | 37,2* | 9,9 |
| Viikko 16 | 50,0* | 11,5 | 51,9* | 20,9 |
a Jos tutkittava oli saanut kohtauslääkettä (rescue-lääke), tällöin käytettiin yhdistelmämuuttujastrategiaa. Taustalla olevat tiedot kohtaushoidon saamisen hetkellä tai sen jälkeen määritettiin huonoimmaksi mahdolliseksi arvoksi, ja vaste johdettiin taustalla olevien tietojen arvosta. Tutkittavien, joilla oli puuttuvia tuloksia, katsottiin jääneen ilman vastetta.
*p-arvo < 0,0001; #p-arvo=0,0025 Ositekorjattu satunnaistettuja ositusmuuttujia käyttäen (analyysikeskus ja lähtötilanteen paino < 90 kg, ≥ 90 kg)
Kuva 3 – Niiden tutkittavien osuus, joilla PP-NRS-mittarin pistemäärä kohentui ≥ 4 pisteellä lähtötilanteesta viikolle 16
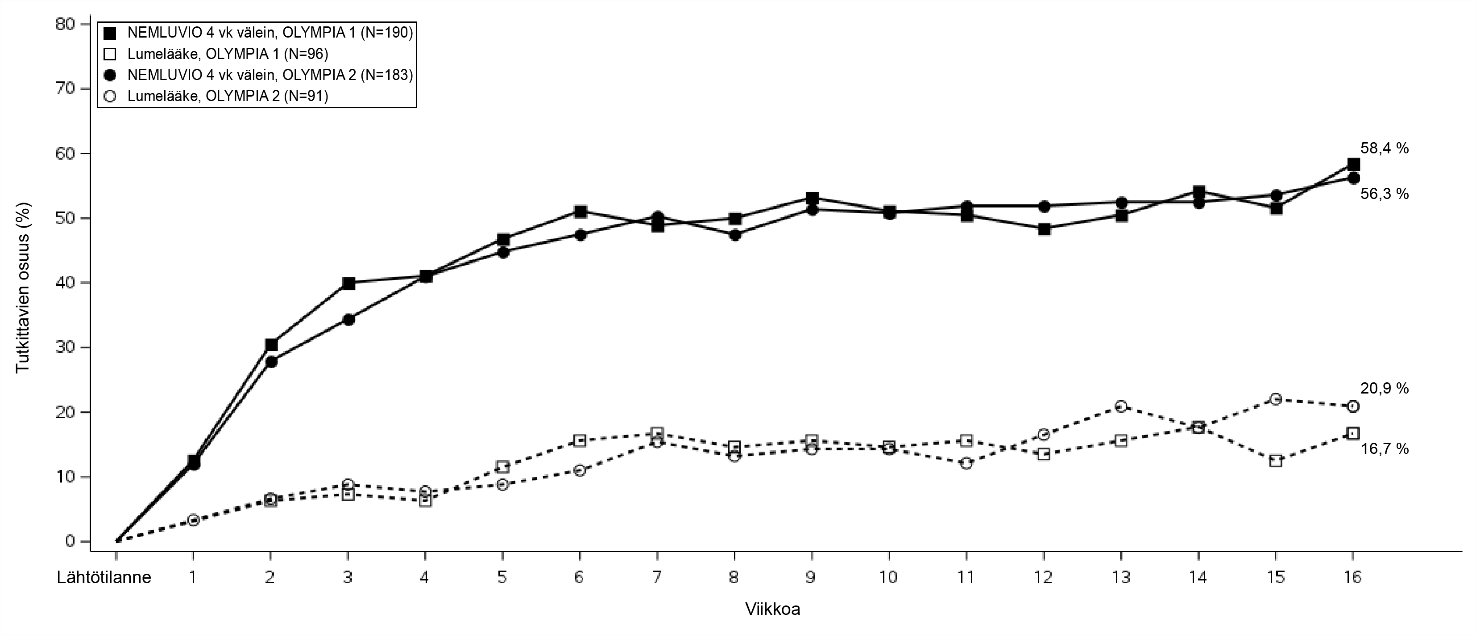
Kuva 4 – IGA-vasteen saaneiden osuus lähtötilanteesta viikolle 16
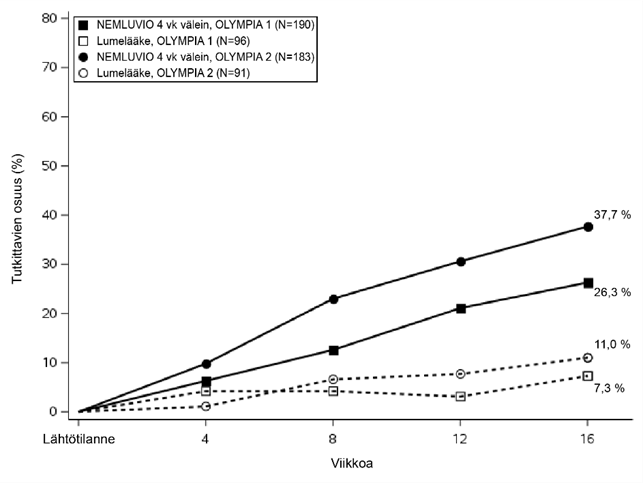
Farmakokinetiikka
Imeytyminen
Kun ihon alle oli annettu 60 mg:n aloitusannos potilaille, joilla oli atooppinen ihottuma tai kyhmykutina, populaatiofarmakinetiikan keskimääräinen (SD) huippupitoisuus (Cmax) oli 6,7 (2,20) mikrog/ml noin 6 vuorokauden kuluttua annoksen saamisesta.
Atooppista ihottumaa sairastavilla tutkittavilla useiden annosten jälkeen populaatiofarmakokineettisesti arvioidut vakaan tilan nemolitsumabin minimipitoisuudet olivat 2,63 (1,27) mikrog/ml annettaessa 30 mg neljän viikon välein ja 0,74 (0,44) mikrog/ml annettaessa 30 mg kahdeksan viikon välein.
Kyhmykutinaa sairastavilla tutkittavilla useiden annosten jälkeen populaatiofarmakokinetiikan arvioidut vakaan tilan nemolitsumabin minimipitoisuudet olivat 3,04 (1,23) mikrog/ml < 90 kg painavilla tutkittavilla annettaessa 30 mg neljän viikon välein ja 3,66 (1,63) mikrog/ml ≥ 90 kg painavilla tutkittavilla annettaessa 60 mg neljän viikon välein.
Sekä atooppisesta ihottumaa että kyhmykutinaa sairastavien potilasjoukoissa nemolitsumabin vakaan tilan pitoisuudet saavutettiin viikkoon 4 mennessä 60 mg:n latausannoksen jälkeen ja viikkoon 12 mennessä ilman latausannosta.
Latausannosta ehdotetaan kyhmykutinaa sairastaville henkilöille, joiden paino on < 90 kg. Henkilöille, joiden paino on ≥ 90 kg, ei kuitenkaan ehdoteta latausannosta, koska 60 mg:n annos oli riittävä samanlaisten nemolitsumabin vakaan tilan pitoisuuksien saavuttamiseen kuin 30 mg:n annoksella (60 mg:n latausannoksen kanssa) toisen annoksen jälkeen (viikon 8 kohdalla).
Jakautuminen
Populaatiofarmakokineettisen analyysin perusteella näennäinen jakautumistilavuus (V/F) oli 7,67 l.
Biotransformaatio
Erityisiä metaboliatutkimuksia ei ole tehty, koska nemolitsumabi on proteiini. Nemolitsumabin odotetaan metaboloituvan pieniksi peptideiksi katabolisten reittien kautta.
Eliminaatio
Nemolitsumabin odotetaan hajoavan samalla tavalla kuin endogeeninen IgG. Populaatiofarmakokineettisessä analyysissä nemolitsumabin terminaalisen eliminaation puoliintumisajan (SD) arvioitiin olevan 18,9 (4,96) vuorokautta ja näennäisen systeemisen puhdistuman (Cl/F) arvioitiin olevan 0,26 l/vrk.
Lineaarisuus/ei-lineaarisuus
Kerta-annoksen jälkeen nemolitsumabin farmakokinetiikka oli lineaarista ja altistukset lisääntyivät suhteessa annokseen annostasolla 0,03–3 mg/kg.
Useiden annosten jälkeen nemolitsumabin systeeminen altistus suureni suunnilleen suhteessa annokseen koko ihon alle annetulla annosalueella annokseen 30 mg saakka. Biologinen hyötyosuus pieneni hieman (9 %) 60 mg:n ihon alle annettua annosta käytettäessä.
Erityisryhmät
Sukupuoli, ikä ja etninen tausta
Sukupuolella, iällä (vaihteluväli 12–85 vuotta atooppista ihottumaa sairastavilla ja 18–84 vuotta kyhmykutinaa sairastavilla) ja etnisellä taustalla ei ollut kliinisesti merkittävää vaikutusta nemolitsumabin farmakokinetiikkaan.
Maksan vajaatoiminta
Monoklonaalisena vasta-aineena nemolitsumabin ei odoteta eliminoituvan merkitsevästi maksan kautta. Maksan vajaatoiminnan vaikutuksesta nemolitsumabin farmakokinetiikkaan ei ole tehty kliinisiä tutkimuksia. Lievän tai kohtalaisen maksan vajaatoiminnan ei havaittu vaikuttavan nemolitsumabin farmakokinetiikkaan populaatiofarmakokineettisen analyysin perusteella. Vaikeaa maksan vajaatoimintaa sairastavista potilaista ei ole saatavilla tietoja.
Munuaisten vajaatoiminta
Monoklonaalisena vasta-aineena nemolitsumabin ei odoteta eliminoituvan merkitsevästi munuaisten kautta. Munuaisten vajaatoiminnan vaikutuksesta nemolitsumabin farmakokinetiikkaan ei ole tehty kliinisiä tutkimuksia. Populaatiofarmakokineettisessä analyysissä ei havaittu lievällä tai kohtalaisella munuaisten vajaatoiminnalla olevan kliinisesti merkittävää vaikutusta nemolitsumabin systeemiseen altistukseen. Vaikeaa munuaisten vajaatoimintaa sairastavista potilaista on saatavilla hyvin vähän tietoja.
Paino
Nemolitsumabialtistus oli pienempää tutkittavilla, joiden paino oli suurempi.
Atooppinen ihottuma
Painosta johtuvalla systeemisen altistuksen erolla ei ollut kliinisesti merkittävää vaikutusta tehoon. Annosta ei tarvitse muuttaa painon perusteella (ks. kohta Annostus ja antotapa).
Kyhmykutina
Painosta johtuvalla systeemisen altistumisen vaihtelulla oli kliinisesti merkittävä vaikutus ihomuutoksiin kohdistuvaan tehoon IGA-vasteen perusteella, mutta ei kutinan lievittymiseen, ja se edellyttää annoksen muuttamista kyhmykutinaa sairastavilla potilailla (ks. kohta Annostus ja antotapa).
Pediatriset potilaat
Atooppinen ihottuma
Populaatiofarmakokineettisessä analyysissä ei todettu kliinisesti merkittävää eroa nemolitsumabin farmakokinetiikassa 12–17-vuotiailla pediatrisilla tutkittavilla aikuisiin verrattuna. Annoksen muuttamista tälle potilasjoukolle ei suositella.
Prekliiniset tiedot turvallisuudesta
Farmakologista turvallisuutta ja toistuvan altistuksen aiheuttamaa toksisuutta koskevien konventionaalisten tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille.
Nemolitsumabin mutageenisuutta ei ole arvioitu. Monoklonaalisten vasta-aineiden ei kuitenkaan odoteta muuttavan DNA:ta tai kromosomeja.
Nemolitsumabilla ei ole tehty karsinogeenisuustutkimuksia. IL-31:n estoon ja eläintoksikologiaan liittyvän saatavilla olevan näytön arviointi ei viittaa valmisteen karsinogeenisuuteen.
Hedelmällisyysparametreihin kohdistuvia vaikutuksia ei havaittu sukukypsillä jaavanmakakiapinoilla pitkäaikaisen ihonalaisen nemolitsumabihoidon jälkeen. Emojen ryhmässä, jota hoidettiin annoksella 25 mg/kg nemolitsumabia kahden viikon välein varhaisesta organogeneesista synnytykseen, jälkeläisten kuolemien havaittiin hieman lisääntyneen syntymän jälkeisenä aikana. Emojen altistukset (AUC) olivat 43-kertaisia tai 34-kertaisia ihmisen altistukseen nähden suurimmalla suositellulla annoksella atooppista ihottumaa tai kyhmykutinaa sairastavilla potilailla). Tämän löydöksen suhdetta nemolitsumabiin ei voida sulkea pois.
Farmaseuttiset tiedot
Apuaineet
Injektiokuiva-aine, liuosta varten
Sakkaroosi
Trometamoli
Trometamolihydrokloridi (pH:n säätämiseen)
Arginiinihydrokloridi
Poloksameeri 188
Liuotin
Injektionesteisiin käytettävä vesi
Yhteensopimattomuudet
Koska yhteensopivuustutkimuksia ei ole tehty, tätä lääkevalmistetta ei saa sekoittaa muiden lääkevalmisteiden kanssa.
Kestoaika
Nemluvio 30 mg injektiokuiva-aine ja liuotin, liuosta varten, esitäytetty kynä
3 vuotta
Kun käyttökuntoon saattamisen vaiheet on suoritettu, Nemluvio on käytettävä 4 tunnin kuluessa ja säilytettävä huoneenlämmössä (enintään 25 °C) tai hävitettävä.
Tarvittaessa esitäytetyn kynän sisältävä pakkaus voidaan ottaa pois jääkaapista ja sitä voidaan säilyttää huoneenlämmössä (enintään 25°C) yhden enintään 90 vuorokauden jakson ajan. Jääkaapista pois ottamisen päivämäärä on merkittävä ulkopakkaukseen merkittyyn tilaan. Älä käytä Nemluvio-valmistetta, jos viimeinen käyttöpäivämäärä on mennyt ohi tai jos valmiste on ollut poissa jääkaapista yli 90 vuorokauden ajan (sen mukaan, kumpi näistä tapahtuu aiemmin).
Säilytys
Säilytä jääkaapissa (2 - 8 °C).
Ei saa jäätyä.
Säilytä alkuperäispakkauksessa. Herkkä valolle.
Käyttökuntoon saatetun lääkevalmisteen säilytys, ks. kohta Kestoaika.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
NEMLUVIO injektiokuiva-aine ja liuotin, liuosta varten, esitäytetty kynä
30 mg (L:ei) 1 kpl (2280,35 €)
PF-selosteen tieto
Nemluvio 30 mg injektiokuiva-aine ja liuotin, liuosta varten, esitäytetty kynä
Kertakäyttöinen, tyypin 1 kaksikammioinen borosilikaattilasista valmistettu sylinteriampulli autoinjektorissa, jossa on ruostumattomasta teräksestä valmistettu kiinteä neula.
Pakkauskoko: 1 esitäytetty kynä, kerrannaispakkaus, joka sisältää 2 (2 x 1) esitäytettyä kynää, kerrannaispakkaus, joka sisältää 3 (3 x 1) esitäytettyä kynää.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Valmisteen kuvaus:
Injektiokuiva-aine, liuosta varten: kylmäkuivattu valkoinen jauhe.
Liuotin injektionestettä, liuosta varten: Kirkas, väritön liuos.
Käyttö- ja käsittelyohjeet
Kattavat ohjeet Nemluvio-valmisteen antamiseen esitäytetyllä kynällä on annettu pakkausselosteen lopussa.
Nemluvio on otettava pois jääkaapista 30–45 minuutin ajaksi ennen käyttökuntoon saattamista.
Tarkasta Nemluvio silmämääräisesti ennen käyttökuntoon saattamista. Älä käytä, jos jauhe ei ole valkoista tai jos neste on sameaa tai hiukkasia on näkyvissä. Tarkasta ennen antamista, että liuos on kirkasta ja väritöntä tai hieman kellertävää eikä sisällä hiukkasia.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
NEMLUVIO injektiokuiva-aine ja liuotin, liuosta varten, esitäytetty kynä
30 mg 1 kpl
- Ei korvausta.
ATC-koodi
D11AH12
Valmisteyhteenvedon muuttamispäivämäärä
08.01.2026
Yhteystiedot
Seminariegatan 21
SE-752 28 Uppsala
Sverige
+46 18 444 0330
www.galdermanordic.com
nordic@galderma.com
