TREMFYA injektioneste, liuos, esitäytetty kynä 45 mg/0,45 ml
Vaikuttavat aineet ja niiden määrät
Yksi esitäytetty kynä sisältää 45 mg guselkumabia 0,45 ml:ssa liuosta. 1 ml liuosta sisältää 100 mg guselkumabia.
Yhdestä esitäytetystä kynästä saadaan 0,1–0,45 ml (vastaa 10–45 mg:aa guselkumabia) 0,05 ml:n lisäyksinä.
Guselkumabi on ihmisen immunoglobuliini-G1-lambdan (IgG1λ) monoklonaalinen vasta-aine, joka tuotetaan yhdistelmä-DNA-tekniikalla kiinanhamsterin munasarjasoluissa.
Apuaine(et), joiden vaikutus tunnetaan
Tämä lääkevalmiste sisältää 0,3 mg polysorbaatti 80:tä (E433) per esitäytetty kynä, mikä vastaa 0,5 mg:aa/ml.
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Injektioneste, liuos (injektioneste), esitäytetty kynä (VarioJect)
Kliiniset tiedot
Käyttöaiheet
Lapsuusiän läiskäpsoriaasi
Tremfya on tarkoitettu keskivaikean tai vaikean läiskäpsoriaasin hoitoon vähintään 6-vuotiaille lapsille ja nuorille, joille harkitaan systeemistä hoitoa.
Ehto
Valmiste on tarkoitettu käytettäväksi käyttöaiheessa mainitun sairauden diagnosointiin ja hoitoon perehtyneen lääkärin ohjauksessa ja seurannassa.
Annostus ja antotapa
Tämä lääkevalmiste on tarkoitettu käytettäväksi läiskäpsoriaasin diagnosointiin ja hoitoon perehtyneen lääkärin ohjauksessa ja seurannassa.
Annostus
45 mg/0,45 ml esitäytetty kynä on tarkoitettu vähintään 6-vuotiaille pediatrisille potilaille, joiden paino on alle 40 kg.
Yksi esitäytetty kynä on yhtä käyttökertaa varten ja tarkoitettu käytettäväksi yhdelle potilaalle. Esitäytetty kynä pitää hävittää välittömästi käytön jälkeen.
Lapsuusiän (6–17-vuotiaiden) läiskäpsoriaasi
Vähintään 6-vuotiaat lapset, joiden paino on alle 40 kg
Suositeltu annos esitetään taulukossa 1 ja on enintään 45 mg. Annos annetaan injektiona ihon alle viikoilla 0 ja 4, minkä jälkeen annetaan ylläpitoannos 8 viikon välein.
| Taulukko 1. Alle 40 kg:n painoisille pediatrisille potilaille suositeltu guselkumabiannos injektiona ihon alle | |
Paino (kg) (antoajankohtana) | Annos (mg) |
| 12–15 kg | 20 |
| 16–19 kg | 25 |
| 20–23 kg | 30 |
| 24–26 kg | 35 |
| 27–30 kg | 40 |
| 31–39 kg | 45 |
Vähintään 6-vuotiaat lapset, joiden paino on vähintään 40 kg
Vähintään 40 kg:n painoisille lapsille on saatavana 100 mg:n esitäytetty ruisku. Ks. annostus ja antotapa Tremfya 100 mg esitäytetyn ruiskun valmisteyhteenvedon kohdasta Annostus ja antotapa.
Jos pediatrisella potilaalla ei todeta vastetta 24 viikon hoidon jälkeen, hoidon lopettamista on harkittava.
Väliin jäänyt annos
Jos annos on jäänyt väliin, se on annettava mahdollisimman pian. Sen jälkeen hoitoa jatketaan tavanomaisen hoitoaikataulun mukaisesti.
Erityiset potilasryhmät
Munuaisten tai maksan vajaatoiminta
Tremfya‑valmistetta ei ole tutkittu näillä potilasryhmillä. Näiden sairauksien ei yleisesti oleteta vaikuttavan merkittävästi monoklonaalisten vasta-aineiden farmakokinetiikkaan eikä annoksen muuttamista katsota tarpeelliseksi. Lisätietoja guselkumabin eliminaatiosta, ks. kohta Farmakokinetiikka.
Pediatriset potilaat
Tremfya‑valmisteen turvallisuutta ja tehoa alle 6 vuoden ikäisten potilaiden hoidossa ei ole varmistettu.
Tietoja ei ole saatavilla.
Antotapa
Vain ihon alle. Jos mahdollista, injektiokohtina ei pidä käyttää ihoalueita, joilla on psoriaasia.
Tremfya ei ole tarkoitettu pediatrisille potilaille omatoimiseen lääkitykseen. Kun potilasta hoitava henkilö on saanut asianmukaisen opastuksen ihon alle annettavien injektioiden injektiotekniikkaan, potilasta hoitava henkilö voi antaa Tremfya‑injektion, jos lääkäri katsoo sen tarkoituksenmukaiseksi. Lääkärin on kuitenkin varmistettava potilaan asianmukainen seuranta. Potilasta hoitavaa henkilöä on neuvottava injisoimaan lääkemääräyksen mukainen liuosmäärä kotelon sisältämien Käyttöohjeiden mukaisesti.
Ks. kohdasta Käyttö- ja käsittelyohjeet ohjeet lääkevalmisteen valmistelusta ennen lääkkeen antoa.
Vasta-aiheet
Vakava yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille.
Kliinisesti tärkeät aktiiviset infektiot (esim. aktiivinen tuberkuloosi, ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Varoitukset ja käyttöön liittyvät varotoimet
Jäljitettävyys
Biologisten lääkevalmisteiden jäljitettävyyden parantamiseksi on annetun valmisteen nimi ja eränumero dokumentoitava selkeästi.
Infektiot
Guselkumabi saattaa lisätä infektioiden riskiä. Jos potilaalla on kliinisesti tärkeä aktiivinen infektio, hoitoa ei saa aloittaa ennen kuin infektio on parantunut tai sitä on hoidettu riittävästi.
Guselkumabihoitoa saavia potilaita pitää kehottaa hakeutumaan lääkäriin, jos heille ilmaantuu kliinisesti tärkeän kroonisen tai akuutin infektion oireita tai löydöksiä. Jos potilaalle kehittyy kliinisesti tärkeä tai vakava infektio tai potilas ei saa hoitovastetta tavanomaiseen hoitoon, potilaan tilaa on seurattava tarkoin ja hoito on keskeytettävä, kunnes infektio on parantunut.
Tuberkuloosin tutkiminen ennen hoitoa
Potilailta on tutkittava tuberkuloosi-infektio ennen hoidon aloittamista. Guselkumabihoitoa saavia potilaita pitää seurata hoidon aikana ja sen jälkeen aktiivisen tuberkuloosin oireiden ja löydösten havaitsemiseksi. Jos potilaalla on aiemmin ollut piilevä tai aktiivinen tuberkuloosi, jonka riittävästä hoidosta ei voida varmistua, tuberkuloosihoidon antamista on harkittava ennen hoidon aloittamista.
Yliherkkyys
Valmisteen markkinoille tulon jälkeen on raportoitu vakavia yliherkkyysreaktioita, mukaan lukien anafylaksiaa (ks. kohta Haittavaikutukset). Osa vakavista yliherkkyysreaktioista ilmeni useita päiviä guselkumabihoidon jälkeen, mukaan lukien tapaukset, joihin liittyi urtikariaa ja hengenahdistusta. Jos ilmaantuu vakava yliherkkyysreaktio, guselkumabin antaminen on lopetettava heti, ja asianmukainen hoito on aloitettava.
Kohonnut maksan transaminaasipitoisuus
Nivelpsoriaasia koskeneissa kliinisissä tutkimuksissa suurentuneiden maksaentsyymipitoisuuksien ilmaantuvuus oli guselkumabihoitoa neljän viikon välein saaneilla potilailla suurempi kuin guselkumabihoitoa kahdeksan viikon välein tai lumehoitoa saaneilla potilailla (ks. kohta Haittavaikutukset).
Rokotukset
Kaikkien iänmukaisten rokotusten antamista voimassa olevien rokotusohjeiden mukaisesti on harkittava ennen hoidon aloittamista. Guselkumabihoitoa saaville potilaille ei saa antaa samanaikaisesti eläviä taudinaiheuttajia sisältäviä rokotteita. Vasteesta eläville tai inaktivoiduille rokotteille ei ole tietoja.
Ennen eläviä viruksia tai eläviä bakteereja sisältävien rokotusten antamista hoito pitää keskeyttää vähintään 12 viikoksi viimeisen annoksen antamisen jälkeen, ja hoitoa voidaan jatkaa aikaisintaan 2 viikon kuluttua rokotuksesta. Lääkkeen määräävän lääkärin pitää tarkistaa kyseisen rokotteen valmisteyhteenvedosta lisätiedot ja ohjeet immunosuppressiivisten aineiden samanaikaisesta käytöstä rokotuksen jälkeen.
Apuaineet, joiden vaikutus tunnetaan
Polysorbaatti 80 -pitoisuus
Tämä lääkevalmiste sisältää 0,3 mg polysorbaatti 80:tä (E433) per esitäytetty kynä, mikä vastaa 0,5 mg:aa/ml. Polysorbaatit saattavat aiheuttaa allergisia reaktioita.
Yhteisvaikutukset
Yhteisvaikutukset CYP450:n substraattien kanssa
Keskivaikeaa tai vaikeaa läiskäpsoriaasia sairastavilla potilailla tehdyssä vaiheen I tutkimuksessa muutokset systeemisessä altistuksessa (Cmax ja AUCinf) midatsolaamille, S‑varfariinille, omepratsolille, dekstrometorfaanille ja kofeiinille eivät olleet guselkumabikerta-annoksen jälkeen kliinisesti oleellisia, mikä osoittaa, että yhteisvaikutukset guselkumabin ja eri CYP-entsyymien substraattien (CYP3A4, CYP2C9, CYP2C19, CYP2D6 ja CYP1A2) välillä eivät ole todennäköisiä. Annosmuutokset eivät ole tarpeen, jos guselkumabia ja CYP450:n substraatteja annetaan samanaikaisesti.
Samanaikainen immunosuppressiivinen hoito tai valohoito
Guselkumabin tehoa ja turvallisuutta yhdistelmänä immunosuppressiivisten lääkeaineiden, mukaan lukien biologisten lääkkeiden, tai valohoidon kanssa ei ole tutkittu psoriaasia koskevissa tutkimuksissa.
Raskaus ja imetys
Naiset, jotka voivat tulla raskaaksi
Naisten, jotka voivat tulla raskaaksi, on käytettävä tehokasta ehkäisymenetelmää hoidon aikana ja vähintään 12 viikon ajan hoidon päättymisen jälkeen.
Raskaus
Guselkumabin käytöstä raskaana oleville naisille on vain vähän tietoja. Eläimillä tehdyissä tutkimuksissa ei ole havaittu suoria eikä epäsuoria haitallisia vaikutuksia raskauteen, alkion tai sikiön kehitykseen, synnytykseen tai syntymänjälkeiseen kehitykseen (ks. kohta Prekliiniset tiedot turvallisuudesta). Varmuuden vuoksi Tremfya‑valmisteen käyttöä on suositeltavaa välttää raskauden aikana.
Imetys
Ei tiedetä, erittyykö guselkumabi ihmisillä äidinmaitoon. Ihmisen IgG:t erittyvät tunnetusti äidinmaitoon muutaman päivän ajan synnytyksen jälkeen. Pian sen jälkeen pitoisuudet pienenevät vähäisiksi. Näin ollen imetettävälle lapselle tänä ajanjaksona aiheutuvaa riskiä ei voida sulkea pois. On päätettävä, lopetetaanko imetys vai pidättäydytäänkö Tremfya-hoidosta ottaen huomioon imetyksen hyödyt lapselle ja hoidosta koituvat hyödyt äidille. Ks. kohdasta Prekliiniset tiedot turvallisuudesta tietoja guselkumabin erittymisestä eläinten (cynomolgus-apinoiden) maitoon.
Hedelmällisyys
Guselkumabin vaikutusta ihmisen hedelmällisyyteen ei ole tutkittu. Eläinkokeissa ei ole havaittu suoria tai epäsuoria haitallisia vaikutuksia hedelmällisyyteen (ks. kohta Prekliiniset tiedot turvallisuudesta).
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Tremfya‑valmisteella ei ole haitallista vaikutusta ajokykyyn ja koneidenkäyttökykyyn.
Haittavaikutukset
Turvallisuusprofiilin yhteenveto
Yleisin haittavaikutus oli hengitystieinfektiot (kliinisissä tutkimuksissa esiintyvyys noin 8 % haavaista paksusuolitulehdusta sairastavilla potilailla, 11 % Crohnin tautia sairastavilla potilailla ja 15 % psoriaasia ja nivelpsoriaasia sairastavilla potilailla).
Tremfya-hoitoa saaneiden psoriaasia, nivelpsoriaasia, haavaista paksusuolitulehdusta tai Crohnin tautia sairastavien potilaiden kokonaisturvallisuusprofiili on samankaltainen.
Haittavaikutustaulukko
Taulukossa 2 luetellaan haittavaikutukset, joita esiintyi psoriaasia, nivelpsoriaasia, haavaista paksusuolitulehdusta ja Crohnin tautia koskeneissa kliinisissä tutkimuksissa sekä valmisteen markkinoille tulon jälkeen raportoidut haittavaikutukset. Haittavaikutukset on luokiteltu MedDRA-elinjärjestelmän ja esiintymistiheyden mukaan seuraavaa käytäntöä noudattaen: hyvin yleinen (≥ 1/10), yleinen (≥ 1/100, < 1/10), melko harvinainen (≥ 1/1 000, < 1/100), harvinainen (≥ 1/10 000, < 1/1 000), hyvin harvinainen (< 1/10 000), tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin). Haittavaikutukset on esitetty kussakin yleisyysluokassa haittavaikutuksen vakavuuden mukaan alenevassa järjestyksessä.
| Taulukko 2. Haittavaikutusluettelo | ||
| Elinjärjestelmä | Esiintymistiheys | Haittavaikutukset |
| Infektiot | Hyvin yleinen | Hengitystieinfektiot |
| Melko harvinainen | Herpes simplex ‑infektiot | |
| Melko harvinainen | Silsainfektiot | |
| Melko harvinainen | Gastroenteriitti | |
| Immuunijärjestelmä | Harvinainen | Yliherkkyys |
| Harvinainen | Anafylaksia | |
| Hermosto | Yleinen | Päänsärky |
| Ruoansulatuselimistö | Yleinen | Ripuli |
| Iho ja ihonalainen kudos | Yleinen | Ihottuma |
| Melko harvinainen | Urtikaria | |
| Luusto, lihakset ja sidekudos | Yleinen | Nivelkipu |
| Yleisoireet ja antopaikassa todettavat haitat | Yleinen | Injektiokohdan reaktiot |
| Tutkimukset | Yleinen | Suurentunut transaminaasipitoisuus |
| Melko harvinainen | Pienentynyt neutrofiilien määrä | |
Valikoitujen haittavaikutusten kuvaus
Suurentunut transaminaasipitoisuus
Kahdessa vaiheen III kliinisessä nivelpsoriaasitutkimuksessa lumekontrolloitujen jaksojen aikana raportoitiin haittavaikutuksina suurentuneita transaminaasipitoisuuksia (joita olivat suurentunut ALAT-arvo, suurentunut ASAT-arvo, suurentunut maksaentsyymipitoisuus, suurentunut transaminaasipitoisuus, poikkeavuudet maksan toimintakokeissa, hypertransaminasemia) guselkumabihoitoa saaneissa ryhmissä (100 mg ihon alle neljän viikon välein saaneessa ryhmässä 8,6 % ja 100 mg ihon alle kahdeksan viikon välein saaneessa ryhmässä 8,3 %) yleisemmin kuin lumeryhmässä (4,6 %). Suurentuneita transaminaasiarvoja (kuten edellä) raportoitiin 1. vuonna haittavaikutuksina 12,9 %:lla potilaista hoitoa neljän viikon välein saaneessa ryhmässä ja 11,7 %:lla potilaista hoitoa kahdeksan viikon välein saaneessa ryhmässä.
Transaminaasipitoisuuden (ASAT ja ALAT) suureneminen oli laboratoriotutkimusten perusteella useimmiten ≤ 3 x ULN (ULN = upper limit of normal, viitearvojen yläraja). Transaminaasipitoisuus suureni harvoin tasoille > 3 – ≤ 5 x ULN ja > 5 x ULN, ja tällaista havaittiin guselkumabihoitoa neljän viikon välein saaneessa ryhmässä useammin kuin guselkumabihoitoa kahdeksan viikon välein saaneessa ryhmässä (taulukko 3). Kaksi vuotta kestäneen vaiheen III kliinisen nivelpsoriaasitutkimuksen loppuun mennessä havaittiin, että esiintyvyys vaikeusasteittain ja hoitoryhmittäin oli samankaltainen.
| Taulukko 3. Suurentuneen transaminaasipitoisuuden esiintyvyys lähtötilanteen jälkeen kahdessa vaiheen III kliinisessä nivelpsoriaasitutkimuksessa | |||||
| 24 viikon aikanaa | 1 vuoden aikanab | ||||
| Lumelääke N = 370c | guselkumabi 100 mg 8 viikon välein N = 373c | guselkumabi 100 mg 4 viikon välein N = 371c | guselkumabi 100 mg 8 viikon välein N = 373c | guselkumabi 100 mg 4 viikon välein N = 371c | |
| ALAT | |||||
| > 1 – ≤ 3 x ULN | 30,0 % | 28,2 % | 35,0 % | 33,5 % | 41,2 % |
| > 3 – ≤ 5 x ULN | 1,4 % | 1,1 % | 2,7 % | 1,6 % | 4,6 % |
| > 5 x ULN | 0,8 % | 0,8 % | 1,1 % | 1,1 % | 1,1 % |
| ASAT | |||||
| > 1 – ≤ 3 x ULN | 20,0 % | 18,8 % | 21,6 % | 22,8 % | 27,8 % |
| > 3 – ≤ 5 x ULN | 0,5 % | 1,6 % | 1,6 % | 2,9 % | 3,8 % |
| > 5 x ULN | 1,1 % | 0,5 % | 1,6 % | 0,5 % | 1,6 % |
| a lumekontrolloitu jakso b mukana ei ole lumehoitoon lähtötilanteessa satunnaistettuja ja myöhemmin guselkumabihoitoon siirtyneitä potilaita c niiden potilaiden lukumäärä, joista ajanjakson aikana vähintään yksi lähtötilanteen jälkeen tehty tietyn laboratoriokokeen tulos | |||||
Kliinisissä psoriaasitutkimuksissa ensimmäisen vuoden aikana suurentuneen transaminaasipitoisuuden (ALAT ja ASAT) esiintyvyys oli guselkumabihoitoa kahdeksan viikon välein saaneessa ryhmässä samankaltainen kuin kliinisissä nivelpsoriaasitutkimuksissa guselkumabihoitoa kahdeksan viikon välein saaneessa ryhmässä. Suurentuneiden transaminaasipitoisuuksien ilmaantuvuus ei lisääntynyt viiden vuoden aikana kutakin guselkumabihoitovuotta kohden arvioituna. Transaminaasipitoisuuksien suureneminen oli useimmiten ≤ 3 x ULN.
Transaminaasipitoisuuden suureneminen oli useimmiten ohimenevää eikä johtanut hoidon lopettamiseen.
Yhdistetyissä vaiheen II ja vaiheen III kliinisissä Crohnin tautia koskeneissa tutkimuksissa suurentuneita transaminaasipitoisuuksia (käsittää suurentuneen ALAT-arvon, suurentuneen ASAT-arvon, suurentuneen maksaentsyymipitoisuuden, suurentuneen transaminaasipitoisuuden ja suurentuneet maksan toimintakokeiden tulokset) koskevia haittavaikutuksia raportoitiin koko lumekontrolloidun induktiojakson (viikot 0–12) aikana yleisemmin guselkumabihoitoa saaneissa ryhmissä (1,7 %:lla potilaista) kuin lumeryhmässä (0,6 %:lla potilaista). Yhdistetyissä vaiheen II ja vaiheen III kliinisissä Crohnin tautia koskeneissa tutkimuksissa suurentuneita transaminaasipitoisuuksia (käsittää suurentuneen ALAT-arvon, suurentuneen ASAT-arvon, suurentuneen maksaentsyymipitoisuuden, suurentuneen transaminaasipitoisuuden, poikkeavan maksan toiminnan ja suurentuneet maksan toimintakokeiden tulokset) koskevia haittavaikutuksia raportoitiin noin yhden vuoden raportointijakson aikana 3,4 %:lla potilaista 200 mg guselkumabia ihon alle neljän viikon välein saaneessa hoitoryhmässä ja 4,1 %:lla potilaista 100 mg guselkumabia ihon alle kahdeksan viikon välein saaneessa hoitoryhmässä verrattuna 2,4 %:iin lumeryhmässä.
Yhdistetyissä vaiheen II ja vaiheen III kliinisissä Crohnin tautia koskeneissa tutkimuksissa tehtyjen laboratoriotutkimusten perusteella kohonneiden ALAT- tai ASAT-arvojen yleisyys oli pienempi kuin nivelpsoriaasia koskeneissa vaiheen III kliinisissä tutkimuksissa. Yhdistettyjen vaiheen II ja vaiheen III kliinisten Crohnin tautia koskeneiden tutkimusten lumekontrolloidun jakson (viikko 12) aikana guselkumabihoitoa saaneilla potilailla raportoitiin tasolle ≥ 3 x ULN kohonneita ALAT-arvoja (< 1 %:lla potilaista) ja ASAT-arvoja (< 1 %:lla potilaista). Yhdistetyissä vaiheen II ja vaiheen III kliinisissä Crohnin tautia koskeneissa tutkimuksissa tasolle ≥ 3 x ULN kohonneita ALAT-arvoja ja/tai ASAT-arvoja raportoitiin noin yhden vuoden raportointijakson aikana 2,7 %:lla potilaista 200 mg guselkumabia ihon alle neljän viikon välein saaneessa ryhmässä ja 2,6 %:lla potilaista 100 mg guselkumabia ihon alle kahdeksan viikon välein saaneessa ryhmässä verrattuna 1,9 %:iin lumeryhmässä. Transaminaasipitoisuuden suureneminen oli useimmiten ohimenevää eikä johtanut hoidon keskeyttämiseen.
Pienentynyt neutrofiilimäärä
Pienentyneitä neutrofiilimääriä raportoitiin kahdessa vaiheen III kliinisessä nivelpsoriaasitutkimuksessa lumekontrolloidun jakson aikana haittavaikutuksena guselkumabihoitoa saaneessa ryhmässä (0,9 %) yleisemmin kuin lumeryhmässä (0 %). Pienentyneitä neutrofiilimääriä raportoitiin 1. vuonna haittavaikutuksena 0,9 %:lla guselkumabihoitoa saaneista potilaista. Veren neutrofiilimäärän väheneminen oli useimmiten lievää, ohimenevää, infektioon liittymätöntä, eikä se johtanut hoidon keskeyttämiseen.
Gastroenteriitti
Gastroenteriittiä esiintyi kahden vaiheen III kliinisen psoriaasitutkimuksen lumekontrolloidun jakson aikana yleisemmin guselkumabihoitoa saaneessa ryhmässä (1,1 %) kuin lumeryhmässä (0,7 %). Viikkoon 264 mennessä 5,8 % kaikista guselkumabihoitoa saaneista potilaista raportoi gastroenteriittiä. Haittavaikutuksena esiintyneet gastroenteriitit eivät olleet vakavia eivätkä johtaneet viikkoon 264 mennessä guselkumabihoidon keskeyttämiseen. Gastroenteriitin esiintyvyyden havaittiin olleen kliinisten nivelpsoriaasitutkimusten lumekontrolloidun jakson aikana samankaltainen kuin kliinisissä psoriaasitutkimuksissa.
Injektiokohdan reaktiot
Injektiokohdan reaktioita liittyi kahden vaiheen III kliinisen psoriaasitutkimuksen viikkoon 48 mennessä 0,7 %:iin guselkumabi‑injektioista ja 0,3 %:iin lumeinjektioista. Viikkoon 264 mennessä 0,4 %:iin guselkumabi-injektioista liittyi injektiokohdan reaktioita. Injektiokohdan reaktiot olivat yleensä vaikeusasteeltaan lieviä tai keskivaikeita, yksikään tapauksista ei ollut vakava; yksi tapaus johti guselkumabihoidon keskeyttämiseen.
Kahdessa vaiheen III kliinisessä nivelpsoriaasitutkimuksessa viikkoon 24 mennessä yhden tai useampia injektiokohdan reaktioita raportoineiden potilaiden lukumäärä oli pieni ja guselkumabiryhmissä hieman suurempi kuin lumeryhmässä: guselkumabihoitoa kahdeksan viikon välein saaneessa ryhmässä 5 (1,3 %) potilasta, guselkumabihoitoa neljän viikon välein saaneessa ryhmässä 4 (1,1 %) potilasta ja lumeryhmässä 1 (0,3 %) potilas. Yksi potilas lopetti guselkumabihoidon kliinisen nivelpsoriaasitutkimuksen lumekontrolloidun jakson aikana injektiokohdan reaktion vuoksi. Yhden tai useamman injektiokohdan reaktion raportoineiden potilaiden osuus 1. vuonna oli 1,6 % guselkumabihoitoa kahdeksan viikon välein saaneessa ryhmässä ja 2,4 % guselkumabihoitoa neljän viikon välein saaneessa ryhmässä. Sellaisten injektioiden lukumäärän, joihin liittyi injektiokohdan reaktioita, havaittiin olleen kliinisten nivelpsoriaasitutkimusten lumekontrolloidun jakson aikana yleisesti samankaltainen kuin kliinisissä psoriaasitutkimuksissa.
Vaiheen III kliinisessä haavaisen paksusuolitulehduksen ylläpitohoitoa koskeneessa tutkimuksessa viikkoon 44 mennessä yhden tai useampia guselkumabista aiheutuneita injektiokohdan reaktioita raportoineiden osuus oli 200 mg guselkumabia ihon alle neljän viikon välein (haavaisen paksusuolitulehduksen ylläpitohoitoa koskeneessa vaiheen III kliinisessä tutkimuksessa 200 mg guselkumabia annettiin kahtena 100 mg:n injektiona) saaneiden potilaiden ryhmässä 7,9 % (2,5 %:ssa injektioista). 100 mg guselkumabia ihon alle kahdeksan viikon välein saaneessa ryhmässä ei raportoitu injektiokohdan reaktioita. Valtaosa injektiokohdan reaktioista oli lieviä eikä yksikään niistä ollut vakava.
Vaiheen II ja vaiheen III kliinisissä Crohnin tautia koskeneissa tutkimuksissa viikkoon 48 mennessä yhden tai useampia guselkumabista aiheutuneita injektiokohdan reaktioita raportoineiden osuus oli 4,1 % (0,8 %:ssa injektioista) hoitoryhmässä, joka sai 200 mg guselkumabia laskimoon induktiohoitona ja sen jälkeen 200 mg guselkumabia ihon alle neljän viikon välein, ja 1,4 % potilaista (0,6 %:ssa injektioista) ryhmässä, joka sai 200 mg guselkumabia laskimoon induktiohoitona ja sen jälkeen 100 mg ihon alle kahdeksan viikon välein. Injektiokohdan reaktiot olivat kaiken kaikkiaan lieviä eikä yksikään niistä ollut vakava.
Vaiheen III kliinisessä Crohnin tautia koskeneessa tutkimuksessa viikkoon 48 mennessä yhden tai useampia guselkumabista aiheutuneita injektiokohdan reaktioita raportoineiden osuus oli 7 % (1,3 %:ssa injektioista) hoitoryhmässä, joka sai 400 mg ihon alle induktiohoitona ja sen jälkeen 200 mg ihon alle neljän viikon välein, ja 4,3 % potilaista (0,7 %:ssa injektioista) ryhmässä, joka sai 400 mg guselkumabia ihon alle induktiohoitona ja sen jälkeen 100 mg ihon alle kahdeksan viikon välein. Valtaosa injektiokohdan reaktioista oli lieviä eikä yksikään niistä ollut vakava.
Immunogeenisuus
Guselkumabin immunogeenisuutta tutkittiin herkän ja lääkettä sietävän immunomäärityksen avulla.
Vaiheen II ja vaiheen III yhdistetyissä psoriaasi- ja nivelpsoriaasipotilaiden analyyseissä 5 %:lle (n = 145) guselkumabihoitoa saaneista potilaista kehittyi lääkevasta-aineita enintään 52 viikon hoidon aikana. Niistä potilaista, joille lääkevasta-aineita kehittyi, noin 8 %:lla (n = 12) vasta-aineet luokiteltiin neutraloiviksi, mikä vastaa 0,4 %:a kaikista guselkumabihoitoa saaneista potilaista. Vaiheen III yhdistetyissä psoriaasipotilaiden analyyseissa todettiin, että hoitoviikkoon 264 mennessä lääkevasta-aineita oli kehittynyt noin 15 %:lle guselkumabihoitoa saaneista potilaista. Niistä potilaista, joille lääkevasta-aineita kehittyi, noin 5 %:lla vasta-aineet luokiteltiin neutraloiviksi, mikä vastaa 0,76 %:a kaikista guselkumabihoitoa saaneista potilaista. Lääkevasta-aineisiin ei liittynyt hoidon tehon heikkenemistä eikä injektiokohdan reaktioiden kehittymistä.
Pediatrisilla potilailla tehdyssä vaiheen III tutkimuksessa 18 %:lle (n = 21) pediatrisista psoriaasipotilaista, jotka saivat guselkumabihoitoa, kehittyi lääkevasta-aineita enintään 44 viikon hoidon aikana. Niistä potilaista, joille lääkevasta-aineita kehittyi, yhdenkään vasta-aineita ei luokiteltu neutraloiviksi. Guselkumabin vasta-aineisiin ei liittynyt muutoksia farmakokinetiikassa, kliinisessä tehossa eikä injektiokohdan reaktioiden kehittymisessä. Niiden potilaiden lukumäärä, joille guselkumabin vasta-aineita kehittyi, on kuitenkin liian pieni varmojen päätelmien tekemiseksi vasta-aineiden vaikutuksesta guselkumabin tehoon ja turvallisuuteen.
Vaiheen II ja vaiheen III yhdistetyissä analyyseissä haavaista paksusuolitulehdusta sairastavista potilaista noin 12 %:lle (n = 58) guselkumabihoitoa enintään 56 viikon ajan saaneista potilaista kehittyi lääkevasta-aineita. Niistä potilaista, joille lääkevasta-aineita kehittyi, noin 16 %:lla (n = 9) oli neutraloiviksi luokiteltavia vasta-aineita, mikä vastaa 2 %:a kaikista guselkumabihoitoa saaneista potilaista. Lääkevasta-aineisiin ei liittynyt heikompaa tehoa eikä injektiokohdan reaktioiden kehittymistä.
Vaiheen II ja vaiheen III yhdistetyissä Crohnin tautia sairastavien potilaiden analyyseissä viikkoon 48 saakka guselkumabia laskimoon annettavana induktiohoitona ja sen jälkeen ihon alle annettavana ylläpitohoitona saaneista potilaista noin 5 %:lle (n = 30) kehittyi lääkevasta-aineita. Niistä potilaista, joille lääkevasta-aineita kehittyi, noin 7 %:lla (n = 2) oli neutraloiviksi luokiteltavia vasta-aineita, mikä vastaa 0,3 %:a guselkumabihoitoa saaneista potilaista. Vaiheen III analyysissä viikkoon 48 saakka Crohnin tautia sairastavista potilaista, jotka saivat guselkumabihoitoa ihon alle annettavana induktiohoitona ja sen jälkeen ihon alle annettavana ylläpitohoitona, noin 9 %:lle (n = 24) kehittyi lääkevasta-aineita. Näistä potilaista 13 %:lla (n = 3) oli vasta-aineita, jotka luokiteltiin neutraloiviksi vasta-aineiksi, mikä vastaa 1 %:a guselkumabihoitoa saaneista potilaista. Lääkevasta-aineisiin ei liittynyt hoidon tehon heikkenemistä eikä injektiokohdan reaktioiden kehittymistä.
Pediatriset potilaat
Läiskäpsoriaasi
Guselkumabin turvallisuutta arvioitiin vaiheen III lumevalmisteella ja vaikuttavalla aineella kontrolloidussa tutkimuksessa pediatrisilla potilailla, joilla oli keskivaikea tai vaikea läiskäpsoriaasi. Tässä kliinisessä tutkimuksessa turvallisuutta arvioitiin viikkoon 52 saakka 120 potilaalla, jotka olivat iältään 6–17-vuotiaita. Ihon alle annettujen guselkumabi-injektioiden turvallisuusprofiili käytettäessä 6–17-vuotiaille pediatrisille potilaille 45 mg/0,45 ml esitäytettyä kynää tai 100 mg:n esitäytettyä ruiskua oli yhdenmukainen aikuisiän läiskäpsoriaasia koskeneissa tutkimuksissa raportoidun turvallisuusprofiilin kanssa (ks. kohta Annostus ja antotapa).
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Kliinisissä tutkimuksissa guselkumabia on annettu laskimoon enintään annoksina 1 200 mg sekä ihon alle enintään annoksina 400 mg yhdellä lääkkeen antoon liittyneellä käynnillä, eikä annosta rajoittavaa toksisuutta esiintynyt. Yliannostapauksessa potilasta on seurattava haittavaikutusten oireiden ja löydösten havaitsemiseksi, ja tarkoituksenmukaista oireenmukaista hoitoa on annettava heti.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Immunosuppressantit, interleukiinin estäjät, ATC-koodi: L04AC16.
Vaikutusmekanismi
Guselkumabi on ihmisen IgG1λ monoklonaalinen vasta-aine, joka sitoutuu erittäin spesifisesti ja suurella affiniteetilla antigeenin sitoutumiskohdan kautta selektiivisesti interleukiini-23-proteiiniin (IL‑23). IL-23 on sytokiini, joka osallistuu inflammatorisiin ja immuunivasteisiin. Guselkumabi estää IL-23:n sitoutumisen reseptoriinsa ja estää siten IL-23-riippuvaista solusignalointia ja tulehdusta edistävien sytokiinien vapautumista.
Läiskäpsoriaasia sairastavan potilaan ihossa IL‑23:n pitoisuus on koholla. Guselkumabin osoitettiin in vitro ‑malleissa estävän IL‑23:n biologista aktiivisuutta salpaamalla sen vuorovaikutuksen solun pinnalla olevan IL‑23-reseptorin kanssa ja keskeyttämällä siten IL‑23-välitteisen signaalinvälityksen, aktivaation ja sytokiinikaskadit. Guselkumabin kliiniset hoitovaikutukset läiskäpsoriaasissa ja nivelpsoriaasissa perustuvat IL‑23:n sytokiinireitin salpaukseen.
Psoriaasissa Fc-gamma-reseptoria 1 (CD64) ilmentävien myeloidisolujen on osoitettu olevan tulehtuneessa kudoksessa IL-23:n pääasiallinen lähde. Guselkumabin on osoitettu in vitro salpaavan IL-23:a ja sitoutuvan CD64:ään. Nämä tulokset viittaavat siihen, että guselkumabi kykenee neutraloimaan IL-23:n tulehduksen lähdesoluissa.
Farmakodynaamiset vaikutukset
Guselkumabihoito johti vaiheen I tutkimuksessa IL-23/Th17-reitin geenien ilmentymisen ja psoriaasiin liittyvien geenien ilmentymisprofiilien vähenemiseen. Tämä osoitettiin läiskäpsoriaasia sairastavien potilaiden leesioista otettujen ihon biopsianäytteiden mRNA-analyyseillä viikolla 12 lähtötilanteeseen verrattuna. Guselkumabihoito johti samassa vaiheen I tutkimuksessa psoriaasin histologisten mittareiden paranemiseen viikolla 12, mukaan lukien epidermiksen ohenemiseen ja T‑solutiheyden vähenemiseen. Guselkumabihoitoa saaneilla potilailla havaittiin lisäksi vaiheen II ja vaiheen III läiskäpsoriaasitutkimuksissa seerumin IL-17A-, IL-17F- ja IL-22-pitoisuuksien pienenemistä verrattuna lumelääkkeeseen. Nämä tulokset ovat yhdenmukaisia läiskäpsoriaasia sairastavilla potilailla guselkumabihoidosta havaitun kliinisen hyödyn kanssa.
Vaiheen III nivelpsoriaasitutkimuksissa akuutin vaiheen proteiinien C-reaktiivisen proteiinin, seerumin amyloidi A:n ja IL-6:n sekä Th17-efektorisytokiinien IL-17A, IL-17F ja IL-22 pitoisuus seerumissa oli lähtötilanteessa koholla. Guselkumabi pienensi näiden proteiinien pitoisuutta 4 viikon kuluessa hoidon aloittamisesta. Guselkumabi lisäksi pienensi näiden proteiinien pitoisuutta viikkoon 24 mennessä lähtötilanteeseen ja myös lumelääkkeeseen verrattuna.
Kliininen teho ja turvallisuus
Aikuisiän läiskäpsoriaasi
Guselkumabin tehoa ja turvallisuutta arvioitiin kolmessa satunnaistetussa, kaksoissokkoutetussa, aktiivisella aineella kontrolloidussa vaiheen III tutkimuksessa aikuispotilailla, joilla oli keskivaikea tai vaikea läiskäpsoriaasi ja joille harkittiin valohoitoa tai systeemistä hoitoa.
VOYAGE 1 ja VOYAGE 2
Kahdessa tutkimuksessa (VOYAGE 1 ja VOYAGE 2) tutkittiin guselkumabin tehoa ja turvallisuutta 1 829 aikuispotilaalla lumehoitoon ja adalimumabiin verrattuna. Guselkumabihoitoon satunnaistetut potilaat (N = 825) saivat 100 mg:n annoksia viikoilla 0 ja 4, ja sen jälkeen 8 viikon välein viikkoon 48 saakka (VOYAGE 1) ja viikkoon 20 saakka (VOYAGE 2). Adalimumabihoitoon satunnaistetut potilaat (N = 582) saivat 80 mg:n annoksen viikolla 0 ja 40 mg:n annoksen viikolla 1, ja sen jälkeen 40 mg joka toinen viikko viikkoon 48 saakka (VOYAGE 1) ja viikkoon 23 saakka (VOYAGE 2). Kummassakin tutkimuksessa lumehoitoon satunnaistetut potilaat (N = 422) saivat guselkumabia 100 mg:n annoksina viikoilla 16 ja 20 sekä sen jälkeen 8 viikon välein. VOYAGE 1-tutkimuksessa kaikki potilaat, myös adalimumabihoitoon viikolla 0 satunnaistetut potilaat, aloittivat avoimen vaiheen guselkumabihoidon (8 viikon välein) viikolla 52. Tutkimuksessa VOYAGE 2 guselkumabihoitoon viikolla 0 satunnaistetut potilaat, jotka olivat saaneet PASI 90 (Psoriasis Area and Severity Index) ‑vasteen viikolla 28, satunnaistettiin uudelleen joko jatkamaan guselkumabihoitoa kahdeksan viikon välein (ylläpitohoito) tai saamaan lumehoitoa (hoidon lopettaminen). Hoidon lopettamiseen satunnaistetut potilaat aloittivat guselkumabihoidon uudestaan (hoitoa annettiin hoidon uudestaan aloittamisajankohtana, 4 viikon kuluttua ja sen jälkeen 8 viikon välein), kun vähintään 50 % viikolla 28 todetusta PASI-vasteen paranemisesta oli hävinnyt. Adalimumabihoitoon viikolla 0 satunnaistetut potilaat, jotka eivät olleet saaneet PASI 90‑vastetta, saivat guselkumabia viikoilla 28 ja 32 ja sen jälkeen 8 viikon välein. VOYAGE 2 -tutkimuksessa kaikki potilaat aloittivat avoimen vaiheen guselkumabihoidon (8 viikon välein) viikolla 76.
Sairauden ominaisuudet lähtötilanteessa olivat tutkimusten VOYAGE 1 ja 2 potilasjoukoissa yhdenmukaiset: kehon pinta-alan (body surface area, BSA) mediaani oli 22 % (VOYAGE 1) ja 24 % (VOYAGE 2), PASI-pisteiden mediaani lähtötilanteessa oli 19 kummassakin tutkimuksessa, DLQI (dermatology quality of life index) ‑pisteiden mediaani lähtötilanteessa oli 14 (VOYAGE 1) ja 14,5 (VOYAGE 2), lähtötilanteen IGA (investigator global assessment) ‑pisteet osoittivat vaikea-asteista sairautta 25 %:lla (VOYAGE 1) ja 23 %:lla (VOYAGE 2) potilaista ja nivelpsoriaasia oli aiemmin sairastanut 19 % (VOYAGE 1) ja 18 % (VOYAGE 2) potilaista.
Kaikista VOYAGE 1- ja VOYAGE 2 -tutkimuksissa mukana olleista potilaista 32 % (VOYAGE 1) ja 29 % (VOYAGE 2) ei ollut aiemmin saanut tavanomaista systeemistä tai biologista hoitoa, 54 % (VOYAGE 1) ja 57 % (VOYAGE 2) oli aiemmin saanut valohoitoa ja 62 % (VOYAGE 1) ja 64 % (VOYAGE 2) oli aiemmin saanut tavanomaista systeemistä hoitoa. Kummassakin tutkimuksessa 21 % oli saanut aiemmin biologista hoitoa: 11 % oli saanut vähintään yhtä tuumorinekroositekijäalfasalpaajaa (TNFα-salpaaja) ja noin 10 % oli saanut IL-12/IL-23-salpaajaa.
Guselkumabin tehoa arvioitiin ihosairauden kokonaistilanteen, sairauden esiintymisalueen (päänahka, kädet ja jalkaterät sekä kynnet) ja elämänlaadun sekä potilaan raportoiman hoitotuloksen suhteen. VOYAGE 1 ja 2 –tutkimuksissa yhdistetty ensisijainen päätetapahtuma oli niiden potilaiden osuus, jotka saavuttivat parantumista tai minimaalista sairautta osoittavat IGA-pisteet (IGA 0/1) ja PASI 90 ‑vasteen viikolla 16 lumehoitoon verrattuna (ks. taulukko 4).
Ihosairauden kokonaistilanne
Guselkumabihoito paransi taudin aktiivisuutta osoittavia mittareita merkittävästi lume- ja adalimumabihoitoon verrattuna viikolla 16 sekä adalimumabihoitoon verrattuna viikoilla 24 ja 48. Ensisijaisen ja tärkeimmän toissijaisen tutkimuksen päätetapahtumien keskeiset tehoa koskevat tulokset esitetään jäljempänä taulukossa 4.
| Taulukko 4. Yhteenveto kliinisistä vasteista tutkimuksissa VOYAGE 1 ja VOYAGE 2 | ||||||
| Potilaiden lukumäärä (%) | ||||||
| VOYAGE 1 | VOYAGE 2 | |||||
Lumelääke (N = 174) | guselkumabi (N = 329) | adalimumabi (N = 334) | Lumelääke (N = 248) | guselkumabi (N = 496) | adalimumabi (N = 248) | |
| Viikko 16 | ||||||
| PASI 75 | 10 (5,7) | 300 (91,2)a | 244 (73,1)b | 20 (8,1) | 428 (86,3)a | 170 (68,5)b |
| PASI 90 | 5 (2,9) | 241 (73,3)c | 166 (49,7)b | 6 (2,4) | 347 (70,0)c | 116 (46,8)b |
| PASI 100 | 1 (0,6) | 123 (37,4)a | 57 (17,1)d | 2 (0,8) | 169 (34,1)a | 51 (20,6)d |
| IGA 0/1 | 12 (6,9) | 280 (85,1)c | 220 (65,9)b | 21 (8,5) | 417 (84,1)c | 168 (67,7)b |
| IGA 0 | 2 (1,1) | 157 (47,7)a | 88 (26,3)d | 2 (0,8) | 215 (43,3)a | 71 (28,6)d |
| Viikko 24 | ||||||
| PASI 75 | - | 300 (91,2) | 241 (72,2)e | - | 442 (89,1) | 176 (71,0)e |
| PASI 90 | - | 264 (80,2) | 177 (53,0)b | - | 373 (75,2) | 136 (54,8)b |
| PASI 100 | - | 146 (44,4) | 83 (24,9)e | - | 219 (44,2) | 66 (26,6)e |
| IGA 0/1 | - | 277 (84,2) | 206 (61,7)b | - | 414 (83,5) | 161 (64,9)b |
| IGA 0 | - | 173 (52,6) | 98 (29,3)b | - | 257 (51,8) | 78 (31,5)b |
| Viikko 48 | ||||||
| PASI 75 | - | 289 (87,8) | 209 (62,6)e | - | - | - |
| PASI 90 | - | 251 (76,3) | 160 (47,9)b | - | - | - |
| PASI 100 | - | 156 (47,4) | 78 (23,4)e | - | - | - |
| IGA 0/1 | - | 265 (80,5) | 185 (55,4)b | - | - | - |
| IGA 0 | - | 166 (50,5) | 86 (25,7)b | - | - | - |
| a p < 0,001 guselkumabin ja lumehoidon vertailulle. b p < 0,001 guselkumabin ja adalimumabin tärkeimpien toissijaisten päätetapahtumien vertailulle. c p < 0,001 guselkumabin ja lumehoidon yhdistetyn ensisijaisen päätetapahtuman vertailulle. d guselkumabin ja adalimumabin välillä ei tehty vertailuja. e p < 0,001 guselkumabin ja adalimumabin väliselle vertailulle. | ||||||
Ajan mittaan todettu vaste
Guselkumabin vaikutuksen todettiin alkavan nopeasti, ja PASI-indeksin paranemisprosentti oli merkittävästi suurempi lumehoitoon verrattuna jo viikolla 2 (p < 0,001). PASI 90 -vasteen saavuttaneiden potilaiden prosenttiosuus oli guselkumabihoidossa numeerisesti suurempi kuin adalimumabihoidossa, mikä oli todettavissa alkaen viikosta 8, ja ero oli suurimmillaan noin viikolla 20 (VOYAGE 1 ja 2) ja säilyi viikkoon 48 saakka (VOYAGE 1) (ks. kuva 1).
Kuva 1. PASI 90 ‑vasteen viikkoon 48 saakka saavuttaneiden potilaiden prosenttiosuus tutkimuksen VOYAGE 1 tutkimuskäynneittäin (potilaat satunnaistettu viikolla 0)
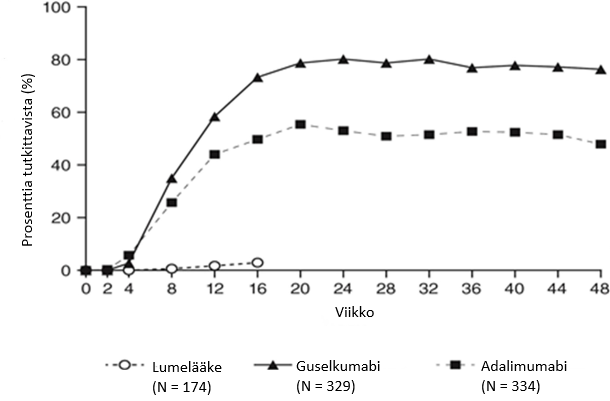
VOYAGE 1 ‑tutkimuksessa jatkuvaa guselkumabihoitoa saavien tutkittavien PASI 90 ‑vaste säilyi viikosta 52 viikkoon 252. Potilailla, jotka satunnaistettiin viikolla 0 adalimumabihoitoon ja siirtyivät viikolla 52 guselkumabihoitoon, PASI 90 ‑vasteluku suureni viikosta 52 viikkoon 76 ja säilyi sen jälkeen viikkoon 252 saakka (ks. kuva 2).
Kuva 2. PASI 90 ‑vasteen saavuttaneiden potilaiden prosenttiosuus tutkimuksen VOYAGE 1 avoimessa vaiheessa tutkimuskäynneittäin
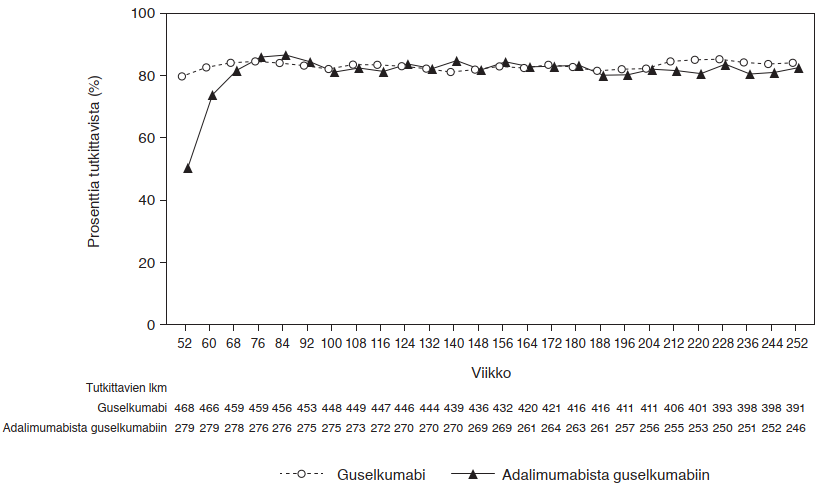
Guselkumabin teho ja turvallisuus osoitettiin riippumatta iästä, sukupuolesta, rodusta, painosta, läiskien sijainnista, sairauden vaikeusasteesta lähtötilanteessa PASI-pisteiden perusteella, samanaikaisesta nivelpsoriaasista ja aiemmasta biologisesta hoidosta. Guselkumabin teho todettiin potilailla, jotka eivät olleet aiemmin saaneet tavanomaista systeemistä tai biologista hoitoa, sekä potilailla, jotka olivat aiemmin saaneet biologista hoitoa.
Tutkimuksessa VOYAGE 2 guselkumabia ylläpitohoitoon viikolla 48 saaneista potilaista 88,6 % oli saanut PASI 90 ‑vasteen verrattuna 36,8 %:iin potilaista, joiden hoito lopetettiin viikolla 28 (p < 0,001). PASI 90 ‑vasteen häviäminen todettiin jo 4 viikkoa guselkumabihoidon lopettamisen jälkeen, ja ajan mediaani PASI 90 ‑vasteen häviämiseen oli noin 15 viikkoa. Niistä potilaista, joiden hoito lopetettiin ja joille sen jälkeen aloitettiin guselkumabihoito uudestaan, 80 % oli saanut PASI 90 ‑vasteen uudelleen, kun vastetta arvioitiin 20 viikkoa hoidon uudestaan aloittamisen jälkeen.
VOYAGE 2 -tutkimuksessa adalimumabihoitoon satunnaistetuista 112 potilaasta, jotka eivät olleet saavuttaneet PASI 90 ‑vastetta viikolla 28, 66 % saavutti PASI 90 ‑vasteen 20 guselkumabihoitoviikon jälkeen, ja 76 % saavutti PASI 90 ‑vasteen 44 guselkumabihoitoviikon jälkeen. Lisäksi guselkumabihoitoon satunnaistetuista 95 potilaasta, jotka eivät olleet saavuttaneet PASI 90 ‑vastetta viikolla 28, 36 % saavutti PASI 90 ‑vasteen vielä 20 viikon ajan jatketun guselkumabihoidon jälkeen, ja 41 % saavutti PASI 90 ‑vasteen vielä 44 viikon ajan jatketun guselkumabihoidon jälkeen. Adalimumabihoidosta guselkumabihoitoon siirtyneillä potilailla ei havaittu uusia turvallisuutta koskevia löydöksiä.
Erityisalueiden sairaus
Tutkimuksissa VOYAGE 1 ja 2 päänahassa, käsissä ja jalkaterissä sekä kynsipsoriaasissa (mitattiin päänahkaspesifisellä tutkijan kokonaisarviolla [Scalp-specific Investigator Global Assessment, ss-IGA], lääkärin kokonaisarviolla käsistä ja/tai jalkateristä [Physician’s Global Assessment of Hands and/or Feet, hf-PGA], lääkärin kokonaisarviolla kynsistä [Fingernail Physician’s Global Assessment, f-PGA] ja kynsipsoriaasin vaikeusasteindeksillä [Nail Psoriasis Severity Index, NAPSI]) todettiin viikolla 16 merkittävää paranemista guselkumabihoitoa saaneilla potilailla verrattuna lumehoitoa saaneisiin potilaisiin (p < 0,001, taulukko 5). Guselkumabi osoitettiin adalimumabia paremmaksi päänahan sekä käsien ja jalkaterien psoriaasin osalta viikolla 24 (VOYAGE 1 ja 2) sekä viikolla 48 (VOYAGE 1) (p ≤ 0,001, lukuun ottamatta käsien ja jalkaterien psoriaasia viikolla 24 [VOYAGE 2] ja viikolla 48 [VOYAGE 1], p < 0,05).
| Taulukko 5. Yhteenveto erityisalueiden sairauden vasteista tutkimuksissa VOYAGE 1 ja VOYAGE 2 | ||||||
| VOYAGE 1 | VOYAGE 2 | |||||
| Lumelääke | guselkumabi | adalimumabi | Lumelääke | guselkumabi | adalimumabi | |
| ss-IGA (N)a | 145 | 277 | 286 | 202 | 408 | 194 |
| ss-IGA 0/1b, n (%) | ||||||
| Viikko 16 | 21 (14,5) | 231 (83,4)c | 201 (70,3)d | 22 (10,9) | 329 (80,6)c | 130 (67,0)d |
| hf-PGA (N)a | 43 | 90 | 95 | 63 | 114 | 56 |
| hf-PGA 0/1b, n (%) | ||||||
| Viikko 16 | 6 (14,0) | 66 (73,3)e | 53 (55,8)d | 9 (14,3) | 88 (77,2)e | 40 (71,4)d |
| f-PGA (N)a | 88 | 174 | 173 | 123 | 246 | 124 |
| f-PGA 0/1, n (%) | ||||||
| Viikko 16 | 14 (15,9) | 68 (39,1)e | 88 (50,9)d | 18 (14,6) | 128 (52,0)e | 74 (59,7)d |
| NAPSI (N)a | 99 | 194 | 191 | 140 | 280 | 140 |
| Paraneminen prosenttia, keskiarvo (keskihajonta) | ||||||
| Viikko 16 | -0,9 (57,9) | 34,4 (42,4)e | 38,0 (53,9)d | 1,8 (53,8) | 39,6 (45,6)e | 46,9 (48,1)d |
| a käsittää vain potilaat, joiden lähtötilanteen ss-IGA-, f-PGA-, hf-PGA-pisteet ≥ 2 tai lähtötilanteen NAPSI-pisteet > 0. b käsittää vain potilaat, jotka saavuttivat ss-IGA- ja/tai hf-PGA-arvioinneissa ≥ 2 yksikön paranemisen lähtötilanteesta. c p < 0,001 guselkumabin ja lumehoidon vertailulle tärkeimmän toissijaisen päätetapahtuman osalta. d guselkumabin ja adalimumabin välillä ei tehty vertailuja. e p < 0,001 guselkumabin ja lumehoidon vertailulle. | ||||||
Terveyteen liittyvä elämänlaatu / potilaiden raportoimat hoitotulokset
Tutkimuksissa VOYAGE 1 ja 2 todettiin guselkumabihoitoa saaneilla potilailla lumehoitoa saaneisiin potilaisiin verrattuna viikolla 16 merkittävästi suurempaa terveyteen liittyvän elämänlaadun paranemista. Tämä mitattiin ihoon liittyvällä elämänlaatuindeksillä (Dermatology Life Quality Index, DLQI) sekä potilaan raportoimilla psoriaasin oireilla (kutina, kipu, kirvely, pistely ja ihon kiristäminen) ja löydöksillä (ihon kuivuus, halkeilu, suomuisuus, irtoaminen tai hilseily, punoitus ja verenvuoto), joita mitattiin psoriaasin oireita ja löydöksiä koskevalla päiväkirjalla (Psoriasis Symptoms and Signs Diary, PSSD) (taulukko 6). Potilaiden raportoimien hoitotulosten perusteella oireiden paraneminen säilyi viikkoon 24 (VOYAGE 1 ja 2) ja viikkoon 48 (VOYAGE 1) saakka. VOYAGE 1 -tutkimuksessa oireiden paraneminen säilyi jatkuvaa guselkumabihoitoa saaneilla potilailla avoimessa vaiheessa viikkoon 252 saakka (taulukko 7).
| Taulukko 6. Yhteenveto potilaiden viikolla 16 raportoimista hoitotuloksista tutkimuksissa VOYAGE 1 ja VOYAGE 2 | ||||||
| VOYAGE 1 | VOYAGE 2 | |||||
| Lumelääke | guselkumabi | adalimumabi | Lumelääke | guselkumabi | adalimumabi | |
| DLQI, potilaiden lähtötilanteen pisteet | 170 | 322 | 328 | 248 | 495 | 247 |
| Muutos lähtötilanteesta, keskiarvo (keskihajonta) | ||||||
| Viikko 16 | -0,6 (6,4) | -11,2 (7,2)c | -9,3 (7,8)b | -2,6 (6,9) | -11,3 (6,8)c | -9,7 (6,8)b |
| PSSD-oireita koskevat pisteet, potilaiden lähtötilanteen pisteet > 0 | 129 | 248 | 273 | 198 | 410 | 200 |
| Oireita koskevat pisteet = 0, n (%) | ||||||
| Viikko 16 | 1 (0,8) | 67 (27,0)a | 45 (16,5)b | 0 | 112 (27,3)a | 30 (15,0)b |
| PSSD-löydöksiä koskevat pisteet, potilaiden lähtötilanteen pisteet > 0 | 129 | 248 | 274 | 198 | 411 | 201 |
| Löydöksiä koskevat pisteet = 0, n (%) | ||||||
| Viikko 16 | 0 | 50 (20,2)a | 32 (11,7)b | 0 | 86 (20,9)a | 21 (10,4)b |
| a p < 0,001 guselkumabin ja lumehoidon vertailulle. b guselkumabin ja adalimumabin välillä ei tehty vertailuja. c p < 0,001 guselkumabin ja lumehoidon vertailulle tärkeimmän toissijaisen päätetapahtuman osalta. | ||||||
| Taulukko 7. Yhteenveto potilaiden raportoimista hoitotuloksista tutkimuksen VOYAGE 1 avoimessa vaiheessa | ||||||
| guselkumabi | adalimumabi-guselkumabi | |||||
| Viikko 76 | Viikko 156 | Viikko 252 | Viikko 76 | Viikko 156 | Viikko 252 | |
| DLQI-pisteet > 1 lähtötilanteessa, n | 445 | 420 | 374 | 264 | 255 | 235 |
| Potilaita, joiden DLQI-pisteet 0/1 | 337 (75,7 %) | 308 (73,3 %) | 272 (72,7 %) | 198 (75,0 %) | 190 (74,5 %) | 174 (74,0 %) |
| PSSD-oireita koskevat pisteet, potilaiden lähtötilanteen pisteet > 0 | 347 | 327 | 297 | 227 | 218 | 200 |
| Oireita koskevat pisteet = 0, n (%) | 136 (39,2 %) | 130 (39,8 %) | 126 (42,4 %) | 99 (43,6 %) | 96 (44,0 %) | 96 (48,0 %) |
| PSSD-löydöksiä koskevat pisteet, potilaiden lähtötilanteen pisteet > 0 | 347 | 327 | 297 | 228 | 219 | 201 |
| Löydöksiä koskevat pisteet = 0, n (%) | 102 (29,4 %) | 94 (28,7 %) | 98 (33,0 %) | 71 (31,1 %) | 69 (31,5 %) | 76 (37,8 %) |
Tutkimuksessa VOYAGE 2 guselkumabihoitoa saaneilla potilailla todettiin viikolla 16 terveyteen liittyvässä elämänlaadussa, ahdistuneisuudessa ja masennuksessa sekä työkyvyn rajoittumisessa merkittävästi suurempaa paranemista lähtötilanteesta lumehoitoon verrattuna. Näitä mitattiin 36‑kohtaisella terveyskyselyllä (Short Form health survey questionnaire, SF-36), sairaalassa tehtävällä ahdistuneisuuden ja masennuksen pisteytyksellä (Hospital Anxiety and Depression Scale, HADS) sekä työkyvyn rajoittumista koskevalla kyselyllä (Work Limitations Questionnaire, WLQ). SF-36-, HADS- ja WLQ-indekseissä todettu paraneminen säilyi viikolla 28 ylläpitohoitoon satunnaistetuilla potilailla viikkoon 48 saakka ja avoimessa vaiheessa viikkoon 252 saakka.
NAVIGATE
NAVIGATE-tutkimuksessa selvitettiin guselkumabin tehoa potilailla, joiden vaste ustekinumabiin oli viikolla 16 riittämätön (eli jotka eivät olleet saavuttaneet vastetta ”parantunut” tai ”minimaalinen” sairaus, joksi oli määritelty IGA ≥ 2). Kaikki potilaat (N = 871) saivat avoimessa tutkimuksessa ustekinumabia (45 mg ≤ 100 kg ja 90 mg > 100 kg) viikoilla 0 ja 4. 268 potilasta, joiden IGA-pisteet olivat ≥ 2, satunnaistettiin viikolla 16 joko jatkamaan ustekinumabihoitoa (N = 133) 12 viikon välein tai aloittamaan guselkumabihoito (N = 135) viikoilla 16 ja 20 ja sen jälkeen 8 viikon välein. Satunnaistettujen potilaiden ominaisuudet olivat lähtötilanteessa samankaltaiset kuin tutkimuksissa VOYAGE 1 ja 2.
Satunnaistamisen jälkeen ensisijainen päätetapahtuma oli satunnaistamisen jälkeisten tutkimuskäyntien lukumäärä viikkojen 12ja 24 välillä, jolloin potilaat saavuttivat IGA-pisteet 0/1 ja ≥ 2 yksikön paranemisen. Potilaat tutkittiin neljän viikon välein yhteensä neljällä tutkimuskäynnillä. Niistä potilaista, joilla vaste ustekinumabiin oli satunnaistamisajankohtana riittämätön, havaittiin merkittävästi suurempaa tehon paranemista siinä potilasjoukossa, joka siirtyi guselkumabihoitoon, verrattuna ustekinumabihoitoa jatkaneisiin potilaisiin. Satunnaistamisen jälkeisten viikkojen 12 ja 24 välillä guselkumabipotilaat saavuttivat IGA-pisteet 0/1 ja ≥ 2 yksikön paranemisen kaksi kertaa niin usein kuin ustekinumabia saaneet potilaat (keskiarvo 1,5 [guselkumabi] vs 0,7 [ustekinumabi] tutkimuskäyntiä, p < 0,001). Lisäksi 12 viikon kuluttua satunnaistamisesta suurempi osuus guselkumabia saaneista potilaista verrattuna ustekinumabia saaneisiin potilaisiin saavutti IGA-pisteet 0/1 ja ≥ 2 yksikön paranemisen (31,1 % [guselkumabi] vs. 14,3 % [ustekinumabi], p = 0,001) ja PASI 90 ‑vasteen (48 % [guselkumabi] vs 23 % [ustekinumabi], p < 0,001). Erot guselkumabi- ja ustekinumabihoitoa saaneiden potilaiden vasteluvuissa havaittiin jo 4 viikkoa satunnaistamisen jälkeen (11,1 % [guselkumabi] ja 9,0 % [ustekinumabi]), ja ne olivat suurimmillaan 24 viikkoa satunnaistamisen jälkeen (ks. kuva 3). Ustekinumabihoidosta guselkumabihoitoon siirtyneillä potilailla ei havaittu uusia turvallisuutta koskevia löydöksiä.
Kuva 3. IGA-pisteet parantunut (0) tai minimaalinen sairaus (1) ja IGA-pisteiden vähintään 2 yksikön paranemisen viikosta 0 viikkoon 24 saakka saavuttaneiden potilaiden prosenttiosuus tutkimuskäynneittäin tutkimuksen NAVIGATE satunnaistamisen jälkeen
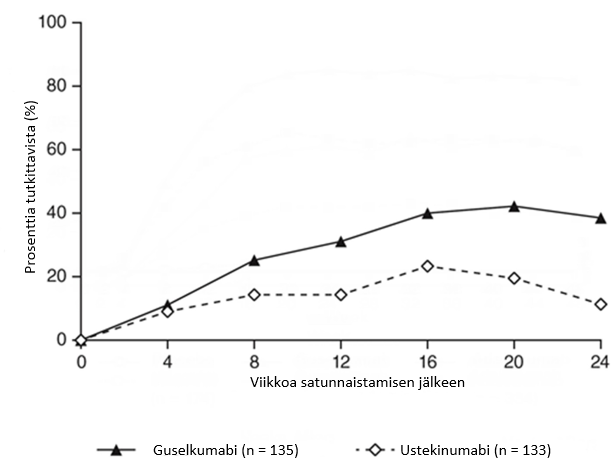
ECLIPSE
Guselkumabin tehoa ja turvallisuutta tutkittiin myös kaksoissokkotutkimuksessa, jossa sitä verrattiin sekukinumabiin. Potilaat satunnaistettiin saamaan guselkumabia (N = 534; 100 mg viikoilla 0 ja 4 ja sen jälkeen kerran 8 viikossa) tai sekukinumabia (N = 514; 300 mg viikoilla 0, 1, 2, 3 ja 4 ja sen jälkeen kerran 4 viikossa). Kummassakin hoitoryhmässä viimeinen annos annettiin viikolla 44.
Sairauden ominaisuudet olivat keskivaikeaa tai vaikeaa läiskäpsoriaasia sairastavilla potilailla lähtötilanteessa yhdenmukaiset: ihottumaa oli 20 %:ssa (mediaani) kehon pinta-alasta, PASI-pisteiden mediaani oli 18, ja 24 %:lla potilaista oli vaikea-asteisen sairauden osoittavat IGA-pisteet.
Ensisijaisella päätetapahtumalla (PASI 90 ‑vaste viikolla 48) mitattuna guselkumabi oli sekukinumabia parempi (84,5 % versus 70,0 %, p < 0,001). PASI-vastelukujen vertailu esitetään taulukossa 8.
| Taulukko 8. PASI-vasteluvut ECLIPSE-tutkimuksessa | ||
| Potilaiden lukumäärä (%) | ||
| guselkumabi (N = 534) | sekukinumabi (N = 514) | |
| Ensisijainen päätetapahtuma | ||
| PASI 90 ‑vaste viikolla 48 | 451 (84,5 %) a | 360 (70,0 %) |
| Tärkeimmät toissijaiset päätetapahtumat | ||
| PASI 75 ‑vaste sekä viikolla 12 että viikolla 48 | 452 (84,6 %)b | 412 (80,2 %) |
| PASI 75 ‑vaste viikolla 12 | 477 (89,3 %)c | 471 (91,6 %) |
| PASI 90 ‑vaste viikolla 12 | 369 (69,1 %)c | 391 (76,1 %) |
| PASI 100 ‑vaste viikolla 48 | 311 (58,2 %)c | 249 (48,4 %) |
| a p < 0,001 paremmuuden osalta b p < 0,001 vertailukelpoisuuden osalta, p = 0,062 paremmuuden osalta c varsinaista tilastollista testausta ei tehty | ||
PASI 90 ‑vasteluvut guselkumabi- ja sekukinumabihoidossa viikkoon 48 saakka esitetään kuvassa 4.
Kuva 4. PASI 90 ‑vasteen viikkoon 48 saakka saavuttaneiden potilaiden prosenttiosuus tutkimuksen ECLIPSE tutkimuskäynneittäin (potilaat satunnaistettu viikolla 0)
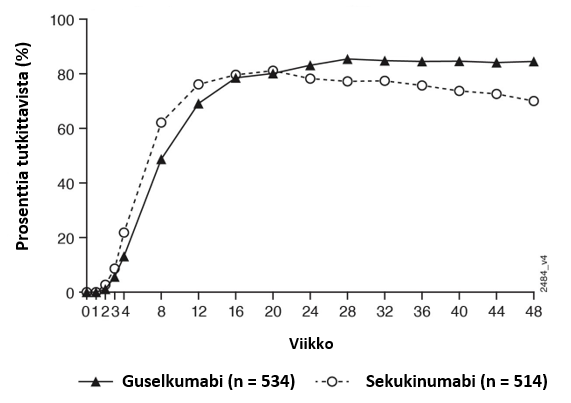
Pediatriset potilaat
Lapsuusiän läiskäpsoriaasi
Guselkumabin turvallisuutta ja tehoa arvioitiin yhdessä satunnaistetussa, lumelääkkeellä ja vaikuttavalla biologisella vertailuvalmisteella kontrolloidussa monikeskustutkimuksessa (PROTOSTAR) 120 pediatrisella potilaalla, jotka olivat iältään 6–17-vuotiaita ja joilla oli keskivaikea tai vaikea läiskäpsoriaasi, joille harkittiin valohoitoa tai systeemistä hoitoa ja joiden sairaus ei ollut valohoidon ja/tai paikallisten hoitojen avulla riittävässä hoitotasapainossa. PROTOSTAR-tutkimus tehtiin kahdessa osassa. Osa 1 käsitti 16 viikon satunnaistetun lumelääkkeellä ja vaikuttavalla vertailuvalmisteella kontrolloidun jakson, jonka jälkeen oli kontrolloimaton jakso, jolloin hoito lopetettiin ja sitä jatkettiin tai aloitettiin viikkoon 52 jatkunut guselkumabihoito. Osa 2 käsitti avoimen guselkumabiryhmän viikkoon 52 saakka.
Mukaan otettujen potilaiden IGA-pisteet olivat ≥ 3 sairauden kokonaisvaikeusastetta kuvaavalla viisiportaisella asteikolla, PASI-vaste oli ≥ 12 ja ihottumaa oli vähimmillään ≥ 10 %:ssa kehon pinta-alasta, ja heillä oli vähintään yksi seuraavista: 1) hyvin paksuja ihomuutoksia, 2) kliinisesti oleellisia psoriaasin oireita kasvoissa, sukupuolielimissä tai käsissä/jalkaterissä, 3) PASI-vaste ≥ 20, 4) ihottumaa > 20 %:ssa kehon pinta-alasta tai 5) IGA-pisteet = 4. Tutkimukseen ei otettu mukaan tutkittavia, joilla oli pisarapsoriaasi, erytroderminen psoriaasi tai märkärakkulainen psoriaasi.
Osassa 1 satunnaistettiin 92 iältään 6–17-vuotiasta potilasta saamaan injektioina ihon alle joko guselkumabia (n = 41) tai lumelääkettä (n = 25) viikoilla 0, 4 ja 12 tai vaikuttavaa biologista vertailuvalmistetta (n = 26) viikoittain. Osassa 2 mukaan otettiin vielä 28 iältään 12–17-vuotiasta nuorta potilasta, jotka saivat guselkumabia injektioina ihon alle viikoilla 0 ja 4 ja sen jälkeen 8 viikon välein. Guselkumabiryhmässä alle 70 kg:n painoiset potilaat saivat annoksen 1,3 mg/kg, joka annettiin 45 mg/0,45 ml esitäytetyllä kynällä, ja vähintään 70 kg:n painoiset potilaat saivat annoksen 100 mg, joka annettiin esitäytetyllä ruiskulla.
Yhdistettyjä ensisijaisia päätetapahtumia olivat niiden potilaiden osuus, jotka saavuttivat PASI 75 ‑vasteen, ja niiden potilaiden osuus, jotka saavuttivat IGA-pisteet 0 (”parantunut”) tai 1 (”minimaalinen”) viikolla 16. Toissijaisia päätetapahtumia olivat niiden potilaiden osuus, jotka saavuttivat PASI 90 ‑vasteen, IGA-pisteet 0 (”parantunut”) tai PASI 100 -vasteen viikolla 16, näihin kuitenkaan rajoittumatta.
Tutkimuksen kontrolloidun osan 92 potilaan lähtötilanteen demografiset ominaisuudet olivat yleisesti verrannolliset tutkimusryhmien välillä. Kaikkiaan yli 55 % oli miespuolisia, 85 % oli valkoihoisia, keskimääräinen paino oli noin 57,3 kg, keskimääräinen ikä oli 12,9 vuotta ja 33 % potilaista oli alle 12-vuotiaita.
Sairauden lähtötilanteen ominaisuudet olivat yleisesti verrannolliset hoitoryhmien välillä, ja ihottumaa oli lähtötilanteessa 20 %:ssa (mediaani) kehon pinta-alasta, lähtötilanteen PASI-pisteet olivat noin 17 (mediaani), lähtötilanteessa vaikea-asteista sairautta osoittavat IGA-pisteet todettiin 20 %:lla (lumelääke) ja 24 %:lla (guselkumabi) potilaista ja 3,3 %:lla potilaista oli anamneesissa nivelpsoriaasi.
Ihosairauden kokonaistilanne
Guselkumabihoito paransi taudin aktiivisuutta koskevaa hoitotulosta osoittavia mittareita merkittävästi lumehoitoon verrattuna viikolla 16. Tutkimuksen päätetapahtumien keskeiset tehoa koskevat tulokset esitetään jäljempänä taulukossa 9.
| Taulukko 9. Yhteenveto päätetapahtumista PROTOSTAR-tutkimuksen viikolla 16 | |||
| Lumelääke (N = 25) | Guselkumabi (N = 41) | p‑arvo | |
| IGA-pisteet ”parantunut” (0) tai ”minimaalinen” (1), n (%) | 4 (16,0 %) | 27 (65,9 %) | < 0,001 |
| IGA-pisteet ”parantunut” (0), n (%) | 1 (4,0 %) | 16 (39,0 %) | 0,004 |
| PASI 75 ‑vasteen saaneet, n (%) | 5 (20,0 %) | 31 (75,6 %) | < 0,001 |
| PASI 90 ‑vasteen saaneet, n (%) | 4 (16,0 %) | 23 (56,1 %) | 0,003 |
| PASI 100 ‑vasteen saaneet, n (%) | 0 | 14 (34,1 %) | 0,002 |
| CDLQI-pisteiden muutos lähtötilanteesta, pienimmän neliösumman keskiarvo (95 %:n luottamusväli) | ‑1,88 (‑3,81; 0,05) | ‑7,28 (‑8,87; ‑5.68) | < 0,001 |
| CDLQI = ihotauteihin liittyvä elämänlaatumittarina käytettävä kysymyssarja (Children’s Dermatology Life Quality Index) | |||
PROTOSTAR-tutkimuksen osaan 1 kuuluneen 16 viikon pituisen lumekontrolloidun jakson jälkeen niiden potilaiden, jotka olivat saaneet guselkumabihoitoa ja saavuttaneet PASI 90 ‑vasteen viikolla 16, hoito lopetettiin. PASI 90 ‑vasteen todettiin hävinneen jo 12 viikon kuluttua guselkumabihoidon lopettamisesta, ja PASI 90 ‑vasteen häviämiseen kuluneen ajan mediaani oli noin 24 viikkoa. Niistä guselkumabihoitoa saaneista potilaista, jotka eivät olleet viikolla 16 saavuttaneet PASI 90 ‑vastetta, guselkumabihoitoa vielä 32 lisäviikon ajan jatkaneista potilaista 72,2 % oli saavuttanut PASI 75 ‑vasteen viikolla 52 ja 61,1 % oli saavuttanut PASI 90 ‑vasteen viikolla 52.
Lumehoitoon viikolla 0 satunnaistetut potilaat, jotka eivät olleet viikolla 16 saavuttaneet PASI 90 ‑vastetta, siirtyivät guselkumabihoitoon. Heistä 95,0 % oli saavuttanut PASI 75 ‑vasteen ja 65,0 % oli saavuttanut PASI 90 ‑vasteen viikolla 52.
Farmakokinetiikka
Pediatriset potilaat
Iältään 6–17-vuotiailla pediatrisilla potilailla, joilla oli keskivaikea tai vaikea läiskäpsoriaasi ja jotka saivat ihon alle guselkumabi-injektioita 45 mg/0,45 ml esitäytetyillä kynillä tai 100 mg:n esitäytetyillä ruiskuilla (ks. kohta Annostus ja antotapa), vakaan tilan pienimmät guselkumabipitoisuudet saavutettiin seerumissa viikkoon 20 mennessä, ja pitoisuudet olivat samansuuruisia kuin aikuisilla oli havaittu.
Suositellusta hoito-ohjelmasta saadaan läiskäpsoriaasia sairastavien pediatristen potilaiden seerumiin samankaltainen ennustettu guselkumabialtistus kuin eripainoisilla aikuisilla.
Aikuiset potilaat
Imeytyminen
Terveille tutkittaville ihon alle annetun 100 mg:n kertainjektion jälkeen guselkumabin maksimipitoisuus (Cmax) seerumissa oli keskimäärin (± keskihajonta) 8,09 ± 3,68 mikrog/ml noin 5,5 vuorokauteen mennessä annoksen jälkeen. Guselkumabin absoluuttisen biologisen hyötyosuuden arvioitiin olevan terveille tutkittaville ihon alle annetun 100 mg:n kertainjektion jälkeen noin 49 %.
Läiskäpsoriaasia sairastavilla potilailla guselkumabin vakaan tilan pitoisuus seerumissa saavutettiin viikoilla 0 ja 4 ja sen jälkeen 8 viikon välein ihon alle annettujen 100 mg:n guselkumabiannosten jälkeen viikkoon 20 mennessä. Vakaan tilan pienimmät guselkumabipitoisuudet seerumissa olivat läiskäpsoriaasia sairastavilla potilailla tehdyissä kahdessa vaiheen III tutkimuksessa keskimäärin (± keskihajonta) 1,15 ± 0,73 mikrog/ml ja 1,23 ± 0,84 mikrog/ml.
Jakautuminen
Terminaalisen vaiheen (Vz) jakautumistilavuuden keskiarvo oli terveille tutkittaville laskimoon annetun kerta-annoksen jälkeen kaikissa tutkimuksissa noin 7–10 l.
Biotransformaatio
Guselkumabin tarkkaa metaboliareittiä ei ole selvitetty. Guselkumabi on ihmisen IgG monoklonaalinen vasta-aine, joten se hajoaa oletettavasti pieniksi peptideiksi ja aminohapoiksi kataboliareittien kautta samalla tavoin kuin endogeeninen IgG.
Eliminaatio
Systeemisen puhdistuman (CL) keskiarvo oli terveille tutkittaville laskimoon annetun kerta-annoksen jälkeen kaikissa tutkimuksissa 0,288–0,479 l/vrk. Guselkumabin puoliintumisajan (T½) keskiarvo oli terveillä tutkittavilla noin 17 vuorokautta, läiskäpsoriaasia sairastavilla potilailla noin 15–18 vuorokautta kaikissa tutkimuksissa.
Populaatiofarmakokineettiset analyysit osoittivat, että tulehduskipulääkkeiden, suun kautta otettavien kortikosteroidien ja csDMARD-lääkkeiden, kuten metotreksaatin, samanaikainen käyttö ei vaikuttanut guselkumabin puhdistumaan.
Lineaarisuus/ei-lineaarisuus
Terveille tutkittaville tai läiskäpsoriaasia sairastaville potilaille ihon alle annetun 10−300 mg:n kertainjektion jälkeen guselkumabin systeeminen altistus (Cmax ja AUC) suureni suunnilleen suhteessa annokseen.
Munuaisten tai maksan vajaatoimintaa sairastavat potilaat
Munuaisten tai maksan vajaatoiminnan vaikutuksesta guselkumabin farmakokinetiikkaan ei ole tehty spesifisiä tutkimuksia. Muuttumaton guselkumabi on monoklonaalinen IgG vasta-aine, ja sen eliminaatio munuaisten kautta on oletettavasti vähäistä ja merkitys on vähäinen. Vastaavasti maksan vajaatoiminta ei oletettavasti vaikuta guselkumabin puhdistumaan, koska monoklonaaliset IgG vasta-aineet eliminoituvat pääasiassa kataboloitumalla solunsisäisesti. Aikuisilla tehtyjen populaatiofarmakokineettisten analyysien perusteella kreatiniinipuhdistumalla tai maksan toiminnalla ei ollut merkittävää vaikutusta guselkumabin puhdistumaan.
Paino
Guselkumabin puhdistuma lisääntyy ja jakautumistilavuus suurenee painon lisääntyessä, joten 40 kg:aan saakka annosta säädetään painon perusteella.
Prekliiniset tiedot turvallisuudesta
Farmakologista turvallisuutta, toistuvan altistuksen aiheuttamaa toksisuutta, lisääntymistoksisuutta ja pre- ja postnataalista kehitystä koskevien konventionaalisten tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille.
Cynomolgus-apinoilla tehdyissä toistuvan altistuksen aiheuttamaa toksisuutta koskeneissa tutkimuksissa laskimoon ja ihon alle annettu guselkumabi oli hyvin siedetty. Viikoittain apinoille ihon alle annetuista 50 mg/kg annoksista aiheutuva altistus (AUC) oli vähintään 23-kertainen verrattuna suurimpaan kliiniseen altistukseen laskimoon annetun 200 mg:n annoksen jälkeen. Cynomolgus-apinoilla tehdyissä toistuvan altistuksen aiheuttamaa toksisuutta tai kohdennettua kardiovaskulaarista turvallisuutta koskeneissa farmakologisissa tutkimuksissa ei havaittu haitallista immunotoksisuutta tai kardiovaskulaarista turvallisuutta koskevia farmakologisia vaikutuksia.
Histopatologisissa tutkimuksissa ei havaittu preneoplastisia muutoksia eläimillä, joita hoidettiin enintään 24 viikon ajan, eikä 12 viikon toipumisjakson jälkeen, jolloin vaikuttavaa ainetta oli seerumissa havaittavissa.
Guselkumabilla ei tehty mutageenisuus- eikä karsinogeenisuustutkimuksia.
Guselkumabia ei havaittu cynomolgus-apinoiden maidossa, kun mittaus tehtiin 28 päivää synnytyksen jälkeen.
Farmaseuttiset tiedot
Apuaineet
Histidiini
Histidiinimonohydrokloridimonohydraatti
Polysorbaatti 80 (E433)
Sakkaroosi
Injektionesteisiin käytettävä vesi
Yhteensopimattomuudet
Koska yhteensopivuustutkimuksia ei ole tehty, tätä lääkevalmistetta ei saa sekoittaa muiden lääkevalmisteiden kanssa.
Kestoaika
2 vuotta.
Säilytys
Säilytä jääkaapissa (2 °C – 8 °C). Ei saa jäätyä.
Pidä esitäytetty kynä ulkopakkauksessa. Herkkä valolle.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
TREMFYA injektioneste, liuos, esitäytetty kynä
45 mg/0,45 ml (L:ei) 1 kpl (0,45 ml (100 mg/ml), VarioJect, automaattinen neulanpistosuoja) (2002,04 €)
PF-selosteen tieto
0,45 ml liuosta lasisessa esitäytetyssä ruiskussa, joka on kertakäyttöisessä esitäytetyssä kynässä. Esitäytetyssä kynässä on automaattinen neulanpistosuoja ja säädettävä annosvalitsinmäntä.
Tremfya-injektionestettä on saatavana yhden esitäytetyn kynän pakkauksina.
Valmisteen kuvaus:
Liuos on kirkasta ja väritöntä tai vaaleankeltaista ja se saattaa sisältää joitakin pieniä valkoisia tai kirkkaita hiukkasia. Sen tavoite-pH on 5,8 ja likimääräinen osmolaarisuus on 367,5 mOsm/l.
Käyttö- ja käsittelyohjeet
Kun esitäytetty kynä on otettu jääkaapista, anna esitäytetyn kynän olla ulkopakkauksessa ja anna sen lämmetä huoneenlämpöiseksi. Odota 30 minuuttia ennen kuin annat Tremfya‑injektion. Esitäytettyä kynää ei saa ravistaa.
Esitäytetty kynä suositellaan tarkistamaan silmämääräisesti ennen käyttöä. Liuoksen pitää olla kirkasta, väritöntä tai vaaleankeltaista, ja se saattaa sisältää joitakin pieniä valkoisia tai kirkkaita hiukkasia. Jos liuos on sameaa tai värjäytynyttä tai siinä on isoja hiukkasia, Tremfya‑liuosta ei saa käyttää.
Jokainen pakkaus sisältää Käyttöohjeet, joissa on tarkat ohjeet injektion valmisteluun ja esitäytetyn kynän käyttöön.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
TREMFYA injektioneste, liuos, esitäytetty kynä
45 mg/0,45 ml 1 kpl
- Ei korvausta.
ATC-koodi
L04AC16
Valmisteyhteenvedon muuttamispäivämäärä
18.12.2025
Yhteystiedot
PL 15
02621 Espoo
020 753 1300
innovativemedicine.jnj.com/finland
jacfi@its.jnj.com

 JANSSEN-CILAG OY
JANSSEN-CILAG OY