TIOTROPIUM STADA inhalaatiojauhe, kapseli, kova 18 mikrog
Vaikuttavat aineet ja niiden määrät
Yksi kapseli sisältää 22,5 mikrogrammaa tiotropiumbromidimonohydraattia vastaten 18 mikrogrammaa tiotropiumia.
Vapautunut annos (annos, joka vapautuu Vertical-Haler ‑laitteen suukappaleesta) on 10 mikrogrammaa tiotropiumia.
Apuaine, jonka vaikutus tunnetaan
Yksi kapseli sisältää 5,204 mg laktoosia (monohydraattina).
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Inhalaatiojauhe, kova kapseli.
Kliiniset tiedot
Käyttöaiheet
Tiotropium Stada on tarkoitettu keuhkoputkia laajentavaksi ylläpitohoitolääkkeeksi helpottamaan keuhkoahtaumatautipotilaiden (COPD) oireita.
Annostus ja antotapa
Annostus
Tiotropiumbromidin suositusannostus on seuraava: yhden kapselin sisältö inhaloidaan Vertical-Haler ‑laitteella kerran päivässä aina samaan aikaan vuorokaudesta. Samasta kapselista pitää hengittää sisään 2 kertaa.
Suositeltua annosta ei saa ylittää.
Tiotropium Stada inhaloidaan ainoastaan Vertical-Haler -laitteella.
Erityisryhmät
Iäkkäät
Iäkkäät voivat käyttää tiotropiumia suositusannostusta noudattaen.
Munuaisten vajaatoiminta
Jos potilaan munuaistoiminta on heikentynyt, hän voi käyttää tiotropiumia suositusannostusta noudattaen. Potilaat, joiden munuaistoiminta on kohtalaisesti tai vaikeasti heikentynyt (kreatiniinipuhdistuma ≤ 50 ml/min), ks. kohta Varoitukset ja käyttöön liittyvät varotoimet ja kohta Farmakokinetiikka.
Maksan vajaatoiminta
Jos potilaan maksan toiminta on heikentynyt, hän voi käyttää tiotropiumia suositusannostusta noudattaen (ks. kohta Farmakokinetiikka).
Pediatriset potilaat
Keuhkoahtaumatauti
Valmisteella ei ole asianmukaista käyttöä pediatrisille potilaille (alle 18-vuotiaille) kohdan Käyttöaiheet käyttöaiheessa.
Kystinen fibroosi
Tiotropium Stada ‑valmisteen turvallisuutta ja tehoa ei ole osoitettu lapsilla ja nuorilla. Tietoja ei ole saatavilla.
Antotapa
Vain inhalaatioon.
Kapseleita ei saa niellä.
Kapseli tulee poistaa läpipainopakkauksesta vasta juuri ennen inhalaattorin käyttöä!
Jotta varmistetaan valmisteen asianmukainen käyttö, lääkärin tai muun terveydenhuoltohenkilökunnan pitää opettaa potilaalle, miten inhalaattoria käytetään.
Käsittely- ja käyttöohjeet
Potilaita tulee neuvoa noudattamaan huolellisesti lääkärin ohjeita Tiotropium Stada ‑valmisteen käytöstä. Vertical-Haler ‑laite on suunniteltu erityisesti Tiotropium Stada ‑valmistetta varten. Sitä ei saa käyttää minkään muun lääkkeen ottamiseen. Samaa Vertical-Haleria voi käyttää enintään 90 päivän ajan lääkkeen ottamiseen.
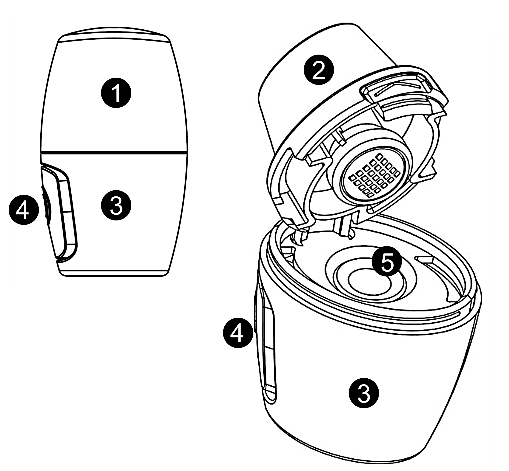 | Vertical-Haler ‑laitteen osat 1 Suojakansi 2 Suukappale 3 Alaosa 4 Kapselin rei’ittämiseen tarkoitettu nappi 5 Kapselikammio |
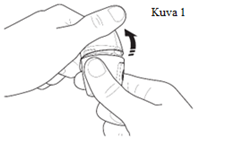 | 1. Suojakannen poistaminen Pidä kiinni Vertical-Halerista ja poista suojakansi vetämällä sitä ylöspäin siten, että suukappale tulee näkyviin (kuva 1). |
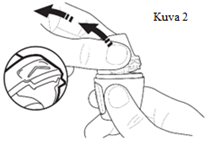 | 2. Avaaminen Jotta Vertical-Halerin saa avattua, pidä alaosan sivuista kiinni. Paina sormenpäällä kohtaa, jossa on merkintä ”˄” (suurennetussa kuvassa). Avaa inhalaattori vetämällä suukappaletta poispäin alaosasta kuvan esittämällä tavalla (kuva 2). |
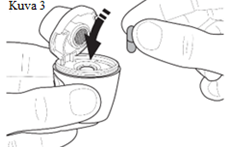 | 3. Kapselin asettaminen Pidä auki oleva Vertical-Haler pystyasennossa. Lisää kapseli kapselikammioon (kuva 3). Huom: Poista kapseli läpipainopakkauksesta vasta juuri ennen inhalaattorin käyttöä! |
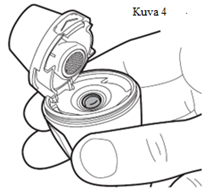 | Varmista, että kapseli on asetettu laitteeseen oikein (kuva 4). |
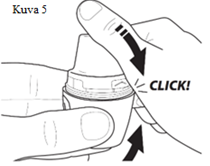 | 4. Kapselilokeron sulkeminen Sulje suukappale painamalla sitä tiukasti alaosaa vasten, kunnes kuulet napsahduksen (kuva 5). |
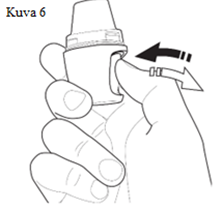 | 5. Kapselin lävistäminen Pidä Vertical-Haleria suukappale ylöspäin. Paina nappia tiukasti kerran, kunnes se on täysin piilossa (kuva 6). Vapauta nappi. Kapseliin tulee näin reiät, joista lääke vapautuu sisäänhengityksen yhteydessä. Huomio:Jos joudut toistamaan vaiheen 5, avaa kapselikammio (kuva 2) varmistaaksesi, että kapseli on asetettu oikein (kuva 4). |
 | 6. Käyttöön valmistautuminen Pidä Vertical-Haler poissa suusi lähettyviltä ja tyhjennä keuhkot hengittämällä ulos. (kuva 7) Älä hengitä ulos Vertical-Halerin kautta. |
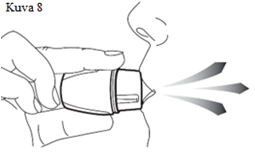 | 7. Inhaloiminen Pidätä seuraavaa hengitystä pään ollessa pystyasennossa, sulje huulesi tiiviisti suukappaleen ympärille. Hengitä sisään hitaasti ja niin syvään kuin mahdollista (kuva 8). Kuulet värisevän äänen, joka johtuu kapselin pyörimisestä kapselikammion sisällä vapauttaen samalla lääkettä. Hengitä sisään, kunnes keuhkosi ovat täynnä. Pidätä sitten hengitystäsi niin kauan kuin se tuntuu miellyttävältä ja ota samalla Vertical‑Haler pois suustasi. Palaa normaaliin hengitystahtiin. Toista vaiheet 6 ja 7 vielä kerran. Sinun pitää hengittää sisään 2 kertaa samasta kapselista. |
Huomio: Kun pidät kiinni inhalaattorista sisäänhengityksen aikana, varmista, että suukappaleen sivuilla olevat ilmanottoaukot eivät tukkeudu. Tämä voi estää ilman virtauksen inhalaattorissa ja vähentää kapselin liikettä ja lääkkeen vapautumista. Älä paina suukappaletta alas sisäänhengityksen aikana. Tämä voi estää kapselin liikkeen. | |
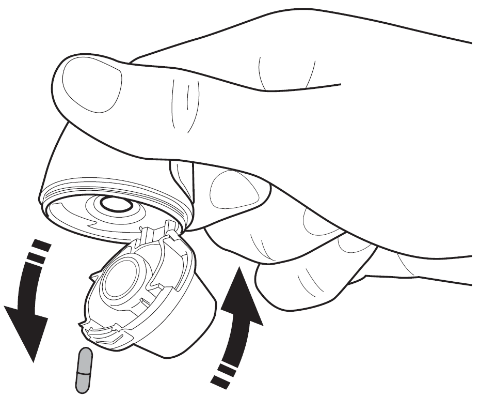 | Vertical-Haler ‑laitteesi puhdistaminen Avaa suukappale käytön jälkeen. Pidä inhalaattoria ylösalaisin, jotta kapseli irtoaa kapselikammiosta. Puhdista suukappale ja kapselikammio puhtaalla, kuivalla liinalla. Vaihtoehtoisesti voidaan käyttää pehmeää, puhdasta harjaa jauhejäämien poistamiseksi kapselikammion sisältä. Sulje suukappale ja aseta kansi paikoilleen. Näin menetellen kuivajauheinhalaattori pysyy puhtaana ja kuivana. Tarvittaessa suukappaleen ulkopinta on puhdistettava kostealla liinalla. |
Kapselit sisältävät vain pienen määrän jauhetta, joten kapseli on täytetty vain osittain.
Vasta-aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille tai atropiinille tai sen johdoksille, kuten ipratropiumille tai oksitropiumille.
Varoitukset ja käyttöön liittyvät varotoimet
Tiotropiumbromidi on kerran päivässä otettava bronkodilaattori ylläpitohoitoon. Sitä ei pidä käyttää akuuttien bronkospasmikohtausten hoitoon ensiapulääkkeenä.
Välittömiä yliherkkyysreaktioita saattaa esiintyä tiotropiumbromidi-inhalaatiojauheen oton jälkeen.
Antikolinergisen aktiivisuutensa vuoksi tiotropiumbromidin käytössä pitää noudattaa varovaisuutta, jos potilaalla on ahdaskulmaglaukooma, eturauhasen liikakasvu tai virtsarakon kaulaosan ahtauma (ks. kohta Haittavaikutukset).
Inhaloitavat lääkkeet saattavat aiheuttaa inhalaatiosta johtuvan bronkospasmin.
Tiotropiumia pitää käyttää varoen potilaille, joilla on hiljattain ollut sydäninfarkti (< 6 kuukautta), mikä tahansa epävakaa tai henkeä uhkaava sydämen rytmihäiriö tai rytmihäiriö, joka on vaatinut toimenpiteitä tai lääkityksen muutosta viimeisen vuoden aikana, tai sydämen vajaatoiminnasta (NYHA-luokka III tai IV) aiheutunut sairaalahoito viimeisen vuoden aikana. Nämä potilaat jätettiin kliinisten tutkimusten ulkopuolelle, ja antikolinerginen vaikutusmekanismi voi vaikuttaa näihin sairauksiin.
Tiotropiumbromidin pitoisuus plasmassa kasvaa, jos potilaan munuaistoiminta on kohtalaisesti tai vaikeasti heikentynyt (kreatiniinipuhdistuma ≤ 50 ml/min). Tiotropiumbromidia saa käyttää vain, jos odotettavissa oleva hyöty on suurempi kuin mahdollisesti aiheutuva haitta. Vaikeaa munuaisten vajaatoimintaa sairastavien pitkäaikaishoidosta ei ole kokemusta (ks. kohta Farmakokinetiikka).
Potilaita tulee kehottaa välttämään lääkejauheen joutumista silmiin. Heille on kerrottava, että se voi laukaista ahdaskulmaglaukooman tai pahentaa sitä tai aiheuttaa kipua tai epämiellyttäviä tuntemuksia silmässä, näön tilapäistä hämärtymistä, valokehien tai värikuvien ilmaantumista näkökenttään sekä silmien punoitusta, johon on syynä sidekalvon verentungos ja sarveiskalvon turvotus. Jos potilaalle kehittyy mikä tahansa näiden silmäoireiden yhdistelmä, potilaan pitää lopettaa tiotropiumbromidin käyttö ja ottaa välittömästi yhteyttä silmälääkäriin.
Suun kuivuminen, jota on havaittu antikolinergisen hoidon yhteydessä, saattaa pitkään jatkuessaan aiheuttaa kariesta.
Tiotropiumbromidia ei saa käyttää useammin kuin kerran päivässä (ks. kohta Yliannostus).
Apuaineet
Tiotropium Stada sisältää laktoosia. Potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, täydellinen laktaasinpuutos tai glukoosi-galaktoosi-imeytymishäiriö, ei pidä käyttää tätä lääkettä.
Apuaine laktoosi saattaa sisältää pieniä määriä maitoproteiineja, jotka saattavat aiheuttaa allergisia reaktioita.
Yhteisvaikutukset
Vaikka yhteisvaikutustutkimuksia ei ole tehty, tiotropiumbromidiinhalaatiojauhetta on käytetty samanaikaisesti muiden lääkkeiden kanssa ilman, että käyttöön on liittynyt kliinistä näyttöä yhteisvaikutuksista. Tällaisia lääkkeitä ovat sympatomimeettiset bronkodilaattorit, metyyliksantiinit, oraaliset ja inhaloitavat steroidit, joita käytetään yleisesti keuhkoahtaumataudin hoidossa.
Pitkävaikutteisen beeta-agonistin tai inhaloitavan kortikosteroidin käytön ei todettu vaikuttavan tiotropiumaltistukseen.
Tiotropiumbromidin samanaikaista käyttöä muiden antikolinergejä sisältävien lääkkeiden kanssa ei ole tutkittu, eikä sitä siksi suositella.
Raskaus ja imetys
Raskaus
Tiotropiumin käytöstä raskaana oleville naisille on vain hyvin vähän tietoa. Eläimillä tehdyissä tutkimuksissa ei ole havaittu suoria tai epäsuoria lisääntymistoksisia vaikutuksia kliinisesti merkityksellisillä annoksilla (ks. kohta Prekliiniset tiedot turvallisuudesta). Varmuuden vuoksi Tiotropium Stada ‑valmisteen käyttöä on suositeltavaa välttää raskauden aikana.
Imetys
Ei tiedetä, erittyykö tiotropiumbromidi ihmisillä äidinmaitoon. Jyrsijöillä tehdyt tutkimukset ovat osoittaneet, että tiotropiumbromidia erittyy maitoon vain pieniä määriä. Tästä huolimatta tiotropiumin käyttöä ei suositella imetyksen aikana. Tiotropiumbromidi on pitkävaikutteinen aine. Päätöksessä jatkaako/lopettaako imetys tai jatkaako/lopettaako tiotropiumin käyttö pitää ottaa huomioon imetyksen hyöty lapselle ja tiotropiumhoidon hyöty imettävälle äidille.
Hedelmällisyys
Kliinisiä tietoja tiotropiumin vaikutuksesta hedelmällisyyteen ei ole saatavilla. Tiotropiumilla tehty non-kliininen tutkimus osoitti, ettei sillä ole haitallista vaikutusta hedelmällisyyteen (ks kohta Prekliiniset tiedot turvallisuudesta).
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Tutkimuksia valmisteen vaikutuksesta ajokykyyn tai koneidenkäyttökykyyn ei ole tehty. Heitehuimauksen, näön hämärtymisen tai päänsäryn esiintyminen voi vaikuttaa ajokykyyn ja koneiden käyttökykyyn.
Haittavaikutukset
Turvallisuusprofiilin yhteenveto
Useita luetelluista haittavaikutuksista voidaan pitää Tiotropium Stada ‑valmisteen antikolinergisten ominaisuuksien aiheuttamina.
Haittavaikutusten taulukkomuotoinen yhteenveto
Alla luetelluille haittavaikutuksille annetut yleisyysluokitukset perustuvat vakioimattomiin haittatapahtumien esiintymistiheyksiin (ts. tiotropiumin aiheuttamat tapahtumat), jotka havaittiin tiotropiumryhmässä (9 647 potilasta) 28 yhdistetyssä lumekontrolloidussa kliinisessä tutkimuksessa, joissa hoitoaika vaihteli neljästä viikosta neljään vuoteen.
Haittavaikutukset on lueteltu elinjärjestelmän ja esiintymistiheyden mukaan. Yleisyydet on määritelty käyttäen seuraavaa tapaa: hyvin yleinen (≥ 1/10), yleinen (≥ 1/100, < 1/10), melko harvinainen (≥ 1/1000, < 1/100), harvinainen (≥ 1/10 000, < 1/1000), hyvin harvinainen (< 1/10 000), tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin).
Elinjärjestelmä / MedDRA:n käyttämä termi | Esiintymistiheys |
Immuunijärjestelmä | |
Yliherkkyys (mukaan luettuina välittömät reaktiot) | Harvinainen |
Anafylaktinen reaktio | Tuntematon |
Aineenvaihdunta ja ravitsemus | |
Kuivuminen | Tuntematon |
Hermosto | |
Heitehuimaus | Melko harvinainen |
Päänsärky | Melko harvinainen |
Makuhäiriö | Melko harvinainen |
Unettomuus | Harvinainen |
Silmät | |
Näön hämärtyminen | Melko harvinainen |
Glaukooma | Harvinainen |
Kohonnut silmän sisäinen paine | Harvinainen |
Sydän | |
Eteisvärinä | Melko harvinainen |
Supraventrikulaarinen takykardia | Harvinainen |
Takykardia | Harvinainen |
Palpitaatio | Harvinainen |
Hengityselimet, rintakehä ja välikarsina | |
Nielutulehdus | Melko harvinainen |
Dysfonia | Melko harvinainen |
Yskä | Melko harvinainen |
Bronkospasmi | Harvinainen |
Nenäverenvuoto | Harvinainen |
Kurkunpääntulehdus | Harvinainen |
Sinuiitti | Harvinainen |
Ruoansulatuselimistö | |
Suun kuivuminen | Yleinen |
Gastroesofageaalinen refluksi | Melko harvinainen |
Ummetus | Melko harvinainen |
Suunielun sammas | Melko harvinainen |
Suolitukos (mukaan luettuna suolen lamaantuminen) | Harvinainen |
Ientulehdus | Harvinainen |
Kielitulehdus | Harvinainen |
Nielemishäiriö | Harvinainen |
Suutulehdus | Harvinainen |
Pahoinvointi | Harvinainen |
Karies | Tuntematon |
Iho ja ihonalainen kudos | |
Ihottuma | Melko harvinainen |
Urtikaria | Harvinainen |
Kutina | Harvinainen |
Angioedeema | Harvinainen |
Ihotulehdus, ihohaava | Tuntematon |
Kuiva iho | Tuntematon |
Luusto, lihakset ja sidekudos | |
Nivelturvotus | Tuntematon |
Munuaiset ja virtsatiet | |
Vaikeutunut virtsaaminen | Melko harvinainen |
Virtsaumpi | Melko harvinainen |
Virtsatieinfektio | Harvinainen |
Kuvaus valikoiduista haittavaikutuksista
Kontrolloiduissa kliinisissä tutkimuksissa usein havaittuja haittavaikutuksia olivat antikolinergiset haittavaikutukset, kuten kuiva suu, jota ilmeni noin 4 %:lla potilaista.
28 kliinisessä tutkimuksessa suun kuivuminen johti 18 potilaan hoidon keskeyttämiseen 9 647 potilaan tiotropiumryhmässä (0,2 %).
Vakavia haittavaikutuksia, jotka liittyvät antikolinergiseen vaikutukseen, ovat glaukooma, ummetus, suolitukos (suolen lamaantuminen mukaan lukien) sekä virtsaumpi.
Muut erityisryhmät
Iän myötä antikolinergisten vaikutusten esiintyminen saattaa kasvaa.
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Suuret tiotropiumbromidiannokset saattavat aiheuttaa antikolinergisia merkkejä ja oireita.
Systeemisiä antikolinergisia haittavaikutuksia ei kuitenkaan esiintynyt, kun terveille vapaaehtoisille annettiin enimmillään 340 mikrog:n inhalaatiokerta-annos tiotropiumbromidia. Oleellisia haittavaikutuksia ei suun kuivumisen lisäksi myöskään havaittu, kun terveille vapaaehtoisille annettiin 7 päivän ajan enimmillään 170 mikrog tiotropiumbromidia. Keuhkoahtaumatautia sairastaville potilaille tehdyssä moniannostutkimuksessa, jossa enimmäisvuorokausiannos oli 43 mikrog tiotropiumbromidia neljän viikon ajan, ei havaittu merkittäviä haittavaikutuksia.
Koska tiotropiumbromidin oraalinen hyötyosuus on pieni, on epätodennäköistä, että kapseleiden tahaton nauttiminen suun kautta aiheuttaisi myrkytyksen.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Muut ahtauttavien hengitystiesairauksien lääkkeet, inhalaatiot, antikolinergit: ATC-koodi: R03B B04
Vaikutusmekanismi
Tiotropiumbromidi on pitkävaikutteinen spesifinen muskariinireseptoriantagonisti, jollaisia kliinisessä lääketieteessä nimitetään usein antikolinergeiksi. Tiotropiumbromidi estää parasympaattisesta hermonpäätteestä vapautuvan asetyylikoliinin kolinergisia (keuhkoputkia supistavia) vaikutuksia sitoutumalla hengitysteiden sileän lihaksen muskariinireseptoreihin. Sillä on samanlainen affiniteetti muskariinireseptorialatyyppeihin M1 - M5. Hengitysteissä tiotropiumbromidi antagonisoi kilpailevasti ja palautuvasti M3-reseptoreja aiheuttaen relaksaation. Vaikutus oli annoksesta riippuva ja kesti yli 24 tuntia. Vaikutuksen pitkä kesto johtuu todennäköisesti hyvin hitaasta dissosioitumisesta M3- reseptoreista, sillä sen dissosiaation puoliintumisaika on merkitsevästi pidempi kuin ipratropiumilla. Koska tiotropiumbromidi on N-kvaternaarinen antikolinergi, se on inhaloitaessa paikallisesti (bronko)selektiivinen antaen hyvän terapeuttisen vasteen ennen kuin systeemisiä antikolinergisiä vaikutuksia ilmenee.
Farmakodynaamiset vaikutukset
Bronkodilataatio on ensisijaisesti paikallinen vaikutus (hengitysteihin), ei systeeminen. Dissosiaatio M2-reseptoreista tapahtuu nopeammin kuin M3-reseptoreista, mikä ilmeni funktionaalisissa in vitro -tutkimuksissa kineettisen reseptorialatyypin selektiivisyytenä siten, että M3:een kohdistuva selektiivisyys oli M2:een kohdistuvaa selektiivisyyttä suurempi. Lääkkeen vaikutuksen suuri voimakkuus ja hidas dissosiaatio reseptoreista ilmeni vastaavasti kliinisesti merkitsevänä ja pitkäkestoisena bronkodilataationa keuhkoahtaumatautia sairastavilla potilailla.
Sydämen elektrofysiologia
Elektrofysiologia: Tiotropium 18 mikrog ja 54 mikrog annoksilla (ts. kolminkertainen terapeuttinen annos) yli 12 päivän ajan ei pidentänyt merkitsevästi QT-aikaa EKG:ssä erityisessä QT-tutkimuksessa, johon osallistui 53 tervettä vapaaehtoista.
Kliininen teho ja turvallisuus
Kliininen kehitysohjelma koostui neljästä vuoden ja kahdesta 6 kuukautta kestäneestä, satunnaistetusta kaksoissokkotutkimuksesta. Tutkimuksiin osallistui 2 663 potilasta (joista 1 308 sai tiotropiumia). Yhden vuoden tutkimuksista kaksi oli lumekontrolloituja ja kahdessa käytettiin vaikuttavaa vertailuvalmistetta (ipratropiumia). Kaksi 6 kuukauden tutkimusta olivat molemmat salmeteroli- ja lumekontrolloituja. Tutkimuksissa mitattiin keuhkojen toimintaa ja terveysvaikutuksia hengenahdistuksen, pahenemisvaiheiden ja terveyteen liittyvän elämänlaadun osalta.
Keuhkojen toiminta
Tiotropium paransi kerran päivässä annettuna merkitsevästi keuhkojen toimintaa (uloshengityksen sekuntikapasiteetti, FEV1, ja nopea vitaalikapasiteetti, FVC) 30 minuutin kuluessa ensimmäisen annoksen ottamisesta. Vaikutus kesti 24 tuntia. Farmakodynaaminen vakaa tila saavutettiin viikon kuluessa siten, että suurin osa bronkodilaatiosta havaittiin kolmanteen päivään mennessä. Potilaan päivittäisten mittausten perusteella tiotropium paransi aamulla ja illalla mitattuja PEF-arvoja (uloshengityksen huippuvirtausarvoja) merkitsevästi. Tiotropiumin keuhkoputkia laajentava vaikutus säilyi koko vuoden mittaisen hoitojakson ajan, eikä viitteitä toleranssin kehittymisestä todettu.
105 keuhkoahtaumapotilaalla tehty satunnaistettu, lumekontrolloitu kliininen tutkimus osoitti, että bronkodilaatio säilyi koko 24 tunnin mittaisen antovälin ajan lumelääkkeeseen verrattuna riippumatta siitä, otettiinko lääke aamulla vai illalla.
Kliiniset tutkimukset (enintään 12 kuukauden mittaiset tutkimukset)
Hengenahdistus, suorituskyky
Tiotropiumin havaittiin lievittävän potilaiden hengenahdistusta merkitsevästi (Transition Dyspnoea -indeksin perusteella arvioituna). Nämä vaikutukset säilyivät koko hoitojakson ajan.
Hengenahdistuksen lievittymisen vaikutusta suorituskykyyn tutkittiin kahdessa satunnaistetussa, kaksoissokkoutetussa, lumelääkekontrolloidussa tutkimuksessa, joissa oli 433 keskivaikeaa tai vaikeaa keuhkoahtaumatautia sairastavaa potilasta. Näissä tutkimuksissa kuuden viikon hoito tiotropiumilla paransi merkitsevästi oireiden rajoittamaa rasituksen kestoa: aika polkupyöräergometriassa kuormituksessa, joka oli 75 % maksimaalisesta suorituskyvystä, parani 19,7 % (tutkimus A) ja 28,3 % (tutkimus B) verrattuna lumelääkkeeseen.
Terveyteen liittyvä elämänlaatu
Tiotropium paransi terveyteen liittyvää elämänlaatua, kun sitä mitattiin St. George’s Respiratory kyselylomakkeen (SGRQ) kokonaistuloksella yhdeksän kuukautta kestäneessä satunnaistetussa, kaksoissokkoutetussa, lumekontrolloidussa kliinisessä tutkimuksessa, johon osallistui 492 potilasta. Tiotropiumilla hoidettujen potilaiden osuus, joka saavutti merkitsevää parannusta SGRQ:n kokonaistuloksessa (ts. > 4 yksikköä) oli 10,9 % korkeampi lumelääkkeeseen verrattuna (59,1 % tiotropiumryhmissä vs. 48,2 % lumeryhmässä (p = 0,029). Keskimääräinen ero ryhmien välillä oli 4,19 yksikköä (p = 0,001; luottamusväli 1,69–6,68). Parannukset SGRQ-pisteiden osa-alueille olivat 8,19 yksikköä ”oireille ”, 3,91 yksikköä ”aktiivisuudelle” ja 3,61 yksikköä ”vaikutukselle päivittäiseen elämään”. Parannukset kaikissa näissä erillisissä osa-alueissa olivat tilastollisesti merkitseviä.
COPD:n pahenemisvaiheet
Satunnaistetussa, kaksoissokkoutetussa, lumelääkekontrolloidussa tutkimuksessa, joka tehtiin 1 829:lle keskivaikeasta hyvin vaikeaan keuhkoahtaumatautia (COPD) sairastavalle potilaalle, tiotropium vähensi tilastollisesti merkitsevästi niiden potilaiden osuutta, joilla oli COPD:n pahenemisvaihe (32,2 %:sta 27,8 %:iin) samoin kuin pahenemisvaiheiden määrää (19 %:lla, 1,05:stä 0,85:een potilasaltistusvuotta kohti). Tiotropiumilla hoidetuista potilaista 7,0 % ja lumelääkityistä 9,5 % (p = 0,056) joutui sairaalahoitoon COPD:n pahenemisen takia. Keuhkoahtaumataudista johtuvien sairaalajaksojen määrä väheni 30 %:lla (0,25:stä 0,18:aan tapausta potilasaltistusvuotta kohti).
Yhden vuoden satunnaistettu kaksoissokko-, kaksoislume-, rinnakkaisryhmätutkimus vertasi tiotropium 18 mikrog (anto kerran päivässä) hoitoa salmeteroli 50 mikrog HFA-inhalaatiosumutteen (anto kaksi kertaa päivässä) hoidon tehoon keskivaikeiden ja vaikeiden pahenemisvaiheiden esiintyvyyteen 7 376 potilaalle, joilla oli keuhkoahtaumatauti (COPD) ja pahenemisvaiheita edeltävänä vuonna.
Taulukko 1: Yhteenveto taudin pahenemisvaiheen päätetapahtumista
| Päätetapahtuma | Tiotropium 18 mikrog (inhalaatiojauhe) N=3 707 | Salmeteroli 50 mikrog (inhalaatiosumute) N=3 669 | Suhde (95 % CI) | p-arvo |
| Aika [päivinä] ensimmäisen pahenemisvaiheen ilmaantumiseen1 | 187 | 145 | 0,83 (0,77–0,90) | < 0,001 |
| Aika ensimmäisen vaikean (sairaalahoitoa vaativan) pahenemisvaiheen ilmaantumiseen2 | - | - | 0,72 (0,61–0,85) | < 0,001 |
| Potilaat, joilla oli ≥ 1 pahenemisvaihetta, n (%)3 | 1 277 (34,4) | 1 414 (38,5) | 0,90 (0,85–0,95) | < 0,001 |
| Potilaat, joilla oli ≥ 1 vaikeaa (sairaalahoitoa vaativaa) pahenemisvaihetta, n (%)3 | 262 (7,1) | 336 (9,2) | 0,77 (0,66–0,89) | < 0,001 |
1 Aika [päivinä] viittaa ensimmäiseen kvartiiliin potilaita. Tapahtumaan kulunut aika mitattiin käyttäen Coxin verrannollisten riskitiheyksien mallia, jossa keskus ja hoito olivat yhdistetysti kovarianttina; suhdeluku viittaa riskisuhteeseen.
2 Tapahtumaan kulunut aika mitattiin käyttäen Coxin verrannollisten riskitiheyksien mallia, jossa keskus ja hoito olivat yhdistetysti kovarianttina; suhdeluku viittaa riskisuhteeseen. Ensimmäisen kvartiilin osalta aikaa (päivinä) ei voida laskea, koska vaikean pahenemisvaiheen saavien potilaiden osuus on liian pieni.
3 Potilaiden lukumäärä, joilla oli tapahtuma, analysoitiin käyttämällä Cochran-Mantel-Haenszel-testiä, jossa luokiteltuna tietona oli yhdistetty tutkimuskeskustieto; suhdeluku viittaa riskisuhteeseen.
Salmeteroliin verrattuna aika ensimmäisen pahenemisvaiheen ilmaantumiseen pidentyi tiotropiumhoidon aikana (187 päivää vs. 145 päivää), riski pieneni 17 %:lla (riskisuhde 0,83; 95 % luottamusväli [CI], 0,77–0,90; p<0,001). Tiotropium myös pidensi aikaa ensimmäisen vaikean (sairaalahoitoa vaativan) pahenemisvaiheen ilmaantumiseen (riskisuhde, 0,72; 95 % CI, 0,61–0,85; p < 0,001).
Pitkäkestoiset kliiniset tutkimukset (yli vuoden mittaiset, enintään neljä vuotta kestäneet tukimukset)
Neljän vuoden satunnaistetussa, kaksoissokkoutetussa, lumelääkekontrolloidussa kliinisessä tutkimuksessa, johon osallistui 5 993 satunnaistettua potilasta (3 006 potilasta sai lumelääkettä ja 2 987 potilasta sai tiotropiumia), tiotropiumhoidosta johtuva FEV1-arvon parannus lumelääkkeeseen verrattuna pysyi muuttumattomana koko 4 vuoden ajan. Tässä tutkimuksessa tiotropiumryhmässä suurempi osuus potilaista käytti ≥ 45 kuukauden hoitonsa loppuun asti lumelääkeryhmään verrattuna (63,8 % vs. 55,4 %, p < 0,001). Vuosittainen FEV1-arvon heikkeneminen verrattuna lumelääkkeeseen oli samanlainen tiotropiumilla ja lumelääkkeellä. Hoidon aikana kuolemanriski väheni 16 %:lla. Kuoleman ilmaantuvuus oli 4,79 / 100 potilasvuotta lumelääkeryhmässä vs. 4,10 / 100 potilasvuotta tiotropiumryhmässä (riskisuhde (tiotropium/lumelääke) = 0,84, 95 % CI = 0,73; 0,97). Tiotropiumhoito vähensi hengitysvajeen riskiä (haittavaikutusraporttien kautta kuvattuna) 19 %:lla (2,09 vs. 1,68 tapausta / 100 potilasvuotta, suhteellinen riski (tiotropium/lumelääke) 0,81, 95 % CI = 0,65; 0,999).
Tiotropium-aktiivikontrolloitu tutkimus
Inhalaatiojauheena ja inhalaationesteenä annostellun tiotropiumbromidin tehoa ja turvallisuutta vertailtiin pitkäkestoisessa, laajassa, satunnaistetussa, kaksoissokkoutetussa, aktiivikontrolloidussa tutkimuksessa, jossa havainnointiaika oli enintään kolme vuotta (5 694 potilasta sai tiotropiuminhalaatiojauhetta ja 5 711 potilasta sai tiotropiuminhalaationestettä). Ensisijaiset päätetapahtumat olivat aika ensimmäiseen keuhkoahtaumataudin pahenemisvaiheeseen, aika mistä tahansa syystä johtuvaan kuolemaan ja alatutkimuksessa (906 potilasta) FEV1-jäännösarvo (ennen annosta).
Aika ensimmäiseen keuhkoahtaumataudin pahenemisvaiheeseen oli tutkimuksen aikana numeerisesti samanlainen tiotropiuminhalaatiojauheella ja tiotropiuminhalaationesteellä (riskisuhde (tiotropiuminhalaatiojauhe/tiotropiuminhalaationeste) 1,02; 95 % CI: 0,97–1,08). Ensimmäisen pahenemisvaiheen ilmaantumiseen kuluneiden päivien mediaani oli tiotropiuminhalaatiojauheella 719 päivää ja tiotropiuminhalaationesteellä 756 päivää.
Tiotropiuminhalaatiojauheen keuhkoputkia laajentava vaikutus säilyi 120 viikon ajan ja oli samanlainen kuin tiotropiuminhalaationesteellä. Keskimääräinen ero FEV1-jäännösarvossa tiotropiuminhalaatiojauheen ja tiotropiuminhalaationesteen välillä oli 0,010 l (95 % CI: -0,018–0,038 l).
Markkinoille tulon jälkeen tehdyssä TIOSPIR-tutkimuksessa vertailtiin tiotropiuminhalaationestettä ja tiotropiuminhalaatiojauhetta. Mistä tahansa syystä johtuva kuolleisuus sisältäen elossaolon seurannan oli samanlainen tutkimuksen aikana tiotropiuminhalaatiojauheen ja tiotropiuminhalaationesteen välillä (riskisuhde (tiotropiuminhalaatiojauhe/tiotropiuminhalaationeste) 1,04, 95 % CI: 0,91–1,19).
Pediatriset potilaat
Euroopan lääkevirasto on myöntänyt vapautuksen velvoitteesta toimittaa tutkimustulokset tiotropiumia sisältävän viitelääkevalmisteen käytöstä keuhkoahtaumataudin ja kystisen fibroosin hoidossa kaikissa pediatrisissa potilasryhmissä (ks. kohdasta Annostus ja antotapa ohjeet käytöstä pediatristen potilaiden hoidossa).
Farmakokinetiikka
Yleistä
Tiotropiumbromidi on ei-kiraalinen kvaternaarinen ammoniumyhdiste, ja se liukenee veteen vähäisessä määrin. Tiotropiumbromidi annetaan jauheinhalaationa. Kun lääke inhaloidaan, suurin osa annoksesta päätyy yleensä maha-suolikanavaan, ja pienempi osuus kohde-elimeen eli keuhkoihin. Suuri osa alla esitetyistä farmakokineettisistä tuloksista on saatu käyttäen suositeltuja hoitoannoksia korkeampia annoksia.
Vaikuttavan aineen yleisiä piirteitä lääkkeen oton jälkeen
Imeytyminen
Nuorille terveille vapaaehtoisille annetun inhalaation jälkeinen absoluuttinen hyötyosuus, 19,5 %, viittaa siihen, että keuhkoihin päätyvän fraktion hyötyosuus on suuri. Tiotropiumoraaliliuosten absoluuttinen hyötyosuus on 2–3 %. Suurimmat tiotropiumpitoisuudet plasmassa havaittiin 5–7 minuuttia inhaloinnin jälkeen.
Vakaassa tilassa tiotropiumin huippupitoisuus plasmassa keuhkoahtaumatautipotilailla oli 12,9 pikog/ml ja pitoisuus pieneni nopeasti monitilamallin mukaisesti. Vakaan tilan matalin plasmapitoisuus oli 1,71 pikog/ml. Systeeminen altistus tiotropiumille oli samanlaista jauhelaitteen kautta inhaloituna kuin nesteinhalaattorin kautta inhaloituna.
Jakautuminen
Tiotropium sitoutuu plasman proteiineihin 72 %:sesti ja sen jakautumistilavuus on 32 l/kg. Paikallisia pitoisuuksia keuhkoissa ei tunneta, mutta antoreitistä johtuen voidaan pitoisuuksien olettaa olevan huomattavasti korkeammat keuhkoissa. Rotilla tehdyt tutkimukset ovat osoittaneet, että tiotropiumbromidi ei läpäise veri-aivoestettä merkitsevässä määrin.
Biotransformaatio
Metabolia on vähäistä, mistä on osoituksena se, että munuaisten kautta erittyy 74 % lääkkeestä muuttumattomana nuorille terveille vapaaehtoisille annetun i.v. annon jälkeen. Tiotropiumesteri hajoaa ei-entsymaattisesti alkoholiksi (N-metyyliskopiini) ja hapoksi (ditienyyliglykolihappo), jotka eivät sitoudu muskariinireseptoreihin. Ihmisen maksan mikrosomeilla ja hepatosyyteillä tehtyjen in vitro -kokeiden mukaan osa lääkkeestä (< 20 % annoksesta i.v. annon jälkeen) metaboloituu edelleen hapettumalla sytokromi P450 entsyymien (CYP) vaikutuksesta ja sen jälkeen glutationikonjugaation kautta erilaisiksi faasin II metaboliiteiksi.
Maksan mikrosomeilla tehdyt in vitro -tutkimukset ovat osoittaneet, että entsymaattista metaboliatietä voidaan estää CYP2D6 (ja 3A4) -estäjillä, kinidiinillä, ketokonatsolilla ja gestodeenillä. Täten CYP2D6 ja 3A4 osallistuvat siihen tiotropiumin metaboliareittiin, joka on vastuussa pienemmästä osasta annoksen eliminaatiota. Tiotropium ei estä CYP:n isoformeja 1A1, 1A2, 2B6, 2C9, 2C19, 2D6, 2E1 eikä 3A ihmisen maksan mikrosomeissa edes terapeuttisia annoksia suuremmilla pitoisuuksilla.
Eliminaatio
Tiotropiumin efektiivinen puoliintumisaika keuhkoahtaumatautipotilailla vaihtelee 27–45 tunnin välillä. Kokonaispuhdistuma oli nuorissa terveissä vapaaehtoisissa 880 ml/min laskimoon annetun annoksen jälkeen. Laskimoon annettu tiotropium erittyy pääosin muuttumattomana virtsaan (74 %). Kun keuhkoahtaumatautipotilaat inhaloivat tiotropiumia jauheena ja saavuttavat vakaan tilan, virtsaan poistuu 7 % (1,3 mikrog) annoksesta muuttumattomana lääkeaineena 24 tunnin aikana. Jäljelle jäävä imeytymätön lääkeaine jää pääosin suoleen ja eliminoituu ulosteessa. Tiotropiumin munuaispuhdistuma on suurempi kuin kreatiniinipuhdistuma, mikä viittaa sen erittymiseen virtsaan. Kun keuhkoahtaumapotilaille annettiin lääkettä pitkään inhalaatio kerran päivässä, farmakokineettisesti vakaa tila saavutettiin 7 vuorokauden kuluessa, eikä kertymistä sen jälkeen tapahtunut.
Lineaarisuus/ei-lineaarisuus
Tiotropiumin farmakokinetiikka on lineaarinen terapeuttisella alueella lääkemuodosta riippumatta.
Erityisryhmät
Iäkkäät potilaat: Kuten kaikista pääasiassa munuaisten kautta poistuvista lääkkeistä voidaan odottaa, korkeaan ikään liittyi tiotropiumin munuaispuhdistuman hidastumista (365 ml/min alle 65-vuotialla keuhkoahtaumatautipotilailla ja 271 ml/min 65-vuotiailla ja sitä vanhemmilla potilailla). Tämä ei johtanut vastaavaan kasvuunAUC0-6,ss- tai Cmax,ss -arvoissa.
Munuaisten vajaatoimintapotilaat: Kun keuhkoahtaumatautipotilaat inhaloivat tiotropiumia kerran päivässä ja saavuttivat vakaan tilan, lievä munuaisten vajaatoiminta (kreatiniinipuhdistuma 50–80 ml/min) johti hieman korkeampiin AUC0-6,ss-arvoihin (1,8–30 % korkeampiin) ja vastaaviin Cmax, ss–arvoihin, verrattuna normaalin munuaistoiminnan omaaviin potilaisiin (kreatiniinipuhdistuma > 80 ml/min).
Keuhkoahtaumatautipotilailla, joilla oli kohtalainen tai vaikea munuaisten vajaatoiminta (kreatiniinipuhdistuma < 50 ml/min), tiotropiumin laskimonsisäinen anto johti kaksinkertaiseen kokonaisaltistumiseen (82 % korkeampi AUC0-4h ja 52 % korkeampi Cmax) verrattuna normaalin munuaistoiminnan omaaviin keuhkoahtaumatautipotilaisiin. Tämä todettiin pitoisuuksina plasmassa jauheinhalaation jälkeen.
Maksan vajaatoimintapotilaat: Maksan vajaatoiminnan ei oleteta vaikuttavan oleellisesti tiotropiumin farmakokinetiikkaan. Tiotropium poistuu pääasiassa munuaisten kautta (74 % nuorilla terveillä vapaaehtoisilla) ja muuttumalla yksinkertaisen ei-entsymaattisen esterihajoamisen kautta farmakologisesti tehottomiksi tuotteiksi.
Japanilaiset COPD-potilaat: Tutkimusten välisessä vertailussa tiotropiumin keskimääräiset huippupitoisuudet plasmassa 10 minuuttia tiotropiuminhalaation jälkeen olivat japanilaisilla COPD-potilailla vakaassa tilassa 20–70 % korkeampia kuin valkoihoisilla COPD-potilailla. Japanilaisilla potilailla ei kuitenkaan havaittu merkkejä korkeammasta kuolleisuudesta tai sydänriskistä verrattuna valkoihoisiin potilaisiin. Muista etnisistä ryhmistä tai roduista saatavilla olevat farmakokineettiset tiedot ovat riittämättömiä.
Lapsipotilaat: Ks. kohta Annostus ja antotapa.
Farmakokineettiset/farmakodynaamiset suhteet
Farmakokinetiikalla ja farmakodynamiikalla ei ole suoria vaikutuksia toisiinsa.
Prekliiniset tiedot turvallisuudesta
Monet farmakologista turvallisuutta, toistetun annon toksisuutta sekä lisääntyvyystoksisuutta koskevien konventionaalisten tutkimusten tulokset selittyvät tiotropiumbromidin antikolinergisillä ominaisuuksilla. Ruoankulutuksen väheneminen, ruumiinpainon lisääntymisen esto, suun ja nenän kuivuminen, kyynel- ja syljenerityksen väheneminen, mydriaasi ja sydämen syketiheyden kasvu olivat tyypillisiä eläimissä havaittuja vaikutuksia. Muita merkittäviä vaikutuksia toistetun annon toksisuuskokeissa olivat lievä hengitysteiden ärtyvyys rotilla ja hiirillä. Näitä tuloksia tukivat nuha ja nenäontelon ja kurkunpään epiteelimuutokset. Rotista havaittiin myös eturauhastulehdukseen viittaavia muutoksia sekä virtsakiviä virtsarakossa.
Raskaudelle, alkion ja sikiön kehitykselle, synnytykselle tai synnytyksen jälkeiselle kehitykselle vahingollisia vaikutuksia voitiin todeta vain annoksista, jotka olivat emolle toksisia. Tiotropium ei ollut teratogeeninen rotille tai kaneille. Rotilla tehdyssä yleisessä lisääntymis- ja fertiliteettitutkimuksessa millään annostasolla ei huomattu olevan haitallista vaikutusta hoitoa saaneiden emojen tai niiden jälkeläisten lisääntymis- tai pariutumiskykyyn.
Hengitystiemuutoksia (ärsytys) ja urogenitaalimuutoksia (eturauhastulehdus) sekä lisääntymistoksisuutta havaittiin paikallisesti tai systeemisesti annetuilla annoksilla, jotka olivat yli viisinkertaiset terapeuttisiin annoksiin nähden. Genotoksisuus- ja karsinogeenisuustutkimukset eivät viittaa mihinkään erityiseen vaaraan ihmisille.
Farmaseuttiset tiedot
Apuaineet
Kapselin sisältö:
Laktoosimonohydraatti (voi sisältää pieniä määriä maitoproteiineja)
Kapselin kuori:
Liivate (E441)
Puhdisvettu vesi
Makrogoli 4000 (E1521)
Titaanidioksidi (E171)
Keltainen rautaoksidi (E172)
Briljanttisininen (E133)
Yhteensopimattomuudet
Ei oleellinen.
Kestoaika
2 vuotta.
Hävitä inhalaattori 90 päivän kuluttua ensimmäisestä käytöstä.
Kapseli pitää käyttää heti läpipainopakkauksen avaamisen jälkeen.
Säilytys
Säilytä alle 30 °C.
Avatun lääkevalmisteen säilytys, ks. kohta Kestoaika.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
TIOTROPIUM STADA inhalaatiojauhe, kapseli, kova
18 mikrog (L:kyllä) 30 fol (Vertical-Haler) (15,54 €), 30 fol (15,54 €), 90 fol (Vertical-Haler) (53,42 €)
PF-selosteen tieto
Kuumasaumattu alumiini-/alumiini ‑läpipainopakkaus, jossa 5 tai 10 kapselia.
Vertical-Haler ‑laite kerta-annosinhalaattori, joka on valmistettu akryylinitriili-butadieeni-styreeni (ABS) muovimateriaalista ja ruostumattomasta teräksestä. Materiaalit, jotka ovat suorassa kosketuksessa valmisteen kanssa inhalaatiohetkellä, ovat: ruostumaton teräs 304 (kapselin lävistävä neula), akryylinitriili-butadieeni-styreeni-ABS (muodostaa suukappaleen, jonka läpi lääke kulkee, ja kapselikammion).
Pakkauskoot:
- Pahvikotelo, jossa on Vertical-Haler ‑laite ja 10 kapselia
- Pahvikotelo, jossa on Vertical-Haler ‑laite ja 15 kapselia
- Pahvikotelo, jossa on Vertical-Haler ‑laite ja 30 kapselia
- Pahvikotelo, jossa on Vertical-Haler ‑laite ja 60 kapselia
- Pahvikotelo, jossa on Vertical-Haler ‑laite ja 90 kapselia
- Sairaalapakkaus: Pahvikotelo, jossa on Vertical-Haler ‑laite ja 5x30 kapselia (monipakkaus)
- Pahvikotelo, jossa on kaksi Vertical-Haler ‑laitetta ja 60 kapselia
- Pahvikotelo, jossa on kolme Vertical-Haler ‑laitetta ja 90 kapselia
- Sairaalapakkaus: Pahvikotelo, jossa on 5x60 kapselia (monipakkaus)
- Pahvikotelo, jossa on 30 kapselia
- Pahvikotelo, jossa on 60 kapselia
- Pahvikotelo, jossa on 90 kapselia
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Valmisteen kuvaus:
Läpinäkymätön inhalaatiojauhetta sisältävä vihreä kapseli, jonka koko on 16 mm x 5,8 mm.
Käyttö- ja käsittelyohjeet
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
TIOTROPIUM STADA inhalaatiojauhe, kapseli, kova
18 mikrog 30 fol, 30 fol, 90 fol
- Alempi erityiskorvaus (65 %). Krooninen keuhkoastma ja sitä läheisesti muistuttavat krooniset obstruktiiviset keuhkosairaudet (203).
- Peruskorvaus (40 %).
- Varmista antolaitteen ja käyttöpakkauksen yhteensopivuus lääkettä vaihdettaessa.
ATC-koodi
R03BB04
Valmisteyhteenvedon muuttamispäivämäärä
27.06.2024
Yhteystiedot
PL 1310, Puolikkotie 8, 02230 Espoo (käyntiosoite)
00101 Helsinki
0207 416 888
