ORSERDU filmdragerad tablett 86 mg, 345 mg
Observera
▼ Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning. Se avsnitt Biverkningar om hur man rapporterar biverkningar.
Kvalitativ och kvantitativ sammansättning
ORSERDU 86 mg filmdragerade tabletter
Varje filmdragerad tablett innehåller elacestrantdihydroklorid motsvarande 86,3 mg elacestrant.
ORSERDU 345 mg filmdragerade tabletter
Varje filmdragerad tablett innehåller elacestrantdihydroklorid motsvarande 345 mg elacestrant.
För fullständig förteckning över hjälpämnen, se avsnitt Förteckning över hjälpämnen.
Läkemedelsform
Filmdragerad tablett
Kliniska uppgifter
Terapeutiska indikationer
Monoterapi med ORSERDU är indicerad för behandling av postmenopausala kvinnor, och män, med östrogenreceptorpositiv (ER-positiv), HER2-negativ, lokalt framskriden eller metastaserande bröstcancer med en aktiverande ESR1-mutation som har progredierande sjukdom efter minst en typ av endokrin behandling med CDK 4/6-hämmare.
Villkor
Ainoastaan syöpälääkkeiden antoon perehtyneen lääkärin tulee aloittaa hoito.
Dosering och administreringssätt
Behandling med ORSERDU bör sättas in av en läkare med erfarenhet av att använda cancerbehandlingar.
Patienter med ER-positiv, HER2-negativ framskriden bröstcancer ska väljas ut för behandling med ORSERDU baserat på förekomst av en aktiverande ESR1-mutation i plasmaprover, med hjälp av ett CE-märkt in vitro-diagnostiskt test för därtill avsett syfte. Om ett CE-märkt in vitro-diagnostiskt test inte är tillgängligt ska förekomsten av en aktiverande ESR1-mutation i plasmaproverbedömas med ett alternativt validerat test.
Dosering
Den rekommenderade dosen är 345 mg (en 345 mg filmdragerad tablett) en gång dagligen.
Den maximala rekommenderade dagliga dosen av ORSERDU är 345 mg.
Behandlingen bör fortsätta så länge klinisk nytta observeras eller tills oacceptabel toxicitet uppstår.
Glömd dos
Om en dos glöms kan den tas omedelbart inom 6 timmar efter den tid då den vanligtvis tas. Efter mer än 6 timmar ska dosen hoppas över för den dagen. Nästa dag ska ORSERDU tas vid den vanliga tidpunkten.
Kräkningar
Om patienten kräks efter att ha tagit ORSERDU-dosen ska patienten inte ta ytterligare en dos den dagen, utan ska återuppta det vanliga doseringsschemat nästa dag vid den vanliga tidpunkten.
Dosjusteringar
Rekommenderade dosjusteringar för elacestrant för patienter med biverkningar (se avsnitt Biverkningar) anges i tabell 1 och 2:
Tabell 1: Dosminskningar av ORSERDU vid biverkningar
Dosnivå av ORSERDU | Dos och schema | Antal tabletter och styrka |
Dosminskning | 258 mg en gång dagligen | Tre tabletter à 86 mg |
Om ytterligare dosminskning under 258 mg en gång dagligen krävs ska ORSERDU sättas ut.
Tabell 2: Riktlinjer för dosminskning av ORSERDU vid biverkningar
Svårighetsgrad | Dosjustering |
Grad 2 | Överväg att avbryta ORSERDU tills återhämtning till grad ≤ 1 eller baslinjen har skett. Återuppta sedan ORSERDU på samma dosnivå. |
Grad 3 | Avbryt ORSERDU tills återhämtning till grad ≤ 1 eller baslinjen har skett. Dosen ska minskas till 258 mg när behandlingen återupptas. Om toxiciteten av grad 3 återkommer ska ORSERDU avbrytas tills återhämtning till grad ≤ 1 eller baslinjen har skett. Den reducerade dosen på 258 mg kan återupptas om den behandlande läkaren bedömer att patienten har nytta av behandlingen. Om en biverkning av grad 3 eller en oacceptabel biverkning återkommer ska ORSERDU sättas ut permanent. |
Grad 4 | Avbryt ORSERDU tills återhämtning till grad ≤ 1 eller baslinjen har skett. Dosen ska minskas till 258 mg när behandlingen återupptas. Om en biverkning av grad 4 eller oacceptabel biverkning återkommer ska ORSERDU sättas ut permanent. |
Användning av ORSERDU med CYP3A4-hämmare
Samtidig användning av starka eller måttliga CYP3A4-hämmare bör undvikas och ett alternativt läkemedel för samtidig administrering utan eller med minimal potential att hämma CYP3A4 bör övervägas.
Om en stark CYP3A4-hämmare måste användas ska dosen av elacestrant minskas till 86 mg en gång dagligen, med noggrann övervakning av hur den tolereras. Om en måttlig CYP3A4-hämmare måste användas ska dosen av elacestrant minskas till 172 mg en gång dagligen, med noggrann övervakning av hur den tolereras. Efterföljande dosminskning till 86 mg en gång dagligen kan övervägas med måttliga CYP3A4-hämmare baserat på tolerabilitet.
Om CYP3A4-hämmaren sätts ut ska dosen av elacestrant ökas till den dos som användes innan CYP3A4-hämmaren sattes in (efter 5 halveringstider för CYP3A4-hämmaren) (se avsnitt Varningar och försiktighet, Interaktioner och Farmakokinetiska egenskaper).
Inga dosjusteringar krävs för samadministrering av ORSERDU och milda CYP3A4-hämmare (se avsnitt Interaktioner).
Användning av ORSERDU med CYP3A4-inducerare
Samtidig användning av starka eller måttliga CYP3A4-inducerare bör undvikas och ett alternativt läkemedel för samtidig administrering utan eller med minimal potential att inducera CYP3A4 bör övervägas.
Om en stark eller måttlig CYP3A4-inducerare måste användas under en kort tid (dvs. ≤ 3 dagar) eller upprepade gånger (dvs. behandlingsperioder ≤ 3 dagar som separeras med minst 2 veckor eller 1 vecka + 5 av CYP3A4-inducerarens halveringstider, beroende på vilket som är längst) ska du fortsätta med elacestrant utan att öka dosen.
Inga dosjusteringar krävs för samadministrering av ORSERDU och milda CYP3A4-inducerare (se avsnitt Varningar och försiktighet, Interaktioner och Farmakokinetiska egenskaper).
Särskilda populationer
Äldre
Ingen dosjustering krävs baserat på patientens ålder. Det finns begränsat med data tillgängliga för patienter ≥ 75 år (se avsnitt Farmakokinetiska egenskaper).
Nedsatt leverfunktion
Ingen dosjustering rekommenderas för patienter med lätt nedsatt leverfunktion (Child-Pugh A). Hos patienter med måttligt nedsatt leverfunktion (Child-Pugh B) ska dosen av ORSERDU minskas till 258 mg. Elacestrant har inte studerats hos patienter med svårt nedsatt leverfunktion (Child-Pugh C) och därför kan ingen dosrekommendation göras för patienter med svårt nedsatt leverfunktion (se avsnitt Varningar och försiktighet).
Nedsatt njurfunktion
Ingen dosjustering krävs för personer med nedsatt njurfunktion. Elacestrant har inte studerats hos patienter med svårt nedsatt njurfunktion och därför kan ingen dosrekommendation göras för patienter med svårt nedsatt njurfunktion (se avsnitt Farmakokinetiska egenskaper).
Pediatrisk population
Säkerhet och effekt för ORSERDU för nyfödda och barn upp till 18 år har inte fastställts. Inga data finns tillgängliga.
Administreringssätt
ORSERDU är avsett för oral användning.
Tabletterna ska sväljas hela. De får inte tuggas, krossas eller delas innan de sväljs. Patienten ska ta sin dos av ORSERDU vid ungefär samma tid varje dag. ORSERDU ska administreras i samband med en lätt måltid. Administrering med mat kan också minska illamående och kräkningar (se avsnitt Farmakokinetiska egenskaper).
Kontraindikationer
Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt Förteckning över hjälpämnen.
Varningar och försiktighet
Nedsatt leverfunktion
ORSERDU metaboliseras av levern och nedsatt leverfunktion kan öka risken för biverkningar. Därför ska ORSERDU användas med försiktighet till patienter med nedsatt leverfunktion och patienternaska övervakas regelbundet och noggrant avseende biverkningar. Administrering av elacestrant ska ske med försiktighet vid en dos på 258 mg en gång dagligen hos patienter med måttligt nedsatt leverfunktion (se avsnitt Dosering och administreringssätt). I avsaknad av kliniska data rekommenderas inte elacestrant för patienter med svårt nedsatt leverfunktion (Child-Pugh C) (se avsnitt Dosering och administreringssätt).
Samtidig användning med CYP3A4-hämmare
Samtidig administrering av ORSERDU med starka CYP3A4-hämmare, inklusive men inte begränsat till klaritromycin, indinavir, itrakonazol, ketokonazol, lopinavir/ritonavir, nefazodon, nelfinavir, posakonazol, sakvinavir, telaprevir, telitromycin, vorikonazol och grapefrukt eller grapefruktjuice bör undvikas. Ett alternativt läkemedel för samtidig administrering utan eller med minimal potential att hämma CYP3A4 bör övervägas. Om det inte går att undvika den starka CYP3A4-hämmaren ska dosjustering av ORSERDU göras (se avsnitt Dosering och administreringssätt och Interaktioner).
Samtidig administrering av ORSERDU med måttliga CYP3A4-hämmare, inklusive men inte begränsat till aprepitant, ciprofloxacin, konivaptan, krizotinib, ciklosporin, diltiazem, dronedaron, erytromycin, flukonazol, fluvoxamin, grapefruktjuice, imatinib, isavukonazol, tofisopam och verapamil bör undvikas. Ett alternativt läkemedel för samtidig administrering utan eller med minimal potential att hämma CYP3A4 bör övervägas. Om det inte går att undvika den måttliga CYP3A4-hämmaren ska dosjustering av ORSERDU göras (se avsnitt Dosering och administreringssätt och Interaktioner).
Samtidig användning med CYP3A4-inducerare
Samtidig administrering av ORSERDU med starka CYP3A4-inducerare, inklusive men inte begränsat till fenytoin, rifampicin, karbamazepin och johannesört (Hypericum perforatum) bör undvikas. Ett alternativt läkemedel för samtidig administrering utan eller med minimal potential att inducera CYP3A4 bör övervägas. Om det inte går att undvika den starka CYP3A4-induceraren ska dosjustering av ORSERDU göras (se avsnitt Dosering och administreringssätt och Interaktioner).
Samtidig administrering av ORSERDU med måttliga CYP3A4-inducerare, inklusive men inte begränsat till bosentan, cenobamat, dabrafenib, efavirenz, etravirin, lorlatinib, fenobarbital, primidon och sotorasib bör undvikas. Ett alternativt läkemedel för samtidig administrering utan eller med minimal potential att inducera CYP3A4 bör övervägas. Om det inte går att undvika den måttliga CYP3A4-induceraren ska dosjustering av ORSERDU göras (se avsnitt Dosering och administreringssätt och Interaktioner).
Tromboemboliska händelser
Tromboemboliska händelser observeras ofta hos patienter med framskriden bröstcancer och har observerats i kliniska studier med ORSERDU (se avsnitt Biverkningar). Detta bör beaktas vid förskrivning av ORSERDU till patienter med ökad risk för tromboemboli.
Interaktioner
ORSERDU metaboliseras främst av CYP3A4 och är ett substrat för den organiska anjontransportpolypeptiden 2B1 (OATP2B1). ORSERDU hämmar effluxtransportörerna P-glykoprotein (P-gp) och bröstcancerresistensprotein (BCRP).
Effekt av andra läkemedel på ORSERDU
CYP3A4-hämmare
Samtidig administrering av den starka CYP3A4-hämmaren itrakonazol (200 mg en gång dagligen i 7 dagar) och ORSERDU (172 mg en gång dagligen i 7 dagar) ökade exponeringen av elacestrant i plasma (AUCinf) och maximal koncentration (Cmax) hos friska försökspersoner 5,3 respektive 4,4 gånger.
Fysiologiskt baserade farmakokinetiska simuleringar (PBPK) hos cancerpatienter tydde på att samtidig administrering av flera dagliga doser av 345 mg elacestrant och 200 mg itrakonazol kan öka AUC vid steady state och Cmax för elacestrant 5,5 respektive 3,9 gånger, vilket kan öka risken för biverkningar.
PBPK-simuleringar hos cancerpatienter tydde på att samtidig administrering av flera dagliga doser av 345 mg elacestrant med måttliga CYP3A4-hämmare kan öka AUC vid steady state och Cmax för elacestrant 2,3 respektive 1,9 gånger, med flukonazol (200 mg en gång dagligen), och med 3,9 respektive 3,0 gånger, med erytromycin (500 mg fyra gånger dagligen), vilket kan öka risken för biverkningar.
CYP3A4-inducerare
Samtidig administrering av den starka CYP3A4-induceraren rifampicin (600 mg en gång dagligen i 7 dagar) och en engångsdos av ORSERDU 345 mg minskade exponeringen av elacestrant i plasma (AUCinf) och maximal koncentration (Cmax) hos friska försökspersoner med 86 % respektive 73 %, vilket kan minska verkan av elacestrant.
PBPK-simuleringar hos cancerpatienter tydde på att samtidig administrering av flera dagliga doser av 345 mg elacestrant och 600 mg rifampicin kan minska AUC vid steady state och Cmax för elacestrant med 84 % respektive 77 %, vilket kan minska verkan av elacestrant.
PBPK-simuleringar hos cancerpatienter tydde på att samtidig administrering av flera dagliga doser av 345 mg elacestrant och den måttliga CYP3A4-induceraren efavirenz (600 mg) kan minska AUC vid steady state och Cmax för elacestrant med 57 % respektive 52 %, vilket kan minska verkan av elacestrant.
OATP2B1-hämmare
Elacestrant är ett substrat för OATP2B1 in vitro. Eftersom det inte kan uteslutas att samtidig administrering av OATP2B1-hämmare eventuellt ökar exponeringen av elacestrant, vilket kan öka risken för biverkningar, rekommenderas försiktighet vid samtidig användning av ORSERDU och OATP2B1-hämmare.
Effekt av ORSERDU på andra läkemedel
P-gp-substrat
Samtidig administrering av ORSERDU (345 mg, engångsdos) och digoxin (0,5 mg, engångsdos) ökade exponeringen av digoxin med 27 % för Cmax och 13 % för AUC. Administreringen av digoxin ska övervakas och dosen minskas vid behov.
Samtidig användning av ORSERDU och andra P-gp-substrat kan öka deras koncentrationer, vilket kan öka biverkningarna som är förknippade med P-gp-substraten. Dosen av samadministrerade P‑gp-substrat ska minskas i enlighet med deras produktresuméer.
BCRP-substrat
Samtidig administrering av ORSERDU (345 mg, engångsdos) och rosuvastatin (20 mg, engångsdos) ökade exponeringen av rosuvastatin med 45 % för Cmax och 23 % för AUC. Administreringen av rosuvastatin ska övervakas och dosen minskas vid behov.
Samtidig användning av ORSERDU och andra BCRP-substrat kan öka deras koncentrationer, vilket kan öka biverkningarna som är förknippade med BCRP-substraten. Dosen av samadministrerade BCRP-substrat ska minskas i enlighet med deras produktresuméer.
Fertilitet, graviditet och amning
Fertila kvinnor/preventivmedel till män och kvinnor
ORSERDU ska inte användas under graviditet eller till fertila kvinnor som inte använder preventivmedel. Baserat på verkningsmekanismen för elacestrant och fynd från reproduktionstoxikologiska djurstudier kan ORSERDU orsaka fosterskador om det administreras till gravida kvinnor. Fertila kvinnor ska instrueras att använda effektiva preventivmedel under behandling med ORSERDU och upp till en vecka efter den sista dosen.
Graviditet
Det finns inga data från användningen av elacestrant hos gravida kvinnor. Djurstudier har visat reproduktionstoxikologiska effekter (se avsnitt Prekliniska säkerhetsuppgifter). ORSERDU ska inte användas under graviditet eller till fertila kvinnor som inte använder preventivmedel. Fertila kvinnors graviditetsstatus ska verifieras innan behandling med ORSERDU inleds. Om graviditet inträffar medan patienten tar ORSERDU måste patienten informeras om den potentiella risken för fostret och möjlig risk för missfall.
Amning
Det är okänt om elacestrant/metaboliter utsöndras i bröstmjölk. På grund av risken för allvarliga biverkningar hos det ammade barnet rekommenderas ammande kvinnor att inte amma under behandling med ORSERDU och under en vecka efter den sista dosen av ORSERDU.
Fertilitet
Baserat på fynd från djurstudier (se avsnitt Prekliniska säkerhetsuppgifter) och verkningsmekanismen för ORSERDU kan detta läkemedel ha en negativ inverkan på fertiliteten hos kvinnor och män som kan få barn.
Effekter på förmågan att framföra fordon och använda maskiner
ORSERDU har ingen eller försumbar effekt på förmågan att framföra fordon och använda maskiner. Eftersom trötthet, asteni och sömnsvårigheter har rapporterats hos vissa patienter som tar elacestrant (se avsnitt Biverkningar) ska dock försiktighet iakttas av patienter som upplever dessa biverkningar vid framförande av fordon eller användning av maskiner.
Biverkningar
Sammanfattning av säkerhetsprofilen
De vanligaste (≥ 10 %) biverkningarna för ORSERDU var illamående, förhöjda triglyceridnivåer, förhöjda kolesterolnivåer, kräkning, trötthet, dyspepsi, diarré, minskade kalciumnivåer, ryggont, ökade kreatininnivåer, artralgi, minskade natriumnivåer, förstoppning, huvudvärk, värmevallningar, buksmärta, anemi, minskade kaliumnivåer och förhöjda nivåer av alaninaminotransferas. De vanligaste biverkningarna av grad ≥ 3 (≥ 2 %) för elacestrant var illamående (2,7 %), förhöjt ASAT-värde (2,7 %), förhöjt ALAT-värde (2,3 %), anemi (2 %), ryggont (2 %) och smärta i skelettet (2 %).
Allvarliga biverkningar som rapporterades hos ≥ 1 % av patienterna inkluderade illamående, dyspné och tromboembolism (venös).
Biverkningar som ledde till att läkemedlet sattes ut för ≥ 1 % av patienterna inkluderade illamående och minskad aptit.
Biverkningar som ledde till dosminskning för ≥ 1 % av patienterna inkluderade illamående.
Biverkningar som ledde till dosavbrott för ≥ 1 % av patienterna inkluderade illamående, buksmärta, förhöjda nivåer av alaninaminotransferas, kräkning, hudutslag, smärta i skelettet, minskad aptit, höjda nivåer av aspartataminotransferas och diarré.
Lista i tabellform över biverkningar
Biverkningar som beskrivs i listan nedan återspeglar exponeringen för elacestrant hos 301 patienter med bröstcancer i tre öppna studier (RAD1901-005, RAD1901-106 och RAD1901-308) där patienterna fick 400 mg elacestrant en gång dagligen som monoterapi. Frekvenserna av biverkningar baseras på frekvenserna av alla biverkningar oavsett orsak som identifierats hos patienter som exponerats för elacestrant vid rekommenderad dos enligt avsedd indikation, medan frekvenserna av förändringar av laboratorieparametrar baseras på försämring från baslinjen med minst 1 grad och växlingar till ≥ grad 3. Medianvaraktigheten på behandlingen var 85 dagar (intervall: 5–1 288).
Biverkningsfrekvenserna från kliniska prövningar baseras på biverkningar oavsett orsak, där en andel av biverkningsfallen kan ha andra orsaker än läkemedlet, som exempelvis sjukdomen, andra läkemedel eller orelaterade orsaker.
Denna konvention används för klassificering av frekvensen av en läkemedelsbiverkning och baseras på riktlinjerna från Council for International Organizations of Medical Sciences (CIOMS): mycket vanliga (≥ 1/10), vanliga (≥ 1/100, < 1/10), mindre vanliga (≥ 1/1 000, < 1/100), sällsynta (≥ 1/10 000, < 1/1 000), mycket sällsynta (< 1/10 000) och ingen känd frekvens (kan inte beräknas från tillgängliga data).
Tabell 3. Biverkningar hos patienter som behandlats med 345 mg elacestrant som monoterapi för metastaserande bröstcancer
Elacestrant N= 301 | ||
| Infektioner och infestationer | Vanliga | Urinvägsinfektion |
| Blodet och lymfsystemet | Mycket vanliga | Anemi |
| Vanliga | Minskat lymfocytantal | |
| Metabolism och nutrition | Mycket vanliga | Minskad aptit |
| Psykiatriska sjukdomar | Vanliga | Sömnsvårigheter |
| Centrala och perifera nervsystemet | Mycket vanliga | Huvudvärk |
| Vanliga | Yrsel, svimning | |
| Vaskulära sjukdomar | Mycket vanliga | Värmevallningar* |
| Mindre vanliga | Tromboembolism (venös)* | |
| Respiratoriska, torakala och mediastinala sjukdomar | Vanliga | Dyspné, hosta* |
| Magtarmkanalen | Mycket vanliga | Illamående, kräkning, diarré, förstoppning, buksmärta*, dyspepsi* |
| Vanliga | Stomatit | |
| Lever och gallvägar | Mindre vanliga | Akut leversvikt |
| Sjukdomar i hud och subkutan vävnad | Vanliga | Hudutslag* |
| Muskuloskeletala systemet och bindväv | Mycket vanliga | Artralgi, ryggont |
| Vanliga | Smärta i extremiteter, muskuloskeletal bröstsmärta*, smärta i skelettet | |
| Allmänna sjukdomar och tillstånd på administreringsställe | Mycket vanliga | Trötthet |
| Vanliga | Asteni | |
| Utredningar | Mycket vanliga | Förhöjd nivå av aspartataminotransferas, förhöjda triglyceridnivåer, förhöjda kolesterolnivåer, förhöjda nivåer av alaninaminotransferas, minskade kalciumnivåer, förhöjda kreatininnivåer, minskade natriumnivåer, minskade kaliumnivåer |
| Vanliga | Förhöjda nivåer av alkaliskt fosfatas i blodet | |
* Incidensen representerar en grupp av liknande begrepp.
Läkemedelsbiverkningarna är listade efter organsystemklass och fallande frekvens.
Beskrivning av utvalda biverkningar
Illamående
Illamående rapporterades hos 35 % av patienterna. Illamåendehändelser av grad 3–4 rapporterades hos 2,5 % av patienterna. Illamående rapporterades i allmänhet tidigt, med en mediantid till debut på 14 dagar (intervall: 1–490 dagar). Illamående uppträdde oftare i den första cykeln och från och med cykel 2 var incidensen för illamående i allmänhet lägre i efterföljande cykler (dvs. över tid). Profylaktisk behandling för illamående ordinerades för 12 (5 %) av deltagarna i elacestrantgruppen och 28 (11,8 %) fick antiemetikum för behandling av illamående under behandlingsperioden.
Äldre
I studien RAD1901-308 var 104 patienter som fick elacestrant ≥ 65 år och 40 patienter var ≥ 75 år. Gastrointestinala störningar rapporterades oftare hos patienter i åldern ≥ 75 år. Den behandlande läkarens övervakning av biverkningar som uppkommer under behandlingen bör inkludera beaktande av patientens ålder och komorbiditeter vid val av individanpassade interventioner.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta-riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning via
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Överdosering
Den högsta dosen av ORSERDU som administrerades i kliniska studier var 1 000 mg per dag. De biverkningar som rapporterades i samband med doser som var högre än den rekommenderade dosen överensstämmer med den fastställda säkerhetsprofilen (se avsnitt Biverkningar). Frekvensen och svårighetsgraden på gastrointestinala störningar (buksmärta, illamående, dyspepsi och kräkning) verkade vara dosrelaterade. Det finns inget känt motgift vid överdosering av ORSERDU. Patienterna ska övervakas noggrant och behandling av överdosering ska bestå av stödjande behandling.
Farmakologiska egenskaper
Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: Endokrinterapi, antiestrogen, ATC-kod: L02BA04
Verkningsmekanism
Elacestrant, en tetrahydronaftalenförening, är en potent, selektiv och oralt aktiv östrogenreceptor-α (ERα)-antagonist och -degraderare.
Farmakodynamiska effekter
Elacestrant hämmar estradiolberoende och oberoende tillväxt av ERα-positiva bröstcancerceller, inklusive modeller med genmutationer av östrogenreceptor 1 (ESR1). Elacestrant visade en kraftig antitumöraktivitet i patientutvunna xenograftmodeller som tidigare exponerats för flera endokrinterapier, och som hade genmutationer av vildtyp av ESR1 eller ESR1 i ligandbindningsdomänen.
Hos patienter med ER-positiv framskriden bröstcancer med ett medianvärde på 2,5 tidigare endokrinbehandlingslinjer, som doserades med 400 mg elacestrantdihydroklorid (345 mg elacestrant) dagligen, var medianreduktionen av tumörupptagning av 16α-18F-fluoro-17ß-estradiol (FES) från baslinjen till dag 14 88,7 %, vilket visade minskad ER-tillgänglighet och antitumöraktivitet uppmätt med FES-PET/DT hos patienter med tidigare endokrinbehandlingar.
Klinisk effekt och säkerhet
Effekt och säkerhet för ORSERDU hos patienter med framskriden ER+/HER2--bröstcancer efter tidigare endokrinbehandling i kombination med en CDK4/6-hämmare utvärderades i RAD1901-308, en randomiserad, öppen multicenterstudie med aktiv kontroll som jämförde ORSERDU med standardvård (fulvestrant för patienter som tidigare fått aromatashämmare vid metastas eller aromatashämmare för patienter som fått fulvestrant vid metastas). Lämpliga patienter för studien var postmenopausala kvinnor och män vars sjukdom hade framskridit trots minst 1 och högst 2 tidigare endokrinbehandlingslinjer. Alla patienter var tvungna att ha en ECOG-funktionsstatus (Eastern Cooperative Oncology Group) på 0 eller 1, och utvärderbara lesioner enligt Response Evaluation Criteria in Solid Tumors (RECIST) version 1.1, dvs. mätbar sjukdom eller enbart skelettsjukdom med utvärderbara lesioner. Tidigare endokrinbehandling måste ha inkluderat en kombination av behandling med CDK4/6-hämmare och högst 1 tidigare typ av cytotoxisk kemoterapi för metastaserande bröstcancer. Det var nödvändigt att patienterna var lämpliga kandidater för endokrinbehandling som monoterapi. Patienter med symtomatisk metastaserande visceral sjukdom, patienter med komorbiditet i hjärtat och patienter med svårt nedsatt leverfunktion uteslöts.
Totalt randomiserades 478 patienter i förhållandet 1:1 till daglig oral administrering av 400 mg elacestrantdihydroklorid (345 mg elacestrant) eller standardvård (239 på elacestrant och 239 på standardvård), inklusive totalt 228 patienter (47,7 %) med ESR1-mutationer vid baslinjen (115 patienter på elacestrant och 113 patienter på standardvård). Bland de 239 patienter som randomiserades till gruppen med standardvård fick 166 fulvestrant och 73 en aromatashämmare som bestod av anastrozol, letrozol eller exemestan. Randomiseringen stratifierades efter ESR1-mutationsstatus (ESR1-mutation kontra ingen ESR1-mutation [inga ESR1-mutationer upptäckta]), tidigare behandling med fulvestrant (ja kontra nej) och visceral metastas (ja kontra nej). ESR1-mutationsstatus fastställdes av tumördeoxiribonukleinsyra (ctDNA) i blodet med hjälp av Guardant360 CDx-analys och begränsades till ESR1-missense-mutationer i ligandbindningsdomänen (mellan kodon 310 och 547).
Medianåldern på patienterna (ORSERDU kontra standardvård) vid baslinjen var 63,0 år (intervall: 24–89) jämfört med 63,0 (intervall: 32–83), och 45,0 % var över 65 (43,5 kontra 46,4). De flesta patienter var kvinnor (97,5 % jämfört med 99,6 %) och de flesta patienter var vita (88,4 % jämfört med 87,2 %), följt av asiater (8,4 % kontra 8,2 %), svarta eller afroamerikaner (2,6 % mot 4,1 %) och andra/okända (0,5 % jämfört med 0,5 %). ECOG-funktionsstatus vid baslinjen var 0 (59,8 % jämfört med 56,5 %), 1 (40,2 % jämfört med 43,1 %) eller > 1 (0 % jämfört med 0,4 %). Patientdemografiska uppgifter för personer med ESR1-muterade tumörer var i allmänhet representativa för den bredare studiepopulationen. Mediantiden för exponering för ORSERDU var 2,8 månader (intervall: 0,4 till 24,8).
Det primära effektmåttet var progressionsfri överlevnad (PFS) enligt bedömning av IRC (oberoende granskningskommitté) hos samtliga patienter, dvs. inklusive patienter med en ESR1-mutation, samt hos patienter med ESR1-mutationer. En statistiskt signifikant PFS-fördel observerades hos alla patienter med en median-PFS på 2,79 månader i Orserdugruppen jämfört med 1,91 månader i standardbehandlingsgruppen (HR = 0,70; 95 % KI: 0,55; 0,88). Effektresultaten presenteras i tabell 4 och figur 1 för patienter med ESR1-mutationer.
Tabell 4: Effektresultat för patienter med ESR1-mutationer (utvärderade av en blindad kommitté för granskning av bilder)
| ORSERDU | Standardvård | |
| Progressionsfri överlevnad (PFS) | N = 115 | N = 113 |
| Antal PFS-händelser, n (%) | 62 (53,9) | 78 (69,0) |
| Median-PFS i månader* (95 % KI) | 3,78 (2,17; 7,26) | 1,87 (1,87; 2,14) |
| Riskkvot** (95 % KI) | 0,546 (0,387; 0,768) | |
| p-värde (stratifierad log-rank) | 0,0005 | |
| Total överlevnad (OS) | N = 115 | N = 113 |
| Antal OS-händelser, n (%) | 61 (53) | 60 (53,1) |
| Median-OS i månader* (95 % KI) | 24,18 (20,53; 28,71) | 23,49 (15,64; 29,90) |
| Riskkvot** (95 % KI) | 0,903 (0,629; 1,298) | |
KI = konfidensintervall; ESR1 = östrogenreceptor 1; PFS = progressionsfri överlevnad.
* Kaplan-Meir-uppskattning, 95 % KI baserat på Brookmeyer-Crowley-metoden med linjär transformation.
** Från en proportionell Cox-riskmodell som stratifierats efter tidigare behandling med fulvestrant (ja kontra nej) och visceral metastas (ja kontra nej).
Brytdatum för data var 6 september 2021 för PFS och 2 september 2022 för OS.
Figur 1: PFS hos patienter med en ESR1-mutation (bedömt av en blindadgranskningskommitté för bilddiagnostik)
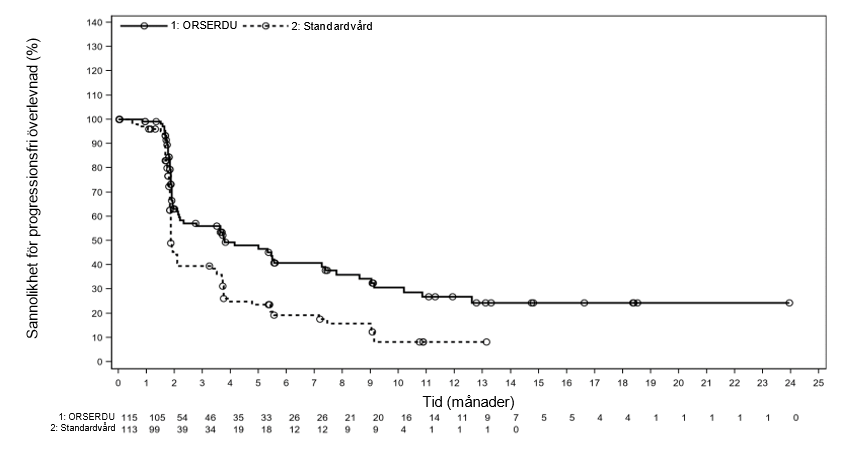
Pediatrisk population
Europeiska läkemedelsmyndigheten har beviljat undantag från kravet att skicka in studieresultat för ORSERDU för alla grupper av den pediatriska populationen för bröstcancer (se avsnitt Dosering och administreringssätt).
Farmakokinetiska egenskaper
Den orala biotillgängligheten för elacestrant är cirka 10 %. Steady state uppnås dag 6 efter dosering en gång dagligen. Cmax och AUC ökar något mer än proportionellt med dosen för doser ≥ 50 mg (saltform).
Absorption
Efter oral administrering absorberades elacestrant snabbt och nådde Cmax inom 1–4 timmar. Det geometriska medelvärdet för Cmax var 52,86 ng/ml (35,2 % variationskoefficient [CV%]) och AUCinf var 1 566 ng*h/ml (38,4 % CV) efter administrering av 345 mg elacestrant som engångsdos på ej fastande mage. Vid steady state förutspås mediankoncentrationen i plasma [min, max] vid 4 timmar efter dosering (C4h) och AUC vara 108 ng/ml [27,5–351] respektive 2 190 ng*h/ml [461–8 470].
Effekt av föda
Administrering av en tablett à 345 mg elacestrant med en kaloririk måltid med hög fetthalt ökade Cmax och AUC med 40 % respektive 20 %, jämfört med administrering på fastande mage. När tabletten administrerades tillsammans med en lätt måltid ökade Cmax och AUC på liknande sätt, dvs. med 30 % respektive 20 %. Intag tillsammans med föda minskar eventuellt gastrointestinala biverkningar.
Effekt av P-gp-transportörer på elacestrant
Elacestrant är ett substrat till P-gp. Transporten är mättad i dosen 258 mg och 345 mg. Eftersom det inte finns några kliniska data tillgängliga om elacestrant i de lägre doserna 86 mg respektive 172 mg administrerat samtidig med en P-gp-hämmare, kan det inte uteslutas att samtidig administrering med en P-gp-hämmare ökar absorptionen vid lägre doser elacestrant.
Distribution
Plasmaproteinbindningen för elacestrant är > 99 % och oberoende av koncentration och leverstatus. Elacestrant penetrerar blod-hjärnbarriären på ett dosberoende sätt. Efter administrering av elacestrant en gång dagligen i 7 dagar i följd var mediankoncentrationerna av elacestrant i cerebrospinalvätskan 0,0966 ng/ml och 0,155 ng/ml vid doserna 200 respektive 500 mg.
Baserat på populationsfarmakokinetisk analys distribueras elacestrant i stor utsträckning i vävnaderna med en skenbar perifer distributionsvolym på 5 411 liter. Den skenbara centrala distributionsvolymen för elacestrant vid steady state är 422 liter.
Metabolism
Elacestrant var en mindre beståndsdel (< 10 % av plasmaradioaktivitet) i human plasma. 4-[2-(etylamino)etyl]bensoesyra (EAEBA)-glukuronid var en stor metabolit i human plasma (cirka 41 % av plasmaradioaktivitet). Elacestrant metaboliseras främst av CYP3A4 med eventuellt viss delaktighet från CYP2A6 och CYP2C9.
Eliminering
Halveringstiden för elacestrant beräknas vara cirka 30 timmar. Efter en engångsdos var den genomsnittliga (% CV) elimineringen av elacestrant 220,3 l/h (38,4 %). Vid steady state beräknas den genomsnittliga (% CV) elimineringen av elacestrant vara 186 l/h (43,5 %).
Efter en oral engångsdos på 345 mg radiomärkt elacestrant återfanns 81,5 % (majoriteten oförändrat) i faeces och 7,53 % (spår som oförändrat) återfanns i urinen. Njurclearance för elacestrant är mycket låg (≤ 2,3 ml/min) och det eliminerades genom oxidativ metabolism och fekal utsöndring.
Särskilda populationer
Effekt av ålder, vikt och kön
Baserat på analyser av populationsfarmakokinetiska data från cancerpatienter motiveras ingen dosjustering utifrån kroppsvikt, ålder eller kön.
Nedsatt leverfunktion
Cmax- och AUC-värdena var likartade mellan deltagarna i gruppen med lindrigt nedsatt leverfunktion (Child-Pugh A) och gruppen med normal leverfunktion vid administrering av 176 mg elacestrant som engångsdos. Det förekom betydande ökningar av AUC0–t (76 %) och AUC0–∞ (83 %) hos gruppen med måttligt nedsatt leverfunktion (Child-Pugh B) jämfört med gruppen med normal leverfunktion. Värdena för Cmax var likartade mellan grupperna med normal funktion och måttligt nedsatt funktion.
Det geometriska medelvärdet för elimineringshalveringstiden (t1/2) tenderade att öka med stigande svårighetsgrad på nedsatt leverfunktion. Elacestrant har inte studerats hos deltagare med svårt nedsatt leverfunktion (Child-Pugh C).
Vid PBPK-modelleringssimulering av elacestrant vid 345 mg förväntades AUC och Cmax vid steady state öka med 2,14 respektive 1,92 gånger hos deltagare med måttligt nedsatt leverfunktion jämfört med patienter med normal leverfunktion.
Prekliniska säkerhetsuppgifter
Elacestrant uppvisade låg akut toxicitet. I dostoxicitetsstudier med upprepad dos hos råttor och apor gav den antiestrogena aktiviteten hos elacestrant upphov till de effekter som sågs, i synnerhet i det kvinnliga fortplantningssystemet, men även i andra organ som är känsliga för hormoner såsom bröstkörtlar, hypofys och testiklar. Sporadiska kräkningar och diarré registrerades hos apor. I långsiktiga studier (26 veckor på råttor och 39 veckor på krabbmakaker) observerades dessutom ökad vakuolisering av mukosalt epitel i den icke-glandulära magen hos råttor och vakuolerade makrofaginfiltrat i tunntarmen noterades hos både råttor och apor. Hos apor uppstod denna effekt vid systemisk exponering på cirka 70 % av den humana exponeringen.
Elacestrant visade ingen gentoxisk potential i Ames test, kromosomavvikelser i humana lymfocyter och vid mikronukleusanalys på råttor.
Fertilitetsstudier på djur har inte utförts. I toxicitetsstudier med upprepad dos observerades effekter relaterade till fertiliteten i fortplantningsorganen hos råttor och apor. Dessa effekter uppträdde under mänsklig exponering vid MRHD (maximal rekommenderad dos). Minskad cellularitet hos Leydig-celler i råttestiklar observerades också vid exponeringsnivåer som var 2,7 gånger högre än för människor.
I studier av embryo-/fosterutveckling hos råttor ledde oral administrering av elacestrant till maternell toxicitet (minskad kroppsvikt, lågt födointag, röda flytningar från vulva) och ökade resorptioner, ökade missfall efter implantation och minskat antal levande foster samt fostervariationer och missbildningar under human exponering vid MHRD.
Farmaceutiska uppgifter
Förteckning över hjälpämnen
Tablettkärna
Mikrokristallin cellulosa [E460]
Kiselifierad mikrokristallin cellulosa
Krospovidon [E1202]
Magnesiumstearat [E470b]
Kolloidal kiseldioxid [E551]
Filmdragering
Opadry II 85F105080 Blue innehållande polyvinylalkohol [E1203], titandioxid [E171], makrogol [E1521], talk [E553b] och briljantblått FCF aluminiumlake [E133]
Inkompatibiliteter
Ej relevant.
Hållbarhet
3 år
Särskilda förvaringsanvisningar
Inga särskilda förvaringsanvisningar.
Förpackningstyp och innehåll
Markkinoilla olevat pakkaukset
Resepti
ORSERDU tabletti, kalvopäällysteinen
86 mg (L:ei) 28 fol (1821,81 €)
345 mg (L:ei) 28 fol (6763,60 €)
PF-selosteen tieto
ORSERDU är förpackat i aluminium-aluminiumblister förpackade i en kartong.
ORSERDU 86 mg filmdragerade tabletter
Förpackningar med 28 filmdragerade tabletter: 4 blister med 7 tabletter i varje
ORSERDU 345 mg filmdragerade tabletter
Förpackningar med 28 filmdragerade tabletter: 4 blister med 7 tabletter i varje
Läkemedlets utseende:
ORSERDU 86 mg filmdragerade tabletter
Blå till ljusblå bikonvex, rund filmdragerad tablett präglad med ”ME” på ena sidan och slät yta på den andra sidan. Ungefärlig diameter: 8,8 mm.
ORSERDU 345 mg filmdragerade tabletter
Blå till ljusblå bikonvex, oval filmdragerad tablett präglad med ”MH” på ena sidan och slät yta på den andra sidan. Ungefärlig storlek: 19,2 mm (längd), 10,8 mm (bredd).
Särskilda anvisningar för destruktion och övrig hantering
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.
Ersättning
ORSERDU tabletti, kalvopäällysteinen
86 mg 28 fol
345 mg 28 fol
- Rajoitettu peruskorvaus lääkärin lausunnolla (40 %). Elasestrantti: Postmenopausaalisten naisten sekä miesten hormonireseptoripositiivisen ja HER2-negatiivisen paikallisesti edenneen tai etäpesäkkeisen rintasyövän hoito monoterapiana erityisin edellytyksin (3105).
Atc-kod
L02BA04
Yhteystiedot
Basisweg 10
1043 AP Amsterdam
Noord-Holland, Nederland
+45 2815 7816
www.menarini.com
srana@menarinistemline.com
