TIOTROPIUM STADA inhalationspulver, hård kapsel 18 mikrog
Kvalitativ och kvantitativ sammansättning
Varje kapsel innehåller 22,5 mikrogram tiotropiumbromidmonohydrat motsvarande 18 mikrogram tiotropium.
Den levererade dosen (dosen som lämnar munstycket på inhalatorn Vertical-Haler) är 10 mikrogram tiotropium.
Hjälpämne med känd effekt
Varje kapsel innehåller 5,204 mg laktos (som monohydrat)
För fullständig förteckning över hjälpämnen, se avsnitt Förteckning över hjälpämnen.
Läkemedelsform
Inhalationspulver, hård kapsel.
Kliniska uppgifter
Terapeutiska indikationer
Tiotropium Stada är en bronkdilaterare för underhållsbehandling för lindring av symtom hos patienter med kroniskt obstruktiv lungsjukdom (KOL).
Dosering och administreringssätt
Dosering
Den rekommenderade doseringen av tiotropiumbromid är inhalation av innehållet i en kapsel en gång per dygn via inhalatorn Vertical-Haler vid ungefär samma tidpunkt. Du måste andas in 2 gånger från samma kapsel.
Den rekommenderade dosen bör inte överskridas.
Tiotropium Stada ska endast inhaleras via inhalatornVertical-Haler.
Speciella patientgrupper:
Äldre
Äldre patienter kan använda tiotropium i rekommenderad dos.
Nedsatt njurfunktion
Patienter med nedsatt njurfunktion kan använda tiotropium i rekommenderad dos. För patienter med måttlig till svår njurfunktionsnedsättning (kreatininclearance ≤50 ml/min), se avsnitt Varningar och försiktighet samt avsnitt Farmakokinetiska egenskaper.
Nedsatt leverfunktion
Patienter med nedsatt leverfunktion kan använda tiotropium i rekommenderad dos (se avsnitt Farmakokinetiska egenskaper).
Pediatrisk population
KOL
Det finns ingen relevant användning för en pediatrisk population (under 18 år) för indikationen enligt avsnitt Terapeutiska indikationer.
Cystisk fibros
Säkerhet och effekt för Tiotropium Stada hos barn och ungdomar har inte fastställts. Inga data finns tillgängliga.
Administreringssätt:
Endast för inhalation.
Kapslen får inte sväljas.
Kapseln ska tas ut blistret omedelbart innan inhalatorn används!
För att säkerställa korrekt administrering av läkemedlet ska patienten tränas, av läkaren eller annan sjukvårdspersonal, i hur inhalatorn används.
Instruktioner för hantering och användning:
Patienten måste rådas att noggrant följa läkarens instruktioner för användning av Tiotropium Stada. Vertical-Haler är speciellt utformad för Tiotropium Stada. Det får inte användas för att ta något annat läkemedel. Vertical-Haler kan användas för att ta läkemedlet i upp till 90 dagar.
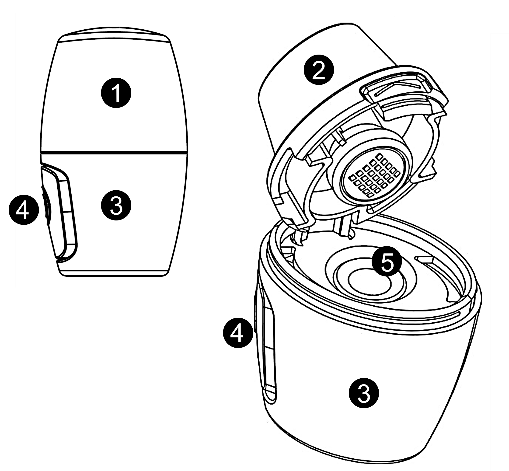 | Vertical-Haler - förklaring av olika delar 1 Skyddslock 2 Munstycke 3 Underdel 4 Tryckknapp 5 Kapselkammare |
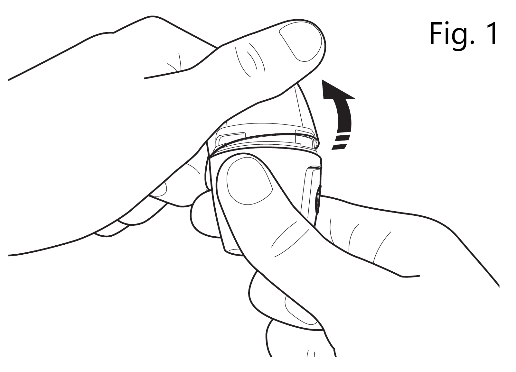 | 1. Ta bort skyddslocket Håll Vertical-Haler inhalatorn och lyft locket uppåt från underdelen för att exponera munstycket som visas (Fig. 1). |
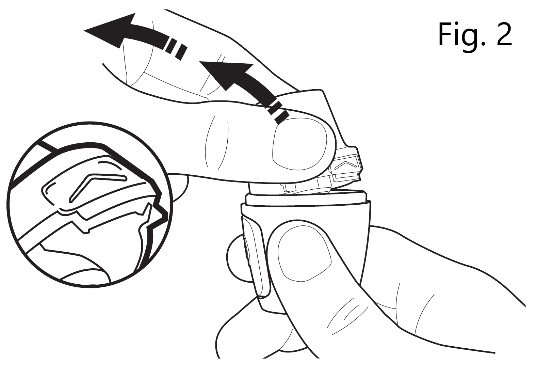 | 2. Öppna För att öppna Vertical-Haler inhalatorn, håll ett fast grepp om underdelen. Tryck på området markerad med "˄" (som visas på den förstorade bilden) med fingerspetsen. Öppna inhalatorn genom att dra munstycket uppåt från underdelen enligt bilden (Fig. 2). |
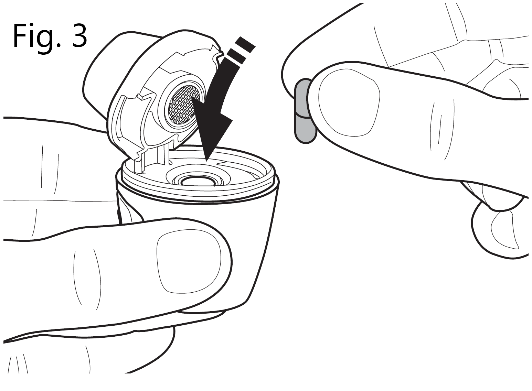 | 3. Sätta in kapseln Håll den öppnade Vertical-Haler inhalatorn med skyddslocket uppåt. Placera kapseln i kammaren i inhalatorns underdel (fig. 3). Observera: Kapseln ska tas ur blisterförpackningen omedelbart före inhalatorn används. |
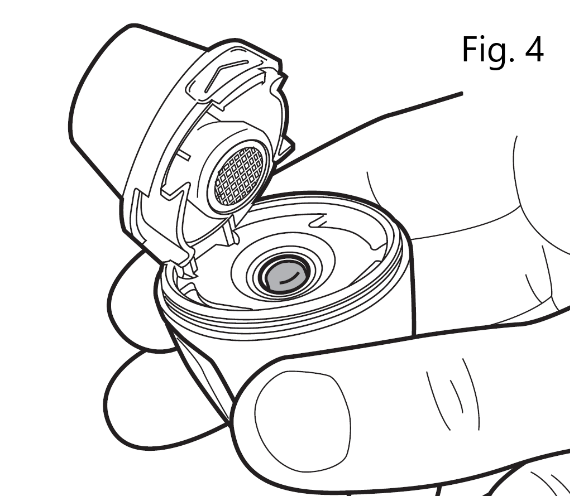 | Se till att kapseln är korrekt isatt (fig. 4). |
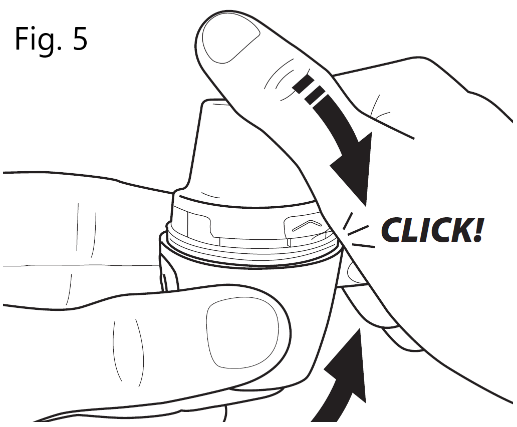 | 4. Stäng munstycket Stäng munstycket bestämt mot underdelen tills du hör ett "klick" (Fig. 5). |
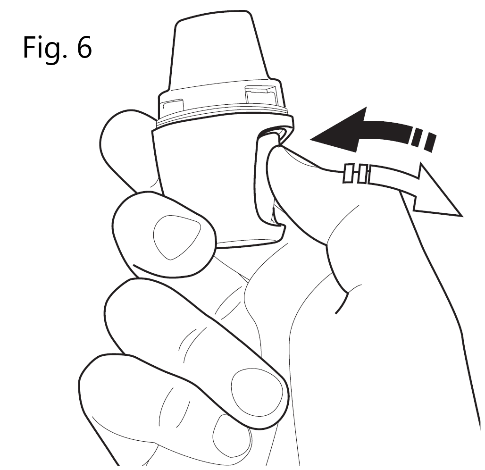 | 5. Punktera kapseln Håll Vertical-Haler inhalatorn med munstycket uppåt. Tryck med ett bestämt tryck in knappen en gång tills den är helt dold (fig. 6). Släpp knappen åter. Därigenom gör du hål i kapseln så att läkemedlet frigörs vid inandning. Observera: Om du behöver upprepa steg 5, öppna kapselkammaren (fig. 2) för att se till att kapseln är korrekt isatt (fig. 4). |
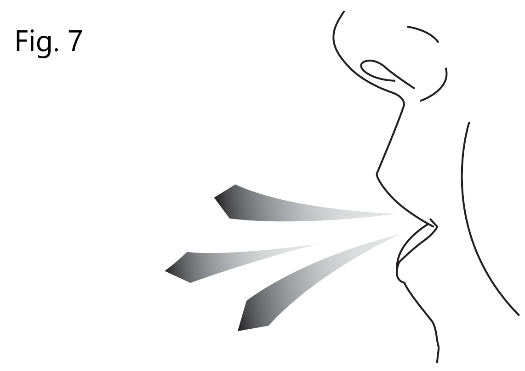 | 6. Förbered dig för användning Håll Vertical-Haler bort från munnen och andas ut för att tömma lungorna på luft. (Fig. 7) Andas inte ut genom din Vertical-Haler. |
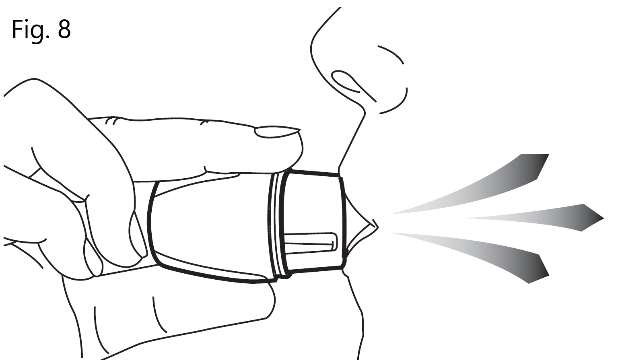 | 7. Inandning Håll ditt nästa andetag med huvudet i upprätt läge, Slut läpparna tätt runt munstycket. Andas in tillräckligt långsamt och djupt (fig. 8). Du kommer att höra ett vibrerande ljud av kapseln som roterar inuti kapselkammaren för att sprida läkemedlet. Andas in tills lungorna är fulla; håll sedan andan så länge det känns bekvämt och ta samtidigt bort Vertical-Haler från munnen. Återgå till normal andning. Upprepa steg 6 och 7 en gång till. Du måste andas in 2 gånger från samma kapsel. |
Observera: När du håller inhalatorn under inhalation, se till att inte blockera luftvägarna på sidorna av munstycket. Detta kan hindra luften att flöda inuti inhalatorn, vilket minskar kapselns rörelser och läkemedelsspridningen. Tryck inte ner munstycket under inandning. Detta kan blockera kapselns rörelse. | |
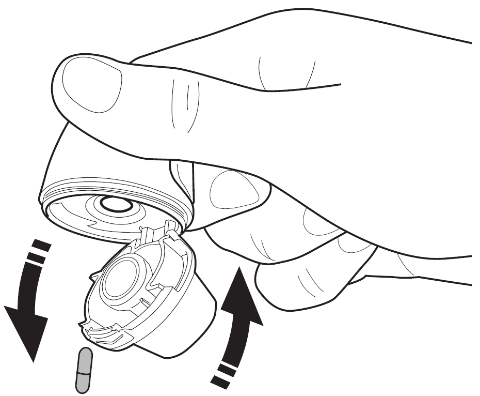 | Rengöring av din Vertical-Haler Öppna munstycket efter användning. Håll inhalatorn nedåt för att hälla ut kapseln från kapselkammaren. Rengör munstycket och kapselkammaren med en ren, torr trasa. Alternativt kan en mjuk, ren borste användas för att ta bort pulverrester inuti kapselkammaren. Stäng munstycket och sätt på locket. Detta kommer att hålla pulverinhalatorn ren och torr. Vid behov kan utsidan av munstycket rengöras med en fuktig trasa. |
Kapslarna innehåller endast en liten mängd pulver och är därför endast delvis fyllda.
Kontraindikationer
Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt Förteckning över hjälpämnen eller mot atropin eller dess derivat, t.ex. ipratropium eller oxitropium.
Varningar och försiktighet
Tiotropium är en bronkdilaterare för underhållsbehandling en gång per dygn. Det ska inte användas för inledande behandling vid akuta attacker av bronkospasm, t ex som vid behovsbehandling.
Omedelbara överkänslighetsreaktioner kan möjligen uppträda efter tillförsel av tiotropiumbromid inhalationspulver.
Som med andra läkemedel med antikolinerg aktivitet ska tiotropiumbromid användas med försiktighet hos patienter med trångvinkelglaukom, prostatahyperplasi eller blåshalsförträngning (se avsnitt Biverkningar).
Inhalationsläkemedel kan orsaka inhalationsutlöst bronkospasm.
Insättning av tiotropium ska ske med försiktighet till patienter som haft hjärtinfarkt under det senaste halvåret; någon form av instabil eller livshotande hjärtarytmi eller hjärtarytmi som krävt intervention eller förändring av läkemedelsbehandlingen det senaste året; sjukhusinläggning på grund av hjärtsvikt (NYHA klass III eller IV) under det senaste året. Dessa patienter exkluderades från de kliniska prövningarna och dessa tillstånd kan påverkas av den antikolinerga verkningsmekanismen.
Eftersom plasmakoncentrationen ökar med minskad njurfunktion hos patienter med måttlig till svår njurfunktionsnedsättning (kreatininclearance ≤50 ml/min) ska tiotropium användas endast om den förväntade nyttan uppväger den potentiella risken. Det finns ingen erfarenhet av långtidsbehandling av patienter med svår njurfunktionsnedsättning (se avsnitt Farmakokinetiska egenskaper).
Patienterna ska uppmärksammas på att de ska undvika att få pulver i ögonen. De ska informeras om att detta kan utlösa eller förvärra trångvinkelglaukom, framkalla smärta eller obehag i ögonen; övergående dimsyn, halo- eller färgfenomen tillsammans med röda ögon beroende på svullnad i konjunktiva och ödem i kornea. Patienterna ska avbryta behandlingen med tiotropiumbromid och kontakta läkare omedelbart om en kombination av några av dessa ögonsymtom uppträder.
Muntorrhet till följd av antikolinergika kan vid långtidsbehandling öka risken för karies.
Tiotropiumbromid ska inte användas oftare än en gång per dygn (se avsnitt Överdosering).
Hjälpämnen
Tiotropium Stada innehåller laktos. Patienter med något av följande sällsynta ärftliga tillstånd bör inte använda detta läkemedel: galaktosintolerans, total laktasbrist eller glukos-galaktosmalabsorption.
Hjälpämnet laktosmonohydrat kan innehålla små mängder av mjölkprotein som kan orsaka allergiska
reaktioner.
Interaktioner
Någon formell interaktionsstudie har inte genomförts. Tiotropiumbromid inhalationspulver har dock använts tillsammans med andra läkemedel utan kliniska tecken på interaktioner. De läkemedel som använts är beta-agonister, metylxantiner, orala och inhalerade steroider; dvs läkemedel som ofta används vid behandling av KOL.
Samtidig användning av långverkande beta-agonister (LABA) eller inhalerade kortikosteroider har inte setts påverka exponeringen av tiotropium.
Samtidig tillförsel av tiotropiumbromid och andra antikolinerga läkemedel har inte undersökts och rekommenderas därför inte.
Fertilitet, graviditet och amning
Graviditet
Det finns mycket begränsade data från användning av tiotropium hos gravida kvinnor. Djurstudier visar inte på några direkta eller indirekta skadliga effekter avseende reproduktionstoxicitet vid kliniskt relevanta doser (se avsnitt Prekliniska säkerhetsuppgifter). Som en försiktighetsåtgärd bör Tiotropium Stada helst inte användas under graviditet.
Amning
Det är okänt om tiotropiumbromid utsöndras i bröstmjölk. Trots att studier på gnagare har visat att utsöndringen av tiotropiumbromid i bröstmjölk är begränsad, rekommenderas inte användning av tiotropium i samband med amning. Tiotropiumbromid är en långverkande substans. Ett beslut att antingen fortsätta/avbryta amningen eller att fortsätta/avbryta behandlingen med tiotropium skall tas med hänsyn till barnets behov av bröstmjölk och moderns behov av behandling med tiotropium.
Fertilitet
Kliniska data avseende fertilitet saknas för tiotropium. Pre-kliniska studier med tiotropium visade inte några tecken på negativ påverkan på fertiliteten (se avsnitt Prekliniska säkerhetsuppgifter).
Effekter på förmågan att framföra fordon och använda maskiner
Inga studier har utförts beträffande förmågan att framföra fordon och använda maskiner. Förekomst av yrsel, dimsyn och huvudvärk kan inverka på förmågan att framföra fordon och använda maskiner.
Biverkningar
Sammanfattning av biverkningsprofilen
Många av biverkningarna kan hänföras till de antikolinerga egenskaperna hos Tiotropium Stada.
Sammanfattning av biverkningar i tabellform
Frekvensen av biverkningar som anges nedan baseras på incidens av biverkningar (dvs händelser som ansetts orsakade av tiotropium), som observerades i tiotropium-gruppen (9 647 patienter) i 28 poolade placebo-kontrollerade, kliniska studier med behandlingsperioder från 4 veckor upp till fyra år.
Biverkningar är listade efter organklass och frekvens. Frekvenserna definieras enligt följande konvention: Mycket vanliga (≥1/10); vanliga (≥1/100, <1/10); mindre vanliga (≥1/1 000, <1/100); sällsynta (≥1/10 000, <1/1 000); mycket sällsynta (<1/10 000); ingen känd frekvens (kan inte beräknas från tillgängliga data).
Organklass/MedDRA ”Preferred Term” | Frekvens |
Immunsystemet | |
Överkänslighet (inkl. omedelbara reaktioner) | Sällsynta |
Anafylaktisk reaktion | Ingen känd frekvens |
Metabolism och nutrition | |
Dehydrering | Ingen känd frekvens |
Centrala och perifera nervsystemet | |
Yrsel | Mindre vanliga |
Huvudväk | Mindre vanliga |
Smakförändring | Mindre vanliga |
Sömnlöshet | Sällsynta |
Ögon | |
Dimsyn | Mindre vanliga |
Glaukom | Sällsynta |
Ökat intraokulärt tryck | Sällsynta |
Hjärtat | |
Förmaksflimmer | Mindre vanliga |
Supraventrikulär takykardi | Sällsynta |
Takykardi | Sällsynta |
Palpitationer | Sällsynta |
Andningsvägar, bröstkorg, mediastinum | |
Faryngit | Mindre vanliga |
Dysfoni | Mindre vanliga |
Hosta | Mindre vanliga |
Bronkospasm | Sällsynta |
Näsblödning | Sällsynta |
Laryngit | Sällsynta |
Sinuit | Sällsynta |
Magtarmkanalen | |
Muntorrhet | Vanliga |
Gastroesofagal refluxsjukdom | Mindre vanliga |
Förstoppning | Mindre vanliga |
Oral candidainfektion | Mindre vanliga |
Tarmobstruktion inkl. paralytisk ileus | Sällsynta |
Gingivit | Sällsynta |
Flossit | Sällsynta |
Svårigheter att svälja | Sällsynta |
Stomatit | Sällsynta |
Illamående | Sällsynta |
Dental karies | Ingen känd frekvens |
Hud och subkutan vävnad | |
Hudutslag | Mindre vanliga |
Urtikaria | Sällsynta |
Klåda | Sällsynta |
Angioödem | Sällsynta |
Hudinfektion, hudulcerationer | Ingen känd frekvens |
Torr hud | Ingen känd frekvens |
Muskuloskeletala systemet och bindväv | |
Ledsvullnad | Ingen känd frekvens |
Njurar och urinvägar | |
Svårighet att tömma urinblåsan | Mindre vanliga |
Urinretention | Mindre vanliga |
Urinvägsinfektion | Sällsynta |
Beskrivning av vissa biverkningar
I kontrollerade kliniska studier var de vanligaste biverkningarna antikolinerga biverkningar som muntorrhet, som förekom hos ca 4 % av patienterna.
I de 28 kliniska studierna medförde muntorrhet att behandlingen avbröts hos 18 av de 9 647 patienter som behandlades med tiotropium (0,2 %).
Allvarliga biverkningar förenliga med antikolinerga effekter, inkluderar glaukom, förstoppning och tarmobstruktion inklusive paralytisk ileus liksom urinretention.
Övriga speciella patientgrupper
En ökad antikolinergisk effekt kan förekomma med ökande ålder.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta-riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning till:
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Överdosering
Höga doser tiotropium kan leda till antikolinerga symtom.
Det förekom dock inga systemiska antikolinerga biverkningar efter en engångsdos av 340 mikrogram tiotropiumbromid via inhalation till friska försökspersoner. Dessutom fann man inga relevanta biverkningar, frånsett muntorrhet, vid 7 dagars tillförsel av upp till 170 mikrogram tiotropiumbromid till friska försökspersoner. I en studie med upprepad dosering till KOL-patienter med maximalt 43 mikrogram tiotropiumbromid/dygn under 4 veckor, uppträdde inga signifikanta biverkningar.
Akut intoxikation genom oavsiktligt oralt intag av tiotropiumbromid kapslar kan inte förväntas, pga. låg oral biotillgänglighet.
Farmakologiska egenskaper
Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: Övriga medel vid obstruktiva luftvägssjukdomar, inhalationer, antikolinergika. ATC-kod: R03B B04
Verkningsmekanism
Tiotropium är en långverkande, specifik muskarin-receptor-antagonist, som i klinisk praxis oftast kallas antikolinergikum. Genom bindning till de muskarina receptorerna i bronkernas glatta muskulatur, hämmar tiotropium den kolinerga (bronkkonstriktiva) effekten av acetylkolin, som frisätts från de parasympatiska nervändarna. Den har liknande affinitet till subtyperna av muskarina receptorer M1 till M5. I luftvägarna hämmar tiotropium kompetitivt och reversibelt M3-receptorn, vilket leder till relaxering. Effekten var dosberoende och varade mer än 24 timmar. Den långa effektdurationen beror troligen på den mycket långsamma frisättningen från M3-receptorn, som leder till en signifikant längre dissociationshalveringstid än den man sett med ipratropium. Som ett N-kvartärt antikolinergikum är tiotropium lokalt (bronk) selektivt vid tillförsel via inhalation, med en acceptabel terapeutisk bredd innan det ger upphov till systemiska antikolinerga effekter.
Farmakodynamisk effekt
Den bronkdilaterande effekten är primärt en lokal effekt i luftvägarna, inte en systemisk effekt. Dissociationen från M2-receptorn är snabbare än från M3, vilket i in vitro studier åstadkommer (kinetiskt kontrollerad) receptor subtyp-selektivitet för M3 över M2. Den kraftiga effekten och långsamma receptordissociationen motsvarar kliniskt den signifikanta och långverkande bronkdilatationen hos patienter med KOL.
Kardiell elektrofysiologi
Elektrofysiologi: I en särskild QT-studie på 53 friska frivilliga personer gav 18 mikrogram och 54 mikrogram tiotropium (dvs tre gånger den terapeutiska dosen) under 12 dagar ingen förlängning av QT-intervallet på EKG.
Klinisk effekt och säkerhet
Det kliniska prövningsprogrammet innehöll fyra ett-årsstudier och två sex-månadersstudier, alla randomiserade och dubbel-blinda, som totalt inkluderade 2663 patienter (1308 fick tiotropium). De studier som pågick ett år utgjordes av två placebokontrollerade studier och två studier med en aktiv kontroll (ipratropium). I de två sex-månadersstudierna användes både salmeterol och placebo som jämförelse. Man studerade lungfunktion och hälsorelaterade parametrar som dyspné, exacerbationer och hälsorelaterad livskvalitet.
Lungfunktion
Tiotropium tillfört en gång per dygn förbättrade lungfunktionen signifikant (forcerad expiratorisk volym under första sekunden, FEV1 och forcerad vitalkapacitet, FVC) inom 30 minuter efter första dosen och effekten bibehölls under 24 timmar. Farmakodynamiskt steady state uppnåddes inom en vecka med maximal bronkdilatation från dag 3. Tiotropium förbättrade signifikant PEFR (Peak Expiratory Flow Rate) morgon och kväll vid patientens dagliga mätningar. Den bronkdilaterande effekten av tiotropium bibehölls under en ettårig behandlingsperiod utan några tecken på toleransutveckling.
En randomiserad, placebokontrollerad klinisk studie av 105 KOL-patienter visade att bronkdilatationen bibehölls under dosintervallet 24 timmar, jämfört med placebo, oberoende av om läkemedlet administrerades på morgonen eller kvällen.
Kliniska studier (upp till 12 månader)
Dyspné, ansträngningstolerans
Tiotropium förbättrade signifikant dyspnén hos patienter, utvärderat enligt Transition Dyspnoea Index. Förbättringen bibehölls under behandlingstiden.
Betydelsen av minskad dyspné vid ansträngning undersöktes i två randomiserade, dubbelblinda, placebokontrollerade studier med 433 patienter med medelsvår till svår KOL. I dessa studier gav 6 veckors behandling med tiotropium signifikant förbättring av symtombegränsande belastningstid vid cykelergonometri vid 75 % av maximal arbetskapacitet med 19,7 % (Studie A) respektive 28,3 % (Studie B) jämfört med placebo.
Hälsorelaterad livskvalitet
I en 9-månaders randomiserad, dubbelblind, placebokontrollerad studie med 492 patienter förbättrade tiotropium den hälsorelaterade livskvaliteten, bestämd som totalpoäng av St. George’s Respiratory Questionnaire (SGRQ). Andelen patienter som behandlades med tiotropium som erhöll en betydelsefull förbättring i SGRQ totalpoäng (dvs >4 enheter) var 10,9% högre jämfört med placebo (59,1% i tiotropium-gruppen jämfört med 48,2% i placebogruppen (p=0,029)). Medelvärdet för skillnaden mellan grupperna var 4,19 enheter (p=0,001; konfidensintervall:1,69-6,68). Förbättringen av SGRQ undergrupper var 8,19 enheter för ”symtom”, 3,91 enheter för ”aktivitet” och 3,61 enheter för ”påverkan på dagligt liv”. Förbättringen av dessa separata undergrupper var statistiskt signifikant.
KOL-exacerbationer
I en randomiserad, dubbelblind, placebokontrollerad studie med 1 829 patienter med måttlig till mycket svår KOL ledde tiotropium till statistiskt signifikant minskning av andelen patienter som fick exacerbationer av KOL (från 32,2% till 27,8%) samt statistiskt signifikant färre exacerbationer, en minskning med 19% (från 1,05 till 0,85 fall per exponerat patientår). Dessutom var andelen patienter inlagda på sjukhus pga exacerbationer av KOL, 7,0% i tiotropiumgruppen och 9,5% i placebogruppen (p=0,056). Antalet sjukhusinläggningar pga KOL minskade med 30% (från 0,25 till 0,18 fall per exponerat patientår).
En randomiserad, dubbelblind, dubbel-dummy-studie på ett år med parallella grupper jämförde effekten av behandlingen med tiotropium 18 mikrogram en gång dagligen med salmeterol inhalationsspray 50 mikrogram två gånger dagligen på incidensen av medelsvåra till svåra exacerbationer hos 7 376 patienter med KOL med exacerbationer i anamnesen föregående år.
Tabell 1: Sammanfattning av effektmått vid exacerbationer
| Effektmått | Tiotropium 18 mikrogram (inhalationspulver) N=3 707 | Salmeterol 50 mikrogram (inhalationsspray) N=3 669 | Kvot (95% KI) | p-värde |
| Tid [dagar] till första exacerbation1 | 187 | 145 | 0,83 (0,77-0,90) | <0,001 |
| Tid till första svåra (kräver sjukhusvård) exacerbation2 | - | - | 0,72 (0,61-0,85) | <0,001 |
| Patiener med ≥1 exacerbation, n (%)3 | 1277 (34,4) | 1414 (38,5) | 0,90 (0,85-0,95) | <0,001 |
| Patienter med ≥1 svår (kräver sjukhusvård) exacerbation, n (%)3 | 262 (7,1) | 336 (9,2) | 0,77 (0,66-0,89) | <0,001 |
1 Tid [dagar] avser första kvartilen patienter. Tid till händelseanalys gjordes med hjälp av Cox proportionella riskmodell med centrea (poolade) och behandling som kovariater. Kvoten avser riskkvot.
2 Tid till händelseanalys gjordes med hjälp av Cox's proportionella riskmodell med centra (poolade) och behandling som kovariabler. Kvoten avser riskkvot. Tid [dagar] för första kvartilen patienter kunde inte beräknas då andelen patienter med svåra exacerbationer var för låg.
3 Antal patienter med händelser analyserades med hjälp av Cochran-Mantel-Haenszels test stratifierat per centra (poolad). Kvoten avser riskkvot.
Jämfört med salmeterol ökade tiotropium tid till första exacerbation (187 dagar jämfört med 145 dagar) med en 17%-ig reduktion av risken (riskkvot 0,83, 95 % konfidensintervall (KI) 0,77 - 0,90, p <0,001). Tiotropium ökade också tiden till första svåra (kräver sjukhusvård) exacerbation (riskkvot 0,72, 95% KI 0,61 - 0,85, p <0,001).
Långtidsstudier (över 1 år, upp till 4 år)
I en randomiserad, dubbelblind, placebokontrollerad klinisk studie med 5 993 randomiserade patienter (3 006 i placebogruppen och 2 987 i tiotropium-gruppen) som behandlades under 4 år bibehölls förbättringen i FEV1 vid behandling med tiotropium jämfört med placebo, konstant under 4 års behandling. En större andel av patienterna i tiotropium-gruppen fullföljde ≥45 månaders behandling än i placebogruppen (63,8% respektive 55,4%, p <0,001). Den årliga försämringen av FEV1 jämfört med placebo var likartad mellan tiotropium och placebo. Under pågående behandling reducerades risken för dödsfall med 16%. Incidensen av dödsfall var 4,79 per 100 patientår i placebogruppen jämfört med 4,10 per 100 patientår i tiotropium-gruppen (riskkvot tiotropium/placebo = 0,84, 95% konfidensintervall = 0,73; 0,97). Behandling med tiotropium reducerade risken för respiratorisk svikt (noterat via biverkningsrapporter) med 19% (2,09 respektive 1,68 fall per 100 patientår, relativ risk tiotropium/placebo = 0,81, 95% konfidensintervall = 0,65; 0,999).
Tiotropium-aktiv kontrollstudie
En storskalig randomiserad, dubbelblind långtidsstudie med aktiv kontroll, med en observationstid på upp till 3 år har genomförts för att jämföra effekt och säkerhet hos tiotropium inhalationspulver och tiotropium inhalationslösning (5 694 patienter fick tiotropium inhalationspulver; 5 711 patienter fick tiotropium inhalationslösning). De primära effektvariablerna var tid till första KOL-exacerbation, mortalitet oavsett orsak och i en undergrupp (906 patienter) dal-FEV1 (före dos).
Tid till första KOL-exacerbation var numeriskt likvärdig under studien med tiotropium inhalationspulver och tiotropium, inhalationsvätska, inhalator (riskkvot tiotropium inhalationspulver/tiotropium, inhalationsvätska, inhalator) 1,02 med 95 % KI på 0,97 till 1,08). Medianen för antal dagar till första KOL-exacerbation var 719 dagar för tiotropium inhalationspulver och 756 dagar för tiotropium, inhalationsvätska, inhalator.
Den bronkdilaterande effekten för tiotropium inhalationspulver bibehölls under 120 veckor, och var liknande den för tiotropium, inhalationsvätska, inhalator. Den genomsnittliga skillnaden av dal-FEV1 för tiotropium inhalationspulver jämfört med tiotropium, inhalationsvätska, inhalator var 0,010 liter (95 % KI -0,018 till 0,038 liter).
I en studie efter marknadsintroduktion, TIOSPIR-studien, där tiotropium, inhalationsvätska, inhalator jämfördes mot tiotropium inhalationspulver, var riskkvoten för mortalitet av alla orsaker (inklusive uppföljning av vital status) lika (riskkvot (tiotropium inhalationspulver/tiotropium, inhalationsvätska, inhalator) 1,04 med 95% KI på 0,91-1,19).
Pediatrisk population
Europeiska läkemedelsmyndigheten har beviljat undantag från kravet att skicka in studieresultat för referensläkemedlet som innehåller tiotropium, för alla grupper av den pediatriska populationen för KOL och cystisk fibros (information om pediatrisk användning finns i avsnitt Dosering och administreringssätt).
Farmakokinetiska egenskaper
Allmän introduktion
Tiotropium är en icke-kiral kvartär ammoniumförening som har begränsad löslighet i vatten. Tiotropium administreras som inhalationspulver. Vid inhalation deponeras huvuddelen av den tillförda dosen i mag-tarmkanalen och en mindre del i målorganet, lungan. Många av de farmakokinetiska uppgifter som beskrivs nedan har framkommit vid högre dosering än den som rekommenderas för behandling.
Allmän beskrivning av den aktiva substansen efter tillförsel av läkemedlet
Absorption
Efter inhalation av inhalationspulver hos unga friska försökspersoner uppvisade tiotropium en biotillgänglighet av 19,5 %, vilket tyder på att den fraktion som når lungorna är höggradigt biotillgänglig. Orala lösningar av tiotropium har en absolut biotillgänglighet på 2-3%. Maximal plasmakoncentration av tiotropium uppmättes 5-7 minuter efter inhalation.
Vid steady state var maximala plasmakoncentrationen av tiotropium hos KOL-patienter 12,9 pg/ml och minskade snabbt enligt flerkompartmentkinetik. Dalvärdeskoncentrationen vid steady state var 1,71 pg/ml. Systemisk exponering för tiotropium efter inhalation av tiotropium inhalationspulver liknade inhalation av tiotropium inhalationsvätska.
Distribution
Tiotropium har en plasmaproteinbindning på 72% och uppvisar en distributionsvolym på 32 liter/kg. Koncentrationen i lungan är inte känd, men administreringsvägen gör att man förväntar avsevärt högre koncentrationer i lungan. Studier på råtta har visat att tiotropium inte passerar blod-hjärn-barriären i någon större utsträckning.
Metabolism
Tiotropium metaboliseras i liten utsträckning. 74% av en intravenös dos utsöndras oförändrat i urin hos friska försökspersoner. Estern tiotropium klyvs på icke enzymatisk väg till alkohol (N-metylskopin) och syra (ditienylglykol-syra) som båda är inaktiva på muskarinreceptorer. In vitro studier i humana levermikrosomer och hepatocyter antyder att en mindre andel av läkemedlet (<20% av dosen efter intravenös tillförsel) metaboliseras genom cytokrom P450(CYP)-beroende oxidation med åtföljande glutation-konjugering till ett antal fas II-metaboliter.
In vitro-studier i levermikrosomer visar att dessa mindre viktiga enzymatiska metabolismvägar, kan hämmas av CYP2D6 (och 3A4)-hämmare, kinidin, ketokonazol och gestoden. Alltså spelar CYP2D6 och 3A4 en roll i den metabolismväg som leder till eliminering av en mindre del av dosen. Tiotropium hämmar inte CYP 1A1, 1A2, 2B6, 2C9, 2C19, 2D6, 2E1 eller 3A i humana levermikrosomer, ens i koncentrationer högt över de terapeutiska.
Eliminering
Efter inhalation var den effektiva halveringstiden för tiotropium mellan 27-45 timmar hos KOL-patienter. Total clearance var 880 ml/min efter intravenös dosering till unga friska försökspersoner. Intravenöst administrerad tiotropium utsöndras huvudsakligen oförändrat via urinen (74%). Efter inhalation av inhalationspulver hos KOL-patienter vid steady state var urinutsöndringen 7 % (1,3 mikrogram) av oförändrad substans under 24 timmar. Återstoden var framför allt substans som ej absorberats utan eliminerades via faeces. Renalt clearance av tiotropium överskrider kreatininclearance, vilket tyder på aktiv sekretion i njurarna. Efter upprepad inhalation en gång dagligen till KOL-patienter uppnås farmakokinetiskt steady state dag 7 utan ytterligare ackumulering.
Linjäritet/ icke-linjäritet
Tiotropium uppvisar linjär farmakokinetik i det terapeutiska området oberoende av beredningsform.
Speciella patientgrupper
Äldre: Liksom för alla läkemedel som främst utsöndras renalt, kan stigande ålder relateras till minskat renalt clearance för tiotropium (365 ml/min hos KOL-patienter yngre än 65 år till 271 ml/min hos KOL-patienter äldre ≥ 65 år). Detta medförde ingen motsvarande ökning av AUC0-6, ss eller Cmax, ss.
Nedsatt njurfunktion: Efter daglig inhalation av tiotropium till steady state hos KOLpatienter, gav lätt nedsättning av njurfunktionen (CLCR 50-80 ml/min) en något högre AUC0-6, ss (mellan 1,8-30 % högre) och Cmax, ss–värden som var jämförbara med patienter med normal njurfunktion (CLCR >80 ml/min).
Hos KOL-patienter med måttlig till kraftigt nedsatt njurfunktion (CLCR <50 ml/min) ledde intravenös administrering av tiotropium till dubblerad total exponering (82 % högre AUC0-4h och 52% högre Cmax) jämfört med KOL-patienter med normal njurfunktion, vilket bekräftades av plasmakoncentrationer efter tillförsel av inhalationspulver.
Nedsatt leverfunktion: Leverinsufficiens förväntas inte ha någon relevant inverkan på farmakokinetiken för tiotropium. Tiotropium utsöndras främst genom renal eliminering (74% hos unga friska försökspersoner) och genom icke-enzymatisk esterklyvning till farmakologiskt inaktiva produkter.
Japanska KOL-patienter: I en jämförelse mellan studier var den genomsnittliga maximala plasmakoncentrationen av tiotropium 10 minuter efter administrering vid steady state 20 till 70% högre hos japanska patienter jämfört med kaukasiska KOL-patienter efter inhalation av tiotropium, men ingen ökad mortalitet eller kardiell risk syntes för japanska patienter jämfört med kaukasier. Farmakokinetiska data för andra etniska grupper är otillräckliga.
Pediatrisk population: Se avsnitt Dosering och administreringssätt.
Farmakokinetiskt / farmakodynamiskt förhållande
Det finns inget direkt samband mellan farmakokinetik och farmakodynamik.
Prekliniska säkerhetsuppgifter
Många effekter som observerades i konventionella studier av säkerhetsfarmakologi, toxicitetsstudier med upprepad dosering och reproduktionsstudier kunde förklaras med de antikolinerga egenskaperna hos tiotropium. Typiska effekter hos djuren var minskat födointag, minskad ökning av kroppsvikten, torr mun och näsa, minskat tårflöde och salivutsöndring, mydriasis och takykardi. Andra relevanta effekter som observerades i toxicitetsstudier med upprepad dosering var en lindrig irritation i luftvägarna hos råtta och mus (rinit och förändringar i epitelet i näshålan och struphuvudet) samt prostatit med avseende på proteindeposition och stenbildning i urinblåsan hos råtta.
Skadliga effekter med hänsyn till graviditet, embryonal/fetal utveckling, förlossning eller postnatal utveckling kunde endast visas vid doser som var toxiska för moderdjuren. Tiotropium hade inga teratogena effekter hos råtta eller kanin. I en allmän reproduktions- och fertilitetsstudie i råtta sågs inga negativa effekter på fertilitet eller parningsförmåga hos behandlade råttor eller deras avkomma, oavsett dos.
Förändringarna i luftvägarna (irritation) och urogenitala organ (prostatit) samt reproduktionstoxikologiska effekter observerades vid lokal eller systemisk tillförsel av mer än 5 gånger den terapeutiska dosen. Studier av genotoxicitet och karcinogen potential visade inga speciella risker för människor.
Farmaceutiska uppgifter
Förteckning över hjälpämnen
Kapselinnehåll:
Laktosmonohydrat (som kan innehålla små mängder mjölkprotein)
Kapselskal:
Gelatin (E441)
Renat vatten
Makrogol 4000 (E1521)
Titandioxid (E171)
Gul järnoxid (E172)
Briljantblått (E133)
Inkompatibiliteter
Ej relevant.
Hållbarhet
2 år.
Kassera inhalatorn 90 dagar efter första användning.
Kapseln ska användas omedelbart efter öppnande av blistret.
Särskilda förvaringsanvisningar
Förvaras vid högst 30 °C.
Förvaringsanvisningar för läkemedlet efter öppnande finns i avsnitt Hållbarhet.
Förpackningstyp och innehåll
Markkinoilla olevat pakkaukset
Resepti
TIOTROPIUM STADA inhalaatiojauhe, kapseli, kova
18 mikrog (L:kyllä) 30 fol (Vertical-Haler) (15,54 €), 30 fol (15,54 €), 90 fol (Vertical-Haler) (53,42 €)
PF-selosteen tieto
Värmeförseglad aluminium-/aluminium-blister som innehåller 5 eller 10 kapslar.
Vertical-Haler är en endosinhalator tillverkad av plastmaterialet akrylnitril-butadien-styren (ABS) och rostfritt stål. Material som kommer i direkt kontakt med produkten vid tidpunkten för inandning är: rostfritt stål 304 (nålar som tränger igenom kapseln), akrylnitril-butadien-styren-ABS (bildar munstycket genom vilket läkemedlet strömmar och kapselkammaren).
Förpackningsstorlekar:
- Kartong innehållande Vertical-Haler inhalator och 10 kapslar
- Kartong innehållande Vertical-Haler inhalator och 15 kapslar
- Kartong innehållande Vertical-Haler inhalator och 30 kapslar
- Kartong innehållande Vertical-Haler inhalator och 60 kapslar
- Kartong innehållande Vertical-Haler inhalator och 90 kapslar
- Sjukhusförpackning: Kartong innehållande Vertical-Haler inhalator och 5x30 kapslar (multipeltförpackning)
- Kartong innehållande två Vertical-Haler inhalatorer och 60 kapslar
- Kartong innehållande tre Vertical-Haler inhalatorer och 90 kapslar
- Sjukhusförpackning: Kartong innehållande 5x60 kapslar (multipeltförpackning)
- Kartong innehållande 30 kapslar
- Kartong innehållande 60 kapslar
- Kartong innehållande 90 kapslar
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Läkemedlets utseende:
Ogenomskinlig, grön kapsel med en storlek på 16 mm x 5,8 mm innehållande inhalationspulvret.
Särskilda anvisningar för destruktion och övrig hantering
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.
Ersättning
TIOTROPIUM STADA inhalaatiojauhe, kapseli, kova
18 mikrog 30 fol, 30 fol, 90 fol
- Alempi erityiskorvaus (65 %). Krooninen keuhkoastma ja sitä läheisesti muistuttavat krooniset obstruktiiviset keuhkosairaudet (203).
- Peruskorvaus (40 %).
- Varmista antolaitteen ja käyttöpakkauksen yhteensopivuus lääkettä vaihdettaessa.
Atc-kod
R03BB04
Datum för översyn av produktresumén
27.06.2024
Yhteystiedot
PL 1310, Puolikkotie 8, 02230 Espoo (käyntiosoite)
00101 Helsinki
0207 416 888
