CIFOBAN infuusioneste, liuos 136 mmol/l
Vaikuttavat aineet ja niiden määrät
Cifoban-pussissa on 1 500 ml käyttövalmista liuosta.
1 000 ml liuosta sisältää:
Natriumsitraattia 40,0 g
Na+ 408 mmol
Sitraatti3- 136 mmol
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Infuusioneste, liuos
Kehonulkoisesti. Annetaan vain kehonulkoiseen verenkiertoon.
Teoreettinen osmolariteetti: 544 mOsm/l
pH: 7,1–7,5
Kliiniset tiedot
Käyttöaiheet
Cifoban-valmistetta käytetään paikalliseen sitraattiantikoagulaatioon jatkuvan venovenoosisen hemodialyysin, jatkuvan venovenoosisen hemodiafiltraation, pitkän matala-annoksisen (päivittäisen) dialyysin ja terapeuttisen plasmanvaihdon yhteydessä, kun plasma erotellaan kalvolla.
Cifoban on tarkoitettu käytettäväksi aikuisten ja kaikenikäisten lasten hoidossa (lukuun ottamatta ennenaikaisia vastasyntyneitä).
Annostus ja antotapa
Cifoban-valmistetta saa määrätä vain sellainen lääkäri, jolla on pätevyys hoitaa sitraattiantikoagulaatiota indikaation mukaisissa hoitomuodoissa. Lapsipotilaille saa hoidon Cifoban-valmisteella aloittaa ja seurata lääkäri, jolla on pätevyys toteuttaa edellä mainittuja hoitoja.
Annostus
Aikuiset
Cifoban-valmisteen suodatinta edeltävä infuusionopeus titrataan niin, että se on suhteessa veren virtaukseen kehonulkoisessa kierrossa, jotta saavutetaan riittävä veren ionisoituneen kalsiumin esto suodattimessa käytettävän sitraattiantikoagulaation hoito-ohjelman mukaisesti. Yleensä tavoitteena pitää olla, että suodattimen jälkeinen ionisoituneen kalsiumin pitoisuus on alle 0.3–0,35 mmol/l. Tämä saavutetaan tavallisesti käyttämällä annostusta 4–5 mmol sitraattia / verilitra. Tarvittava Cifoban-virtaus (ml/min) voidaan laskea kertomalla sitraattiannos verenkierron virtauksella (ml/min) ja jakamalla se 136 millimoolilla per litra (mmol/l, eli Cifoban-valmisteen sitraattikonsentraatiolla). Potilaan systeeminen ionisoituneen kalsiumin pitoisuus pitää säilyttää normaalilla fysiologisella vaihteluvälillä, mihin yleensä tarvitaan kalsiumlisän antamista.
Cifoban-valmisteen antomäärä ei aikuisille potilaille saa ylittää 10,4 litraa vuorokaudessa. Kehonulkoisen verenvirtauksen pitää olla riittävä, jotta hoidon tavoitteet saavutetaan, mutta niin pieni, että vältetään tarpeeton sitraatti-infuusio ja edistetään sitraatin poistumista käytettävästä suodattimesta. Tällä pienennetään sitraattiylikuormituksen kehittymisen ja sitraatin elimistöön kertymisen riskiä (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet). Jos veren virtaus on suurempi ja Cifoban-valmisteen annostus on pienempi, suodattimen auki pysyminen voi tarpeettomasti heikentyä. Käytettävän hoito-ohjelman mukaisen dialyysi- ja korvausliuosten koostumuksen suhteen pitää harkita sellaisten liuosten käyttöä, jotka eivät sisällä kalsiumia ja sisältävät vähän natriumia ja bikarbonaattia. Ne pitää valita ottaen huomioon Cifoban-valmisteeseen liittyvä natriumin ja puskurin anto käytettävän hoito-ohjelman mukaisesti.
Kalsiumia sisältämätöntä dialyysiliuosta pitää harkita erityisesti, kun kyseessä on jatkuvasti annettu hoito. Kalsiumia sisältävää dialyysiliuosta voidaan harkita pitkän matala-annoksisen (päivittäisen) dialyysin yhteydessä, kun sopivaa kalsiumia sisältämätöntä liuosta ei ole käytettävissä. Tällaisessa tapauksessa voidaan hyväksyä suurempi suodattimen jälkeinen ionisoituneen kalsiumin pitoisuus, kun hoitoaika on suhteellisen lyhyt, tai vaihtoehtoisesti Cifoban-valmistetta voidaan antaa niin, että sen pitoisuus hoidettavaa verilitraa kohden on suurempi. Suurempi suodattimen jälkeinen ionisoituneen kalsiumin pitoisuus voi olla mahdollinen myös terapeuttisen plasmanvaihdon yhteydessä, erityisesti silloin kun korvausliuos sisältää sitraattia (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet). Tällaisessa tapauksessa Cifoban-valmistetta pitää antaa niin, että pitoisuus hoidettavaa verilitraa kohden on pienempi.
Kun sitraattia käytetään yhdessä sellaisen kalsiumia sisältämättömän jatkuvan venovenoosisen hemodialyysinesteen tai jatkuvan venovenoosisen hemodiafiltraationesteen kanssa, jonka natriumpitoisuus on 133 mmol/l ja bikarbonaattipitoisuus on 20 mmol/l, vereen ennen dialyysisuodatinta lisätyn sitraatin määrän tavoite pitää olla 3–5 mmol/verilitra jatkuvan venovenoosisen hemodialyysin aikana ja 3−5,5 mmol/verilitra jatkuvan venovenoosisen hemodiafiltraation aikana. Vastaavia annostusohjeita voidaan soveltaa muihin hoito-ohjelmiin.
Erityisryhmät
Potilaat, joiden sitraattimetabolia on heikentynyt
Cifoban-valmistetta voidaan käyttää sellaisten potilaiden hoidossa, joilla on sitraattimetabolian heikentymisen riski (esim. sokki ja siihen liittyvä vaikea maitohappoasidoosi, vaikea maksan vajaatoiminta).
Hoito pitää aloittaa käyttämällä riittävän pientä sitraattiannosta.
Kun jatkuvan venovenoosisen hemodialyysin tai jatkuvan venovenoosisen hemodiafiltraation hoidossa verenvirtaus on enintään 100–200 ml/min, sitraattikuorma pysyy yleensä riittävän pienenä. Sitraattiannostus voidaan aloittaa käyttämällä annosta 4–5 mmol/verilitra, hoito-ohjelman mukaisesti, ja sitä on ehkä tarpeen pienentää vain siinä tapauksessa, että ilmenee selviä merkkejä sitraatin kertymisestä elimistöön (ks. lisätietoja kohdasta Varoitukset ja käyttöön liittyvät varotoimet).
Kun pitkän matala-annoksisen (päivittäisen) dialyysihoidon yhteydessä verenvirtaus on enintään noin 150–200 ml/min, dialysaatin virtaus on vähintään sama ja hoidon kesto on enintään 12 tuntia, potilaan sitraattikuorma pysyy yleensä riittävän pienenä. Kun käytetään kalsiumia sisältävää dialysaattia, sitraatin anto voidaan aloittaa käyttämällä enintään annosta 6–7 mmol/verilitra, hoito-ohjelman mukaisesti, ja sitä on ehkä tarpeen pienentää vain siinä tapauksessa, että ilmenee selviä merkkejä sitraatin kertymisestä elimistöön (ks. lisätietoja kohdasta Varoitukset ja käyttöön liittyvät varotoimet).
TPE-hoidossa sitraatin puhdistuma suodattimesta on yleensä rajallista ja suhteellisesti vähäisempää, mikä johtuu suurimmista hyväksytyistä filtraatiofraktioista. Altistus sitraatille voi lisääntyä edelleen, kun vaihdossa käytetään jääplasmaa. Kun vaihto tehdään käyttämällä jääplasmaa, suositeltu verenvirtaus on enintään 100–120 ml/min. Sitraatin anto voidaan aloittaa käyttämällä annosta 3−4 mmol/verilitra, hoito-ohjelman mukaisesti, ja sitä on ehkä tarpeen pienentää vain siinä tapauksessa, että ilmenee selviä merkkejä sitraatin kertymisestä elimistöön (ks. lisätietoja kohdasta Varoitukset ja käyttöön liittyvät varotoimet).
Kaikkien näiden hoitojen yhteydessä suositellaan tehostettua seurantaa sitraatin elimistöön kertymisen ehkäisemiseksi (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Iäkkäät potilaat
Iäkkäillä potilailla voi olla sitraattimetabolian heikentymisen riski. Annoksen muuttaminen ei ole tarpeen. Tiheää seurantaa suositellaan sitraatin elimistöön kertymisen havaitsemiseksi (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Pediatriset potilaat
Cifoban-valmisteen turvallisuutta ja tehoa ennenaikaisten vastasyntyneiden hoidossa ei ole vielä varmistettu. Käytettävissä olevat tiedot ovat riittämättömiä (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Cifoban-valmistetta voidaan käyttää kaikkiin ikäryhmiin kuuluvien lasten hoidossa (täysiaikaisista vastasyntyneistä nuoriin), kun potilaan sitraattikuorma pysyy riittävän pienenä. On huomattava, että pienimmistä potilaista on käytettävissä vain hyvin vähän tietoa. Hoidossa käytettävien laitteiden ja tarvittavan pienten verenvirtausten on oltava potilaan painon mukaan hoitoon sopivia.
Verenvirtausta ja sitraattiannosta koskevat ohjeet ikäryhmien mukaan
- Vastasyntyneet−taaperoikäiset (0–23 kuukautta): jos käytettävien laitteiden takia tarvitaan verenvirtausta nopeudella 7–8 ml/kg/min (tai enemmän), sitraatin anto aloitetaan noin annoksella 3 mmol/verilitra.
- Lapset (2−11-vuotiaat): verenvirtaus saa olla enintään 5−6 ml/kg/min; sitraatin anto voidaan aloittaa noin annoksella 4 mmol/verilitra, hoito-ohjelman mukaisesti.
- Nuoret (12–17-vuotiaat): verenvirtauksen pitää olla riittävä, jotta saavutetaan hoidon tavoitteet, eikä se yleisesti ottaen saa olla suurempi kuin samanpainoisilla aikuisilla. Sitraatin anto voidaan aloittaa noin annoksella 4 mmol/verilitra, hoito-ohjelman mukaisesti.
Annettavaa sitraatin määrää voi olla tarpeen pienentää, jos ilmenee selviä merkkejä sitraatin kertymisestä elimistöön (ks. lisätietoja kohdasta Varoitukset ja käyttöön liittyvät varotoimet). Jatkuvan venovenoosisen hemodialyysin tai jatkuvan venovenoosisen hemodiafiltraation hoidossa tavoitellaan mieluiten suodattimen jälkeistä ionisoidun kalsiumin pitoisuutta alle 0,3–0,35 mmol/l, mutta tämä tavoite riippuu toteutettamiskelpoisesta sitraattiannoksesta.
Tehostettu seuranta sitraattiylikuormituksen kehittymisen ja sitraatin elimistöön kertymisen ehkäisemiseksi (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet) on tarpeen vastasyntyneiden ja taaperoikäisten hoidon yhteydessä ja suositeltavaa lapsille ja nuorille. Lisäksi on otettava huomioon yllä mainittu, annostusta koskeva harkinta tapauksissa, kun potilaan sitraattimetabolia on heikentynyt. Kun vaihdossa käytetään jääplasmaa, kohtuullinen vaihtonopeus on tarpeen potilaan sitraattikuorman rajoittamiseksi. Samanaikaisesti suositellaan kalsiumin korvausta, jotta säilytetään normaali systeeminen ionisoidun kalsiumin pitoisuus.
Alla olevassa taulukossa kerrotaan suurimmat infuusionopeudet täysiaikaisista vastasyntyneistä nuoriin. On huomattava, että tyypilliset vuorokausittaiset antomäärät pysyvät selvästi näiden rajojen alapuolella sen seurauksena, että käytetään yllä kuvattuja maltillisia verenvirtauksia.
| Paino (kg) | Suurin antomäärä (litraa/vrk) |
| 2,5 | 1,6 |
| 3 | 1,9 |
| 5 | 2,2 |
| 10 | 3,2 |
| 20 | 4,9 |
| 30 | 6,4 |
| 40 | 8,5 |
| 50 ja yli | 10,4 |
Antotapa
Kehonulkoisesti. Annetaan vain kehonulkoiseen verenkiertoon.
Infuusio voidaan antaa vain sellaisen kehonulkoiseen verenpuhdistuslaitteeseen sisäänrakennetun pumpun avulla, joka on valmistajan mukaan tarkoitettu väkevän sitraattiliuoksen antamiseen letkuston ennen pumppua olevassa osassa, jotta pienennetään tahattoman yliannostuksen riskiä (ks. kohta Yliannostus). Laitteen pitää myös poistaa Cifoban-neste ulos virtaavaan nesteeseen nesteylikuormituksen ehkäisemiseksi (ks. kohta Haittavaikutukset).
Kohdassa Varoitukset ja käyttöön liittyvät varotoimet mainitut varoitukset ja käyttöön liittyvät varotoimet, erityisesti seurantaa ja lisäksi annettavan korvauksen tarvetta koskevat kohdat, pitää ottaa huomioon.
Lisäksi:
- Cifoban-valmistetta saa käyttää vain asianmukaisen paikalliseen sitraattiantikoagulaatioon soveltuvan hoito-ohjelman mukaisesti. Valmistetta saa käyttää ainoastaan lääkäri, jolla on pätevyys käyttää paikallista sitraattiantikoagulaatiota sekä terveydenhuollon ammattilaiset, jotka on riittävän hyvin koulutettu antamaan kyseisiä hoitoja ja annostelemaan hoitoihin liittyviä valmisteita, tai tällaisten henkilöiden valvonnassa.
- Käytettävän kehonulkoisen verenpuhdistuslaitteen käyttöohjeita pitää noudattaa ja valmistajan toimittamaa letkustojärjestelmää pitää käyttää.
- Cifoban-valmistetta voidaan käyttää paikalliseen sitraattiantikoagulaatioon tehohoitoyksikössä tai vastaavissa olosuhteissa, joissa hoitohenkilökunnan pitää valvoa hoitoa huolellisesti ja seurata sitä jatkuvasti.
Katso ohjeet lääkevalmisteen käsittelystä ennen sen antamista kohdasta Käyttö- ja käsittelyohjeet.
Vasta-aiheet
- Yliherkkyys vaikuttavalle aineelle
- Tiedossa oleva vaikea sitraattimetabolian heikentyminen (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet Sitraatin kertyminen elimistöön heikentyneen metabolian takia)
Varoitukset ja käyttöön liittyvät varotoimet
Varoitukset
Potilaan muuttuneiden seerumiarvojen seurantatiheydet
Mainittujen hoitojen yhteydessä edellytetään potilaan hemodynaamisen tilan, nestetasapainon, glukoosipitoisuuden, elektrolyytti- ja happo-emästasapainon tarkkaa seurantaa ennen hoidon aloittamista ja hoidon aikana. Seurannan täsmällinen tiheys riippuu potilaan tilasta ja siitä, miten nopeasti hoidolla saadaan aikaan muutoksia potilaan veren tilavuuteen ja koostumukseen: esimerkiksi terapeuttisessa plasmanvaihdossa nämä muutokset voivat tapahtua nopeammin kuin jatkuvassa venovenoosisessa hemodialyysissa. Potilaan hoito-ohjelma ja paikallisen sitraattiantikoagulaation hoito-ohjelma pitää laatia tämän mukaisesti.
Cifoban-valmisteen käytössä voidaan noudattaa seuraavia seurantatiheyksiä ja seurantaan liittyviä seikkoja:
- Potilaan ionisoitu kalsium, pH ja bikarbonaatti, natrium- ja laktaattitasot kliinisen tarpeen mukaan, on mitattava ennen ja vähintään tunnin kuluttua hoidon aloittamisesta. Jatkomittauksiin sopivat tiheydet ovat terapeuttisessa plasmanvaihdossa tunneittain, pitkässä matala-annoksisessa (päivittäisessä) dialyysissä 3−4 tunnin välein sekä jatkuvassa venovenoosisessa hemodialyysissä ja jatkuvassa venovenoosisessa hemodiafiltraatiossa enintään 6−8 tunnin välein.
- Balansoituja liuoksia käytettäessä magnesiumin ja kokonaiskalsiumin mittaus ennen hoitoa ja hoidon jälkeen (terapeuttinen plasmanvaihto, pitkä matala-annoksinen (päivittäinen) dialyysi) tai vuorokausittain (jatkuva venovenoosinen hemodialyysi, jatkuva venovenoosinen hemodiafiltraatio) voi olla riittävä.
- Tehostetumpi seuranta pitää toteuttaa yleensä 2−4 kertaa tiheämmin.
- Verikaasuanalysaattori on oltava välittömästi käytettävissä.
- Erillinen valtimoyhteys on suositeltava näytteenottokohta. Letkustoon on usein saatavissa portti näytteenottoa varten, mutta sen käyttö voi kuitenkin aiheuttaa vääriä mittaustuloksia, jos katetrin päässä tapahtuu takaisinkiertoa.
Jos kierron ionisoidun kalsiumin seuranta kuuluu noudatettavaan paikallisen sitraattiantikoagulaation hoito-ohjelmaan, tarvitaan sitä varten näytteenottoportti. Paikallisessa sitraattiantikoagulaatiossa voidaan edellyttää ensimmäistä mittausta 20−30 minuutin kuluessa hoidon aloituksesta, jolloin vahvistetaan, että kierto toimii oikein. Seuraavat mittaukset tehdään jokaisen Cifoban-valmisteen annoksen muuttamisen jälkeen (odota > 5 minuuttia säädön jälkeen ennen näytteen ottoa, jotta saat uuden ionisoituneen kalsiumin pitoisuuden oikein).
Sitraatin kertyminen elimistöön heikentyneen metabolian takia
Kun lapsi- tai aikuispotilailla on heikentynyt sitraattimetabolia, esimerkiksi heikentyneen maksan toiminnan, hypoksian (hypoksemian) tai häiriintyneen happiaineenvaihdunnan takia, paikallinen sitraattiantikoagulaatio voi johtaa sitraatin kertymiseen elimistöön. Sen merkkejä ovat ionisoituneen kalsiumin pitoisuuden liiallinen pieneneminen, kalsiumin korvaustarpeen lisääntyminen, kokonaiskalsiumin ja ionisoituneen kalsiumin suhteen suureneminen arvon 2,25 yli ja/tai metabolinen asidoosi. Varhainen merkki voi olla mm. laktaatin puhdistuman väheneminen hoidon aikana. Sen jälkeen voi olla tarpeen lisätä dialysaatin virtausta, vähentää sitraattiannostusta tai lopettaa Cifoban-valmisteen käyttö antikoagulaatioon. Tehostettua seurantaa suositellaan.
Sitraattiylikuormitus
Cifoban on hyponatreeminen ja metaboloiduttuaan bikarbonaatin lähde. Kun päätetään muiden paikallisen sitraattiantikoagulaation hoito-ohjelmaan kuuluvien nesteiden koostumuksesta, vähän natriumia ja vähän bikarbonaattia sisältävät valmisteet ovat parempia (ks. lisätietoja kohdasta Annostus ja antotapaAnnostus ja antotapa). On kuitenkin mahdollista, että potilaalle kehittyy hoidosta johtuva alkaloosi ja hypernatremia, ja niitä voidaan hoitaa vähentämällä verenvirtausta tai, käytettävän paikallisen sitraattiantikoagulaation hoito-ohjelman niin salliessa, lisäämällä dialysaatin virtausta. Nämä toimenpiteet vähentävät potilaan natriumsitraattikuormaa. Metabolista alkaloosia voidaan hoitaa myös antamalla kontrolloidusti infuusiona 0,9-prosenttista natriumkloridia. Hypernatremiaa voidaan myös hoitaa antamalla kontrolloidusti infuusiona esimerkiksi 5-prosenttista glukoosiliuosta. Molemmissa tapauksissa hoitavan lääkärin on otettava huomioon lisävolyymikuorma.
Suodattimen tukkeutuminen (eli suodattimen läpäisevyyden väheneminen) voi johtaa sitraattiylikuormitukseen. Suodattimen tukkeutuminen voi vähentää kalsiumin, sitraatin, natriumin ja muiden aineiden poistumista ja johtaa hyperkalsemiaan, metaboliseen alkaloosiin, hypernatremiaan ja muihin poikkeamiin odotetuista hoidon vaikutuksista. Tällaisessa tilanteessa ei todennäköisesti enää ole mahdollista korjata poikkeavuuksia yllä mainituilla keinoilla. Silloin pitää vaihtaa suodatin.
Lääkevalmisteen tahattoman yliannostuksen tapahtuessa katso lisätietoja kohdasta Yliannostus.
Riittämätön sitraattikuorma
Jos muut paikallisen sitraattiantikoagulaation hoito-ohjelmassa käytetyt liuokset ylikompensoivat natrium- ja bikarbonaattipuskurin saantia Cifoban-valmisteesta, potilaalle voi kehittyä hoidosta johtuva metabolinen asidoosi ja hyponatremia. Näitä seerumin epätasapainoja voidaan hoitaa lisäämällä verenvirtausta tai, käytettävän paikallisen sitraattiantikoagulaation hoito-ohjelman niin salliessa, vähentämällä dialysaatin virtausta. Nämä toimenpiteet lisäävät potilaan natriumsitraattikuormaa. Lisäksi sitkeää metabolista asidoosia ja hyponatremiaa voidaan hoitaa antamalla kontrolloidusti infuusiona natriumvetykarbonaattiliuosta.
Potilaan pidentynyt immobilisaatio
Paikallisen sitraattiantikoagulaation aikana kalsiumin infuusionopeuden väheneminen voi peittää ionisoituneen kalsiumin määrän suurenemiseen viittaavan varhaisen merkin. Erityisesti tilanteissa, joissa potilas joutuu olemaan pitkään paikallaan, voi tapahtua luun uudelleen muotoutumista/demineralisaatiota, joka johtaa kalsiumin vapautumiseen luista. Tämä voi lopulta johtaa luunmurtumiin. Jos potilasta hoidetaan paikallisella sitraattiantikoagulaatiolla jatkuvasti yli 2 viikon ajan tai jos kalsiumin fuusionopeus vähenee asteittain, luun uusiutumista kuvaavia merkkiaineita pitäisi seurata tarkasti.
Hyytyminen varhaisessa vaiheessa paikallisesta sitraattiantikoagulaatiosta huolimatta
Veren hyytymistä voi tapahtua varhaisessa vaiheessa paikallisesta sitraattiantikoagulaatiosta huolimatta, kun potilaan veren hyytyminen on (tai epäillään olevan) lisääntynyt (esim. hepariinin aikaansaama tyypin II trombosytopenia). Tällöin voidaan tarvita asianmukaisesti valittua systeemistä antikoagulanttia. Myös paikallista sitraattiantikoagulaatiota voidaan käyttää parantamaan edelleen suodattimen auki pysymistä.
Varotoimet
Mitokondriaalista toimintahäiriötä aiheuttavat myrkytykset
Potilaita, joilla on tunnettu vaikea mitokondriaalinen toimintahäiriö (esim. parasetamoli- ja metformiinimyrkytys), voi olla parempi hoitaa vaihtoehtoisen antikoagulaatiohoito-ohjelman mukaisesti, jotta pienennetään sitraatin elimistöön kertymisen riskiä (ks. lisätietoja kohdasta Varoitukset ja käyttöön liittyvät varotoimet yllä). Jos Cifoban-hoito aloitetaan, on noudatettava kohdassa Annostus ja antotapa mainittua erityisryhmien annostusta.
Olemassa oleva hypokalsemia
Kriittisesti sairailla potilailla voi olla hypokalsemiaa. Käytettäessä paikallista sitraattiantikoagulaatiota systeemisen ionisoituneen kalsiumin pitoisuus voi laskea hoidon ensimmäisten tuntien aikana. Pitoisuus palautuu myöhemmin. Tämän vuoksi olemassa oleva hypokalsemia on parempi hoitaa ennen toimenpiteen aloittamista. Tällä pienennetään hoidon aloittamisen jälkeen ilmenevän kliinisesti merkittävän hypokalsemian riskiä.
Kompleksien muodostuminen ja kalsiumin ja magnesiumin puhdistuminen
Sitraatti kelatoi kalsium- ja magnesiumioneja, jotka voivat aiheuttaa hypokalsemiaa eliminoituessaan myöhemmin suodattimessa (ks. kohdat Haittavaikutukset ja Yliannostus) ja/tai hypomagnesemiaa (ks. kohta Haittavaikutukset). Kalsiuminfuusio hypokalsemian korjaamiseksi on usein vakiokäytäntö, ja magnesiumlisä voi myös olla tarpeen. Kompensaatiotarpeen pitää kuulua paikallisen sitraattiantikoagulaation hoito-ohjelmaan.
Verivalmisteiden korvaus (terapeuttinen plasmanvaihto)
Sitraattia sisältävät veriplasmavalmisteet, kuten jääplasma, kuuluvat yleisesti osana terapeuttisen plasmanvaihdon hoito-ohjelmaan kriittisesti sairailla potilailla. Sitraattikuorman lisäksi verivalmisteet voivat myös olla hypernatreemisia. Tästä johtuen sekä sitraatin elimistöön kertymisen että sitraattiylikuormituksen riski ovat suurentuneet (ks. yllä). Näiden tilojen hoidon pitää kuulua paikallisen sitraattiantikoagulaation hoito-ohjelmaan.
Yhteisvaikutukset
Tuotekohtaiset yhteisvaikutukset
Cifoban-valmisteen aineosien ei odoteta aiheuttavan farmakodynaamisia yhteisvaikutuksia. Yhteisvaikutuksia voidaan odottaa vain siinä tapauksessa, että liuosta käytetään riittämättöminä määrinä tai väärään käyttöaiheeseen (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Yliannostus).
Yhteisvaikutus- tai yhteensopivuustutkimuksia muiden lääkevalmisteiden kanssa ei ole tehty. Näin ollen Cifoban-valmisteeseen ei saa lisätä muita aineita tai liuoksia (ks. myös kohta Yhteensopimattomuudet).
Suodattimen tasolla tai ennen dialysaattoria annetut kalsiumia sisältävät liuokset (esim. dialyysineste) voivat heikentää Cifoban-valmisten tehoa.
Yhteisvaikutukset ovat mahdollisia käytettäessä natriumilla rikastettuja tuotteita, jotka voivat suurentaa hypernatermian riskiä (ks. kohta Haittavaikutukset). Vastaavasti vetykarbonaattia sisältävät tuotteet (tai vetykarbonaattia metaboloituessaan tuottavat esiasteet, esim. asetaatti) voivat suurentaa suuren vetykarbonaattipitoisuuden riskiä veressä (metabolinen alkaloosi, ks. kohta Haittavaikutukset). Vastaavasti sitraattia sisältävät verivalmisteet voivat suurentaa veren suurentuneen sitraattipitoisuuden riskiä (hypokalsemia, metabolinen asidoosi, ks. kohta Haittavaikutukset) ja veren suuren vetykarbonaattipitoisuuden riskiä (metabolinen alkaloosi, ks. kohta Haittavaikutukset).
Raskaus ja imetys
Raskaus ja imetys
Ei ole olemassa tietoja Cifoban-valmisteen käytöstä raskaana oleville tai imettäville naisille.
Ei ole tehty riittäviä eläinkokeita lisääntymistoksisuuden selvittämiseksi.
Cifoban-valmistetta ei pidä käyttää raskauden eikä imetyksen aikana, ellei naisen kliininen tilanne edellytä hoitoa paikallisella sitraattiantikoagulaatiolla.
Hedelmällisyys
Ihmisillä tehdyistä kokeista saatuja tietoja natriumin ja sitraatin vaikutuksesta hedelmällisyyteen ei ole saatavilla.
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Ei merkityksellinen
Haittavaikutukset
Cifoban-liuoksen käyttö tai dialyysihoito voi aiheuttaa haittavaikutuksia.
Haittavaikutukset on listattu otsikoiden alle esiintymistiheyden mukaan käyttäen seuraavaa luokittelua:
| Hyvin yleinen | ≥ 1/10 |
| Yleinen | ≥ 1/100, < 1/10 |
| Melko harvinainen | ≥ 1/1 000, < 1/100 |
| Harvinainen | ≥ 1/10 000, <1/1 000 |
| Hyvin harvinainen | < 1/10 000 |
| Tuntematon | saatavissa oleva tieto ei riitä esiintyvyyden arviointiin |
| Elinjärjestelmäluokka | Esiintymistiheys | Haittavaikutukset (suositeltu termi) |
| Immuunijärjestelmä | Tuntematon | Yliherkkyys |
| Aineenvaihdunta ja ravitsemus | Hyvin yleinen | Hypokalsemia (< 1,1 mmol/l) (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet) |
Hypernatremia (> 145 mmol/l) (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet) | ||
Metabolinen alkaloosi (pH > 7,45) (ks. sitraattiylikuormitus kohdassa Varoitukset ja käyttöön liittyvät varotoimet) | ||
| Yleinen | Vaikea hypokalsemia (< 0,9 mmol/l) (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Yliannostus) | |
Hypomagnesemia (< 0,7 mmol/l) (ks. sitraatin kelaatio kohdassa Varoitukset ja käyttöön liittyvät varotoimet) | ||
Vaikea hypernatremia (> 155 mmol/l) (ks. kohdat Varoitukset ja käyttöön liittyvät varotoimet ja Yliannostus) | ||
Vaikea metabolinen alkaloosi (pH > 7,55) (ks. sitraattiylikuormitus kohdassa Varoitukset ja käyttöön liittyvät varotoimet) | ||
Vaikea metabolinen asidoosi (pH < 7,2) (ks. sitraatinen kertyminen elimistöön kohdassa Varoitukset ja käyttöön liittyvät varotoimet) | ||
| Tuntematon | Nesteylikuormitus (ks. antotapa kohdassa Annostus ja antotapa) | |
| Hermosto | Tuntematon | Päänsärky* |
| Kouristuskohtaukset* | ||
| Kooma*# | ||
| Sydän | Tuntematon | Rytmihäiriöt* |
| Sydämenpysähdys*# | ||
| Keuhkopöhö (vaikeasta metabolisesta asidoosista johtuva) | ||
| Verisuonisto | Tuntematon | Hypotensio* |
| Hengityselimet, rintakehä ja välikarsina | Tuntematon | Bronkospasmi* |
| Hengityksen pysähtyminen*# | ||
| Takypnea (vaikeasta metabolisesta asidoosista johtuva Kussmaulin hengitys) | ||
| Ruoansulatuselimistö | Tuntematon | Oksentelu* |
| Luusto, lihakset ja sidekudos | Tuntematon | Lihaskouristukset* |
* Johtuu (vaikeasta) elektrolyyttien epätasapainosta (esim. hypokalsemia, hypernatremia, hypomagnesemia) tai metabolisesta alkaloosista
# mahdollisesti henkeä uhkaava
Haittatapahtumat voivat johtua myös hoidossa käytettävistä laitteista ja muista liuoksista. Katso lisätietoja asianmukaisesta pakkausselosteesta/käyttöohjeesta.
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan epäillyistä lääkkeen haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Tahaton liian suuren Cifoban-määrän anto voi johtaa yliannostukseen, joka voi aiheuttaa potilaalle henkeä uhkaavan tilanteen.
Tarkoitukseen sopimaton liian suuren sitraattimäärän anto aiheuttaa akuuttia hypokalsemiaa (ja metabolisen alkaloosin, hypernatremiaa) ja voi altistaa potilaan neurologisille ja sydämeen liittyville komplikaatioille. Tämä häiriö pitää korjata lopettamalla valmisteen anto / vähentämällä Cifoban-liuoksen määrää välittömästi ja antamalla kalsiumia laskimoon.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Hemodialyysiliuokset ja hemofiltraatit, hemofiltraatit
ATC-koodi: B05ZB
Jatkuvan venovenoosisen hemodialyysin, jatkuvan venovenoosisen hemodiafiltraation, pitkän matala-annoksisen (päivittäisen) dialyysin ja terapeuttisen plasmanvaihdon yhteydessä paikallisessa sitraattiantikoagulaatiossa käytettävä liuos.
Paikallinen sitraattiantikoagulaatio on menetelmä, jolla verta antikoaguloidaan paikallisesti verenpuhdistukseen tarkoitetussa kehonulkoisessa kierrossa ilman, että on tarvetta käyttää systeemistä antikoagulanttia. Paikallista sitraattiantikoagulaatiota voidaan käyttää sellaisissa kehonulkoisissa kierroissa, joissa verenvirtaus on vähäinen tai kohtalainen ja joissa mieluiten tietty sitraatin osa poistetaan verenpuhdistushoidolla. Tieteellisestä kirjallisuudesta saadut tiedot viittaavat siihen, että paikallista sitraattiantikoagulaatiota voidaan käyttää ensilinjan antikoagulanttina aiheellisissa hoidoissa; siitä voi olla hyötyä erityisesti potilaille, joilla on aktiivista verenvuotoa tai joilla verenvuodon riski on suurentunut. Tavallisesti voidaan pyrkiä tehokkaampaan antikoagulaatioon kuin käytettäessä systeemistä antikoagulaatiota, mistä on hyötyä kierron auki pysymisen ja hoidon tehon kannalta.
Yksilöllisestä sitraattiantikoagulaatiolla toteutetusta kehonulkoisesta verenpuhdistushoidosta riippuen potilaan verestä poistetaan vaihtelevia määriä kalsiumia, minkä vuoksi kalsiumin korvaaminen on tarpeen. Lisäksi osa paikallista sitraattiantikoagulaatiota varten infuusiona annetusta sitraatista päätyy vääjäämättä potilaan systeemiseen verenkiertoon, kun veri palautetaan sinne takaisin. Tämä suurentaa systeemistä sitraattipitoisuutta, joka yleensä stabiloituu uudelle tasolle riippuen sitraatti-infuusion todellisesta nopeudesta ja sitraatin metaboliasta maksassa ja muissa kudoksissa.
Potilaan veressä olevat kalsiumsitraatti-kelaattikompleksit hajoavat, kun sitraattia metaboloituu enemmän kuin sitä on systeemisesti annettu infuusiona. Nettovaikutuksena vapaa ionisoitunut kalsium jää potilaan vereen ja leviää sitten potilaan elimistöön, missä sillä on olennainen merkitys sekä luuston uudistumisessa että tärkeänä elektrolyyttinä koko elimistön solujen (esim. lihas- ja hermosolujen) toiminnoissa.
Farmakokinetiikka
Sitraatti on normaali ihmiselimistön metaboliitti ja välisubstraatti Krebsin kierrossa. Yhdessä hengitysketjun kanssa tämä fysiologinen reitti kykenee suurimmalla osalla potilaista käsittelemään suuria määriä sitraattia. Krebsin kierto tapahtuu mitokondrioissa, ja kaikki solut, joissa on näitä soluelimiä, voivat metaboloida sitraattia. Kudokset, joissa on paljon mitokondrioita, kuten maksa, luustolihakset ja munuaiset, kykenevät siten paremmin generoimaan ja eliminoimaan sitraattia.
Imeytyminen ja jakautuminen
Natriumin ja sitraatin imeytyminen ja jakautuminen määräytyvät potilaan kliinisen tilan, metabolisen tilan ja munuaisten toiminnan mukaan.
Biotransformaatio
Ihmisillä sitraatti on keskeisen metaboliareitin, Krebsin kierron, väliaine, kuten edellä mainittiin. Sitraatti metaboloituu nopeasti useissa elimissä/kudoksissa.
Eliminaatio
Huomattava osa sitraatista eliminoituu ulos virtaavan nesteen mukana.
Systeemiseen verenkiertoon infuusiona tullut sitraatti metaboloituu useimmissa somaattisissa soluissa.
Prekliiniset tiedot turvallisuudesta
Lääkkeen määräämiseen liittyviä olennaisia prekliinisiä tietoja ei ole.
Farmaseuttiset tiedot
Apuaineet
Injektionesteisiin käytettävä vesi
Kloorivetyhappo (pH:n säätämiseen)
Yhteensopimattomuudet
Koska yhteensopimattomuustutkimuksia ei ole tehty, lääkevalmistetta ei saa sekoittaa muiden lääkevalmisteiden kanssa.
Kestoaika
2 vuotta
Kestoaika avaamisen jälkeen:
Mikrobiologiselta kannalta lääkevalmiste tulee käyttää välittömästi. Jos sitä ei käytetä välittömästi, käytön aikaiset säilytysajat ja -olosuhteet ovat käyttäjän vastuulla.
Säilytys
Älä säilytä kylmässä. Ei saa jäätyä.
Säilytä pussit ulkopakkauksessa. Herkkä valolle.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
CIFOBAN infuusioneste, liuos
136 mmol/l (L:ei) 8 x 1500 ml (SecuNect) (209,95 €)
PF-selosteen tieto
Lääkevalmiste on pakattu suojapussissa pareittain kahteen identtiseen pussiin, jotka voidaan erottaa toisistaan repäisysaumaa pitkin.
Liuospussi on valmistettu polypropyleenin ja elastomeerin sekoituksesta. Pussissa on polypropyleenin ja elastomeerin sekoituksesta tehty infuusioletkusto sekä polykarbonaatista tehty liitin, ja pussia suojaa polyolefiinipohjainen, monikerroksinen pussi.
Pakkauskoot
SecuNect-liitinjärjestelmä:
8 x 1 500 ml:n pussi
Safe●Lock-liitinjärjestelmä:
8 x 1 500 ml:n pussi
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Valmisteen kuvaus:
Liuos on kirkasta ja väritöntä eikä siinä käytännöllisesti katsoen ole hiukkasia.
Käyttö- ja käsittelyohjeet
Hävittäminen
Liuos on tarkoitettu vain kertakäyttöön. Käyttämättä jäänyt liuos ja vioittunut pakkaus on hävitettävä paikallisten vaatimusten mukaisesti.
Käsittely
Liuospusseissa on joko SecuNect-liitin tai Safe●Lock-liitin.
Seuraavat seikat pitää ottaa huomioon ennen liuospussin käyttöä:
Aseptista tekniikkaa pitää noudattaa koko ajan, kun valmistetta annetaan potilaalle. Liuos pitää käyttää välittömästi pakkauksen avaamisen jälkeen mikrobiologisen kontaminaation välttämiseksi.
Kehonulkoisesti. Annetaan vain kehonulkoiseen verenkiertoon.
Liuosta ei ole tarkoitettu käytettäväksi lääkkeiden lisäämiseen.
Liuospussit, joissa on SecuNect-liitin (läpinäkyvä, vihreä rengas):
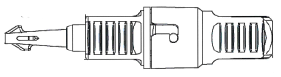
- Erota pussit toisistaan repäisysaumaa pitkin niin, että päällyskalvo ei vaurioidu.
-
Poista päällyspussi vasta juuri ennen liuoksen käyttöä. Tarkasta liuospussi (etiketti, viimeinen käyttöpäivämäärä, liuoksen kirkkaus, liuospussin ja päällyskalvon eheys).
Muovipakkaukset voivat joskus vahingoittua kuljetuksen aikana valmistajalta sairaalaan tai sairaalassa. Tällöin liuos voi kontaminoitua ja liuokseen voi tulla bakteeri- tai sienikasvustoa. Sen vuoksi on erittäin tärkeää tarkastaa pussi ja liuos huolellisesti ennen käyttöä. Erityistä huomiota on kiinnitettävä pussin suljinten, saumojen ja kulmien pienimpiinkin vaurioihin. Liuosta saa käyttää vain, jos se on väritöntä ja kirkasta, ja pussi ja liitin ovat vahingoittumattomia ja ehjiä. - Ripusta pussi telineeseen ripustinkahvasta.
- Poista suojakorkki SecuNect-liittimestä, jossa on vihreä rengas, ja kiinnitä liitin ainoastaan sen samanväriseen vastakappaleeseen; näin estät väärän liitännän. Älä koske sisäosiin äläkä etenkään liittimen kärkeen. Liittimen sisäpuoli on steriili eikä sitä ole tarkoitus enää desinfioida kemiallisilla desinfiointiaineilla. Yhdistä pussin liitin infuusioletkun liittimeen käsin kiertämällä niin, että kierrät voimakkaasti, kunnes kuuluu naksahdus ja liittimet on yhdistetty toisiinsa.
- Katkaise pussin liittimen helposti katkaistavissa oleva tappi ennen hoidon aloittamista ja pussin vaihdon yhteydessä. Varmista, että tappi katkeaa kokonaan.
- Jatka hoidossa käytettävän paikallisen sitraattiantikoagulaation hoito-ohjeiden mukaisesti.
Liuospussit, joissa on Safe●Lock-liitin (läpinäkyvä):
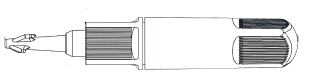
- Erota pussit toisistaan repäisysaumaa pitkin niin, että päällyskalvo ei vaurioidu.
-
Poista päällyspussi vasta juuri ennen liuoksen käyttöä. Tarkasta liuospussi (etiketti, viimeinen käyttöpäivämäärä, liuoksen kirkkaus, liuospussin ja päällyskalvon eheys).
Muovipakkaukset voivat joskus vaurioitua kuljetuksen aikana valmistajalta sairaalaan tai sairaalassa. Tällöin liuos saattaa kontaminoitua ja liuokseen voi tulla bakteeri- tai sienikasvustoa. Sen vuoksi on erittäin tärkeää tarkastaa pussi ja liuos huolellisesti ennen käyttöä. Erityistä huomiota on kiinnitettävä pussin suljinten, saumojen ja kulmien pienimpiinkin vaurioihin. Liuosta saa käyttää vain, jos se on väritöntä ja kirkasta, ja pussi ja liitin ovat vahingoittumattomia ja ehjiä. - Ripusta pussi telineeseen ripustinkahvasta.
- Poista suojakorkki läpinäkyvästäSafe●Lock-liittimestä ja kiinnitä liitin ainoastaan sen vastakappaleeseen; näin estät väärän liitännän. Älä koske sisäosiin äläkä etenkään liittimen kärkeen. Liittimen sisäpuoli on steriili eikä sitä ole tarkoitus enää desinfioida kemiallisilla desinfiointiaineilla. Yhdistä pussin liitin asianmukaiseen vastakappaleeseen ja väännä ne kiinni.
- Katkaise pussin liittimen helposti katkaistavissa oleva tappi ennen hoidon aloittamista ja pussin vaihdoin yhteydessä. Varmista, että tappi katkeaa kokonaan.
- Jatka käytettävän paikallisen sitraattiantikoagulaation hoito-ohjeiden mukaisesti.
Korvattavuus
CIFOBAN infuusioneste, liuos
136 mmol/l 8 x 1500 ml
- Ei korvausta.
ATC-koodi
B05ZB
Valmisteyhteenvedon muuttamispäivämäärä
09.11.2023
Yhteystiedot
Takomotie 1
00380 Helsinki
09 561 650
www.freseniussuomi.fi
etunimi.sukunimi@fmc-ag.com

 FRESENIUS MEDICAL CARE SUOMI OY
FRESENIUS MEDICAL CARE SUOMI OY