JADELLE SINE INSERTER implantat 2x75 mg
Observera
PRODUKTRESUMÈ
Kvalitativ och kvantitativ sammansättning
Produkten innehåller två implantat. Ett implantat innehåller 75 mg levonorgestrel.
En månad efter insättningen frisätter implantaten cirka 100 mikrog levonorgestrel per dygn. Mängden som frisätts minskar inom det första året till 40 mikrog/dygn, inom tre år till 30 mikrog/dygn och inom fem år till 25 mikrog/dygn.
För fullständig förteckning över hjälpämnen, se avsnitt Förteckning över hjälpämnen.
Läkemedelsform
Implantat
Kliniska uppgifter
Terapeutiska indikationer
Antikonception. Klinisk effekt och säkerhet har visats hos kvinnor mellan 18 och 40 år.
Dosering och administreringssätt
Subkutan användning.
Jadelle-implantat är en metod avsedd för långvarig (högst fem år) antikonception (se avsnitt Varningar och försiktighet). Användaren ska informeras om att implantaten på begäran kan tas ut när som helst.
Pediatrisk population
Det finns ingen terapeutisk indikation för Jadelle före menarche.
Insättning av Jadelle-implantat
En förpackning med Jadelle innehåller två sterila implantat förpackade i en påse. Insättning och uttagning av implantaten kräver träning och det rekommenderas att behörig vårdpersonal utför dessa ingrepp. Anvisningarna ska följas noga. Implantaten införs med en steril engångstroakar precis under huden.
OBS: engångstroakaren får användas endast en gång! Efter insättningen ska troakaren kasseras i en behållare för vassa föremål.
Ingreppet ska utföras helt aseptiskt. Implantaten ska för högerhänta placeras på insidan av vänster överarm och för vänsterhänta på insidan av höger överarm, cirka 8 cm från armbågsvecket. Rengör huden med ett antiseptiskt medel före insättningen och bedöva insättningsstället. Gör ett tvärgående snitt på två millimeter i huden med en skalpell. För in implantaten under huden med troakaren i riktning mot armhålan, i en V-formad vinkel mot varandra. När implantaten insätts korrekt är de lätta att ta ut med tiden och ärrbildningen blir minsta möjliga. Tryck snittets kanter mot varandra när båda implantaten är insatta, fixera med plåster och lägg ett förband på insättningsstället.
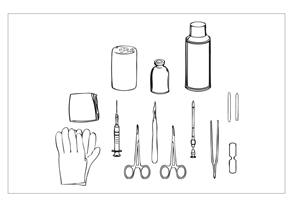
| Bild 1 Vid insättning av Jadelle-implantat behövs följande:
sterila dukar, sterilt instrumentbord, sterila handskar (talkfria), huddesinfektionsmedel
Jadelle troakar, skalpell, pincett
|
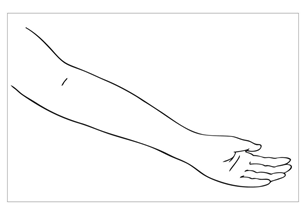
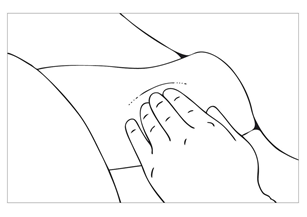
| Bild 2 Låt patienten ligga ner på rygg på britsen med vänster arm (höger arm för vänsterhänta) utsträckt på en steril duk på hjälpbordet i rak vinkel mot kroppen. Implantaten insätts subdermalt via ett snitt i ett smalt V-format läge med V-öppningen riktad mot armhålan. |
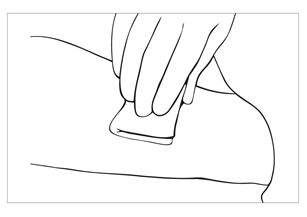
| Bild 3 Rengör och desinficera armen med en antiseptisk lösning och täck den med två sterila dukar eller med en steril duk med hål. Det bästa området för insättning är på insidan av överarmen, vid fördjupningen mellan musklerna, ca 6–8 cm ovanför armbågsvecket. |
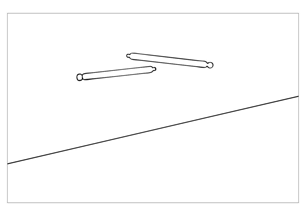
| Bild 4 Öppna påsen med Jadelle genom att dra isär påsens membran och låt de två implantaten falla på en steril duk. Vidrör inte påsens innerdel eller dess innehåll med bara händer. OBSERVERA: Använd alltid handskar eller tång vid hantering av implantaten. Om en stav blir smutsig, till exempel om den har fallit på golvet, ska den kasseras. Ta i så fall en ny påse för att fortsätta ingreppet. |
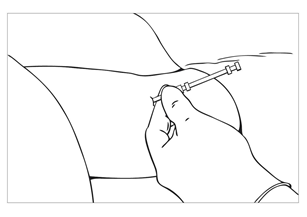
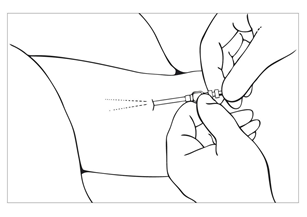
| Bild 5 Allergi mot bedövningsmedlet eller mot liknande ämnen ska utredas först. Dra upp ca 2–4 ml lokalbedövningsmedel i en spruta. Bedöva insättningsstället genom att föra in nålen ca 5–5,5 cm under huden i de riktningar dit troakaren kommer att införas. |
| Bild 6 Gör ett litet ca 2 mm långt snitt genom huden. Alternativt kan troakaren föras in genom huden utan snitt även om detta inte rekommenderas för Jadelle sine inserter. |
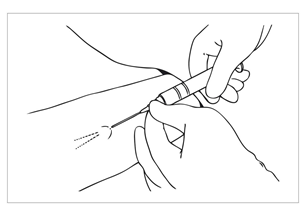
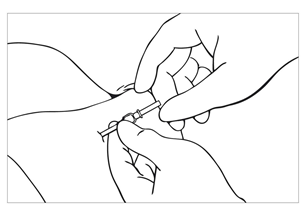
| Bild 7 På engångstroakaren för Jadelle finns det två markeringar. Den ena finns nära handtaget och visar hur djupt troakaren ligger under huden innan implantatet laddas. Markeringen nära spetsen visar troakarens insättningsdjup när implantatet har frigjorts För in troakaren under huden via snittet utan att vidröra troakardelen som går under huden. |
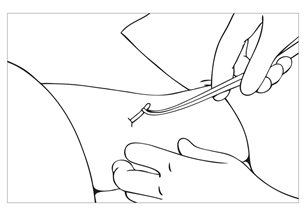
| Bild 8 För in troakaren i riktning med huden när spetsen är under huden så att implantaten kommer direkt under huden. Under hela insättningen ska troakarens snedslipade sida vända uppåt. Det är viktigt att hålla troakaren precis i skiktet under huden genom att lyfta huden med troakaren eftersom implantaten annars kan hamna för djupt och det är svårare att ta ut dem. För in troakaren försiktigt under huden ca 5,5 cm från snittet fram till markeringen på troakaren. Tvinga inte troakaren framåt och testa en annan riktning om motstånd känns. |
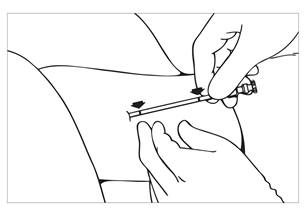
| Bild 9 Ta bort obturatorn när troakaren ligger på rätt djup och ladda det första implantatet i troakaren antingen med fingrarna eller med pincett. |
| Bild 10 Skjut försiktigt in implantatet till troakarens spets med obturatorn tills ett motstånd känns. Skjut aldrig in obturatorn med våld. |
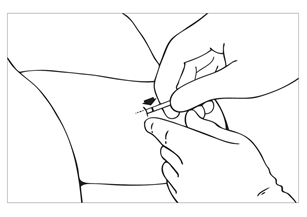
| Bild 11 Håll obturatorn på plats och dra försiktigt troakaren längs obturatorn tillbaka till kolvhandtaget. Det är viktigt att hålla obturatorn på plats. Skjut inte in implantatet i vävnaden. Dra troakaren endast fram till markeringen nära spetsen. Avlägsna den först när båda implantaten är insatta. |
| Bild 12 När markeringen nära troakarens spets blir synlig har implantatet frigjorts och ligger under huden. Detta kan bekräftas genom palpering. |
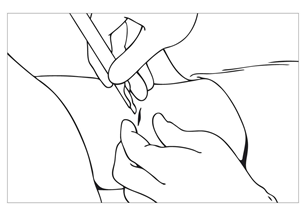
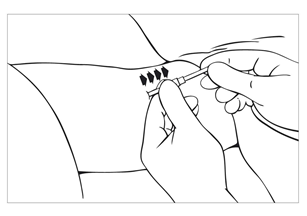
| Bild 13 Sätt in det andra implantatet bredvid det första i ett smalt V-format läge. Följ med vänster pekfinger det föregående implantatet och för in troakaren längs fingrets kant. Därmed insätts implantaten på lämpligt avstånd från varandra. För att undvika expulsioner ska ett avstånd på cirka 0,5 cm lämnas från snittet till implantatens ändar. Korrekt läge kan även bekräftas genom att försiktigt palpera införingsområdet. |
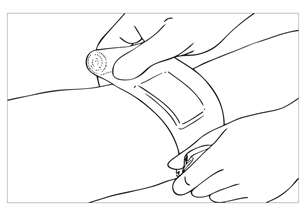
| Bild 14 Tryck snittkanterna mot varandra efter insättningen och slut snittet med ett sterilt plåster. Snittet behöver inte sys eftersom det kan öka ärrbildningen. OBS: efter insättningen får engångstroakaren inte användas för fler insättningar. Troakaren ska kasseras i en lämplig uppsamlingsbehållare. |
| Bild 15 Täck insättningsstället med kompresser och lägg ett stadigt förband över det för att förhindra blodutgjutning. Patienten ska observeras på mottagningen under några minuter före hemfärden. |
Uppmana patienten att hålla insättningsområdet torrt i tre dagar och ge henne en bipacksedel för Jadelle-implantat med notering om insättningsdag och tidpunkt för det första kontrollbesöket. Kompressen och förbandet kan tas bort när såret har läkt, i regel efter 3–5 dagar.
Att börja använda Jadelle-implantat
Ingen föregående hormonell preventivmetod under föregående månad
Jadelle-implantaten ska insättas inom sju dagar efter att menstruationen har börjat. Om implantaten sätts in i något annat skede av cykeln ska det först säkerställas på ett tillförlitligt sätt att patienten inte är gravid och dessutom ska en icke-hormonell preventivmetod användas i minst sju dagar efter insättningen.
Byte från kombinerade preventivtabletter (kombinerade p-piller, p-ring eller p-plåster)
Implantaten ska helst sättas in på dagen efter den sista kombinerade preventivtabletten med aktiv substans men senast dagen efter tablettpausen eller den sjunde dagen i placebocykeln. Vid byte från p-ring eller p-plåster till Jadelle-implantat ska implantatet helst insättas den dag då ringen eller plåstret tas bort, men senast den dag då den nya ringen eller plåstret skulle appliceras.
Byte från en annan preventivmetod med enbart progestin (minipiller, injektion, implantat)
Byte från minipiller kan göras när som helst, från ett annat implantat på uttagningsdagen och från injektion på nästa planerade injektionsdag.
Att börja använda Jadelle efter avbruten graviditet under första trimestern
Implantaten kan sättas in genast. I detta fall behövs inget kompletterande skydd.
Att börja använda Jadelle efter förlossning eller avbruten graviditet under andra trimestern
Implantaten kan sättas in genast efter förlossning eller avbruten graviditet under andra trimestern. Om implantaten sätts in senare än 21 dagar efter förlossning ska det först säkerställas på ett tillförlitligt sätt att patienten inte är gravid och dessutom ska en icke-hormonell preventivmetod användas i minst sju dagar efter insättningen.
Uttagning av Jadelle-implantat
Implantaten kan tas ut när som helst av hälsomässiga eller personliga skäl och de ska tas ut senast fem år efter insättningen. Implantaten kan tas ut när som helst i menstruationscykeln. Preventiveffekten upphör praktiskt taget genast och om graviditet inte är planerad måste byte göras till en annan preventivmetod. Vid uttagningen rengörs huden först och bedövningsmedel injiceras under implantatens ändar. Ett snitt på 2–4 millimeter görs med skalpell under "V". Implantaten tas ut med små peanger (t.ex. myggtång). Implantaten ska tas ut mycket försiktigt och uttagning tar mer tid än insättning. Implantatet kan vid uttagning få skråmor eller jack eller brytas. Om uttagningen visar sig svår eller om båda implantaten inte kan tas ut ska du be patienten att komma tillbaka till mottagningen när insättningsstället har läkt. Icke-hormonella preventivmetoder ska användas tills båda implantaten har tagits ut helt. Om patienten vill fortsätta använda Jadelle-implantat kan nya implantat insättas i samma snitt antingen i samma eller i motsatt riktning.
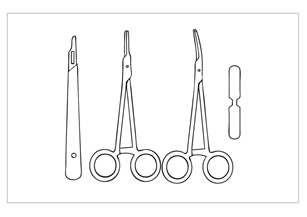
| Bild 16 För uttagning behövs följande:
|
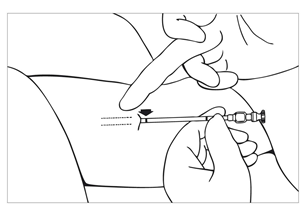
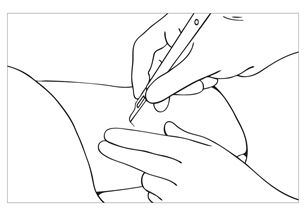
| Bild 17 Lokalisera implantaten genom palpation och markera eventuellt området på huden med en penna. Om implantaten inte kan palperas kan ultraljud eller mjukvävnadsröntgen användas för att lokalisera dem. Injicera en liten mängd bedövningsmedel i huden under implantatändarna som är närmast varandra. Om bedövningsmedlet injiceras ovanpå implantaten blir deras exakta läge oklart och uttagningen försvåras. Mer bedövningsmedel kan injiceras litet i taget om det behövs. |
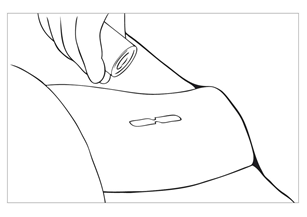
| Bild 18 Gör ett snitt på 4 mm nära ändarna på implantaten med en skalpell. Undvik ett stort snitt. |
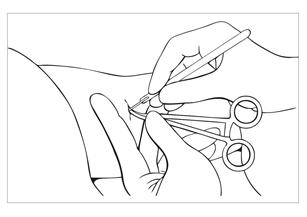
| Bild 19 Skjut försiktigt implantatet mot snittet med fingrarna mot huden. Fatta tag om det med en peang (Mosquito) när det blir synligt i snittet. Öppna den omgivande vävnadskapseln försiktigt med skalpellen. |
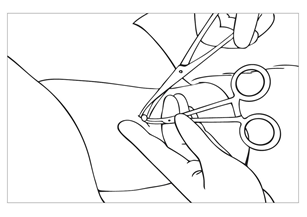
| Bild 20 Fatta tag om stavens ända med en annan peang (Crile). |
| Bild 21 Ta ut implantatet försiktigt genom snittet. Upprepa åtgärden med den andra staven. |
Mät implantaten efter uttagningen. Jadelle-implantatens längd är 43 mm. På detta sätt säkerställs det att patienten har haft två Jadelle-implantat och inga andra implantat.
Slut såret när ingreppet har utförts och lägg ett förband på det enligt beskrivningen för insättning. Armen ska hållas torr i några dagar.
Graviditet är möjlig när som helst efter uttagningen.
Kontraindikationer
Överkänslighet mot levonorgestrel eller mot något hjälpämne som anges i avsnitt Förteckning över hjälpämnen. Odiagnostiserad vaginalblödning. Känd eller misstänkt tumör som är beroende av könshormoner. akut eller tidigare genomgången svår leversjukdom där levervärdena inte har normaliserats. Benign eller malign levertumör. tromboembolisk sjukdom.
Varningar och försiktighet vid användning
Varningar
Kliniska prövningar har visat att Jadelle-implantatens preventiva effekt avtar efter det fjärde användningsåret. Därför ska uttagning av Jadelle-implantaten och byte till nya implantat övervägas efter fyra års användning, särskilt för kvinnor som väger mer än 60 kg (se avsnitt Farmakodynamiska egenskaper). Koncentrationen av levonorgestrel i serum är lägre i slutet av behandlingsperioden och omvänt proportionell mot användarens vikt.
Utstötning av implantaten kan ske innan såret är läkt om implantaten placeras mycket nära hudytan eller för nära hudsnittet eller om insättningsstället blir infekterat. Ett utstött implantat ska alltid bytas ut mot ett nytt, sterilt implantat.
Mindre förskjutningar av implantaten har rapporterats vid användning av andra levonorgestrelimplantat av samma typ. De flesta av dem har varit små förändringar av implantatens läge. I vissa sällsynta fall har förskjutningen varit betydande (någon eller flera centimeter). En del av dessa fall har enligt rapporter medfört smärta eller andra besvär. Om implantaten förskjutits kan andra metoder än de som anges i instruktionerna, ytterligare snitt eller fler besök hos läkaren behövas för att ta ut dem.
Förändrade lipoproteinnivåer i serum har observerats i kliniska prövningar med Jadelle-implantat. Även om nivåerna för totalt kolesterol, HDL (high-density lipoprotein) och LDL (low-density lipoprotein) samt triglycerider har konstaterats minska statistiskt signifikant har medelvärdet för alla stannat inom normala gränser. Den kliniska relevansen på lång sikt av dessa resultat har hittills inte fastställts.
Jadelle-implantaten har visat varierande effekter på koagulationsfaktorer.
Om patienten tidigare har haft tromboembolisk sjukdom ska Jadelle-implantat användas endast om andra preventivmetoder inte är lämpliga och även i detta fall ska riskerna och fördelarna noga övervägas. Tromboemboliska och kardiovaskulära biverkningar som stroke, hjärtinfarkt, lungemboli och djupa ventromboser har rapporterats hos personer som har använt andra levonorgestrelimplantat. Jadelle-implantaten ska tas ut om en patient utvecklar trombos eller emboli (se även avsnittet Stora och små kirurgiska ingrepp). Tromboflebit och ytlig veninflammation har förekommit oftare i den arm där implantaten har insatts. En del fall har associerats med trauma i den aktuella armen.
Särskild försiktighet ska iakttas vid användning av Jadelle-implantat hos patienter med kända riskfaktorer eller annan känslighet för artärsjukdom.
Om bestående hypertoni utvecklas vid användning av Jadelle-implantat eller om blodtryckssänkande behandling inte ger ett adekvat svar på signifikant förhöjt blodtryck ska Jadelle-implantaten tas ut.
Om en patient har haft eller utvecklar fokal migrän eller migrän av crescendotyp eller om migrän av denna typ förvärras vid användning av Jadelle-implantat ska situationen utvärderas noggrant.
Kontakta ögonläkare om en patient som använder kontaktlinser får nedsatt syn eller tolererar kontaktlinser sämre. Det kan finnas anledning att avbryta eller avsluta användning av kontaktlinser.
Förändringar i glukostolerans och insulinkänslighet har rapporterats i ett fåtal studier bland användare av Jadelle-implantat vid oralt glukosbelastningsprov. Den kliniska betydelsen av dessa fynd är okänd men tillståndet hos diabetiker som använder Jadelle-implantat ska övervakas noga. Viktökning vid användning av Jadelle-implantat är möjlig.
Om en användare av Jadelle-implantat utvecklar kolestatisk hepatit eller gulsot ska implantaten tas ut. En mild till måttlig övergående ökning av totalt bilirubin i serum är vanlig i den inledande fasen av användning. En lätt ökad risk för gallsten har rapporterats med andra levonorgestrelimplantat av samma typ. Metabolismen av levonorgestrel kan försämras hos patienter med leverinsufficiens.
Nedstämdhet och depression är kända biverkningar vid användning av hormonella preventivmedel (se avsnitt Biverkningar). En depression kan vara allvarlig och är en känd riskfaktor för självmordsbeteende och självmord. Kvinnor ska rådas att kontakta läkare vid humörförändringar och depressiva symtom, även direkt efter inledd behandling. Uttagning av Jadelle-implantaten ska också övervägas om patienten är allvarligt deprimerad eftersom symtomet kan vara hormonellt. Hos patienter som tidigare har haft depression ska tillståndet övervakas noggrant och uttagning av Jadelle-implantaten ska övervägas vid tydliga symtom.
Steroidhormoner kan orsaka viss vätskeansamling som kan leda till viktökning. Användning av Jadelle-implantat ska övervägas noga när det gäller patienter med underliggande sjukdom som kan förvärras av vätskeansamling och deras tillstånd ska övervakas noga under behandlingen.
Idiopatisk förhöjning av hjärntrycket har rapporterats hos ett fåtal patienter som har använt levonorgestrelimplantat. Belägget baseras endast på individuella rapporter. Denna möjlighet ska övervägas om patienten har ständig huvudvärk och/eller synstörningar under behandling med Jadelle-implantat, särskilt om patienten är överviktig eller nyligen har gått upp i vikt. Om en idiopatisk förhöjning av hjärntrycket observeras hos en patient ska Jadelle-implantaten tas ut.
Jadelle-implantat påverkar menstruationscykeln hos de flesta användare. Oregelbunden och långvarig blödning, mellanblödningar, stänkblödningar och amenorré har rapporterats. Blödningarna blir i regel mer regelbundna med tiden. Betydande blodförlust som leder till anemi är sällsynt och de genomsnittliga hemoglobinvärdena förbättras något under behandling med Jadelle-implantat.
Eftersom menstruationen ibland kan utebli hos vissa användare av Jadelle-implantat kan det inte enbart med ledning av utebliven menstruation avgöras om en patient är gravid. Om en graviditet misstänks ska ett graviditetstest göras. En blödningsfri period på sex veckor eller mer hos en patient med tidigare regelbunden menstruation kan innebära graviditet. Om patienten blir gravid ska implantaten avlägsnas.
Extrauterina graviditeter har i sällsynta fall rapporterats hos användare av levonorgestrelimplantat: mindre än ett fall per tusen användarår. Om en användare av Jadelle-implantat har smärtor i nedre delen av buken eller konstateras vara gravid, är det viktigt att kontrollera att det inte är en extrauterin graviditet.
Folliklar utvecklas under användning av Jadelle-implantat men deras atresi kan försenas och de kan bli större än normalt. Hos de flesta kvinnor försvinner förstorade folliklar av sig själva. I en del sällsynta fall kan de dock vridas eller brista och orsaka buksmärtor. Konservativ behandling är indicerad även om patienten har symtom, men möjligheten till extrauterin graviditet måste utredas. Kirurgiska ingrepp behövs endast i undantagsfall.
I ett fåtal sällsynta fall har autoimmuna sjukdomar som sklerodermi, LED (lupus erythematosus disseminata) eller reumatoid artrit rapporterats hos patienter som använder levonorgestrelimplantat. Något orsakssamband med användning av implantat som innehåller levonorgestrel har dock inte fastställts. Följande tillstånd har rapporterats både under graviditet och under behandling med könssteroider men något samband med progestiner har inte fastställts: ikterus och/eller pruritus associerad med kolestas, gallsten, hemolytiskt uremiskt syndrom, herpes gestationis och otosklerosrelaterad hörselnedsättning.
Även om inget tydligt orsakssamband har fastställts mellan preventivtabletter och bröstcancer har en något ökad risk för bröstcancer observerats i en metaanalys av epidemiologiska studier (RR=1,24) hos dem som använde kombinerade preventivtabletter vid tidpunkten för studien. Den ökade risken försvinner gradvis inom tio år efter avslutad behandling. Vid användning av preventivmetoder med enbart progestin kan risken vara ungefär densamma som vid användning av kombinerade p-piller.
Varningar och försiktighet
Innan behandlingen påbörjas eller återupptas efter ett uppehåll ska möjligheten för graviditet uteslutas och patientens medicinska historia och släktanamnes noga utredas. Blodtrycksmätning och läkarundersökning ska utföras med tanke på kontraindikationer samt varningar och försiktighet vid användning. Patienten ska även uppmanas att noga läsa bipacksedeln och följa anvisningarna samt kontakta läkare vid eventuella problem på insättningsstället. Kontrollbesökens frekvens och typ ska baseras på fastställda riktlinjer och anpassas individuellt till varje patient.
Vid kontrollbesöken ska insättningsstället alltid kontrolleras. Om en patient har odiagnostiserad, ihållande eller återkommande vaginal blödning ska det säkerställas att det inte handlar om en elakartad sjukdom. Om en patient har en släktanamnes med bröstcancer eller har godartade knölar i ett bröst eller mastopati ska patientens tillstånd övervakas särskilt noga.
Kvinnor ska informeras om att Jadelle-implantat inte skyddar mot HIV-infektion (AIDS) eller andra sexuellt överförbara sjukdomar.
Stora och små kirurgiska ingrepp
Jadelle innehåller inte östrogen och användning av dem behöver liksom för andra liknande preventivpreparat vanligtvis inte avbrytas vid kirurgiska ingrepp. Om det emellertid finns risk för trombos ska åtgärder vidtas för att förhindra den. På grund av risken för tromboembolism kan uttagning av implantaten övervägas antingen vid kirurgi eller långvarig immobilisering av andra skäl.
Anvisningar för patienten
Förpackningen innehåller en bipacksedel som gör det lättare att förklara Jadelle-implantatens egenskaper för patienten. Informationen ska ges till alla patienter. Patienten ska informeras ingående om nackdelarna och fördelarna med Jadelle-implantat, andra preventivmetoder och att vara utan graviditetsskydd. Dessutom ska information ges om insättning och uttagning av implantaten.
Interaktioner
4.5.1 Effekter av andra läkemedel på Jadelle-implantat
Interaktioner kan förekomma med läkemedel som inducerar mikrosomala enzymer, vilket kan öka clearance av könshormoner och leda till förändrad blödningsprofil och/eller utebliven prevention.
Kvinnor som behandlas med något av dessa läkemedel ska tillfälligt använda antingen en barriärmetod eller en annan preventivmetod utöver Jadelle. Barriärmetoden ska användas under hela den samtidiga läkemedelsbehandlingen och i ytterligare 28 dagar efter avslutad användning av läkemedlet.
Läkemedel som ökar clearance av levonorgestrel (enzyminducerad minskning av Jadelle-implantatets effekt) inkluderar:
Fenytoin, barbiturater, primidon, karbamazepin, rifampicin och eventuellt även oxkarbamazepin, topiramat, bosentan, felbamat, griseofulvin och naturpreparat som innehåller johannesört.
Maximal enzyminduktion kan generellt ses inom några veckor. Enzyminduktion kan kvarstå under cirka 4 veckor efter avslutad läkemedelsbehandling.
Kvinnor som använder Jadelle ska varnas för eventuellt minskad preventiv effekt vid behandling med preparat (som de ovanstående) som har enzyminducerande effekt eftersom genombrottsblödning och oavsiktliga graviditeter har rapporterats.
Läkemedel som minskar clearance av levonorgestrel (enzymhämmare)
Starka och måttliga CYP3A4-hämmare såsom azolläkemedel mot svampinfektioner (bl.a. itrakonazol, voriconazol, flukonazol), verapamil, makrolider (bl.a. klaritromycin, erytromycin), diltiazem och grapefruktjuice kan öka plasmakoncentrationen av progestin.
Läkemedel med varierande effekter på clearance av levonorgestrel
Många kombinationer av HIV-/HCV-proteashämmare och icke-nukleosida hämmare av omvänt transkriptas kan vid samtidig användning med könshormoner öka eller minska plasmakoncentrationen av progestin (minska [bl.a. nelfinavir, ritonavir, darunavir/ritonavir, (fos)amprenavir/ritonavir, lopinavir/ritonavir och tipranavir/ritonavir, nevirapin, efavirenz] eller öka [bl.a. indinavir och atazanavir/ritonavir, etravirin]).
4.5.2 Effekter av Jadelle-implantat på andra läkemedel
Jadelle kan påverka metabolismen av andra läkemedel. Dessutom kan plasma- och vävnadskoncentrationerna antingen öka (bl.a. ciklosporin) eller minska (bl.a. lamotrigin).
Obs: Eventuella interaktioner ska kontrolleras i produktresumén för samtidiga läkemedel.
4.5.3 Övriga interaktioner
Laboratorietester
Användning av preventivhormoner kan påverka resultaten av vissa laboratorietester. Jadelle kan påverka resultaten av vissa endokrinologiska laboratorietester:
1. minska koncentrationen av SHBG (könshormonbindande globulin)
2. minska serumkoncentrationen av tyroxin och öka värdena för trijodtyroninbindande test.
Fertilitet, graviditet och amning
Graviditet
Om patienten blir gravid ska Jadelle-implantaten avlägsnas. Djurstudier har visat att stora mängder progestinsubstanser kan orsaka maskulinisering av flickfoster. De flesta epidemiologiska undersökningar av oavsiktlig fosterexponering för en kombination av östrogener och progestogener har inte visat någon teratogen eller fostertoxisk effekt. Det finns inga undersökningar av effekten av Jadelle-implantat under eller före graviditet.
Amning
Levonorgestrel utsöndras i bröstmjölk, men terapeutiska doser av Jadelle-implantat förväntas inte ha någon effekt på ammade barn nyfödda eller spädbarn. Levonorgestrelkoncentrationerna under användning av Jadelle-implantat påverkar inte modersmjölkens kvalitet eller mängd.
Effekter på förmågan att framföra fordon och använda maskiner
Inga effekter av preparatet på förmågan att framföra fordon och använda maskiner har observerats.
Biverkningar
Följande biverkningar har rapporterats under kliniska prövningar med Jadelle-implantat:
Mycket vanliga biverkningar (hos mer än 10 % av användarna):
Förändringar i blödningsmönstret såsom frekventa, oregelbundna eller långvariga menstruationsblödningar, stänkblödningar, oligomenorré eller amenorré är bland de vanligaste biverkningarna hos de flesta användare under det första året. 14 % slutade använda Jadelle-implantat inom fem år på grund av störningar i blödningsmönstret. Andra mycket vanliga biverkningar är: huvudvärk, nervositet, yrsel, illamående, inflammation i livmoderhalsen, vita flytningar, genital klåda, smärta i nedre delen av buken, ömma bröst, viktökning.
Organsystem | Mycket vanliga biverkningar > 1/10 | Vanliga biverkningar > 1/100, < 1/10 | Mindre vanliga biverkningar > 1/1 000, < 1/100 | Sällsynta biverkningar > 1/10 000, < 1/1 000 |
Psykiska störningar | humörsvängningar, depression förändrat libido, samlagssmärtor | |||
Centrala och perifera nervsystemet | huvudvärk, nervositet, yrsel | migrän | ||
Hjärtat | hjärtklappning, bröstsmärta | |||
Blodkärl | högt blodtryck, åderbråck | |||
Andningsvägar, bröstkorg och mediastinum | andfåddhet | |||
Magtarmkanalen | illamående | bukbesvär | ||
Lever och gallvägar | förhöjda koncentrationer av totalbilirubin i serum | |||
Hud och subkutan vävnad | akne, kontaktdermatit, skallighet, ökad behåring, utslag, klåda, missfärgad hud | |||
Njurar och urinvägar | urinvägssymtom | |||
Reproduktionsorgan och bröstkörtel | störningar i blödningsmönstret såsom täta, oregelbundna eller långdragna blödningar, stänkblödningar, oligomenorré eller amenorré, inflammation i livmoderhalsen, vita flytningar, genital klåda, smärta i nedre delen av buken, ömma bröst | slidkatarr, ovarialcystor, godartade bröstknölar, utsöndring från brösten | ||
Allmänna symtom och/eller symtom vid administreringsstället | viktökning | klåda vid insättningsstället, allmän smärta, trötthet, ryggsmärtor, viktminskning | blåmärken vid insättningsstället, inflammation vid insättningsstället | utstötning av implantatet, smärta i armen, domningar, stickningar och ärrbildning i armen, svår uttagning av implantatet, skada på ulnarisnerven vid uttagning av implantatet, hyperpigmentering vid implantaten |
Utstötning eller förskjutning av implantaten är möjlig (se även avsnitt Dosering och administreringssätt).
I sällsynta fall har extrauterina graviditeter rapporterats (se även avsnitt Varningar och försiktighet).
Vid användning av andra levonorgestrelimplantat av samma typ på olika håll runt om i världen har dessutom blåsor, sår och fjällning på ett smalt hudområde i sällsynta fall observerats.
Mycket sällsynta fall av kolestatisk hepatit, gulsot, bilirubinemi och tromboemboliska komplikationer har rapporterats med andra levonorgestrelimplantat av samma typ (se även avsnitt Varningar och försiktighet).
Vid användning av andra levonorgestrelimplantat har leverfläckar förekommit.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta-riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning till:
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Överdosering
Erfarenhet saknas av överdosering med Jadelle-implantat.
Farmakologiska egenskaper
Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: progestogener, levonorgestrel, ATC-kod: G03AC03
Den aktiva substansen i Jadelle-implantat, levonorgestrel, är ett syntetiskt progestin. Levonorgestrel som frigörs från implantat har visats ha en varierande effekt på äggstockarnas funktion så som att follikel- och gulkroppsfunktionen kan hämmas helt, folliklarnas utveckling kan vara normal men gulkroppens funktion bristfällig eller att ovulation kan inträffa normalt. Levonorgestrel gör sekretet i livmoderhalsen tjockt och segt så att spermierna inte kan passera till livmodern samt gör livmoderslemhinnan tunn så att den inte kan ta emot en blastocyst.
Den preventiva effekten av Jadelle-implantat har undersökts i kliniska multicenterprövningar som följde 4 657 användarår hos 1 393 kvinnor, varav 525 använde Jadelle-implantat i fem år. Pearl Index var under fem år 0,17 (95 % konfidensintervall 0,04–0,30) per 100 användarår. Under det femte året var Pearl Index 0,84 per 100 användarår (95 % konfidensintervall 0,09–1,57). Det årliga graviditetstalet var 0,1±0,1 per 100 användare under det första, andra och tredje året, 0,0±0,0 per 100 användare under det fjärde året och 0,8±0,5 (SE) per 100 användare under det femte året. I olika viktgrupper under det femte året var graviditetstalet 0,9±0,9 per 100 användare som väger mindre än 50 kg, 0,5±0,5 per 100 användare som väger 50–59 kg, 1,1±0,7 per 100 användare som väger 60–69 kg och 1,1±1,1 per 100 användare som väger 70 kg eller mer. För alla användare som väger 60 kg eller mer var det årliga graviditetstalet per 100 användare 0,2±0,2 under det första året, 0,2±0,2 under det andra året, 0,3±0,3 under det tredje året, 0,0±0,0 under det fjärde året och 1,1±0,6 under det femte året.
Efter uttagning av implantaten återgår fertiliteten snabbt till det normala. När Jadelle-implantaten togs ut när graviditet önskades blev 45 % gravida inom tre månader och 86 % inom ett år.
Produktens effekt är inte beroende av behandlingsföljsamhet.
Farmakokinetiska egenskaper
Den enda aktiva substansen i Jadelle-implantat är levonorgestrel som tillhör progestinerna. Implantaten insätts under huden.
Absorption
Implantaten frisläpper levonorgestrel direkt i vävnadsvätska. Maximala koncentrationer i serum, cirka 772 pg/ml, nås två dagar efter insättning av stavarna. Efter den inledande fasen sjunker koncentrationerna av levonorgestrel till 435 pg/ml efter en månad, 355 pg/ml efter sex månader, 341 pg/ml efter ett år och 277 pg/ml efter fem år.
Distribution
Serumkoncentrationen av levonorgestrel är omvänt proportionell mot vikten; skillnaden är ungefär tvåfaldig mellan kvinnor som väger 50 kg och 70 kg. Serumkoncentrationer av levonorgestrel har dock inget individuellt prognostiskt värde avseende graviditetsrisk på grund av stor variation i koncentrationer och respons. Serumkoncentrationen av levonorgestrel är betydligt lägre hos dem som använder Jadelle-implantat än hos dem som använder preventivtabletter med levonorgestrel.
I serum är levonorgestrel främst bundet till könshormonbindande globulin (SHBG). SHBG-nivåerna minskar på grund av levonorgestrels effekter inom några dagar, vilket minskar den totala koncentrationen av levonorgestrel i serum.
Metabolism
Levonorgestrel (LNG) metaboliseras i stor utsträckning. De viktigaste metaboliseringsvägarna är reduktionen av Δ4-3-oxogruppen och hydroxyleringar vid positionerna 2α, 1β och 16β, följt av konjugering. CYP3A4 är det huvudsakliga enzymet som är involverat i levonorgestrels oxidativa metabolism. Tillgängliga in vitro-data tyder på att CYP-medierade biotransformationsreaktioner kan vara av mindre betydelse jämfört med reduktion och konjugering.
Eliminering
Metaboliskt clearance varierar mångfaldigt mellan olika individer, vilket antas förklara den stora variationen i serumkoncentrationer av levonorgestrel hos implantatanvändare. Halveringstiden för eliminering är 13–18 timmar. Levonorgestrel och dess metaboliter utsöndras främst (40–68 %) med urinen och 16–48 % utsöndras i avföringen. Efter uttagning av implantaten minskar serumkoncentrationerna av levonorgestrel under detektionsgränsen inom 5–14 dagar.
Prekliniska säkerhetsuppgifter
Toxicitetsprofilen för levonorgestrel har studerats väl och orsakar inga andra särskilda risker för människans hälsa än de som anges i produktresuméns övriga avsnitt.
Inga tecken på gentoxicitet har observerats i mutagenicitets- och biokompatibilitetsstudier. Den lokala toleransen för levonorgestrel och icke-aktiva polymerenheter i Jadelle-implantatet konstaterades vara bra.
Farmaceutiska uppgifter
Förteckning över hjälpämnen
Polydimetylsiloxan
Vattenfri, kolloidal kiseldioxid
Inkompatibiliteter
Ej relevant.
Hållbarhet
5 år
Särskilda förvaringsanvisningar
Inga särskilda förvaringsanvisningar.
Förpackningstyp och innehåll
Markkinoilla olevat pakkaukset
Resepti
JADELLE SINE INSERTER implantaatti
2x75 mg (L:ei) 1 pakkaus (175,16 €)
PF-selosteen tieto
Två sterila implantat förpackade i en påse av PE-filament och PET/PE-membran.
Läkemedlets utseende:
Implantaten är böjliga, kompakta, vita eller nästan vita stavar med längd cirka 43 mm och diameter 2,5 mm.
Särskilda anvisningar för destruktion och övrig hantering
I avsnitt Dosering och administreringssätt samt i instruktionerna för insättning av Jadelle sine inserter implantat finns anvisningar för insättning och uttagning av implantaten. I produktresumén för läkare finns noggranna instruktioner för insättning och uttagning av implantaten.
Ersättning
JADELLE SINE INSERTER implantaatti
2x75 mg 1 pakkaus
- Ei korvausta.
Atc-kod
G03AC03
Datum för översyn av produktresumén
22.12.2021
Yhteystiedot
Tuulikuja 2, PL 73
02151 Espoo
020 785 21
www.bayer.fi

 BAYER OY
BAYER OY