PECFENT nenäsumute, liuos 100 mikrog/suihke, 400 mikrog/suihke
 Lääketurva
Lääketurva
Riskienminimointimateriaalit
Apteekki
Lääkäri
Potilas
Vaikuttavat aineet ja niiden määrät
PecFent 100 mikrogrammaa/suihke, nenäsumute, liuos
Yksi millilitra liuosta sisältää fentanyylisitraattia määrän, joka vastaa 1 000 mikrogrammaa fentanyyliä
Yksi suihke (100 mikrolitraa) sisältää fentanyylisitraattia määrän, joka vastaa 100 mikrogrammaa fentanyyliä
Jokainen pullo sisältää 1,55 ml (1 550 mikrogrammaa fentanyyliä).
PecFent 400 mikrogrammaa/suihke, nenäsumute, liuos
Yksi millilitra liuosta sisältää fentanyylisitraattia määrän, joka vastaa 4 000 mikrogrammaa fentanyyliä
Yksi suihke (100 mikrolitraa) sisältää fentanyylisitraattia määrän, joka vastaa 400 mikrogrammaa fentanyyliä
Jokainen pullo sisältää 1,55 ml (6 200 mikrogrammaa fentanyyliä)
Apuaineet, joiden vaikutus tunnetaan:
Jokainen suihke sisältää 0,02 mg propyyliparahydroksibentsoaattia (E 216).
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Nenäsumute, liuos (nenäsumute).
Kliiniset tiedot
Käyttöaiheet
PecFentiä käytetään läpilyöntikivun hoitoon aikuisilla, joiden kroonista syöpäkipua jo hoidetaan opioidilla. Läpilyöntikipu on ohimenevä kivun pahenemisvaihe, jota esiintyy muuten hallinnassa olevan jatkuvan kivun ylläpitohoidon aikana.
Opioidia ylläpitohoitona saavat potilaat käyttävät vähintään 60 mg suun kautta otettavaa morfiinia vuorokaudessa, vähintään 25 mikrogrammaa ihon läpi annettavaa fentanyyliä tunnissa, vähintään 30 mg oksikodonia vuorokaudessa, vähintään 8 mg suun kautta otettavaa hydromorfonia vuorokaudessa tai ekvianalgeettisen annoksen jotain muuta opioidia viikon ajan tai pidempään.
Ehto
Hoito on aloitettava ja annettava syöpäpotilaiden opioidihoitoon perehtyneen lääkärin ohjauksessa.
Annostus ja antotapa
Hoidon aloittaa ja sitä valvoo syöpäpotilaiden opioidihoitoon perehtynyt lääkäri. Lääkäreiden pitää muistaa fentanyylin väärinkäytön mahdollisuus.
Annostus
Potilaille titrataan yksilöllisesti sellainen “tehokas” annos, jolla kipu lievittyy riittävästi ja haittavaikutukset vähenevät minimiin aikaansaamatta aiheettomia (tai sietämättömiä) haittavaikutuksia kahden perättäisen hoidetun läpilyöntikipuvaiheen aikana. Annoksen tehokkuutta tulee arvioida kohtausta seuraavan 30 minuutin aikana.
Potilaita tulee seurata tarkasti titrauksen aikana kunnes tehokas annos on saavutettu.
PecFentiä on saatavana kahta eri vahvuutta: 100 mikrogrammaa/suihke ja 400 mikrogrammaa/suihke.
Yksi annos PecFentiä voi käsittää 1 suihkeen (100 mikrogramman tai 400 mikrogramman annos) tai 2 suihketta (200 mikrogramman tai 800 mikrogramman annos) samaa vahvuutta (joko 100 mikrogramman tai 400 mikrogramman vahvuutta).
Potilaat eivät saa käyttää enempää kuin 4 annosta vuorokaudessa. Potilaiden on odotettava vähintään 4 tuntia annoksen jälkeen ennen seuraavan läpilyöntikipukohtauksen hoitamista PecFentillä.
PecFentiä voidaan antaa 100, 200, 400 tai 800 mikrogramman annoksina seuraavasti:
| Vaadittava annos (mikrogrammoina) | Valmisteen vahvuus (mikrogrammoina) | Määrä |
| 100 | 100 | Yksi suihke yhteen sieraimeen |
| 200 | 100 | Yksi suihke molempiin sieraimiin |
| 400 | 400 | Yksi suihke yhteen sieraimeen |
| 800 | 400 | Yksi suihke molempiin sieraimiin |
Aloitusannos
- PecFentin aloitusannos läpilyöntikipukohtauksien hoidossa on aina 100 mikrogrammaa (yksi suihke), silloinkin kun potilas siirretään toisista fentanyylia sisältävistä tuotteista PecFentiin läpilyöntikipukohtauksien hoidossa.
- Potilaan tulee odottaa vähintään 4 tuntia ennen uuden läpilyöntikipukohtauksen hoitoa PecFentillä.
Titrausmenetelmä
- Potilaille tulee määrätä titrausta varten aluksi yksi pullo (8 suihketta) PecFent 100 mikrogrammaa/suihke -valmistetta
- Potilaita, joiden aloitusannos on 100 mikrogrammaa ja joilla on tarve titrata suurempaan annokseen tehon puutteen vuoksi, voidaan neuvoa käyttämään kaksi 100 mikrogramman suihketta (yksi kumpaankiin sieraimeen) seuraavan läpilyöntikipukohtauksen hoitoon. Jos tämä annos ei tehoa, potilaalle voidaan määrätä PecFent 400 mikrogrammaa/suihke -pullo ja neuvoa käyttämään yhtä 400 mikrogramman suihketta seuraavan kipukohtauksen hoitoa varten. Jos tämä annos ei tehoa, potilasta voidaan neuvoa lisäämään annosta kahteen 400 mikrogramman suihkeeseen (yksi kumpaankiin sieraimeen).
- Hoidon aloittamisesta lähtien potilaita on seurattava tarkasti ja annosta titrattava, kunnes tehokas annos on saavutettu ja vahvistettu kahden toisiaan seuraavan läpilyöntikipukohtauksen hoidossa.
Titraus potilailla, jotka vaihtavat välittömästi vapautuvaa fentanyyliä sisältävää tuotetta
Eri välittömästi vapautuvaa fentanyyliä sisältävien lääkevalmisteiden farmakokineettisten profiilien välillä voi olla huomattavia eroja, minkä vuoksi valmisteiden sisältämän fentanyylin imeytymisen nopeudessa ja määrässä voi myös olla kliinisesti merkittäviä eroja. Läpilyöntikivun hoitoon tarkoitettuja fentanyyliä sisältäviä lääkevalmisteita – mukaan lukien nenänsisäisiä tuotteita – vaihdettaessa potilaan annos on siksi aina titrattava uudelleen, eikä vaihdettava suoraan (mikrogrammamäärältään) samansuuruiseen annokseen.
Ylläpitohoito
Kun oikea annos on määritetty titraamalla, potilaan tulee jatkaa saman annoksen ottamista korkeintaan 4 kertaa vuorokaudessa.
Annoksen muuttaminen
Yleisesti ottaen PecFent-valmisteen ylläpitoannosta suurennetaan ainoastaan silloin, jos käytetty annos ei ole riittävä useiden perättäisten läpilyöntikipukohtauksien hoidossa.
Taustakivun hoitoon käytettävän opioidin annoksen muuttaminen saattaa olla tarpeen, jos potilaalla on jatkuvasti yli neljä läpilyöntikipukohtausta vuorokauden aikana.
Jos kipua ei saada riittävän hyvin hallintaan, hyperalgesian, sietokyvyn kasvun ja taustalla olevan sairauden etenemisen mahdollisuudet tulee ottaa huomioon (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Jos haittavaikutukset ovat sietämättömiä tai jatkuvia, PecFent annosta tulee pienentää tai PecFent-hoito korvata toisella kipulääkkeellä.
Hoidon kesto ja tavoitteet
Ennen PecFent-valmisteen käytön aloittamista on sovittava kivun hallintaa koskevien ohjeiden mukaisesti yhdessä potilaan kanssa hoitostrategiasta, joka käsittää hoidon keston ja hoitotavoitteet sekä hoidon lopettamista koskevan suunnitelman. Hoidon aikana lääkärin ja potilaan on pidettävä tiiviisti yhteyttä voidakseen arvioida hoidon jatkamistarvetta, harkita hoidon keskeyttämistä ja muuttaa tarvittaessa annostusta. Jos kipu ei lievity riittävästi, on otettava huomioon hyperalgesian, toleranssin ja perussairauden etenemisen mahdollisuus (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet). PecFent-valmistetta ei pidä käyttää pidempään kuin on tarpeen.
Hoidon lopettaminen
PecFent-valmisteen käyttö tulee lopettaa välittömästi, jos potilaalla ei enää esiinny läpilyöntikipukohtauksia.
Jatkuvan taustakivun hoitoa ei saa muuttaa.
Jos kaikki opioidihoito on tarpeen lopettaa, opioidihoito tulee titrata alaspäin asteittain äkillisten vieroitusoireiden välttämiseksi. Lääkärin tulee seurata potilaan tilaa tarkasti.
Erityisryhmät
Iäkkäät potilaat (yli 65-vuotiaat)
PecFentin kliinisessä tutkimusohjelmassa 104 (26,1 %) potilasta oli yli 60-vuotiaita, 67 (16,8 %) yli 65-vuotiaita ja 15 (3,8 %) yli 75-vuotiaita. Ei ollut mitään osoituksia siitä, että vanhempien potilaiden annosta tulisi titrata pienempiin annoksiin tai että heillä esiintyisi enemmän haittavaikutuksia kuin muilla. Ottaen kuitenkin huomioon munuaisten ja maksan toiminnan tärkeyden fentanyylin aineenvaihdunnassa ja puhdistumassa, erityistä huolellisuutta on noudatettava käytettäessä PecFentiä iäkkäillä. Tietoja PecFentin farmakokinetiikasta iäkkäillä potilailla ei ole saatavilla.
Maksan tai munuaisten vajaatoiminta
PecFentiä tulee annostella varoen keskivaikeaa tai vaikeaa maksan tai munuaisten vajaatoimintaa sairastavilla potilailla (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Pediatriset potilaat
PecFent-valmisteen turvallisuutta ja tehoa lasten ja alle 18 vuoden ikäisten nuorten hoidossa ei ole vielä varmistettu.
Tietoja ei ole saatavilla.
Antotapa
Vain nenään.
Pullo tulee poistaa lapsiturvallisesta pakkauksesta vasta välittömästi ennen käyttöä ja suojakorkki on poistettava. Pullo tulee ensin valmistaa käyttökuntoon pitämällä sitä pystysuorassa ja painamalla alas suutinta ympäröivää reunusta kummaltakin puolelta, kunnes laskinruutuun ilmaantuu vihreä pylväs (sen tulisi ilmaantua neljän suihkeen jälkeen).
Jos valmistetta ei ole käytetty yli 5 vuorokauteen, pullo on valmisteltava uudelleen käyttökuntoon suihkauttamalla kerran. Potilasta tulee neuvoa kirjoittamaan ensimmäisen käyttökerran päivämäärä sitä varten varatulle alueelle lapsiturvallisen pakkauksen myyntipäällysmerkinnöissä.
PecFent annostellaan asettamalla suuttimen pää jonkin verran (noin 1 cm) sieraimen sisään tähdäten hieman nenänselkää kohti. Suihke annostellaan sitten painamalla ja vapauttamalla sormipitimet suuttimen kummallakin puolella. Tällöin kuuluu napsahdus, ja laskinruudussa näkyvä numero etenee yhdellä.
Potilaille on kerrottava, ettei suihkeen annostelu ehkä tunnu missään ja että heidän on sen vuoksi luotettava kuuluvaan napsahdukseen ja laskinruudussa etenevään numeroon merkkinä siitä, että suihke on annosteltu.
PecFentin suihkepisarat muodostavat geelin nenän sisällä. Potilaita on neuvottava olemaan niistämättä nenäänsä välittömästi PecFentin annostelun jälkeen.
Suojakorkki on asetettava paikoilleen jokaisen käytön jälkeen ja pullo laitettava takaisin lapsiturvalliseen pakkaukseen turvallista säilytystä varten.
Vasta-aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille.
Potilaat, jotka eivät käytä opioideja ylläpitohoitona, sillä hengityslaman vaara suurenee.
Vakava hengityslama tai vakavat tukkeuttavat keuhkosairaudet.
Akuutin kivun, muun kuin läpilyöntikivun, hoito.
Potilaat, jotka saavat hoitoa natriumoksibaattia sisältävillä lääkevalmisteilla.
Varoitukset ja käyttöön liittyvät varotoimet
Vahingossa tapahtuvaan altistumiseen, virheelliseen käyttöön ja väärinkäyttöön liittyvien, myös kuolemaan johtavien, riskien vuoksi potilaita ja heidän hoitajiaan on kehotettava säilyttämään PecFent-valmiste turvallisessa paikassa, johon muilla ei ole pääsyä.
Potilaita ja heidän huoltajiaan on varoitettava siitä, että PecFent sisältää vaikuttavaa ainetta siinä määrin, että se voi olla hengenvaarallista lapselle.
Opioideihin liittyvien haittavaikutusten minimoimiseksi ja tehokkaan annoksen tunnistamiseksi on erityisen tärkeätä, että terveydenhuoltohenkilökunta tarkkailee potilaita huolellisesti titraatiovaiheen aikana.
On tärkeätä, että pitkävaikutteiselle opioidihoidolle potilaan jatkuvaan kipuun on määritetty vakaa annos ennen PecFent-hoidon aloittamista.
Hyperalgesia
Kuten muitakin opioideja käytettäessä, jos fentanyylinannoksen suurentaminen ei johda riittävään kivun hallintaan, on huomioitava opioidien aiheuttaman hyperalgesian mahdollisuus. Fentanyyliannoksen pienentäminen, fentanyylihoidon lopettaminen tai taustakipuun annettavan hoidon muuttaminen saattavat olla tarpeen.
Hengityslama
Fentanyylin käyttöön liittyy kliinisesti merkittävän hengityslaman riski. Kroonista opioidihoitoa saaville kipupotilaille kehittyy hengityslaman sietokyky ja sen vuoksi hengitystielaman riski näillä potilailla vähentyy. Keskushermostoa lamauttavien lääkkeiden samanaikainen käyttö saattaa lisätä hengityslaman riskiä (ks. kohta Yhteisvaikutukset).
Krooninen keuhkosairaus
Kroonisia keuhkoahtaumasairauksia potevilla potilailla fentanyyli saattaa aiheuttaa vakavampia haittavaikutuksia. Näillä potilailla opioidit saattavat heikentää hengitysrefleksiä ja lisätä hengitystieresistenssiä.
Lisääntynyt kallonsisäinen paine
PecFentiä tulee annostella äärimmäistä varovaisuutta noudattaen potilailla, joilla saattaa olla erityinen taipumus CO2-retention kallonsisäisille vaikutuksille, esim. kun on näyttöä lisääntyneestä kallonsisäisestä paineesta tai alentuneesta tajunnantasosta. Opioidit saattavat peittää kliinisen sairauden kulun potilailla, joilla on päävamma, ja niitä tulee käyttää ainoastaan silloin, kun käyttö on kliinisesti perusteltua.
Sydänsairaus
Fentanyyli voi aiheuttaa bradykardiaa. PecFentin käytössä on sen vuoksi noudatettava varovaisuutta, jos potilaalla on entuudestaan tai on aikaisemmin ollut hitaita rytmihäiriöitä.
Maksan tai munuaisten vajaatoiminta
Lisäksi PecFentiä tulee annostella varoen maksan tai munuaisten vajaatoimintaa sairastaville potilaille. Maksan tai munuaisten vajaatoiminnan vaikutusta lääkevalmisteen farmakokinetiikkaan ei ole tutkittu. Laskimonsisäisesti annosteltuna fentanyylin puhdistuman on kuitenkin osoitettu muuttuvan maksan ja munuaisten vajaatoiminnassa metabolisen puhdistuman ja plasman proteiinien muutosten vuoksi. Titraatiovaiheessa on sen takia noudatettava erityistä huolellisuutta keskivaikeaa tai vaikeaa maksan tai munuaisten vajaatoimintaa sairastavilla potilailla.
Hoitoa on harkittava tarkkaan potilailla, joilla on hypovolemiaa ja hypotensiota.
Toleranssi ja opioidien käyttöhäiriö (väärinkäyttö ja riippuvuus)
Sietokyvyn kasvu sekä fyysisen ja/tai psykologisen riippuvuuden kehittyminen on mahdollista opioidien kuten fentanyylin toistuvien annostelujen yhteydessä.
PecFent-valmisteen toistuva käyttö saattaa johtaa opioidien haitalliseen käyttöön. Opioidihoidon annoksen suurentaminen ja keston pidentäminen voivat lisätä opioidien käyttöhäiriön kehittymisen riskiä. PecFent-valmisteen väärinkäytöstä tai tarkoituksellisesta virheellisestä käytöstä voi aiheutua yliannostus ja/tai kuolema. Opioidien haitallisen käytön kehittymisen riski on suurentunut potilailla, joilla itsellään tai joiden sukulaisella (vanhemmilla tai sisaruksilla) on ollut päihteiden käyttöä (mukaan lukien alkoholismia), tupakoivilla potilailla ja potilailla, joilla on ollut muita mielenterveyshäiriöitä (esim. vakava masennus, ahdistuneisuus tai persoonallisuushäiriö).
Ennen PecFent-valmisteen käytön aloittamista ja hoidon aikana on sovittava potilaan kanssa hoitotavoitteista ja hoidon lopettamista koskevasta suunnitelmasta (ks. kohta Annostus ja antotapa). Potilaalle on ennen hoitoa ja sen aikana kerrottava myös opioidien käyttöhäiriön riskeistä ja merkeistä. Potilaita on kehotettava ottamaan yhteyttä lääkäriin, jos näitä merkkejä ilmenee.
Potilaita on seurattava päihdehakuisen käyttäytymisen merkkien (esim. liian tiheän lääkemääräysten tarpeen) havaitsemiseksi. Seurantaan sisältyy myös muiden opioidien ja psykoaktiivisten lääkkeiden (kuten bentsodiatsepiinien) samanaikaisen käytön tarkkailu. Jos potilaalla on opioidien haitalliseen käyttöön liittyviä merkkejä ja oireita, on harkittava päihderiippuvuuksiin erikoistuneen lääkärin konsultoimista.
Urheilijoita tulee varoittaa, että fentanyylihoito voi aiheuttaa positiivisen tuloksen doping-testissä.
Serotoniinioireyhtymä
Varovaisuutta on noudatettava, kun PecFentiä annetaan yhdessä serotoninergisiin välittäjäainejärjestelmiin vaikuttavien lääkevalmisteiden kanssa.
Mahdollisesti henkeä uhkaava serotoniinioireyhtymä saattaa kehittyä ja ilmetä käytettäessä samanaikaisesti serotoninergisiä lääkevalmisteita, kuten selektiivisiä serotoniinin takaisinoton estäjiä (SSRI‑lääkkeitä) ja serotoniinin ja noradrenaliinin takaisinoton estäjiä (SNRI‑lääkkeitä), ja käytettäessä lääkevalmisteita, jotka heikentävät serotoniinin metaboliaa (mukaan lukien monoamiinioksidaasin estäjät [MAO:n estäjät]). Tämä saattaa tapahtua suositeltua annosta käytettäessä (ks. kohta Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset).
Serotoniinioireyhtymän oireita saattavat olla psyykkisen tilan muutokset (esim. agitaatio, aistiharhat, kooma), autonomisen hermoston epävakaus (esim. takykardia, verenpainemuutokset, hypertermia), hermo-lihastoiminnan poikkeavuudet (esim. heijasteiden vilkastuminen, koordinaatiokyvyn heikkeneminen, jäykkyys) ja/ tai ruoansulatuskanavan oireet (esim. pahoinvointi, oksentelu, ripuli).
Jos serotoniinioireyhtymää epäillään, PecFent-hoito pitää lopettaa.
Antoreitti
PecFent on tarkoitettu annosteltavaksi vain nenään. Mitään muita annostelureittejä ei saa käyttää. Valmisteen apuaineiden fysikaaliskemiallisten ominaisuuksien vuoksi varsinkin laskimon- tai valtimonsisäistä injektiota on vältettävä.
Nenän vaivat
Jos potilaalla esiintyy toistuvia nenäverenvuotoja tai nenävaivoja PecFentin ottamisen yhteydessä, tulee harkita vaihtoehtoista, muulla tavalla annosteltavaa hoitoa läpilyöntikipuun.
Unenaikaiset hengityshäiriöt
Opioidit voivat aiheuttaa unenaikaisia hengityshäiriöitä, kuten sentraalista uniapneaa ja unenaikaista hypoksemiaa. Opioidien käyttö suurentaa sentraalisen uniapnean riskiä annosriippuvaisesti. Jos potilaalla on sentraalista uniapneaa, opioidien kokonaisannoksen pienentämistä on harkittava.
Samanaikainen käyttö sedatiivien kanssa
PecFentin ja sedatiivisten lääkkeiden, kuten bentsodiatsepiinien tai vastaavien lääkeaineiden, samanaikainen käyttö saattaa aiheuttaa sedaatiota, hengityslamaa, kooman ja kuoleman. Näiden riskien vuoksi PecFentiä saa määrätä samanaikaisesti tällaisten sedatiivisten lääkkeiden kanssa vain potilaille, joille muut hoitovaihtoehdot eivät ole mahdollisia. Jos PecFentiä päätetään määrätä samanaikaisesti sedatiivisten lääkkeiden kanssa, on käytettävä pienintä mahdollista tehokasta annosta ja hoidon keston on oltava mahdollisimman lyhyt.
Potilaita on seurattava huolellisesti hengityslaman ja sedaation oireiden ja merkkien varalta.
Tämän vuoksi on erittäin suositeltavaa, että potilasta ja hänen hoitajiaan neuvotaan kiinnittämään huomiota näihin oireisiin (ks. kohta Yhteisvaikutukset).
PecFentin apuaineet
PecFent sisältää propyyliparahydroksibentsoaattia (E 216). Propyyliparahydroksibentsoaatti voi aiheuttaa allergisia reaktioita (mahdollisesti viivästyneitä) ja poikkeustapauksissa bronkospasmia (jos lääkevalmistetta ei annostella oikein).
Yhteisvaikutukset
Natriumoksibaattia sisältävien lääkevalmisteiden ja fentanyylin samanaikainen käyttö on vasta-aiheista (ks. kohta Vasta-aiheet). Natriumoksibaattihoito on lopetetettava ennen PecFent-hoidon aloittamista.
Fentanyyli metaboloituu ihmisellä pääasiassa sytokromi P450 3A4 -isoentsyymijärjestelmän kautta (CYP3A4), joten yhteisvaikutukset ovat mahdollisia, kun PecFent-valmistetta käytetään samanaikaisesti CYP3A4-entsyymin toimintaan vaikuttavien lääkevalmisteiden kanssa. Samanaikainen käyttö CYP3A4-entsyymin toimintaa indusoivien lääkevalmisteiden kanssa saattaa heikentää PecFent-valmisteen tehoa. PecFent-valmisteen käyttö yhdessä voimakkaiden CYP3A4-estäjien (kuten ritonaviirin, ketokonatsolin, itrakonatsolin, troleandomysiinin, klaritromysiinin ja nelfinaviirin) tai keskivahvojen CYP3A4-estäjien (kuten amprenaviirin, aprepitantin, diltiatseemin, erytromysiinin, flukonatsolin, fosamprenaviirin ja verapamiilin) kanssa saattaa suurentaa fentanyylin pitoisuuksia plasmassa; tästä voi mahdollisesti aiheutua vakavia haittavaikutuksia mukaan lukien kuolemaan johtava hengityslama. Jos potilas saa PecFent-valmistetta samaan aikaan keskivahvojen tai voimakkaiden CYP3A4-estäjien kanssa, hänen tilaansa tulee seurata huolellisesti pitkän aikaa. Annosta tulee suurentaa varoen.
Samanaikainen muiden keskushermostoa lamaavien aineiden, mukaan lukien muiden opioidien, sedatiivien tai unilääkkeiden, yleisanesteettien, fenotiatsiinien, rauhoituslääkkeiden, lihasrelaksanttien, gabapentinoidien (gabapentiinin tai pregabaliinin), sedatiivisten antihistamiinien ja alkoholin, käyttö saattaa lisätä lamaavaa vaikutusta. Opiodien ja sedatiivisten lääkkeiden, kuten bentsodiatsepiinien tai vastaavien lääkevalmisteiden, samanaikainen käyttö lisää sedaation, hengityslaman, kooman ja kuoleman riskiä additiivisen keskushermostoa lamaavan vaikutuksen vuoksi. Sedatiivisten lääkkeiden pienintä tehokasta annosta on käytettävä, ja samanaikaisen käytön kestoa on rajoitettava (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Serotoninergiset lääkevalmisteet
Fentanyylin antaminen samanaikaisesti serotoninergisen lääkevalmisteen, kuten selektiivisen serotoniinin takaisinoton estäjän (SSRI) tai serotoniinin ja noradrenaliinin takaisinoton estäjän (SNRI) tai monoamiinioksidaasin estäjän (MAO:n estäjän), kanssa saattaa lisätä mahdollisesti henkeä uhkaavan sairauden, serotoniinioireyhtymän, riskiä.
PecFentin käyttö ei ole suositeltavaa, jos potilas on käyttänyt MAO:n estäjiä edeltävien 14 päivän aikana, sillä MAO:n estäjien on ilmoitettu voimistaneen opioidikipulääkkeiden vaikutuksia. Vaikutus on ollut voimakas ja ennalta-arvaamaton.
Osittaisten opioidiagonistien/-antagonistien (kuten buprenorfiinin, nalbufiinin, pentatsosiinin) samanaikaista käyttöä ei suositella. Niillä on suuri affiniteetti opioidireseptoreihin ja suhteellisen vähäinen ominaisvaikutus, ja sen vuoksi ne antagonisoivat osittain fentanyylin analgeettista tehoa ja saattavat aiheuttaa vieroitusoireita potilaille, jotka ovat riippuvaisia opioideista.
Nenään annosteltavan oksimetatsoliinin samanaikaisen käytön on osoitettu vähentävän PecFentin imeytymistä (ks. kohta Farmakokinetiikka). Nenään annosteltavien vasokonstriktiivisten dekongestanttien samanaikaista käyttöä titrauksen aikana ei sen vuoksi suositella, sillä se voi johtaa siihen, että potilaat titraavat tarvetta suuremman annoksen. PecFent-ylläpitohoito saattaa myös olla vähemmän tehokasta riniittiä sairastavilla potilailla, jos lääkettä käytetään samanaikaisesti nenään annosteltavan vasokonstriktiivisen dekongestantin kanssa. Jos näin tapahtuu, potilasta tulee neuvoa lopettamaan dekongestantin käyttö.
PecFent-valmisteen ja muiden nenään annosteltavien tuotteiden (muiden kuin oksimetatsoliinin) yhteiskäyttöä ei ole arvioitu kliinisissä tutkimuksissa. Muita nenään annosteltavia hoitoja tulee välttää 15 minuutin ajan PecFentin annostelun jälkeen.
Raskaus ja imetys
Raskaus
Ei ole olemassa riittävästi tietoja fentanyylin käytöstä raskaana oleville naisille. Eläinkokeissa on havaittu lisääntymistoksisuutta (ks. kohta Prekliiniset tiedot turvallisuudesta). Mahdollista riskiä ihmisille ei tunneta. PecFent-valmistetta ei pidä käyttää raskauden aikana, mikäli käyttö ei ole selvästi välttämätöntä.
Pitkään kestäneen käytön jälkeen fentanyyli saattaa aiheuttaa vieroitusoireita vastasyntyneelle lapselle. Fentanyylin käyttö synnytyksen aikana ei ole suositeltavaa (ei myöskään keisarileikkauksen aikana), sillä fentanyyli läpäisee istukan ja saattaa aiheuttaa hengityslaman sikiölle. Jos PecFent-valmistetta käytetään, vastalääkettä lasta varten tulee olla välittömästi saatavilla.
Imetys
Fentanyyli erittyy ihmisen rintamaitoon ja saattaa aiheuttaa sedaatiota ja hengityslamaa imetettävälle lapselle. Imettävien naisten ei pidä käyttää fentanyyliä, eikä imetystä saa jatkaa ennen kuin vähintään 5 vuorokautta viimeisen fentanyyliannoksen jälkeen.
Hedelmällisyys
Kliinisiä tietoja fentanyylin vaikutuksesta fertiliteettiin ei ole.
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Opioidikipulääkkeet voivat heikentää ajettaessa tai koneita käytettäessä tarvittavaa psyykkistä ja/tai fyysistä suorituskykyä.
Potilaita tulee neuvoa olemaan ajamatta tai käyttämättä koneita, jos heillä esiintyy uneliaisuutta, heitehuimausta, näköhäiriöitä tai muita haittavaikutuksia, jotka voivat heikentää ajokykyä ja koneiden käyttökykyä.
Haittavaikutukset
Turvallisuustietojen yhteenveto
PecFent-valmisteen käytön aikana on odotettavissa tyypillisiä opioidien haittavaikutuksia. Ne häviävät tai lievenevät usein lääkevalmisteen käytön jatkuessa, kun potilaalle titrataan sopivin annos. Vakavimpia haittavaikutuksia ovat kuitenkin hengityslama (voi johtaa hengityskatkoihin tai hengityspysähdykseen), verenkiertolama, hypotensio ja sokki, ja kaikkien potilaiden tilaa tulee seurata huolellisesti näiden haittavaikutusten varalta.
PecFent-valmisteen kliinisissä tutkimuksissa arvioitiin valmisteen turvallisuutta ja tehoa läpilyöntikivun hoidossa. Kaikki potilaat käyttivät myös samanaikaisesti opioideja, kuten hitaasti vapautuvaa morfiinia tai ihon läpi annettavaa fentanyyliä, jatkuvan kivunhoitoon. Näin ollen pelkän PecFent-valmisteen vaikutuksia ei ollut mahdollista erottaa ehdottomalla varmuudella.
Haittavaikutustaulukko
Kliinisissä tutkimuksissa ja myyntiluvan saamisen jälkeisessä haittavaikutusseurannassa on raportoitu PecFentin ja/tai muiden fentanyyliä sisältävien yhdisteiden käytön yhteydessä seuraavia haittavaikutuksia (seuraavien esiintymistiheyksien mukaan: hyvin yleinen (≥ 1/10), yleinen (≥ 1/100, < 1/10), melko harvinainen (≥ 1/1 000, < 1/100), harvinainen (≥ 1/10 000, < 1/1 000), hyvin harvinainen (<1/10 000); tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin)).
| Yleinen | Melko harvinainen | Tuntematon |
|---|---|---|---|
| Infektiot | Keuhkokuume Nasofaryngiitti Faryngiitti Riniitti | ||
| Veri ja imukudos | Neutropenia | ||
| Immuunijärjestelmä | Yliherkkyys | ||
| Aineenvaihdunta ja ravitsemus | Dehydraatio Hyperglykemia Ruokahalun vähentyminen Ruokahalun lisääntyminen | ||
| Psyykkiset häiriöt | Desorientaatio | Houretilat Aistiharhat Sekavuustilat Masennus Tarkkaavuus- ja ylivilkkaushäiriö Ahdistuneisuus Euforia Hermostuneisuus | Unettomuus Lääkeriippuvuus (addiktio) Lääkkeen väärinkäyttö |
| Hermosto | Makuhäiriöt Heitehuimaus Uneliaisuus Päänsärky | Tajuttomuus Tajunnan tason lasku Kouristukset Makuaistin puute Anosmia Muistin huononeminen Parosmia Puhehäiriöt Sedaatio Letargia Vapina | |
| Kuulo ja tasapainoelin | Vertigo | ||
| Sydän | Syanoosi | ||
| Verisuonisto | Kardiovaskulaarinen vajaatoiminta Lymfedeema Hypotensio Kuumat aallot | Punastuminen | |
| Hengityselimet, rintakehä ja välikarsina | Nenäverenvuoto Voimakas nuha Nenävaivat (kuten nenän kirvely)
| Ylähengitysteiden ahtauma Nielun ja kurkunpään kipu Rinalgia Nenän limakalvojen sairaus Yskä Hengenahdistus Aivastelu Ylähengitysteiden kongestio Nenän kongestio Nenänsisäinen hypestesia Kurkun ärsytys Takanielun limaisuus Nenän kuivuus | Hengityslama |
| Ruoansulatuselimistö | Oksentelu Pahoinvointi Ummetus | Suolen perforaatio Vatsakalvotulehdus Suun hypestesia Suun parestesia Ripuli Yökkäily Vatsakipu Kielen sairaus Suun haavaumat Dyspepsia Suun kuivuminen | |
| Iho ja ihonalainen kudos | Kutina | Hyperhidroosi Nokkosihottuma | |
| Luusto, lihakset ja sidekudos | Artralgia Lihasnykäykset | ||
| Munuaiset ja virtsatiet | Virtsanerityksen puute Kivulias virtsaaminen Valkuaisvirtsaisuus Virtsaamisarkuus | ||
| Sukupuolielimet ja rinnat | Emättimen verenvuoto | ||
| Yleisoireet ja antopaikassa todettavat haitat | Muu kuin sydänperäinen rintakipu Astenia Vilunväreet Kasvojen turvotus Perifeerinen edeema Kävelyhäiriö Kuume Uupumus Huonovointisuus Jano | Vieroitusoireyhtymä* Vastasyntyneen vieroitusoireyhtymä, lääketoleranssi | |
| Tutkimukset | Verihiutaleiden väheneminen Painon nousu | ||
| Vammat, myrkytykset ja hoitokomplikaatiot | Kaatuminen Tarkoituksellinen lääkkeen väärinkäyttö Lääkitysvirhe |
*Opioidivieroitusoireita, kuten pahoinvointia, oksentelua, ripulia, ahdistuneisuutta, vilunväreitä, vapinaa ja hikoilua, on havaittu limakalvon läpi imeytyvän fentanyylin käytön yhteydessä.
Kuvaus valikoiduista haittavaikutuksista
Toleranssi
Toleranssi voi kehittyä toistuvan käytön seurauksena.
Lääkeriippuvuus
PecFent-valmisteen toistuva käyttö voi johtaa lääkeriippuvuuteen, vaikka sitä käytetään hoitoannoksina. Lääkeriippuvuuden riski voi vaihdella potilaan yksilöllisten riskitekijöiden, annostuksen ja opioidihoidon keston mukaan (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
On oletettavaa, että fentanyylin yliannostuksen oireet nenään annosteltaessa ovat samankaltaisia kuin sen ja muiden opioidien vaikutukset laskimonsisäisesti annosteltaessa ja että ne kuuluvat aineen farmakologisiin vaikutuksiin. Vakavin merkittävä vaikutus on hengityslama. Myös kooma on mahdollinen.
Opioidien yliannostuksen välittömiin hoitotoimenpiteisiin kuuluu hengitystien varmistaminen, potilaan fyysinen ja sanallinen stimulaatio, tajunnan tason, hengityksen ja verenkierron statuksen arviointi sekä avustettu ventilaatio (hengitystuki) tarpeen mukaan.
Fentanyylin yliannostuksen yhteydessä on havaittu myös toksista leukoenkefalopatiaa.
Hoidettaessa (vahingossa tapahtunutta) yliannostusta henkilöllä, joka ei ole aikaisemmin saanut opioideja, on varmistettava laskimonsisäinen annostelureitti, ja naloksonia tai muita opioidiantagonisteja tulee käyttää kliinisen tilan mukaan. Yliannostuksen jälkeisen hengityslaman kesto saattaa olla pitempi kuin opioidiantagonistin vaikutuksen pituus (esim. naloksonin puoliintumisaika vaihtelee välillä 30–81 minuuttia), joten lisäannostelu saattaa olla tarpeen. Tiedot tällaisesta käytöstä on tarkistettava yksittäisen opioidiantagonistin valmisteyhteenvedosta.
Yliannostuksen hoidossa potilailla, jotka saavat opioideja ylläpitohoitona, on varmistettava laskimonsisäinen annostelureitti. Hyvin harkittu naloksonin tai muun opioidiantagonistin käyttö saattaa olla asianmukaista joissakin tapauksissa, mutta se saattaa nopeuttaa akuutin vieroitusoireyhtymän syntymistä.
On huomioitava, että vaikka tilastollisesti merkitsevää Cmax-tasojen nousua todettiin toisen PecFent-annoksen jälkeen, kun se annettiin joko yhden tai kahden tunnin kuluttua aloitusannoksesta, tämän nousun ei katsota olevan tarpeeksi suuri, jotta se aiheuttaisi kliinisesti merkittävää kertymistä tai liika-altistusta. Näin ollen suositeltu annosteluväli 4 tuntia sisältää leveän turvamarginaalin.
Vaikka PecFentin käytön jälkeisestä hengitykseen vaikuttavasta lihasjäykkyydestä ei ole näyttöä, sen mahdollisuus liittyy fentanyylin ja muiden opioidien käyttöön. Jos oire ilmaantuu, se tulee hoitaa avustetun ventilaation, opioidiantagonistin tai viimeisenä vaihtoehtona neuromuskulaarisen salpaajan avulla.
Fentanyylin yliannostustapauksissa on havaittu Cheyne-Stokesin hengitystä etenkin potilailla, joilla on anamneesissa sydämen vajaatoiminta.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Analgeetit, opioidit, fenyylipiperidiinijohdokset; ATC-koodi: N02A B03.
Vaikutusmekanismi
Fentanyyli on opioidikipulääke, joka vaikuttaa pääasiassa μ-opioidireseptorin kanssa. Sen ensisijaisia terapeuttisia vaikutuksia ovat kivunlievitys ja sedaatio. Toissijaisia farmakologisia vaikutuksia ovat hengityslama, bradykardia, hypotermia, ummetus, mioosi, fyysinen riippuvuus ja euforia.
Opioidit saattavat vaikuttaa hypotalamus-aivolisäke-lisämunuaisakseliin tai hypotalamus-aivolisäke-sukupuolirauhasakseliin. Havaittavia muutoksia ovat muun muassa seerumin prolaktiinipitoisuuden nousu ja plasman kortisoli- ja testosteronipitoisuuksien lasku. Nämä hormonaaliset muutokset saattavat aiheuttaa kliinisiä merkkejä ja oireita.
Farmakodynaamiset vaikutukset
Kaksoissokkoutetussa, satunnaistetussa, lumekontrolloidussa vaihtovuoroisessa tutkimuksessa 114 potilasta, joilla oli keskimäärin 1–4 läpilyöntikipukohtausta vuorokaudessa saadessaan opioideja ylläpitohoitona, osallistui ensin avoimeen titraatiovaiheeseen, jossa määritettiin tehokas PecFent-annos (Tutkimus CP043). Kaksoissokkovaiheeseen jatkaneet potilaat hoitivat enintään kymmentä läpilyöntikipukohtausta satunnaisessa järjestyksessä joko PecFentillä (7 kohtausta) tai lumelääkkeellä (3 kohtausta).
Titraatiovaiheeseen mukaan otetuista potilaista vain seitsemälle (6,1 %) ei onnistuttu titraamaan tehokasta annosta huonon hoitovasteen vuoksi. Kuusi potilasta (5,3 %) luopui tutkimuksesta haittavaikutusten vuoksi.
Primaarinen päätetapahtuma oli kivun vahvuuden eron summan vertailu 30 minuutin kuluttua annostelusta (SPID30), joka oli PecFent-hoitoa saaneissa kohtauksissa 6,57 ja lumehoitoa saaneissa 4,45 (p < 0,0001). SPID PecFentillä hoidetuissa kohtauksissa erosi merkitsevästi lumelääkkeellä hoidetuista myös 10, 15, 45 ja 60 minuuttia annostelusta.
Keskimääräistä kivun voimakkuutta osoittavat pisteet (73 potilasta) kaikissa PecFentillä hoidetuissa kohtauksissa (459 kohtausta) olivat merkitsevästi alhaisempia kuin lumelääkkeellä hoidetuissa kohtauksissa (200 kohtausta) 5, 10, 15, 30, 45 ja 60 minuuttia annostelun jälkeen (ks. Kuva 1).
Kuva 1: Keskimääräiset (± SE) kivun voimakkuutta osoittavat pisteet jokaisessa aikapisteessä (modified intent to treat, mITT-väestö)
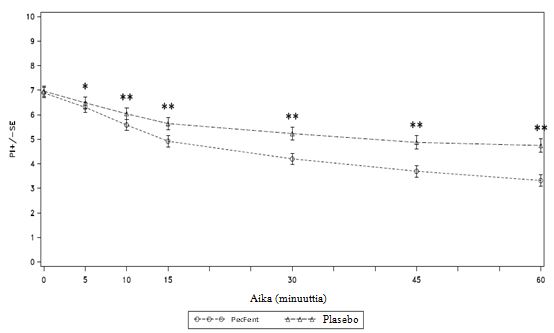
Kivun voimakkuutta osoittavat pisteet (koehenkilöiden keskiarvojen keskiarvo) PecFentin ja plasebon annostelun jälkeen.
*Merkitsevä ero havaittu tasolla alfa <= 0,05 PecFentin ja plasebon välillä kyseisessä aikapisteessä.
**Merkitsevä ero havaittu tasolla alfa <= 0,01 PecFentin ja plasebon välillä kyseisessä aikapisteessä.
PecFentin parempaa tehoa lumelääkkeeseen nähden tukivat sekundaaristen päätetapahtumien tulokset mukaan lukien sellaisten kohtausten lukumäärä, joihin saatiin kliinisesti merkittävää kivun lievitystä (kliinisesti merkittävä kivun lievitys määriteltiin vähintään 2:n pisteen laskuna kivun voimakkuutta kuvaavalla asteikolla) (kuva 2).
Kuva 2: Kliinisesti merkittävä kivunlievitys – PecFent ja lumelääke: % potilaiden kohtauksista, joihin saatiin ≥ 2 pisteen kivun voimakkuuden lasku
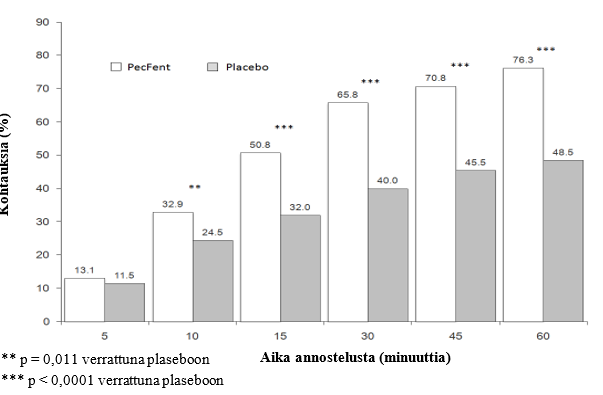
Kaksoissokkoutetussa, satunnaistetussa verrokkitutkimuksessa (Tutkimus 044), joka oli samantyyppinen kuin Tutkimus 043 ja joka tehtiin opioideja sietävillä potilailla, joilla oli syövän aiheuttamaa läpilyöntikipua saadessaan säännöllistä opioidihoitoa vakaina annoksina, PecFentin osoitettiin olevan välittömästi vapautuvaa morfiinisulfaattia (IRMS) parempi. Paremmuus osoitettiin primaarisella lopputapahtumalla, kivun voimakkuuserolla (PID) 15 minuutin kuluessa annostelusta, joka oli 3,02 PecFentiä saaneilla ja 2,69 IRMS:ää saaneilla (p = 0,0396).
Pitkäkestoisessa, avoimessa turvallisuustutkimuksessa (Tutkimus 045) 355 potilasta osallistui 16 viikon pituiseen hoitovaiheeseen, jonka aikana 42 227 syövän läpilyöntikipukohtausta (BTP) hoidettiin PecFentillä. Potilaista 100 jatkoi hoitoa vielä korkeintaan 26 kuukauden ajan tutkimuksen jatkovaiheessa. Avoimessa hoitovaiheessa hoidetuista 355 potilaasta 90 %:lla ei annosta tarvinnut nostaa.
Satunnaistetussa, lumekontrolloidussa tutkimuksessa (CP043) 9,4 % PecFentillä hoidetuista 459 läpilyöntikipukohtauksesta 73 potilaalla vaati muuta (hätä)lääkitystä 60 minuutin sisällä annostelusta. Pitkäkestoisessa, avoimessa tutkimuksessa (CP045) vastaava osuus oli 6,0 % 42 227 kohtauksesta 355 potilaalla, jotka saivat PecFent-hoitoa jopa 159 päivän ajan.
Farmakokinetiikka
Yleistä
Fentanyyli on hyvin lipofiilinen ja se voi imeytyä nopeasti nenän limakalvojen läpi sekä hitaammin maha-suolikanavan kautta. Se käy läpi ensikierron metabolian maksassa ja suolessa, eivätkä sen metaboliitit vaikuta fetanyylin terapeuttiseen tehoon.
PecFent hyödyntää PecSys-nenälääkeannostelujärjestelmää, joka vaikuttaa fentanyylin annosteluun ja imeytymiseen. PecSys-järjestelmän ansiosta valmiste voidaan suihkuttaa nenäontelon etuosaan hienona pisarasumuna, joka muuttuu geeliksi kun se joutuu kosketukseen nenän limakalvoilla olevien kalsiumionien kanssa. Fentanyyli hajaantuu geelistä ja imeytyy nenän limakalvojen läpi. Fentanyylin imeytyminen geelistä rajoittaa plasman huippupitoisuutta (Cmax) ja tekee samalla mahdolliseksi sen nopean saavuttamisen (Tmax).
Imeytyminen
Farmakokineettisessä tutkimuksessa, jossa vertailtiin PecFentiä (100, 200, 400 ja 800 mikrogrammaa) suun kautta annettavaan limakalvon läpi imeytyvään fentanyylisitraattiin (OTFC, 200 mikrogrammaa), fentanyylin osoitettiin imeytyvän nopeasti PecFentin nenään annetun kerta-annoksen jälkeen, jolloin Tmax-arvon mediaani oli 15–21 minuuttia (OTCF:n Tmax oli noin 90 minuuttia). Fentanyylin farmakokinetiikka vaihteli suuresti sekä PecFent- että OTFC-hoidon jälkeen. PecFent-hoidon fentanyylin suhteellinen biologinen hyötyosuus 200 mikrogrammaan OTFC:tä verrattaessa oli noin 120 %.
Pääasialliset farmakokineettiset parametrit on esitetty seuraavassa taulukossa.
Farmakokineettiset parametrit aikuisilla koehenkilöillä, jotka saivat PecFentiä ja OTFC:tä
| Farmakokineettiset parametrit (keskiarvo (% CV) | PecFent | OTFC | |||
| 100 mikrog | 200 mikrog | 400 mikrog | 800 mikrog | 200 mikrog | |
| Tmax (tuntia)* | 0,33 (0,08–1,50) | 0,25 (0,17–1,60) | 0,35 (0,25–0,75) | 0,34 (0,17–3,00) | 1,50 (0,50–8,00) |
| Cmax (pg/ml) | 351,5 (51,3) | 780,8 (48,4) | 1552,1 (26,2) | 2844,0 (56,0) | 317,4 (29,9) |
| AUC (pg/h/ml) | 2460,5 (17,9) | 4359,9 (29,8) | 7513,4 (26,7) | 17272 (48,9) | 3735,0 (32,8) |
| t1/2 (tuntia) | 21,9 (13,6) | 24,9 (51,3) | 15,0 (24,7) | 24,9 (92,5) | 18,6 (31,4) |
* Tmax-luvut esitetty mediaanina (vaihteluväli).
Jokaisen annostason käyrät ovat samanlaisia muodoltaan; nousevat annostasot nostavat fentanyylin tasoja plasmassa. Cmax-arvolle ja pitoisuuspinta-alalle (AUC) suhteellisuus annokseen nähden osoitettiin annosvälillä 100–800 mikrogrammaa (ks. kuva 3). Jos potilaalle vaihdetaan PecFent jonkin muun läpilyöntikipukohtauksien hoitoon käytettävän fentanyylivalmisteen tilalle, PecFent-annos on titrattava erikseen, sillä biologinen hyötyosuus eri valmisteiden välillä vaihtelee merkittävästi.
Kuva 3: Plasman keskimääräiset fentanyylipitoisuudet PecFent- ja OTCF-kerta-annosten jälkeen terveillä koehenkilöillä
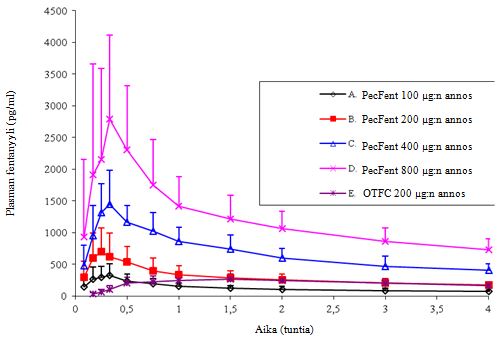
PecFentin kerta-annoksen imeytymisen ja siedettävyyden arvioimiseksi potilailla, joilla oli siitepölyn aiheuttama kausiluontoinen allerginen riniitti, suoritettiin farmakokineettinen tutkimus, jossa verrattiin altistumatonta tilaa, akuutisti altistunutta (riniittistä) tilaa sekä akuutisti altistunutta tilaa, jota hoidettiin oksimetatsoliinilla.
Akuutti riniitti ei vaikuttanut kliinisesti merkittävästi Cmax:iin, Tmax :iin tai yleiseen fentanyylialtistukseen, kun verrattiin altistumatonta tilaa akuutisti altistuneisiin tiloihin. Kun akuuttia riniittistä tilaa oli hoidettu oksimetatsoliinilla, Cmax ja altistuminen laskivat ja Tmax nousi tilastollisesti merkitsevästi ja mahdollisesti myös kliinisesti merkittävästi.
Jakautuminen
Fentanyyli on erittäin lipofiilinen ja se jakautuu hyvin muuallekin kuin verisuonistoon. Sen jakautumistilavuus on ilmeisen suuri. Eläinkokeista saadut tiedot ovat osoittaneet, että imeytymisen jälkeen fentanyyli jakautuu nopeasti aivoihin, sydämeen, keuhkoihin, munuaisiin ja pernaan. Tätä seuraa hitaampi uudelleenjakautuminen lihaksiin ja rasvakudokseen.
Fentanyyli sitoutuu plasman proteiineihin 80–85-prosenttisesti. Pääasiallinen sitojaproteiini on alfa-1-happo-glykoproteiini, mutta sekä albumiini että lipoproteiinit osallistuvat jossain määrin. Fentanyylin vapaa fraktio lisääntyy asidoosin myötä.
Biotransformaatio
PecFentin nenään annostelun jälkeisiä metabolisia kulkureittejä ei ole kuvattu kliinisissä tutkimuksissa. Fentanyyli metaboloituu maksassa norfentanyyliksi sytokromi-CYP3A4-isoformin avulla. Norfentanyyli ei osoita farmakologista aktiivisuutta eläinkokeissa. Se eliminoituu yli 90-prosenttisesti biotransformoitumalla N‑dealkyloiduiksi ja hydroksyloiduiksi inaktiivisiksi metaboliiteiksi.
Eliminaatio
PecFentin nenään annostelun jälkeistä fentanyylin eliminoitumista ei ole kuvattu massataseen tutkimuksessa (mass balance study). Alle 7 % fentanyyliannoksesta erittyy muuttumattomana virtsaan ja vain 1 % erittyy muuttumattomana ulosteeseen. Metaboliitit erittyvät pääasiassa virtsaan ja vain vähäisessä määrin ulosteeseen.
Fentanyylin kokonaisplasmapuhdistuma laskimonsisäisen annostelun jälkeen on noin 42 litraa/tunti.
Lineaarisuus/ei-lineaarisuus
Cmax:in ja AUC:n suhteellisuus annokseen nähden osoitettiin annosvälillä 100–800 mikrogrammaa.
Munuaisten tai maksan vajaatoiminnan vaikutusta PecFentin farmakokinetiikkaan ei ole tutkittu.
Prekliiniset tiedot turvallisuudesta
Farmakologista turvallisuutta, toistuvan altistuksen aiheuttamaa toksisuutta, genotoksisuutta ja karsinogeenisuutta koskevien konventionaalisten tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille.
Alkion ja sikiön kehitystä koskevissa toksisuustutkimuksissa rotilla ja kaniineilla ei havaittu aineen aiheuttamia epämuodostumia tai kehitysmuutoksia, kun annostelu tapahtui organogeneesin aikana.
Rotilla tehdyssä hedelmällisyyttä ja alkion varhaista kehitystä koskevassa tutkimuksessa havaittiin uroksen välittämä vaikutus suurilla annoksilla (300 mikrog/kg/vrk, subkutaanisti), mikä on yhdenmukaista eläinkokeissa havaittujen fentanyylin sedaatiivisten vaikutusten kanssa.
Rottien pre- ja postnataalia kehitystä seuraavissa tutkimuksissa jälkeläisten eloonjäämisprosentti laski merkitsevästi käytettäessä annoksia, jotka aiheuttivat vakavaa toksisuutta emolla. Muita F1-poikasissa havaittuja löydöksiä emolle toksisilla annoksilla olivat viivästynyt fyysinen kehitys sekä vaikutukset aistien toimintaan, reflekseihin ja käyttäytymiseen. Nämä vaikutukset voivat johtua joko epäsuorasti emon antaman hoidon muuttumisesta ja/tai vähentyneestä laktaationopeudesta tai fentanyylin välittömästä vaikutuksesta poikasiin.
Fentanyylillä tehdyissä karsinogeenisuustutkimuksissa (26 viikon dermaalinen vaihtoehtoinen biotesti Tg.AC-transgeenisilla hiirillä sekä 2 vuoden subkutaaninen karsinogeenisuustutkimus rotilla) ei havaittu mitään karsinogeeniseen potentiaaliin viittaavaa. Rotilla tehdystä karsinogeenisuustutkimuksesta saatuja aivonäytteitä tarkastellessa havaittiin aivoleesioita eläimillä, joille oli annettu suuria annoksia fentanyylisitraattia. Näiden havaintojen merkitystä ihmisen kannalta ei tiedetä.
Farmaseuttiset tiedot
Apuaineet
Pektiini (E 440)
Mannitoli (E 421)
Fenyylietyylialkoholi
Propyyliparahydroksibentsoaatti (E 216)
Sakkaroosi
Suolahappo (0,36 %) tai natriumhydroksidi (pH:n säätämiseen)
Puhdistettu vesi
Yhteensopimattomuudet
Ei oleellinen.
Kestoaika
3 vuotta.
Ensimmäisen käytön jälkeen: 60 vuorokautta.
Säilytys
Säilytä alle 25 °C.
Ei saa jäätyä.
Säilytä pullo lapsiturvallisessa pakkauksessa. Herkkä valolle.
Säilytä pullo aina lapsiturvallisessa pakkauksessa, myös tyhjänä.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
PECFENT nenäsumute, liuos
100 mikrog/suihke (L:ei) 8 annosta (59,42 €)
400 mikrog/suihke (L:ei) 8 annosta (59,42 €)
PF-selosteen tieto
Pullo (kirkasta tyypin I lasia), jossa on annostelupumppu ja siihen liittyvä äänellinen annoslaskin sekä läpikuultava suojakorkki. Pakattu simpukan kuorta muistuttavaan lapsiturvalliseen pakkaukseen.
Jokainen pullo sisältää 1,55 ml, joka riittää 8 täyteen suihkeeseen.
Lapsiturvallisissa pakkauksissa olevat pullot toimitetaan rasioissa, jotka sisältävät yhden pullon.
Valmisteen kuvaus:
Kirkkaasta lähes kirkkaaseen vaihteleva väritön vesiliuos.
Käyttö- ja käsittelyohjeet
Osittain käytetyt PecFent-pullot voivat sisältää lapselle haitallisen tai hengenvaarallisen määrän lääkeainetta. Vaikka lääkeainetta olisi pullossa vain vähän tai ei lainkaan, PecFent on hävitettävä asianmukaisesti seuraavien ohjeiden mukaan:
- Potilaita ja hoitajia on neuvottava hävittämään kaikki käyttämättömät, osittain käytetyt jakäytetyt PecFent-pullot asianmukaisesti. Potilasta on neuvottava, kuinka tämä tehdään oikein.
-
Jos pulloon jää ylimääräistä suihketta, potilasta on neuvottava suihkuttamaan pullo tyhjäksi seuraavasti:
- Osoita suutin itsestäsi (ja muista ihmisistä) poispäin. Suihkutusta jatketaan, kunnes laskinruutuun ilmestyy punainen numero 8 eikä pullossa ole enää täysiä suihkeita jäljellä.
- Kun laskinruudussa on numero 8, potilaan on yhä painettava reunusta (vastus kasvaa hieman) yhteensä neljä kertaa, jotta pullo saadaan tyhjennettyä lopusta lääkeaineesta.
- Kun 8 suihketta on käytetty, napsahdusta ei enää kuulu eikä laskuri etene numeron 8 yli. Tämän jälkeen suihkutettavat suihkeet eivät ole täysiä, eikä niitä saa käyttää hoitotarkoituksiin.
Välittömästi sen jälkeen kun PecFentiä ei enää tarvita potilaita ja heidän kotitaloutensa jäseniä tulee neuvoa systemaattisesti hävittämään kaikki lääkemääräykseen liittyvät pullot mahdollisimman pian laittamalla ne takaisin lapsiturvallisiin pakkauksiinsa ja hävittämällä ne paikallisten vaatimusten mukaisesti tai palauttamalla ne apteekkiin.
Korvattavuus
PECFENT nenäsumute, liuos
100 mikrog/suihke 8 annosta
400 mikrog/suihke 8 annosta
- Ylempi erityiskorvaus (100 %). Rintasyöpä (115), Eturauhassyöpä (116), Leukemiat, muut pahanlaatuiset veri- ja luuydintaudit sekä pahanlaatuiset imukudostaudit (117), Gynekologiset syövät (128), Pahanlaatuiset kasvaimet, joita ei ole edellä erikseen mainittu (130).
- Peruskorvaus (40 %).
ATC-koodi
N02AB03
Valmisteyhteenvedon muuttamispäivämäärä
16.05.2024
Yhteystiedot
Arne Jacobsens Allé 7
2300 København S
Denmark
