OTRIVIN COMP nenäsumute, liuos 0,5/0,6 mg/ml
Vaikuttavat aineet ja niiden määrät
Yksi ml sisältää 0,5 mg ksylometatsoliinihydrokloridia ja 0,6 mg ipratropiumbromidia.
Yksi sumuteannos (noin 140 mikrolitraa) sisältää 70 mikrogrammaa ksylometatsoliinihydrokloridia ja 84 mikrogrammaa ipratropiumbromidia.
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Nenäsumute, liuos.
Kliiniset tiedot
Käyttöaiheet
Flunssaan liittyvän nenän tukkoisuuden ja nuhan oireenmukainen hoito.
Annostus ja antotapa
Annostus
Aikuiset: Yksi sumuteannos kumpaankin sieraimeen enintään 3 kertaa vuorokaudessa. Kahden lääkkeenoton välin on oltava vähintään 6 tuntia. Enimmäisannostusta (3 sumuteannosta vuorokaudessa kumpaankin sieraimeen) ei saa ylittää.
Hoidon kesto ei saa ylittää 7 vuorokautta (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Ilmoitettua annosta ei saa ylittää. On käytettävä pienintä tehokasta annosta ja lyhyintä mahdollista hoitoaikaa.
Haittavaikutusten riskin pienentämiseksi Otrivin Comp -hoito suositellaan lopetettavaksi, kun oireet ovat vähentyneet, jopa ennen kuin hoito on kestänyt 7 vuorokauden enimmäisaikaa (ks. kohta Haittavaikutukset).
Pediatriset potilaat
Otrivin Comp -nenäsumutetta ei suositella lasten ja alle 18-vuotiaiden nuorten hoitoon, koska sitä ei ole dokumentoitu riittävästi.
Iäkkäät potilaat
Otrivin Comp -nenäsumutteen käytöstä yli 70-vuotiaille potilaille on vain vähän kokemusta.
Antotapa
Kahden sormen pystysuunnassa laukaistava sumutepumppu:
Ennen ensimmäistä käyttökertaa sumutepumppu saatetaan käyttökuntoon painamalla sitä 4 kertaa. Käyttökuntoon saatettu pumppu pysyy normaalisti toimintavalmiina koko hoitojakson ajan.
- Niistä nenä.
- Pidä pulloa pystyasennossa siten, että peukalo on pohjan alla ja suutin kahden sormen välissä.
- Kallista päätä hieman eteenpäin ja vie suutin sieraimeen.
- Suihkuta ja hengitä samalla varovasti nenän kautta sisään.
- Toista tämä toimenpide toiseen sieraimeen.
- Puhdista ja kuivaa suutin, ennen kuin laitat korkin takaisin paikalleen heti käytön jälkeen.
Jos suihketta ei tule ulos, kun pumppu painetaan ääriasentoon tai jos valmistetta ei ole käytetty yli 6 päivään, pumppu pitää saattaa uudelleen käyttökuntoon pumppaamalla sitä 4 kertaa kuten ennen ensimmäistä käyttökertaa. Jos pumpusta ei tule täyttä suihketta, annosta ei pidä toistaa.
Peukalolla sivulta laukaistava sumutepumppu:
Ennen ensimmäistä käyttöä
Sumutepumppu saadaan käyttökuntoon painamalla annospainiketta 5 kertaa. Käyttövalmis pumppu pysyy normaalisti toimintavalmiina säännöllisten päivittäisten hoitojaksojen ajan.
Irrota korkki.
1. Niistä nenä.
2. Pidä pulloa pystyasennossa peukalo annospainikkeella.
3. Pysy pystyasennossa suihkutetun liuoksen sieraimesta valumisen välttämiseksi ja vie suutin toiseen sieraimeen.
4. Paina annospainiketta suihkuttaaksesi ja hengitä samalla varovasti nenän kautta sisään. Toista tämä toimenpide (vaiheet 2-4) toiseen sieraimeen.
5. Jokaisen käytön jälkeen puhdista ja kuivaa suutin.
6. Aseta suojakorkki takaisin paikalleen niin, että kuuluu napsahdus.
 | 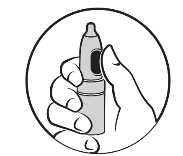 | 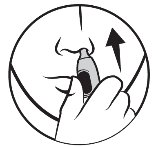 | 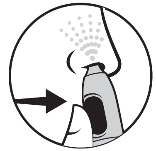 | 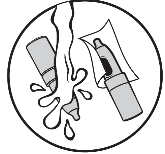 |  |
| 2. Peukalo annospainikkeelle | 3. Vie nenään | 4. Paina annospainiketta | 5. Puhdista ja kuivaa | 6. Laita korkki takaisin paikalleen |
Jos suihketta ei tule ulos kun annospainike painetaan ääriasentoon tai jos valmistetta ei ole käytetty yli 7 päivään, pumppu pitää saattaa uudelleen käyttökuntoon painamalla annospainiketta 2 kertaa.
Jos pumpusta ei tule täyttä suihketta, annosta ei saa toistaa.
Infektion mahdollisen leviämisen välttämiseksi, sumutepulloa saa käyttää vain yksi henkilö.
Varo suihkuttamasta silmiin.
Vasta-aiheet
Otrivin Comp -nenäsumutetta ei saa antaa alle 18-vuotiaille lapsille, koska hoitoa ei ole dokumentoitu riittävästi.
Yliherkkyys vaikuttaville aineille tai kohdassa Apuaineet mainituille apuaineille.
Yliherkkyys atropiinille tai atropiinin kaltaisille aineille, kuten hyoskyamiinille ja skopolamiinille.
Kirurgisten toimenpiteiden jälkeen, kun kovakalvo on saatettu läpäistä, esim. kitaluun kautta tehtävä aivolisäkkeen poistoleikkaus tai muu nenän kautta tehty toimenpide.
Glaukooma.
Karstanuha tai atrofinen nuha.
Varoitukset ja käyttöön liittyvät varotoimet
Tätä lääkevalmistetta on käytettävä varoen potilaille, jotka ovat herkkiä adrenergisille aineille, jotka voivat aiheuttaa oireita, kuten unihäiriöitä, heitehuimausta, vapinaa, sydämen rytmihäiriöitä tai verenpaineen kohoamista.
Tätä lääkevalmistetta on annettava varoen, jos potilaalla on jokin seuraavista:
- hypertensio, sydän- ja verisuonitauti. Pitkä QT -oireyhtymää sairastavilla potilailla, joita hoidetaan ksylometatsoliinilla, voi olla suurempi vakavan kammioperäisen rytmihäiriön riski.
- kilpirauhasen liikatoiminta, diabetes,
- eturauhasen liikakasvu, virtsanjohdinten ahtauma,
- feokromosytooma,
- kystinen fibroosi.
- Jos potilasta hoidetaan monoamiinioksidaasin estäjillä (MAO:n estäjät) tai jos hän on saanut niitä kahden viimeksi kuluneen viikon aikana (ks. kohta Yhteisvaikutukset Yhteisvaikutukset).
- Jos potilas saa tri- tai tetrasyklisiä masennuslääkkeitä ja tai jos hän on saanut niitä kahden viimeksi kuluneen viikon aikana (ks. kohta Yhteisvaikutukset Yhteisvaikutukset).
- Beeta2-agonistihoito (ks.kohta Yhteisvaikutukset Yhteisvaikutukset).
Hoidossa on oltava varovainen, jos potilaalla on taipumus:
- ahdaskulmaglaukoomaan
- nenäverenvuotoihin (esim. iäkkäät)
- paralyyttiseen ileukseen.
Välittömiä yliherkkyysreaktioita, mm. nokkosihottumaa, angioedeemaa, ihottumaa, bronkospasmia, nielun turvotusta ja anafylaksiaa, saattaa esiintyä.
Hoidon enimmäiskesto on 7 vuorokautta, koska ksylometatsoliinihydrokloridin pitkäaikainen käyttö saattaa aiheuttaa nenän limakalvojen turvotusta ja eritystoiminnan lisääntymistä, kun solujen herkkyys lisääntyy (rebound-ilmiö, ns. lääkenuha).
Potilaita on kehotettava välttämään Otrivin Comp -nenäsumutteen sumuttamista silmään tai silmänseudulle. Jos Otrivin Comp -nenäsumutetta joutuu silmiin, voi esiintyä ohimenevää näön hämärtymistä, silmien ärsytystä, kipua ja punoitusta. Ahdaskulmaglaukooma voi myös pahentua.
Potilasta on neuvottava huuhtelemaan silmät kylmällä vedellä, jos Otrivin Comp -nenäsumutetta pääsee suoraan kosketukseen silmien kanssa, ja ottamaan yhteyttä lääkäriin, jos silmissä tuntuu kipua tai näkö hämärtyy.
Ei lasten ulottuville eikä näkyville.
Yhteisvaikutukset
Monoamiinioksidaasin estäjät (MAO:n estäjät) tai tri- ja tetrasykliset masennuslääkkeet | Sympatomimeettisten valmisteiden samanaikainen käyttö tai niiden käyttö kahden viimeksi kuluneen viikon aikana voi aiheuttaa vaikeaa verenpaineen nousua eikä sitä siksi suositella. Sympatomimeettiset valmisteet vapauttavat katekoliamiineja, mikä johtaa noradrenaliinin voimakkaaseen vapautumiseen. Tällä puolestaan on verisuonia supistava vaikutus, mikä johtaa verenpaineen nousuun. Jos verenpaine on noussut kriittisesti, hoito Otrivin Comp -nenäsumutteella on lopetettava ja kohonnut verenpaine on hoidettava. (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet Varoitukset ja varotoimet) |
Beeta2-agonistit | Ipratropiumin samanaikainen käyttö voi lisätä akuutin glaukooman riskiä potilailla, joilla on aiemmin ollut ahdaskulmaglaukooma. Yksittäisiä tapauksia silmäkomplikaatioita (ts. mydriaasia, silmänpaineen kohoamista, ahdaskulmaglaukoomaa ja silmien kipua) on ilmoitettu, kun aerosolimuodossa oleva ipratropiumbromidi joko yksinään tai yhdessä adrenergisen beta2-agonistin kanssa on joutunut kosketuksiin silmien kanssa. (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet Varoitukset ja varotoimet) |
Muiden antikolinergisten lääkeaineiden samanaikainen antaminen voi voimistaa antikolinergisiä vaikutuksia.
Edellä mainittuja yhteisvaikutuksia on tutkittu kummallakin Otrivin Comp -nenäsumutteen vaikuttavalla aineella erikseen, mutta ei yhdistelmänä.
Varsinaisia yhteisvaikutustutkimuksia ei ole tehty muilla lääkeaineilla.
Raskaus ja imetys
Raskaus
Tämän valmisteen käytöstä raskaana oleville naisille ei ole riittävästi tietoja. Ei ole tehty riittäviä eläinkokeita lisääntymistoksisuuden selvittämiseksi (ks. non-kliiniset tiedot). Tämän valmisteen käyttöä ei suositella raskauden aikana.
Ksylometatsoliini
Saatavilla olevien tietojen mukaan ksylometatsoliinilla voi olla systeeminen verisuonia supistava vaikutus. Systeemisen verisuonia supistavan vaikutuksensa takia ksylometatsoliinin käyttöä raskauden aikana ei suositella.
Ipratropium
Ipratropiumbromidin kliinistä turvallisuutta ihmisen raskausaikana ei ole varmistettu. Non-kliiniset tiedot ovat osoittaneet ipratropiumbromidin olevan sikiötoksinen, kun sitä on annettu inhalaationa kaneille kliinisiä annoksia suurempina annoksina (ks. non-kliiniset tiedot).
Imetys
Ei ole riittävästi tietoja siitä, erittyykö tämä valmistee ihmisen rintamaitoon. Tätä valmistetta saa käyttää imetysaikana vain, jos lääkäri niin neuvoo. Jos hoidosta odotettu hyöty äidille on suurempi kuin mahdollinen lapseen kohdistuva riski, on harkittava pienintä tehokasta annosta ja hoidon kesto on huomioitava.
Ksylometatsoliini
Rintaruokittuun lapseen kohdistuvista haittavaikutuksista ei ole näyttöä. Ei tiedetä, erittyykö ksylometatsoliini rintamaitoon.
Ipratropium
Ei tiedetä, erittyykö ipratropiumbromidi rintamaitoon.
Hedelmällisyys
Ei ole riittävästi tietoa tämän valmisteen vaikutuksesta hedelmällisyyteen.
Ksylometatsoliini
Ksylometatsoliinihydrokloridin vaikutuksista hedelmällisyyteen ei ole riittäviä tietoja, eikä eläinkokeita ole saatavilla.
Ipratropium
Non-kliiniset tiedot eivät ole osoittaneet hedelmällisyyden heikkenemistä, kun ipratropiumbromidia on annettu rotille suun kautta kliinistä annosta suurempina annoksina (ks. prekliiniset tiedot turvallisuudesta).
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Näköhäiriöitä (mm. näön hämärtymistä ja mustuaisten laajenemista), heitehuimausta ja väsymystä on ilmoitettu Otrivin Comp -valmisteen käytön yhteydessä. Potilaalle on kerrottava, että jos oireita ilmaantuu, hänen ei pidä ajaa, käyttää koneita eikä osallistua toimiin, joissa oireet saattavat aiheuttaa vaaraa hänelle itselleen tai muille.
Haittavaikutukset
Yhteenveto turvallisuutta koskevista tiedoista
Yleisimmin ilmoitettuja haittavaikutuksia ovat nenäverenvuoto, jota esiintyy 14,8 prosentilla, ja nenän kuivuminen, 11,3 prosentilla potilaista.
Monet ilmoitetuista haittavaikutuksista ovat myös flunssan oireita.
Haittavaikutustaulukko
Haittavaikutukset esitetään elinjärjestelmän ja esiintymistiheyden mukaan. Esiintymistiheydet määritellään seuraavasti:
Hyvin yleinen (≥1/10)
Yleinen (≥1/100, <1/10)
Melko harvinainen (≥1/1 000, <1/100)
Harvinainen (≥1/10 000, <1/1 000)
Hyvin harvinainen (<1/10 000)
Tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin).
Ksylometatsoliini ja ipratropium
Seuraavia haittavaikutuksia ilmoitettiin ksylometatsoliinin ja ipratropiumin yhdistelmävalmisteella tehdyissä kahdessa satunnaistetussa kliinisessä tutkimuksessa ja yhdessä valmisteen markkinoilletulon jälkeisessä ei-interventiotutkimuksessa sekä markkinoilletulon jälkeisessä seurannassa.
MeDRA elinjärjestelmä | Haittavaikutukset | Esiintymistiheys |
Immuunijärjestelmä | Yliherkkyysreaktio (angioedeema, ihottuma, kutina) | Hyvin harvinainen |
Psyykkiset häiriöt | Unettomuus | Melko harvinainen |
Hermosto | Makuaistin häiriöt | Yleinen |
Parosmia, vapina | Melko harvinainen | |
Silmät | Ärtyneet silmät, kuivat silmät | Melko harvinainen |
Fotopsia | Tuntematon | |
Sydän | Palpitaatiot, takykardia | Melko harvinainen |
Hengityselimet, rintakehä ja välikarsina | Nenäverenvuoto | Hyvin yleinen |
Nenän tukkoisuus, rinalgia | Yleinen | |
Haavaumat nenässä, äänen käheys, suunielun kipu, aivastelu | Melko harvinainen | |
Vetinen nuha | Harvinainen | |
Epämukava olo nenän sivuonteloissa | Tuntematon | |
Ruoansulatuselimistö | Ylävatsavaivat | Melko harvinainen |
Nielemisvaikeudet | Tuntematon | |
Yleisoireet ja antopaikassa todettavat haitat | Väsymys, epämukava olo | Melko harvinainen |
Epämukava olo rintakehän alueella, jano | Tuntematon |
Ksylometatsoliini
Seuraavia haittavaikutuksia on ilmoitettu ksylometatsoliinilla tehdyissä kliinisissä tutkimuksissa ja markkinoilletulon jälkeisessä seurannassa.
MeDRA elinjärjestelmä | Haittavaikutukset | Esiintymistiheys |
Hermosto | Päänsärky | Yleinen |
Silmät | Näön heikentyminen | Hyvin harvinainen |
Hengityselimet, rintakehä ja välikarsina | Nenän kuivuminen, epämukava olo nenässä | Yleinen |
Nenäverenvuoto | Melko harvinainen | |
Ruoansulatuselimistö | Pahoinvointi | Yleinen |
Yleisoireet ja antopaikassa todettavat haitat | Antopaikan kirvely | Yleinen |
Ipratropiumbromidi
Seuraavia haittavaikutuksia on tunnistettu tiedoista, joita on saatu kliinisissä tutkimuksissa ja lääketurvatoiminnassa myyntiluvan myöntämisen jälkeisen käytön aikana.
MeDRA elinjärjestelmä | Haittavaikutukset | Esiintymistiheys |
Immuunijärjestelmä | Anafylaktinen reaktio, yliherkkyys | Tuntematon |
Hermosto | Heitehuimaus, päänsärky | Yleinen |
Silmät | Sarveiskalvon turvotus, sidekalvon hyperemia | Melko harvinainen |
Glaukooma, silmänpaineen kohoaminen, akkommodaatiohäiriö, näön hämärtyminen, haloilmiö, mustuaisten laajeneminen, silmäkipu | Tuntematon | |
Sydän | Supraventrikulaarinen takykardia, palpitaatiot | Melko harvinainen |
Eteisvärinä | Tuntematon | |
Hengityselimet, rintakehä ja välikarsina | Kurkun ärsytys, kurkun kuivuminen | Yleinen |
Yskä | Melko harvinainen | |
Laryngospasmi, nielun turvotus | Tuntematon | |
Ruoansulatuselimistö | Suun kuivuminen | Yleinen |
Pahoinvointi | Melko harvinainen | |
Iho ja ihonalainen kudos | Ihottuma, nokkosihottuma, kutina | Tuntematon |
Munuaiset ja virtsatiet | Virtsaumpi | Tuntematon |
Valittujen haittavaikutusten kuvaus
Useita esiintymistiheydellä ”tuntematon” esitettyjä haittavaikutuksia on ilmoitettu vain kerran valmisteen käytön yhteydessä kliinisissä tutkimuksissa tai vain markkinoilletulon jälkeisessä seurannassa, joten niiden esiintymistiheyttä ei voida arvioida Otrivin Comp ‑nenäsumutteella hoidettujen nykyisten potilasmäärien perusteella.
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haitta-tasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Suun kautta tapahtunut yliannostus tai ksylometatsoliinihydrokloridin liiallinen paikallinen anto voi aiheuttaa vaikeaa heitehuimausta, hikoilua, vaikea-asteista ruumiinlämmön alenemista, päänsärkyä, bradykardiaa, hypertensiota, hengityslamaa, kooman ja kouristuksia. Hypertension jälkeen voi ilmaantua hypotensio. Pikkulapset ovat herkempiä valmisteen haitoille kuin aikuiset.
Imeytyminen nenän tai suun kautta tapahtuneen annon jälkeen on hyvin vähäistä, joten nenään annetusta ipratropiumbromidista aiheutuva akuutti yliannostus on epätodennäköinen, mutta jos yliannostusta tapahtuu, sen oireisiin kuuluvat suun kuivuminen, akkommodaatiovaikeudet ja takykardia. Yliannostuksen hoito on oireenmukainen.
Huomattava yliannostus voi aiheuttaa antikolinergisiä keskushermosto-oireita, kuten aistiharhoja, jotka on hoidettava koliiniesteraasin estäjillä.
Asianmukaisiin tukitoimiin on ryhdyttävä kaikilla potilailla, joilla epäillään yliannostusta, ja kiireellinen oireenmukainen hoito lääkärin valvonnassa on aiheellista perustelluissa tilanteissa. Tähän kuuluu mm. potilaan seuranta vähintään 6 tunnin ajan. Jos vaikeaan yliannostukseen liittyy sydämenpysähdys, elvytystä on jatkettava vähintään tunnin ajan. Jatkohoito on toteutettava kliinisen tarpeen mukaan tai kansallisen myrkytystietokeskuksen suositusten mukaisesti, jos tällaiset suositukset ovat saatavilla.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Sympatomimeettien ja muiden lääkeaineiden (ei kortikosteroidien) yhdistelmävalmisteet, ATC-koodi: R01AB06
Ksylometatsoliinihydrokloridi on sympatomimeetti, joka vaikuttaa alfa-adrenergisiin reseptoreihin. Ksylometatsoliini vaikuttaa verisuonia supistavasti. Vaikutus ilmaantuu 5-10 minuutin kuluttua ja kestää 6-8 tuntia.
Ipratropiumbromidi on kvaternaarinen ammoniumyhdiste, jolla on antikolinerginen vaikutus. Kun valmistetta annetaan nenään, se vähentää nenän eritystä estämällä kilpailevasti nenäepiteelin ympäristössä sijaitsevia kolinergisiä reseptoreja. Vaikutus ilmaantuu yleensä 15 minuutin kuluessa ja kestää keskimäärin 6 tuntia.
Farmakokinetiikka
Kun 24 terveelle koehenkilölle annettiin yksi sumuteannos (140 μg ksylometatsoliinia ja 84 μg ipratropiumbromidia) sierainta kohden, ipratropiumbromidin keskimääräinen huippupitoisuus tunnin kuluttua annosta oli 0,085 ng/ml ja ksylometatsoliinin keskimääräinen huippupitoisuus kahden tunnin kuluttua annosta oli 0,13 ng/ml. Pitoisuudet veressä ovat hyvin pieniä. Käytettävissä olevien tietojen perusteella kuitenkin odotetaan, että ipratropiumbromidi ja etenkin ksylometatsoliini kumuloituvat ehdotetulla annostuksella kolme kertaa vuorokaudessa.
Prekliiniset tiedot turvallisuudesta
Ksylometatsoliinihydrokloridin ja ipratropiumbromidin non-kliiniset turvallisuustiedot eivät ole paljastaneet löydöksiä, joilla olisi merkitystä valmisteen suositellun annostuksen ja käytön kannalta.
Karsinogeneesi ja mutageneesi
Ksylometatsoliinihydrokloridista ei ole karsinogeenisuustietoja. Saatavilla olevat tätä vaikuttavaa ainetta koskevat in vitro ja in vivo ‑genotoksisuustiedot eivät kuitenkaan osoita genotoksista potentiaalia. Non-kliiniset tutkimukset ipratropiumbromidilla osoittivat, että tämä yhdiste ei ollut mutageeninen, genotoksinen, tai karsinogeeninen.
Lisääntymistoksikologia
Ksylometatsoliinin lisääntymis- ja kehitystoksikologiasta ei ole saatavilla non-kliinisiä tietoja. Non-kliiniset tiedot ipratropiumbromidista osoittivat sen olevan alkiotoksinen kaneille inhaloidulla annoksella, joka oli noin 14 kertaa suurempi kuin ihmisen ekvivalenttiannokseen perustuva kliininen annos.
Farmaseuttiset tiedot
Apuaineet
Dinatriumedetaatti
Glyseroli (85-prosenttinen)
Suolahappo (pH:n säätöön)
Natriumhydroksidi (pH:n säätöön)
Puhdistettu vesi
Yhteensopimattomuudet
Ei oleellinen.
Kestoaika
3 vuotta.
Avattu pakkaus on käyttökelpoinen pakkaukseen merkittyyn viimeiseen käyttöpäivämäärään asti.
Säilytys
Säilytä alle 25 °C.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Itsehoito
OTRIVIN COMP nenäsumute, liuos
0,5/0,6 mg/ml (L:ei) 10 ml (pystysuuntainen pumppu) (10,44 €), 10 ml (11,94 €)
PF-selosteen tieto
10 ml:n HDPE-moniannospullo (noin 70 sumuteannosta), jossa kiinteä annossumutepumppu ja PP-kärki ja suojus. Nenäsumuteliuoksen kanssa kosketuksissa olevat pakkausmateriaalit: LDPE, HDPE, PE/butyyli, ruostumaton teräs).
Saatavilla on 2 erilaista sumutinpumppua: kahden sormen pystysuunnassa laukaistava pumppu ja peukalolla sivulta laukaistava pumppu suojakorkilla.
Valmisteen kuvaus:
Kirkas, väritön liuos.
Käyttö- ja käsittelyohjeet
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
OTRIVIN COMP nenäsumute, liuos
0,5/0,6 mg/ml 10 ml, 10 ml
- Ei korvausta.
ATC-koodi
R01AB06
Valmisteyhteenvedon muuttamispäivämäärä
02.10.2023
Yhteystiedot
Energiakuja 3
00180 Helsinki
Suomi
0800 77 40 80
www.haleon.com
mystory.nd@haleon.com
