YAZ tabletti, kalvopäällysteinen 0,02/3 mg
 Lääketurva
Lääketurva
Riskienminimointimateriaalit
Lääkäri
Tarkistuslista yhdistelmäehkäisyvalmisteiden määrääjille
Tiedote terveydenhuollon ammattilaisille
Yleinen
Vaikuttavat aineet ja niiden määrät
24 vaaleanpunaista kalvopäällysteistä tablettia:
Jokainen kalvopäälysteinentabletti sisältää 0,02 mg etinyyliestradiolia (beetadeksiklatraattina) ja 3 mg drospirenonia.
Apuaine, jonka vaikutus tunnetaan: Laktoosi 46 mg (laktoosimonohydraattina 48,18 mg)
4 valkoista kalvopäällysteistä lumetablettia (plasebo):
Tabletti ei sisällä vaikuttavia aineita.
Apuaine, jonka vaikutus tunnetaan: Laktoosi 22 mg (laktoosimonohydraattinaa 23,21 mg)
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Tabletti, kalvopäällysteinen
Kliiniset tiedot
Käyttöaiheet
Raskauden ehkäisy.
Yaz-valmisteen määräämistä koskevassa päätöksessä on otettava huomioon valmisteen käyttäjän nykyiset riskitekijät, erityisesti laskimotromboembolian (VTE) riskitekijät, ja millainen Yaz valmisteen käytön VTE:n riski on verrattuna muiden yhdistelmäehkäisyvalmisteiden riskeihin (ks. kohdat Vasta-aiheet sekä Varoitukset ja käyttöön liittyvät varotoimet).
Annostus ja antotapa
Antotapa
Suun kautta
Annostus
Miten Yaz-tabletteja käytetään
Tabletit otetaan läpipainopakkaukseen merkityssä järjestyksessä joka päivä suunnilleen samaan aikaan, tarvittaessa pienen nestemäärän kanssa. Tabletteja otetaan yksi päivässä 28 perättäisen päivän ajan, ilman taukoja. Uusi läpipainopakkaus aloitetaan heti seuraavana päivänä kun edellisen pakkauksen viimeinen tabletti on otettu. Tyhjennysvuoto alkaa tavallisesti 2–3 päivän kuluttua lumetablettien (läpipainopakkauksen viimeinen tablettirivi) käytön aloittamisesta eikä välttämättä ole päättynyt ennen seuraavan pakkauksen aloittamista.
Miten Yaz-tablettien käyttö aloitetaan
Ei aiempaa hormonaalista ehkäisyä (edeltäneen kuukauden aikana):
Tablettien käyttö aloitetaan luonnollisen kuukautiskierron ensimmäisenä päivänä (= ensimmäinen vuotopäivä).
Vaihto Yaz-tabletteihin hormonaalisesta yhdistelmäehkäisyvalmisteesta (yhdistelmäehkäisytabletti, ehkäisyrengas tai ehkäisylaastari):
Yaz-tablettien käyttö aloitetaan mieluiten aiemman yhdistelmäehkäisyvalmisteen viimeisen vaikuttavia aineita sisältävän tabletin ottamista seuraavana päivänä, mutta viimeistään seuraavana päivänä aiemman yhdistelmävalmisteen tauon tai lumetablettijakson jälkeen. Jos käytössä on ollut ehkäisyrengas tai ehkäisylaastari, voidaan Yaz-tablettien käyttö aloittaa samana päivänä kun valmiste poistetaan, mutta viimeistään silloin, kun uusi ehkäisyrengas tai ehkäisylaastari olisi pitänyt laittaa.
Vaihto Yaz-tabletteihin pelkkää progestiinia sisältävästä ehkäisyvalmisteesta (ehkäisytabletti (minipilleri), injektio, implantaatti) tai progestiinia vapauttavasta kohdunsisäisestä ehkäisimestä:
Minipilleristä voidaan siirtyä käyttämään Yaz-tabletteja koska tahansa (implantaatista ja kohdunsisäisestä ehkäisimestä niiden poistopäivänä, injektiosta seuraavana suunniteltuna injektiopäivänä). Kaikissa näissä tapauksissa tulee kuitenkin käyttää lisäehkäisynä jotain estemenetelmää 7 ensimmäisen tablettipäivän ajan.
Ensimmäisellä raskauskolmanneksella tapahtuneen raskauden keskeytymisen jälkeen:
Tablettien käyttö voidaan aloittaa heti. Muita ehkäisymenetelmiä ei tällöin tarvita.
Synnytyksen tai toisella raskauskolmanneksella tapahtuneen raskauden keskeytymisen jälkeen:
Tablettien käyttö aloitetaan 21–28 vuorokautta synnytyksen tai toisella raskauskolmanneksella tapahtuneen raskauden keskeytymisen jälkeen. Jos tablettien käyttö aloitetaan myöhemmin, tulee 7 ensimmäisen tablettipäivän aikana käyttää lisäksi jotain muuta estemenetelmää. Jos nainen on jo ollut yhdynnässä, raskaus on suljettava pois ennen yhdistelmäehkäisytablettien käytön varsinaista aloittamista tai odotettava seuraavien kuukautisten alkamista.
Imetys, ks. kohta Raskaus ja imetys.
Tabletin unohtaminen
Lumetabletit läpipainopakkauksen viimeisellä (neljännellä) rivillä voidaan jättää huomioimatta. Ne tulee kuitenkin hävittää, jotta lumetablettijakso ei pitkity tarpeettomasti. Seuraavat ohjeet koskevat ainoastaan unohdettuja, vaikuttavia aineita sisältäviä tabletteja:
Jos tabletin unohtamisesta on kulunut alle 24 tuntia, tablettien raskautta ehkäisevä vaikutus ei ole heikentynyt. Unohtunut tabletti tulee ottaa heti muistettaessa ja seuraavat tabletit tavanomaiseen aikaan.
Jos tabletin unohtamisesta on kulunut yli 24 tuntia, tablettien raskautta ehkäisevä vaikutus saattaa olla heikentynyt. Seuraavat kaksi perussääntöä pätevät tapauksissa, joissa tablettien ottaminen on unohtunut:
- Lumetablettijakson suositeltu pituus on 4 päivää, mutta tablettien ottamista ei tule koskaan keskeyttää yli 7 päivän ajaksi.
- Hypotalamus-aivolisäke-munasarja -akselin riittävä suppressio edellyttää tablettien ottamista yhtäjaksoisesti 7 päivän ajan.
Yllä olevan perusteella voidaan antaa seuraavat käytännön ohjeet:
Päivät 1–7:
Viimeinen unohtunut tabletti otetaan heti muistettaessa, vaikka tällöin olisikin otettava kaksi tablettia samalla kertaa. Seuraavat tabletit otetaan normaaliin aikaan. Lisäksi seuraavien 7 päivän ajan tulee käyttää jotain estemenetelmää, kuten kondomia. Jos nainen on ollut yhdynnässä tabletin unohtamista edeltävien 7 päivän aikana, raskauden mahdollisuus on otettava huomioon. Raskauden mahdollisuus on sitä suurempi, mitä useampi tabletti on unohtunut ja mitä lähempänä lumetablettijaksoa unohtuneet tabletit ovat.
Päivät 8–14:
Viimeinen unohtunut tabletti otetaan heti muistettaessa, vaikka tällöin olisikin otettava kaksi tablettia samalla kertaa. Seuraavat tabletit otetaan normaaliin aikaan. Jos tabletteja on otettu säännöllisesti ohjeen mukaan 7 päivän ajan ennen ensimmäistä unohtunutta tablettia, lisäehkäisyä ei tarvita. Jos nainen on unohtanut useampia tabletteja, häntä on neuvottava käyttämään lisäehkäisyä seuraavien 7 päivän ajan.
Päivät 15–24:
Ehkäisyteho on uhattuna koska lumetablettijakso on lähellä. Ehkäisytehon heikkeneminen voidaan kuitenkin estää muuttamalla tablettien ottoaikataulu. Toimittaessa alla olevan ohjeen 1 tai ohjeen 2 mukaan lisäehkäisyä ei tarvita, jos tabletteja on otettu oikein 7 päivän ajan ennen ensimmäistä unohtunutta tablettia. Jos tabletteja ei ole otettu oikein, tulee toimia ohjeen 1 mukaan ja käyttää lisäehkäisyä seuraavien 7 päivän ajan.
- Viimeinen unohtunut tabletti otetaan heti muistettaessa, vaikka tällöin olisikin otettava kaksi tablettia samalla kertaa. Seuraavat tabletit otetaan normaaliin aikaan, kunnes vaikuttavia aineita sisältävät tabletit on käytetty loppuun. Viimeisen rivin neljä lumetablettia tulee hävittää. Seuraava läpipainopakkaus aloitetaan heti. Tyhjennysvuoto jää todennäköisesti tulematta ennen uuden pakkauksen vaikuttavia aineita sisältävien tablettien loppumista, mutta tablettien käytön aikana voi esiintyä tiputtelu- tai läpäisyvuotoa.
- Vaikuttavia aineita sisältävien tablettien ottaminen käytössä olleesta läpipainopakkauksesta voidaan myös keskeyttää. Tällöin siirrytään viimeisen rivin lumetablettien käyttöön korkeintaan neljän päivän ajaksi, mukaan lukien tähän jokainen päivä, jolloin vaikuttavia aineita sisältävä tabletti unohdettiin ottaa. Lumetablettien jälkeen tablettien ottamista jatketaan normaalisti uudesta läpipainopakkauksesta.
Jos useampi tabletti on jäänyt ottamatta eikä tyhjennysvuotoa tule lumetablettijakson aikana, raskauden mahdollisuus on otettava huomioon.
Ohjeet ruoansulatuskanavan häiriöiden yhteydessä
Vaikeiden ruoansulatuskanavan häiriöiden (esim. oksentelun ja ripulin) yhteydessä vaikuttavien aineiden imeytyminen saattaa olla epätäydellistä ja tällöin tulee käyttää lisäehkäisyä. Jos oksentelua esiintyy 3–4 tunnin kuluessa vaikuttavia aineita sisältävän tabletin ottamisesta, uusi (korvaava) tabletti tulee ottaa mahdollisimman pian. Uusi tabletti tulee ottaa 24 tunnin kuluessa tavallisesta tabletin ottamisajasta, mikäli mahdollista. Jos aiemman tabletin ottamisesta on kulunut yli 24 tuntia, sovelletaan tablettien unohtamista koskevia ohjeita kohdassa Tabletin unohtaminen. Jos nainen ei halua muuttaa tablettien normaalia käyttöaikatauluaan, hänen on otettava ylimääräinen tabletti (/ylimääräiset tabletit) toisesta läpipainopakkauksesta.
Tyhjennysvuodon siirtäminen
Kuukautisia voidaan siirtää aloittamalla uusi Yaz-läpipainopakkaus ilman käytössä olleen pakkauksen lumetablettien ottamista. Kuukautisia voidaan siirtää niin pitkälle kuin halutaan, aina toisen pakkauksen vaikuttavaa ainetta sisältävien tablettien loppumiseen asti. Tänä aikana voi esiintyä läpäisy- tai tiputteluvuotoa. Yaz-tablettien säännöllinen käyttö aloitetaan uudestaan lumetablettijakson jälkeen.
Jos nainen haluaa muuttaa kuukautisten alkamispäivän nykyisestä joksikin toiseksi viikonpäiväksi, häntä voidaan neuvoa lyhentämään seuraavaa lumetablettijaksoa niin monella päivällä kuin hän haluaa. Mitä lyhyempi tauko on, sitä suurempi on riski, että tyhjennysvuotoa ei tule lyhennetyn tauon aikana ja että seuraavan pakkauksen käytön aikana esiintyy läpäisy- ja tiputteluvuotoa (kuten kuukautisia siirrettäessä).
Lisätietoa erityispotilasryhmistä
Pediatriset potilaat
Yaz on tarkoitettu käytettäväksi vain kuukautisten alkamisen jälkeen.
Iäkkäät
Yaz ei ole tarkoitettu käyttöön vaihdevuosien jälkeen.
Maksan vajaatoiminta
Yaz-valmistetta ei saa käyttää naisille, joilla on vaikea maksasairaus. Ks. myös kohdat Vasta-aiheet ja Prekliiniset tiedot turvallisuudesta.
Munuaisten vajaatoiminta
Yaz-valmistetta ei saa käyttää naisille, joilla on vaikea tai äkillinen munuaisten vajaatoimintaa. Ks. myös kohdat Vasta-aiheet ja Prekliiniset tiedot turvallisuudesta.
Vasta-aiheet
Yhdistelmäehkäisyvalmisteita ei pidä käyttää seuraavien tilojen yhteydessä. Jos jokin näistä tiloista ilmenee ensimmäistä kertaa yhdistelmäehkäisyvalmisteen käytön aikana, valmisteen käyttö on lopetettava heti.
-
laskimotromboembolia (VTE) tai sen riski
- laskimotromboembolia tällä hetkellä esiintyvä VTE (potilas antikoagulanttilääkityksellä) tai anamneesissa VTE (esim. syvä laskimotromboosi [SLT] tai keuhkoembolia)
- tiedossa oleva perinnöllinen tai hankittu laskimotromboembolia-alttius, kuten APC-resistenssi, (mukaan lukien Faktori V Leiden), antitrombiini III:n puutos, C-proteiinin puutos, S-proteiinin puutos
- suuri leikkaus ja siihen liittyvä pitkittynyt immobilisaatio (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet)
- useiden riskitekijöiden aiheuttama suuri laskimotromboembolian riski (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet)
-
valtimotromboembolia tai sen riski
- valtimotromboembolia tällä hetkellä esiintyvä tai aiemmin esiintynyt valtimotromboembolia (esim. sydäninfarkti) tai sitä ennakoiva tila (esim. angina pectoris)
- aivoverisuonisairaus tällä hetkellä esiintyvä tai aiemmin esiintynyt aivohalvaus tai sitä ennakoiva tila (esim. ohimenevä aivoverenkiertohäiriö, TIA)
- tiedossa oleva perinnöllinen tai hankittu valtimotromboembolia-alttius, kuten hyperhomokysteinemia ja fosfolipidivasta-aineet (kardiolipiinivasta-aineet, lupusantikoagulantti)
- anamneesissa migreeni, johon liittyy fokaalisia neurologisia oireita
- monista riskitekijöistä (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet) tai yhden vakavan riskitekijän esiintymisestä johtuva suuri valtimotromboemboliariski. Näitä riskitekijöitä voivat olla:
- vaikea dyslipoproteinemia
- vaikea hypertensio
- diabetes, jossa esiintyy verisuonioireita
- vaikea maksasairaus, tämänhetkinen tai aiemmin ilmennyt, niin kauan kuin maksa-arvot eivät ole palautuneet normaaleiksi
- vaikea tai akuutti munuaisten vajaatoiminta
- tämänhetkinen tai aiemmin ilmennyt hyvän- tai pahanlaatuinen maksakasvain
- sukupuolihormoniriippuvaiset maligniteetit tai niiden epäily (esim. sukupuolielimissä tai rinnoissa)
- emätinverenvuoto, jonka syy on selvittämättä
- yliherkkyys vaikuttaville aineille tai kohdassa Apuaineet mainituille apuaineille.
-
ombitasviirin, paritapreviirin ja ritonaviirin yhdistelmää sekä dasabuviiria, glekapreviirin ja pibrentasviirin yhdistelmää tai sofosbuviirin, velpatasviirin ja voksilapreviirin yhdistelmää sisältävien lääkevalmisteiden samanaikainen käyttö (ks. kohta Yhteisvaikutukset).
Varoitukset ja käyttöön liittyvät varotoimet
Varoitukset
Yaz-valmisteen soveltuvuudesta on keskusteltava naisen kanssa, jos hänellä esiintyy mikä tahansa alla mainituista tiloista tai riskitekijöistä.
Jos jokin näistä tiloista tai riskitekijöistä pahenee tai ilmenee ensimmäisen kerran, käyttäjää on kehotettava ottamaan yhteys lääkäriin, joka päättää, pitääkö Yaz-valmisteen käyttö keskeyttää.
Yhdistelmäehkäisyvalmisteiden käyttö tulee keskeyttää tromboosilöydöksen tai sen epäilyn yhteydessä. Antikoagulanttihoidon (kumariinit) teratogeenisyyden vuoksi potilasta tulee neuvoa käyttämään asianmukaista vaihtoehtoista ehkäisymenetelmää ko. hoidon aikana.
Verenkiertohäiriöt
Laskimotromboembolian (VTE) riski
Minkä tahansa yhdistelmäehkäisyvalmisteen käyttö lisää laskimotromboembolian (VTE) riskiä verrattuna siihen, että tällaista valmistetta ei käytetä lainkaan. Levonorgestreelia, norgestimaattia tai noretisteronia sisältäviin valmisteisiin liittyy pienin VTE:n riski. Tämä riski voi olla jopa kaksinkertainen muilla valmisteilla, kuten esimerkiksi Yaz valmisteella. Päätöksen muun kuin VTE:n riskiltään pienimmän valmisteen käyttämisestä saa tehdä vain sen jälkeen, kun ehkäisyä harkitsevan naisen kanssa on keskusteltu. Keskustelussa on varmistettava, että hän ymmärtää Yaz valmisteen käyttöön liittyvän VTE:n riskin, miten hänen nykyiset riskitekijänsä vaikuttavat tähän riskiin ja että hänen VTE:n riskinsä on suurimmillaan ensimmäisen vuoden aikana, jona hän käyttää yhdistelmäehkäisyvalmistetta ensimmäistä kertaa elämässään. On myös jonkin verran näyttöä siitä, että riski suurenee, kun yhdistelmäehkäisyvalmisteen käyttö aloitetaan uudelleen vähintään 4 viikon tauon jälkeen.
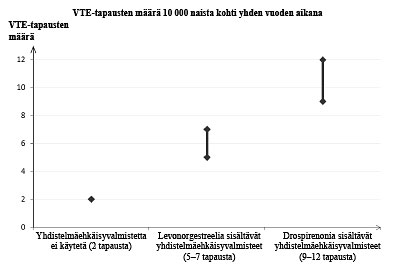
Noin kahdelle naiselle 10 000:sta, jotka eivät käytä yhdistelmäehkäisyvalmistetta eivätkä ole raskaana, kehittyy VTE yhden vuoden aikana. Yksittäisellä naisella tämä riski voi kuitenkin olla suurempi riippuen hänen omista, taustalla vaikuttavista riskitekijöistä (ks. jäljempänä).
Arviolta noin 9–12 naiselle1 10 000:sta, jotka käyttävät drospirenonia sisältävää yhdistelmäehkäisyvalmistetta, kehittyy VTE yhden vuoden aikana. Levonorgestreelia sisältävää yhdistelmäehkäisyvalmistetta käyttävillä naisilla vastaava luku on 62.
Kaikkien yhdistelmäehkäisytablettien käyttö lisää laskimotromboembolian riskiä ei-käyttäjiin verrattuna. Laskimotromboembolian lisääntynyt riski on suurin yhdistelmäehkäisytablettien ensimmäisen käyttövuoden aikana, kun käyttö aloitetaan ensimmäistä kertaa tai uudelleen vähintään kuukauden tauon jälkeen.
1 Ilmaantuvuus arvioitiin kaikista epidemiologisista tutkimustuloksista vertaamalla eri valmisteiden suhteellisia riskejä levonorgestreelia sisältäviin yhdistelmäehkäisyvalmisteisiin.
2 Vaihteluvälin 5–7 keskipiste 10 000 naisvuotta kohden, mikä perustuu levonorgestreelia sisältävien yhdistelmäehkäisyvalmisteiden käytön suhteelliseen riskiin verrattuna käyttämättömyyteen, jolloin riski on noin 2,3–3,6.
Molemmissa tapauksissa VTE-tapausten määrä vuotta kohti on pienempi kuin määrä, joka on odotettavissa raskauden aikana tai synnytyksen jälkeisenä aikana.
VTE saattaa aiheuttaa kuoleman 1–2 %:ssa tapauksista.
Yhdistelmäehkäisyvalmisteiden käyttäjillä tromboosia on erittäin harvoin raportoitu esiintyneen muissa verisuonissa (esim. maksan, suoliliepeen, munuaisten tai verkkokalvon laskimoissa ja valtimoissa).
Laskimotromboembolian riskitekijät
Yhdistelmäehkäisyvalmisteiden käyttäjillä esiintyvien laskimotromboembolisten komplikaatioiden riski voi suurentua huomattavasti, jos naisella on muita riskitekijöitä, erityisesti jos riskitekijöitä on useita (ks. taulukko).
Yaz-valmiste on vasta-aiheinen naisella, jolla on useita riskitekijöitä, jotka aiheuttavat suuren VTE:n riskin (ks. kohta Vasta-aiheet). Jos naisella on useampia kuin yksi riskitekijä, nämä yhdessä voivat muodostaa yksittäisten tekijöiden summaa suuremman riskin – tässä tapauksessa VTE:n kokonaisriski on otettava huomioon. Jos hyöty-riski-suhteen katsotaan olevan negatiivinen, yhdistelmäehkäisyvalmistetta ei pidä määrätä (ks. kohta Vasta-aiheet).
Taulukko: Laskimotromboembolian (VTE) riskitekijät
| Riskitekijä | Kommentti |
| Ylipaino (painoindeksi yli 30 kg/m2) | Riski suurenee huomattavasti painoindeksin noustessa. Huomioitava erityisesti silloin, jos muita riskitekijöitä on myös olemassa. |
Pitkittynyt immobilisaatio, suuri leikkaus, kaikki jalkojen tai lantion alueen leikkaukset, neurokirurgia tai merkittävä trauma Huomioitavaa: väliaikainen immobilisaatio, mukaan lukien > 4 tunnin lentomatka, voi myös olla VTE:n riskitekijä, erityisesti naisilla, joilla on myös muita riskitekijöitä | Näissä tilanteissa on suositeltavaa lopettaa laastarin/tabletin/renkaan käyttö (elektiivisen leikkauksen kohdalla vähintään neljä viikkoa etukäteen), eikä sitä pidä jatkaa ennen kuin käyttäjä on ollut kaksi viikkoa täysin liikuntakykyinen. Jotain muuta raskaudenehkäisymenetelmää on käytettävä ei-toivotun raskauden ehkäisemiseksi. Antitromboottista hoitoa on harkittava, ellei Yaz-valmisteen käyttöä ole lopetettu etukäteen. |
| Positiivinen sukuanamneesi (tämänhetkinen tai aikaisempi VTE sisaruksella tai vanhemmalla, etenkin suhteellisen nuorella iällä, esim. alle 50-vuotiaana) | Jos perinnöllistä alttiutta epäillään, potilas on syytä ohjata erikoislääkärin tutkimuksiin ennen kuin minkään yhdistelmäehkäisyvalmisteen käytöstä päätetään. |
| Muut laskimotromboemboliaan liitetyt sairaudet | Syöpä, systeeminen lupus erythematosus, hemolyyttis-ureeminen oireyhtymä, krooninen tulehduksellinen suolistosairaus (Crohnin tauti tai haavainen koliitti) ja sirppisoluanemia |
| Ikääntyminen | Erityisesti yli 35 vuoden ikä |
Suonikohjujen ja pinnallisen laskimontukkotulehduksen mahdollisesta yhteydestä laskimotromboosin alkamiseen tai etenemiseen ei ole yksimielisyyttä.
Laskimotromboembolian suurempi riski raskauden ja erityisesti synnytyksen jälkeisten noin 6 viikon aikana on otettava huomioon (ks. lisätiedot kohdasta Hedelmällisyys, raskaus ja imetys)
Laskimotromboembolian oireet (syvä laskimotromboosi ja keuhkoembolia)
Jos oireita ilmaantuu, naisia on neuvottava hakeutumaan välittömästi lääkärin hoitoon ja kertomaan, että he käyttävät yhdistelmäehkäisyvalmistetta.
Syvän laskimotromboosin (SLT) oireita voivat olla:
- toisen jalan ja/tai jalkaterän turvotus tai turvotus jalan laskimon kohdalla
- jalan kipu tai arkuus, joka saattaa tuntua vain seistessä tai kävellessä
- jalan lisääntynyt lämmöntunne, jalan ihon värin muutos tai punoitus.
Keuhkoembolian oireita voivat olla:
- äkillisesti alkanut, selittämätön hengenahdistus tai nopeutunut hengitys
- äkillinen yskä, johon saattaa liittyä veriysköksiä
- pistävä rintakipu
- vaikea pyörrytys tai huimaus
- nopea tai epäsäännöllinen sydämen syke.
Jotkut näistä oireista (esim. hengenahdistus, yskä) ovat epäspesifisiä, ja ne voidaan tulkita virheellisesti yleisluontoisemmiksi tai vähemmän vaikeiksi tapahtumiksi (esim. hengitystieinfektioksi).
Muita verisuonitukoksen merkkejä voivat olla mm.: äkillinen kipu, turvotus ja sinertävä värimuutos raajassa.
Jos tukos tulee silmään, oireena voi olla esim. kivuton näön hämärtyminen, joka voi edetä näön menetykseen. Joskus näön menetys voi tapahtua lähes välittömästi.
Valtimotromboembolian (ATE) riski
Epidemiologisissa tutkimuksissa on osoitettu, että yhdistelmäehkäisyvalmisteiden käyttöön liittyy suurentunut valtimotromboembolian (sydäninfarkti) tai aivoverisuonitapahtuman (esim. aivojen ohimenevä verenkiertohäiriö (TIA), aivohalvaus) riski. Valtimotromboemboliset tapahtumat voivat johtaa kuolemaan.
Valtimotromboembolian (ATE) riskitekijät
Valtimotromboembolisten komplikaatioiden tai aivoverisuonitapahtuman riski yhdistelmäehkäisyvalmisteen käyttäjillä on korkeampi niillä naisilla, joilla on riskitekijöitä (ks. taulukko). Yaz valmiste on vasta-aiheinen, jos naisella on joko yksi vakava tai useampia ATE:n riskitekijöitä, mikä aiheuttaa suuren valtimotromboemboliariskin (ks. kohta Vasta-aiheet). Jos naisella on useampi kuin yksi riskitekijä, nämä yhdessä voivat muodostaa yksittäisten tekijöiden summaa suuremman riskin – tässä tapauksessa kokonaisriski on otettava huomioon. Jos hyöty-riski-suhteen katsotaan olevan negatiivinen, yhdistelmäehkäisyvalmistetta ei pidä määrätä (ks. kohta Vasta-aiheet).
Taulukko: Valtimotromboembolian (ATE) riskitekijät
| Riskitekijä | Kommentti |
| Ikääntyminen | Erityisesti yli 35 vuoden ikä |
| Tupakointi | Yhdistelmäehkäisyvalmistetta käyttäviä naisia on neuvottava olemaan tupakoimatta. Yli 35-vuotiaita, tupakoimista jatkavia naisia on vakavasti kehotettava käyttämään jotakin muuta ehkäisymenetelmää. |
| Korkea verenpaine | |
| Ylipaino (painoindeksi yli 30 kg/m2) | Riski kasvaa huomattavasti painoindeksin noustessa. Erityisen tärkeää naisilla, joilla on muitakin riskitekijöitä. |
| Positiivinen sukuanamneesi (tämänhetkinen tai aikaisempi valtimotromboembolia sisaruksella tai vanhemmalla, etenkin suhteellisen nuorella iällä, alle 50-vuotiaana) | Jos perinnöllistä alttiutta epäillään, potilas on syytä ohjata erikoislääkärin tutkimuksiin ennen kuin minkään yhdistelmäehkäisyvalmisteen käytöstä päätetään. |
| Migreeni | Migreenin esiintymistiheyden kasvu tai vaikeusasteen lisääntyminen (mikä saattaa olla aivoverisuonitapahtumaa ennakoiva oire) yhdistelmäehkäisyvalmisteen käytön aikana voi olla syy yhdistelmäehkäisyvalmisteen käytön välittömään keskeyttämiseen. |
| Muut verisuoniston haittatapahtumiin liitetyt sairaudet | Diabetes, hyperhomokysteinemia, sydämen läppävika ja eteisvärinä, dyslipoproteinemia ja systeeminen lupus erythematosus (SLE). |
Valtimotromboembolian (ATE) oireet
Jos oireita ilmaantuu, naisia on neuvottava hakeutumaan välittömästi lääkärin hoitoon ja kertomaan, että he käyttävät yhdistelmäehkäisyvalmistetta.
Aivoverisuonitapahtuman oireita voivat olla:
- kasvojen, käsivarren tai jalan äkillinen tunnottomuus tai heikkous (varsinkin vain yhdellä puolella vartaloa esiintyvä)
- äkillinen kävelyn vaikeutuminen, huimaus, tasapainon tai koordinaation menetys
- äkillinen sekavuus, puhe- tai ymmärtämisvaikeudet
- äkillinen näön heikentyminen yhdessä tai molemmissa silmissä
- äkillinen, voimakas tai pitkittynyt päänsärky, jonka syytä ei tiedetä
-
tajunnan menetys tai pyörtyminen, johon saattaa liittyä kouristuskohtaus.
Ohimenevät oireet viittaavat siihen, että tapahtuma on ohimenevä aivoverenkiertohäiriö (TIA).
Sydäninfarktin oireita voivat olla:
- kipu, epämiellyttävä tunne, paineen tunne, painon tunne, puristuksen tai täysinäisyyden tunne rinnassa, käsivarressa tai rintalastan takana
- selkään, leukaan, kurkkuun, käsivarteen ja/tai vatsaan säteilevä epämiellyttävä tunne
- täyteläisyyden, ruoansulatushäiriöiden tai tukehtumisen tunne
- hikoilu, pahoinvointi, oksentelu tai huimaus
- erittäin voimakas heikkouden tunne, ahdistuneisuus tai hengenahdistus
- nopea tai epäsäännöllinen sydämen syke.
Kasvaimet
Joissakin epidemiologisissa tutkimuksissa on raportoitu kohdunkaulasyövän riskin kasvaneen yhdistelmäehkäisyvalmisteen pitkäaikaiskäytön yhteydessä (> 5 vuotta), mutta yksimielisyyttä ei ole siitä, missä määrin tähän havaintoon vaikuttavat sekoittavat tekijät, kuten sukupuolikäyttäytyminen ja muut tekijät, kuten ihmisen papilloomavirus (HPV).
Meta-analyysi 54 epidemiologisesta tutkimuksesta osoitti, että yhdistelmäehkäisytablettien käyttäjien suhteellinen rintasyöpäriski on hieman suurentunut (suhteellinen riskikerroin 1,24). Tämä riski häviää vähitellen 10 vuoden kuluessa yhdistelmäehkäisytablettien käytön lopettamisesta. Koska rintasyöpä on harvinainen alle 40-vuotiailla naisilla, yhdistelmäehkäisytabletteja käyttävillä tai hiljattain niitä käyttäneillä havaittu rintasyöpädiagnoosien ylimäärä on pieni verrattuna rintasyöpäriskiin koko elinaikana. Tutkimukset eivät anna kuitenkaan näyttöä syy-seuraussuhteesta. Havaittu suurentunut riski voi johtua rintasyövän varhaisemmasta diagnoosista suun kautta otettavien yhdistelmäehkäisytablettien käyttäjillä, suun kautta otettavan yhdistelmäehkäisytablettien biologisista vaikutuksista tai molemmista. Lisäksi käyttäjiltä diagnosoidut rintasyöpätapaukset ovat yleensä kliinisesti varhaisemmassa vaiheessa kuin ehkäisytabletteja käyttämättömiltä diagnosoidut rintasyöpätapaukset.
Harvoissa tapauksissa yhdistelmäehkäisytablettien käyttäjillä on todettu hyvänlaatuisia ja vielä harvemmin pahanlaatuisia maksakasvaimia. Yksittäistapauksissa nämä kasvaimet ovat johtaneet hengenvaarallisiin sisäisiin vatsaonteloverenvuotoihin. Erotusdiagnostisesti maksakasvaimen mahdollisuutta tulisi harkita, kun yhdistelmäehkäisytablettien käyttäjällä on voimakasta ylävatsakipua, suurentunut maksa tai merkkejä vatsaontelonsisäisestä verenvuodosta.
Korkeampiannoksisia yhdistelmäehkäisytabletteja (50 mikrog etinyyliestradiolia) käytettäessä sekä kohdun limakalvon- että munasarjasyövän esiintymisen riski pienenee. Se, koskeeko tämä myös matala-annoksisia yhdistelmäehkäisytabletteja, on vielä vahvistamatta.
Muut sairaudet
Yaz-valmisteen sisältämä progestiini on aldosteroniantagonisti, jolla on kaliumia säästäviä ominaisuuksia. Valtaosalla käyttäjistä seerumin kaliumtason nousua ei kuitenkaan ole odotettavissa. Joillakin lievää tai keskivaikeaa munuaisten vajaatoimintaa sairastavilla potilailla on kliinisessä tutkimuksessa havaittu vähäistä, mutta ei merkitsevää, seerumin kaliumtason nousua kaliumia säästävien lääkkeiden ja drospirenonin samanaikaisen käytön yhteydessä. Sen vuoksi on suositeltavaa tarkistaa munuaisten vajaatoimintaa sairastavien potilaiden seerumin kaliumtaso ensimmäisen hoitosyklin aikana sekä sellaisten potilaiden, joiden kaliumpitoisuus seerumissa on ennen hoitoa viitealueen ylärajalla, ja varsinkin, jos potilas käyttää kaliumia säästäviä lääkkeitä.Ks. myös kohta Yhteisvaikutukset.
Naisilla, joilla on hypertriglyseridemia tai sitä esiintyy suvussa, saattaa olla suurentunut haimatulehduksen riski yhdistelmäehkäisytablettien käytön aikana.
Vähäistä verenpaineen kohoamista on raportoitu yhdistelmäehkäisytablettien käyttäjillä, mutta kliinisesti merkitsevä verenpaineen kohoaminen on harvinaista. Vain merkittävän verenpaineen nousun yhteydessä yhdistelmäehkäisytablettien käyttö on aiheellista lopettaa välittömästi. Yhdistelmäehkäisytablettien käyttö tulee keskeyttää, jos niiden käytön aikana hypertensiopotilaan jatkuvasti koholla olevat verenpainearvot tai verenpaineen merkittävä nousu eivät reagoi riittävästi verenpainelääkitykseen. Tablettien käyttöä voidaan jatkaa, jos verenpainelääkityksellä saadaan aikaan normotensio.
Seuraavia sairaustiloja tai niiden pahenemista on raportoitu esiintyneen sekä raskauden että yhdistelmäehkäisytablettien käytön yhteydessä, mutta niiden yhteydestä yhdistelmäehkäisytablettien käyttöön ei ole pitävää näyttöä: kolestaasiin liittyvä keltaisuus ja/tai kutina, sappikivet, porfyria, SLE, hemolyyttis-ureeminen oireyhtymä, Sydenhamin korea, herpes gestationis, otoskleroosiin liittyvä kuulonalenema.
Eksogeeniset estrogeenit voivat indusoida tai pahentaa perinnöllisen ja hankinnaisen angioedeeman oireita.
Suun kautta otettavan yhdistelmäehkäisytablettien käytön keskeyttäminen saattaa olla tarpeen akuuteissa tai kroonisissa maksan toimintahäiriöissä, kunnes maksafunktioarvot ovat normalisoituneet. Yhdistelmäehkäisytablettien käyttö on lopetettava, jos aiemmin raskausaikana tai aiemman sukupuolihormonien käytön aikana ilmennyt kolestaasiin liittyvä keltaisuus ja/tai kutina uusiutuu.
Vaikka yhdistelmäehkäisytabletit voivat vaikuttaa perifeeriseen insuliiniresistenssiin tai glukoosinsietoon, matalaestrogeenisia yhdistelmäehkäisytabletteja (< 0,05 mg etinyyliestradiolia) käyttävien naisten diabeteshoidon muuttamistarpeesta ei ole näyttöä. Yhdistelmäehkäisytabletteja käyttäviä diabeetikkoja tulee kuitenkin seurata huolellisesti erityisesti ehkäisytablettien käytön alkuvaiheessa.
Epilepsian, Crohnin taudin ja colitis ulcerosan pahenemista on raportoitu ilmenneen yhdistelmäehkäisytablettien käytön aikana.
Masentunut mieliala ja masennus ovat tunnettuja hormonaalisten ehkäisyvalmisteiden käyttöön liittyviä haittavaikutuksia (ks. kohta Haittavaikutukset). Masennus voi olla vakavaa, ja se on itsetuhoisen käyttäytymisen ja itsemurhan tunnettu riskitekijä. Naisia on kehotettava ottamaan yhteyttä lääkäriinsä, jos heillä esiintyy mielialan muutoksia ja masennuksen oireita, myös pian hoidon aloittamisen jälkeen.
Maksaläiskiä voi joskus esiintyä, erityisesti jos niitä on esiintynyt raskausaikana. Maksaläiskien saamiseen taipuvaisten naisten tulisi välttää aurinkoa ja ultraviolettisäteilyaltistusta yhdistelmäehkäisytablettien käytön aikana.
Yksi vaaleanpunainen kalvopäällysteinen tabletti sisältää 46 mg laktoosia ja yksi valkoinen sisältää 22 mg laktoosia. Laktoositonta ruokavaliota noudattavien potilaiden, joilla on harvinainen perinnöllinen galaktoosi-intoleranssi, LAPP-hypolaktasia (saamelaisilla esiintyvä laktaasinpuutos) tai glukoosi-galaktoosi-imeytymishäiriö, tulee huomioida tämä laktoosimäärä.
Lääkärintutkimus
Ennen Yaz-tablettien käytön aloittamista tai uudelleen aloittamista, potilaan sairaushistoria on selvitettävä täydellisesti (mukaan lukien sukuanamneesi), ja raskaus on suljettava pois. Naisen verenpaine on mitattava, ja hänelle on tehtävä lääkärintarkastus ottaen huomioon vasta-aiheet (ks. kohta Vasta-aiheet) ja varoitukset (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet). On tärkeää kiinnittää naisen huomiota laskimo- ja valtimoveritulppia koskeviin tietoihin, kuten Yaz-valmisteen käyttöön liittyvään riskiin verrattuna muihin yhdistelmäehkäisyvalmisteisiin, laskimo- ja valtimoveritulppien oireisiin, tiedossa oleviin riskitekijöihin sekä siihen, mitä tehdä, jos epäilee veritulppaa.
Naista on myös neuvottava lukemaan pakkausseloste huolellisesti ja noudattamaan siinä annettuja ohjeita. Tarkastuskäyntien tiheyden ja luonteen pitää perustua vakiintuneisiin hoitosuosituksiin, ja ne on toteutettava kunkin naisen kliinisten tarpeiden mukaisesti.
Naisia on varoitettava siitä, että hormonaaliset ehkäisyvalmisteet eivät suojaa HIV-infektiolta (AIDS) tai muilta sukupuoliteitse tarttuvilta taudeilta.
Tehon heikkeneminen
Vaikuttavia aineita sisältävien tablettien unohtaminen (ks. kohta Annostus ja antotapa), oksentelu ja vaikea ripuli (ks. kohta Annostus ja antotapa) tai muu samanaikainen lääkitys (ks. Yhteisvaikutukset) voivat heikentää yhdistelmäehkäisytablettien tehoa.
Syklikontrollin heikentyminen
Kaikki yhdistelmäehkäisytabletit voivat aiheuttaa epäsäännöllistä verenvuotoa emättimestä (tiputtelu- tai läpäisyvuotoa) etenkin ensimmäisten käyttökuukausien aikana. Siksi epäsäännöllistä vuotoa kannattaa alkaa tutkia vasta noin kolme kiertoa kestävän sopeutumisvaiheen jälkeen.
Jos vuotohäiriöt jatkuvat tai niitä ilmaantuu kiertojen oltua aiemmin säännölliset, ei-hormonaaliset syyt on syytä ottaa huomioon. Asianmukaiset diagnostiset toimenpiteet, mahdollisesti myös kaavinta, ovat perusteltuja maligniteetin tai raskauden poissulkemiseksi.
Joissakin tapauksissa lumetablettijakson aikana ei tule tyhjennysvuotoa. Jos yhdistelmäehkäisytabletteja on käytetty kohdassa Annostus ja antotapa annettujen ohjeiden mukaan, käyttäjä ei todennäköisesti ole raskaana. Jos tabletteja ei kuitenkaan ole käytetty ohjeiden mukaan ennen tyhjennysvuodon ensimmäistä poisjääntiä tai jos jo kaksi tyhjennysvuotoa on jäänyt tulematta, raskauden mahdollisuus on suljettava pois ennen yhdistelmäehkäisytablettien käytön jatkamista.
Yhteisvaikutukset
Huomautus: Mahdollisten yhteisvaikutusten varalta tulee tutustua kaikkien samanaikaisesti käytettävien lääkkeiden valmisteyhteenvetoihin.
Muiden lääkevalmisteiden vaikutus Yaz-valmisteeseen
Lääkeaineinteraktioita voi esiintyä käytettäessä maksaentsyymejä indusoivia lääkkeitä, mikä voi johtaa sukupuolihormonien lisääntyneeseen puhdistumaan ja voi heikentää ehkäisyvalmisteen tehoa ja/tai aiheuttaa läpäisyvuotoja.
Kuinka toimia
Entsyymi-induktio on havaittavissa jo oarin hoitopäivän jälkeen. Maksimaalinen entsyymi-induktio havaitaan yleensä muutaman viikon sisällä. Induktio voi jatkua vielä neljän viikon ajan lääkehoidon päätyttyä.
Lyhytaikainen hoito
Käytettäessä entsyymejä indusoivia lääkkeitä, tulee yhdistelmäehkäisytablettien lisäksi käyttää lisäehkäisynä tilapäisesti jotain estemenetelmää tai jotain muuta ehkäisymenetelmää. Estemenetelmää tulee käyttää koko lääkehoidon ajan ja vielä 28 päivän ajan sen loppumisen jälkeen. Jos lääkehoito kestää kauemmin kuin yhdistelmäehkäisytablettien pakkauksen vaikuttavia aineita sisältävät tabletit, lumetabletit on hävitettävä ja seuraava pakkaus on aloitettava heti.
Pitkäaikainen hoito
Naisille, jotka pitkäaikaisesti käyttävät maksaentsyymejä indusoivia lääkeaineita, suositellaan jonkin muun luotettavan, ei-hormonaalisen ehkäisymenetelmän käyttöä.
Kirjallisuudessa on raportoitu alla mainittuja yhteisvaikutuksia.
Lääkeaineet, jotka lisäävät sukupuolihormonien puhdistumaa (entsyymi-induktion aiheuttama yhdistelmäehkäisyvalmisteen tehon heikkeneminen):
Barbituraatit, bosentaani, karbamatsepiini, fenytoiini, primidoni, rifampisiini ja HIV-lääkkkeet ritonaviiri, nevirapiini ja efavirentsi sekä mahdollisesti myös felbamaatti, griseofulviini, okskarbatsepiini, topiramaatti ja mäkikuismaa (Hypericum perforatum) sisältävät rohdosvalmisteet.
Lääkeaineet, joilla on vaihteleva vaikutus sukupuolihormonien puhdistumaan
Useat HIV-proteaasin estäjien ja ei-nukleosdiset käänteiskopioijaentsyymin estäjien yhdistelmä (mukaan lukien HCV-proteaasin estäjien yhdistelmät) saattavat suurentaa tai pienentää estrogeenin tai progestiinin plasmakonsentraatiota käytettäessä samanaikaisesti yhdistelmäehkäisyvalmisteita. Näiden muutosten kokonaisvaikutus voi tietyissä tapauksissa olla kliinisesti merkittävä.
Tämän vuoksi samanaikaisen HIV/HCV-lääkityksen valmisteyhteenveto pitää tarkastaa potentiaalisten yhteisvaikutusten varalta ja niiden suhteen annettujen lisäohjeiden osalta. Naisen, joka käyttää proteaasin estäjää tai ei-nukleosidista käänteiskopioijaentsyymin estäjää, tulee lisäksi käyttää lisäehkäisynä jotain estemenetelmää, jos yhteisvaikutuksen mahdollisuutta epäilllään.
Aineet jotka vähentävät yhdistelmäehkäisyvalmisteiden puhdistumaa (entsyymi-inhibiittorit):
Entsyymi-inhibiittoreiden ja yhdistelmäehkäisytablettien välisten mahdollisten yhteisvaikutusten kliininen merkittävyys on tuntematon.
Vahvojen CYP3A4-inhibiittoreiden ja yhdistelmäehkäisyvalmisteiden yhtäaikainen käyttö voi nostaa plasman estrogeenin ja/tai progestiinin pitoisuutta.
Drospirenoni (3 mg päivässä) / etinyyliestradioli (0,02 mg päivässä) -yhdistelmällä tehdyssä moniannostutkimuksessa yhtäaikainen vahvan CYP3A4-inhibiittorin, ketokonatsolin, annostelu 10 päivän ajan, nosti AUC-arvoa (0-24 h) drospirenonilla 2,7-kertaiseksi ja etinyyliestradiolilla 1,4-kertaiseksi.
Etorikoksibin 60–120 mg päiväannoksen on havaittu nostavan etinyyliestradiolin plasmapitoisuutta 1,4–1,6-kertaiseksi käytettäessä samanaikaisesti yhdistelmäehkäisyvalmisteiden kanssa, jotka sisältävät 0,035 mg etinyyliestradiolia.
Yaz-valmisteen vaikutus muihin lääkevalmisteisiin
Yhdistelmäehkäisytabletit saattavat muuttaa muiden vaikuttavien aineiden metaboliaa, jolloin niiden pitoisuus plasmassa ja kudoksessa voi joko nousta (esim. siklosporiini) tai laskea (esim. lamotrigiini).
Vapaaehtoisilla naisilla tehtyjen in vivo -interaktiotutkimusten (merkkiaineina omepratsoli, simvastatiini tai midatsolaami) perusteella 3 mg:n drospirenoniannoksen kliinisesti merkittävä yhteisvaikutus muiden lääkeaineiden metaboliaanvaikuttavien aineiden metabolian kanssa on epätodennäköistä.
Kliinisen tutkimustiedon perusteella etinyyliestradioli estää CYP1A2-substraattien puhdistumaa, joka johtaa heikkoon (mm. teofylliini) tai kohtalaiseen (tisanidiini) nousuun näiden plasmapitoisuuksissa.
Farmakodynaamiset yhteisvaikutukset
Kun kliinisissä tutkimuksissa hoidettiin hepatiitti C -virusinfektiota (HCV) ombitasviirin, paritapreviirin ja ritonaviirin yhdistelmällä ja dasabuviirilla ribaviriinin kanssa tai ilman, transaminaasiarvon (ALAT) kohoamista yli 5 x ULN (viitealueen yläraja) esiintyi merkitsevästi useammin naisilla, jotka käyttivät etinyyliestradiolia sisältävää valmistetta, kuten yhdistelmäehkäisyvalmistetta. Myös glekapreviirin ja pibrentasviirin yhdistelmää tai sofosbuviirin, velpatasviirin ja voksilapreviirin yhdistelmää käyttävillä potilailla ALAT-arvojen kohoamista havaittiin etinyyliestradiolia sisältävää valmistetta (kuten yhdistelmäehkäisyvalmistetta) käyttävillä naisilla (ks. kohta Vasta-aiheet).
Tämän vuoksi Yaz-valmisteen käyttäjien pitää vaihtaa toisen ehkäisymenetelmän käyttöön (pelkkää progestiinia sisältävät ehkäisyvalmisteet tai ei-hormonaaliset menetelmät) ennen kyseisten yhdistelmähoitojen aloittamista. Yaz-valmisteen käyttö voidaan aloittaa uudestaan 2 viikkoa näiden yhdistelmähoitojen päättymisen jälkeen.
Potilailla, jotka eivät sairasta munuaisten vajaatoimintaa, drospirenonin ja ACE:n estäjien tai tulehduskipulääkkeiden samanaikaisen käytön ei havaittu vaikuttavan merkittävästi seerumin kaliumtasoon. Yaz-tablettien samanaikaista käyttöä aldosteroniantagonistien tai kaliumia säästävien diureettien kanssa ei ole tutkittu. Siksi tällaisissa tilanteissa seerumin kaliumtasoa on syytä seurata ensimmäisen hoitosyklin aikana. Ks. Varoitukset ja käyttöön liittyvät varotoimet
Muut yhteisvaikutukset
Laboratoriotutkimukset
Steroidiehkäisyn käyttö voi vaikuttaa eräisiin laboratorioarvoihin, kuten maksan, kilpirauhasen, lisämunuaisten ja munuaisten toiminnan biokemiallisiin parametreihin, kantajaproteiinien (esim. kortikosteroideja sitova globuliini ja lipidi/lipoproteiinifraktiot) pitoisuuksiin plasmassa, hiilihydraattiaineenvaihdunnan parametreihin sekä veren hyytymis- ja fibrinolyysiparametreihin. Muutokset tapahtuvat yleensä viitealueen sisällä. Lievän antimineralokortikoidiaktiivisuuden johdosta drospirenoni aiheuttaa plasman reniiniaktiivisuuden lisääntymistä ja indusoi plasman aldosteronimuodostusta.
Raskaus ja imetys
Raskaus
Yaz-tabletteja ei saa käyttää raskauden aikana.
Jos nainen tulee raskaaksi Yaz-tablettien käytön aikana, niiden käyttö tulee lopettaa heti. Laajojen epidemiologisten tutkimusten mukaan synnynnäisten kehityshäiriöiden riski lapsella ei ole suurentunut raskautta edeltäneen yhdistelmäehkäisytablettien käytön yhteydessä, eikä teratogeenisten vaikutusten riski silloin, kun yhdistelmäehkäisytabletteja on käytetty tahattomasti raskauden varhaisvaiheessa.
Eläimillä tehdyissä tutkimuksissa on havaittu tiineys- ja imetysaikana esiintyviä haittavaikutuksia (ks. kohta Prekliiniset tiedot turvallisuudesta). Näiden eläinkokeiden perusteella vaikuttavien aineiden hormonivaikutusten mahdollisesti aiheuttamia haittavaikutuksia ei voida poissulkea.
Yhdistelmäehkäisytablettien raskaudenaikaisesta käytöstä saadun yleisen kliinisen kokemuksen mukaan ei kuitenkaan ole todettu, että niillä olisi varsinaisia ihmiseen kohdistuvia haittavaikutuksia.
Yaz-tablettien raskauden aikaisesta käytöstä tähän mennessä kertyneen tiedon perusteella ei voida tehdä päätelmiä raskauteen, sikiön tai vastasyntyneen terveyteen kohdistuvista negatiivisista vaikutuksista. Epidemiologisia tietoja ei vielä ole.
Kun Yaz-valmisteen käyttö aloitetaan uudelleen, on huomioitava, että laskimotromboembolian riski on suurentunut synnytyksen jälkeisenä aikana (ks. kohdat Annostus ja antotapa sekä Varoitukset ja käyttöön liittyvät varotoimet).
Imetys
Yhdistelmäehkäisytabletit saattavat vaikuttaa imetykseen, sillä ne voivat vähentää rintamaidon määrää ja muuttaa sen koostumusta. Siksi yhdistelmäehkäisytabletteja suositellaan yleensä käytettäviksi vasta, kun lapsi on vieroitettu rintamaidosta. Pieniä määriä kontraseptiivisiä steroideja ja/tai niiden metaboliitteja, joilla voi olla vaikutusta lapseen, voi erittyä rintamaitoon yhdistelmäehkäisytablettien käytön aikana.
Fertiliteetti
Yaz-tabletit on tarkoitettu raskauden ehkäisyyn. Lisätietoja hedelmällisyyden palautumisesta, ks. kohta Farmakodynamiikka
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Tutkimuksia valmisteen vaikutuksesta ajokykyyn tai koneiden käyttökykyyn ei ole tehty. Yhdistelmäehkäisytablettien käyttäjillä ei ole todettu vaikutuksia ajokykyyn tai koneiden käyttökykyyn.
Haittavaikutukset
Vakavat haittavaikutukset yhdistelmäehkäisytabletteja käyttävillä naisilla, ks. myös kohta Varoitukset ja käyttöön liittuvät varotoimet.
Yaz-tablettien käyttäjillä on raportoitu seuraavia haittavaikutuksia:
Haittavaikutukset esitetään oheisessa taulukossa MedDRA-elinjärjestelmän mukaan
(MedDRA SOCs). Esiintyvyysluvut perustuvat kliinisiin tutkimuksiin. Sopivinta MedDRA-termiä käytetään kuvaamaan tiettyä reaktiota ja sen synonyymejä sekä siihen liittyviä oireita.
Haittavaikutukset, jotka on liitetty Yaz-tablettien käyttöön raskauden ehkäisyssä tai keskivaikean aknen hoidossa, MedDRA-elinjärjestelmän ja MedDRA-käsitteiden mukaan
Yleinen: ≥1/100, <1/10; melko harvinainen ≥1/1000, <1/100; harvinainen ≥1/10000, <1/1000; tuntematon (koska saatavissa oleva tieto ei riitä arviointiin)
| Elinjärjestelmä (MedDRA versio 9.1) | ||
| Infektiot | Harvinainen | Kandidiaasi |
| Veri ja imukudos | Harvinainen | Anemia, trombosytemia |
| Immuunijärjestelmä | Harvinainen | Allerginen reaktio |
| Tuntematon | Yliherkkyys, Perinnöllisen tai hankinnaisen angioedeeman oireiden paheneminen | |
| Umpieritys | Harvinainen | Umpierityshäiriö |
| Aineenvaihdunta ja ravitsemus | Harvinainen | Lisääntynyt ruokahalu, anoreksia, hyperkalemia, hyponatremia |
| Psyykkiset häiriöt | Yleinen | Mielialan ailahtelu |
| Melko harvinainen | Masennus, hermostuneisuus, uneliaisuus | |
| Harvinainen | Anorgasmia, unettomuus | |
| Hermosto | Yleinen | Päänsärky |
| Melko harvinainen | Huimaus, parestesia | |
| Harvinainen | Kiertohuimaus, vapina | |
| Silmät | Harvinainen | Konjunktiviitti, silmien kuivuus, silmien häiriöt |
| Sydän | Harvinainen | Takykardia |
| Verisuonisto | Melko harvinainen | Migreeni, suonikohjut, hypertensio |
| Harvinainen | Laskimotromboembolia, valtimotromboembolia, flebiitti, verisuoniin liittyvät häiriöt, epistaksis, synkopee | |
| Ruoansulatuselimistö | Yleinen | Pahoinvointi |
| Melko harvinainen | Vatsakipu, oksentelu, dyspepsia, ilmavaivat, gastriitti, ripuli | |
| Harvinainen | Suurentunut vatsa, ruoansulatuskanavan häiriöt, ruoansulatuskanavan kylläisyydentunne, hiatustyrä, suun kandidiaasi, ummetus, suun kuivuus | |
| Maksa ja sappi | Harvinainen | Sappikivi, kolekystiitti |
| Iho ja ihonalainen kudos | Melko harvinainen | Akne, kutina, ihottuma |
| Harvinainen | Kloasma, ekseema, alopesia, aknetyyppinen ihottuma, ihon kuivuus, erythema nodosum, hypertrikoosi, ihohäiriö, ihojuovat, kosketusdermatiitti, valoihottuma, ihokyhmyt | |
| Tuntematon | Erythema multiforme | |
| Luusto, lihakset ja sidekudos | Melko harvinainen | Selkäkipu, raajakipu, lihaskrampit |
| Sukuelimet ja rinnat | Yleinen | Rintojen kipu, metrorragia*, amenorrea |
| Melko harvinainen | Emättimen kandidiaasi, lantiokipu, rintojen suureneminen, fibrokystiset rinnat, verenvuoto kohdusta/emättimestä*, eritevuoto emättimestä, kuumat aallot, emätintulehdus, kuukautishäiriöt, dysmenorrea, hypomenorrea, menorragia, emättimen kuivuus, epäilyttävä papa-näyte, libidon väheneminen | |
| Harvinainen | Dyspareunia, vulvovaginiitti, verenvuoto yhdynnän jälkeen, tyhjennysvuoto, rintakysta, rintojen liikakasvu, rintakasvain, kohdunkaulan polyyppi, kohdun limakalvon surkastuma, munasarjakysta, kohdun laajeneminen | |
| Yleisoireet ja antopaikassa todettavat haitat | Melko harvinainen | Astenia, lisääntynyt hikoilu, edeema (yleistynyt edeema, perifeerinen edeema, kasvojen edeema) |
| Harvinainen | Huonovointisuus | |
| Tutkimukset | Melko harvinainen | Painon nousu |
| Harvinainen | Painon lasku | |
* Epäsäännöllinen vuoto häviää yleensä hoidon jatkuessa
Tiettyjen haittavaikutusten kuvaus
Yhdistelmäehkäisyvalmisteita käyttävillä naisilla on havaittu valtimoiden ja laskimoiden tromboottisten ja tromboembolisten tapahtumien lisääntynyt riski. Näitä tapahtumia ovat mm. sydäninfarkti, aivohalvaus, ohimenevät aivoverenkiertohäiriöt (TIA), laskimoveritulppa ja keuhkoembolia. Tapahtumia kuvataan tarkemmin kohdassa Varoitukset ja käyttöön liittyvät varotoimet.
Yhdistelmäehkäisytablettien käyttäjillä on raportoitu esiintyneen seuraavia vakavia haittatapahtumia, joista on kerrottu enemmän kohdassa Varoitukset ja käyttöön liittyvät varotoimet:
- laskimotromboemboliset tapahtumat
- valtimotromboemboliset tapahtumat
- korkea verenpaine
- maksakasvaimet
- seuraavia sairaustiloja tai niiden pahenemista on raportoitu, mutta niiden yhteydestä yhdistelmäehkäisytablettien käyttöön ei ole pitävää näyttöä: Crohnin tauti, colitis ulcerosa, epilepsia, kohdun lihaskasvain, porfyria, SLE, herpes gestationis, Sydenhamin korea, hemolyyttis-ureeminen oireyhtymä, kolestaasiin liittyvä keltaisuus.
- kloasma
- suun kautta otettavan yhdistelmäehkäisytablettien käytön keskeyttäminen saattaa olla tarpeen akuuteissa tai kroonisissa maksan toimintahäiriöissä, kunnes maksafunktioarvot ovat normalisoituneet.
Rintasyöpädiagnoosien esiintyvyys on hyvin vähän suurentunut yhdistelmäehkäisytablettien käyttäjillä. Koska rintasyöpä on harvinainen alle 40-vuotiailla naisilla, rintasyöpädiagnoosien ylimäärä on pieni verrattuna rintasyöpäriskiin koko elinaikana. Varmaa näyttöä riskin yhteydestä yhdistelmäehkäisytablettien käyttöön ei ole. Lisätietoja, ks. kohdat Vasta-aiheet ja Varoitukset ja käyttöön liittyvät varotoimet.
Yhteisvaikutukset
Läpäisyvuotoja ja/tai ehkäisyn pettäminen voi seurata muiden lääkkeiden (entsyymi-induktorien) ja suun kautta otettavien yhdistelmäehkäisyvalmisteiden yhteisvaikutusten vuoksi (ks. kohta Yhteisvaikutukset).
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haitta- tasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista seuraavalle taholle:
www-sivusto: www.fimea.fi
Yliannostus
Yaz-tablettien yliannostuksesta ei ole toistaiseksi kokemusta. Muiden yhdistelmäehkäisytablettien käyttöön liittyvän kokemuksen perusteella mahdollisia yliannostusoireita ovat pahoinvointi, oksentelu ja tyhjennysvuoto. Tyhjennysvuotoa voi esiintyä tytöillä myös ennen kuukautisten alkamista, jos he vahingossa ottavat tätä lääkevalmistetta. Antidoottia ei ole ja hoito on oireenmukaista.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Progestageenit ja estrogeenit, kiinteät yhdistelmät
ATC-koodi: G03AA12
Pearlin luku: 0,41 (ylempi kaksisuuntainen 95 % luottamusraja: 0,85)
Pearlin kokonaisluku (menetelmän virhearvo + potilaan virhearvo): 0,80 (ylempi kaksisuuntainen 95 % luottamusraja: 1.30)
Yaz-tablettien ehkäisyteho perustuu monen eri tekijän yhteisvaikutukseen. Näistä tärkeimpiä ovat ovulaation estyminen ja muutokset kohdun limakalvolla.
Kun kolmen syklin ovulaationesto tutkimuksessa verrattiin drospirenonin 3 mg / etinyyliestradiolin 0,020 mg 24 päivän annostelua ja 21 päivän annostelua, 24 päivän annostelu esti enemmän munarakkuloiden kehittymistä. Kun kolmannen syklin aikana tarkoituksellisesti lisättiin annosteluvirheitä, suuremmalla osuudella naisista 21 päivän annostelun ryhmässä oli munasarjojen toimintaa, esimerkiksi ei-toivottuja ovulaatioita, verrattuna naisiin, jotka olivat 24 päivän annostelun ryhmässä. Munasarjojen toiminta palasi käyttöä edeltäneelle tasolle tutkimusta seuraavan syklin aikana 91,8 % naisista, jotka olivat 24 päivän annostelun ryhmässä.
Yaz on yhdistelmäehkäisytabletti, joka sisältää etinyyliestradiolia ja drospirenonia (progestogeeni). Raskauden ehkäisyyn käytettävällä drospirenoniannoksella on myös antiandrogeeninen ja lievä antimineralokortikoidinen vaikutus. Sillä ei ole estrogeenista, glukokortikoidista eikä antiglukokortikoidista vaikutusta. Drospirenonin farmakologinen profiili muistuttaakin hyvin paljon luonnon keltarauhashormonia progesteronia.
Kliinisten tutkimusten perusteella on näyttöä siitä, että drospirenonin lievien antimineralokortikoidisten ominaisuuksien seurauksena Yaz-valmisteeella on lievä antimineralokortikoidinen vaikutus.
Kaksi kaksoissokkoutettua, satunnaistettua, lumelääkekontrolloitua monikeskustutkimusta tehtiin Yaz-tablettien tehon ja turvallisuuden arvioimiseksi keskivaikean acne vulgariksen hoidossa naisilla.
Lumetabletteihin verrattuna Yaz-tabletit vähensivät kuuden kuukauden hoidon aikana leesioita tilastollisesti merkitsevästi paremmin: Yaz vähensi tulehduksellisia leesioita 15,6 % paremmin (49,3 % vs. 33,7 %), ei-tulehduksellisia leesioita 18,5 % paremmin (40,6 % vs. 22,1 %) ja kaikkia leesioita yhteensä 16,5 % paremmin (44,6 % vs. 28,1 %). Lisäksi Yaz-valmisteen käyttäjistä 11,8 % (18,6 % vs. 6,8 %) useammalla kuin lumelääkeryhmässä arviointi oli “oireeton” tai “lähes oireeton” Investigator’s Static Global Assessment (ISGA) -asteikolla.
Farmakokinetiikka
Drospirenoni
Imeytyminen
Suun kautta otettu drospirenoni imeytyy nopeasti ja lähes täydellisesti. Huippupitoisuus seerumissa, noin 38 ng/ml, saavutetaan 1–2 tunnissa kerta-annoksen ottamisen jälkeen. Drospirenonin biologinen hyötyosuus on 76–85 %. Samanaikaisella ruoan nauttimisella ei ole vaikutusta drospirenonin hyötyosuuteen.
Jakautuminen
Suun kautta otetun drospirenonin pitoisuus seerumissa laskee loppuvaiheen puoliintumisajalla 31 tuntia. Drospirenoni sitoutuu seerumin albumiiniin. Se ei sitoudu sukupuolihormonia sitovaan globuliiniin (SHBG) eikä kortikoidia sitovaan globuliiniin (CBG). Vain 3–5 % drospirenonin kokonaismäärästä seerumissa esiintyy vapaana steroidina. Etinyyliestradiolin indusoima SHBG-pitoisuuden nousu ei vaikuta drospirenonin sitoutumiseen seerumin proteiineihin. Drospirenonin jakautumistilavuus on keskimäärin 3,7 ± 1,2 l/kg.
Biotransformaatio
Suun kautta otettu drospirenoni metaboloituu täydellisesti. Sen päämetaboliitit plasmassa ovat drospirenonihappo, jota muodostuu laktonirenkaan avautumisen jälkeen, ja 4,5-dihydro-drospirenoni-3-sulfaatti, joka muodostuu pelkistymistä seuraavan sulfaation seurauksena. Drospirenoniin kohdistuu myös CYP3A4:n katalysoima oksidatiivinen metabolia.
In vitro drospirenoni estää heikosti tai kohtalaisesti sytokromi P450 -entsyymejä CYP1A1, CYP2C9, CYP2C19 ja CYP3A4.
Eliminaatio
Drospirenonin metabolinen puhdistuma seerumista on 1,5 ± 0,2 ml/min/kg. Muuttumatonta lääkeainetta ei juurikaan erity. Drospirenonin metaboliitit erittyvät ulosteeseen ja virtsaan suhteessa 1,2:1,4. Metaboliittien erittymisen puoliintumisaika on noin 40 h.
Vakaa tila
Drospirenonin vakaan tilan huippupitoisuus seerumissa, noin 70 ng/ml, saavutetaan noin 8 päivän hoidon jälkeen. Drospirenonin loppuvaiheen puoliintumisajasta ja valmisteen antovälistä johtuen drospirenonin pitoisuus seerumissa kumuloituu ensimmäisen hoitosyklin aikana noin kolminkertaiseksi.
Erityiset käyttäjäryhmät
Munuaisten vajaatoiminta
Vakaan tilan drospirenonipitoisuus seerumissa naisilla, joilla on lievä munuaisten vajaatoiminta (kreatiniinipuhdistuma CLcr, 50–80 ml/min), vastasi hyvin tilannetta naisilla, joilla oli normaali munuaistoiminta. Drospirenonipitoisuus seerumissa oli noin 37 % korkeampi naisilla, joilla oli keskivaikea munuaisten vajaatoiminta (CLcr 30–50 ml/min), verrattuna normaalin munuaistoiminnan omaaviin naisiin. Myös naiset, jotka sairastivat lievää tai keskivaikeaa munuaisten vajaatoimintaa, sietivät drospirenonihoitoa hyvin. Drospirenonihoidolla ei ollut kliinisesti merkittäviä vaikutuksia seerumin kaliumtasoon.
Maksan vajaatoiminta
Keskivaikeaa maksan vajaatoimintaa sairastavilla vapaaehtoisilla havaittiin noin 50 % lasku oraalisessa puhdistumassa (CL/F) verrattuna normaalin maksan toiminnan omaaviin vapaaehtoisiin. Havaitun drospirenonipuhdistuman pienenemisen keskivaikeaa maksan vajaatoimintaa sairastavilla ei todettu johtavan mihinkään olennaiseen eroon seerumin kaliumtasossa. Kaliumpitoisuuden suurenemista seerumissa yli normaalin ylärajan ei myöskään havaittu diabeteksen ja samanaikaisen spironolaktonihoidon yhteydessä (kaksi tekijää, jotka voivat altistaa potilaan hyperkalemialle). Voidaan päätellä, että drospirenoni on hyvin siedetty potilailla, joilla on lievä tai keskivaikea maksan vajaatoiminta (Child-Pugh B).
Etniset ryhmät
Drospirenonin ja etinyyliestradiolin farmakokinetiikassa ei havaittu olevan eroa japanilaisten ja kaukasialaisten naisten välillä.
Etinyyliestradioli
Imeytyminen
Suun kautta otettu etinyyliestradioli imeytyy nopeasti ja täydellisesti. Huippupitoisuus plasmassa, noin 33 pg/ml, saavutetaan suun kautta otetun kerta-annon jälkeen 1–2 tunnissa. Presysteemisen konjugaation ja maksan ensikierron metabolian johdosta etinyyliestradiolin absoluuttinen biologinen hyötyosuus on noin 60 %. Noin 25 %:lla koehenkilöistä samanaikainen ruoan nauttiminen vähensi etinyyliestradiolin hyötyosuutta, mutta lopuilla koehenkilöistä muutosta ei havaittu.
Jakautuminen
Etinyyliestradiolipitoisuus seerumissa laskee kahdessa vaiheessa. Loppuvaiheen jakautumisvaiheen puoliintumisaika on noin 24 tuntia. Etinyyliestradioli sitoutuu runsaasti, mutta ei spesifisesti plasman albumiiniin (noin 98,5 %) ja indusoi SHBG:n sekä kortikosteroideja sitovan globuliinin (CBG) pitoisuuden nousua seerumissa. Jakautumistilavuus on noin 5 l/kg.
Biotransformaatio
Etinyyliestradioli altistuu merkittävälle suolessa ja maksassa tapahtuvalle ensikierron metabolialle. Etinyyliestradioli metaboloituu pääasiassa aromaattisen hydroksylaation kautta, mutta reaktiossa muodostuu laajasti erilaisia hydroksyloituja ja metyloituja metaboliitteja, jotka esiintyvät vapaina metaboliitteina ja konjugoituneina glukuronidien sulfaattien kanssa.. Etinyyliestradiolin metaboliateitse tapahtuva plasmapuhdistuma on 5 ml/min/kg.
In vitro, etinyyliestradioli on CYP2C19, CYP1A1 ja CYP1A2-entsyymien palautuva inhibiittori sekä CYP3A4/5, CYP2C8 ja CYP2J2-entsyymien mekanismiin perustuva inhibiittori.
Eliminaatio
Etinyyliestradioli ei erity merkitsevässä määrin muuttumattomassa muodossa. Etinyyliestradiolin metaboliitit erittyvät virtsaan ja sappeen suhteessa 4:6, ja niiden eliminaation puoliintumisaika on noin 1 päivä.
Vakaa tila
Vakaa tila saavutetaan syklin jälkipuoliskolla, ja etinyyliestradiolipitoisuus seerumissa kumuloituu 2,0–2,3 kertaiseksi.
Prekliiniset tiedot turvallisuudesta
Laboratorioeläimillä drospirenonin ja etinyyliestradiolin vaikutukset rajoittuivat niihin, jotka liittyvät tunnettuun farmakologiseen vaikutukseen. Erityisesti lisääntymistoksikologisissa tutkimuksissa havaittiin lajispesifisenä pidettäviä alkio- ja sikiötoksisia vaikutuksia. Kun eläimille annettiin suurempia annoksia kuin ihmisille annettavat Yaz-annokset ovat, sen havaittiin vaikuttavan sukupuolen eriytymiseen rottien sikiöissä, mutta ei apinoissa. Ympäristöön kohdistuvia riskejä arvioivissa tutkimuksissa on havaittu, että etinyyliestradioli ja drospirenoni voivat mahdollisesti aiheuttaa haittaa vesistölle (ks. kohta Erityiset varotoimet hävittämiselle ja muut käsittelyohjeet).
Farmaseuttiset tiedot
Apuaineet
Vaikuttavia aineita sisältävät tabletit (vaaleanpunainen):
Tabletin ydin: Laktoosimonohydraatti, maissitärkkelys, magnesiumstearaatti (E470b).
Tabletin kalvopäällyste: Hypromelloosi (E464), talkki (E553b), titaanidioksidi (E171), punainen rautaoksidi (E172).
Lumetabletit (valkoinen):
Tabletin ydin: Laktoosimonohydraatti, Mikrokiteinen selluloosa, magnesiumstearaatti (E470b).
Tabletin kalvopäällyste: Hypromelloosi (E464), talkki (E553b), titaanidioksidi (E171).
Yhteensopimattomuudet
Ei oleellinen.
Kestoaika
5 vuotta.
Säilytys
Tämä lääkevalmiste ei vaadi erityisiä säilytysolosuhteita.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
YAZ tabletti, kalvopäällysteinen
0,02/3 mg (L:kyllä) 28 fol (13,62 €), 3 x 28 fol (37,92 €), 6 x 28 fol (73,37 €)
PF-selosteen tieto
Läpinäkyvä PVC-/alumiiniläpipainopakkaus.
Pakkauskoot: 28, 3x28 ja 6x28 tablettia
Jokainen läpipainopakkaus sisältää 24 vaaleanpunaista kalvopäällysteistä tablettia sekä neljä valkoista kalvopäällysteistä lumetablettia.
Valmisteen kuvaus:
Vaikuttavia aineita sisältävä tabletti on vaaleanpunainen, pyöreä, kupera tabletti, jonka toisella puolella on merkintä ”DS” tasasivuisen kuusikulmion sisällä.
Lumetabletti on valkoinen, pyöreä, kupera tabletti, jonka toisella puolella on merkintä ”DP” tasasivuisen kuusikulmion sisällä.
Käyttö- ja käsittelyohjeet
Tällä lääkevalmisteella voi olla haitallisia vaikutuksia ympäristölle (ks. kohta Prekliiniset tiedot turvallisuudesta). Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
YAZ tabletti, kalvopäällysteinen
0,02/3 mg 28 fol, 3 x 28 fol, 6 x 28 fol
- Ei korvausta.
ATC-koodi
G03AA12
Valmisteyhteenvedon muuttamispäivämäärä
25.05.2023
Yhteystiedot
Tuulikuja 2, PL 73
02151 Espoo
020 785 21
www.bayer.fi

 BAYER OY
BAYER OY