AZELASTINE/FLUTICASONE ADVANZ PHARMA nässpray, suspension 125/50 mikrog/annos
Kvalitativ och kvantitativ sammansättning
Varje g suspension innehåller 1000 mikrogram azelastinhydroklorid (motsvarande 913 mikrogram azelastin) och 365 mikrogram flutikasonpropionat (motsvarande 262,8 mikrogram flutikason).
En sprayning (0,14 g) ger 137 mikrogram azelastinhydroklorid (motsvarande 125 mikrogram azelastin) och 50 mikrogram flutikasonpropionat (motsvarande 36 mikrogram flutikason).
Hjälpämne med känd effekt:
En sprayning (0,14 g) ger 0,014 mg bensalkoniumklorid.
För fullständig förteckning över hjälpämnen, se avsnitt Förteckning över hjälpämnen.
Läkemedelsform
Nässpray, suspension.
Kliniska uppgifter
Terapeutiska indikationer
Lindring av symtom vid måttlig till svår säsongsbunden och perenn allergisk rinit hos vuxna och pediatriska patienter från 12 år, om monoterapi med antingen intranasalt antihistamin eller glukokortikoid inte anses vara tillräcklig.
Dosering och administreringssätt
Dosering
Regelbunden användning är viktig för att uppnå full terapeutisk effekt.
Kontakt med ögonen ska undvikas.
Vuxna och ungdomar (från 12 år)
En sprayning i vardera näsborren två gånger dagligen (morgon och kväll).
Barn under 12 år
Azelastine/Fluticasone Advanz Pharma nässpray rekommenderas inte till barn under 12 år eftersom säkerhet och effekt för denna åldersgrupp inte har fastställts.
Äldre
Ingen dosjustering krävs för äldre patienter.
Nedsatt njur- och leverfunktion
Det finns inga data avseende patienter med nedsatt njur- och leverfunktion.
Behandlingens längd
Azelastine/Fluticasone Advanz Pharma nässpray lämpar sig för långtidsbruk.
Behandlingens längd ska överensstämma med perioden av allergenexponering.
Administreringssätt
Azelastine/Fluticasone Advanz Pharma nässpray är endast avsedd för nasal användning.
Bruksanvisning
Förbereda sprayen:
Flaskan ska skakas försiktigt i cirka 5 sekunder före användning genom att vända den upp och ned, och därefter ska skyddslocket tas bort. Azelastine/Fluticasone Advanz Pharma nässpray måste aktiveras före första användning genom att trycka ned och släppa pumpen 6 gånger. Om Azelastine/Fluticasone Advanz Pharma nässpray inte har använts på mer än 7 dagar ska den återaktiveras genom att trycka ned och släppa pumpen en gång.
Använda sprayen:
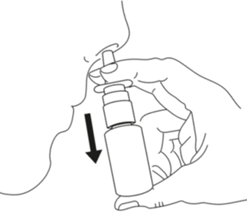
Näsan ska snytas varefter suspensionen sprayas en gång i vardera näsborre samtidigt som huvudet hålls nedåtböjt (se bilden nedan). Efter användning ska sprayspetsen torkas av och skyddslocket sättas tillbaka.
Kontraindikationer
Överkänslighet mot de aktiva substanserna eller mot något hjälpämne som anges i avsnitt Förteckning över hjälpämnen.
Varningar och försiktighet
Efter marknadsintroduktion har det förekommit rapporter om kliniskt signifikanta läkemedelsinteraktioner hos patienter som behandlats med flutikasonpropionat och ritonavir, vilka resulterat i systemiska kortikosteroida effekter, inklusive Cushings syndrom och binjurebarksuppression. Samtidig användning av flutikasonpropionat och ritonavir ska därför undvikas, såvida inte den eventuella nyttan för patienten överväger risken för systemiska biverkningar av kortikosteroiden (se avsnitt Interaktioner).
Systemiska effekter av nasala kortikosteroider kan förekomma, särskilt vid ordinering av höga doser under längre tidsperioder. Jämfört med orala kortikosteroider är det mycket mindre troligt att dessa effekter uppkommer, och de kan variera mellan enskilda patienter och olika kortikosteroidpreparat. Eventuella systemiska effekter kan inkludera Cushings syndrom, cushingliknande tecken, binjurebarksuppression, hämmad tillväxt hos barn och ungdomar, katarakt, glaukom och mer sällsynt en rad psykologiska störningar eller beteendestörningar, inklusive psykomotorisk hyperaktivitet, sömnstörningar, oro, depression eller aggression (särskilt hos barn).
Detta läkemedel genomgår omfattande förstapassagemetabolism. Den systemiska exponeringen av intranasalt flutikasonpropionat hos patienter med svår leversjukdom är således sannolikt högre. Detta kan leda till en högre frekvens av systemiska biverkningar. Försiktighet rekommenderas vid behandling av dessa patienter.
Behandling med nasala kortikosteroider i doser som överstiger rekommenderade doser kan leda till kliniskt signifikant binjurebarksuppression. Om det finns belägg för att högre doser än de rekommenderade har använts, ska tillägg av systemiska kortikosteroider övervägas under perioder av stress eller vid planerad kirurgi.
I allmänhet ska dosen intranasalt flutikasonpreparat minskas till den lägsta dosen vid vilken effektiv symtomkontroll av rinit bibehålls. Högre doser än den rekommenderade (se avsnitt Dosering och administreringssätt) har inte testats för azelastinhydroklorid/flutikasonpropionat nässpray. I likhet med alla intranasala kortikosteroider ska den totala systemiska bördan av kortikosteroider beaktas när andra typer av kortikosteroider ordineras samtidigt.
Hämmad tillväxt har rapporterats hos barn som fått nasala kortikosteroider i rekommenderade doser. Eftersom även ungdomar fortfarande växer, rekommenderas regelbunden kontroll av tillväxten också hos ungdomar som står på långtidsbehandling med nasala kortikosteroider. Om tillväxten hämmas ska behandlingen omprövas för att om möjligt minska dosen nasala kortikosteroider till den lägsta dos vid vilken effektiv symtomkontroll bibehålls.
Synrubbning kan rapporteras vid systemisk och topisk användning av kortikosteroider. Om en patient inkommer med symtom såsom dimsyn eller andra synrubbningar ska man överväga att remittera patienten till en oftalmolog för utredning av möjliga orsaker. Dessa kan innefatta katarakt, glaukom eller sällsynta sjukdomar, såsom central serös korioretinopati (CSCR), som har rapporterats efter användning av systemiska och topiska kortikosteroider.
Noggrann övervakning krävs hos patienter med en synförändring eller en anamnes på ökat okulärt tryck, glaukom och/eller katarakt.
Om det kan antas att binjurebarksfunktionen är nedsatt, måste försiktighet iakttas när patienter överförs från behandling med systemiska steroider till Azelastine/Fluticasone Advanz Pharma nässpray.
Hos patienter som har tuberkulos, någon form av obehandlad infektion eller som nyligen har genomgått en kirurgisk operation av näsan eller munnen eller som har skadat näsan eller munnen ska de eventuella fördelarna av behandlingen med Azelastine/Fluticasone Advanz Pharma nässpray vägas mot den eventuella risken.
Infektioner i näsans luftvägar ska behandlas med antibakteriella medel eller medel mot svamp, men de utgör ingen specifik kontraindikation för behandling med Azelastine/Fluticasone Advanz Pharma nässpray.
Detta läkemedel innehåller 0,014 mg bensalkoniumklorid i varje sprayning, motsvarande 0,1 mg/g. Långtidsbruk kan orsaka ödem i nässlemhinnan.
Interaktioner
Flutikasonpropionat
Under normala förhållanden uppnås låga plasmakoncentrationer av flutikasonpropionat efter intranasal administrering på grund av omfattande förstapassagemetabolism och högt systemiskt clearance som medieras av cytokrom P450 3A4 i tarm och lever. Kliniskt signifikanta läkemedelsinteraktioner medierade av flutikasonpropionat är därför osannolika.
En läkemedelsinteraktionsstudie på friska individer har visat att ritonavir (en mycket potent cytokrom P450 3A4‑hämmare) kan kraftigt öka plasmakoncentrationen av flutikasonpropionat. Som en följd av detta minskar serumkortisolkoncentrationen markant. Efter marknadsintroduktion har det förekommit rapporter om kliniskt signifikanta läkemedelsinteraktioner hos patienter som fått intranasalt eller inhalerat flutikasonpropionat och ritonavir, vilka resulterat i systemiska kortikosteroida effekter. Samtidig behandling med andra CYP3A4‑hämmare, inklusive läkemedel som innehåller kobicistat, väntas också öka risken för systemiska biverkningar. Kombinationen ska undvikas såvida inte nyttan överväger den ökade risken för systemiska biverkningar av kortikosteroider, och om så är fallet ska patienter övervakas avseende systemiska biverkningar av kortikosteroider.
Studier har visat att andra cytokrom P450 3A4‑hämmare ökar den systemiska exponeringen av flutikasonpropionat försumbart (erytromycin) eller i liten utsträckning (ketokonazol) utan någon nämnvärd sänkning av serumkortisolkoncentrationen. Försiktighet ska ändå iakttas vid samtidig administrering av potenta cytokrom P450 3A4‑hämmare (t.ex. ketokonazol) eftersom det finns risk för ökad systemisk exponering av flutikasonpropionat.
Azelastinhydroklorid
Inga specifika interaktionsstudier med azelastinhydroklorid nässpray har utförts. Interaktionsstudier med höga orala doser har utförts. Dessa är emellertid inte relevanta för azelastin nässpray eftersom rekommenderade nasala doser leder till en mycket lägre systemisk exponering. Försiktighet ska ändå iakttagas vid administrering av azelastinhydroklorid hos patienter som samtidigt tar sedativa läkemedel eller läkemedel som påverkar centrala nervsystemet, eftersom den sedativa effekten kan förstärkas. Alkohol kan också förstärka denna effekt (se avsnitt Effekter på förmågan att framföra fordon och använda maskiner).
Fertilitet, graviditet och amning
Fertilitet
Det finns endast begränsade data avseende fertilitet (se avsnitt Prekliniska säkerhetsuppgifter).
Graviditet
Det finns inga eller begränsad mängd data från användningen av azelastinhydroklorid och flutikasonpropionat hos gravida kvinnor. Azelastine/Fluticasone Advanz Pharma nässpray ska således användas under graviditet enbart om den potentiella nyttan överväger den potentiella risken för fostret (se avsnitt Prekliniska säkerhetsuppgifter).
Amning
Det är okänt om nasalt administrerat azelastinhydroklorid/metaboliter eller flutikasonpropionat/metaboliter utsöndras i bröstmjölk. Azelastine/Fluticasone Advanz Pharma nässpray ska användas under amning enbart om den potentiella nyttan överväger den potentiella risken för det nyfödda barnet/spädbarnet (se avsnitt Prekliniska säkerhetsuppgifter).
Effekter på förmågan att framföra fordon och använda maskiner
Azelastine/Fluticasone Advanz Pharma nässpray har mindre effekt på förmågan att framföra fordon och använda maskiner.
I enstaka fall kan utmattning, trötthet, yrsel eller svaghet, som också kan orsakas av själva sjukdomen, uppkomma vid användning av Azelastine/Fluticasone Advanz Pharma nässpray. I dessa fall kan förmågan att framföra fordon och använda maskiner vara nedsatt. Alkohol kan förstärka denna effekt.
Biverkningar
Det är vanligt att dysgeusi, en substansspecifik obehaglig smak, kan upplevas efter administrering (ofta beroende på felaktig appliceringsmetod, nämligen att huvudet böjts för mycket bakåt under administreringen).
Biverkningar anges nedan klassificerade enligt organsystem och frekvens. Frekvenser definieras som:
Mycket vanliga (≥ 1/10)
Vanliga (≥ 1/100, < 1/10)
Mindre vanliga (≥ 1/1 000, < 1/100)
Sällsynta (≥ 1/10 000, < 1/1 000)
Mycket sällsynta (< 1/10 000)
Ingen känd frekvens (kan inte beräknas från tillgängliga data)
Frekvens Organsystem | Mycket vanliga | Vanliga | Mindre vanliga | Sällsynta | Mycket sällsynta | Ingen känd frekvens |
| Immunsystemet | Överkänslighet inklusive anafylaktiska reaktioner, angioödem (ödem i ansikte eller på tungan och hudutslag), bronkospasm | |||||
| Centrala och perifera nervsystemet | Huvudvärk, dysgeusi (obehaglig smak), obehaglig lukt | Yrsel, somnolens (dåsighet, sömnighet) | ||||
| Ögon* | Glaukom, ökat intraokulärt tryck, katarakt | Dimsyn (se avsnitt Varningar och försiktighet) | ||||
| Andningsvägar, bröstkorg och mediastinum | Näsblödning | Nasalt obehag (inklusive nasal irritation, sveda, klåda), nysning, nasal torrhet, hosta, torr hals, halsirritation | Perforation av nässkiljevägg**, slemhinneerosion | Nässår | ||
| Magtarmkanalen | Muntorrhet | Illamående | ||||
| Hud och subkutan vävnad | Hudutslag, pruritus, urtikaria | |||||
| Allmänna symtom och/eller symtom vid administreringsstället | Fatigue (trötthet, utmattning), svaghet (se avsnitt Effekter på förmågan att framföra fordon och använda maskiner) |
* Ett mycket litet antal spontana rapporter har identifierats efter långvarig behandling med intranasalt flutikasonpropionat.
** Perforation av nässkiljeväggen har rapporterats efter användning av intranasala kortikosteroider.
Systemiska effekter av vissa nasala kortikosteroider kan förekomma, särskilt vid administrering av höga doser under långa perioder (se avsnitt Varningar och försiktighet).
Hämmad tillväxt har rapporterats hos barn som får nasala kortikosteroider. Hämmad tillväxt kan även drabba ungdomar (se avsnitt Varningar och försiktighet).
I sällsynta fall har osteoporos observerats vid långvarig administrering av nasala glukokortikoider.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta‑riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning till:
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Överdosering
Vid nasal administrering förväntas inga överdoseringsreaktioner.
Det finns inga tillgängliga patientdata avseende effekterna av akut eller kronisk överdosering med intranasalt flutikasonpropionat.
Intranasal administrering av 2 milligram flutikasonpropionat (10 gånger den rekommenderade dagliga dosen) två gånger dagligen i sju dagar till friska frivilliga har ingen effekt på hypotalamus‑hypofys‑binjurebarkaxelns (HPA‑axelns) funktion.
Administrering av högre doser än de rekommenderade under en längre tid kan leda till tillfällig suppression av binjurebarksfunktionen.
Hos dessa patienter ska behandling med Azelastine/Fluticasone Advanz Pharma nässpray fortsätta med en dos tillräcklig för att kontrollera symtomen. Binjurebarksfunktionen återhämtar sig inom några dagar och kan verifieras genom mätning av plasmakortisol.
I händelse av överdosering efter oavsiktligt oralt intag kan störningar i centrala nervsystemet (inklusive dåsighet, förvirring, koma, takykardi och hypotension) orsakade av azelastinhydroklorid förväntas baserat på resultaten av djurförsök.
Behandlingen av dessa tillstånd ska vara symtomatisk. Beroende på svald mängd rekommenderas ventrikelsköljning. Det finns ingen känd antidot.
Farmakologiska egenskaper
Farmakodynamiska egenskaper
Farmakoterapeutisk grupp: Avsvällande och övriga medel för lokal behandling vid nässjukdomar, kortikosteroider/flutikason, kombinationer, ATC‑kod: R01AD58.
Verkningsmekanism och farmakodynamisk effekt
Azelastine/Fluticasone Advanz Pharma nässpray innehåller azelastinhydroklorid och flutikasonpropionat, som har olika verkningsmekanismer och visar synergistiska effekter när det gäller förbättring av symtom på allergisk rinit och rinokonjunktivit.
Flutikasonpropionat
Flutikasonpropionat är en syntetisk trifluorinerad kortikosteroid som har en mycket hög affinitet för glukokortikoidreceptorn och en potent antiinflammatorisk effekt, t.ex. 3‑5 gånger mer potent än dexametason vid bindnings- och genexpressionsanalyser på klonad human glukokortikoidreceptor.
Azelastinhydroklorid
Azelastin, ett ftalazinonderivat, klassificeras som en potent långverkande antiallergen substans med selektiva H1‑antagonistegenskaper samt mastcellsstabiliserande och antiinflammatoriska egenskaper. Data från studier in vivo (prekliniska) och in vitro visar att azelastin hämmar syntesen eller frisättningen av kemiska mediatorer som är kända för att vara inblandade i tidiga och sena stadier av allergiska reaktioner, t.ex. leukotriener, histamin, trombocytaktiverande faktor (PAF) och serotonin.
Lindring av nasala allergisymtom observeras inom 15 minuter efter administrering.
Azelastin/flutikason nässpray
I fyra kliniska studier hos vuxna och ungdomar med allergisk rinit förbättrade en sprayning med azelastin/flutikason nässpray i vardera näsborren två gånger dagligen signifikant de nasala symtomen (bestående av rinorré, nästäppa, nysning och näsklåda) jämfört med antingen placebo, enbart azelastinhydroklorid eller enbart flutikasonpropionat. Nässprayen gav en signifikant förbättring av okulära symtom (bestående av klåda, tårfyllda/rinnande och röda ögon) och av patientens sjukdomsrelaterade livskvalitet (Rhinoconjunctivitis Quality of Life Questionnaire – RQLQ) i alla fyra studier.
Jämfört med en godkänd flutikasonpropionat nässpray uppnåddes väsentlig symtomförbättring (50 % minskning av nässymtomens svårighetsgrad) signifikant tidigare (3 dagar eller mer) med azelastin/flutikason nässpray. Den överlägsna effekten av kombinerad formulering jämfört med flutikasonpropionat nässpray kvarstod under en ettårig studie hos patienter med kronisk ihållande allergisk rinit och icke‑allergisk/vasomotorisk rinit.
I en exponeringskammarstudie av allergener från ambrosiapollen observerades första statistiskt signifikanta lindringen av nässymtom 5 minuter efter administrering av azelastin/flutikason nässpray (jämfört med placebo). Vid 15 minuter efter administrering av azelastin/flutikason rapporterade 60 % av patienterna en kliniskt relevant minskning av symtompoäng på minst 30 %.
Farmakokinetiska egenskaper
Absorption
Efter intranasal administrering av två sprayningar per näsborre (548 mikrogram azelastinhydroklorid och 200 mikrogram flutikason) av azelastin/flutikason nässpray var den genomsnittliga (± standardavvikelse) maximala plasmaexponeringen (Cmax) 194,5 ± 74,4 pg/ml för azelastin och 10,3 ± 3,9 pg/ml för flutikasonpropionat, och den genomsnittliga totala exponeringen (AUC) var 4 217 ± 2 618 pg/ml*timme för azelastin och 97,7 ± 43,1 pg/ml*timme för flutikason. Mediantiden till maximal exponering (tmax) med en enkeldos var 0,5 timme för azelastin och 1,0 timme för flutikason.
Den systemiska exponeringen av flutikason ökade med cirka 50 % vid jämförelse mellan azelastin/flutikason nässpray och en godkänd flutikason nässpray. Azelastin/flutikason nässpray var likvärdig med en godkänd azelastin nässpray när det gäller systemisk exponering av azelastin. Det fanns inga belägg för farmakokinetiska interaktioner mellan azelastinhydroklorid och flutikasonpropionat.
Distribution
Flutikasonpropionat har en stor distributionsvolym vid steady‑state (cirka 318 liter). Plasmaproteinbindningen är 91 %.
Distributionsvolymen för azelastin är hög vilket indikerar distribution till i huvudsak perifer vävnad. Proteinbindningen är 80‑90 %. Dessutom har båda läkemedlen ett brett terapeutiskt fönster. Således är displacement‑reaktioner av läkemedlet osannolika.
Metabolism
Flutikasonpropionat försvinner snabbt från den systemiska cirkulationen, främst via hepatisk metabolism till en inaktiv karboxylsyrametabolit, via cytokrom P450‑enzymet CYP3A4. Nedsvalt flutikasonpropionat är också föremål för omfattande förstapassagemetabolism. Azelastin metaboliseras till N‑desmetylazelastin via olika CYP‑isoenzymer, i huvudsak CYP3A4, CYP2D6 och CYP2C19.
Eliminering
Elimineringshastigheten för intravenöst administrerat flutikasonpropionat är linjär över doseringsintervallet på 250‑1000 mikrogram och kännetecknas av ett högt plasmaclearance (CL = 1,1 l/min). Maximala plasmakoncentrationer minskar med cirka 98 % inom 3‑4 timmar, och endast låga plasmakoncentrationer är kopplade till den terminala halveringstiden på 7,8 timmar. Renalt clearance av flutikasonpropionat är försumbart (< 0,2 %), och mindre än 5 % avlägsnas som karboxylsyrametaboliten. Den huvudsakliga elimineringsvägen är utsöndring av flutikasonpropionat och dess metaboliter via gallan.
Halveringstiden i plasma efter en enkeldos azelastin är cirka 20‑25 timmar för azelastin och cirka 45 timmar för den terapeutiskt aktiva metaboliten N‑desmetylazelastin. Utsöndring sker i huvudsak via feces. Den fördröjda utsöndringen av små mängder av dosen i feces tyder på att viss enterohepatisk cirkulation kan förekomma.
Prekliniska säkerhetsuppgifter
Flutikasonpropionat
Fynden från allmänna toxikologiska studier motsvarade de som observerats med andra glukokortikoider och förknippas med hög farmakologisk aktivitet. Dessa fynd är sannolikt inte relevanta när rekommenderade nasala doser ges till människa, eftersom doserna leder till minimal systemisk exponering. Inga genotoxiska effekter av flutikasonpropionat har observerats i vanliga genotoxicitetstester. Dessutom sågs inga behandlingsrelaterade ökningar av incidensen av tumörer i tvååriga inhalationsstudier på råtta och mus.
I djurstudier har glukokortikoider visat sig framkalla missbildningar, såsom gomspalt och intrauterin tillväxthämning. Detta är sannolikt inte heller relevant när rekommenderade nasala doser ges till människa, eftersom doserna leder till minimal systemisk exponering (se avsnitt Farmakokinetiska egenskaper).
Azelastinhydroklorid
Azelastinhydroklorid visade ingen sensibiliserande potential hos marsvin. Azelastin visade ingen genotoxisk potential i ett flertal in vitro- och in vivo‑tester, och inte heller någon karcinogenicitet hos råtta och mus. Hos råttor av båda könen orsakade orala doser av azelastin högre än 3 mg/kg/dag en dosrelaterad minskning av fertilitetsindex. I kroniska toxicitetsstudier observerades inga substansrelaterade förändringar i fortplantningsorganen hos något av könen. Hos råtta, mus och kanin uppträdde embryotoxiska och teratogena effekter endast efter doser som var toxiska för modern (till exempel skelettmissbildningar observerades hos råtta och mus vid doser om 68,6 mg/kg/dag).
Azelastin/flutikason nässpray
Studier avseende allmäntoxicitet, där intranasala doser av azelastin/flutikason nässpray gavs till råtta under en period på upp till 90 dagar och till hund i 14 dagar, visade inga nya biverkningar jämfört med de enskilda komponenterna.
Farmaceutiska uppgifter
Förteckning över hjälpämnen
Dinatriumedetat
Glycerol
Mikrokristallin cellulosa (E 460)
Karmellosnatrium (E 466)
Polysorbat 80 (E 433)
Bensalkoniumklorid
Fenyletylalkohol
Renat vatten
Inkompatibiliteter
Ej relevant.
Hållbarhet
2 år.
Hållbarhet i öppnad förpackning (efter första användning): 1 år.
Särskilda förvaringsanvisningar
Förvaras i skydd mot kyla. Får ej frysas.
Förpackningstyp och innehåll
Markkinoilla olevat pakkaukset
Resepti
AZELASTINE/FLUTICASONE ADVANZ PHARMA nenäsumute, suspensio
125/50 mikrog/annos (L:ei) 120 annosta (5,47 €)
PF-selosteen tieto
Bärnstensfärgad flaska av typ I glas med spraypump, nasal applikator (aktuator) av polypropen och skyddslock, innehållande 23 g (minst 120 sprayningar) suspension.
Förpackningsstorlekar:
1 flaska om 25 ml med 23 g suspension (minst 120 sprayningar)
Multipelförpackning innehållande 3 flaskor om 25 ml med vardera 23 g suspension (minst 120 sprayningar)
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Läkemedlets utseende:
Vit, homogen suspension.
Särskilda anvisningar för destruktion och övrig hantering
Skaka flaskan försiktigt före användning.
Inga särskilda anvisningar för destruktion.
Ersättning
AZELASTINE/FLUTICASONE ADVANZ PHARMA nenäsumute, suspensio
125/50 mikrog/annos 120 annosta
- Peruskorvaus (40 %).
Atc-kod
R01AD58
Datum för översyn av produktresumén
14.07.2025
Yhteystiedot
P.O. Box 1452
SE-25114 Helsingborg
Sweden
+46 42 13 57 70
www.advanzpharma.com
medicalinformation@advanzpharma.com
General enquiries: InfoAbcur@advanzpharma.com
Telefon: +46 42 13 57 70
Medical enquiries, Adverse events, product complaints: medicalinformation@advanzpharma.com
Telefon: +358 800 416231
