VEVIZYE silmätipat, liuos 1 mg/ml
Vaikuttavat aineet ja niiden määrät
Yksi millilitra liuosta sisältää 1 mg siklosporiinia.
Täydellinen apuaineluettelo, ks. kohta Apuaineet.
Lääkemuoto
Silmätipat, liuos
Kliiniset tiedot
Käyttöaiheet
Keskivaikean tai vaikean kuivasilmäisyyden (keratoconjunctivitis sicca) hoitoon aikuispotilaille, joiden tila ei ole parantunut keinokyynelhoidosta huolimatta (ks. kohta Farmakodynamiikka).
Ehto
Silmätautien erikoislääkärin on aloitettava hoito ja valvottava sitä.
Annostus ja antotapa
Hoidon aloittaa ja sitä valvoo silmätautien erikoislääkäri.
Annostus
Suositeltu annos on yksi tippa (vastaa 0,01 mg:aa siklosporiinia) kumpaankin silmään kahdesti vuorokaudessa noin 12 tunnin välein.
Jos annos jää väliin, hoitoa jatketaan normaalisti seuraavasta annoksesta. Potilasta on neuvottava tiputtamaan kumpaankin silmään vain yksi tippa.
Iäkkäät potilaat
Annosta ei tarvitse muuttaa iäkkäille potilaille.
Pediatriset potilaat
Ei ole asianmukaista käyttää siklosporiinia pediatrisille potilaille kuivasilmäisyyden hoitoon.
Antotapa
Vain silmän pinnalle.
Potilasta on neuvottava pesemään ensin kädet. Potilasta on neuvottava varmistamaan, ettei tiputtimen kärki pääse kosketuksiin silmän tai minkään pinnan kanssa, sillä tämä voi kontaminoida liuoksen.
Jos potilas käyttää muitakin paikallisesti annosteltavia silmälääkkeitä, lääkevalmisteiden käyttämisen välillä on pidettävä vähintään 15 minuutin tauko (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet). Piilolaseja käyttävät potilaat, ks. kohta Varoitukset ja käyttöön liittyvät varotoimet.
Vasta-aiheet
Yliherkkyys vaikuttavalle aineelle tai kohdassa Apuaineet mainituille apuaineille.
Silmän tai silmänympäryksen maligniteetit tai syövän esiasteet.
Aktiivinen tai epäilty silmän tai silmänympäryksen infektio.
Varoitukset ja käyttöön liittyvät varotoimet
Seuranta
Silmien paikallisen siklosporiinihoidon aikana suositellaan säännöllisiä silmätutkimuksia, esim. 3 kuukauden kuluessa hoidon aloittamisesta ja sen jälkeen noin 6 kuukauden välein.
Glaukooma
Siklosporiinin käytöstä silmänpaine- tai glaukoomapotilaiden hoidossa on vain vähän kokemusta. Säännöllinen kliininen seuranta on tarpeen hoidettaessa potilaita, jotka saavat glaukoomalääkkeitä ja siklosporiinia sisältäviä silmätippoja.
Piilolasit
Vevizye-valmistetta ei pidä annostella silmiin, joissa on piilolasit. Jos potilas käyttää piilolaseja, ne on otettava pois ennen liuoksen annostelua. Piilolasit voi laittaa takaisin, kun Vevizye-valmisteen annostelusta on kulunut 15 minuuttia.
Immuunijärjestelmään kohdistuvat vaikutukset
Silmälääkkeet, joilla on immuunijärjestelmään kohdistuvia vaikutuksia, kuten siklosporiini, saattavat vaikuttaa elimistön kykyyn vastustaa paikallisia infektioita ja maligniteetteja. Jos silmäinfektion merkkejä havaitaan, potilaan on hakeuduttava lääkärin hoitoon.
Yhteisvaikutukset
Vevizye-valmisteella ei ole tehty yhteisvaikutustutkimuksia.
Systeemisiä yhteisvaikutuksia ei ole odotettavissa, sillä siklosporiini ei imeydy systeemisesti Vevizye-valmisteen käytön jälkeen. Kortikosteroideja sisältävien silmätippojen samanaikainen käyttö saattaa voimistaa siklosporiinin vaikutusta immuunijärjestelmään (ks. kohta Varoitukset ja käyttöön liittyvät varotoimet).
Raskaus ja imetys
Raskaus
Vevizye-valmisteen käytöstä raskaana oleville naisille ei ole olemassa tietoja.
Eläimillä tehdyissä tutkimuksissa on havaittu lisääntymistoksisuutta siklosporiinin systeemisen annon jälkeen vain silloin, kun on käytetty altistusta, joka ylittää suurimman ihmisille käytettävän annostuksen niin huomattavasti, että asialla on kliinisen käytön kannalta vain vähäinen merkitys.
Vevizye-valmisteen käyttöä ei suositella raskauden aikana, paitsi jos äidille koituva hyöty on suurempi kuin sikiöön mahdollisesti kohdistuva riski.
Imetys
Vaikutuksia imetettäviin vauvoihin ei ole odotettavissa, sillä imettävän naisen systeeminen altistus Vevizye-valmisteen sisältämälle siklosporiinille on erittäin pieni. Varmuuden vuoksi Vevizye-valmisteen käyttöä on suositeltavaa välttää imetyksen aikana.
Hedelmällisyys
Vevizye-valmisteen vaikutuksista ihmisen hedelmällisyyteen ei ole olemassa tietoja.
Hedelmällisyyteen kohdistuvia vaikutuksia ei ole odotettavissa, sillä systeeminen altistus siklosporiinille on erittäin pieni.
Vaikutus ajokykyyn ja koneiden käyttökykyyn
Vevizye-valmisteella on vähäinen vaikutus ajokykyyn ja koneidenkäyttökykyyn. Jos annostelun jälkeen ilmenee ohimenevää näön hämärtymistä, potilaan on odotettava näön kirkastumista ennen autolla ajamista tai koneiden käyttöä.
Haittavaikutukset
Turvallisuusprofiilin yhteenveto
Yleisimpiä haittavaikutuksia ovat lääkkeen tiputuskohdan reaktiot (8,1 %) ja näön hämärtyminen (0,8 %). Lääkkeen tiputuskohdan reaktiot olivat yleisempiä ≥ 65-vuotiailla potilailla kuin nuoremmilla potilailla.
Haittavaikutustaulukko
Seuraavia alla lueteltuja haittavaikutuksia havaittiin kliinisissä tutkimuksissa.
Haittavaikutukset esitetään MedDRA-elinjärjestelmäluokituksen mukaisesti (elinjärjestelmäluokka ja suositeltu termi). Ne esitetään yleisyyden mukaisessa järjestyksessä: hyvin yleinen (≥ 1/10); yleinen (≥ 1/100, < 1/10); melko harvinainen (≥ 1/1 000, < 1/100); harvinainen (≥ 1/10 000, < 1/1 000); hyvin harvinainen (< 1/10 000) tai tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin).
Taulukko 1: Haittavaikutukset
| Elinjärjestelmäluokka | Yleisyys | Haittavaikutukset |
| Yleisoireet ja antopaikassa todettavat haitat | Yleinen | Lääkkeen tiputuskohdan kipu (kirvely) |
| Silmät | Melko harvinainen | Näön hämärtyminen Silmän ärsytys Silmäkipu Silmän punoitus Heikentynyt näöntarkkuus Silmän kutina |
Valikoitujen haittavaikutusten kuvaus:
Kliinisissä tutkimuksissa yleisin Vevizye-valmisteen käyttöön liittynyt haittavaikutus oli lääkkeen tiputuskohdan kipu (raportoitiin kirvelynä) (7,9 %). Muita lääkkeen tiputuskohdan reaktioita, kuten punoitusta tai kutinaa, esiintyi harvemmin (0,1 %). Kaikki lääkkeen tiputuskohdan reaktiot ovat tyypillisesti lieviä ja ohimeneviä.
Epäillyistä haittavaikutuksista ilmoittaminen
On tärkeää ilmoittaa myyntiluvan myöntämisen jälkeisistä lääkevalmisteen epäillyistä haittavaikutuksista. Se mahdollistaa lääkevalmisteen hyöty-haittatasapainon jatkuvan arvioinnin. Terveydenhuollon ammattilaisia pyydetään ilmoittamaan kaikista epäillyistä haittavaikutuksista kansallisen ilmoitusjärjestelmän kautta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Yliannostus
Paikallinen yliannostus on epätodennäköistä silmään annon jälkeen. Vevizye-valmisteen yliannostustapauksessa tulee antaa oireenmukaista hoitoa.
Farmakologiset ominaisuudet
Farmakodynamiikka
Farmakoterapeuttinen ryhmä: Silmätautien lääkkeet, muut silmätautien lääkkeet, ATC-koodi: S01XA18.
Vaikutusmekanismi
Siklosporiini on kalsineuriinin estäjä, jolla on anti-inflammatorisia ja immunosuppressiivisia ominaisuuksia. Kalsineuriinin estolla on useita sekundaarisia vaikutuksia: (a) mitokondrioiden permeabiliteetin transitiokanavien (MPTP) avautumisen salpaus, joka estää kaspaasien aktivaatiota mitokondrioissa ja tulehtuneiden sidekalvon solujen apoptoosia ja palauttaa pikarisolujen tiiviyden; (b) silmän pinnan aktivoituneiden T-solujen MPTP-kanavien avautuminen, joka aktivoi apoptoosia; (c) tumatekijä kappa-B:n (NFκB) translokaatio ja mitogeeniaktivoidun proteiinikinaasireitin salpaus, joka estää inflammatoristen sytokiinien transkriptiota ja erittymistä ja siten T-solujen rekrytointia.
Vedettömän vehikkelin leviämisominaisuudet vähentävät kitkaa ja parantavat valmisteen tehoa.
Kliininen teho ja turvallisuus
Vevizye-valmisteen tehoa kuivasilmäisyyden hoidossa arvioitiin kahdessa satunnaistetussa, kaksoissokkoutetussa, vehikkelikontrolloidussa monikeskustutkimuksessa (ESSENCE-1 ja ESSENCE-2). Molemmissa tutkimuksissa oli mukana potilaita, joilla oli keskivaikea tai vaikea kuivasilmäisyys, joka määriteltiin sarveiskalvon kokonaisvärjäytymisen (tCFS) pistearvoksi ≥ 10 Yhdysvaltain kansallisen silmäinstituutin (National Eye Institute, NEI) asteikolla, ilman puudutusta tehdyn Schirmerin testin tulokseksi 1–10 mm, sidekalvon lissamiinivihreätestin kokonaispistearvoksi ≥ 2 ja oireiden esiintymiseksi.
ESSENCE-1-tutkimuksessa 328 potilasta satunnaistettiin suhteessa 1:1 saamaan joko Vevizye-valmistetta (N = 162) tai vehikkeliä (N = 166) kahdesti viikossa 3 kuukauden ajan. ESSENCE-2-tutkimuksessa 834 potilasta satunnaistettiin suhteessa 1:1 saamaan joko Vevizye-valmistetta (N = 423) tai vehikkeliä (N = 411) kahdesti viikossa 1 kuukauden ajan.
Molempien tutkimusten ensisijainen päätetapahtuma oli tCFS-pistearvon muutos lähtötilanteesta päivänä 29. tCFS-pistearvo oli sarveiskalvon viiden osa-alueen (inferiorinen, superiorinen, sentraalinen, nasaalinen ja temporaalinen) summapistearvo (vaihteluväli 0–15). Tutkija pisteytti kunkin alueen Yhdysvaltain kansallisen silmäinstituutin (NEI) asteikolla, joka vaihteli asteesta 0 (ei värjäytymistä) asteeseen 3 (voimakas värjäytyminen). Ensisijaisia oirepäätetapahtumia olivat ESSENCE-1-tutkimuksessa silmän pinnan tauti-indeksi (ocular surface disease index, OSDI, vaihteluväli 0–100) ja ESSENCE-2-tutkimuksessa kuivuuspistearvo (visuaalinen analogiasteikko, vaihteluväli 0–100). Tärkeimpiä toissijaisia päätetapahtumia olivat tCFS-pistearvo päivänä 15, tCFS-vasteen eli määritelmän mukaan ≥ 3 asteen paraneman saavuttaneet potilaat, sidekalvon lissamiinivihreävärjäyksen pistearvo (Oxfordin temporaalisten ja nasaalisten pisteiden summa; vaihteluväli 0–10) päivänä 29, sentraalisen sarveiskalvon fluoreseiinivärjäyksen pistearvo (central corneal fluorescein staining, cCFS [Yhdysvaltain kansallisen silmäinstituutin asteikko; vaihteluväli 0–3]) ja näön hämärtymisen pistearvo (visuaalinen analogiasteikko, vaihteluväli 0–100) sekä Schirmerin testissä vasteen saaneet potilaat päivänä 85 ESSENCE-1-tutkimuksessa ja päivänä 29 ESSENCE-2-tutkimuksessa.
Suurin osa tähän kliiniseen ohjelmaan osallistuneista potilaista oli naispuolisia (73 %), potilaiden keskimääräinen ikä (keskihajonta [SD]) oli 58 (15,2) vuotta ja potilaista 38 % oli vähintään 65-vuotiaita. Keskimääräinen (SD) lähtötilanteen tCFS-pistearvo oli 11,5 (1,35), keskimääräinen (SD) lähtötilanteen cCFS-pistearvo oli 2,1 (0,60), keskimääräinen lähtötilanteen sidekalvon lissamiinivihreävärjäyksen pistearvo oli 3,9 (1,71), keskimääräinen (SD) lähtötilanteessa ilman puudutusta tehdyn Schirmerin kyyneltestin pistearvo oli 5,0 mm (2,83), keskimääräinen (SD) lähtötilanteen OSDI-pistearvo oli 47,1 (19,23) ja keskimääräinen (SD) lähtötilanteen kuivuuspistearvo oli 69,9 (15,43).
Päivänä 29 molemmissa tutkimuksissa havaittiin tilastollisesti merkitsevä tCFS-pistearvon lasku Vevizye-valmisteen eduksi (ks. kuva 1).
Kuva 1: tCFS-pistearvon keskimääräinen muutos (SD) lähtötilanteesta päivänä 29
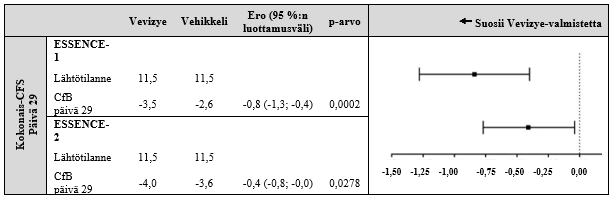
CFS = sarveiskalvon fluoreseiinivärjäys; CfB = muutos lähtötilanteesta
Vasteen saavuttaneiden analyysit osoittivat, että niiden potilaiden osuudet, jotka olivat saavuttaneet kliinisesti merkityksellisen ≥ 3 asteen paraneman tCFS-pistearvossa päivänä 29, olivat molemmissa tutkimuksissa tilastollisesti merkitsevästi erilaiset ja suosivat Vevizye-valmistetta (ks. taulukko 2).
Taulukko 2: Niiden potilaiden prosenttiosuudet, jotka olivat saavuttaneet ≥ 3 asteen paraneman sarveiskalvon fluoreseiinivärjäyksen (tCFS) kokonaispistearvossa päivänä 29 kuivasilmäisyydestä kärsivillä potilailla tehdyissä tutkimuksissa
| ESSENCE-1 | ESSENCE-2 | |||
| Vevizye | Vehikkeli | Vevizye | Vehikkeli | |
| Tutkittavien lukumäärä päivänä 29 | 157 | 165 | 409 | 395 |
| ≥ 3 asteen paranema tCFS-pistearvossa päivänä 29 (% tutkittavista) | 52,9 % | 40,6 % | 71,6 % | 59,7 % |
| Ero (95 %:n luottamusväli) | 12,3 % (1,3 %; 23,0 %) | 12,6 % (6,0 %; 19,3 %) | ||
| p-arvo | 0,0337 | 0,0002 | ||
ESSENCE-1-tutkimuksessa toisessa hierarkkisesti testatussa ensisijaisen oirepäätetapahtuman muutoksessa lähtötilanteesta OSDI-pistearvona havaittiin päivänä 29 numeerista paranemista Vevizye-ryhmässä (pienimmän neliösumman [LS] keskiarvo -8,8), mutta se ei ollut tilastollisesti merkitsevää vehikkeliin verrattuna (LS-keskiarvo -6,8) (p = 0,2634).
ESSENCE-2-tutkimuksessa toinen hierarkkisesti testattu ensisijainen oirepäätetapahtuma, kuivuuspistearvo, parani tilastollisesti merkitsevästi lähtötilanteeseen verrattuna molemmissa ryhmissä: Vevizye-ryhmän LS-keskiarvo oli -12,2 ja vehikkeliryhmän LS-keskiarvo oli -13,6, eikä ryhmien välinen ero ollut merkitsevä (p = 0,3842).
Kaikissa muissa tärkeimmissä silmän pinnan oireita koskeneissa toissijaisissa päätetapahtumissa (tCFS päivänä 15, sidekalvon värjäytyminen päivänä 29 ja sentraalisen sarveiskalvon värjäytyminen päivänä 29) todettiin molemmissa tutkimuksissa tilastollisesti merkitseviä vaikutuksia, jotka suosivat Vevizye-valmistetta (ks. kuva 2).
Lisäksi potilailla, joilla oli merkittävät sentraalisen värjäytymisen pisteet lähtötilanteessa ja jotka saivat Vevizye-hoitoa, todettiin molemmissa tutkimuksissa tilastollisesti merkitsevästi suurempi näön hämärtymispisteiden vähenemä päivänä 29 verrattuna vastaavaan potilasryhmään, jotka saivat vehikkeliä (ks. kuva 2).
Kuva 2: Tärkeimpien toissijaisten päätetapahtumien keskimääräinen muutos (SD) lähtötilanteesta molemmissa avaintutkimuksissa
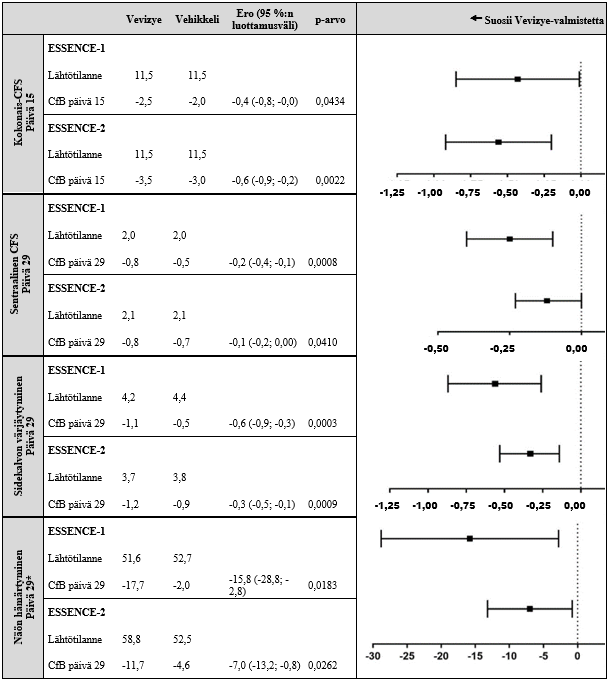
* Alaryhmä, jossa esiintyi voimakasta sentraalista värjäytymistä; CFS = sarveiskalvon fluoreseiinivärjäys; CfB = muutos lähtötilanteesta
Schirmerin kyyneltestissä vasteen saavuttaneiden potilaiden osuus oli vaikuttavaa hoitoa saaneessa ryhmässä tilastollisesti merkitsevästi suurempi kuin vehikkeliä saaneessa ryhmässä ESSENCE-1-tutkimuksen päivänä 85 (Δ 6,74 % [95 %:n luottamusväli 0,50–12,98 %] p = 0,0344) ja ESSENCE-2-tutkimuksen päivänä 29 (Δ 3,92 % [95 %:n luottamusväli 0,02–7,82 %]
p = 0,0487).
Yhteensä 202 potilasta, jotka suorittivat ESSENCE-2-tutkimuksen loppuun, osallistui 12 kuukauden ajan avoimeen jatkotutkimukseen (ESSENCE-2-OLE). Soveltuvat potilaat saivat Vevizye-hoitoa molempiin silmiin kahdesti vuorokaudessa vielä 1 lisävuoden ajan. Yli 80 % potilaista saavutti vasteen (≥ 3 astetta tCFS-pistearvossa) 4 viikon jälkeen, ja tämä vaste säilyi koko havainnointijakson ajan.
Pediatriset potilaat
Euroopan lääkevirasto on myöntänyt vapautuksen velvoitteesta toimittaa tutkimustulokset Vevizye-valmisteen käytöstä kuivasilmäisyyden hoidossa kaikissa pediatrisissa potilasryhmissä (ks. kohta Annostus ja antotapa ohjeet käytöstä pediatristen potilaiden hoidossa).
Farmakokinetiikka
Siklosporiinin farmakokinetiikkaa tutkittiin kahdessa kliinisessä tutkimuksessa 47 vapaaehtoisella. Veren siklosporiinipitoisuuksia Vevizye-valmisteen kerta-annosten tai useampien annosten jälkeen ei voitu mitata, sillä kaikkien analysoitujen näytteiden pitoisuudet olivat kvantifiointirajan (0,100 ng/ml) alapuolella.
Vehikkelin fysikaalis-kemialliset ominaisuudet tehostavat siklosporiinin paikallista jakautumista ja suurentavat sen biologista hyötyosuutta.
Prekliiniset tiedot turvallisuudesta
Vevizye-valmisteen formulaatiosta saatujen tietojen ja siklosporiinia koskevan tieteellisen kirjallisuuden perusteella farmakologista turvallisuutta, toistuvan altistuksen aiheuttamaa toksisuutta, genotoksisuutta, karsinogeenisuutta sekä lisääntymis- ja kehitystoksisuutta koskevien konventionaalisten tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille, sillä systeemistä altistumista siklosporiinille ei ole osoitettu.
Apuaine perfluorobutyylipentaanin osalta farmakologista turvallisuutta, toistuvan altistuksen aiheuttamaa toksisuutta ja genotoksisuutta koskevien konventionaalisten tutkimusten tulokset eivät viittaa erityiseen vaaraan ihmisille.
Ympäristöön kohdistuvien riskien arviointitutkimukset ovat osoittaneet, että apuaine perfluorobutyylipentaani saattaa olla hitaasti hajoava.
Farmaseuttiset tiedot
Apuaineet
Perfluorobutyylipentaani
Etanoli, vedetön
Yhteensopimattomuudet
Koska yhteensopivuustutkimuksia ei ole tehty, tätä lääkevalmistetta ei saa sekoittaa muiden lääkevalmisteiden kanssa.
Kestoaika
2 vuotta.
Vevizye-valmistetta voidaan käyttää 4 viikon ajan pullon ensimmäisen avaamisen jälkeen. Pullo on pidettävä tiukasti suljettuna, kun sitä ei käytetä.
Säilytys
Säilytä alle 25 °C.
Ei saa jäätyä. Älä säilytä kylmässä.
Pakkaukset ja valmisteen kuvaus
Markkinoilla olevat pakkaukset
Resepti
VEVIZYE silmätipat, liuos
1 mg/ml (L:ei) 2 ml (103,69 €)
PF-selosteen tieto
Vevizye 1 mg/ml silmätipat, liuos toimitetaan läpikuultavasta polypropyleenistä valmistetussa moniannospullossa, jossa on läpikuultavasta polypropyleenistä valmistettu kärki ja valkoisesta polyetyleenistä valmistettu turvarengas.
Kotelo sisältää yhden 5 ml:n pullon tai kolme 5 ml:n pulloa, jonka/joiden täyttötilavuus on 2 ml.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Valmisteen kuvaus:
Kirkas, väritön liuos.
Käyttö- ja käsittelyohjeet
Tämä lääkevalmiste saattaa olla vaarallinen ympäristölle (ks. kohta Prekliiniset tiedot turvallisuudesta). Lääkejätettä ei pidä kaataa WC-pönttöön eikä lavuaariin. Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Korvattavuus
VEVIZYE silmätipat, liuos
1 mg/ml 2 ml
- Alempi erityiskorvaus (65 %). Siklosporiini-silmätippa: Vaikean sarveiskalvotulehduksen hoito Sjögrenin oireyhtymää sairastavilla potilailla erityisin edellytyksin (286).
- Peruskorvaus (40 %).
ATC-koodi
S01XA18
Valmisteyhteenvedon muuttamispäivämäärä
23.04.2025
Yhteystiedot
Storgatan 55
703 63 Örebro
Sweden
+46 1933 3780
www.thea-nordic.fi
info@thea-nordic.com
