VETORYL purutabletti 20 mg
ELÄINLÄÄKEVALMISTEEN NIMI
Vetoryl 20 mg purutabletit koiralle
VAIKUTTAVAT JA MUUT AINEET
Yksi tabletti sisältää:
Trilostaani 20 mg
Vaaleanruskea, ruskeapilkullinen, pyöreä ja kupera maustettu 7 mm:n purutabletti, jonka toisella puolella on ristinmuotoinen jakouurre.
KÄYTTÖAIHEET
Aivolisäkeperäisen ja lisämunuaisperäisen lisämunuaiskuoren liikatoiminnan (Cushingin tauti ja oireyhtymä) hoitoon.
VASTA-AIHEET
Ei saa käyttää perussairautena maksasairautta ja/tai munuaisten vajaatoimintaa sairastaville eläimille.
Ei saa käyttää tapauksissa, joissa esiintyy yliherkkyyttä vaikuttavalle aineelle tai apuaineille.
Ei saa käyttää alle 3 kg painaville koirille.
HAITTAVAIKUTUKSET
Koira:
Melko harvinainen (1–10 eläintä 1 000 hoidetusta eläimestä): | Letargiaa,b, ruokahaluttomuusa,b, oksentelua,b, ripulia,b |
Harvinainen (1–10 eläintä 10 000 hoidetusta eläimestä): | Lisämunuaiskuoren vajaatoimintac, kuolaaminend, turvotusd, ataksiad, lihasten vapinad, ihosairaudetd, munuaisten vajaatoimintae, niveltulehduse, heikkousa,b |
Hyvin harvinainen (< 1 eläin 10 000 hoidetusta eläimestä, yksittäiset ilmoitukset mukaan luettuina): | Lisämunuaisten nekroosif, äkkikuolema |
a Liittyy iatrogeeniseen lisämunuaiskuoren vajaatoimintaan, etenkin ellei seuranta ole riittävää (ks. kohta ”Annostus, antoreitit ja antotavat kohde-eläinlajeittain”); yleensä korjattavissa vaihtelevassa ajassa hoidon lopettamisen jälkeen.
b Havaittu trilostaanilla hoidetuilla koirilla ilman näyttöä lisämunuaiskuoren vajaatoiminnasta.
c Mukaan lukien akuutti Addisonin kriisi (tajunnan tason heikentyminen) (ks. kohta ”Erityisvaroitukset”).
d Lievä.
e Tulee esiin hoidossa, koska valmiste pienentää endogeenistä kortikosteroidipitoisuutta.
f Saattaa johtaa lisämunuaiskuoren vajaatoimintaan.
Kortikosteroidien vieroitusoireyhtymä tai kortisolin vajaaeritys täytyy erottaa lisämunuaiskuoren vajaatoiminnasta arvioimalla seerumin elektrolyytit.
Haittatapahtumista ilmoittaminen on tärkeää. Se mahdollistaa tuotteen turvallisuuden jatkuvan seurannan. Jos havaitset haittavaikutuksia, myös sellaisia, joita ei ole mainittu tässä pakkausselosteessa, tai olet sitä mieltä, että lääke ei ole tehonnut, ilmoita ensisijaisesti asiasta eläinlääkärillesi. Voit ilmoittaa kaikista haittavaikutuksista myös myyntiluvan haltijalle tai myyntiluvan haltijan paikalliselle edustajalle käyttämällä tämän pakkausselosteen lopussa olevia yhteystietoja tai kansallisen ilmoitusjärjestelmän kautta:
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
www-sivusto: https://www.fimea.fi/elainlaakkeet/
KOHDE-ELÄINLAJI
Koira.
ANNOSTUS, ANTOREITIT JA ANTOTAVAT KOHDE-ELÄINLAJEITTAIN
Annetaan suun kautta.
Hoidon aloitusannos on noin 2 mg/kg.
Annetaan kerran päivässä ruoan kanssa.
Oikean annostuksen varmistamiseksi eläimen paino on määritettävä mahdollisimman tarkasti.
Eläinlääkäri säätää annoksen yksilöllisen vasteen mukaan seurannan perusteella (ks. alla). Jos annosta täytyy suurentaa, suurenna kerran päivässä annettavaa annosta hitaasti käyttämällä sopivaa tablettivahvuutta ja tabletin osaa. Laaja valikoima erivahvuisia jaettavia tabletteja mahdollistaa parhaan annostelun kullekin koiralle. Anna pienin tarvittava annos, jolla kliiniset oireet pysyvät hallinnassa.
Jos oireita ei kuitenkaan saada hallintaan annosten välisten 24 tunnin aikana, harkitse kokonaisvuorokausiannoksen suurentamista enintään 50 %:lla niin, että se jaetaan samankokoisiksi aamulla ja illalla annettaviksi annoksiksi.
Pieni osa eläimistä saattaa tarvita huomattavasti suuremman annoksen kuin 10 mg painokiloa kohti vuorokaudessa. Näissä tilanteissa toteutetaan riittävä lisäseuranta.
Annoksen muuttaminen voi olla tarpeen, jos koiran hoito vaihdetaan kovista Vetoryl-kapseleista Vetoryl-purutabletteihin tai päinvastoin; täydellistä vaihdettavuutta näiden kahden valmisteen välillä ei voida taata, koska jotkin koirat saattavat reagoida eri tavalla lääkemuodon vaihtoon.
Seuranta:
Biokemiallisia kokeita (myös elektrolyyttejä) ja ACTH-koetta (adrenokortikotropiinikoetta) varten otetaan näytteet ennen hoitoa ja sitten 10 päivän, 4 viikon ja 12 viikon kuluttua ja sen jälkeen 3 kuukauden välein, ensimmäisen diagnoosin ja jokaisen annosmuutoksen jälkeen sekä vaihdettaessa kovista Vetoryl-kapseleista Vetoryl-purutabletteihin tai päinvastoin. Tulosten tarkkaa tulkintaa varten ACTH-kokeet täytyy ehdottomasti tehdä 4–6 tunnin kuluttua lääkkeen antamisesta. Lääke on parasta antaa aamuisin, koska tällöin eläinlääkäri voi suorittaa seurantakokeet 4–6 tunnin kuluttua lääkkeen antamisesta. Säännölliset sairauden kliinisen etenemisen arvioinnit on myös tehtävä edellä mainittuina ajankohtina.
Jos ACTH-kokeessa ei todeta stimulaatiota seurannan aikana, hoito keskeytetään 7 päiväksi ja aloitetaan sitten uudelleen pienemmällä annoksella. Toista ACTH-koe vielä 14 päivän kuluttua. Jos kokeessa ei edelleenkään todeta stimulaatiota, hoito keskeytetään lisämunuaiskuoren liikatoiminnan oireiden uusiutumiseen asti. Toista ACTH-koe kuukauden kuluttua hoidon uudelleen aloittamisesta.
ANNOSTUSOHJEET
Tabletit voi jakaa kahteen tai neljään yhtä suureen osaan tarkkaa annostusta varten. Pane tabletti tasaiselle pinnalle uurrettu puoli ylöspäin ja kupera (pyöristetty) puoli alaspäin.
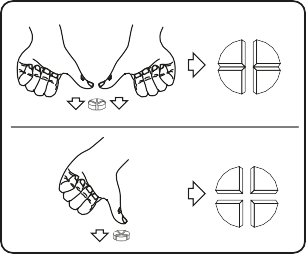
Kahteen yhtä suureen osaan: paina peukaloilla tabletin kumpaakin puolta.
Neljään yhtä suureen osaan: paina peukalolla tabletin keskustaa.
VAROAIKA
Ei oleellinen.
SÄILYTYSOLOSUHTEET
Ei lasten näkyville eikä ulottuville.
Käyttämättömät tabletin osat säilytetään alkuperäisessä läpipainopakkauksessa ja ulkopakkauksessa ja käytetään seuraavalla antokerralla. Älä käytä tätä eläinlääkettä viimeisen käyttöpäivämäärän jälkeen, joka on ilmoitettu läpipainopakkauksessa merkinnän Exp. jälkeen. Viimeisellä käyttöpäivämäärällä tarkoitetaan kuukauden viimeistä päivää.
Älä säilytä yli 30 °C.
ERITYISVAROITUKSET
Erityisvaroitukset:
Lisämunuaiskuoren liikatoiminta täytyy diagnosoida oikein.
Diagnoosi arvioidaan uudelleen, jos hoitoon ei ole ilmeistä vastetta. Annosta voidaan joutua suurentamaan.
Eläinlääkärien täytyy huomioida, että lisämunuaiskuoren liikatoimintaa sairastavilla koirilla on kohonnut haimatulehduksen riski. Hoito trilostaanilla ei välttämättä vähennä tätä riskiä.
Erityiset varotoimet, jotka liittyvät turvalliseen käyttöön kohde-eläinlajilla:
Suurin osa lisämunuaiskuoren liikatoimintatapauksista diagnosoidaan 10–15-vuotiailla koirilla, joten niillä on usein myös muita patologisia prosesseja. On erityisen tärkeää seuloa tapaukset primaarisen maksasairauden ja munuaisten vajaatoiminnan varalta, koska tämä eläinlääke on näissä tapauksissa vasta-aiheinen.
Sen jälkeen hoidon aikana tarvitaan huolellista seurantaa. Erityisesti täytyy huomioida maksaentsyyymit, elektrolyytit, urea ja kreatiniini.
Diabetes mellituksen ja lisämunuaiskuoren liikatoiminnan samanaikainen esiintyminen vaatii erityisseurantaa. Jos koiraa on aiemmin hoidettu mitotaanilla, sen lisämunuaisten toiminta on vähentynyt. Käytännön kokemuksen perusteella mitotaanin lopettamisen ja trilostaanin aloittamisen välillä pitäisi olla vähintään kuukauden tauko. Lisämunuaisten toiminnan huolellista seurantaa suositellaan, koska koirat saattavat olla alttiimpia trilostaanin vaikutuksille.
Tätä eläinlääkettä pitää käyttää erittäin varovasti koirille, joilla on olemassa oleva anemia, koska lääke saattaa edelleen laskea hematokriittiä ja hemoglobiinia. Koiria täytyy seurata säännöllisin väliajoin primaarisen maksasairauden, munuaissairauden ja diabetes mellituksen varalta.
Tabletit ovat makutabletteja. Vahingossa tapahtuvan nielemisen estämiseksi säilytä tabletit poissa eläinten ulottuvilta.
Erityiset varotoimenpiteet, joita eläinlääkettä eläimille antavan henkilön on noudatettava:
Trilostaani saattaa vähentää testosteronisynteesiä, ja sillä on progesteronin vastavaikutusominaisuuksia. Raskaana olevat ja raskautta suunnittelevat eivät saa käsitellä tätä eläinlääkettä.
Pese kädet käytön jälkeen. Henkilöiden, jotka ovat yliherkkiä trilostaanille tai jollekin apuaineista, tulee välttää kosketusta eläinlääkkeen kanssa.
Käytetyt läpipainopakkaukset säilytetään alkuperäisessä ulkopakkauksessa poissa lasten näkyviltä ja ulottuvilta, jotta lapset eivät pääse käsiksi tabletteihin.
Jos vahingossa nielet valmistetta, käänny välittömästi lääkärin puoleen ja näytä hänelle pakkausseloste tai myyntipäällys. Vahingossa nieleminen saattaa aiheuttaa haittavaikutuksia, muun muassa oksentelua ja ripulia.
Tiineys ja laktaatio:
Ei saa käyttää tiineille tai imettäville naaraille.
Hedelmällisyys:
Ei saa käyttää siitoseläimillä.
Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset:
Mahdollisia yhteisvaikutuksia muiden lääkevalmisteiden kanssa ei ole erityisesti tutkittu. Koska lisämunuaiskuoren liikatoimintaa on usein iäkkäämmillä koirilla, monet niistä saavat samanaikaisesti muita lääkkeitä. Kliinisissä tutkimuksissa yhteisvaikutuksia ei havaittu.
Hyperkalemian kehittymisen riski täytyy huomioida, jos trilostaania käytetään yhdessä kaliumia säästävien diureettien tai angiotensiinikonvertaasin (ACE) estäjien kanssa. Tällaisten lääkkeiden samanaikaisen käytön pitää perustua eläinlääkärin tekemään hyöty-riskiarvioon, koska kuolemia (myös äkkikuolemia) on ilmoitettu koirilla, joita on hoidettu samanaikaisesti trilostaanilla ja ACE:n estäjällä.
Yliannostus:
Jos valmistetta annetaan yliannostus, kysy heti neuvoa eläinlääkäriltä.
Yliannostus saattaa aiheuttaa lisämunuaiskuoren vajaatoiminnan oireita (letargia, ruokahaluttomuus, oksentelu, ripuli, sydän- ja verisuonioireet, tajunnan tason heikentyminen). Kuolemantapauksia ei ilmennyt pitkäaikaisessa käytössä terveille koirille annoksella 32 mg/kg, mutta kuolemantapaukset voivat olla odotettavia, jos lisämunuaiskuoren liikatoimintaa sairastaville koirille annetaan suurempia annoksia.
Trilostaanille ei ole erityistä vastalääkettä. Hoito lopetetaan, ja kliinisistä oireista riippuen tukihoito, mukaan lukien kortikosteroidit, elektrolyyttitasapainon korjaus ja nestehoito, voi olla aiheellista.
Akuutissa yliannostuksessa oksennuttaminen ja sen jälkeen lääkehiilen antaminen voi olla hyödyksi.
Mahdollinen iatrogeeninen lisämunuaiskuoren vajaatoiminta korjaantuu yleensä nopeasti hoidon lopettamisen jälkeen. Pienellä osalla koirista vaikutukset voivat kuitenkin pitkittyä. Kun trilostaanihoidon keskeyttämisestä on kulunut viikko, hoito aloitetaan uudestaan pienemmällä annoksella.
ERITYISET VAROTOIMET KÄYTTÄMÄTTÖMÄN VALMISTEEN TAI JÄTEMATERIAALIN HÄVITTÄMISEKSI
Lääkkeitä ei saa kaataa viemäriin eikä hävittää talousjätteiden mukana.
Eläinlääkkeiden tai niiden käytöstä syntyvien jätemateriaalien hävittämisessä käytetään lääkkeiden paikallisia palauttamisjärjestelyjä sekä kyseessä olevaan eläinlääkkeeseen sovellettavia kansallisia keräysjärjestelmiä. Näiden toimenpiteiden avulla voidaan suojella ympäristöä.
Kysy käyttämättömien lääkkeiden hävittämisestä eläinlääkäriltäsi tai apteekista.
PÄIVÄMÄÄRÄ, JOLLOIN PAKKAUSSELOSTE ON VIIMEKSI HYVÄKSYTTY
10.12.2025
Tätä eläinlääkettä koskevaa yksityiskohtaista tietoa on saatavilla unionin valmistetietokannassa (https://medicines.health.europa.eu/veterinary).
MYYNTILUVAN HALTIJAN NIMI JA OSOITE SEKÄ ERÄN VAPAUTTAMISESTA VASTAAVAN VALMISTAJAN NIMI JA OSOITE EUROOPAN TALOUSALUEELLA, JOS ERI
Myyntiluvan haltija:
Dechra Regulatory B.V.
Handelsweg 25
5531 AE Bladel
Alankomaat
Erän vapauttamisesta vastaava valmistaja:
LelyPharma B.V.
Zuiveringweg 42
8243 PZ Lelystad
Alankomaat
Paikalliset edustajat ja yhteystiedot epäillyistä haittatapahtumista ilmoittamista varten:
Dechra Veterinary Products Oy
Yliopistonkatu 31
20100 Turku
Suomi
Puh.: +358 (0)22510500