Pakkausseloste
PREDNICORTONE VET tabletti 5 mg, 20 mg
ELÄINLÄÄKEVALMISTEEN NIMI
Prednicortone vet 5 mg tabletit koiralle ja kissalle
Prednicortone vet 20 mg tabletit koiralle ja kissalle
VAIKUTTAVAT JA MUUT AINEET
Yksi tabletti sisältää:
Vaikuttava aine:
Prednisoloni 5 mg
Prednisoloni 20 mg
Vaaleanruskea, pyöreä ja kupera maustettu tabletti, jossa on ruskeita pilkkuja ja toisella puolella ristikkäisjakouurre. Tabletin voi jakaa kahteen tai neljään yhtä suureen osaan.
KÄYTTÖAIHEET
Tulehduksellisten ja immuunivälitteisten tilojen oireenmukaiseen hoitoon tai tukihoitoon koirilla ja kissoilla.
VASTA-AIHEET
Ei saa käyttää eläimille, joilla on virus- tai sieni-infektio, joka ei ole asianmukaisella hoidolla hallinnassa.
Ei saa käyttää eläimille, joilla on sokeritauti (diabetes mellitus) tai lisämunuaisen liikatoiminta (hyperadrenokortisismi).
Ei saa käyttää eläimille, joilla on luukato (osteoporoosi).
Ei saa käyttää eläimille, joilla on sydämen tai munuaisten vajaatoiminta.
Ei saa käyttää eläimille, joilla on sarveiskalvon haavaumia.
Ei saa käyttää eläimille, joilla on ruoansulatuskanavan haavaumia.
Ei saa käyttää eläimille, joilla on palovammoja.
Ei saa käyttää samanaikaisesti heikennettyjen elävien rokotteiden kanssa.
Ei saa käyttää eläimille, joilla on silmänpainetauti (glaukooma).
Ei saa käyttää tiineyden aikana. Katso myös Erityisvaroitukset; Tiineys ja imetys.
Ei saa käyttää tapauksissa, joissa esiintyy yliherkkyyttä vaikuttavalle aineelle, kortikosteroideille tai apuaineille.
Katso myös Erityisvaroitukset; Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset.
HAITTAVAIKUTUKSET
Koira ja kissa.
Hyvin yleinen (> 1 eläin 10 hoidetusta eläimestä): | kortisolierityksen estyminen1 triglyseridipitoisuuksien nousu2 |
Hyvin harvinainen (< 1 eläin 10 000 hoidetusta eläimestä, yksittäiset ilmoitukset mukaan luettuina): | Kiihotus Haimatulehdus Cushingin tauti3 ,Diabetes mellitus Hepatomegalia Kohonnut seerumin alkalinen fosfataasi (ALP)4 , kohonneet maksaentsyymit, eosinopenia, neutrofiilia5, lymfopenia, hypokalemiaa6 matala tyroksiini (T4) Lihasheikkous ,lihaskato Polyuria7 (lisääntynyt virtsaneritys) Ihon oheneminen, ihon kalkkeutuminen Polyfagia7 (lisääntynyt ruokahalu), polydipsia7 (lisääntynyt janontunne) |
| Määrittämätön esiintymistiheys (ei voida arvioida käytettävissä olevan tiedon perusteella) | Ruoansulatuskanavan haavaumat8 Vähentynyt aspartaattiaminotransferaasi (AST), vähentynyt laktaattidehydrogenaasi (LDH), hyperalbuminemia, matala trijodityroniini (T3), kohonnut lisäkilpirauhashormonin (PTH) pitoisuus Pitkittäisen luun kasvun estyminen, osteoporoosi Viivästynyt paraneminen9, natriumin ja veden kertyminen6 , rasvan jakautumisen muutokset, painonnousu Immuunisuppressio10, heikentynyt vastustuskyky tai olemassa olevien infektioiden paheneminen10 Lisämunuaisen vajaatoiminta11, lisämunuaisen kuorikerroksen surkastuminen11 |
¹ Annostuksesta riippuvaista, johtuen siitä, että tehokkaat annokset tukahduttavat hypotalamus-aivolisäke-lisämunuaisakselin.
² Osana mahdollista iatrogeenista hyperadrenokortikismia (Cushingin tauti).
³ Iatrogeenista, sisältäen merkittävän muutoksen rasva-, hiilihydraatti-, proteiini- ja mineraaliaineenvaihdunnassa.
⁴ Voi liittyä maksan suurenemiseen (hepatomegalia) ja lisääntyneisiin seerumin maksaentsyymeihin.
⁵ Segmentoituneiden neutrofiilien lisääntyminen.
⁶ Pitkäaikaisessa käytössä.
⁷ Systeemisen antamisen jälkeen ja erityisesti hoidon alkuvaiheessa.
⁸ Saattaa pahentua steroideilla eläimillä, jotka saavat ei-steroidisia tulehduskipulääkkeitä, ja eläimillä, joilla on selkäydinvamma.
⁹ Haava.
¹⁰ Virustartuntojen yhteydessä kortikosteroidit voivat pahentaa tai nopeuttaa taudin etenemistä.
¹¹ Voi ilmetä hoidon lopettamisen jälkeen, mikä saattaa estää eläimen riittävän reagoinnin stressaaviin tilanteisiin. On siis syytä harkita keinoja lisämunuaisen vajaatoiminnan ongelmien minimoimiseksi hoidon lopettamisen yhteydessä.
Anti-inflammatoristen kortikosteroidien, kuten prednisolonin, tiedetään aiheuttavan monenlaisia haittavaikutuksia. Yksittäiset korkeat annokset ovat yleensä hyvin siedettyjä, mutta samat annokset voivat pitkään käytettynä aiheuttaa vakavia haittavaikutuksia. Keskipitkiä ja pitkiä hoitojaksoja käytettäessä tulisi annos säätää alhaisimmaksi annokseksi, joka riittää pitämään oireet kurissa.
Katso myös Erityisvaroitukset; Raskaus ja maidon erittyminen.
Haittatapahtumista ilmoittaminen on tärkeää. Se mahdollistaa eläinlääkkeen turvallisuuden jatkuvan seurannan. Jos havaitset haittavaikutuksia, myös sellaisia, joita ei ole mainittu tässä pakkausselosteessa, tai olet sitä mieltä, että lääke ei ole tehonnut, ilmoita ensisijaisesti asiasta eläinlääkärillesi. Voit ilmoittaa kaikista haittavaikutuksista myös myyntiluvan haltijalle tai myyntiluvan haltijan paikalliselle edustajalle käyttämällä tämän pakkausselosteen lopussa olevia yhteystietoja tai kansallisen ilmoitusjärjestelmän kautta:
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
www-sivusto: https://www.fimea.fi/elainlaakkeet/
KOHDE-ELÄINLAJI
Koira ja kissa.

![]()
ANNOSTUS, ANTOREITIT JA ANTOTAVAT KOHDE-ELÄINLAJEITTAIN
Suun kautta.
Eläinlääkäri arvioi tarvittavan annoksen ja hoidon keston yksilöllisesti oireiden vakavuuden perusteella. Alhaisinta tehokasta annosta on käytettävä.
Aloitusannos on 0,5–4 mg elopainokiloa kohti vuorokaudessa.
Jatkohoidossa, kun päivittäisen annostelun jälkeen on saavutettu toivottu teho, annosta tulee laskea kunnes alhaisin tehokas annos saavutetaan.
Annoksen pienentäminen tulee tehdä annostelemalla joka toinen päivä ja/tai puolittamalla annos 5–7 vuorokauden jaksoissa kunnes alhaisin tehokas annos on saavutettu.
ANNOSTUSOHJEET
Koirat lääkitään aamulla ja kissat illalla erilaisen päivärytmin takia.
Tabletit voidaan jakaa kahteen tai neljään yhtä suureen osaan tarkan annostelun varmistamiseksi. Aseta tabletti tasaiselle alustalle jakouurteellinen puoli ylöspäin ja kupera (pyöreä) puoli alustaa vasten.
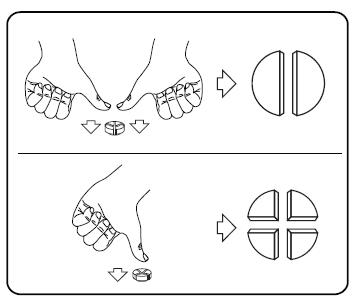
Puolikkaat: paina peukaloilla tabletin molempia sivuja.
Neljännekset: paina peukalolla tabletin keskeltä.
VAROAIKA
Ei oleellinen.
SÄILYTYSOLOSUHTEET
Ei lasten näkyville eikä ulottuville.
Osiin jaettujen tablettien kestoaika: 4 vuorokautta.
Käyttämättömät tabletin osat on säilytettävä avatussa läpipainopakkauksessa, joka laitetaan takaisin pahvikoteloon.
Tämä eläinlääke ei vaadi lämpötilan suhteen erityisiä säilytysolosuhteita.
Älä käytä tätä eläinlääkettä viimeisen käyttöpäivämäärän jälkeen, joka on ilmoitettu läpipainopakkauksessa ja pahvikotelossa merkinnän Exp. jälkeen. Viimeisellä käyttöpäivämäärällä tarkoitetaan kuukauden viimeistä päivää.
ERITYISVAROITUKSET
Erityisvaroitukset:
Kortikoideja käytetään lieventämään kliinisiä oireita, ei varsinaisesti parantamaan sairautta. Hoito tulee yhdistää taustalla olevan sairauden hoitoon ja ympäristöolosuhteiden muuttamiseen.
Erityiset varotoimet, jotka liittyvät turvalliseen käyttöön kohde-eläinlajilla:
Tapauksissa, joissa on bakteerien aiheuttama tulehdus, eläinlääkettä tulee käyttää yhdistettynä sopivaan antibakteeriseen hoitoon. Prednisolonin farmakologisista ominaisuuksista johtuen erityistä varovaisuutta on noudatettava hoidettaessa eläimiä, joiden immuunivaste on heikentynyt.
Kortikoidit, kuten prednisoloni, kiihdyttävät proteiinien aineenvaihdunnallista hajoamista. Tästä syystä eläinlääkettä tulee käyttää harkiten vanhoilla tai aliravituilla eläimillä.
Vaikuttavat annostasot voivat aiheuttaa lisämunuaisen kuorikerroksen surkastumista ja siitä johtuvaa lisämunuaisen vajaatoimintaa. Tämä voi tulla näkyviin etenkin kortikosteroidiannostelun päätyttyä. Lisämunuaisen vajaatoiminnan riskiä voidaan pienentää annostelemalla lääke joka toinen päivä, jos se on mahdollista. Annoksen pienentäminen ja lääkityksen lopettaminen tulee tehdä asteittain, jotta lisämunuaisen vajaatoiminnan kehittymistä voidaan välttää. Katso Annostus, antoreitit ja antotavat kohde-eläinlajeittain.
Kortikoideja, kuten prednisolonia, pitää käyttää varoen potilailla, joilla on verenpainetauti, epilepsia, aiemmin ollut steroidimyopatia, immuunipuutteisilla eläimillä ja nuorilla eläimillä, koska kortikosteroidit voivat viivästyttää kasvua.
Tabletit sisältävät makuainetta. Tahattoman nielemisen välttämiseksi säilytä tabletit eläinten ulottumattomissa.
Erityiset varotoimenpiteet, joita eläinlääkettä eläimille antavan henkilön on noudatettava:
Prednisoloni tai muut kortikosteroidit voivat aiheuttaa yliherkkyyttä (allergisia reaktioita).
- Henkilöiden, jotka ovat yliherkkiä prednisolonille, muille kortikosteroideille tai apuaineille (kuivattu hiiva, kana-aromi, laktoosimonohydraatti, selluloosajauhe, natriumtärkkelysglykolaatti tyyppi A, magnesiumstearaatti), tulee välttää kosketusta eläinlääkevalmisteen kanssa.
- Jotta vältetään tahaton nieleminen, etenkin että lapsi nielisi valmistetta, käyttämättömät tabletin osat on laitettava takaisin avattuun läpipainopakkaukseen, joka laitetaan takaisin pahvikoteloon.
- Jos vahingossa nielet valmistetta, etenkin jos lapsi nielee sitä, käänny välittömästi lääkärin puoleen ja näytä hänelle pakkausseloste tai myyntipäällys.
- Kortikosteroidit voivat aiheuttaa sikiön epämuodostumia. Siksi raskaana olevien naisten on suositeltavaa välttää eläinlääkevalmisteen käsittelyä.
- Pese kädet huolellisesti heti tablettien käsittelyn jälkeen.
Tiineys ja laktaatio:
Ei saa käyttää tiineyden aikana. Laboratoriotutkimuksissa on löydetty näyttöä sikiölle epämuodostumia aiheuttavista vaikutuksista alkutiineyden aikana käytettynä. Myöhemmin tiineyden aikana käytettynä saattaa aiheuttaa aborttia tai aikaisen synnytyksen. Glukokortikoidit erittyvät maitoon ja voivat aiheuttaa imetettäville nuorille eläimille kasvun heikentymistä.
Katso myös Vasta-aiheet.
Imetyksen aikana voidaan käyttää ainoastaan hoitavan eläinlääkärin tekemän hyöty-haitta‑arvion perusteella.
Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset:
Fenytoiini, barbituraatit, efedriini ja rifampisiini voivat nopeuttaa kortikosteroidien poistumista elimistöstä, mikä aiheuttaa alhaisempia lääkeainepitoisuuksia veressä ja heikentynyttä fysiologista vaikutusta. Tämän eläinlääkevalmisteen samanaikainen käyttö ei-steroidisten tulehduskipulääkkeiden kanssa voi pahentaa mahasuolikanavan haavautumista. Koska kortikosteroidit saattavat heikentää rokotusvastetta, prednisolonia ei pidä käyttää samanaikaisesti rokotusten kanssa eikä ennen kuin on kulunut kaksi viikkoa rokotuksesta. Prednisolonin annostelu saattaa aiheuttaa alhaisia kaliumpitoisuuksia ja siten lisätä sydänglykosidien haittojen riskiä. Alhaisen kaliumpitoisuuden riski saattaa suurentua, jos prednisolonia käytetään yhdessä kaliumia säästävien nesteenpoistolääkkeiden kanssa.
Yliannostus:
Yliannostus ei aiheuta muita kuin kohdassa Haittavaikutukset mainittuja haittavaikutuksia. Vasta-ainetta ei tunneta.
ERITYISET VAROTOIMET KÄYTTÄMÄTTÖMÄN VALMISTEEN TAI JÄTEMATERIAALIN HÄVITTÄMISEKSI
Lääkkeitä ei saa kaataa viemäriin eikä hävittää talousjätteiden mukana.
Eläinlääkkeiden tai niiden käytöstä syntyvien jätemateriaalien hävittämisessä käytetään paikallisia palauttamisjärjestelyjä sekä kyseessä olevaan eläinlääkkeeseen sovellettavia kansallisia keräysjärjestelmiä. Näiden toimenpiteiden avulla voidaan suojella ympäristöä.
Kysy käyttämättömien lääkkeiden hävittämisestä eläinlääkäriltäsi tai apteekista.
PÄIVÄMÄÄRÄ, JOLLOIN PAKKAUSSELOSTE ON VIIMEKSI HYVÄKSYTTY
30.04.2025
Tätä eläinlääkettä koskevaa yksityiskohtaista tietoa on saatavilla unionin valmistetietokannassa (https://medicines.health.europa.eu/veterinary).
MUUT TIEDOT
Jaettava tabletti.
MYYNTILUVAN HALTIJAN NIMI JA OSOITE SEKÄ ERÄN VAPAUTTAMISESTA VASTAAVAN VALMISTAJAN NIMI JA OSOITE EUROOPAN TALOUSALUEELLA, JOS ERI
Myyntiluvan haltija:
Dechra Regulatory B.V.
Handelsweg 25
5531 AE Bladel
Alankomaat
Erän vapauttamisesta vastaava valmistaja:
LelyPharma B.V.
Zuiveringsweg 42
8243 PZ Lelystad
Alankomaat
Genera Inc.
Svetonedeljska cesta 2, Kalinovica
10436 Rakov Potok
Kroatia
Paikalliset edustajat ja yhteystiedot epäillyistä haittatapahtumista ilmoittamista varten:
Dechra Veterinary Products Oy
Linnoitustie 4
02600 ESPOO
Suomi
Puh.: +358 (0)22510500
Lisätietoja tästä eläinlääkkeestä saa myyntiluvan haltijan paikalliselta edustajalta.