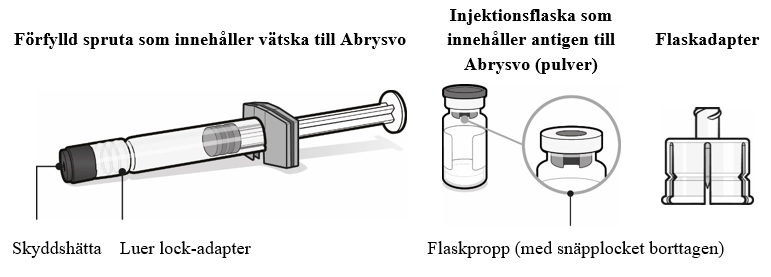
ABRYSVO pulver och vätska till injektionsvätska, lösning
Tilläggsinformation
Abrysvo pulver och vätska till injektionsvätska, lösning
vaccin mot respiratoriskt syncytievirus (bivalent, rekombinant)
Utökad övervakning
▼Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar du eventuellt får. Information om hur du rapporterar biverkningar finns i slutet av avsnitt Eventuella biverkningar.
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du får detta vaccin. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad Abrysvo är och vad det används för
2. Vad du behöver veta innan du får Abrysvo
3. Hur Abrysvo ges
4. Eventuella biverkningar
5. Hur Abrysvo ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Abrysvo är ett vaccin för att förebygga lungsjukdom (sjukdom i luftvägarna) orsakad av ett virus som kallas respiratoriskt syncytievirus (RSV eller RS-virus). Abrysvo ges till:
- gravida personer för att skydda deras spädbarn från födseln upp till 6 månaders ålder
eller
- personer som är 18 år och äldre.
RS-virus är ett vanligt virus som i de flesta fall orsakar milda förkylningsliknande symtom såsom halsont, hosta och nästäppa. Hos små spädbarn kan RS-virus ändå orsaka allvarliga lungproblem. Hos äldre vuxna och hos personer med kroniska medicinska tillstånd kan RS-virus förvärra sjukdomar såsom kroniskt obstruktiv lungsjukdom (KOL) och hjärtsvikt. RS-virus kan leda till inläggning på sjukhus i allvarliga fall och i vissa fall till dödsfall.
Hur Abrysvo fungerar
Detta vaccin hjälper immunsystemet (kroppens naturliga försvar) att bilda antikroppar (ämnen i blodet som hjälper kroppen att bekämpa infektioner). Antikropparna skyddar mot lungsjukdom orsakad av RS-virus. Hos gravida personer som är vaccinerade mellan graviditetsvecka 24 och 36, överförs dessa antikroppar till spädbarnet innan födseln genom moderkakan. Det skyddar spädbarn under den tid som de löper som störst risk från RS-virus.
Vad du behöver veta innan produkten används
Abrysvo ska inte ges
- om du är allergisk mot de aktiva substanserna eller något annat innehållsämne i detta vaccin (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du får detta vaccin
- om du någon gång har fått en allvarlig allergisk reaktion eller andningsproblem efter att du hade fått en injektion med något annat vaccin eller när du tidigare hade fått Abrysvo.
- om du känner dig nervös inför att få vaccinet eller någon gång har svimmat efter en nålinjektion. Svimning kan inträffa före eller efter alla injektioner.
- om du har en infektion med hög feber. I sådana fall kan vaccinationen skjutas upp. Det finns ingen anledning att skjuta upp vaccinationen vid en lindrigare infektion, men tala först med läkare.
- om du har blödningsproblem eller har lätt att få blåmärken.
- om du har ett försvagat immunsystem som kan förhindra att Abrysvo verkar fullt ut.
- om du är gravid men ännu inte nått graviditetsvecka 24.
Om något av ovanstående gäller för dig (eller om du är osäker huruvida det gäller för dig), tala med läkare, apotekspersonal eller sjuksköterska innan du får Abrysvo.
Abrysvo, liksom alla vacciner, kanske inte ger fullgott skydd åt alla som vaccineras.
Barn och ungdomar
Abrysvo rekommenderas inte till barn och ungdomar under 18 år förutom under graviditet (se avsnittet ”Graviditet” nedan).
Andra läkemedel och Abrysvo
Tala om för läkare eller apotekspersonal om du använder, nyligen har använt eller kan tänkas använda andra läkemedel eller nyligen har fått ett annat vaccin.
Abrysvo kan ges samtidigt som ett influensavaccin eller ett covid-19-vaccin. Det bör gå minst två veckor mellan vaccinering med Abrysvo och vaccinering med vaccin mot stelkramp, difteri och kikhosta.
Graviditet och amning
Gravida personer kan ges detta vaccin sent i andra trimestern eller i tredje trimestern (vecka 24 till 36). Rådfråga läkare eller sjuksköterska innan du får detta vaccin om du ammar.
Körförmåga och användning av maskiner
Abrysvo påverkar sannolikt inte din förmåga att köra bil eller använda maskiner.
Abrysvo innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per dos, d.v.s. är näst intill ”natriumfritt”.
Abrysvo innehåller polysorbat 80
Detta läkemedel innehåller 0,08 mg polysorbat 80 per dos. Polysorbater kan orsaka allergiska reaktioner. Tala om för din läkare om du har några kända allergier.
Hur produkten används
Du kommer att få en injektion med 0,5 ml i muskeln i överarmen.
Om du har frågor om Abrysvo, kontakta läkare, apotekspersonal eller sjuksköterska.
Eventuella biverkningar
Liksom alla vacciner kan detta vaccin orsaka biverkningar, men alla användare behöver inte få dem.
Allvarliga biverkningar
Mycket sällsynta (kan förekomma hos upp till 1 av 10 000 användare)
- allvarliga allergiska reaktioner – tecken på en allvarlig allergisk reaktion innefattar svullnad av ansikte, läppar, tunga eller hals, svårigheter att andas eller svälja samt yrsel. Se även avsnitt Vad du behöver veta innan produkten används.
- Guillain-Barrés syndrom (en neurologisk störning som vanligtvis börjar med stickningar och domningar i huden och muskelsvaghet i armar eller ben och kan leda till förlamning i delar av eller i hela kroppen).
Tala omedelbart om för läkare om du upplever tecken på dessa allvarliga biverkningar.
Följande biverkningar har rapporterats hos gravida personer
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare)
- smärta vid injektionsstället
- huvudvärk
- muskelsmärta (myalgi).
Vanliga (kan förekomma hos upp till 1 av 10 användare)
- rodnad vid injektionsstället
- svullnad vid injektionsstället.
Sällsynta (kan förekomma hos upp till 1 av 1 000 användare)
- allergiska reaktioner såsom hudutslag och nässelutslag
- svullna körtlar (lymfkörtelförstoring).
Inga biverkningar har rapporterats hos spädbarn som fötts av vaccinerade mödrar.
Följande biverkningar har rapporterats hos personer som är 18 år och äldre
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare)
- utmattning
- huvudvärk
- smärta vid injektionsstället
- muskelsmärta (myalgi).
Vanliga (kan förekomma hos upp till 1 av 10 användare)
- ledsmärta (artralgi)
- rodnad vid injektionsstället
- svullnad vid injektionsstället.
Mindre vanliga (kan förekomma hos upp till 1 av 100 användare)
- feber (pyrexi).
Sällsynta (kan förekomma hos upp till 1 av 1 000 användare)
- allergiska reaktioner såsom hudutslag och nässelutslag
- svullna körtlar (lymfkörtelförstoring)
- blåmärke vid injektionsstället
- klåda vid injektionsstället.
Mycket sällsynta (kan förekomma hos upp till 1 av 10 000 användare)
- allvarliga allergiska reaktioner (se Allvarliga biverkningar ovan)
- Guillain-Barrés syndrom (se Allvarliga biverkningar ovan).
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på kartongen och etiketten efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras i kylskåp (2 ºC – 8 ºC).
Får ej frysas. Kassera om kartongen har varit fryst.
Efter beredning ska Abrysvo administreras omedelbart eller inom 4 timmar vid förvaring 15 °C ‑ 30 °C. Får ej frysas.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
De aktiva substanserna är:
stabiliserat prefusion F-antigen från RSV-subgrupp A1,2 60 mikrogram
stabiliserat prefusion F-antigen från RSV-subgrupp B1,2 60 mikrogram
(RSV-antigen)
1Glykoprotein F stabiliserat i prefusionskonformation.
2Framställt i ovarialceller från kinesisk hamster med rekombinant DNA-teknik.
Övriga innehållsämnen är:
pulver
- trometamol
- trometamolhydroklorid
- sackaros
- mannitol (E 421)
- polysorbat 80 (E 433)
- natriumklorid
- saltsyra
vätska
- vatten för injektionsvätskor
Läkemedlets utseende och förpackningsstorlekar
Abrysvo tillhandahålls som
- ett vitt pulver i en injektionsflaska av glas
- vätska i en förfylld spruta eller en injektionsflaska att lösa upp pulvret i.
När pulvret har lösts upp i vätskan är lösningen klar och färglös.
Abrysvo är tillgängligt i
- en kartong med 1 injektionsflaska med pulver, 1 förfylld spruta med vätska och 1 flaskadapter, med 1 nål eller utan nålar (förpackning med 1 dos).
- en kartong med 5 injektionsflaskor med pulver, 5 förfyllda sprutor med vätska och 5 flaskadaptrar, med 5 nålar eller utan nålar (förpackning med 5 doser).
- en kartong med 10 injektionsflaskor med pulver, 10 förfyllda sprutor med vätska och 10 flaskadaptrar, med 10 nålar eller utan nålar (förpackning med 10 doser).
- en kartong med 5 injektionsflaskor med pulver och 5 injektionsflaskor med vätska (förpackning med 5 doser).
- en kartong med 10 injektionsflaskor med pulver och 10 injektionsflaskor med vätska (förpackning med 10 doser).
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning
Pfizer Europe MA EEIG
Boulevard de la Plaine 17
1050 Bruxelles
Belgien
Tillverkare
Pfizer Manufacturing Belgium NV
Rijksweg 12
2870 Puurs-Sint-Amands
Belgien
Kontakta ombudet för innehavaren av godkännandet för försäljning om du vill veta mer om detta läkemedel:
Suomi/Finland
Pfizer Oy
Puh/Tel: +358 (0)9 430 040
Denna bipacksedel ändrades senast 04/2026.
Övriga informationskällor
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats https://www.ema.europa.eu.
Direktiv för experterna inom hälsovården
Spårbarhet
För att underlätta spårbarhet av biologiska läkemedel ska läkemedlets namn och tillverkningssatsnummer dokumenteras.
Administrering
Abrysvo är endast avsett för intramuskulär användning.
Den oöppnade injektionsflaskan är stabil i 5 dagar om den förvaras i en temperatur mellan 8 °C och 30 °C. Efter denna tidsperiod ska Abrysvo användas eller kasseras. Denna information är endast avsedd som vägledning för hälso- och sjukvårdspersonal vid tillfälliga temperaturskillnader.
Förvaring efter beredning
Abrysvo ska användas omedelbart efter beredning eller inom 4 timmar. Förvara det färdigberedda vaccinet mellan 15 ºC och 30 ºC. Färdigberett vaccin får ej frysas.
Kemisk och fysikalisk stabilitet vid användning har visats för 4 timmar mellan 15 °C och 30 °C. Ur mikrobiologisk synvinkel ska produkten användas omedelbart. Om den inte används omedelbart ansvarar användaren för förvaringsförhållanden och förvaringstid före användning.
Förberedelse inför administrering
Abrysvo pulver och vätska till injektionsvätska, lösning
Förfylld spruta
Pulvret får endast beredas med den medföljande vätskan i den förfyllda sprutan och med hjälp av flaskadaptern.
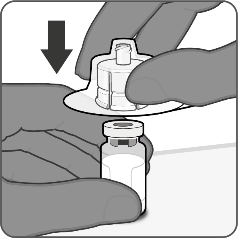 |
Steg 1. Sätt fast flaskadaptern
|
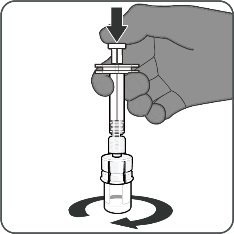 |
Steg 2. Bered pulverkomponenten (antigen) för att bilda Abrysvo
|
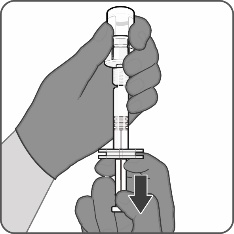 |
Steg 3. Dra upp det beredda vaccinet
|
Det beredda vaccinet är en klar, färglös lösning. Kontrollera vaccinet visuellt med avseende på stora partiklar och missfärgningar före administrering. Använd inte vaccinet om det innehåller stora partiklar eller är missfärgat.
Abrysvo pulver och vätska till injektionsvätska, lösning
Endosinjektionsflaskor
Pulvret får endast beredas med den medföljande injektionsflaskan med vätska.
- Använd en steril nål och steril spruta. Dra upp allt innehåll från injektionsflaskan som innehåller vätska och injicera allt innehåll som finns i sprutan in i injektionsflaskan som innehåller pulver.
- Snurra injektionsflaskan försiktigt i en cirkelrörelse tills pulvret är helt upplöst. Skaka inte.
- Dra upp 0,5 ml från injektionsflaskan som innehåller det beredda vaccinet.
Det beredda vaccinet är en klar, färglös lösning. Kontrollera vaccinet visuellt med avseende på stora partiklar och missfärgningar före administrering. Använd inte vaccinet om det innehåller stora partiklar eller är missfärgat.
Kassering
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.