NIAPELF injektionsvätska, depotsuspension 50 mg, 75 mg, 100 mg, 150 mg
Tilläggsinformation
Niapelf 25 mg injektionsvätska, depotsuspension
Niapelf 50 mg injektionsvätska, depotsuspension
Niapelf 75 mg injektionsvätska, depotsuspension
Niapelf 100 mg injektionsvätska, depotsuspension
Niapelf 150 mg injektionsvätska, depotsuspension
Paliperidon
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad Nipelf är och vad det används för
- Vad du behöver veta innan du använder Niapelf
- Hur du använder Niapelf
- Eventuella biverkningar
- Hur Niapelf ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Niapelf innehåller den aktiva substansen paliperidon som är ett antipsykosläkemedel och används som underhållsbehandling mot symtomen vid schizofreni hos vuxna patienter som har en stabiliserad behandling med paliperidon eller risperidon.
Om du tidigare har svarat på behandling med paliperidon eller risperidon och har lindriga eller måttliga symtom kan din läkare påbörja behandlingen med Niapelf utan föregående stabilisering med paliperidon eller risperidon.
Schizofreni är en sjukdom med "positiva" och "negativa" symtom. Positiva symtom betyder förekomst av symtom som normalt inte förekommer. En person med schizofreni kan till exempel höra röster eller se saker som inte finns (kallas hallucinationer), tro saker som inte är sanna (kallas vanföreställningar) eller känna sig ovanligt misstänksam mot andra. Negativa symtom betyder brist på beteenden eller känslor som normalt förekommer. En person med schizofreni kan till exempel förefalla tillbakadragen, känslomässigt utarmad och kan ha svårt att prata på ett tydligt och logiskt sätt. Människor med denna sjukdom kan också känna sig nedstämda, oroliga, skuldtyngda eller spända.
Paliperidon kan hjälpa till att lindra symtomen av din sjukdom och hindra dina symtom att komma tillbaka.
Vad du behöver veta innan produkten används
Använd inte Niapelf
- om du är allergisk mot paliperidon eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du använder Niapelf.
Detta läkemedel har inte studerats hos äldre patienter med demens. Äldre patienter med demens, som behandlas med andra liknande typer av läkemedel, kan emellertid ha ökad risk att få stroke eller att dö, (se avsnitt Eventuella biverkningar, Eventuella biverkningar)
Alla läkemedel kan orsaka biverkningar och vissa av de biverkningar som orsakas av detta läkemedel kan förvärra symtomen av andra medicinska tillstånd. Det är därför viktigt att du rådgör med din läkare om något av följande tillstånd, som skulle kunna förvärras under behandlingen med detta läkemedel:
- om du har Parkinsons sjukdom
- om du någon gång har fått diagnosen malignt neuroleptikasyndrom, ett tillstånd där symtomen bland annat är feber och muskelstelhet
- om du någon gång har haft onormala tung- eller ansiktsrörelser (tardiv dyskinesi)
- om du vet att du har haft låga nivåer av vita blodkroppar tidigare (detta kan men behöver inte ha orsakats av andra läkemedel)
- om du är diabetiker eller har anlag för att få diabetes
- om du har haft bröstcancer eller en tumör i hjärnans hypofys
- om du har en hjärtsjukdom eller får behandling mot en hjärtsjukdom som gör att blodtrycket kan bli lågt
- om du har lågt blodtryck när du reser dig upp eller sätter dig upp snabbt
- om du har epilepsi
- om du har njurproblem
- om du har leverproblem
- om du har utdragna och/eller smärtsamma erektioner
- om du har störningar i regleringen av kroppstemperaturen eller har förhöjd kroppstemperatur
- om du har en onormalt hög nivå av hormonet prolaktin i blodet eller om du har en tumör som kan vara prolaktinberoende
- om du eller någon annan i din familj har haft blodproppar, eftersom antipsykotiska läkemedel har förknippats med bildningen av blodproppar.
Om du har något av dessa tillstånd, tala med din läkare eftersom han/hon kan vilja anpassa din dos eller följa upp dig med kontroller under en tid.
I sällsynta fall har en farligt låg nivå av en viss typ av vita blodkroppar som behövs för att bekämpa infektion i blodet setts hos patienter som tar detta läkemedel. Din doktor kan komma att kontrollera dina nivåer av vita blodkroppar.
Även om du tidigare har tålt paliperidon eller risperidon taget via munnen kan allergiska reaktioner i sällsynta fall uppkomma efter att du fått injektioner av Niapelf. Sök omgående medicinsk vård om du får hudutslag, svullnad i halsen, klåda eller andningsproblem eftersom dessa kan vara tecken på en allvarlig allergisk reaktion.
Detta läkemedel kan orsaka viktökning. Påtaglig viktökning kan ha en negativ inverkan på din hälsa. Din läkare ska kontrollera din kroppsvikt regelbundet.
Din läkare ska titta efter tecken på högt blodsocker eftersom diabetes mellitus eller försämring av befintlig diabetes har setts hos patienter som använder detta läkemedel. Hos patienter med befintlig diabetes ska blodsockret kontrolleras regelbundet.
Eftersom detta läkemedel kan minska driften att kräkas finns det en risk för att det döljer kroppens normala reaktion om man fått i sig något giftigt ämne eller andra medicinska tillstånd.
Vid gråstarroperation (katarakt) kan det förekomma att pupillen (den svarta cirkeln i ögats mitt) inte ökar i storlek så mycket som behövs. Dessutom kan man få nedsatt muskelspänning i iris (ögats färgade del) under operationen och det kan leda till ögonskador. Om du har en ögonoperation inplanerad måste du informera din ögonläkare om att du använder detta läkemedel.
Barn och ungdomar
Detta läkemedel är inte avsett för patienter under 18 år.
Andra läkemedel och Niapelf
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
Om du tar detta läkemedel tillsammans med karbamazepin (används mot epilepsi och som humörstabiliserande läkemedel) kan dosen av detta läkemedel behöva ändras.
Eftersom detta läkemedel i första hand har effekt i hjärnan kan störningar från andra läkemedel som också verkar i hjärnan orsaka en förvärring av biverkningar som sömnighet eller andra effekter på hjärnan, t.ex. andra läkemedel för att behandla psykiska tillstånd, opioider, antihistaminer och sömnmedel.
Eftersom detta läkemedel kan sänka blodtrycket ska försiktighet iakttas när läkemedlet används tillsammans med andra läkemedel som sänker blodtrycket.
Detta läkemedel kan minska effekten av läkemedel mot Parkinsons sjukdom och myrkrypningar i benen (t.ex. levodopa).
Detta läkemedel kan orsaka onormala EKG på så vis att det tar längre tid än vanligt för en elektrisk impuls att förflytta sig till en viss del av hjärtat (tillståndet kallas "QT-förlängning"). Andra läkemedel som orsakar en sådan effekt är bland annat vissa läkemedel som används för att behandla hjärtarytmier eller för att behandla infektioner, samt andra antipsykotiska läkemedel.
Om du har anlag för att utveckla kramper kan detta läkemedel öka risken för att du gör det. Andra läkemedel som orsakar en sådan effekt är bland annat vissa läkemedel som används för att behandla depression eller för att behandla infektioner, samt andra antipsykotiska läkemedel.
Niapelf bör användas med försiktighet med läkemedel som ökar aktiviteten i det centrala nervsystemet (psykostimulantia, t.ex. metylfenidat).
Niapelf med alkohol
Alkohol bör undvikas.
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du använder detta läkemedel. Du ska inte använda detta läkemedel under graviditet, såvida du inte har diskuterat detta med din läkare. Hos nyfödda barn vars mammor har tagit paliperidon under den sista trimestern (de sista tre månaderna av graviditeten), kan följande symtom förekomma: skakningar, stela och/eller svaga muskler, sömnighet, upprördhet, andningsproblem och svårigheter att äta. Om ditt barn får några av dessa symtom kan du behöva kontakta din läkare.
Detta läkemedel kan föras över från modern till barnet via bröstmjölk, vilket kan vara skadligt för barnet. Du ska därför inte amma när du använder detta läkemedel.
Körförmåga och användning av maskiner
Yrsel, extrem trötthet och synproblem kan uppträda under behandling med detta läkemedel (se avsnitt Eventuella biverkningar). Detta ska beaktas i situationer då full vakenhet krävs, t.ex. då man kör bil eller hanterar maskiner.
Niapelf innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per dos, d.v.s. är näst intill ”natriumfritt”.
Hur produkten används
Detta läkemedel ges till dig av din läkare eller av annan sjukvårdspersonal. Läkaren kommer att meddela dig när du behöver nästa injektion. Det är viktigt att du inte missar en inplanerad dos. Om du inte kan komma till ett inplanerat besök hos läkaren ska du omedelbart kontakta honom eller henne för att få en ny tid så snart som möjligt.
Du kommer att få den första injektionen (150 mg) och andra injektionen (100 mg) av detta läkemedel i överarmen med ungefär 1 veckas mellanrum. Därefter kommer du att få en injektion (från 25 mg till 150 mg) i antingen överarmen eller skinkan en gång per månad.
Om din läkare ändrar din behandling från risperidon långverkade injektion till detta läkemedel kommer du att få din första injektion med detta läkemedel (från 25 mg till 150 mg) i antingen överarmen eller skinkan på det datum då din nästa injektion var planerad. Därefter kommer du att få en injektion (från 25 mg till 150 mg) i antingen överarmen eller skinkan en gång per månad.
Beroende på dina symtom kan läkaren öka eller minska mängden läkemedel du får med en dosnivå när det är dags för den inplanerade månatliga injektionen.
Patienter med njurproblem
Din läkare kan behöva justera din dosering beroende på din njurfunktion. Om du har lätta njurproblem kan din läkare ordinera en lägre dos. Om du har medelsvåra eller svåra njurproblem ska detta läkemedel inte användas.
Äldre
Din läkare kan behöva reducera din dosering av detta läkemedel om du har försämrad njurfunktion.
Om du har fått för stor mängd av Niapelf
Du kommer att få detta läkemedel av utbildad sjukvårdspersonal och det är därför inte troligt att du får för mycket.
Patienter som har fått för mycket paliperidon kan få följande symtom: dåsighet eller sömnighet, snabb hjärtrytm, lågt blodtryck, onormalt EKG (elektrisk övervakning av hjärtat), eller långsamma eller onormala rörelser i ansiktet, kroppen, armarna eller benen.
Om du slutar att använda Niapelf
Om du slutar med dina injektioner kommer läkemedlets effekt att avta. Du ska inte sluta använda detta läkemedel såvida inte din läkare sagt att du ska göra det, eftersom dina symtom då kan komma tillbaka.
Om du har ytterligare frågor om detta läkemedel kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan det här läkemedlet orsaka biverkningar men alla användare behöver inte få dem.
Tala omedelbart om för din läkare om du:
- får blodproppar, särskilt i benen (symtomen är svullnad, smärta och rodnad på benen), vilka kan förflytta sig via blodkärlen till lungorna och orsaka bröstsmärta och andningssvårigheter. Om du upplever något av dessa symtom ska du omedelbart söka vård.
- har demens och upplever en plötslig mental förändring eller plötslig svaghet eller domningar i ansiktet, armar eller ben, speciellt på en sida, eller sluddrigt tal, även under en kort period. Detta kan vara tecken på stroke.
- upplever feber, muskelstelhet, svettningar eller sänkt medvetandegrad (ett tillstånd som kallas ”malignt neuroleptikasyndrom”). Omedelbar medicinsk behandling kan behövas.
- är man och upplever ihållande eller smärtfull erektion. Detta kallas priapism. Omedelbar medicinsk behandling kan behövas.
- upplever ofrivilliga rytmiska rörelser i tungan, munnen och ansiktet. Behandling med paliperidon kan behöva avslutas.
- drabbas av en svår allergisk reaktion med feber, svullnad av mun, ansikte, läppar eller tunga, andnöd, klåda, hudutslag och ibland blodtrycksfall (en s.k. anafylaktisk reaktion). Även om du tidigare har tolererat risperidon eller paliperidon som intagits via munnen, kan allergiska reaktioner i sällsynta fall förekomma efter att ha erhållit injektioner av paliperidon.
- har en ögonoperation inplanerad. Du måste informera din ögonläkare om att du använder detta läkemedel. Vid operation för gråstarr (katarakt) kan det förekomma att man får nedsatt muskelspänning i iris (ögats färgade del) under operationen (s.k. ”floppy iris syndrome”) vilket kan leda till ögonskador.
- vet med dig att du har farligt låga nivåer av en viss typ av vita blodkroppar som behövs för att skydda dig mot infektion i blodet.
Följande biverkningar kan förekomma:
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare):
- svårigheter att somna eller sova utan avbrott.
Vanliga (kan förekomma hos upp till 1 av 10 användare):
- förkylningssymtom, urinvägsinfektion, influensaliknande symtom
- Niapelf kan öka dina nivåer av ett hormon som kallas ”prolaktin” i ett blodprov (detta kan men behöver inte ge symtom). Symtom av höga prolaktinnivåer hos män kan vara svullna bröst, svårigheter att få eller bibehålla erektion eller annan sexuell dysfunktion. Hos kvinnor kan symtomen vara obehag från brösten, mjölkläckage, missade menstruationsperioder eller andra problem med menstruationscykeln
- högt blodsocker, viktökning, viktnedgång, minskad aptit
- irritabilitet, depression, ångest
- parkinsonism: det här tillståndet kan innefatta minskade eller försvagade kroppsrörelser, känsla av spända eller stela muskler (som gör dina rörelser ryckiga) och ibland till och med en känsla av att rörelsen stannar upp och sedan börjar om. Andra tecken på parkinsonism innefattar en långsam släpande gång, skakningar vid vila, ökad salivproduktion och/eller dreglande, och en avsaknad av ansiktsuttryck.
- rastlöshet, att känna sig sömnig eller mindre alert
- dystoni: ett tillstånd innefattande långsamma eller ihållande ofrivilliga muskelsammandragningar. Dystoni kan påverka vilken del av kroppen som helst (och leda till en onormal hållning) men påverkar ofta musklerna i ansiktet, inklusive onormala rörelser i ögon, mun, tunga eller käke.
- Yrsel
- dyskinesi: det här är ett tillstånd innefattande ofrivilliga muskelrörelser och kan inkludera repetitiva, spastiska eller förvridna rörelser eller ryckningar
- tremor (skakningar)
- huvudvärk
- snabb hjärtrytm
- högt blodtryck
- hosta, nästäppa
- buksmärta, kräkning, illamående, förstoppning, diarré, dålig matsmältning, tandvärk
- ökade levertransaminaser i blod
- ben- eller muskelvärk, ryggsmärta, ledsmärta
- utebliven menstruation
- feber, svaghet, trötthet
- reaktion vid injektionsstället, inklusive klåda, smärta eller svullnad.
Mindre vanliga (kan förekomma hos upp till 1 av 100 användare):
- lunginflammation, luftrörskatarr (bronkit), luftvägsinfektion, bihåleinflammation, infektion i urinblåsan, öroninflammation, nagelsvamp, halsfluss, hudinfektion
- minskning av antalet vita blodkroppar, minskning av den typ av vita blodkroppar som hjälper till att skydda dig mot infektioner, blodbrist
- allergisk reaktion
- diabetes eller försämring av diabetes, ökad mängd insulin (ett hormon som reglerar blodsockernivåerna) i blodet
- ökad aptit
- • förlust av aptit som leder till undernäring och låg kroppsvikt
- hög nivå av triglycerider i blodet (en typ av blodfett), ökad kolesterolnivå i blodet
- sömnstörning, upprymd sinnesstämning (mani), minskad sexlust, nervositet, mardrömmar
- tardiv dyskinesi (ofrivilliga ryckande rörelser i ansiktet, tungan eller andra delar av kroppen). Berätta genast för din doktor om du upplever ofrivilliga rytmiska rörelser av tunga, mun eller ansikte. Behandlingen med detta läkemedel kan behöva avslutas.
- svimning, ett rastlöst behov att röra på delar av kroppen, yrsel när man ställer sig upp, uppmärksamhetsstörning, talproblem, smakförlust eller onormal smakupplevelse, minskad känsla i huden för beröring och smärta, pirrande eller stickande känsla, eller domningar i huden
- dimsyn, ögoninfektion, torra ögon
- känsla av att det snurrar (yrsel), ringningar i öronen, öronsmärta
- störning i impulsöverledningen mellan övre och nedre delarna av hjärtat, onormal elektrisk ledning i hjärtat, förlängt QT-intervall från hjärtat, snabb hjärtrytm då man ställer sig upp, långsam hjärtrytm, onormal elektrisk signal i hjärtat (elektrokardiogram eller EKG), en fladdrande eller dunkande känsla i bröstkorgen (hjärtklappning)
- lågt blodtryck, lågt blodtryck då man ställer sig upp (följaktligen kan en del som tar detta läkemedel känna sig svaga, yra eller svimma när de sätter eller ställer sig upp plötsligt)
- andnöd, halsont, näsblod
- buksmärta, mag- eller tarminfektion, sväljsvårigheter, muntorrhet
- omåttlig gasbildning
- ökad gamma-GT (ett leverenzym kallat gammaglutamyltransferas) i blodet, ökade nivåer av leverenzymer i blodet
- utslag (nässelutslag), klåda, utslag, håravfall, eksem, torr hud, hudrodnad, akne, varansamling under huden
- ökning av CPK (kreatinfosfokinas) i blodet, ett enzym som ibland frisätts vid nedbrytning av muskler
- muskelspasmer, ledstelhet, muskelsvaghet
- urininkontinens, täta trängningar, smärta vid urinering
- erektil dysfunktion (nedsatt förmåga hos penis att få eller behålla en erektion), ejakulationsstörning, uteblivna menstruationsperioder eller andra problem med menstruationscykeln (kvinnor), bröstutveckling hos män, sexuell dysfunktion, bröstsmärta, mjölkläckage från brösten
- svullnad av ansikte, mun, ögon eller läppar, svullnad av kropp, armar eller ben
- • en ökning av kroppstemperatur
- förändring i sättet att gå
- smärta i bröstkorgen, obehag i bröstkorgen, sjukdomskänsla
- hudförhårdnander
- fall.
Sällsynta (kan förekomma hos upp till 1 av 1 000 användare):
- ögoninfektion
- hudinflammation orsakad av kvalster, flagnande kliande hårbotten eller hud
- ökning av eosinofiler (en typ av vita blodkroppar) i blodet
- minskning av antalet blodplättar (blodkroppar som gör så att blodet stelnar (koagulerar))
- huvudskakningar
- otillräcklig insöndring av ett hormon som reglerar urinvolymen
- socker i urinen
- livshotande komplikationer av okontrollerad diabetes
- lågt blodsocker
- överdrivet vattendrickande
- orörlighet och brist på reaktionsförmåga i vaket tillstånd (katatoni)
- förvirring
- gå i sömnen
- brist på känslor
- oförmåga att få orgasm
- malignt neuroleptikasyndrom (förvirring, minskat eller förlust av medvetande, hög feber och svår muskelstelhet), problem med blodkärl i hjärnan, inklusive plötslig minskning av blodtillförseln till hjärnan (stroke eller ministroke), avsaknad av respons på stimuli, medvetandeförlust, låg medvetandegrad, krampanfall, balansstörning
- onormal koordination
- glaukom (ökat tryck inuti ögongloben)
- problem med att röra på ögonen, ögonrullning, överkänslighet mot ljus, ökat tårflöde, röda ögon
- förmaksflimmer (en onormal hjärtrytm), oregelbunden hjärtrytm
- blodproppar i lungorna som kan orsaka bröstsmärtor och andningsvårigheter. Om du får något av dessa symtom ska du omedelbart söka läkarvård.
- blodproppar i venerna, särskilt i benen (symtom innefattar svullnad, smärta och rodnad i benen). Om du får något av dessa symtom ska du omedelbart söka läkarvård.
- flushing (värmekänsla och rodnad i huden)
- svårt att andas under sömn (sömnapné)
- ökad blodmängd (blodstockning) i lungorna, blodstockning i luftvägarna
- knastrande andningsljud, pipande och väsande andning
- bukspottskörtelinflammation, svullen tunga, avföringsinkontinens, mycket hård avföring
- stopp i tarmen
- nariga läppar
- läkemedelsutslag på huden, förtjockning av huden, mjäll
- nedbrytning av muskelfiber och smärta i muskler (rabdomyolys)
- ledsvullnad
- oförmåga att kissa
- obehag från brösten, förstorning av bröstkörtlarna, bröstförstoring
- vaginal flytning
- priapism (förlängd erektion av penis som kan kräva kirurgisk behandling)
- väldigt låg kroppstemperatur, frossa, törstkänsla
- utsättningsbesvär
- ackumulering av var orsakad av infektion vid infektionsstället, djup hudinfektion, en cysta vid injektionsstället, blåmärken vid injektionsstället.
Ingen känd frekvens (kan inte beräknas från tillgängliga data):
- farligt låga nivåer av en viss typ av vita blodkroppar som behövs för att skydda dig mot infektion i blodet
- svåra allergiska reaktioner som kännetecknas av feber, svullen mun, ansikte, läpp eller tunga, andnöd, klåda, utslag och ibland blodtrycksfall
- farligt överdrivet intag av vatten
- sömnrelaterad ätstörning
- koma till följd av okontrollerad diabetes
- minskat syreflöde i delar av kroppen (på grund av minskat blodflöde)
- snabb ytlig andning, lunginflammation till följd av inandning av föda, röststörning
- avsaknad av tarmmuskelrörelser (orsakar stopp)
- gulfärgning av huden och ögonen (gulsot)
- allvarliga eller livshotande utslag med blåsor och flagnande hud som kan börja i och kring mun, näsa, ögon eller könsorgan och sprida sig till andra delar av kroppen (Stevens-Johnsons syndrom eller toxisk epidermal nekrolys)
- allvarlig allergisk reaktion med svullnad som kan innefatta halsen och leda till andningssvårigheter
- missfärning av huden
- onormal hållning
- nyfödda barn, vars mammor har tagit Niapelf under graviditeten, kan få biverkningar av läkemedlet och/eller utsättningssymtom såsom irritabilitet, stela och/eller ihållande muskelkontraktioner, skakningar, sömnighet, andningsproblem och svårigheter att äta
- en minskning av kroppstemperatur
- döda hudceller vid injektionsstället och sår vid injektionsstället.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet listat i bilaga V.* Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på kartongen efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Inga särskilda förvaringsanvisningar.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
Den aktiva substansen är paliperidon.
Den aktiva substansen är paliperidon.
Varje Niapelf 25 mg förfylld spruta innehåller 39 mg paliperidonpalmitat.
Varje Niapelf 50 mg förfylld spruta innehåller 78 mg paliperidonpalmitate.
Varje Niapelf 75 mg förfylld spruta innehåller 117 mg paliperidonpalmitat.
Varje Niapelf 100 mg förfylld spruta innehåller 156 mg paliperidonepalmitat.
Varje Niapelf 150 mg förfylld spruta innehåller 234 mg paliperidonepalmitat.
Övriga innehållsämnen är:
Polysorbat 20
Makrogol
Citronsyramonohydrat (E-330)
Dinatriumfosfat
Natriumdivätefosfatmonohydrat
Natriuhydroxid (E-524) (för pH-justering)
Vatten för injektionsvätskor
Läkemedlets utseende och förpackningsstorlekar
Niapelf är en vit till benvit depotsuspension injektionsvätska i en förfylld spruta. Varje förpackning innehåller 1 förfylld spruta och 2 nålar.
Förpackning för behandlingsinsättning:
Varje förpackning innehåller en förpackning av Niapelf 150 mg och en förpackning Niapelf 100 mg.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning
Neuraxpharm Pharmaceuticals, S.L.
Avda. Barcelona 69
08970 Sant Joan Despí
Barcelona
Spanien
Tillverkare
Neuraxpharm Pharmaceuticals, S.L.
Avda. Barcelona 69
08970 Sant Joan Despí
Barcelona
Spanien
Neuraxpharm Arzneimittel GmbH
Elisabeth-Selbert-Strasse 23
Richrath, Langenfeld (Rheinland)
40764
Tyskland
Kontakta ombudet för innehavaren av godkännandet för försäljning om du vill veta mer om detta läkemedel:
België/Belgique/Belgien Neuraxpharm Belgium Tél/Tel: +32 (0)2 732 56 95 | Lietuva Neuraxpharm Pharmaceuticals, S.L. Tel:+34 93 475 96 00 |
България Neuraxpharm Pharmaceuticals, S.L. Teл.: +34 93 475 96 00 | Luxembourg/Luxemburg Neuraxpharm France Tél/Tel: +32 474 62 24 24 |
Česká republika Neuraxpharm Bohemia s.r.o. Tel:+420 739 232 258 | Magyarország Neuraxpharm Hungary Kft. Tel.: +36 (30) 542 2071 |
Danmark Neuraxpharm Sweden AB Tlf: +46 (0)8 30 91 41 (Sverige) | Malta Neuraxpharm Pharmaceuticals, S.L. Tel:+34 93 475 96 00 |
Deutschland neuraxpharm Arzneimittel GmbH Tel: +49 2173 1060 0 | Nederland Neuraxpharm Netherlands B.V Tel: +31 70 208 5211 |
Eesti Neuraxpharm Pharmaceuticals, S.L. Tel:+34 93 475 96 00 | Norge Neuraxpharm Sweden AB Tlf: +46 (0)8 30 91 41 (Sverige) |
Ελλάδα Brain Therapeutics ΙΚΕ Τηλ: +302109931458 | Österreich Neuraxpharm Austria GmbH Tel.:+43 2236 320038 |
España Neuraxpharm Spain, S.L.U. Tel: +34 93 475 96 00 | Polska Neuraxpharm Polska Sp. z.o.o. Tel.: +48 783 423 453 |
France Neuraxpharm France Tél: +33 1.53.62.42.90 | Portugal Neuraxpharm Portugal, Unipessoal Lda Tel: +351 910 259 536 |
Hrvatska Neuraxpharm Pharmaceuticals, S.L. T +34 93 602 24 21 | România Neuraxpharm Pharmaceuticals, S.L. Tel: +34 93 475 96 00 |
Ireland Neuraxpharm Ireland Ltd. Tel: +353 1 428 7777 | Slovenija Neuraxpharm Pharmaceuticals, S.L. T +34 93 475 96 00 |
Ísland Neuraxpharm Sweden AB Sími: +46 (0)8 30 91 41 (Svíþjóð) | Slovenská republika Neuraxpharm Slovakia a.s. Tel: +421 255 425 562 |
Italia Neuraxpharm Italy S.p.A. Tel: +39 0736 980619 | Suomi/Finland Neuraxpharm Sweden AB Puh/Tel: +46 (0)8 30 91 41 (Ruotsi/Sverige) |
Κύπρος Brain Therapeutics ΙΚΕ Τηλ: +302109931458 | Sverige Neuraxpharm Sweden AB Tel: +46 (0)8 30 91 41 |
Latvija Neuraxpharm Pharmaceuticals, S.L. Tel: +34 93 475 96 00 | United Kingdom (Northern Ireland) Neuraxpharm Ireland Ltd. Tel: +353 1 428 7777 |
Denna bipacksedel ändrades senast 31.03.2024
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats http://www.ema.europa.eu.
Direktiv för experterna inom hälsovården
Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal och ska läsas av hälso- och sjukvårdsutövaren tillsammans med den fullständiga förskrivarinformation (produktresumé).
Suspensionen för injektion är endast avsedd för engångsbruk. Den ska kontrolleras visuellt för främmande partiklar innan den administreras. Använd inte sprutan om den inte är visuellt fri från främmande partiklar.
Förpackningen innehåller en förfylld spruta och 2 säkerhetskanyler (en 1½ tum, 22 gauge nål [38,1 mm x 0,72 mm] och en 1 tum 23 gauge nål [25,4 mm x 0,64 mm] för intramuskulär injektion. Niapelf finns även i en förpackning för behandlingsinsättning som innehåller 2 förfyllda sprutor (150 g + 100 mg) och 2 extra säkerhetskanyler.
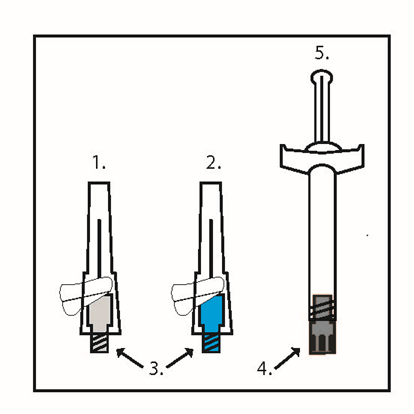
(1) 22 G x 1½ tum (Grå koppling)
(2) 23 G x 1 tum (Blå koppling)
(3) Koppling
(4) Ändpropp
(5) Förfylld spruta
- Skaka sprutan kraftigt under minst 10 sekunder för att suspensionen ska bli homogen.
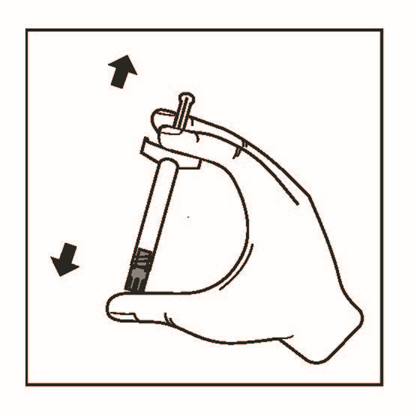
2. Välj lämplig kanyl.
Den första initieringsdosen av Niapelf (150 mg) ) ska adminstreras på Dag 1 i DELTA-muskeln med nålen för DELTA-injektion. Den andra initieringsdosen av Niapelf (100 mg) ska också injiceras i DELTA-muskeln med nålen för DELTA-injektion en vecka senare (dag 8).
Om patienten ska byta från risperidon långverkade injektion till Niapelf kan den första injektionen med Niapelf (från 25 mg till 150 mg) administreras i antingen DELTA- eller GLUTEUS-muskeln med den nål som är avsedd för injektionsstället vid tidpunkten för nästa planerade injektion.
Därefter kan de månatliga underhållsinjektionerna administreras i antingen DELTA- eller GLUTEUS-muskeln med den nål som är avsedd för injektionsstället.
För injektioner i DELTA-muskeln: om patienten väger < 90 kg, använd 1 tum, 23 gauge-nålen (25,4 mm x 0,64 mm) (nålen med blå koppling); om patienten väger ≥ 90 kg, använd 1½- tum, 22 gauge-nålen (38,1 mm x 0,72 mm) (nålen med grå koppling).
För injektioner i GLUTEUS-muskeln: använd 1½ tum, 22 gauge nålen (38,1 mm x 0,72 mm) (nålen med grå koppling).
3. Håll sprutan med ändproppen vänd uppåt och avlägsna gummiproppen med en försiktig vridrörelse.
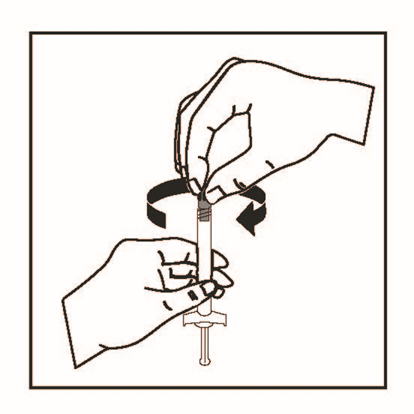
4. Öppna blisterpåsen med säkerhetskanylen till hälften. Fatta tag om nålskyddet med hjälp av blisterpåsen. Fäst säkerhetsnålen på toppanslutningen på sprutan med en försiktig medsols vridrörelse.
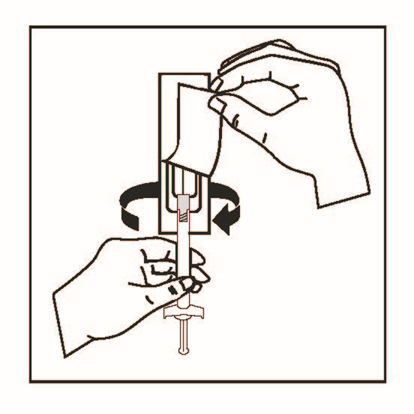
5. Drag av nålskyddet rakt ut, bort från nålen. Vrid inte skyddet eftersom nålen då kan lossna från sprutan.
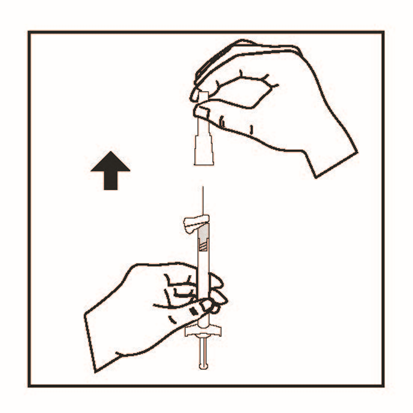
6. Vänd sprutan med den anslutna kanylen uppåt för att avlägsna luft. Avlägsna luft i sprutan genom att försiktigt trycka fram pistongen.
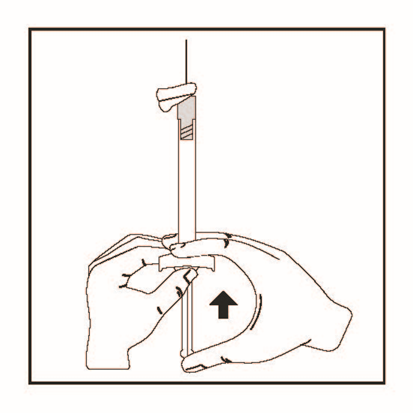
7. Injicera patienten med sprutans hela innehåll sakta, djupt intramuskulärt i den utvalda delta eller gluteusmuskeln. Administrera inte intravaskulärt eller subkutant.
8. När injektionen är slutförd aktiveras nålskyddssystemet med hjälp av antingen tummen eller fingret (8a, 8b) eller mot en plan yta (8c). När man hör ett "klick" är systemet helt aktiverat. Kassera sprutan med nålen enligt gällande anvisningar.
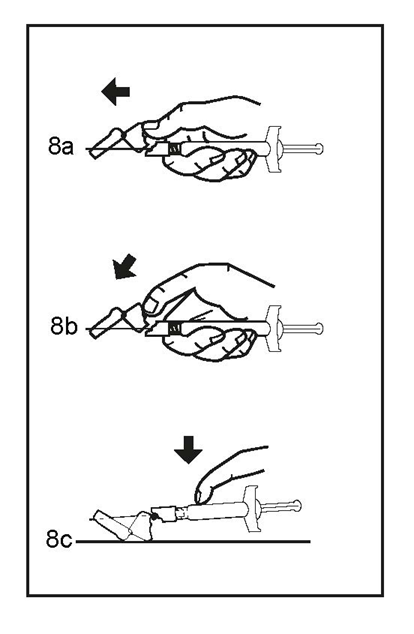
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.