ATROPIN injektionsvätska, lösning 1 mg/ml
Tilläggsinformation
Atropin 1 mg/ml-injektionsvätska, lösning
atropinsulfat
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad Atropin är och vad det används för
2. Vad du behöver veta innan du använder Atropin
3. Hur du använder Atropin
4. Eventuella biverkningar
5. Hur Atropin ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Atropin används för premedicinering vid anestesi, upphävning av muskelrelaxation (icke-depolariserande muskelrelaxanter), organofosfatförgiftningar, förgiftningar orsakade av antikolinesteraser och bradykardi.
Atropinsulfat som finns i Atropin kan också vara godkänt för att behandla andra sjukdomar som inte nämns i denna produktinformation. Fråga läkare, apotek eller annan hälsovårdspersonal om du har ytterligare frågor och följ alltid deras instruktion.
Vad du behöver veta innan produkten används
Använd inte Atropin
- om du är allergisk mot atropinsulfat eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar)
- om du har glaukom, förträngning i urinvägarna (såsom prostataförstoring), obstruktion i mag-tarmkanalen, tarmförlamning, svår sårig tjocktarmsinflammation, hjärt- och blodcirculationsproblem i anslutning till plötslig blödning eller hypertyreos eller myasthenia gravis.
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du använder Atropin.
Eftersom Atropin försnabbar hjärtpulsen ska det ges med försiktighet till patienter med kongestivt hjärtfel, kranskärlssjukdom, rytmrubbningar, blodtryckssjukdom eller hypertyreos samt under hjärtoperation. I samband med akut hjärtinfarkt ska atropin användas med försiktighet eftersom ämnet kan öka syrebristen i vävnaderna och därmed utvidga infarktområdet. Efter hjärttransplantation ska atropin användas med försiktighet vid diagnostiska åtgärder; EKG bör då följas och det bör finnas beredskap för omedelbar defibrillering, eftersom atropin kan orsaka paradoxalt atrioventrikulärt block (mellan förmak och-kammare) eller kollaps i sinusknutans funktion.
Atropin ska ges med försiktighet till patienter med obstruktiv lungsjukdom eftersom en minskning i luftrörssekretionen kan leda till uppkomsten av slemproppar i luftrören.
Atropin gör att magsäcken töms långsammare, minskar magsäckens rörelse och relaxerar matstrupens nedre magmun; och atropin bör därför användas med försiktighet vid behandling av patienter vars sjukdomstillstånd kan förvärras genom sådan inverkan (till exempel inflammation i matstrupen orsakad av reflux av maginnehåll).
Eftersom atropin förhindrar svettning, ska det ges med försiktighet till patienter som vistas i miljöer med hög temperatur samt till patienter som har feber (då minskad svettning ökar risken för förhöjd kroppstemperatur).
Vid behandling av äldre patienter ska särskild försiktighet iakttas vid doseringen av atropin på grund av kardiovaskulära biverkningar och biverkningar som rör det centrala nervsystemet.
Försiktighet ska iakttas också vid behandling av barn, unga och nyfödda samt patienter med Downs syndrom, diarré, prostatahyperplasi som orsakar urinretention och patienter med risk för urinretention.
Andra läkemedel och Atropin
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
Ett samtidigt bruk av atropin och andra antikolinerga läkemedel; såsom läkemedel mot rytmrubbningar, illamående och parkinsons sjukdom, spasmolytika, hämmare av saltsyrasekretionen, mydriater och läkemedel som orsakar cykloplegi, muskelrelaxanter, perifera kärlvidgande medel, neuroleptika, tricykliska antidepressiva och andra depressionsmediciner av liknande typ; kan ha additiv effekt och leda till kraftigare antikolinerga effekter samt antikolinerg förgiftning.
Atropin och parasympatomimetika kan uppväga varandras effekter.
Ett samtidigt bruk av fenylefrin, som får blodkärlen att dra sig samman, och atropin, som blockerar funktionen hos det kolinerga systemet, kan leda till en okontrollerad blodtrycksförhöjning.
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du använder detta läkemedel.
Det finns endast lite information om användning av Atropin vid behandling av gravida kvinnor. Atropin passerar snabbt genom moderkakan. Inga direkta eller indirekta reproduktionstoxikologiska effekter har observerats i djurförsök. För säkerhets skull rekommenderas ett undvikande av Atropin injektionsvätska under graviditet.
Ingen neonataltoxicitet har förknippats med exponering för atropin via bröstmjölk. Eftersom atropin dock utsöndras i bröstmjölk hos människa, ska både den ammande moderns och barnets tillstånd följas upp.
Körförmåga och användning av maskiner
Användning av atropin kan förorsaka dimsyn på grund av pupillutvidgning, ljuskänslighet och förlorad ackommodationsförmåga, samt p.g.a. svindel och andra effekter som kan försämra prestationsförmågan i trafiken och förmågan att använda maskiner.
Du är själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbeten som kräver skärpt uppmärksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användning av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med din läkare eller apotekspersonal om du är osäker.
Atropin innehåller natrium
Detta läkemedel innehåller 3,54 mg natrium (huvudingrediensen i koksalt/bordssalt) per 1 ml ampull. Detta motsvarar 0,18 % av högsta rekommenderat dagligt intag av natrium för vuxna.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Atropin injektionsvätska är avsedd att administreras endast av läkare intravenöst eller som intramuskulär injektion. Dosen bestäms alltid av den behandlande läkaren.
Om du använt för stor mängd av Atropin
Om du fått i dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedlet av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel. 0800 147 111) för bedömning av risken samt rådgivning.
Symptomen vid en överdos av atropin härrör sig ofta från det centrala nervsystemet; såsom rastlöshet, irritation, hallucinationer, förvirringstillstånd och kramper. Andra symptom på överdosering är varm eller rödskiftande hud, torr mun eller armhålor, pupillutvidgning, urinstopp och långsammare tarmfunktion. En överdos av atropin kan också orsaka retledningsrubbningar i hjärtat, rytmrubbningar, förhöjt blodtryck och perifer vasodilatation, och slutligen leda till att blodcirkulationen slås ut. Behandlingen är symtomatisk.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare):
- synrubbningar, såsom pupillutvidgning, förlamad ciliarmuskel (cycloplegi), dubbelseende och ljuskänslighet
- minskad slemutsöndring i luftrören.
- muntorrhet förknippat med svårigheter att svälja och tala, försvagad tonus och rörlighet i matsmältningskanalen, vilket leder till förstoppning eller till att innehållet i magsäcken strömmar tillbaka i matstrupen
- törst
- hudrodnad, värmekänsla och torrhet på grund av försvagad svettkörtelfunktion
- svårigheter att urinera.
Vanliga (kan förekomma hos upp till 1 av 10 användare):
- förvirringstillstånd, hallucinationer, upphetsning, försämrat korttidsminne
- hjärtrytmrubbningar
- feber på grund av försvagad svettkörtelfunktion.
Sällsynta (kan förekomma hos upp till 1 av 1 000 användare):
- psykotiska störningar, anfall, sedering.
Mycket sällsynta (kan förekomma hos upp till 1 av 10 000 användare):
- anafylaktiska reaktioner, kammarflimmer, förmaksflimmer, hypertensiv kris, bröstsmärta.
Ingen känd frekvens (förekomst kan inte beräknas från tillgängliga data):
- delirium
- svindel
- ökningen av intraokulärt tryck och en attack av glaukom hos patienter med blockerat kammarvinkelglaukom
- angina pectoris
- flush, d.v.s. plötslig hudrodnad; förhöjd kroppstemperatur till följd av försämrad aktivitet hos svettkörtlarna
- urinretention.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen on läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvaras vid högst 25 °C. Ljuskänsligt.
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på förpackningen. Utgångsdatumet är den sista dagen i angiven månad.
Använd inte detta läkemedel om det synbart har förändrats.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är atropinsulfat.
- Övriga innehållsämnen är natriumklorid, saltsyra och vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlek
Klar, färglös lösning
25 x 1 ml
Färglös glasampull med två gröna ringar vid halsen
Innehavare av godkännande för försäljning
Takeda Oy, PB 1406, 00101 Helsingfors, tel. 020 746 5000
Tillverkare
Takeda Austria GmbH, St. Peter Strasse 25 och 4020, Linz, Österrike
Denna bipacksedel ändrades senast 1.2.2023
Direktiv för experterna inom hälsovården
Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal:
Ampullerna med Atropin-injektionsvätska är s.k. One-Point-Cut-ampuller (OPC) som ska öppnas genom att spetsen bryts av för hand, utan fil eller andra hjälpmedel. På ampullens spets finns en punkt som man ska trycka på då man öppnar ampullen.
Då ampullen öppnas enligt följande anvisning, kommer inga glasskärvor eller färgämnen från de färgade ringarna att hamna i lösningen. Anvisningen är avsedd för högerhänta personer.
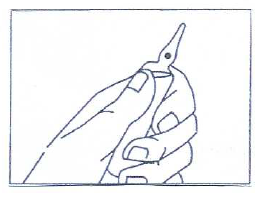
STEG 1:
Håll ampullen i din vänstra hand med dess nedre del mellan tumme och pekfinger så att fingrarna är placerade strax under ampullens hals. Kläm inte åt för hårt. Håll ampullen med spetsen mot dig själv.
STEG 2:
Fatta tag om ampullens övre del med högra handens tumme och pekfinger så att tummen täcker hela den övre delen.
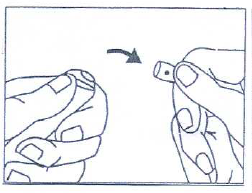
STEG 3:
Tryck den övre delen bortåt från dig själv med höger tumme och håll emot med vänstra handens pekfinger som håller om den nedre delen. Dra eller skruva inte på ampullen (rör inte händerna i motsatta riktningar och för dem inte heller närmare varandra). Använd inte för mycket kraft, utan tryck jämnt för att bryta av ampullens hals.
Doseringsanvisningar:
Premedicinering vid anestesi: 0,01 mg/kg intramuskulärt (ad 0,6 mg) ca 30−60 minuter innan anestesin inleds eller intravenöst strax före induktionen av anestesin.
Upphävning av muskelrelaxation: 0,015−0,02 mg/kg tillsammans med neostigmin (0,03−0,04 g/kg) intravenöst.
Organofosfatförgiftning: Introduktionsdos 75–100 mg (2–5 mg/dos) intravenöst eller intramuskulärt med 10–30 minuters intervall, dygnsdos 150 mg–1(–3) g. Uttorkningen av sekret (sekret från luftrör, spott) och korrigeringen av hypotensionen och bradykardin ska följas upp under behandlingen.
Antikolinesterasförgiftning: Dosering på samma sätt som vid organofosfatförgiftning, men de doser som behövs är vanligen mindre och beror på ämnet som orsakat förgiftningen - och så även behandlingstiden.
Bradykardi: Introduktionsdos 0,5 mg intravenöst, vid behov upprepas dosen med 3–5 minuters intervall upp till den maximala dosen på 3 mg.
Vid behandling av äldre personer kan det vara nödvändigt att använda mindre doser på grund av biverkningar i hjärta, blodkärl eller det centrala nervsystemet.