CUROSURF instillationsvätska för luftvägarna, suspension 80 mg/ml
Tilläggsinformation
Curosurf® 80 mg/ml, instillationsvätska för luftvägarna, suspension
porcina lunglipider och protein
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller sjuksköterska.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad Curosurf är och vad det används för
- Vad du behöver veta innan du använder Curosurf
- Hur du använder Curosurf
- Eventuella biverkningar
- Hur Curosurf ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Curosurf är en steril vätska (suspension) i injektionsflaska som innehåller 120 mg resp. 240 mg lunglipider från grisar.
Curosurf används till behandling av för tidigt födda barn som har eller löper risk att drabbas av RDS (respiratory distress syndrom).
Vad du behöver veta innan produkten används
Använd inte Curosurf
- om du är allergisk mot porcina lunglipider och protein eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
Administering av Curosurf till för tidigt födda barn med nedsatt njur- eller leverfunktion har inte studerats.
Andra läkemedel och Curosurf
Det är inte känt om Curosurf påverkar eller påverkas av annan läkemedelsbehandling.
Curosurf innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per injektionsflaska, dvs. är näst intill “natriumfritt”.
Hur produkten används
Curosurf får endast ges av personal utbildad för och med erfarenhet av att vårda för tidigt födda barn, ge dem återupplivningsbehandling eller stabilisera deras tillstånd. Dosen beräknas utifrån barnets kroppsvikt och beror på om behandlingen är förebyggande eller behandlande.
Om du får mera Curosurf än vad du borde
Det har inte rapporterats om överdosering efter administrering av Curosurf.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare eller sjuksköterska.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Biverkningar som i kliniska undersökningar observerats under behandlingen samt biverkningar som rapporterats efter att preparatet lanserades på marknaden uppräknas i tabellen nedan i enlighet med MeDRA:s organklassificeringssystem. I tabellen används följande frekvenser: mycket vanliga (≥ 1/10), vanliga (≥ 1/100, < 1/10), mindre vanliga (≥ 1/1 000, < 1/100), sällsynta (≥ 1/10 000, < 1/1 000), mycket sällsynta (< 1/10 000), ingen känd frekvens (kan inte beräknas från tillgängliga data).
| Organklass |
Biverkning |
Frekvens |
| Infektioner och infestationer |
Sepsis |
Mindre vanliga |
| Centrala och perifera nervsystemet |
Intrakraniell blödning |
Mindre vanliga |
| Hjärtat |
Bradykardi |
Sällsynta |
| Blodkärl |
Hypotension |
Sällsynta |
| Andningsvägar, bröstkorg och mediastinum |
Bronchopulmonal dysplasi |
Sällsynta |
| Pneumothorax |
Mindre vanliga |
|
| Lungblödning |
Sällsynta |
|
| Hyperoxi |
Ingen känd frekvens |
|
| Neonatal cyanos |
Ingen känd frekvens |
|
| Apne |
Ingen känd frekvens |
|
| Undersökningar |
Sänkt syresaturation |
Sällsynta |
| Onormal EKG |
Ingen känd frekvens |
|
| Skador och förgiftningar och behandlingskomplikationer |
Komplikation vid intubation |
Ingen känd frekvens |
De ovan nämnda komplikationerna kan förekomma som en följd av att barnet föds för tidigt.
När Curosurf har administrerats genom en tunn kateter har några milda och övergående biverkningar observerats: bradykardi (låg hjärtfrekvens), apné (avbrott i andningen), minskad syremättnad, fradga i munnen, hosta, luftvägshinder och nysning.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Curosurf finns i injektionsflaskor som är färdiga för användning. Förvaras i originalförpackningen. Ljuskänsligt. Förvaras i kylskåp (2 °C-8 °C). Mängden som blir kvar efter första behandlingen får inte användas.
Oöppnade, oanvända Curosurf-injektionsflaskor som värmts upp till rumstemperatur kan återföras till kylskåp inom 24 timmar för kommande användning. Injektionsflaskan får värmas upp till rumstemperatur och återföras till kylskåp endast en gång.
Används före utgångsdatum som anges på förpackningen. Utgångsdatumet är den sista dagen i angiven månad.
Använd inte detta läkemedel om det synbart har förändrats.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- De aktiva substanserna är porcina lunglipider och protein.
- Övriga innehållsämnen är natriumklorid, natriumvätekarbonat (för pH-justering) och vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar
Vit eller gul steril suspension.
1 x 1,5 ml och 1 x 3 ml, klar, färglös injektionsflaska, plast- och aluminiumkork samt gummipropp.
Innehavare av godkännande för försäljning
Chiesi Farmaceutici S.p.A., via Palermo 26/A, 43122 Parma, Italien
Tillverkare
Chiesi Farmaceutici S.p.A., Via Palermo 26/A, 43122 Parma, Italien
eller
Chiesi Farmaceutici S.p.A., Via San Leonardo 96, 43122 Parma, Italien
Denna bipacksedel ändrades senast 10.04.2018
Direktiv för experterna inom hälsovården
Curosurf får ges endast av personal utbildad för och med erfarenhet av att vårda för tidigt födda barn, ge dem återupplivningsbehandling eller stabilisera deras tillstånd och endast under förutsättning att det finns lämplig utrustning för ventilation och övervakning av barn med RDS.
Profylaktisk användning: En dos om 1,25–2,50 ml/kg (100–200 mg/kg) kroppsvikt administreras så fort som möjligt efter födseln (helst inom 15 minuter). Ytterligare doser om 1,25 ml/kg (100 mg/kg) kan ges 6–12 timmar efter den första dosen och sedan 12 timmar senare till barn som har kvarstående tecken på RDS och behov av respiratorbehandling (maximal dos totalt: 3,75–5,0 ml/kg (300–400 mg/kg).
Behandling av RDS: Behandling bör ske så snart som möjligt efter diagnostisering. En dos om 1,25–2,5 ml/kg (100–200 mg/kg) kroppsvikt instilleras intratrakealt. Ytterligare en andra och tredje dos av samma storlek kan ges med 12 och 24 timmars intervall på ovan beskrivet sätt (maximal dos totalt 300–400 mg/kg).
Administrering: Injektionsflaskan värms till rumstemperatur före användning. Flaskan omskakas inte men vänds försiktigt upp och ner tills en jämn suspension erhålles. Skumbildning skall undvikas.
Suspensionen dras upp ur injektionsflaskan med en steril nål och spruta.
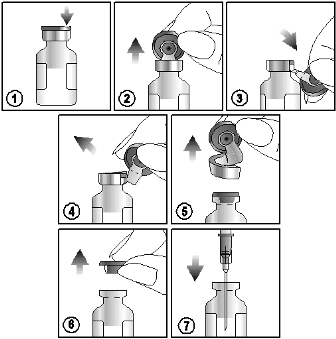
Ta upp suspensionen ur injektionsflaskan enligt följande anvisningar:
1) Hitta skåran som finns på den färgade plastkorken (LYFT ↑ UPP).
2) Lyft upp skåran och dra uppåt.
3) Dra plastkorken och dess aluminiumdel nedåt
4) och 5) avlägsna hela ringen genom att dra bort aluminiumhöljet
6) och 7) ta bort gummiproppen så att du kommer åt innehållet i injektionsflaskan.
För engångsbruk. Förstör det som inte använts. Spara inte oanvänt läkemedel för senare användning.
Oanvänd produkt och avfallet ska förstöras enligt lokala rekommendationer.
Curosurf kan ges med olika metoder via endotrakealtub enligt följande: Läkemedlet kan ges om barnet är kopplat till respirator eller har kopplats loss från respirator. Läkemedlet kan också vid behov ges i förlossningsrummet via en endotrakealtub innan den mekaniska ventilationen (för hand) inleds. Barnets luftvägar sugs rena före administrering. Barnet placeras i ryggläge. Curosurf ges via en kateter vars längd avpassas individuellt, så att spetsen sticker fram precis ovanför barnets carina. Curosurf ges under 2–3 sekunder. Efter administrering återansluts barnet till respiratorn (om barnet var bortkopplad från respiratorn under administreringen av läkemedlet) med samma syrekoncentration som före administreringen. Respiratorn måste därefter justeras med hänsyn till det kliniska svaret. Effekt kan väntas inom 5 minuter. Efter administrering får inte luftvägarna sugas på åtminstone 6 timmar om det inte är fråga om en livshotande situation.
Mindre invasiv administrering av surfaktant genom en tunn kateter (LISA): Till för tidigt födda barn som andas spontant kan Curosurf administreras med hjälp av mindre invasiv teknik för administrering av surfaktant genom en tunn kateter (LISA). Doserna är de samma som de ovan angivna. En kateter med liten diameter placeras i barnets luftstrupe så att man ser stämbanden med laryngoskop. För att försäkra kontinuerlig spontan andning är barnet kopplat till en CPAP-apparat. En engångsbolus av Curosurf ges under 0,5–3 minuter. Efter administrering av Curosurf avlägsnas katetern genast. CPAP-behandlingen ska fortsätta under hela ingreppet. Vid administrering av surfaktant ska katetrar som är CE-märkta för detta ändamål användas.
Erfarenheten av långtidsuppföljning är begränsad. För ytterligare information se godkänd produktresumé.