POMBILITI kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos 105 mg
Pombiliti 105 mg kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos
sipaglukosidaasi alfa
Lisäseuranta
![]() Tähän lääkevalmisteeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista. Ks. kohdan Mahdolliset haittavaikutukset lopusta, miten haittavaikutuksista ilmoitetaan.
Tähän lääkevalmisteeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista. Ks. kohdan Mahdolliset haittavaikutukset lopusta, miten haittavaikutuksista ilmoitetaan.
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin sinulle annetaan tätä lääkettä, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä Pombiliti on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin sinulle annetaan Pombiliti-valmistetta
3. Miten Pombiliti-valmistetta annetaan
4. Mahdolliset haittavaikutukset
5. Pombiliti-valmisteen säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Mitä Pombiliti on
Pombiliti on erääntyyppinen entsyymikorvaushoito, jota käytetään myöhään alkaneen Pompen taudin hoidossa aikuisilla. Lääkkeen vaikuttava aine on sipaglukosidaasi alfa.
Mihin sitä käytetään
Pombiliti-valmistetta käytetään aina toisen lääkkeen, miglustaatti 65 mg kovien kapseleiden, kanssa. On erittäin tärkeää, että luet myös miglustaatti 65 mg kovat kapselit ‑valmisteen pakkausselosteen.
Jos sinulla on kysyttävää lääkkeistäsi, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Miten Pombiliti toimii
Pompen tautia sairastavilla henkilöillä on vähäinen hapan alfa-glukosidaasi (GAA) ‑entsyymin pitoisuus. Tämä entsyymi auttaa säätelemään glykogeenin määriä elimistössä (glykogeeni on eräs hiilihydraattityyppi).
Pompen taudissa lihaksiin kertyy runsaasti glykogeenia. Tämä estää lihaksia, kuten kävelyä mahdollistavia lihaksia, hengittämistä edistäviä keuhkojen alla olevia lihaksia ja sydänlihasta, toimimasta kunnolla.
Pombiliti kulkeutuu Pompen taudin heikentämiin lihassoluihin. Soluissa ollessaan tämä lääke toimii GAA‑entsyymin tavoin ja auttaa pilkkomaan glykogeenia ja säätelemään sen määriä.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Sinulle ei saa antaa Pombiliti-valmistetta
- jos sinulla on joskus ollut hengenvaarallisia yliherkkyysreaktioita jollekin seuraavista:
- sipaglukosidaasi alfa
- miglustaatti
- tämän lääkkeen jokin muu aine (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
- jos jokin aiempi infuusio oli lopetettava eikä sitä voitu aloittaa uudelleen hengenvaarallisen yliherkkyysreaktion takia.
Varoitukset ja varotoimet
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin käytät Pombiliti-valmistetta.
Kerro lääkärille tai sairaanhoitajalle välittömästi, jos seuraava koskee sinua, jos uskot, että se saattaa koskea sinua, tai jos sinulla on joskus ollut tällaisia reaktioita toisen entsyymikorvaushoidon yhteydessä:
- allergiset reaktiot, kuten anafylaksi (vaikea allerginen reaktio) – ks. jäljempänä kohta Mahdolliset haittavaikutukset ”Mahdolliset haittavaikutukset”, jossa luetellaan hengenvaarallisten reaktioiden oireita.
- infuusioon liittyvä reaktio saadessasi lääkettä tai muutaman tunnin kuluessa lääkkeen saamisesta – ks. jäljempänä kohta Mahdolliset haittavaikutukset ”Mahdolliset haittavaikutukset”, jossa luetellaan hengenvaarallisten reaktioiden oireita.
Kerro lääkärille, jos sinulla on tai on ollut sydän- tai keuhkosairaus. Nämä sairaudet voivat pahentua Pombiliti-infuusion aikana tai heti sen jälkeen. Kerro lääkärille tai sairaanhoitajalle heti, jos sinulla ilmenee hengenahdistusta, yskää, nopeaa tai epäsäännöllistä sykettä tai mitään muita näiden sairauksien vaikutuksia.
Kerro lääkärille myös, jos säärissäsi on turvotusta tai ruumiissasi on laajalle levinnyttä turvotusta, sinulla on vaikea ihottuma tai virtsasi on vaahtoavaa. Lääkäri päättää, pitääkö Pombiliti-infuusio lopettaa, ja hän antaa sinulle asianmukaista hoitoa. Lääkäri päättää myös, voitko jatkaa Pombiliti-valmisteen saamista.
Hoitoa edeltävät lääkkeet
Lääkärisi saattaa antaa sinulle muita lääkkeitä ennen Pombiliti-hoitoa. Näitä lääkkeitä ovat:
- antihistamiinit ja kortikosteroidit infuusioon liittyvien reaktioiden ehkäisemiseksi tai lievittämiseksi
- antipyreetit (kuumelääkkeet) kuumeen alentamiseksi.
Lapset ja nuoret
Tätä lääkettä ei saa antaa alle 18‑vuotiaille potilaille. Tämä johtuu siitä, että Pombiliti‑valmisteen ja miglustaatin yhdistelmän vaikutuksia tässä ikäryhmässä ei tunneta.
Muut lääkevalmisteet ja Pombiliti
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä. Tämä koskee myös ilman reseptiä saatavia lääkkeitä sekä rohdosvalmisteita.
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, älä ota tätä lääkettä vaan kysy välittömästi lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
Pombiliti-valmisteen käytöstä yhdessä miglustaatin kanssa raskauden aikana ei ole kokemusta.
- Sinun ei pidä käyttää Pombiliti-valmistetta ja/tai miglustaatti 65 mg kovia kapseleita, jos olet raskaana. Kerro lääkärille välittömästi, jos tulet raskaaksi, epäilet olevasi raskaana tai jos suunnittelet raskautta. Syntymättömään lapseen voi kohdistua riskejä.
- Pombiliti-valmistetta yhdessä miglustaatin kanssa ei pidä antaa imettäville naisille. On päätettävä, lopetetaanko hoito vai lopetetaanko imetys.
Ehkäisy ja hedelmällisyys
Naispotilaiden, jotka voivat tulla raskaaksi, on käytettävä luotettavia ehkäisymenetelmiä molempien lääkkeiden käytön aikana ja neljän viikon ajan molempien lääkkeiden käytön lopettamisen jälkeen.
Ajaminen ja koneiden käyttö
Sinulle voi tulla huimausta, uneliaisuutta tai matalaa verenpainetta (hypotensiota) Pombiliti-valmisteen tai esilääkityksen saamisen jälkeen. Jos näin käy, älä aja autoa äläkä käytä työkaluja tai koneita.
Pombiliti sisältää natriumia
Tämä lääkevalmiste sisältää 10,5 mg natriumia (ruokasuolan toinen ainesosa) per injektiopullo. Tämä vastaa 0,52 %:a suositellusta natriumin enimmäisvuorokausiannoksesta aikuiselle.
Miten valmistetta käytetään
Lääkäri tai sairaanhoitaja antaa sinulle Pombiliti-valmisteen. Se annetaan tiputuksena laskimoon. Tätä kutsutaan laskimoinfuusioksi.
Kerro lääkärillesi, jos haluat, että sinua hoidetaan kotona. Lääkäri päättää arvioinnin jälkeen, voitko saada Pombiliti-infuusion turvallisesti kotona. Jos Pombiliti-infuusion aikana ilmenee haittavaikutuksia, kotona infuusion antava hoitohenkilökunnan jäsen saattaa lopettaa infuusion ja aloittaa asianmukaisen hoidon.
Pombiliti-valmistetta on käytettävä yhdessä miglustaatin kanssa. Voit käyttää sipaglukosidaasi alfan kanssa vain 65 mg:n miglustaattikapseleita. ÄLÄ käytä 100 mg:n miglustaattikapseleita (eri valmiste). Noudata lääkärin ohjeita ja lue miglustaatti 65 mg kovien kapseleiden suositeltu annos kyseisen valmisteen pakkausselosteesta.
Miten paljon Pombiliti-valmistetta annetaan
Sinulle annettavan lääkkeen määrä perustuu painoosi. Suositeltu annos on 20 mg jokaista painokilogrammaa kohti.
Milloin ja miten kauan Pombiliti-valmistetta annetaan
- Sinua hoidetaan Pombiliti-valmisteella joka toinen viikko. Miglustaatti 65 mg kapselit otetaan samana päivänä kuin Pombiliti. Katso miglustaatti 65 mg kovat kapselit ‑valmisteen pakkausselosteesta ohjeet miglustaatin ottamiseen.
- Sipaglukosidaasi alfan on aloitettava 1 tunti miglustaatti 65 mg kovat kapselit ‑valmisteen ottamisen jälkeen.
- Infuusion viivästyessä infuusio on aloitettava viimeistään 3 tunnin kuluessa miglustaatin ottamisesta.
- Sipaglukosidaasi alfan infuusion anto kestää noin 4 tuntia.
Kuva 1. Annoksen aikajana
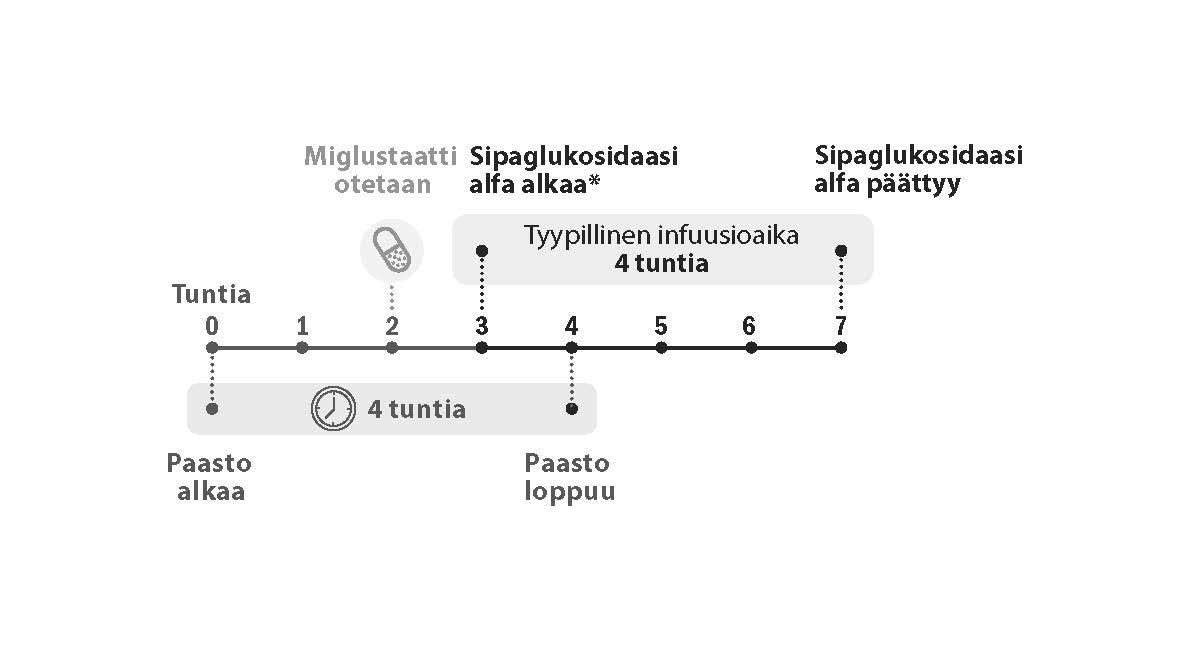
*Sipaglukosidaasi alfan -infuusio on aloitettava 1 tunnin kuluttua miglustaattikapseleiden ottamisesta. Jos infuusio viivästyy, infuusio on aloitettava viimeistään 3 tunnin kuluttua miglustaatin ottamisesta.
Siirtyminen toisesta entsyymikorvaushoidosta
Jos sinua hoidetaan tällä hetkellä toisella entsyymikorvaushoidolla:
- Lääkärisi kertoo sinulle, milloin toinen entsyymikorvaushoito on lopetettava ennen Pombiliti‑hoidon aloittamista.
- Kerro lääkärillesi, milloin olet saanut viimeisimmän entsyymikorvaushoitoannoksesi.
Jos saat enemmän Pombiliti-valmistetta kuin sinun pitäisi
Jos sinulla on hengitysvaikeuksia, turvotusta tai vatsan pullotusta tai sydämesi pamppailee, sinulle on ehkä annettu liikaa Pombiliti-valmistetta. Kerro asiasta heti lääkärillesi. Liian suuri Pombiliti-valmisteen infuusionopeus voi aiheuttaa oireita, jotka liittyvät elimistön liialliseen nestemäärään, kuten hengenahdistusta, nopeaa sydämen sykettä tai ruumiissa laajalle leviävää turvotusta.
Jos sinulta jää väliin Pombiliti-annos
Jos sinulta on jäänyt väliin infuusio, ota yhteyttä lääkäriin tai sairaanhoitajaan mahdollisimman pian, jotta Pombiliti-valmisteen ja miglustaatin yhdistelmä voidaan aikatauluttaa uudelleen 24 tunnin päähän viimeisimmästä miglustaatin otosta.
Jos lopetat Pombiliti-valmisteen käytön
Keskustele lääkärisi kanssa, jos haluat lopettaa Pombiliti-hoidon. Sairautesi oireet voivat pahentua, jos lopetat hoidon.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Pombiliti-valmistetta käytetään yhdessä miglustaatin kanssa, ja kumpikin näistä lääkkeistä voi aiheuttaa haittavaikutuksia. Haittavaikutuksia havaittiin pääasiassa potilaiden saadessa Pombiliti-infuusiota (infuusioon liittyvät vaikutukset) tai pian sen jälkeen. Kerro lääkärillesi välittömästi, jos saat infuusioon liittyvän reaktion tai allergisen reaktion. Jotkin näistä reaktioista voivat muodostua vakaviksi ja hengenvaarallisiksi. Lääkärisi saattaa antaa sinulle lääkkeitä ennen infuusiota näiden reaktioiden estämiseksi.
Infuusioon liittyvät reaktiot
Useimmat infuusioon liittyvät reaktiot ovat lieviä tai keskivaikeita. Infuusioon liittyvän reaktion oireita voivat olla hengitysvaikeudet, vatsan pullotus, kuume, vilunväristykset, heitehuimaus, ihon punoitus, kutiseva iho ja ihottuma.
Allergiset reaktiot
Allergisten reaktioiden oireita voivat olla mm. ihottuma missä tahansa ruumiin kohdassa, turvonneet silmät, pitkittyneet hengitysvaikeudet, yskä, huulten, kielen tai nielun turvotus, kutiseva iho ja nokkosihottuma.
Hyvin yleiset (voivat esiintyä useammalla kuin yhdellä henkilöllä 10:stä)
- päänsärky.
Yleiset (voivat esiintyä enintään yhdellä henkilöllä 10:stä)
- vakava ja hengenvaarallinen allerginen reaktio (anafylaktinen reaktio)
- huimauksen tunne
- vapina
- uneliaisuuden tunne
- makuaistin muuttuminen
- puutumisen ja pistelyn tunne (parestesia)
- nopea syke
- ihon punoitus
- matala verenpaine
- hengenahdistus
- yskä
- ripuli
- pahoinvointi
- vatsakipu
- ilmavaivat
- turvotus
- oksentelu
- nokkosihottuma
- kutiava iho
- ihottuma
- liikahikoilu
- kivuliaat lihaskrampit
- lihaskipu
- lihasheikkous
- kipu nivelissä
- väsymys
- kuume
- vilunväristykset
- epämukava tunne rinnassa
- turvotus kehon alueella, johon neula pistettiin
- kipu
- kämmenten, jalkaterien, nilkkojen tai säärien turvotus
- verenpaineen nousu.
Melko harvinaiset (voivat esiintyä enintään yhdellä henkilöllä 100:sta)
- allerginen reaktio
- kyvyttömyys säilyttää tai ylläpitää tasapainoa
- polttava tunne
- migreeni
- tunne lähellä pyörtymistä olemisesta
- ihon epätavallinen kalpeus
- astma
- vinkuva ääni (hengityksen vinkuminen)
- epämukava tunne suussa ja nielussa
- nielun turvotus
- ruuansulatushäiriö
- kipu ruokatorvessa tai kivuliaat ruokatorven supistukset
- suun kipu tai epämukava tunne suussa
- kielen turvotus
- ihon värimuutokset
- ihon turvotus
- kipu lonkan ja kylkiluun välisellä alueella
- lihasväsymys
- lihasjäykkyys
- heikkouden tunne
- posken, ikenien, huulten tai leuan kipu
- kipu kehon alueella, johon neula pistettiin
- yleinen huonovointisuuden tunne
- kipu rinnassa
- kasvojen turvotus
- kehon lämpötilan vaihtelu
- naarmut ja ihovauriot.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
Valmisteen säilyttäminen
Lääkäri, apteekkihenkilökunta tai sairaanhoitaja on vastuussa tämän lääkkeen säilyttämisestä ja avattujen injektiopullojen asianmukaisesta hävittämisestä. Seuraavat tiedot on tarkoitettu terveydenhuollon ammattilaisille.
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pullossa ja kotelossa mainitun viimeisen käyttöpäivämäärän (Käyt. viim.) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Avaamattomat injektiopullot: Säilytä jääkaapissa (2 °C – 8 °C). Pidä injektiopullo ulkopakkauksessa. Herkkä valolle.
Valmiste on suositeltavaa käyttää välittömästi laimentamisen jälkeen. Pombiliti-valmistetta sisältävän infuusiopussin säilyvyys on kuitenkin osoitettu 6 tunnin ajalta 20 °C – 25 °C:ssa ja 24 tunnin ajalta 2 °C – 8 °C:ssa.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Pombiliti sisältää
Vaikuttava aine on sipaglukosidaasi alfa. Yksi injektiopullo sisältää 105 mg sipaglukosidaasi alfaa. Käyttökuntoon saattamisen jälkeen injektiopullossa oleva liuos sisältää 15 mg sipaglukosidaasi alfaa per ml. Laskimopussiin laimennetun sipaglukosidaasi alfan suositeltu lopullinen pitoisuus on 0,5 mg/ml – 4 mg/ml.
- Muut aineet ovat:
- Natriumsitraattidihydraatti (E331)
- Sitruunahappomonohydraatti (E330)
- Mannitoli (E421)
- Polysorbaatti 80 (E433).
Lääkevalmisteen kuvaus ja pakkauskoko (-koot)
Pombiliti on valkoinen tai hieman kellertävä. Käyttökuntoon saattamisen jälkeen se näyttää kirkkaalta tai opaalinhohtoiselta, värittömältä tai hieman keltaiselta liuokselta, jossa ei ole vierashiukkasia eikä käytännössä lainkaan valkoisia tai läpikuultavia hiukkasia. Käyttökuntoon saatettu liuos on laimennettava edelleen infuusiopussiin.
Pombiliti on injektiopullossa toimitettava kuiva-aine välikonsentraatiksi infuusionestettä varten, liuos.
Pakkauskoot ovat 1 injektiopullo, 10 injektiopulloa ja 25 injektiopulloa.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija
Amicus Therapeutics Europe Limited
Block 1, Blanchardstown Corporate Park
Ballycoolin Road
Blanchardstown, Dublin
D15 AKK1
Irlanti
Puh: +353 (0) 1 588 0836
Faksi: +353 (0) 1 588 6851
Sähköposti: info@amicusrx.co.uk
Valmistaja
Manufacturing Packaging Farmaca (MPF) B.V.
Neptunus 12
Heerenveen
8448CN
Alankomaat
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
België/Belgique/Belgien Amicus Therapeutics Europe Limited Tél/Tel: (+32) 0800 89172 e-mail: MedInfo@amicusrx.com | Lietuva Amicus Therapeutics Europe Limited Tel: (+370) 8800 33167 El. paštas: MedInfo@amicusrx.com |
България Amicus Therapeutics Europe Limited Teл.: (+359) 00800 111 3214 имейл: MedInfo@amicusrx.com | Luxembourg/Luxemburg Amicus Therapeutics Europe Limited Tél/Tel: (+352) 800 27003 e-mail: MedInfo@amicusrx.com |
Česká republika Amicus Therapeutics Europe Limited Tel.: (+420) 800 142 207 e-mail: MedInfo@amicusrx.com | Magyarország Amicus Therapeutics Europe Limited Tel.: (+36) 06 800 21202 e-mail: MedInfo@amicusrx.com |
Danmark Amicus Therapeutics Europe Limited Tlf: (+45) 80 253 262 e-mail: MedInfo@amicusrx.com | Malta Amicus Therapeutics Europe Limited Tel: (+356) 800 62674 e-mail: MedInfo@amicusrx.com |
Deutschland Amicus Therapeutics GmbH Tel: (+49) 0800 000 2038 E-Mail: MedInfo@amicusrx.com | Nederland Amicus Therapeutics BV Tel: (+31) 20 235 8510 / (+31) 0800 022 8399 e-mail: MedInfo@amicusrx.com |
Eesti Amicus Therapeutics Europe Limited Tel: (+372) 800 0111 911 e-post: MedInfo@amicusrx.com | Norge Amicus Therapeutics Europe Limited Tlf: (+47) 800 13837 e-post: MedInfo@amicusrx.com |
Ελλάδα Amicus Therapeutics Europe Limited Τηλ: (+30) 00800 126 169 e-mail: MedInfo@amicusrx.com | Österreich Amicus Therapeutics Europe Limited Tel: (+43) 0800 909 639 E-Mail: MedInfo@amicusrx.com |
España Amicus Therapeutics S.L.U. Tel: (+34) 900 941 616 e-mail: MedInfo@amicusrx.com | Polska Amicus Therapeutics Europe Limited Tel.: (+48) 0080 012 15475 e-mail: MedInfo@amicusrx.com |
France Amicus Therapeutics SAS Tél: (+33) 0 800 906 788 e-mail: MedInfo@amicusrx.com | Portugal Amicus Therapeutics Europe Limited Tel: (+351) 800 812 531 e-mail: MedInfo@amicusrx.com |
Hrvatska Amicus Therapeutics Europe Limited Tel: (+358) 0800 222 452 e-pošta: MedInfo@amicusrx.com | România Amicus Therapeutics Europe Limited Tel.: (+40) 0808 034 288 e-mail: MedInfo@amicusrx.com |
Ireland Amicus Therapeutics Europe Limited Tel: (+353) 1800 936 230 e-mail: MedInfo@amicusrx.com | Slovenija Amicus Therapeutics Europe Limited Tel.: (+386) 0800 81794 e-pošta: MedInfo@amicusrx.com |
Ísland Amicus Therapeutics Europe Limited Sími: (+354) 800 7634 Netfang: MedInfo@amicusrx.com | Slovenská republika Amicus Therapeutics Europe Limited Tel: (+421) 0800 002 437 e-mail: MedInfo@amicusrx.com |
Italia Amicus Therapeutics S.r.l. Tel: (+39) 800 795 572 e-mail: MedInfo@amicusrx.com | Suomi/Finland Amicus Therapeutics Europe Limited Puh/Tel: (+358) 0800 917 780 sähköposti/e-mail: MedInfo@amicusrx.com |
Κύπρος Amicus Therapeutics Europe Limited Τηλ: (+357) 800 97595 e-mail: MedInfo@amicusrx.com | Sverige Amicus Therapeutics Europe Limited Tfn: (+46) 020 795 493 e-post: MedInfo@amicusrx.com |
Latvija Amicus Therapeutics Europe Limited Tel: (+371) 800 05391 e-pasts: MedInfo@amicusrx.com | United Kingdom (Northern Ireland) Amicus Therapeutics, UK Limited Tel: (+44) 08 0823 46864 e-mail: MedInfo@amicusrx.com |
Tämä pakkausseloste on tarkistettu viimeksi 12.09.2024
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla http://www.ema.europa.eu/. Siellä on myös linkkejä muille harvinaisia sairauksia ja niiden hoitoja käsitteleville verkkosivuille.
Ohjeet terveydenhuollon ammattilaiselle
Seuraavat tiedot on tarkoitettu vain terveydenhuollon ammattilaisille:
Käyttöohjeet – käyttökuntoon saattaminen, laimentaminen ja anto
Pombiliti on saatettava käyttökuntoon injektionesteisiin käytettävällä vedellä, laimennettava sen jälkeen injektionesteisiin tarkoitetulla natriumkloridiliuoksella 9 mg/ml (0,9 %) ja annettava sitten laskimoinfuusiona. Käyttökuntoon saattaminen ja laimentaminen on tehtävä hyvien käytäntöjen mukaisesti, erityisesti aseptiikan osalta.
Koska tämä lääke on proteiini, käyttökuntoon saatettuun liuokseen ja lopullisiin laimennukseen käytettyihin infuusiopusseihin voi muodostua hiukkasia. Siksi antoon on käytettävä 0,2 mikronin vähän proteiineja sitovaa in‑line‑suodatinta. On osoitettu, että 0,2 mikronin in‑line‑suodattimen käyttö poistaa näkyviä hiukkasia eikä johda proteiinin tai aktiivisuuden ilmeiseen katoon.
Määritä käyttökuntoon saatettavien injektiopullojen määrä potilaan annostusohjelman (mg/kg) perusteella ja ota tarvittavat injektiopullot jääkaapista, jotta ne saavuttavat huoneenlämpötilan (noin 30 minuutissa). Jokainen Pombiliti-injektiopullo on kertakäyttöinen.
Käytä aseptista tekniikkaa.
Käyttökuntoon saattaminen
Saata kunkin injektiopullon sisältämät 105 mg Pombiliti-valmistetta käyttökuntoon 7,2 ml:lla injektionesteisiin käytettävää vettä käyttämällä ruiskua, jonka neulan läpimitta on enintään 18 G. Lisää injektionesteisiin käytettävä vesi hitaasti tiputtamalla sitä tipoittain pullon sisäpuolta pitkin alaspäin, älä suoraan kylmäkuivattuun jauheeseen. Kallista ja pyöritä jokaista injektiopulloa varovasti. Älä käännä ylösalaisin, kieputa äläkä ravista injektiopulloa. Saatu tilavuus näyttää kirkkaalta tai opaalinhohtoiselta, värittömältä tai hieman keltaiselta liuokselta, jossa ei ole vierashiukkasia eikä käytännössä lainkaan valkoisia tai läpikuultavia hiukkasia. Tarkasta välittömästi käyttökuntoon saatetut injektiopullot hiukkasten ja värimuutosten varalta. Ei saa käyttää, jos välittömässä tarkastuksessa havaitaan muita kuin edellä kuvattuja vierashiukkasia tai jos käyttökuntoon saatetussa liuoksessa on värimuutoksia. Käyttökuntoon saatetun liuoksen pH on noin 6,0.
Käyttökuntoon saattamisen jälkeen on suositeltavaa laimentaa injektiopullot viipymättä (ks. alla).
Laimennus
Yllä kuvatulla tavalla käyttökuntoon saatetussa injektiopullossa oleva liuos sisältää 15 mg sipaglukosidaasi alfaa per ml. Käyttökuntoon saatettu tilavuus mahdollistaa 7,0 ml:n (vastaa 105 mg:aa) tarkan ottamisen kustakin injektiopullosta. Tämä tulee sitten laimentaa edelleen seuraavasti: Vedä käyttökuntoon saatettu liuos hitaasti kustakin injektiopullosta ruiskulla, jonka neulan läpimitta on enintään 18 G, mukaan lukien alle 7,0 ml osittain käytettävästä injektiopullosta, kunnes potilaan annos saavutetaan. Infuusiopussiin laimennetun sipaglukosidaasi alfan suositeltu lopullinen pitoisuus on 0,5 mg/ml – 4 mg/ml. Poista ilmatila infuusiopussista. Poista myös yhtä suuri määrä injektionesteisiin käytettävää natriumkloridiliuosta 9 mg/ml (0,9 %), joka korvataan käyttökuntoon saatetulla Pombiliti-valmisteella. Injisoi käyttökuntoon saatettu Pombiliti-valmiste hitaasti suoraan injektionesteisiin käytettävään natriumkloridi 9 mg/ml (0,9 %) ‑liuokseen. Käännä infuusiopussi varovasti ylösalaisin tai hiero varovasti pussia laimennetun liuoksen sekoittamiseksi. Älä ravista tai heiluttele voimakkaasti infuusiopussia.
Lopullinen infuusioliuos on annettava mahdollisimman lähellä valmisteluaikaa.
Käyttämätön lääke tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Anto
Pombiliti-infuusio on aloitettava 1 tunti miglustaattikapseleiden ottamisen jälkeen. Jos infuusio viivästyy, infuusio on aloitettava viimeistään 3 tunnin kuluessa miglustaatin ottamisesta.
Pombiliti-valmisteen suositeltu annostus on 20 mg/painokilo kahden viikon välein infuusiona laskimoon.
Infuusiot on annettava asteittain. On suositeltavaa, että infuusio aloitetaan aloitusnopeudella 1 mg/kg/h ja sitä nostetaan asteittain 2 mg/kg/h:lla 30 minuutin välein, jos merkkejä infuusioon liittyvistä reaktioista ei ole, kunnes saavutetaan enimmäisnopeus 7 mg/kg/h.