VYDURA tabletti, kylmäkuivattu 75 mg
VYDURA 75 mg tabletti, kylmäkuivattu
rimegepantti
Lisäseuranta
▼ Tähän lääkevalmisteeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista. Ks. kohdan Mahdolliset haittavaikutukset lopusta, miten haittavaikutuksista ilmoitetaan.
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen ottamisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä pidä antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä VYDURA on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin otat VYDURA-valmistetta
3. Miten VYDURA-valmistetta otetaan
4. Mahdolliset haittavaikutukset
5. VYDURA-valmisteen säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
VYDURA-valmisteen sisältämä vaikuttava aine on rimegepantti, joka estää elimistössä olevan kalsitoniinigeeniin liittyväksi peptidiksi (CGRP:ksi) kutsutun aineen toimintaa. Migreeniä sairastavilla CGRP-taso saattaa olla koholla. Rimegepantti kiinnittyy CGRP:n reseptoreihin ja estää siten CGRP:tä kiinnittymästä samoihin reseptoreihin. Tämä vähentää CGRP:n toimintaa, millä on kaksi vaikutusta:
1) jo alkanut migreenikohtaus voi mennä ohi
2) migreenikohtausten määrä voi vähentyä, kun lääkettä otetaan ennaltaehkäisevästi.
VYDURA-valmistetta käytetään aikuisten migreenikohtausten hoitoon ja ennaltaehkäisyyn.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä ota VYDURA-valmistetta
- jos olet allerginen rimegepantille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
Varoitukset ja varotoimet
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen VYDURA-valmisteen ottamista, jos jokin seuraavista koskee sinua:
- jos sinulla on vaikeita maksaongelmia
- jos munuaistesi toiminta on heikentynyt tai saat dialyysihoitoa.
Lopeta VYDURA-hoidon aikana tämän lääkkeen ottaminen ja kerro heti lääkärille
- jos sinulla esiintyy allergisen reaktion oireita, kuten hengitysvaikeuksia tai vaikeaa ihottumaa. Näitä oireita voi ilmaantua useiden päivien jälkeen lääkkeen ottamisesta.
Lapset ja nuoret
VYDURA-valmistetta ei saa antaa lapsille eikä alle 18‑vuotiaille nuorille, koska sitä ei ole vielä tutkittu tässä ikäryhmässä.
Muut lääkevalmisteet ja VYDURA
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan otat, olet äskettäin ottanut tai saatat ottaa muita lääkkeitä. Jotkin lääkkeet saattavat vaikuttaa siihen, miten VYDURA toimii, tai VYDURA saattaa vaikuttaa siihen, miten jotkin muut lääkkeet toimivat.
Vältä seuraavien lääkkeiden käyttöä VYDURA-valmisteen ottamisen aikana:
- itrakonatsoli ja klaritromysiini (sieni- tai bakteeri-infektioiden hoitoon käytettäviä lääkkeitä)
- ritonaviiri ja efavirentsi (HIV-infektion hoitoon käytettäviä lääkkeitä)
- bosentaani (korkean verenpaineen hoitoon käytettävä lääke)
- mäkikuisma (masennuksen hoitoon käytettävä rohdosvalmiste)
- fenobarbitaali (epilepsian hoitoon käytettävä lääke)
- rifampisiini (tuberkuloosin hoitoon käytettävä lääke)
- modafiniili (narkolepsian hoitoon käytettävä lääke).
Älä ota VYDURA-valmistetta useammin kuin 48 tunnin välein, jos otat sitä samanaikaisesti seuraavien lääkkeiden kanssa:
- flukonatsoli ja erytromysiini (sieni- tai bakteeri-infektioiden hoitoon käytettäviä lääkkeitä)
- diltiatseemi, kinidiini ja verapamiili (sydämen rytmihäiriöiden, rasitusrintakivun tai korkean verenpaineen hoitoon käytettäviä lääkkeitä)
- siklosporiini (elinsiirron jälkeisen hyljinnän ehkäisyyn käytettävä lääke).
Raskaus ja imetys
Jos olet raskaana, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä. VYDURA-valmisteen käyttöä on suositeltavaa välttää raskauden aikana, koska sen vaikutuksia raskaana olevilla naisilla ei tunneta.
Jos imetät tai suunnittelet imettämisen aloittamista, keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen tämän lääkkeen käyttöä. Sinun ja lääkärin tulee yhdessä päättää, käytätkö VYDURA-valmistetta imetyksen aikana.
Ajaminen ja koneiden käyttö
VYDURA-valmisteen ei odoteta vaikuttavan ajokykyysi tai koneidenkäyttökykyysi.
Miten valmistetta käytetään
Ota tätä lääkettä juuri siten kuin lääkäri on määrännyt tai apteekkihenkilökunta on neuvonut. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma.
Kuinka paljon tätä lääkettä otetaan
Migreenin ennaltaehkäisyyn suositeltu annos on yksi kylmäkuivattu tabletti (75 mg rimegepanttia) joka toinen päivä.
Jo alkaneen migreenikohtauksen hoitoon suositeltu annos on yksi kylmäkuivattu tabletti (75 mg rimegepanttia) enintään kerran päivässä, tarpeen mukaan.
Enimmäisannos vuorokautta kohden on yksi kylmäkuivattu tabletti (75 mg rimegepanttia).
Miten tätä lääkettä otetaan
VYDURA on tarkoitettu suun kautta otettavaksi.
Kylmäkuivatun tabletin voi ottaa ruoan tai veden kanssa tai ilman ruokaa tai vettä.
Ohjeet:
|
|
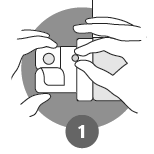
Avaa pakkaus kuivin käsin. Poista yhden läpipainopakkauksen taustafolio ja ota kylmäkuivattu tabletti varovasti pakkauksesta. Älä paina kylmäkuivattua tablettia folion läpi. |
|
|
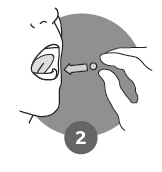
Ota kylmäkuivattu tabletti läpipainopakkauksesta heti avaamisen jälkeen, ja aseta se kielen päälle tai alle, jossa se liukenee. Vettä tai muuta nestettä ei tarvita. Älä säilytä kylmäkuivattua tablettia läpipainopakkauksen ulkopuolella tulevaa käyttöä varten. |
Jos otat enemmän VYDURA-valmistetta kuin sinun pitäisi
Ota yhteys lääkäriin tai apteekkiin tai hakeudu suoraan sairaalaan. Ota lääkkeen pakkaus ja tämä pakkausseloste mukaasi.
Jos unohdat ottaa VYDURA-valmistetta
Jos otat VYDURA-valmistetta migreenin ennaltaehkäisyyn ja unohdat ottaa annoksen, ota seuraava annos normaaliin aikaan. Älä ota kaksinkertaista annosta korvataksesi unohtamasi kerta-annoksen.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Lopeta VYDURA-valmisteen käyttö ja ota välittömästi yhteys lääkäriin, jos sinulla esiintyy allergisen reaktion oireita, kuten vaikeaa ihottumaa tai hengenahdistusta. VYDURA-valmisteen aiheuttamat allergiset reaktiot ovat melko harvinaisia (saattaa esiintyä enintään yhdellä henkilöllä 100:sta).
Pahoinvointi on yleinen haittavaikutus (saattaa esiintyä enintään yhdellä henkilöllä 10:stä).
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www‐sivusto: www.fimea.fi
Lääkealan turvallisuus‐ ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
FI‐00034 Fimea
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä kotelossa ja läpipainopakkauksessa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä alle 30°C. Säilytä alkuperäisessä läpipainopakkauksessa. Herkkä kosteudelle.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä VYDURA sisältää
- Vaikuttava aine on rimegepantti. Yksi kylmäkuivattu tabletti sisältää 75 mg rimegepanttia (sulfaattina).
- Muut aineet ovat: liivate, mannitoli, minttuaromi ja sukraloosi.
Lääkevalmisteen kuvaus ja pakkauskoko (-koot)
VYDURA 75 mg kylmäkuivatut tabletit ovat valkoisia tai luonnonvalkoisia, pyöreitä, ja niihin on kaiverrettu symboli ![]() .
.
Pakkauskoot:
- 2 x 1 kylmäkuivattua tablettia rei’itetyissä yksittäispakatuissa läpipainopakkauksissa.
- 8 x 1 kylmäkuivattua tablettia rei’itetyissä yksittäispakatuissa läpipainopakkauksissa.
- 16 x 1 kylmäkuivattua tablettia rei’itetyissä yksittäispakatuissa läpipainopakkauksissa.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija
Pfizer Europe MA EEIG
Boulevard de la Plaine 17
1050 Bruxelles
Belgia
Valmistaja
HiTech Health Limited
5-7 Main Street
Blackrock
Co. Dublin
A94 R5Y4
Irlanti
Millmount Healthcare Limited
Block-7, City North Business Campus
Stamullen
Co. Meath
K32 YD60
Irlanti
Pfizer Ireland Pharmaceuticals Unlimited Company
Little Connell
Newbridge
Co. Kildare
W12 HX57
Irlanti
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Suomi/Finland
Pfizer Oy
Puh/Tel: +358 (0)9 430 040
Tämä pakkausseloste on tarkistettu viimeksi 04/2025.
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla https://www.ema.europa.eu.