DROVELIS tabletti, kalvopäällysteinen 3/14,2 mg
Drovelis 3 mg/14,2 mg kalvopäällysteiset tabletit
drospirenoni/estetroli
Yleisiä ohjeita
Tärkeää tietää hormonaalisista yhdistelmäehkäisyvalmisteista:
- Oikein käytettynä ne ovat yksi luotettavimmista palautuvista raskaudenehkäisymenetelmistä.
- Ne lisäävät hieman laskimoiden ja valtimoiden veritulppien riskiä erityisesti ensimmäisen käyttövuoden aikana tai kun hormonaalisen yhdistelmäehkäisyvalmisteen käyttö aloitetaan uudelleen vähintään 4 viikon tauon jälkeen.
- Ole valppaana ja käänny lääkärin puoleen, jos epäilet, että sinulla saattaa olla veritulpan oireita (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Veritulpat”).
Lue tämä pakkausseloste huolellisesti ennen kuin aloitat tämän lääkkeen ottamisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä pidä antaa muiden käyttöön. Se voi aiheuttaa haittaa muille.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä Drovelis on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin otat Drovelis-valmistetta
- Miten Drovelis-valmistetta otetaan
- Mahdolliset haittavaikutukset
- Drovelis-valmisteen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Drovelis on ehkäisyvalmiste, jota käytetään raskauden ehkäisyyn.
- Kaikki 24 vaaleanpunaista, kalvopäällysteistä tablettia ovat vaikuttavia aineita sisältäviä tabletteja, jotka sisältävät kahta naissukupuolihormonia, estetrolia ja drospirenonia.
- 4 valkoista, kalvopäällysteistä tablettia ovat epäaktiivisia tabletteja eivätkä ne sisällä hormoneja. Niitä kutsutaan lumetableteiksi.
- Ehkäisytabletteja, jotka sisältävät kahta eri hormonia, kuten Drovelisia, kutsutaan yhdistelmäehkäisytableteiksi. Valmisteen sisältämät hormonit toimivat yhdessä ja estävät raskaaksi tulemista estämällä ovulaation (munasolun irtoamisen munasarjoista) ja vähentämällä mahdollisesti irronneen munasolun hedelmöittymistä.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Yleisiä ohjeita Lue kohdasta Mitä sinun on tiedettävä ennen valmisteen käyttöä tietoja veritulpista, ennen kuin aloitat Drovelis-tablettien käytön. Tutustuminen veritulppien oireisiin on erityisen tärkeää; katso kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Veritulpat”. |
Drovelis-valmisteen vasta-aiheet
Et saa käyttää Drovelis-tabletteja, jos sinulla on jokin alla mainituista sairauksista. Sinun on kerrottava lääkärille, jos sinulla on jokin näistä sairauksista. Lääkäri keskustelee kanssasi muista sinulle paremmin soveltuvista ehkäisymenetelmistä,
- jos olet allerginen estetrolille tai drospirenonille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa)
- jos sinulla on (tai on joskus ollut) verisuonitukos alaraajassa (syvä laskimotukos), keuhkoissa (keuhkoveritulppa) tai muissa elimissä
- jos tiedät, että sinulla on veren hyytymishäiriö, esimerkiksi proteiini C:n puutos, proteiini S:n puutos, antitrombiini III:n puutos, hyytymistekijä V:n mutaatio (faktori V Leiden) tai fosfolipidivasta-aineita
- jos tarvitset leikkausta tai olet vuodelevossa pitkään (ks. kohta ”Veritulpat”)
- jos sinulla on joskus ollut sydänkohtaus tai aivohalvaus
- jos sinulla on (tai on joskus ollut) angina pectoris (tila, joka saattaa aiheuttaa voimakasta rintakipua ja voi olla ensimmäinen merkki sydänkohtauksesta) tai ohimenevä aivoverenkiertohäiriö (TIA-kohtaus eli lievä, ohimenevä aivohalvaus, josta ei jää pysyviä oireita)
- jos sinulla on jokin seuraavista sairauksista, jotka voivat lisätä valtimotukoksen riskiä:
- vaikea diabetes, johon liittyy verisuonivaurioita
- korkea verenpaine
- erittäin korkea veren rasva-ainepitoisuus (kolesteroli- tai triglyseridipitoisuus)
- hyperhomokystinemiaksi kutsuttu tila
- jos sinulla on (tai joskus on ollut) ns. aurallinen migreeni
- jos sinulla on (ollut) hyvän- tai pahanlaatuinen maksakasvain
- jos sinulla on (tai on joskus ollut) maksasairaus, eivätkä maksan toimintakokeet ole vielä normaaleja
- jos munuaisesi eivät toimi hyvin (munuaisten vajaatoiminta)
- jos sinulla on (ollut) tai sinulla epäillään olevan rintasyöpä tai sukupuolielinten syöpä
jos sinulla esiintyy tuntemattomasta syystä johtuvaa verenvuotoa emättimestä.
Jos sinulla esiintyy jokin yllä mainituista sairauksista tai tiloista ensimmäistä kertaa Drovelis-tablettien käytön aikana, lopeta tablettien käyttö välittömästi ja ota yhteys lääkäriin. Käytä sillä välin ei-hormonaalista ehkäisymenetelmää. Ks. myös edellä kohta "Yleistä" kappaleesta 2.
Varoitukset ja varotoimet
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin käytät Drovelis-valmistetta.
Milloin sinun on otettava yhteys lääkäriin?
Näiden vakavien haittavaikutusten oireet löydät kohdasta ”Veritulpan tunnusmerkit”. |
Kerro lääkärille, jos jokin seuraavista koskee sinua.
Ota yhteyttä lääkäriin myös, jos jokin seuraavista tiloista ilmenee ensimmäistä kertaa tai pahenee Drovelis-valmisteen käytön aikana:
- jos lähisukulaisellasi on tai on joskus ollut rintasyöpä
- jos sinulla on perinnöllinen tai hankinnainen angioödeema. Estrogeenia sisältävät lääkevalmisteet saattavat aiheuttaa tai pahentaa angioödeeman oireita. Käänny heti lääkärin puoleen, jos sinulle ilmaantuu angioödeeman oireita, kuten kasvojen, kielen ja/tai kurkun turpoamista ja/tai nielemisvaikeuksia tai nokkosihottumaa, joihin liittyy hengitysvaikeuksia.
- jos sinulla on maksasairaus tai sappirakkosairaus
- jos sinulla on munuaissairaus
- jos sinulla on diabetes
- jos sairastat masennusta
- jos sinulla on epilepsia (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Muut lääkevalmisteet ja Drovelis”)
- jos sinulla on Crohnin tauti tai haavainen paksusuolitulehdus (krooninen tulehduksellinen suolistosairaus)
- jos sinulla on systeeminen lupus erythematosus (SLE, immuunijärjestelmään vaikuttava sairaus)
- jos sinulla on hemolyyttis-ureeminen oireyhtymä (HUS, munuaisten vajaatoimintaa aiheuttava veren hyytymishäiriö)
- jos sinulla on sirppisoluanemia (perinnöllinen veren punasolusairaus)
- jos veren rasva-arvosi ovat kohonneet (hypertriglyseridemia) tai suvussasi esiintyy kohonneita veren rasva-arvoja. Hypertriglyseridemiaan on liitetty korkeampi haimatulehduksen kehittymisen riski.
- jos joudut leikkaukseen tai olet vuodelevossa pitkään (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Veritulpat”)
- jos olet äskettäin synnyttänyt, veritulppariskisi on korkeampi. Kysy lääkäriltä, kuinka pian synnytyksen jälkeen voit aloittaa Drovelis-tablettien käytön.
- jos sinulla on ihonalainen laskimotulehdus (pinnallinen laskimontukkotulehdus)
- jos sinulla on suonikohjuja
- jos sinulla on tai on joskus ollut maksaläiskiä (ihon värittyminen erityisesti kasvoilla ja kaulalla; tunnetaan myös raskausläiskinä). Vältä tässä tapauksessa suoraa auringonvaloa ja ultraviolettisäteilyä.
- jos sinulla on sairaus, joka ilmestyi raskauden aikana tai kun aiemmin käytit sukupuolihormoneja (esimerkiksi kuulon heikkeneminen, porfyriaksi kutsuttu verisairaus, rakkulainen ihottuma raskauden aikana [raskaudenaikainen herpes] tai pakkoliikkeitä aiheuttava hermostosairaus [Sydehamin korea]).
VERITULPAT
Hormonaalisen yhdistelmäehkäisyvalmisteen, kuten Drovelis-tabletin, käyttö lisää riskiäsi saada verisuonitukos verrattuna henkilöihin, jotka eivät käytä tällaista valmistetta. Veritulppa voi harvinaisissa tapauksissa tukkia verisuonia ja aiheuttaa vakavia haittoja.
Veritulppa voi kehittyä
- laskimoon (laskimotukos eli laskimotromboembolia)
- valtimoon (valtimotukos eli valtimotromboembolia)
Toipuminen veritulpasta ei aina ole täydellistä. Harvoissa tapauksissa veritulpan jälkeen voi ilmetä vakavia pitkäaikaisia vaikutuksia, jotka erittäin harvoin voivat johtaa kuolemaan.
On tärkeää muistaa, että Drovelis-valmisteen käytön aiheuttaman vahingollisen veritulpan kokonaisriski on pieni.
VERITULPAN TUNNUSMERKIT
Hakeudu heti lääkärinhoitoon, jos huomaat seuraavia oireita:
| Onko sinulla jokin seuraavista oireista? | Minkä oireita ne voisivat olla? |
| syvä laskimotukos |
Keskustele lääkärin kanssa, jos olet epävarma. Jotkin näistä oireista, kuten yskiminen tai hengenahdistus, voidaan virheellisesti tulkita lievemmäksi sairaudeksi, kuten hengitystieinfektioksi (esim. tavalliseksi flunssaksi). | Keuhkoveritulppa |
Oireet, jotka useimmiten ilmenevät toisessa silmässä:
kivuton näön hämärtyminen, joka voi edetä näönmenetykseksi | Verkkokalvon laskimotukos (veritulppa silmässä) |
| Sydänkohtaus |
Joskus aivohalvauksen oireet voivat olla lyhytkestoisia ja ne saattavat korjautua lähes välittömästi ja kokonaan, mutta silti sinun pitää hakeutua lääkärin hoitoon, koska vaarana voi olla toinen aivohalvaus. | Aivohalvaus |
| Veritulpat, jotka tukkivat muita verisuonia |
LASKIMOVERITULPAT
Mitä voi tapahtua, jos laskimoon muodostuu veritulppa?
- Hormonaalisten yhdistelmäehkäisyvalmisteiden käyttöön on liittynyt lisääntynyt laskimoveritulppien (laskimotukosten) riski. Nämä haittavaikutukset ovat kuitenkin harvinaisia. Useimmiten ne ilmenevät hormonaalisen yhdistelmäehkäisyvalmisteen ensimmäisen käyttövuoden aikana.
- Jos jalan tai jalkaterän laskimoon muodostuu tukos, se voi aiheuttaa syvän laskimotukoksen.
- Jos veritulppa lähtee liikkeelle jalasta ja kulkeutuu keuhkoihin, se voi aiheuttaa keuhkoveritulpan.
- Erittäin harvinaisissa tapauksissa veritulppa voi muodostua laskimoon jossakin muussa elimessä, kuten silmässä (verkkokalvon laskimotukos).
Milloin laskimotukoksen muodostumisen riski on suurin?
Laskimoveritulpan muodostumisen riski on suurimmillaan ensimmäisen vuoden aikana, kun käytät hormonaalisia yhdistelmäehkäisyvalmisteita ensimmäistä kertaa. Riski voi myös olla suurempi, jos aloitat hormonaalisen yhdistelmäehkäisyvalmisteen (saman tai eri valmisteen) käytön uudelleen vähintään 4 viikon tauon jälkeen.
Ensimmäisen vuoden jälkeen riski pienenee, mutta pysyy aina hieman suurempana kuin silloin, jos et käytä hormonaalista yhdistelmäehkäisyvalmistetta.
Kun lopetat Drovelis-tablettien käytön, veritulppien riski palautuu normaaliksi muutaman viikon kuluessa.
Kuinka suuri veritulpan muodostumisen riski on?
Riski riippuu yksilöllisestä laskimoveritulppariskistäsi ja siitä, minkä tyyppinen hormonaalinen yhdistelmäehkäisyvalmiste on käytössä.
Drovelis-valmisteen käyttöön liittyvä jalan tai keuhkoveritulpan (syvän laskimotukoksen tai keuhkoembolian) riski on kaiken kaikkiaan pieni.
- Noin 2 naiselle 10 000:sta, jotka eivät käytä mitään hormonaalista yhdistelmäehkäisyvalmistetta eivätkä ole raskaana, kehittyy veritulppa yhden vuoden aikana.
- Naisilla, jotka käyttävät pieniannoksista (< 50 mikrogrammaa etinyyliestradiolia) hormonaalista yhdistelmäehkäisyvalmistetta, jossa on mukana levonorgestreelia, noretisteronia tai norgestimaattia, on havaittu, että yhden vuoden aikana 5–7:lle 10 000:sta kehittyy laskimotromboembolia.
- Toistaiseksi ei tiedetä, millainen Drovelis-valmisteen käyttöön liittyvä riski on verrattuna hormonaalisiin yhdistelmäehkäisyvalmisteisiin, jotka sisältävät levonorgestreelia.
- Veritulpan saamisen riski vaihtelee oman sairaushistoriasi mukaan (ks. jäljempänä kohta ”Veritulppariskiä suurentavat tekijät”).
| Veritulpan kehittymisen riski vuoden aikana | |
| Naiset, jotka eivät käytä yhdistelmähormonipilleriä, -laastaria tai -rengasta ja jotka eivät ole raskaana | Noin 2 naista 10 000:sta |
| Naisilla, jotka käyttävät pieniannoksista etinyyliestradiolia (< 50 mikrogrammaa) sisältävää hormonaalista yhdistelmäehkäisyvalmistetta, jossa on mukana levonorgestreelia, noretisteronia tai norgestimaattia | Noin 5–7 naista 10 000:sta |
| Drovelis-tabletteja käyttävät naiset | Ei vielä tiedossa |
Laskimoveritulppariskiä lisäävät tekijät
Drovelis-valmisteen käyttöön liittyvä veritulppariski on pieni, mutta jotkin tilat tai sairaudet kasvattavat riskiä. Riski on kohdallasi suurempi:
- jos olet selvästi ylipainoinen (painoindeksi eli BMI yli 30 kg/m2)
- jos lähisukulaisellasi on nuorena (esimerkiksi alle 50-vuotiaana) ollut veritulppa jalassa, keuhkossa tai muussa elimessä. Siinä tapauksessa sinulla saattaa olla perinnöllinen verenhyytymishäiriö.
- jos joudut leikkaukseen tai olet vuodelevossa pidemmän aikaa vamman tai sairauden vuoksi tai jalkasi on kipsissä. Drovelis-valmisteen käyttö voidaan joutua keskeyttämään usean viikon ajaksi ennen leikkausta tai kun et pysty liikkumaan normaalisti. Kysy lääkäriltä, milloin voit aloittaa Drovelis-valmisteen käytön uudelleen.
- iän myötä (erityisesti 35 ikävuoden jälkeen)
- jos olet synnyttänyt muutaman viikon sisällä.
Veritulpan kehittymisen riski suurenee sen mukaan, kuinka monta riskitekijää sinulla on.
Lentomatkustaminen (yli 4 tunnin lento) voi väliaikaisesti suurentaa veritulppariskiä kohdallasi erityisesti silloin, jos jokin muista mainituista riskitekijöistä koskee sinua.
Vaikka olisit epävarma, on tärkeää kertoa lääkärille, jos jokin näistä tiloista koskee sinua. Lääkäri voi päättää, että Drovelis-valmisteen käyttö on lopetettava.
Kerro lääkärille, jos jossakin edellä mainituista tiloista tapahtuu muutos Drovelis-valmisteen käytön aikana, esimerkiksi lähisukulaisella on verisuonitukos, jonka syy on epäselvä, tai painosi nousee voimakkaasti.
VALTIMOTUKOKSET
Mitä voi tapahtua, jos valtimoon muodostuu veritulppa?
Laskimotukosten tavoin valtimotukokset voivat aiheuttaa vakavia ongelmia. Laskimotukos voi esimerkiksi aiheuttaa sydänkohtauksen tai halvauksen.
Valtimoveritulppariskiä kasvattavat tekijät
On tärkeää tietää, että Drovelis-valmisteen käyttöön liittyvä sydänkohtauksen tai aivohalvauksen riski on pieni, mutta riski suurenee:
- iän myötä (noin 35 ikävuoden jälkeen);
- jos tupakoit. Sinua neuvotaan lopettamaan tupakointi, jos käytät Drovelis-valmisteen kaltaista hormonaalista yhdistelmäehkäisyvalmistetta. Lääkäri kehottaa sinua käyttämään erityyppistä ehkäisyvalmistetta, jos et pysty lopettamaan tupakointia ja olet yli 35-vuotias.
- jos olet ylipainoinen
- sinulla on korkea verenpaine
- jos lähisukulaisellasi on ollut sydänkohtaus tai aivohalvaus nuorena (alle 50-vuotiaana). Siinä tapauksessa myös sinulla voi olla suurentunut sydänkohtauksen tai aivohalvauksen riski.
- jos sinun tai lähisukulaisesi veren rasvatasot ovat suuria (kolesteroli- tai triglyseriditasot)
- jos sinulla on migreeni, erityisesti aurallinen migreeni
- jos sinulla on sydänvaivoja (läppävika tai rytmihäiriö, jota kutsutaan eteisvärinäksi)
- jos sinulla on diabetes.
Jos sinulla on useampi kuin yksi näistä tiloista tai jokin niistä on erityisen vakava, veritulppariski voi kasvaa entisestään.
Kerro lääkärille, jos jossakin edellä mainituista tiloista tapahtuu muutos Drovelis-valmisteen käytön aikana, esimerkiksi aloitat tupakoinnin, lähisukulaisella on verisuonitukos, jonka syy on epäselvä, tai painosi nousee voimakkaasti.
Syöpä
Yhdistelmäehkäisytabletteja käyttävillä naisilla on todettu rintasyöpää hieman useammin, mutta ei tiedetä, onko syöpä yhteydessä ehkäisyhoitoon. On esimerkiksi mahdollista, että kasvaimia löydetään enemmän yhdistelmäehkäisytablettien käyttäjiltä, koska he käyvät useammin lääkärintarkastuksissa. Yhdistelmäehkäisytablettien käytön lopettamisen jälkeen tämä kohonnut rintasyövän riski pienenee vähitellen. On tärkeää, että tutkit rintasi säännöllisesti ja että otat yhteyttä lääkäriin, jos havaitset kyhmyn. Sinun on myös kerrottava lääkärille, jos läheisellä sukulaisellasi on tai on joskus ollut rintasyöpä (katso kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Varoitukset ja varotoimet”).
Harvoissa tapauksissa ehkäisytablettien käyttäjillä on todettu hyvänlaatuisia ja vielä harvemmin pahanlaatuisia maksakasvaimia. Ota yhteyttä lääkäriin, jos sinulla esiintyy epätavallista, vaikeaa vatsakipua.
Papilloomavirusinfektio (HPV) aiheuttaa kohdunkaulan syöpää. Sitä on todettu hieman enemmän naisilla, jotka ovat käyttäneet ehkäisytabletteja yli 5 vuotta. Ei tiedetä, johtuuko tämä hormoneita sisältävistä ehkäisyvalmisteista vai muista tekijöistä (kuten eroista sukupuolikäyttäytymisessä).
Psyykkiset häiriöt
Jotkut hormonaalisia ehkäisyvalmisteita, myös Drovelis-valmistetta, käyttävistä naisista ovat ilmoittaneet masennuksesta tai masentuneesta mielialasta. Masennus voi olla vakavaa ja aiheuttaa toisinaan myös itsetuhoisia ajatuksia. Jos koet mielialan muutoksia tai masennusoireita, ota mahdollisimman pian yhteyttä lääkäriin, jotta voit saada neuvontaa.
Verenvuoto kuukautisten välillä
Normaalisti kuukautisesi alkavat, kun otat Drovelis-pakkauksen valkoisia lumetabletteja. Drovelis-valmisteen ensimmäisten käyttökuukausien aikana voit kokea odottamatonta vuotoa (verenvuotoa lumepäivien ulkopuolella). Tämä vuoto on useimmiten heikkoa eikä yleensä vaadi kuukautissuojaa. Jos tällaista vuotoa ilmenee kauemmin kuin muutaman kuukauden ajan tai jos se alkaa muutaman käyttökuukauden kuluttua, lääkärin on selvitettävä tilannetta.
Mitä sinun on tehtävä, jos lumepäivinä ei tule vuotoa
Jos olet ottanut kaikki vaaleanpunaiset, vaikuttavaa ainetta sisältävät tabletit ohjeiden mukaisesti eikä sinulla ole ollut oksentelua tai voimakasta ripulia etkä ole käyttänyt muita lääkkeitä, on hyvin epätodennäköistä, että olisit raskaana. Jatka Drovelis-valmisteen käyttöä tavalliseen tapaan. Jos et ole ottanut kaikkia tabletteja oikein tai jos odotettua verenvuotoa ei ole tapahtunut kahden peräkkäisen kierron aikana, saatat olla raskaana. Ota välittömästi yhteyttä lääkäriin. Aloita seuraava levy vasta, kun olet varma, ettet ole raskaana. Ks. myös kohta Miten valmistetta käytetään ”Jos oksennat tai sinulla on vaikea ripuli” ja kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Muut lääkevalmisteet ja Drovelis”.
Lapset ja nuoret
Drovelis-valmiste on tarkoitettu käytettäväksi vasta ensimmäisten kuukautisten alkamisen jälkeen.
Muut lääkevalmisteet ja Drovelis
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan otat, olet äskettäin ottanut tai saatat ottaa muita lääkkeitä. Kerro myös muille sinulle lääkkeitä määrääville lääkäreille tai hammaslääkäreille (tai apteekkihenkilökunnalle), että käytät Drovelis-valmistetta. He osaavat kertoa, jos sinun pitää käyttää lisäehkäisyä (esim. kondomeja) ja kuinka pitkään lisäehkäisyä pitäisi jatkaa. He osaavat myös kertoa, jos jokin toinen käyttämistäsi lääkkeistä pitää vaihtaa.
Tietyt lääkkeet voivat vaikuttaa veren Drovelis-tasoon ja aiheuttaa sen raskautta ehkäisevän vaikutuksen heikkenemistä. Ne voivat myös aiheuttaa odottamatonta vuotoa. Tällaisia lääkkeitä ovat:
- epilepsialääkkeet (esim. barbituraatit, karbamatsepiini, fenytoiini, primidoni, felbamaatti, okskarbatsepiini, topiramaatti);
- tuberkuloosilääkkeet (esim. rifampisiini)
- HIV- ja Hepatiitti C -virusinfektiolääkkeet (eli HCV-lääkkeet, esim. niin kutsutut proteaasin estäjät ja ei-nukleosidiset käänteiskopioijan estäjät, kuten ritonaviiri, nevirapiini, efavirentsi);
- sieni-infektiolääkkeet (esim. griseofulviini);
- keuhkoverisuonten korkean verenpaineen hoitoon käytettävät lääkkeet (esim. bosentaani).
Myös mäkikuisma (Hypericum perforatum) saattaa keskeyttää Drovelis-valmisteen normaalin toiminnan. Jos haluat käyttää mäkikuismaa sisältäviä rohdosvalmisteita Drovelis-valmisteen käytön aikana, keskustele asiasta ensin lääkärin kanssa.
Jos käytät lääke- tai kasvirohdosvalmisteita, jotka saattavat vähentää Drovelis-tablettien tehoa, on sinun käytettävä myös lisäehkäisyä. Estemenetelmää on käytettävä koko samanaikaisen lääkehoidon ajan ja lisäksi 28 päivän ajan sen päättymisen jälkeen. Jos samanaikainen lääkehoito kestää kauemmin kuin käytössä olevan pakkauksen vaaleanpunaiset, vaikuttavaa ainetta sisältävät tabletit, valkoiset lumetabletit on hävitettävä ja seuraava tablettipakkaus on aloitettava heti
Jos pitkäkestoinen hoito yllämainituilla lääkkeillä on välttämätöntä, sinun on käytettävä ei-hormonaalista ehkäisymenetelmää. Kysy neuvoa lääkäriltäsi tai apteekista.
Drovelis saattaa vaikuttaa joidenkin muiden lääkkeiden tehoon, esim. seuraavien:
- syklosporiini (lääke, jota käytetään elinsiirtoleikkauksen jälkeisen kudoksen hyljinnän estämiseen);
- lamotrigiini (lääke, jota käytetään epilepsian hoitoon)
Hepatiitti C -viruksen (HCV) hoitoon tarkoitettu yhdistelmä ombitasviiri/paritapreviiri/ritonaviiri/dasabuviiri erillisenä hoitona tai yhdessä ribaviriinin kanssa sekä yhdistelmä glekapreviiri/pibrentasviiri tai yhdistelmä sofosbuviiri/velpatasviiri/voksilapreviiri voi nostaa maksan toimintaa mittaavien verikokeiden tuloksia (maksan ALAT-entsyymiarvo nousee) potilailla, jotka käyttävät etinyyliestradiolia sisältävää hormonaalista yhdistelmäehkäisyvalmistetta. Drovelis sisältää estetrolia etinyyliestradiolin asemasta. Ei ole tiedossa, nouseeko maksan ALAT-entsyymiarvo, kun Drovelis-tabletteja käytetään samanaikaisesti näiden HCV-yhdistelmähoitojen kanssa. Lääkäri antaa sinulle tästä lisätietoa.
Kysy lääkäriltä tai apteekista neuvoa ennen minkään lääkkeen käyttöä.
Laboratoriokokeet
Jos sinulle tehdään veri- tai virtsakokeita, kerro lääkärille, että käytät Drovelis-tabletteja, sillä ne voivat vaikuttaa joidenkin kokeiden tuloksiin.
Drovelis ruuan ja juoman kanssa
Tämä lääke voidaan ottaa ruoan kanssa tai ilman, tarvittaessa pienen vesimäärän kanssa.
Raskaus ja imetys
Älä ota tätä lääkettä raskauden aikana tai jos epäilet olevasi raskaana.
Jos tulet raskaaksi Drovelis-valmisteen käytön aikana, lopeta valmisteen käyttö välittömästi ja ota yhteys lääkäriin.
Jos haluat tulla raskaaksi, voit lopettaa Drovelis-valmisteen käytön milloin tahansa (ks. kohta Miten valmistetta käytetään. ”Jos lopetat Drovelis-tablettien ottamisen”).
Tämän lääkkeen käyttöä imetyksen aikana ei suositella. Jos haluat käyttää ehkäisytabletteja imetyksen aikana, kysy neuvoa lääkäriltä.
Ajaminen ja koneiden käyttö
Drovelis-valmisteella ei ole haitallista vaikutusta ajokykyyn ja koneidenkäyttökykyyn.
Drovelis sisältää laktoosia ja natriumia
Jos lääkäri on kertonut, että sinulla on jokin sokeri-intoleranssi, keskustele lääkärin kanssa ennen tämän lääkevalmisteen ottamista.
Vaaleanpunaiset, vaikuttavia aineita sisältävät tabletit sisältävät alle 1 mmol natriumia (23 mg) per tabletti eli sen voidaan sanoa olevan ”natriumiton”.
Miten valmistetta käytetään
Ota tätä lääkettä juuri siten kuin lääkäri on määrännyt tai apteekkihenkilökunta on neuvonut. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma.
Milloin ja miten tabletit otetaan
Läpipainopakkaus sisältää 28 kalvopäällysteistä tablettia: 24 vaikuttavia aineita sisältävää vaaleanpunaista tablettia (numerot 1–24) sekä 4 valkoista lumetablettia (numerot 25–28), jotka eivät sisällä vaikuttavia aineita.
Aloita uusi Drovelis-läpipainoliuska ottamalla vaaleanpunainen vaikuttavia aineita sisältävä tabletti numero 1 (ks. ”Aloita”). Valitse seitsemästä viikonpäivätarrasta se tarra, joka alkaa sillä viikonpäivällä, jona aloitat tablettien ottamisen. Jos aloitat tablettien ottamisen esimerkiksi keskiviikkona, valitse tarra, jossa on ensimmäisenä ”Ke”. Kiinnitä tarraliuska läpipainolevyn kohtaan, jossa on ”![]() ” -symboli. Kukin päivä osuu pilleririvin kohdalle. Näin sinun on helpompi tarkistaa, oletko ottanut kyseisen päivän tabletin.
” -symboli. Kukin päivä osuu pilleririvin kohdalle. Näin sinun on helpompi tarkistaa, oletko ottanut kyseisen päivän tabletin.
Ota tabletti joka päivä suunnilleen samaan aikaan, tarvittaessa pienen vesimäärän kanssa.
Noudata läpipainoliuskaan merkityn nuolen suuntaa ja ota ensin vaikuttavia aineita sisältävät vaaleanpunaiset tabletit ja sen jälkeen valkoiset lumetabletit.
Kuukautisesi alkavat niiden neljän päivän aikana, jolloin otat valkoisia lumetabletteja (ns. tyhjennysvuoto). Vuoto alkaa tavallisesti 2–4 päivää viimeisen vaikuttavia aineita sisältävän vaaleanpunaisen tabletin ottamisen jälkeen, eikä ole välttämättä loppunut ennen uuden läpipainoliuskan aloittamista.
Aloita tablettien ottaminen uudesta läpipainoliuskasta heti viimeisen valkoisen lumetabletin ottamisen jälkeen, vaikka kuukautisesi eivät olisi vielä loppuneet. Tämä tarkoittaa sitä, että aloitat uuden läpipainoliuskan aina samana viikonpäivänä ja että kuukautisesi alkavat joka kuukausi suunnilleen samana päivänä kuukaudessa.
Osalle käyttäjistä ei tule kuukautisia joka kuukausi valkoisten lumetablettien ottamisen aikana. Jos olet ottanut Drovelis-tabletteja joka päivä näiden ohjeiden mukaisesti, on epätodennäköistä, että olisit raskaana.
Ensimmäisen Drovelis-pakkauksen aloittaminen
Jos et ole käyttänyt hormonia sisältävää ehkäisyä viimeisen kuukauden kuluessa
Aloita Drovelis kuukautiskiertosi ensimmäisenä päivänä (eli kuukautistesi ensimmäisenä päivänä). Jos aloitat Drovelis-valmisteen käytön kuukautisten ensimmäisenä päivänä, raskauden ehkäisy toimii heti.
Voit aloittaa Drovelis-valmisteen käytön myös kuukautisten 2.–5. päivänä, mutta silloin sinun on käytettävä lisäehkäisyä (esim. kondomia) ensimmäisten 7 tabletin ottamispäivänä.
Vaihto hormonaalisesta yhdistelmäehkäisyvalmisteesta (yhdistelmäehkäisytabletti, emätinrengas tai ehkäisylaastari)
Voit aloittaa Drovelis-valmisteen käytön seuraavana päivänä siitä, kun olet ottanut edellisten tablettien viimeisen vaikuttavia aineita sisältävän tabletin. Voit aloittaa sen käytön myös edellisen valmisteen tabletittomina päivinä (tai viimeisenä lumetablettipäivänä). Kun vaihdat ehkäisyrenkaasta tai ehkäisylaastarista (yhdistelmäehkäisystä) Drovelis-valmisteeseen, noudata lääkärin ohjeita.
Vaihto pelkkää progestiinia sisältävästä ehkäisyvalmisteesta (vain progestogeenia sisältävä pilleri, implantaatti, injektio tai hormonia vapauttavasta kohdunsisäisestä ehkäisimestä)
Progestogeenipillereistä voidaan siirtyä käyttämään Drovelis-tabletteja koska tahansa. Implantaatti tai hormonia vapauttava kohdunsisäinen ehkäisin voidaan poistaa minä päivänä tahansa, jolloin Drovelis-tablettien käyttö aloitetaan poistopäivänä, ehkäisyinjektion tapauksessa tablettien ottaminen aloitetaan seuraavana suunniteltuna injektiopäivänä. Kaikissa näissä tapauksissa on käytettävä lisäksi estemenetelmää, kunnes läpipainopakkauksesta on käytetty keskeytyksettä 7 tablettia.
Keskenmenon tai raskaudenkeskeytyksen jälkeen
Noudata lääkärin ohjeita.
Synnytyksen jälkeen
Voit aloittaa Drovelis-tablettien käytön 21–28 päivää synnytyksen jälkeen. Jos aloitat tablettien käytön myöhemmin kuin päivänä 28, käytä lisäehkäisynä estemenetelmää seitsemänä ensimmäisenä Drovelis-valmisteen käyttöpäivänä. Jos olet synnyttänyt ja olet ollut yhdynnässä ennen Drovelis-valmisteen käytön aloittamista, varmista, ettet ole raskaana, tai odota seuraaviin kuukautisiin saakka.
Jos haluat aloittaa Drovelis-tablettien käytön synnytyksen jälkeen imetyksen aikana
Lue kohta ”Imetys”.
Kysy neuvoa lääkäriltä, jos et ole varma, milloin voit aloittaa tablettien käytön.
Jos otat enemmän Drovelis-valmistetta kuin sinun pitäisi
Drovelis-tablettien yliannostuksen yhteydessä ei ole raportoitu vakavia haittavaikutuksia.
Usean tabletin ottaminen samanaikaisesti voi aiheuttaa pahoinvointia, oksentelua ja verenvuotoa emättimestä. Tällaista vuotoa voi esiintyä jopa nuorilla tytöillä ennen kuukautisten alkamista, jos he ottavat tätä lääkevalmistetta vahingossa.
Jos olet ottanut liian monta Drovelis-tablettia tai huomaat, että lapsi on ottanut tabletteja, kysy neuvoa lääkäriltä tai apteekista.
Jos unohdat ottaa Drovelis-tabletin
Liuskan 4 viimeistä tablettia ovat lumetabletteja. Jos yksi näistä tableteista jää ottamatta, sillä ei ole vaikutusta Drovelis-valmisteen tehoon. Heitä unohtunut valkoinen lumetabletti pois.
Jos sinulta unohtuu vaaleanpunainen, vaikuttavia aineita sisältävä tabletti (läpipainolevyn tabletit 1–24), toimi seuraavasti:
- Jos vaaleanpunaisen, vaikuttavia aineita sisältävän tabletin unohtamisesta on kulunut alle 24 tuntia, valmisteen ehkäisyteho ei ole heikentynyt. Ota tabletti heti, kun se on mahdollista, ja ota seuraavat tabletit tavanomaiseen aikaan.
- Jos vaaleanpunaisen, vaikuttavia aineita sisältävän tabletin unohtamisesta on kulunut yli 24 tuntia, valmisteen ehkäisyteho saattaa olla heikentynyt. Mitä suurempi määrä tabletteja on jäänyt ottamatta, sitä suurempi on riski tulla raskaaksi.
Raskaaksi tulemisen riski on suurempi, jos unohdat ottaa vaikuttavia aineita sisältäviä vaaleanpunaisia tabletteja läpipainoliuskan alku- tai loppupäästä. Siksi sinun on pidettävä mielessä seuraavat säännöt (katso myös kaavio):
Tästä liuskasta on unohtunut ottaa useampi kuin yksi tabletti
Ota yhteys lääkäriin.
Yksi vaaleanpunainen, vaikuttavia aineita sisältävä tabletti unohtui päivien 1–7 välisenä aikana
Ota unohtunut tabletti mahdollisimman pian, vaikka tällöin olisikin otettava kaksi tablettia samalla kertaa. Jatka tablettien ottamista normaalisti ja käytä lisäehkäisyä, esimerkiksi kondomia, seuraavien 7 päivän ajan, jolloin otat tabletteja oikea-aikaisesti. Jos olet ollut yhdynnässä tabletin unohtamista edeltävällä viikolla, on huomattava, että raskauden riski on olemassa. Ota tällaisessa tapauksessa yhteys lääkäriin.
Yksi vaaleanpunainen, vaikuttavia aineita sisältävä tabletti on unohtunut päivien 8–17 välisenä aikana
Ota unohtunut tabletti mahdollisimman pian, vaikka tällöin olisikin otettava kaksi tablettia samalla kertaa. Jatka seuraavien tablettien ottamista tavanomaiseen aikaan. Raskautta ehkäisevä vaikutus ei ole vähentynyt eikä sinun tarvitse käyttää lisäehkäisyä.
Yksi vaaleanpunainen, vaikuttavia aineita sisältävä tabletti unohtui päivien 18–24 välisenä aikana
Voit valita kahdesta vaihtoehdosta:
- Ota unohtunut tabletti mahdollisimman pian, vaikka tällöin olisikin otettava kaksi tablettia samalla kertaa. Jatka seuraavien tablettien ottamista tavanomaiseen aikaan. Valkoisten lumetablettien ottamisen sijaan heitä ne pois ja aloita uusi liuska (jolloin aloituspäiväsi vaihtuu).
Sinulla on kuukautiset todennäköisimmin toisen liuskan lopussa, kun otat valkoisia lumetabletteja, mutta sinulla voi olla lievää tai kuukautistyyppistä verenvuotoa myös toisen liuskan ottamisen aikana.
- Voit myös lopettaa vaaleanpunaisten, vaikuttavia aineita sisältävien tablettien ottamisen ja siirtyä suoraan ottamaan liuskan 4 valkoista lumetablettia. Ennen kuin otat valkoisia lumetabletteja, kirjaa muistiin päivä, jona unohdit tabletin. Lumejakso ei saa kestää yli 4:ää päivää. Jos haluat aloittaa uuden liuskan samana aloituspäivänä kuin ennenkin, voit ottaa valkoisia lumetabletteja alle neljänä päivänä.
Jos seuraat jompaa kumpaa näistä ohjeista, raskauden ehkäisy toimii edelleen.
Jos olet unohtanut jonkun liuskan tableteista etkä saa vuotoa lumetablettipäivinä, tämä voi tarkoittaa, että olet raskaana. Tällöin sinun on otettava yhteys lääkäriin ennen seuraavan liuskan aloittamista.
Jos vaaleanpunaisen, vaikuttavia aineita sisältävän tabletin unohtamisesta on kulunut yli 24 tuntia
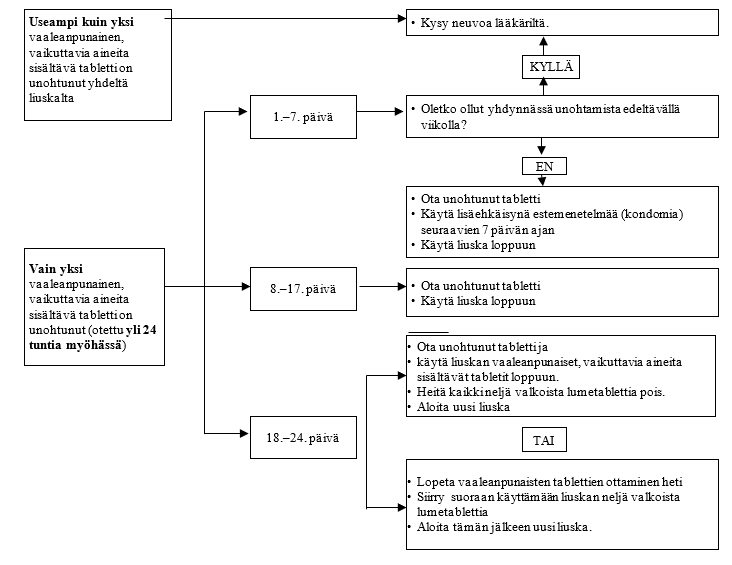
Tästä liuskasta on unohdettu ottaa useampi kuin yksi tabletti
Noudata lääkärin ohjeita.
Jos oksennat tai sinulla on vaikea ripuli
Jos olet oksentanut 3–4 tunnin kuluessa vaaleanpunaisen, vaikuttavia aineita sisältävän tabletin ottamisesta tai jos sinulla on vaikea ripuli, on mahdollista, että tabletin vaikuttavat aineet eivät ole täysin imeytyneet kehoosi. Tilanne on lähes sama, kuin jos tabletti olisi jäänyt ottamatta. Oksentelun tai ripulin jälkeen sinun on mahdollisimman pian otettava toinen vaaleanpunainen, vaikuttavia aineita sisältävä tabletti varalla olevasta läpipainoliuskasta. Ota se mahdollisuuksien mukaan 24 tunnin kuluessa tabletin normaalista ottoajankohdasta. Mikäli tämä ei ole mahdollista tai aikaa on jo kulunut vähintään 24, noudata kohdan "Jos unohdat ottaa Drovelis-tabletin” ohjeita.
Kuukautisten siirtäminen: tärkeää tietoa
Vaikka kuukautisten siirtämistä ei suositella, se on kuitenkin mahdollista jättämällä neljännen rivin valkoiset lumetabletit ottamatta ja siirtymällä suoraan uuteen Drovelis-liuskaan ja käyttämällä sen loppuun. Sinulla voi esiintyä vähäistä tai kuukautisten kaltaista vuotoa toisen läpipainoliuskan käytön aikana. Lopeta tämä toinen liuska ottamalla sen neljä valkoista lumetablettia tavalliseen tapaan. Aloita tämän jälkeen uusi liuska. Kysy neuvoa lääkäriltä ennen kuin päätät siirtää kuukautisiasi.
Jos haluat muuttaa kuukautistesi alkamispäivää
Jos käytät tabletteja ohjeiden mukaisesti, kuukautisesi alkavat lumetablettien ottamisen aikana. Jos haluat muuttaa kuukautisten alkamispäivää, voit lyhentää lumejaksoa eli valkoisten lumetablettien käyttöjaksoa, mutta et koskaan pidentää sitä (4 lumetablettia on aina enimmäismäärä). Jos aloitat valkoisten lumetablettien ottamisen esimerkiksi perjantaina ja haluat siirtää lumetabletin ottamisen alkamaan tiistaina (3 päivää aikaisemmaksi), aloita uusi läpipainoliuska kolme päivää tavanomaista aikaisemmin. Sinulle ei välttämättä tule vuotoa valkoisten lumetablettien lyhennetyn käyttöjakson aikana. Sinulla voi kuitenkin esiintyä tiputtelua (veripisaroita tai -pilkkuja) tai läpäisyvuotoa seuraavan läpipainoliuskan vaikuttavia aineita sisältävien, vaaleanpunaisten tablettien ottamisen aikana.
Jos et ole varma, miten sinun tulisi toimia, keskustele lääkärin kanssa tai kysy lisätietoja apteekista.
Jos lopetat Drovelis-valmisteen oton
Voit lopettaa Drovelis-valmisteen käytön milloin tahansa. Jos et halua tulla raskaaksi, kysy lääkäriltä muista ehkäisymenetelmistä.
Jos lopetat Drovelis-tablettien käytön siksi, että haluat tulla raskaaksi, on parasta odottaa ensimmäisten luonnollisten kuukautisten tuloa ennen kuin yrität tulla raskaaksi. Tämä helpottaa synnytyksen ajankohdan määrittämistä.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa. Kerro lääkärille, jos sinulla ilmenee haittavaikutuksia, erityisesti jos ne ovat voimakkaita ja jatkuvia, tai jos terveydentilassasi tapahtuu muutoksia, joiden arvelet voivan liittyä Drovelis-valmisteen käyttöön.
Kaikilla hormonaalisia yhdistelmäehkäisyvalmisteita käyttävillä naisilla on suurentunut laskimoveritulppien tai valtimoveritulppien riski. Katso lisätietoja hormonaalisen yhdistelmäehkäisyvalmisteen käyttöön liittyvistä erilaisista riskeistä kohdasta Mitä sinun on tiedettävä ennen valmisteen käyttöä
Drovelis-valmisteen käyttöön on liittynyt seuraavia haittavaikutuksia:
Yleiset (voivat esiintyä enintään yhdellä henkilöllä 10:stä)
- mielialahäiriöt, libidon häiriöt
- päänsärky
- vatsakipu, pahoinvointi
- akne
- kipu rinnoissa, kivuliaat kuukautiset, emätinverenvuoto (kuukautisten aikana tai niiden ulkopuolella, runsasta epäsäännöllistä verenvuotoa)
- painon vaihtelu.
Melko harvinainen (voivat esiintyä enintään yhdellä henkilöllä 100:sta)
- sieni-infektio, emätininfektio, virtsatieinfektio
- ruokahalun muutokset (ruokahalun häiriöt)
- masennus, tunnehäiriö, ahdistuneisuushäiriö, stressi, uniongelmat
- migreeni, huimaus, pistely, uneliaisuus
- kuumat aallot
- vatsan turpoaminen, oksentelu, ripuli
- hiustenlähtö, runsas hikoilu, kuiva iho, ihottuma, ihon turpoaminen
- selkäkipu
- rintojen turpoaminen, kyhmyt rinnoissa, epänormaali verenvuoto sukuelimistä, yhdyntäkivut, maitorauhasen rakkulatauti (rinnoissa yksi tai useampi kysta), runsas kuukautisvuoto, ei kuukautisvuotoa, kuukautishäiriöt, kuukautisia edeltävä oireyhtymä (PMS), kohdun kouristelu, verenvuoto kohdusta tai emättimestä (myös tiputtelu), emätinvuoto, ulkosynnyttimien häiriö (kuivuus, kipu, haju, epämukavuus)
- väsymys, turvotus eri puolilla kehoa, esim. nilkat (ödeema), rintakivut, epänormaaliuden tunne
- verikokeissa maksaentsyymipitoisuuksien nousu, muutokset tietyissä rasvoissa (lipideissä).
Harvinainen: (voivat esiintyä enintään yhdellä henkilöllä 1 000:sta)
- rintojen tulehdus
- hyvänlaatuinen massa rinnoissa
- yliherkkyys (allergia)
- nesteen kertyminen elimistöön, veren kohonneet kaliumpitoisuudet
- hermostuneisuus
- unohtelevaisuus
- silmien kuivuminen, näön hämärtyminen, näön heikkeneminen
- pyörrytys
- kohonnut tai matala verenpaine, verisuonitulehdus ilman veritulpan muodostumista (tromboflebiitti), suonikohjut
- ummetus, suun kuivuus, ruoansulatushäiriöt, huulten turvotus, ilmavaivat, suolen tulehdus, närästys (refluksitauti), epänormaalit suolen supistukset
- allergiset ihoreaktiot, maksaläiskät ja muut pigmenttihäiriöt, miestyyppinen karvan kasvu, runsas karvankasvu, ihosairaudet, kuten dermatiitti, kutiseva dermatiitti, hilse ja rasvainen iho (seborrea) ja muut ihotaudit
- lihasten kouristukset ja nivelten turvotus, kivut ja vaivat
- kipu virtsateissä, epänormaali haju virtsassa
- kohdun ulkopuolinen raskaus
- munasarjakysta, kasvanut spontaani maidon virtaus, lantion alueen kipu, rintojen värimuutokset, verenvuotoa yhdynnässä, kohdun limakalvon häiriöt, nännin häiriöt, epänormaali kohdun verenvuoto
- huonovointisuus ja yleinen huono olo, kehon lämpötilan nousu, kipu
- verenpaineen nousu, muutokset verikokeissa (epänormaalit munuaisten toimintakokeet, veren kohonnut kaliumpitoisuus, kohonnut verensokeri, hemoglobiinitason laskeminen, pienentyneet rautavarastot veressä, verta virtsassa)
- haitalliset veritulpat laskimossa, esimerkiksi:
- jalassa tai jalkaterässä (syvä laskimotukos)
- keuhkossa (keuhkoembolia)
- sydänkohtaus
- aivohalvaus
- pienet, väliaikaiset aivohalvauksen kaltaiset oireet, joita kutsutaan ohimeneväksi aivoverenkiertohäiriöksi
- veritulpat maksassa, mahassa/suolistossa, munuaisissa tai silmässä.
Veritulpan kehittymisen riski voi olla suurempi, jos sinulla on jokin muu tila, joka suurentaa tätä riskiä (ks. kohdasta Mitä sinun on tiedettävä ennen valmisteen käyttöä Lisätietoja veritulpan oireista ja tiloista, jotka suurentavat veritulppariskiä).
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa ja läpipainopakkauksessa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Tämä lääke ei vaadi erityisiä säilytysolosuhteita.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Drovelis sisältää
Vaikuttavat aineet ovat drospirenoni ja estetroli.
Yhdessä vaaleanpunaisessa, vaikuttavia aineita sisältävässä tabletissa on 3 mg drospirenonia ja 14,2 mg estetrolia vastaava määrä estetrolimonohydrattia.
Valkoiset kalvopäällysteiset lumelääketabletit eivät sisällä vaikuttavia aineita.
Muut apuaineet ovat:
Vaaleanpunaiset kalvopäällysteiset tabletit
Tabletin ydin
Laktoosimonohydraatti (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Drovelis sisältää laktoosia ja natriumia”), natriumtärkkelysglykolaatti (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Drovelis sisältää laktoosia ja natriumia”), maissitärkkelys, povidoni K30, magnesiumstearaatti (E470b).
Tabletin päällyste
Hypromelloosi (E464), hydroksipropyyliselluloosa (E463), talkki (E553b), puuvillansiemenöljy, hydrattu, titaanidioksidi (E171), punainen rautaoksidi (E172).
Valkoiset kalvopäällysteiset lumetabletit
Tabletin ydin
Laktoosimonohydraatti (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä ”Drovelis sisältää laktoosia ja natriumia”), maissitärkkelys, magnesiumstearaatti (E470b).
Tabletin päällyste
Hypromelloosi (E464), hydroksipropyyliselluloosa (E463), talkki (E553b), puuvillansiemenöljy, hydrattu, titaanidioksidi (E171).
Drovelis-valmisteen kuvaus ja pakkauskoko (-koot)
Vaikuttavaa ainetta sisältävät kalvopäällysteiset tabletit ovat vaaleanpunaisia, pyöreitä, läpimitaltaan 6 mm, kaksoiskuperia ja niissä pisaranmuotoinen logo kohokuviona toisella puolella.
Kalvopäällysteiset lumetabletit ovat valkoisia tai valkeahkoja pyöreitä, läpimitaltaan 6 mm, kaksoiskuperia ja niissä pisaranmuotoinen logo kohokuvana toisella puolella.
Drovelis-valmistetta on saatavana 28 kalvopäällysteisen tabletin läpipainoliuskoja (24 vaikuttavaa ainetta sisältävää, vaaleanpunaista tablettia ja 4 valkoista lumetablettia) sisältävinä pakkauksina. Läpipainolevyjen lisäksi Drovelis-kotelo sisältää säilytyspussin ja 1, 3, 6, tai 13 viikonpäivätarraa. Viikonpäivätarrojen lukumäärä riippuu läpipainolevyjen lukumäärästä.
Pakkauskoot: 28 (1 × 28), 84 (3 × 28), 168 (6 × 28) tai 364 (13 × 28) kalvopäällysteistä tablettia.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija
Gedeon Richter Plc.
Gyömrői út 19-21.
1103 Budapest
Unkari
Valmistaja
Haupt Pharma Münster GmbH
Schleebrüggenkamp 15
48159 Münster
Saksa
Gedeon Richter Plc.
Gyömrői út 19-21.
1103 Budapest
Unkari
Tämä pakkausseloste on tarkistettu viimeksi 10.03.2026
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla https://www.ema.europa.eu.