ADYNOVI pulver och vätska till injektionsvätska, lösning 1000 IU, 2000 IU
Tilläggsinformation
ADYNOVI 250 IE/2 ml pulver och vätska till injektionsvätska, lösning
ADYNOVI 500 IE/2 ml pulver och vätska till injektionsvätska, lösning
ADYNOVI 1 000 IE/2 ml pulver och vätska till injektionsvätska, lösning
ADYNOVI 250 IE/5 ml pulver och vätska till injektionsvätska, lösning
ADYNOVI 500 IE/5 ml pulver och vätska till injektionsvätska, lösning
ADYNOVI 1 000 IE/5 ml pulver och vätska till injektionsvätska, lösning
ADYNOVI 2 000 IE/5 ml pulver och vätska till injektionsvätska, lösning
ADYNOVI 3 000 IE/5 ml pulver och vätska till injektionsvätska, lösning
rurioktokog alfa pegol (pegylerad rekombinant human koagulationsfaktor VIII)
Utökad övervakning
![]() Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar du eventuellt får. Information om hur du rapporterar biverkningar finns i slutet av avsnitt Eventuella biverkningar.
Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar du eventuellt får. Information om hur du rapporterar biverkningar finns i slutet av avsnitt Eventuella biverkningar.
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad ADYNOVI är och vad det används för
2. Vad du behöver veta innan du använder ADYNOVI
3. Hur du använder ADYNOVI
4. Eventuella biverkningar
5. Hur ADYNOVI ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
ADYNOVI innehåller den aktiva substansen rurioktokog alfa pegol, pegylerad human koagulationsfaktor VIII. Den humana koagulationsfaktorn VIII har modifierats för att den ska verka under längre tid. Faktor VIII behövs för att blodet ska kunna koagulera och stoppa blödningar. Hos patienter med hemofili A (medfödd brist på faktor VIII) saknas faktor VIII, eller så fungerar det inte normalt.
ADYNOVI används för att behandla och förebygga blödningar hos patienter från 12 års ålder med hemofili A (en ärftlig form av blödarsjuka som orsakas av brist på faktor VIII).
Vad du behöver veta innan produkten används
Använd inte ADYNOVI:
- om du är allergisk mot rurioktokog alfa pegol, oktokog alfa eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar)
- om du är allergisk mot mus- eller hamsterproteiner.
Rådfråga läkare om du är osäker.
Varningar och försiktighet
Det är viktigt att du håller reda på batchnumret för ADYNOVI. Varje gång du får en ny förpackning ADYNOVI, anteckna datum och batchnummer (som står på förpackningen efter Lot) på en säker plats.
Tala med läkare innan du använder ADYNOVI.
Det finns en liten risk att du kan få en anafylaktisk reaktion (en allvarlig, plötslig allergisk reaktion) när du använder ADYNOVI. Du bör känna till de tidiga tecknen på allergiska reaktioner såsom utslag, nässelutslag, allmän klåda, svullnad av läppar och tunga, andningssvårighet, väsande andning, tryck över bröstet, allmän sjukdomskänsla och yrsel. Dessa kan vara tidiga symtom på anafylaktisk chock. Andra symtom kan vara svår yrsel, medvetslöshet och extrem andningssvårighet.
Om något av dessa symtom inträffar ska du omedelbart avbryta injektionen och kontakta läkare. Allvarliga symtom, inklusive andningssvårighet och att du (nästan) svimmar, kräver omedelbar akut behandling.
Om du lider av en hjärtsjukdom ska du informera din läkare om detta, eftersom det finns en ökad risk för komplikationer som rör koagulationen (blodets förmåga att levra sig).
Patienter som utvecklar faktor VIII-inhibitorer
Utveckling av inhibitorer (antikroppar) är en känd komplikation som kan uppträda vid behandling med alla faktor VIII-läkemedel. Inhibitorerna förhindrar att behandlingen fungerar som den ska, särskilt vid höga halter. Du eller ditt barn kommer att övervakas noggrant avseende utveckling av inhibitorer. Om du eller ditt barn drabbas av en blödning som inte kan fås under kontroll med ADYNOVI ska du omedelbart tala om det för din läkare.
Komplikationer relaterade till kateter
Om du behöver en central venkateter (CVAD) ska läkaren överväga risken för CVAD-relaterade komplikationer, bland annat lokala infektioner, förekomst av bakterier i blodet och blodpropp på kateterstället.
Barn och ungdomar
ADYNOVI kan endast användas hos ungdomar och vuxna (12 år och äldre). Informationen om varningar och försiktighet gäller också ungdomar.
Andra läkemedel och ADYNOVI
Tala om för läkare om du använder, nyligen har använt eller kan tänkas använda andra läkemedel.
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare innan du använder detta läkemedel. Hemofili A är sällsynt hos kvinnor. Därför finns det ingen erfarenhet av användning av ADYNOVI under graviditet och amning.
Körförmåga och användning av maskiner
ADYNOVI har ingen eller försumbar effekt på förmågan att framföra fordon och använda maskiner.
ADYNOVI innehåller natrium
ADYNOVI innehåller upp till 12,42 mg natrium (den huvudsakligea beståndsdelen i koksalt/bordssalt) per injektionsflaska. Detta motsvarar 0,62 % av det rekommenderade högsta dagliga intaget för vuxna. Beroende på din kroppsvikt och dosering av ADYNOVI kan du tilldelas mer än en flaska. Detta måste beaktas om du äter en kost med reducerat saltintag.
Hur produkten används
Behandlingen med ADYNOVI kommer att påbörjas och övervakas av läkare, som har erfarenhet av behandling av patienter med hemofili A.
Din läkare beräknar vilken dos av ADYNOVI som passar dig beroende på ditt tillstånd, din vikt samt om det används för att förebygga eller behandla blödning. Hur ofta behandlingen ges beror på hur väl ADYNOVI fungerar för dig. Ersättningsbehandling med ADYNOVI är vanligen en livslång behandling.
Använd alltid detta läkemedel enligt läkarens anvisningar. Fråga din läkare om du är osäker.
Förebyggande mot blödningar
Den vanliga dosen av ADYNOVI är 40 till 50 IE per kg kroppsvikt som administreras 2 gånger per vecka.
Behandling av blödning
Dosen av ADYNOVI beräknas utifrån din kroppsvikt och vilka faktor VIII-nivåer som ska uppnås. Målnivåerna för faktor VIII beror på hur allvarlig blödningen är och var den uppstår.
Tala med läkare om du tror att effekten av ADYNOVI inte är tillräcklig.
Din läkare kommer att utföra lämpliga laboratorietester för att se till att du har rätt faktor VIII-nivå. Detta är särskilt viktigt om du ska genomgå en större operation.
Användning för barn och ungdomar
ADYNOVI kan endast användas för ungdomar och vuxna (12 år och äldre). Dosen för ungdomar beräknas också efter kroppsvikt och är densamma som för vuxna.
Hur ADYNOVI ges
ADYNOVI injiceras vanligtvis i en ven (intravenöst) av en läkare eller sjuksköterska. Du själv eller någon annan kan också administrera ADYNOVI som en injektion, men bara efter nödvändig utbildning. Detaljerade instruktioner för hur man ger sig själv läkemedlet finns i slutet av denna bipacksedel.
Om du har använt för stor mängd av ADYNOVI
Använd alltid ADYNOVI enligt anvisningar från läkare. Rådfråga läkare om du är osäker. Om du har injicerat mer ADYNOVI än vad som rekommenderas, tala med din läkare snarast möjligt.
Om du har glömt att använda ADYNOVI
Ta inte dubbel dos för att kompensera för glömd dos. Ta nästa dos som planerat och fortsätt enligt läkares föreskrift.
Om du slutar att använda ADYNOVI
Sluta inte använda ADYNOVI utan att rådfråga din läkare.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Vid en allvarlig och plötslig allergisk reaktion (anafylaktisk chock) måste injektionen avbrytas omedelbart. Om du får något av följande tidiga symtom på en allergisk reaktion måste du omedelbart kontakta läkare:
- utslag, nässelutslag, allmän klåda
- svullnad av läppar och tunga
- andningssvårigheter, väsande andning, tryck över bröstet
- allmän sjukdomskänsla
- yrsel och medvetslöshet.
Allvarliga symtom, inklusive andningssvårighet och att du (nästan) svimmar, kräver omedelbar akut behandling.
Hos patienter som tidigare har behandlats med faktor VIII (mer än 150 dagars behandling) kan hämmande antikroppar (inhibitorer) bildas (se avsnitt Vad du behöver veta innan produkten används). Denna komplikation klassas som mindre vanlig (förekommer hos färre än 1 av 100 användare). Om detta inträffar kan din läkemedelsbehandling sluta att fungera som den ska, och du kan få ihållande blödningar. Kontakta läkare omedelbart om detta händer.
Mycket vanliga biverkningar (kan förekomma hos fler än 1 av 10 personer)
Huvudvärk
Vanliga biverkningar (kan förekomma hos upp till 1 av 10 personer)
Illamående
Diarré
Utslag
Yrsel
Nässelutslag
Mindre vanliga biverkningar (kan förekomma hos upp till 1 av 100 personer)
Rodnad, allergisk reaktion (överkänslighet)
Antikroppar (inhibitorer) mot faktor VIII (hos patienter som har fått tidigare behandling med faktor VIII (mer än 150 dagars behandling))
Förhöjda nivåer av vissa typer av vita blodkroppar
Infusionsreaktion
Röda ögon
Hudreaktioner
Biverkningar med okänd frekvens (kan inte beräknas från tillgängliga data)
Potentiellt livshotande reaktioner (anafylaxi)
Ytterligare biverkningar hos barn
Biverkningarnas frekvens, typ och allvarlighetsgrad hos barn förväntas vara desamma som hos vuxna.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
Webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på etiketten och kartongen efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras i kylskåp (2 °C–8 °C).
Får ej frysas.
Förvara injektionsflaskan i ytterkartongen. Ljuskänsligt.
Under hållbarhetstiden kan injektionsflaskan med pulver förvaras i rumstemperatur (upp till 30 °C) under en sammanhängande period på högst 3 månader. Utgångsdatum för läkemedlet är då slutet av denna 3-månadersperiod, alternativt det utgångsdatum som står tryckt på injektionsflaskan, beroende på vilket som infaller tidigast. Notera slutdatumet för 3-månadersperioden på ytterkartongen. Läkemedlet får inte förvaras i kylskåp efter att det har förvarats i rumstemperatur. Lösningen får inte förvaras i kylskåp efter beredningen.
Använd läkemedlet inom 3 timmar efter att pulvret har lösts upp helt.
Läkemedlet är endast för engångsbruk. Kassera överbliven lösning på lämpligt sätt.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är rurioktokog alfa pegol (pegylerad human koagulationsfaktor VIII framställd med rekombinant DNA-teknik). Varje injektionsflaska med pulver innehåller nominellt 250, 500, 1 000, 2 000 eller 3 000 IE rurioktokog alfa pegol.
- Injektionsflaskan med lösningsvätska innehåller 2 / 5 ml vatten för injektionsvätskor.
- Övriga innehållsämnen är mannitol, trehalosdihydrat, histidin, glutation, natriumklorid, kalciumkloriddihydrat, tris(hydroximetyl)aminometan och polysorbat 80. Se avsnitt Vad du behöver veta innan produkten används ”ADYNOVI innehåller natrium”.
Läkemedlets utseende och förpackningsstorlekar
ADYNOVI tillhandahålls som ett pulver och vätska till injektionsvätska, lösning (pulver för injektionsvätska, lösning). Pulvret är ett vitt till benvitt kornigt pulver. Lösningsvätskan är en klar och färglös lösning. Efter beredningen är lösningen klar, färglös och fri från främmande partiklar.
Varje förpackning innehåller en injektionsflaska med pulver, en injektionsflaska med lösningsvätska och en beredningsanordning (BAXJECT II Hi‑Flow).
Innehavare av godkännande för försäljning
Baxalta Innovations GmbH
Industriestrasse 67
A-1221 Wien
Tillverkare
Baxalta Belgium Manufacturing SA
Boulevard René Branquart 80
B‑7860 Lessines
Belgien
Denna bipacksedel ändrades senast 07/2023
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats http://www.ema.europa.eu/
För information om detta läkemedel, vänligen kontakta den lokala representanten för innehavaren av godkännandet för försäljning:
Takeda Oy
Tel: 0800 774 051
medinfoEMEA@takeda.com
Instruktioner för beredning och administrering
ADYNOVI får inte blandas med andra läkemedel eller lösningsvätskor.
Det rekommenderas starkt att läkemedlets namn och batchnummer antecknas varje gång ADYNOVI ges. Avtagbara etiketter finns på blisterförpackningen.
Anvisningar för beredning
Injektionsflaska
- Används före utgångsdatumet som anges på etiketterna och kartongen.
- Använd inte om BAXJECT II Hi-Flow-anordningen, sterilskyddet eller förpackningen är skadad eller visar tecken på försämring.
- Använd aseptisk teknik (mycket rena förhållanden) och en plan arbetsyta vid beredning.
- Injektionsflaskorna med pulver och lösningsvätska ska vara rumstempererade (mellan 15 °C och 25 °C) innan de används.
- Ta bort plastlocken från injektionsflaskorna med pulver och lösningsvätska.
- Rengör gummipropparna med en alkoholtork och låt torka före användning.
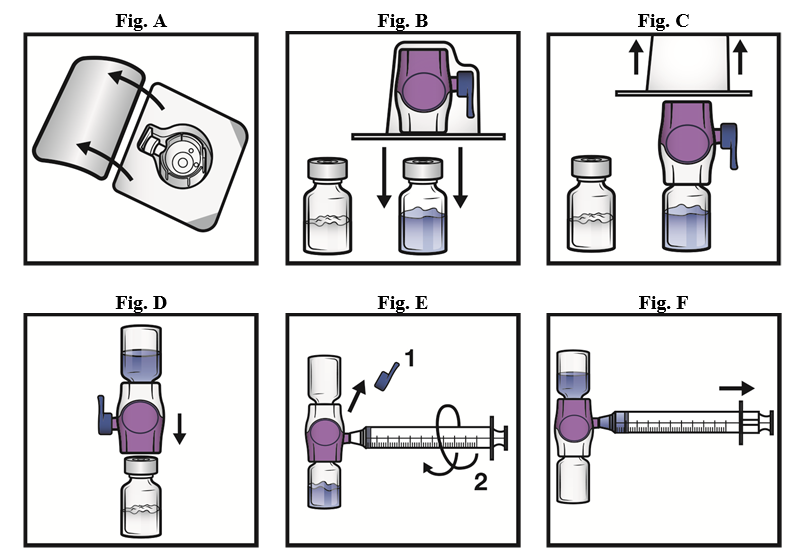
- Öppna förpackningen med BAXJECT II Hi‑Flow-anordningen genom att dra bort ovansidan utan att vidröra insidan (Fig. A). Ta inte ut anordningen ur förpackningen.
- Vänd på förpackningen. Tryck rakt ned för att föra in den genomskinliga plastspetsen helt genom proppen i injektionsflaskan med lösningsvätska (Fig. B).
- Ta tag i kanten av BAXJECT II Hi‑Flow-förpackningen och dra bort förpackningen från anordningen (Fig. C). Ta inte bort det blå locket från BAXJECT II Hi‑Flow-anordningen. Vidrör inte den exponerade lila plastspetsen.
- Vänd på systemet så att flaskan med lösningsvätska hamnar överst. För snabbt in den lila plastspetsen helt genom proppen på injektionsflaskan med pulver genom att trycka rakt ned (Fig. D). Vakuumet drar in lösningsvätskan i injektionsflaskan med pulver.
- Snurra försiktigt tills pulvret har lösts upp helt. Får inte förvaras i kylskåp efter beredningen.
Injektionsflaska med pulver
- Används före utgångsdatumet som anges på etiketterna och kartongen.
- Använd inte om inte locket på blistret är helt förslutet
- Lösningen får inte förvaras i kylskåp efter beredningen.
- Om läkemedlet fortfarande förvaras i kylskåp: ta det förslutna blistret (som innehåller injektionsflaskor med pulver och lösningsvätska ihopsatta med beredningssystemet) ur kylskåpet och låt det uppnå rumstemperatur (mellan 15 °C och 25 °C).
- Tvätta händerna noggrant med tvål och varmt vatten.
- Öppna blisterförpackningen med ADYNOVI genom att dra av ovansidan. Ta ut BAXJECT III-systemet ur blistret.
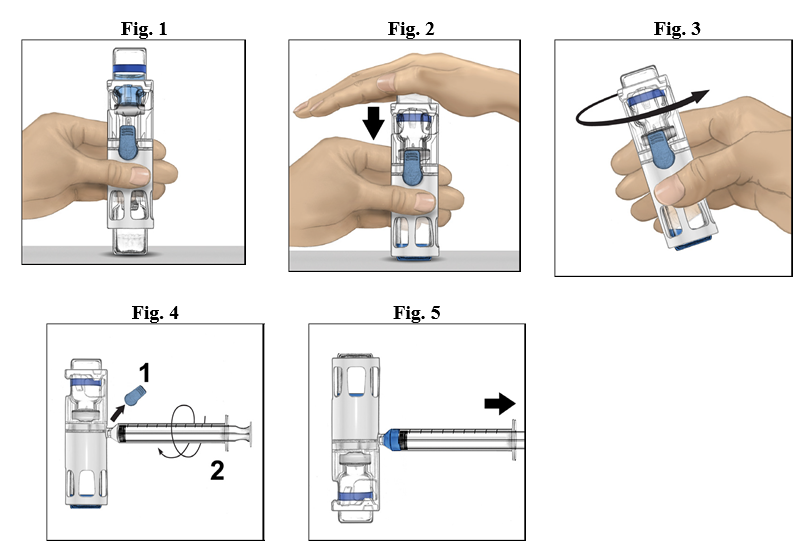
- Placera injektionsflaskan med pulver på en plan yta med injektionsflaskan med lösningsvätska överst (Fig. 1). Injektionsflaskan med lösningsvätska har en blå rand. Ta inte av det blå locket förrän du uppmanas att göra det i ett senare steg.
- Håll injektionsflaskan med pulver i BAXJECT III-systemet med ena handen och tryck stadigt ned injektionsflaskan med lösningsvätska med den andra handen tills systemet har tryckts ihop helt och lösningsvätskan rinner ner i injektionsflaskan med pulver (Fig. 2). Luta inte systemet förrän all lösningsvätska har runnit ner i injektionsflaskan med pulver.
- Kontrollera att all lösningsvätska har överförts. Snurra flaskan försiktigt tills allt pulver har lösts upp (Fig. 3). Se till att pulvret är fullständigt upplöst, annars kan inte all beredd lösning passera igenom filtret. Läkemedlet löses upp snabbt (vanligtvis på mindre än 1 minut). Efter beredningen ska lösningen vara klar, färglös och fri från främmande partiklar.
Anvisningar för injektion
Aseptisk teknik (mycket rena förhållanden rena förhållanden) måste användas under injektionen.
OBS!
- Inspektera den beredda lösningen för partiklar och missfärgning före injektion (lösningen ska vara klar, färglös och fri från partiklar).
Läkemedlet får inte användas om lösningen inte är helt klar eller om pulvret inte har lösts upp helt.
Injektionsflaska
- Ta bort det blå locket från BAXJECT II Hi‑Flow-anordningen (Fig. E). Dra inte in luft i sprutan. Anslut sprutan till BAXJECT II Hi-Flow-anordningen. Användning av en spruta med luer-lock rekommenderas.
- Vänd systemet upp och ned (så att injektionsflaskan med pulver hamnar överst). Dra upp den beredda lösningen i sprutan genom att långsamt dra tillbaka kolven (Fig. F).
- Ta loss sprutan. Sätt på en lämplig nål och injicera intravenöst. Om en patient ska få mer än en injektionsflaska med ADYNOVI kan innehållet i flera injektionsflaskor dras upp i samma spruta.
Det behövs en separat BAXJECT II Hi‑Flow-anordning för att bereda varje injektionsflaska med ADYNOVI med lösningsvätskan. - Injicera under upp till max 5 minuter (maximal infusionshastighet 10 ml per min).
- Kassera överbliven lösning på lämpligt sätt.
Injektionsflaska med pulver
- Ta bort det blå locket från BAXJECT III. Dra inte in luft i sprutan. Anslut sprutan till BAXJECT III. Användning av en spruta med luer-lock rekommenderas.
- Vänd systemet upp och ned (så att injektionsflaskan med pulver hamnar överst). Dra upp den beredda lösningen i sprutan genom att långsamt dra tillbaka kolven.
- Koppla loss sprutan och fäst sedan en fjärilsnål på den och injicera den beredda lösningen i en ven. Lösningen ska administreras långsamt, med en hastighet som avgörs av patientens komfortnivå men som inte överstiger 10 ml per minut. (Se avsnitt Eventuella biverkningar ”Eventuella biverkningar”).
- Kassera överbliven lösning på lämpligt sätt.
Direktiv för experterna inom hälsovården
Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal:
Behandling vid behov
Beräkningen av erforderlig dos av faktor VIII baseras på den empiriska upptäckten att 1 IE faktor VIII per kg kroppsvikt ökar aktiviteten av faktor VIII i plasma med 2 IE/dl. Erforderlig dos fastställs med hjälp av följande formel. Tabellen nedan kan användas som vägledning för dosering vid blödningsepisoder och kirurgiska ingrepp.
Tabell 1 Vägledning för dosering vid blödningsepisoder och kirurgiska ingrepp
|
Grad av blödning/typ av kirurgiskt ingrepp |
Erforderlig faktor VIII-nivå (% eller IE/dl) |
Dosintervall (timmar)/behandlingens längd (antal dagar) |
|
Blödning |
|
|
|
Tidig hemartros, muskelblödning eller blödning i munnen. |
20 – 40 |
Upprepa injektionerna var 12:e till 24:e timme. Minst 1 dag tills blödningsepisoden (upplevd smärta) upphört eller läkning har uppnåtts.
|
|
Mer omfattande hemartros, muskelblödning eller hematom. |
30 – 60 |
Upprepa injektionerna var 12:e till 24:e timme i 3–4 dagar eller längre tills smärtlindring uppnåtts och den akuta rörelsebegränsningen hävts.
|
|
Livshotande blödningar. |
60 – 100 |
Upprepa injektionerna var 8:e till 24:e timme tills det kritiska tillståndet är över. |
|
Kirurgiskt ingrepp |
|
|
|
Mindre Inklusive tandutdragning. |
30 – 60 |
Var 24:e timme under minst 1 dag, tills läkning uppnåtts.
|
|
Större |
80 – 100 (pre- och postoperativt) |
Upprepa injektionerna var 8:e till 24:e timme tills sårläkning inträtt, fortsätt därefter behandlingen i ytterligare minst 7 dagar för att upprätthålla en faktor VIII-aktivitet på 30 %–60 % (IE/dl). |
Profylax
För långtidsprofylax rekommenderas en dos på 40 till 50 IE ADYNOVI per kg kroppsvikt två gånger i veckan med 3–4 dagars intervall. Justering av doser och administreringsintervall kan övervägas beroende på uppnådda FVIII-nivåer och individuell blödningstendens.
Pediatrisk population
Doseringen för användning vid behov är densamma för pediatriska patienter (12 till 18 år) som för vuxna patienter. Profylaktisk behandling av patienter från 12 till <18 år är likadan som för vuxna patienter. Säkerheten på längre sikt för ADYNOVI hos barn under 12 år har ännu inte fastställts. Justering av doser och administreringsintervall kan övervägas beroende på uppnådda FVIII-nivåer och individuell blödningstendens.