Pakkausseloste
GHEMAXAN injektionsvätska, lösning i förfylld spruta 2000 IU (20 mg)/0,2 ml, 4000 IU (40 mg)/0,4 ml, 10000 IU (100 mg)/1 ml
Utökad övervakning
![]() Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar du eventuellt får. Information om hur du rapporterar biverkningar finns i slutet av avsnitt Eventuella biverkningar.
Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar du eventuellt får. Information om hur du rapporterar biverkningar finns i slutet av avsnitt Eventuella biverkningar.
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad Ghemaxan är och vad det används för
2. Vad du behöver veta innan du använder Ghemaxan
3. Hur du använder Ghemaxan
4. Eventuella biverkningar
5. Hur Ghemaxan ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Ghemaxan innehåller den aktiva substansen enoxaparinnatrium, vilken är en lågmolekylär heparin.
Ghemaxan fungerar på två sätt.
- Det hindrar befintliga blodproppar från att bli större. Detta gör det lättare för kroppen att bryta ner dem och hindra dem från att orsaka skada.
- Det förhindrar att blodproppar bildas i blodet.
Ghemaxan kan användas för att:
- behandla blodproppar som finns i ditt blod
- förhindra att blodproppar bildas i blodet i följande situationer:
- före och efter en operation
- när du är akut sjuk och kommer ha begränsad rörlighet under en period
- för att förhindra att fler blodproppar bildas om du fått blodproppar på grund av cancer
- när du har instabil angina (ett tillstånd med otillräcklig blodtillförsel till hjärtat)
- efter en hjärtinfarkt
- förhindra blodproppsbildning i slangar i en dialysmaskin (används för personer med svåra njurproblem).
Enoxaparinnatrium som finns i Ghemaxan kan också vara godkänd för att behandla andra sjukdomar som inte nämns i denna produktinformation. Fråga läkare, apoteks- eller annan hälso- och sjukvårdspersonal om du har ytterligare frågor och följ alltid deras instruktion.
Vad du behöver veta innan produkten används
Använd inte Ghemaxan
- om du är allergisk mot enoxaparinnatrium eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar). Exempel på tecken på allergisk reaktion: hudutslag, svälj- eller andningssvårigheter, uppsvullnad av läppar, ansikte, hals eller tunga.
- om du är allergisk mot heparin eller andra lågmolekylära hepariner såsom nadroparin, tinzaparin eller dalteparin
- om du har reagerat på heparin med kraftig minskning av antalet blodplättar – denna reaktion kallas heparininducerad trombocytopeni – de senaste 100 dagarna, eller om du har antikroppar mot enoxaparinnatrium i blodet
- om du blöder kraftigt eller har ett tillstånd med ökad blödningsbenägenhet (såsom vid magsår eller nyligen genomgången hjärn- eller ögonoperation), om du nyligen har haft hjärnblödning
- om du använder Ghemaxan för att behandla blodproppar och kommer att få spinal- eller epiduralbedövning (bedövning i eller utanför ryggmärgskanalen) eller genomgå lumbalpunktion (provtagning av ryggmärgsvätska) inom 24 timmar.
Varningar och försiktighet
Ghemaxan ska inte bytas ut mot andra läkemedel inom gruppen lågmolekylära hepariner. Det beror på att de inte är exakt lika och inte har samma verkan och användaranvisningar.
Tala med läkare eller apotekspersonal innan du använder Ghemaxan om:
- du någon gång har reagerat på heparin med kraftig minskning av antalet blodplättar
- du kommer att få spinal- eller epiduralbedövning (bedövning i eller utanför ryggmärgskanalen) eller genomgå lumbalpunktion (provtagning av ryggmärgsvätska) (se avsnitt ”Operationer och bedövningsmedel”): uppehåll ska göras mellan behandling med Ghemaxan och dessa behandlingar
- du har en hjärtklaffprotes
- du har endokardit (infektion i hjärtats klaffar)
- du någon gång har haft magsår
- du nyligen haft en stroke
- om du har högt blodtryck
- om du har diabetes eller besvär med blodkärlen i ögat orsakad av diabetes (diabetesretinopati)
- du nyligen har genomgått en operation i ögonen eller hjärnan
- du är äldre (över 65 år) och särskilt om du är över 75 år
- du har problem med njurarna
- du har problem med levern
- om du är underviktig eller överviktig
- du har förhöjda kaliumnivåer i blodet (kan kontrolleras med ett blodprov)
- du använder läkemedel som påverkar blödning (se avsnitt ”Andra läkemedel och Ghemaxan” nedan).
Du kan komma att få lämna blodprov innan du börjar använda det här läkemedlet och då och då medan du använder det. Det är för att kontrollera mängden blodplättar och kalium i blodet.
Andra läkemedel och Ghemaxan
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
- Warfarin – används som blodförtunnande
- Acetylsalicylsyra (också känt som ASA), klopidogrel eller andra läkemedel som används för att förhindra blodkoagulation (se också avsnitt Hur produkten används ”Byte av blodförtunnande medel”)
- Dextraninjektion – används som blodersättning
- Ibuprofen, diklofenak, ketorolak eller andra läkemedel av typen icke-steroida antiinflammatoriska medel (NSAID) som används för att behandla smärta och svullnad vid ledinflammation (artrit) och andra tillstånd.
- Prednisolon, dexametason eller andra läkemedel som används för att behandla astma, reumatoid artrit och andra tillstånd
- Läkemedel som ökar kaliumnivån i blodet, såsom kaliumsalter, vätskedrivande medel, vissa hjärtmediciner.
Operationer och bedövningsmedel
Om du ska genomgå lumbalpunktion (provtagning av ryggmärgsvätska) eller en operation där epidural- eller spinalbedövning (bedövning i eller utanför ryggmärgskanalen) används ska du tala om för läkaren att du använder Ghemaxan. Se ”Använd inte Ghemaxan”. Tala också om för läkaren om du har problem med ryggraden eller om du någonsin genomgått en ryggradsoperation.
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du använder detta läkemedel.
Om du är gravid och har en hjärtklaffprotes kan du ha ökad risk att bilda blodproppar. Din läkare bör diskutera detta med dig.
Körförmåga och användning av maskiner
Ghemaxan har ingen effekt på förmågan att framföra fordon och använda maskiner.
Ghemaxan innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol natrium (23 mg) per dos dvs. är näst intill ”natriumfritt”.
Det rekommenderas att läkemedlets namn och satsnummer antecknas av sjukvårdspersonalen.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Att använda detta läkemedel
- Det är vanligtvis läkaren eller sjuksköterskan som ger dig Ghemaxan eftersom det ges som en injektion.
- När du åker hem kan du behöva fortsätta använda Ghemaxan och ta det själv (se anvisningar nedan om hur du gör detta).
- Ghemaxan ges vanligtvis som en injektion under huden (subkutant).
- Ghemaxan kan ges som injektion i en ven (intravenöst) efter vissa typer av hjärtinfarkter eller operationer.
- Ghemaxan kan ges till slangen som lämnar kroppen (artärslangen) vid början av en dialysbehandling.
Injicera inte Ghemaxan i en muskel.
Hur mycket du kommer att få
- Läkaren avgör hur stor mängd Ghemaxan du får. Hur stor mängd läkemedel du får beror på orsaken till att det används.
- Om du har problem med njurarna kan du få en mindre mängd av Ghemaxan.
- Behandling av blodproppar
Normaldos är 150 IE (1,5 mg) per kilogram kroppsvikt per dag, eller 100 IE (1 mg) per kilogram kroppsvikt två gånger dagligen.
Läkaren avgör hur länge du ska använda Ghemaxan.
2.
Förhindra blodproppsbildning i blodet vid följande situationer:
a) Vid operationer eller vid begränsad rörlighet på grund av sjukdom
- Dosen beror på hur benägen du är att bilda blodproppar. Du kommer att ges 2 000 IE (20 mg) eller 4 000 IE (40 mg) Ghemaxan per dag.
- Om du ska opereras kommer din första injektion normalt att ges 2 timmar eller 12 timmar före operationen.
- Om du har begränsad rörlighet på grund av sjukdom ges du normal 4 000 IE (40 mg) Ghemaxan per dag.
- Läkaren avgör hur länge du ska använda Ghemaxan.
b) Efter en hjärtinfarkt
Ghemaxan kan användas för två typer av hjärtinfarkter som kallas STEMI (akut hjärtinfarkt med ST-höjning) och NSTEMI (akut hjärtinfarkt utan ST-höjning). Mängden Ghemaxan du får beror på din ålder och typen av hjärtinfarkt du haft.
Hjärtinfarkt av typen NSTEMI:
- Normaldosen är 100 IE (1 mg) per kilogram kroppsvikt var 12:e timme.
- Läkaren ber dig vanligtvis att ta acetylsalicylsyra också.
- Läkaren avgör hur länge du ska använda Ghemaxan.
Hjärtinfarkt av typen STEMI om du är under 75 år:
- En startdos på 3 000 IE (30 mg) Ghemaxan ges som injektion i en ven.
- Samtidigt ges du också Ghemaxan som en injektion under huden (subkutan injektion). Normaldosen är 100 IE (1 mg) per kilogram kroppsvikt var 12:e timme.
- Läkaren ber dig vanligtvis att ta acetylsalicylsyra också.
- Läkaren avgör hur länge du ska använda Ghemaxan.
Hjärtinfarkt av typen STEMI om du är 75 år eller äldre:
- Normaldosen är 75 IE (0,75 mg) per kilogram kroppsvikt, var 12:e timme.
- Maximal mängd av Ghemaxan som ges med de första två injektionerna är 7 500 IE (75 mg).
- Läkaren avgör hur länge du ska använda Ghemaxan.
För patienter som genomgår en kranskärlsoperation via perifera kärl (perkutan koronarintervention):
Beroende på när du senast fick Ghemaxan kan din läkare besluta att ge ytterligare en Ghemaxan-dos innan operationen. Det görs via injektion i en ven.
3. Förhindra blodproppar från att bildas i slangar på din dialysmaskin
- Normaldosen är 100 IE (1 mg) per kilogram kroppsvikt.
- Ghemaxan tillsätts i slangen som lämnar kroppen (artärslangen) vid början av en dialysomgång. Mängden räcker oftast för en 4-timmarsdialys. Men läkaren kan ge dig en ytterligare dos på 50 IE till 100 IE (0,5 till 1 mg) per kilogram kroppsvikt, vid behov.
Administreringssätt
Den förfyllda sprutan är klar för omedelbar användning.
Detta läkemedel får inte injiceras i en muskel.
Injektion i artärslangen på en dialysmaskin
För att förebygga att blodproppar bildas i slangarna på dialysmaskinen injiceras detta läkemedel i slangen som lämnar kroppen (artärslangen).
Intravenös injektion (endast vid akut STEMI)
Behandling av akut STEMI ska inledas med en enstaka snabb injektion i en ven (intravenös injektion), omedelbart följt av en injektion under huden (subkutan injektion).
Subkutan injektion
Detta läkemedel ges vanligtvis som en injektion under huden (subkutant).
Injektionen görs helst som en djup subkutan injektion medan patienten ligger ned. Växla mellan att ge injektionen i vänster och höger sida av magen. Hela nålen ska föras in vertikalt i ett hudveck som hålls mellan tummen och pekfingret. Hudvecket ska inte släppas förrän injektionen är avslutad.
Gnugga inte injektionsstället efter administrering.
Om du använder en förfylld spruta med 20 mg eller 40 mg ska luftbubblan i sprutan inte avlägsnas före injektion, eftersom detta kan resultera i en mindre dos.
Den förfyllda sprutan är endast avsedd för engångsbruk.
Använd inte detta läkemedel om du märker att lösningens utseende har förändrats.
Hur du injicerar dig själv med Ghemaxan
Om du kan ge dig själv en injektion av Ghemaxan, kommer läkare eller sjuksköterska visa dig hur du ska göra detta. Försök inte injicera dig själv om du inte har blivit visad hur du ska göra. Om du inte är säker på hur du ska göra, kontakta omedelbart läkare eller sjuksköterska.
Innan du injicerar dig själv med Ghemaxan
- Kontrollera läkemedlets utgångsdatum. Använd inte om utgångsdatumet har passerat.
- Kontrollera att sprutan inte är skadad och att läkemedlet är en klar lösning. Om inte, använd en annan spruta.
- Använd inte detta läkemedel om du märker att lösningens utseende har förändrats.
- Se till att du vet hur mycket du ska injicera.
- Kontrollera din mage för att se om den förra injektionen orsakade någon rodnad, förändrad hudfärg, svullnad, vätskande sår eller om det fortfarande gör ont. Kontakta i sådant fall läkare eller sjuksköterska.
- Välj ut ett injektionsställe. Byt injektionsställe varje gång och växla mellan magens högra och vänstra sida. Ghemaxan ska injiceras strax under huden på magen, men inte för nära naveln eller eventuell ärrvävnad (minst 5 cm från dessa).
Den förfyllda sprutan är endast avsedd för engångsbruk. Två olika slags sprutor är tillgängliga:
- förfylld spruta med nålskydd.
- förfylld spruta utan nålskydd
Anvisningar om hur du ger dig själv en injektion av Ghemaxan
Du bör ligga ner och ta Ghemaxan som en djup subkutan injektion. Välj ett område på höger eller vänster sida av magen. Detta bör vara minst 5 cm från naveln och ut mot sidorna.
Ghemaxan förfyllda sprutor och graderade förfyllda sprutor är endast för engångsbruk. Det finns sprutor med och utan nålskydd.
Ta ut den förfyllda sprutan ur blisterförpackningen genom att dra vid pilen så som visas på blistret. Ta inte ut sprutan genom att dra i kolven eftersom detta kan skada sprutan.
1) Avlägsna nålhättan genom att dra det rakt ut från sprutan.
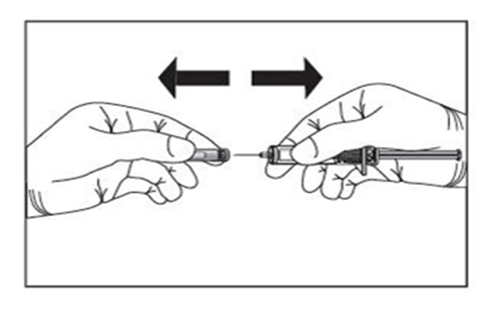
2) Nyp försiktigt ihop det rengjorda området på magen mellan tummen och pekfingret så att ett hudveck bildas. Håll kvar hudvecket under hela injektionen. För in hela nålen i hudvecket och injicera läkemedlet genom att trycka kolven hela vägen in i sprutan.
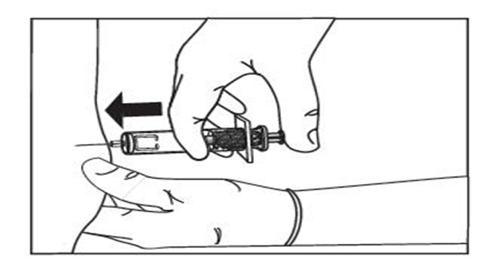
3) Dra ut sprutan ur huden med kolven fortfarande intryckt. Du kan nu släppa hudvecket. För att undvika blåmärken, gnid inte injektionsstället efter injektionen.
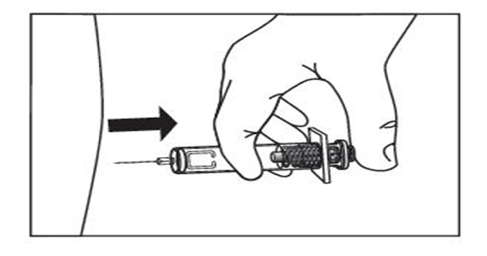
4a) Förfyllda sprutor som är försedda med nålskydd.
Efter injektionen, håll sprutcylindern med ett stadigt tag i ena handen. Håll basen av sprutan, ”vingarna”, med den andra handen och dra tills du hör ett ”klick”. Nålen är nu helt täckt. Nålskyddet tillhandahålls med en spärr för att kunna låsa och låsa upp mekanismen.
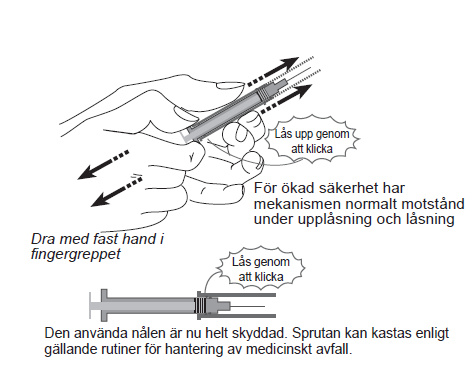
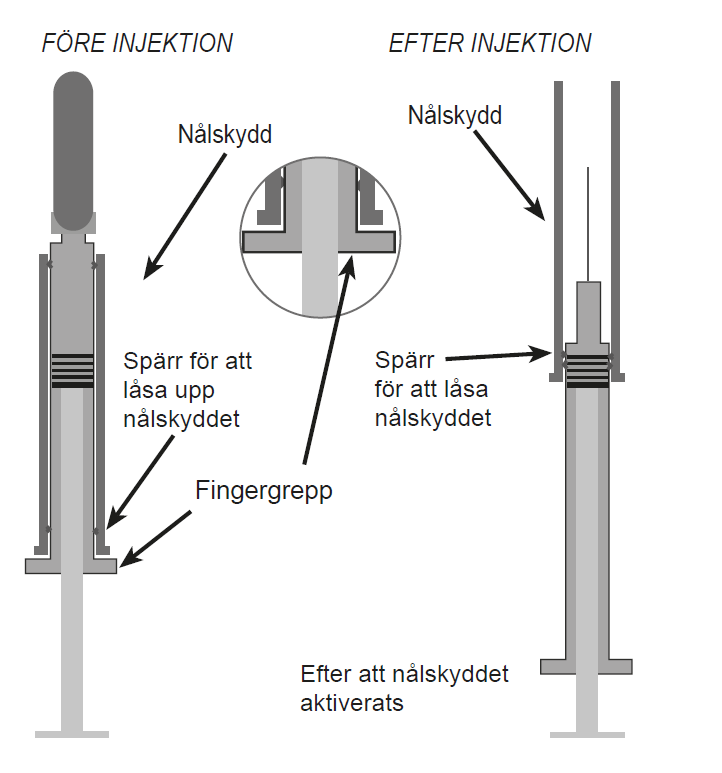
Kassera omedelbart sprutan i den avsedda behållaren.
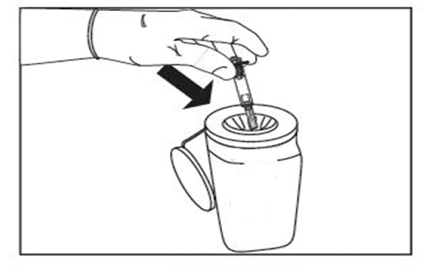
4b) Förfyllda sprutor som inte är försedda med nålskydd.
Kassera omedelbart sprutan i den avsedda behållaren.
Byte av blodförtunnande medel (antikoagulantia)
- Byte från Ghemaxan till blodförtunnande medel av typen vitamin-K-antagonister (t.ex. warfarin)
Läkaren kommer att begära att du tar ett blodprov som kallas INR och talar utifrån det om för dig när du ska sluta med Ghemaxan.
- Byte från blodförtunnande medel av typen vitamin-K antagonister (t.ex. warfarin) till Ghemaxan
Sluta ta vitamin K-antagonisten. Läkaren kommer att begära att du tar ett blodprov som kallas INR och talar utifrån det om när du ska börja med Ghemaxan.
- Byte från Ghemaxan till behandling med direktverkande blodförtunnande medel som tas via munnen
Sluta ta Ghemaxan. Börja med det direktverkande blodförtunnande medlet 0‑2 timmar före den tid då du skulle ha tagit nästa injektion, och fortsätt därefter med normaldosering.
- Byte från behandling med direktverkande blodförtunnande medel som tas via munnen till Ghemaxan
Sluta ta det direktverkande blodförtunnande medlet. Påbörja inte behandling med Ghemaxan förrän 12 timmar efter den sista dosen med det direktverkande blodförtunnande medlet.
Användning för barn och ungdomar
Effekt och säkerhet för Ghemaxan har inte undersökts hos barn och ungdomar.
Om du använt för stor mängd av Ghemaxan
Om du tror att du har använt för stor eller för liten mängd av Ghemaxan ska du informera läkare, sjuksköterska eller apotekspersonal omedelbart eller kontakta Giftinformationscentralen (0800 147 111) även om du inte har några symtom. Om ett barn injicerar eller sväljer detta läkemedel av misstag ska du omedelbart ta dem till en akutmottagning.
Om du har glömt att använda Ghemaxan
Om du har glömt att ge dig själv en dos ska du ta den så snart du kommer ihåg det. Ge inte dig själv en dubbel dos för att kompensera för glömd dos. För att göra det lättare att inte glömma bort en dos kan du föra dagbok.
Om du slutar att använda Ghemaxan
Om du har ytterligare frågor om detta läkemedel, kontakta läkare, apotekspersonal eller sjuksköterska. Det är viktigt att du fortsätter använda Ghemaxan tills läkaren beslutar att behandlingen ska avslutas. Om du avbryter behandlingen kan du få en blodpropp vilket kan vara mycket farligt.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Allvarliga biverkningar
Sluta använda Ghemaxan och prata med en läkare eller sjuksköterska direkt om du får några tecken på
allvarliga allergiska reaktioner (såsom andningssvårigheter, svullnad av läppar, mun, hals eller ögon).
Sluta använda Ghemaxan och sök omedelbart medicinsk vård om du upptäcker något av följande symtom:
- Rött, fjällande utbrett utslag med knölar under huden och blåsor som åtföljs av feber. Symtomen uppstår vanligen i början av behandlingen (akut generaliserad exantematös pustulos).
Liksom andra liknande läkemedel, som används mot blodproppar, kan Ghemaxan orsaka blödning som kan vara livshotande. I vissa fall är blödningen inte uppenbar.
Prata med läkare direkt om:
- du får en blödning som inte upphör av sig själv
- du får symtom på blodförlust såsom uttalad svaghet, trötthet, blekhet, yrsel med huvudvärk eller oförklarlig svullnad
Läkare kan besluta att hålla dig under särskild observation eller byta ut ditt läkemedel.
Du ska meddela din läkare direkt:
- om du har några tecken på blodpropp i en blodådra såsom:
krampsmärta, rodnad, värme eller svullnad i ett av dina ben - dessa är symtom på djup ventrombos
- andfåddhet, bröstsmärta, svimning eller upphostning av blod - dessa är symtom på blodpropp i lungan
om du har en smärtsam rodnad med mörkröda fläckar under huden som inte försvinner när du trycker på dem.
Din läkare kan begära att du lämnar ett blodprov för att kontrollera mängden blodplättar.
Övriga biverkningar:
Mycket vanliga (kan förekomma hos fler än 1 av 10 personer)
- Blödning
- Ökning av leverenzymer
Vanliga (kan förekomma hos upp till 1 av 10 personer)
- Du får blåmärken lättare än vanligt. Detta kan bero på problem med låg nivå av blodplättar.
- Rosa fläckar på huden. Dessa uppträder oftare på ställen där Ghemaxan har injicerats.
- Nässelutslag
- Kliande röd hud
- Blåmärke eller smärta vid injektionsstället
- Minskning av röda blodkroppar
- Höga nivåer av blodplättar
- Huvudvärk.
Mindre vanliga (kan förekomma hos upp till 1 av 100 personer)
- Plötslig svår huvudvärk. Detta kan vara ett tecken på blödning i hjärnan.
- En ömmande känsla eller svullnad i buken. Du kan ha en blödning i magen.
- Stora röda oregelbundna hudskador med eller utan blåsor
- Irriterad hud (lokal irritation)
- Hud eller ögon gulnar och urinen blir mörkare. Detta kan bero på leverproblem
Sällsynta (kan förekomma hos upp till 1 av 1 000 personer)
- Svår allergisk reaktion. Symtom kan omfatta: hudutslag, svälj- eller andningssvårigheter, svullnad i läppar, ansikte, svalg eller tunga.
- Ökad kaliumnivå i blodet. Detta är troligare hos personer med njurproblem eller diabetes. Din läkare kan kontrollera detta med ett blodprov.
- Ökning av antalet eosinofiler (en typ av vita blodkroppar) i blodet. Din läkare kan kontrollera detta med ett blodprov.
- Håravfall
- Osteoporos (benskörhet) efter lång tids användning
- Stickande känsla, domningar och muskelsvaghet (särskilt i underkroppen) när du fått spinal punktion eller spinalbedövning (ryggbedövning)
- Förlorad kontroll över blås- eller tarmfunktion (så att du inte kan kontrollera när du går på toaletten)
- Förhårdnad eller klump vid injektionsstället.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på kartongen efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Använd inte detta läkemedel om du märker synliga förändringar i lösningens utseende.
Får ej frysas.
Ghemaxan förfyllda sprutor är endast avsedda för engångsbruk. Ej använd lösning ska kasseras.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Varje förfylld spruta innehåller enoxaparinnatrium 2 000 IE anti-Xa-aktivitet (motsvarande 20 mg) i 0,2 ml vatten för injektionsvätskor
- Varje förfylld spruta innehåller enoxaparinnatrium 4 000 IE anti-Xa-aktivitet (motsvarande 40 mg) i 0,4 ml vatten för injektionsvätskor
- Varje förfylld spruta innehåller enoxaparinnatrium 10 000 IE anti-Xa-aktivitet (motsvarande 100 mg) i 1,0 ml vatten för injektionsvätskor
- Övriga innehållsämnen är vatten för injektionsvätskor
Läkemedlets utseende och förpackningsstorlekar
Ghemaxan är en klar, färglös till ljusgul injektionsvätska, lösning i en förfylld spruta av typ I-glas med fastsatt nål och nålhätta. Sprutan kan vara utrustad med eller utan nålskydd.
- Sprutor som är försedda med nålskydd
Ghemaxan 2 000 IE (20 mg)/0,2 ml injektionsvätska, lösning i förfylld spruta:
Förpackningar med 2, 6 eller 10 förfyllda sprutor, multipelförpackningar med 12 (2 förpackningar med 6), 20 (2 förpackningar med 10), 24 (4 förpackningar med 6), 30 (3 förpackningar med 10), 50 (5 förpackningar med 10) och 90 (9 förpackningar med 10) förfyllda sprutor
Ghemaxan 4 000 IE (40 mg)/0,4 ml injektionsvätska, lösning i förfylld spruta:
Förpackningar med 2, 6 eller 10 förfyllda sprutor, multipelförpackningar med 12 (2 förpackningar med 6), 20 (2 förpackningar med 10), 24 (4 förpackningar med 6), 30 (3 förpackningar med 10), 50 (5 förpackningar med 10) och 90 (9 förpackningar med 10) förfyllda sprutor
Ghemaxan 10 000 IE (100 mg)/1 ml injektionsvätska, lösning i förfylld spruta:
Förpackningar med 2, 6 eller 10 graderade förfyllda sprutor, multipelförpackningar med 12 (2 förpackningar med 6), 20 (2 förpackningar med 10), 24 (4 förpackningar med 6), 30 (3 förpackningar med 10), 50 (5 förpackningar med 10) och 90 (9 förpackningar med 10) graderade förfyllda sprutor
- Sprutor som inte är försedda med nålskydd
Ghemaxan 2 000 IE (20 mg)/0,2 ml injektionsvätska, lösning i förfylld spruta:
Förpackningar med 2 och 10 förfyllda sprutor
Ghemaxan 4 000 IE (40 mg)/0,4 ml injektionsvätska, lösning i förfylld spruta:
Förpackningar med 2 och 10 förfyllda sprutor, multipelförpackning med 30 (3 förpackningar med 10) förfyllda sprutor
Ghemaxan 10 000 IE (100 mg)/1 ml injektionsvätska, lösning i förfylld spruta:
Förpackningar med 2 och 10 graderade förfyllda sprutor, multipelförpackning med 30 (3 förpackningar med 10) graderade förfyllda sprutor
Följande förfyllda sprutor är graderade: 10 000 IE (100 mg)/1 ml.
Eventuellt kommer inte alla förpackningsstorlekar att markadsföras.
Innehavare av godkännande för försäljning
Chemi S.p.A
Via dei Lavoratori, 54
20092 Cinisello Balsamo (MI)
Italien
Tillverkare
Italfarmaco S.p.A
Viale F. Testi 330
20126 Milano
Italien
Lokal företrädare
CampusPharma AB
Karl Gustavsgatan 1A
411 25 Göteborg
Sverige
Detta läkemedel är godkänt inom Europeiska ekonomiska samarbetsområdet under namnen:
Belgien: Ghemaxan
Tyskland: Hepaxane
Danmark: Ghemaxan
Grekland: Havetra
Spanien: Hepaxane
Finland: Ghemaxan
Italien: Ghemaxan
Nederländerna: Ghemaxan
Norge: Ghemaxan
Österrike: Ghemaxan
Frankrike: Ghemaxan
Irland: Ghemaxan
Sverige: Ghemaxan
Portugal: Hepaxane
Ungern: Hepaxane
Rumänien: Hepaxane
Slovakien: Ghemaxan
Denna bipacksedel ändrades senast 22.08.2024
Övriga informationskällor
Ytterligare information om detta läkemedel finns på Fimeas webbplats www.fimea.fi .