SYCREST resoriblett, sublingual 5 mg, 10 mg
Tilläggsinformation
Sycrest 10 mg resoribletter, sublingual
asenapin
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad Sycrest är och vad det används för
- Vad du behöver veta innan du tar Sycrest
- Hur du tar Sycrest
- Eventuella biverkningar
- Hur Sycrest ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Sycrest innehåller den aktiva substansen asenapin. Det här läkemedlet tillhör en grupp läkemedel som kallas för antipsykotika. Sycrest används för att behandla måttliga till allvarliga maniska episoder vid bipolär I-sjukdom hos vuxna. Antipsykotiska läkemedel påverkar kemiska signalsubstanser som möjliggör kontakt mellan nervceller (neurotransmittorer). Sjukdomar som påverkar hjärnan, såsom bipolär I-sjukdom, kan bero på att kemiska signalsubstanser i hjärnan, såsom dopamin och serotonin, är i obalans och denna obalans kan orsaka några av de symtom som du kan uppleva. Det är inte exakt känt hur det här läkemedlet verkar men det antas att det reglerar jämnvikten mellan dessa kemiska signalsubstanser.
Maniska episoder förknippade med bipolär I-sjukdom är ett tillstånd med symtom såsom att man känner sig ”hög”, har ett överskott av energi, ett mycket mindre sömnbehov än vanligt, talar mycket snabbt med tankeflykt och ibland är mycket lättirriterad.
Vad du behöver veta innan produkten används
Ta inte Sycrest
Om du är allergisk mot asenapin eller mot något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du tar Sycrest.
Sycrest har inte undersökts hos äldre patienter som har demens. Äldre patienter som har demens, som behandlas med andra liknande typer av läkemedel, kan emellertid ha en ökad risk för slaganfall eller att dö. Sycrest är inte godkänt för behandling av äldre patienter med demens och rekommenderas inte för denna grupp av patienter.
Sycrest kan orsaka lågt blodtryck. Under den inledande delen av behandlingen kan vissa personer svimma, speciellt när de reser sig från liggande till sittande ställning. Detta går vanligen över av sig själv men om det inte gör det ska du tala med din läkare. Dosen kan behöva justeras.
Asenapin kan orsaka sömnighet, plötsligt blodtrycksfall när du reser dig upp, yrsel och förändrad rörelse- och balansförmåga. Detta kan leda till fallolyckor och därmed frakturer eller andra skador. Patienter med risk för fallolyckor ska utvärderas före ordination av asenapin.
Tala genast om för din läkare om du får
- ofrivilliga rytmiska rörelser i tungan, munnen och ansiktet. Det kan bli nödvändigt att avsluta behandling med Sycrest.
- feber, allvarlig muskelstelhet, svettningar eller nedsatt medvetandegrad (ett tillstånd som kallas ”neuroleptiskt malignt syndrom”). Omedelbar medicinsk behandling kan behövas.
Kontrollera med din läkare eller apotekspersonal innan du tar Sycrest:
- om du någonsin har fått diagnos på ett tillstånd vars symtom omfattar hög kroppstemperatur och muskelstelhet (också känt som neuroleptiskt malignt syndrom).
- om du någonsin har upplevt onormala rörelser i tungan eller i ansiktet (tardiv dyskinesi).
- Du ska känna till att man kan få båda dessa tillstånd av denna typ av läkemedel.
- om du har en hjärtsjukdom eller får behandling för en hjärtsjukdom som gör att du kan få lågt blodtryck.
- om du har diabetes eller har anlag för att få diabetes
- om du har Parkinsons sjukdom eller demens
- om du har epilepsi (kramper)
- om du har svårt att svälja (dysfagi)
- om du har allvarliga leverproblem. Om du har det ska du inte använda Sycrest
- om du har svårt att reglera kroppstemperaturen
- om du har självmordstankar
- om du har onormalt höga prolaktinhalter i blodet (hyperprolaktinemi)
Var noga med att tala om för din läkare om något av dessa tillstånd gäller dig eftersom han/hon kan behöva ändra dosen eller övervaka dig under en period. Kontakta också genast din läkare om något av dessa tillstånd uppträder eller förvärras när du tar Sycrest.
Barn och ungdomar
Sycrest rekommenderas inte för användning hos patienter under 18 års ålder.
Andra läkemedel och Sycrest
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel. Vissa läkemedel kan minska eller öka effekten av Sycrest.
Om du tar andra läkemedel ska Sycrest tas sist.
Du ska tala om för din läkare om du tar antidepressiva läkemedel (speciellt fluvoxamin, paroxetin eller fluoxetin) eftersom det kan vara nödvändigt att ändra Sycrestdosen eller dosen för det antidepressiva läkemedlet.
Du ska tala om för din läkare om du tar läkemedel mot Parkinsons sjukdom (såsom levodopa) eftersom det här läkemedlet kan försämra deras effekt.
Eftersom Sycrest i huvudsak påverkar hjärnan, kan det uppstå störningar från andra läkemedel (eller alkohol) som påverkar hjärnan vilket beror på en additiv effekt på hjärnans funktion.
Eftersom Sycrest kan sänka blodtrycket ska man vara försiktig med att ta Sycrest tillsammans med andra läkemedel som sänker blodtrycket.
Sycrest med mat, dryck och alkohol
Ät och drick inte under 10 minuter efter intag av detta läkemedel.
Du ska undvika att dricka alkohol när du använder detta läkemedel
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du tar detta läkemedel.
Ta inte Sycrest när du är gravid, om inte din läkare har sagt till dig att göra det. Om du tar detta läkemedel och blir gravid eller försöker att bli gravid, fråga din läkare så snart som möjligt om du kan fortsätta att ta Sycrest.
Hos nyfödda barn vars mammor har tagit Sycrest under den sista trimestern (de sista tre månaderna av graviditeten) kan följande symtom förekomma: skakningar, stela och/eller svaga muskler, sömnighet, upprördhet, andningsproblem och svårigheter att äta. Om ditt barn får några av dessa symtom kan du behöva kontakta din läkare.
Du ska inte amma när du tar Sycrest.
Körförmåga och användning av maskiner
Sycrest kan orsaka sömnighet eller nedsatt vakenhet. Försäkra dig därför om att din koncentration och vakenhet inte är påverkade innan du framför fordon eller använder verktyg eller maskiner.
Hur produkten används
Ta alltid detta läkemedel enligt läkarens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Rekommenderad dos är en sublingual resoriblett, 5 mg eller 10 mg, två gånger dagligen. En dos tas på morgonen och en på kvällen.
Användarinstruktion
Sycrest ska läggas under tungan.
Sycrest rekommenderas inte om du inte kan ta tabletten på det sätt som beskrivs nedan. Om du inte kan ta detta läkemedel på det sätt som beskrivs nedan, kan det hända att effekten av behandlingen uteblir.
- Ta inte ut en sublingual resoriblett från blistern förrän du är redo att ta den.
- Händerna ska vara torra när du tar i tabletten.
- Tryck inte ut tabletten från blistern. Klipp eller riv inte blistern.
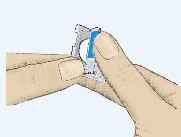
- Drag tillbaka den färgade fliken (Figur 1).
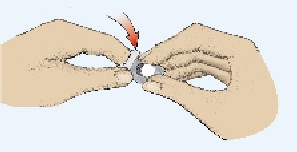
- Tag försiktigt ur tabletten (Figur 2). Krossa inte tabletten.
- För att säkerställa optimal absorption, ska du placera tabletten under tungan och vänta tills den helt lösts upp (Figur 3). Tabletten löses upp i saliven inom några sekunder.
- Svälj eller tugga inte tabletten.
- Ät och drick inte under 10 minuter efter intag av tabletten.
|
Figur 1 |
Figur 2 |
Figur 3 |
Om du har tagit för stor mängd av Sycrest
Om du har tagit för mycket Sycrest kontakta genast läkare. Tag med dig läkemedelsförpackningen. I händelse av överdosering kan du känna dig sömning eller trött, eller ha onormala kroppsrörelser, problem med att stå eller gå, känna dig yr på grund av lågt blodtryck och känna dig upprörd och förvirrad.
Om du har glömt att ta Sycrest
Ta inte dubbel dos för att kompensera för glömd dos. Om du har glömt en dos, ta nästa dos som vanligt. Om du har glömt två doser eller fler kontakta din läkare eller apotekspersonal.
Om du slutar att ta Sycrest
Om du slutar att ta Sycrest uteblir effekten av detta läkemedel. Du ska inte sluta att ta läkemedlet om inte din läkare sagt det eftersom dina symtom kan återkomma.
Om du har ytterligare frågor om detta läkemedel kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem.
Allvarliga biverkningar har rapporterats med detta läkemedel. Uppsök sjukvård omedelbart om du har något av följande symtom:
- allergiska reaktioner (Ofta förekommer en kombination av olika symtom som andningssvårigheter eller svårigheter att svälja, svullnad i ansikte, läppar, tunga eller svalg, hudutslag, klåda och snabbare hjärtslag.)
- plötslig ökning av kroppstemperaturen med svettningar, snabba hjärtslag, svår muskelstelhet, förvirring och varierande blodtryck vilket kan leda till koma
- krampanfall
- svimning
- fallolyckor, vilka kan inträffa som en följd av en eller flera följande biverkningar: sömnighet, plötsligt blodtrycksfall när du ställer dig upp, yrsel och förändrad rörelse- och balansförmåga.
Tala omedelbart om för din läkare om du har:
- tecken på förhöjda blodsockernivåer så som överdriven törst, hunger eller urinering, svaghet eller försämrad diabetes
- ofrivilliga rörelser av tungan eller andra okontrollerade rörelser i tunga, mun, kinder eller käke, som även kan kännas i armar och ben
Andra biverkningar som rapporterats med detta läkemedel inkluderar:
Mycket vanliga biverkningar (kan förekomma hos fler än 1 av 10 användare)
- ångest
- sömnighet
Vanliga biverkningar (kan förekomma hos färre än 1 av 10 användare)
- viktökning
- ökad aptit
- långsamma eller bestående muskelkontraktioner
- rastlöshet
- ofrivilliga muskelkontraktioner
- långsamma rörelser, skakningar
- dåsighet
- yrsel
- illamående
- förändrad smak
- domningskänsla i tungan eller i munnen
- ökad saliv (dregling)
- muskelspändhet
- trötthet
- ökning av leverproteinnivåer
Mindre vanliga biverkningar (kan förekomma hos färre än 1 av 100 användare)
- onormala kroppsrörelser: en samling av symtom som kallas extrapyramidala symtom (EPS) som kan omfatta en eller flera av följande: onormala rörelser av muskler, tunga eller käke, långsamma eller bestående muskelkontraktioner, muskelspasm, tremor (skakningar), onormala ögonrörelser, ofrivilliga muskelkontraktioner, långsamma rörelser eller rastlöshet.
- obehaglig känsla i benen, också kallad "restless legs syndrome" (engelska för rastlösa ben)
- talsvårigheter
- onormalt långsamma eller snabba hjärtslag
- hjärtblock (störningar i hjärtats retledningssystem)
- onormalt elektrokardiogram (EKG), (förlängning av QT-intervallet)
- lågt blodtryck vid stående
- lågt blodtryck
- stickningar i tungan eller i munnen
- svullnad eller smärta i tungan
- sväljningssvårigheter
- sår, ömhet, rodnad, svullnad och blåsor i munnen
- sexuell dysfunktion
- oregelbundna menstruationsperioder
Sällsynta biverkningar (kan förekomma hos färre än 1 av 1 000 användare)
- förändringar i värden av vita blodkroppar
- svårighet att fokusera med ögonen
- blodproppar i blodkärlen till lungorna som medför bröstsmärtor och andningssvårigheter
- muskelsjukdom som yttrar sig som oförklarlig värk och smärta
- bröstförstorning hos män
- läckage av mjölk eller vätska från brösten
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på blistern och kartongen efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras i originalförpackningen. Ljuskänsligt. Fuktkänsligt.
Inga särskilda temperaturanvisningar.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är asenapin.
- Varje Sycrest 5 mg sublingual resoriblett innehåller 5 mg asenapin.
- Varje Sycrest 10 mg sublingual resoriblett innehåller 10 mg asenapin.
- Den exakta mängden anges på din Sycrestförpackning.
- Övriga innehållsämnen är gelatin och mannitol (E421).
Läkemedlets utseende och förpackningsstorlekar
5 mg resoribletter, sublingual, är runda vita till benvita präglade med ”5” på ena sidan.
10 mg resoribletter, sublingual, är runda vita till benvita präglade med ”10” på ena sidan.
Resoribletterna finns i avdragbara blister som innehåller 10 tabletter vardera. Förpackningar kan innehålla 20, 60 eller 100 tabletter.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning
N.V. Organon
Kloosterstraat 6
NL-5349 AB Oss
Nederländerna
Tillverkare
Organon Heist bv
Industriepark 30
2220 Heist-op-den-Berg, Belgien
Kontakta ombudet för innehavaren av godkännandet för försäljning om du vill veta mer om detta läkemedel:
Suomi/Finland
Organon Finland Oy
Tel: +358 (0) 29 170 3520
dpoc.finland@organon.com
Denna bipacksedel ändrades senast 12/2022
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats http://www.ema.europa.eu.