DARZALEX injektionsvätska, lösning 1800 mg
Tilläggsinformation
DARZALEX 1 800 mg injektionsvätska, lösning
daratumumab
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller sjuksköterska.
- Om du får biverkningar, tala med läkare eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad DARZALEX är och vad det används för
2. Vad du behöver veta innan du får DARZALEX
3. Hur DARZALEX ges
4. Eventuella biverkningar
5. Hur DARZALEX ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Vad DARZALEX är
DARZALEX är ett läkemedel som innehåller den aktiva substansen daratumumab. Det tillhör en grupp av läkemedel som kallas monoklonala antikroppar. Monoklonala antikroppar är proteiner som har utformats för att känna igen och sätta sig fast på specifika mål i kroppen. Daratumumab har utformats för att sätta sig fast på specifika onormala blodceller i din kropp så att immunförsvaret kan förstöra dessa celler.
Vad DARZALEX används för
DARZALEX används till vuxna som är 18 år eller äldre och som har en typ av cancer kallad multipelt myelom. Det är en cancer i benmärgen.
DARZALEX används till vuxna som är 18 år eller äldre och som har en typ av blod- och benmärgssjukdom som kallas asymtomatiskt multipelt myelom, som kan utvecklas till multipelt myelom.
DARZALEX används också till vuxna som är 18 år eller äldre som har en blodsjukdom som kallas ”AL-amyloidos”. Vid AL-amyloidos tillverkar onormala blodceller höga halter av onormala proteiner som lagras i olika organ, vilket gör att organen inte fungerar som de ska.
Vad du behöver veta innan produkten används
Du får inte behandlas med DARZALEX
- om du är allergisk mot daratumumab eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
Använd inte DARZALEX om ovanstående stämmer in på dig. Om du känner dig osäker ska du tala med läkare eller sjuksköterska innan du får DARZALEX.
Varningar och försiktighet
Tala med läkare eller sjuksköterska innan du får DARZALEX.
Infusionsrelaterade reaktioner
DARZALEX ges som en subkutan injektion med en tunn nål för att injicera läkemedlet under huden. Före och efter varje injektion får du läkemedel som hjälper till att minska risken för infusionsrelaterade reaktioner (se ”Läkemedel som ges under behandlingen med DARZALEX” i avsnitt Hur produkten används). Dessa reaktioner uppkommer mest sannolikt under den första injektionen och de flesta reaktioner uppkommer samma dag. Om du har haft en infusionsrelaterad reaktion en gång är det mindre troligt att det händer igen. Fördröjda reaktioner kan dock uppkomma 3‑4 dagar efter injektionen. Läkaren kan besluta att inte använda DARZALEX om du får en kraftig reaktion efter injektionen.
I vissa fall kan du få en allvarlig allergisk reaktion som kan omfatta svullet ansikte, läppar, mun, tunga eller hals, svårigheter att svälja eller andas eller kliande utslag (nässelfeber). Se avsnitt Eventuella biverkningar.
Tala genast om för läkare eller sjuksköterska om du får någon av de infusionsrelaterade reaktionerna eller relaterade symtom som listas högst upp i avsnitt Eventuella biverkningar. Om du får infusionsrelaterade reaktioner kan du behöva få andra läkemedel för att behandla dina symtom eller så måste kanske injektionen avbrytas. När dessa reaktioner försvinner eller lindras kan injektionen startas igen.
Minskat antal blodkroppar
DARZALEX kan minska antalet vita blodkroppar som hjälper kroppen att bekämpa infektioner, och blodkroppar som kallas blodplättar och som gör att blodet koagulerar. Tala om för läkare eller sjuksköterska om du får symtom på infektion såsom feber, andningssvårigheter, hosta, sveda eller smärta när du kissar eller symtom på minskat antal blodplättar såsom blåmärken eller blödningar.
Blodtransfusioner
Om du behöver få en blodtransfusion tar man först ett blodprov för att kontrollera din blodtyp. DARZALEX kan påverka resultaten av det blodprovet. Tala om för personen som tar provet att du behandlas med DARZALEX.
Hepatit B
Tala om för läkare om du någonsin haft eller nu kan ha hepatit B-infektion. Skälet till detta är att DARZALEX kan leda till återaktivering av hepatit B-virus. Läkaren kommer att kontrollera dig med avseende på tecken på denna infektion före, under och en tid efter behandlingen med DARZALEX. Tala omedelbart om för läkare om du får förvärrad trötthet eller gulnande hud eller ögonvitor.
Barn och ungdomar
Ge inte DARZALEX till barn eller ungdomar under 18 år. Anledningen till detta är att det inte är känt hur läkemedlet kommer att påverka dem.
Andra läkemedel och DARZALEX
Tala om för läkare eller sjuksköterska om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel. Detta gäller även receptfria läkemedel och naturläkemedel.
Graviditet
Om du är gravid, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare innan du får detta läkemedel.
Om du blir gravid under behandlingen med detta läkemedel ska du genast tala om det för läkare eller sjuksköterska. Du och din läkare kommer att bestämma om nyttan av läkemedlet är större än risken för ditt barn.
Preventivmedel
Kvinnor som behandlas med DARZALEX ska använda effektiva preventivmedel under behandlingen och under 3 månader efter behandlingen.
Amning
Du och din läkare avgör om nyttan med amningen överväger riskerna för ditt barn. Anledningen till detta är att läkemedlet kan passera över i bröstmjölk och det är inte känt hur läkemedlet kan påverka barnet.
Körförmåga och användning av maskiner
Du kan känna dig trött efter att ha tagit DARZALEX vilket kan påverka din förmåga att köra bil eller använda maskiner.
DARZALEX injektionsvätska, lösning för subkutan injektion innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per 15 ml, d.v.s. är näst intill “natriumfritt”.
DARZALEX injektionsvätska, lösning för subkutan injektion innehåller sorbitol
Sorbitol är en källa till fruktos. Om du inte tål vissa sockerarter, eller om du har diagnostiserats med hereditär fruktosintolerans, en sällsynt, ärftlig sjukdom som gör att man inte kan bryta ner fruktos, kontakta läkare innan du använder detta läkemedel.
DARZALEX injektionsvätska, lösning för subkutan injektion innehåller polysorbat
Detta läkemedel innehåller 0,4 mg polysorbat 20 i varje ml motsvarande 6,0 mg per 15 ml injektionsflaska. Polysorbater kan orsaka allergiska reaktioner. Tala om för din läkare om du har några kända allergier.
Hur produkten används
Hur mycket DARZALEX ska du få?
Dosen av DARZALEX injektionsvätska, lösning för subkutan injektion är 1 800 mg.
DARZALEX kan ges ensamt eller tillsammans med andra läkemedel som används för att behandla multipelt myelom, eller med andra läkemedel som används för att behandla AL-amyloidos. DARZALEX ges vanligen enligt följande:
- en gång i veckan under de första 8 veckorna
- därefter en gång varannan vecka i 16 veckor
- därefter en gång var 4:e vecka så länge som ditt tillstånd inte förvärras.
När DARZALEX ges tillsammans med andra läkemedel kan din läkare ändra tiden mellan doserna och hur många behandlingar du ska få.
Hur läkemedlet ges
Du får DARZALEX av en läkare eller sjuksköterska som en injektion under huden (subkutan injektion) under cirka 3 till 5 minuter. Det ges i magen (buken) men inte på andra ställen på kroppen. Det ges heller inte på ställen i buken där huden är röd, blånad, öm, hård eller där det finns ärr.
Om du upplever smärta under injektionen kan läkaren eller sjuksköterskan avbryta injektionen och ge dig den kvarvarande injektionen i ett annat område i buken.
Läkaren avgör om du eller din vårdare kan ge DARZALEX efter lämplig utbildning.
Använd alltid detta läkemedel enligt läkarens eller sjuksköterskans anvisningar. Rådfråga läkare, apotekspersonal eller sjuksköterska om du är osäker. Tala med läkare eller apotekspersonal om du känner dig sjuk. Tala med läkaren om när du ska ha dina injektioner och gå på uppföljningsbesök.
Läkemedel som ges under behandlingen med DARZALEX
Du kan få läkemedel som minskar risken att få bältros.
Före varje injektion med DARZALEX kommer du att få läkemedel som hjälper till att minska risken för infusionsrelaterade reaktioner. Det kan vara:
- läkemedel mot allergiska reaktioner (antihistaminer)
- läkemedel mot inflammation (kortikosteroider)
- läkemedel mot feber (t.ex. paracetamol).
Efter varje injektion med DARZALEX kommer du att få läkemedel (t.ex. kortikosteroider) för att minska risken för infusionsrelaterade reaktioner.
Personer med andningsproblem
Om du har andningsproblem, t.ex. astma eller kroniskt obstruktiv lungsjukdom (KOL), kommer du att få läkemedel som du inhalerar och som hjälper mot dina andningsproblem:
- läkemedel som hjälper luftvägarna i lungorna att hålla sig öppna (bronkdilaterare)
- läkemedel som minskar svullnad och irritation i lungorna (kortikosteroider).
Om du har fått för stor mängd av DARZALEX
Detta läkemedel kommer att ges av läkare eller sjuksköterska. Om det osannolika skulle inträffa att du får för mycket (en överdos) kommer din läkare att kontrollera om du får några biverkningar.
Om du glömmer ett behandlingstillfälle med DARZALEX
Det är mycket viktigt att du kommer till alla inbokade behandlingstillfällen för att din behandling ska fungera. Om du glömmer ett behandlingstillfälle ska du boka in ett nytt så fort som möjligt.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare eller sjuksköterska.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Infusionsrelaterade reaktioner
Tala genast om för läkare eller sjuksköterska om du får något av följande symtom inom 3‑4 dagar efter injektionen. Du kan behöva andra läkemedel, eller behandlingen kan behöva justeras.
Dessa reaktioner inkluderar följande symtom:
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare):
- frossa
- halsont, hosta
- illamående
- kräkningar
- kliande, rinnande eller täppt näsa
- andfåddhet eller andra andningsproblem.
Vanliga (kan förekomma hos upp till 1 av 10 användare):
- obehag i bröstet
- yrsel eller svimningskänsla (blodtrycksfall)
- klåda
- väsande andning.
Sällsynta (kan förekomma hos upp till 1 av 1 000 användare):
- allvarlig allergisk reaktion som kan omfatta svullet ansikte, läppar, mun, tunga eller hals, svårigheter att svälja eller andas eller kliande utslag (nässelfeber). Se avsnitt Vad du behöver veta innan produkten används
- ögonsmärta
- dimsyn.
Om du får någon av ovanstående infusionsrelaterade reaktioner, ska du genast tala om det för läkare eller sjuksköterska.
Reaktioner vid injektionsstället
Hudreaktioner vid eller nära injektionsstället (lokalt), inklusive reaktioner vid injektionsstället kan uppkomma med DARZALEX injektionsvätska, lösning för subkutan injektion. Dessa reaktioner är mycket vanliga (kan förekomma hos fler än 1 av 10 användare). Symtomen vid injektionsstället kan inkludera hudrodnad, klåda, svullnad, smärta, blåmärken, hudutslag, blödning.
Andra biverkningar
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare):
- feber
- kraftig trötthet
- diarré
- förstoppning
- buksmärta
- minskad aptit
- sömnsvårigheter
- huvudvärk
- nervskada som kan ge stickningar, domningar eller smärta
- hudutslag
- muskelspasmer
- muskel- och ledsmärta (inklusive ryggsmärta och bröstmuskelsmärta)
- svullna händer, vrister eller fötter
- svaghetskänsla
- lunginfektion (lunginflammation)
- luftrörskatarr
- infektioner i luftvägarna – t.ex. i näsa, bihålor eller svalg
- lågt antal röda blodkroppar som transporterar syre i blodet (anemi, blodbrist)
- lågt antal vita blodkroppar som hjälper till att bekämpa infektioner (neutropeni, lymfopeni, leukopeni)
- lågt antal av en typ av blodkroppar som kallas blodplättar och som hjälper blodet att koagulera (trombocytopeni)
- låg nivå av kalium i blodet (hypokalemi)
- covid-19.
Vanliga (kan förekomma hos upp till 1 av 10 användare):
- oregelbundna hjärtslag (förmaksflimmer)
- vätskeansamling i lungorna som leder till andfåddhet
- urinvägsinfektion
- svår infektion som påverkar hela kroppen (sepsis)
- uttorkning
- hög blodsockernivå
- låg kalciumnivå i blodet
- låg antikroppsnivå av så kallade ”immunoglobuliner” i blodet, vilka hjälper till att bekämpa infektioner (hypogammaglobulinemi)
- yrsel
- svimning
- frossa
- klåda
- onormal känsla i huden (en stickande eller krypande känsla)
- bukspottkörtelinflammation
- högt blodtryck.
Mindre vanliga (kan förekomma hos upp till 1 av 100 användare):
- leverinflammation (hepatit)
- en typ av herpesvirusinfektion (cytomegalovirusinfektion).
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på kartongen och injektionsflaskans etikett efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras i kylskåp (2 °C ‑ 8 °C). Får ej frysas.
Förvaras i originalförpackningen. Ljuskänsligt.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Sjukvårdspersonalen kommer att kasta allt läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är daratumumab. 1 ml lösning innehåller 120 mg daratumumab. 1 injektionsflaska med 15 ml injektionsvätska, lösning innehåller 1 800 mg daratumumab.
- Övriga innehållsämnen är rekombinant humant hyaluronidas (rHuPH20), L‑histidin, L‑histidinhydrokloridmonohydrat, L‑metionin, polysorbat 20 (E432), sorbitol (E420) och vatten för injektionsvätskor (se DARZALEX innehåller natrium och sorbitol i avsnitt Vad du behöver veta innan produkten används).
Läkemedlets utseende och förpackningsstorlekar
DARZALEX injektionsvätska, lösning för subkutan injektion är en färglös till gul vätska.
DARZALEX injektionsvätska, lösning för subkutan injektion tillhandahålls i en kartong innehållande 1 injektionsflaska med en engångsdos.
Innehavare av godkännande för försäljning
Janssen-Cilag International NV
Turnhoutseweg 30
B-2340 Beerse
Belgien
Tillverkare
Janssen Biologics B.V.
Einsteinweg 101
NL-2333 CB Leiden
Nederländerna
Janssen Pharmaceutica NV
Turnhoutseweg 30
B-2340 Beerse
Belgien
Kontakta ombudet för innehavaren av godkännandet för försäljning om du vill veta mer om detta läkemedel:
Suomi/Finland Janssen-Cilag Oy Puh/Tel: +358 207 531 300 jacfi@its.jnj.com |
Denna bipacksedel ändrades senast 03/2026.
Övriga informationskällor
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats https://www.ema.europa.eu.
Direktiv för experterna inom hälsovården
DARZALEX injektionsvätska, lösning för subkutan injektion ska administreras av hälso- och sjukvårdspersonal.
För att förhindra medicineringsfel är det viktigt att kontrollera injektionsflaskornas etiketter för att säkerställa att korrekt beredning (intravenös eller subkutan beredning) och dos ges till patienten enligt ordination. DARZALEX injektionsvätska, lösning ska endast ges som en subkutan injektion i de rekommenderade doserna. DARZALEX subkutan beredning är inte avsedd för intravenös administrering.
DARZALEX injektionsvätska, lösning för subkutan injektion är avsedd för engångsbruk och är bruksfärdig.
- DARZALEX injektionsvätska, lösning för subkutan injektion är kompatibel med sprutmaterial av polypropen eller polyeten, subkutana infusionsset av polypropen, polyeten eller polyvinylklorid (PVC) och överförings- och injektionsnålar av rostfritt stål.
- DARZALEX injektionsvätska, lösning för subkutan injektion ska vara en klar till opaliserande och färglös till gul lösning. Använd inte om opaka partiklar, missfärgning eller andra främmande partiklar förekommer.
- Ta ut DARZALEX injektionsvätska, lösning för subkutan injektion ur kylskåpet (2 °C ‑ 8 °C) och låt den uppnå omgivningstemperatur (15 °C ‑ 30 °C). Den opunkterade injektionsflaskan kan förvaras i omgivningstemperatur och omgivningsljus under högst 24 timmar i originalkartongen. Ljuskänsligt. Förvara inte i direkt solljus. Skaka inte.
- Bered doseringssprutan under kontrollerade och validerade aseptiska förhållanden. Dra upp 15 ml från injektionsflaskan med en överföringsnål på 18 G–22 G med standardspets för att minimera risken för att partiklar från proppen lossnar och följer med in i injektionsflaskan. För in nålspetsen i injektionsflaskan i 90° vinkel inom ringen som omger proppen, och minimera antalet punkteringar för att motverka att partiklar lossnar från proppen. Inspektera innehållet i sprutan för att säkerställa att det inte förekommer några partiklar, missfärgningar eller andra främmande partiklar.
- För att förhindra att nålen täpps till ska den hypodermiska injektionsnålen eller det subkutana infusionssetet monteras på sprutan precis före injektion.
Förvaring av beredd spruta
- Om sprutan med DARZALEX inte används omedelbart, kan den förvaras upp till 24 timmar i kylskåp, följt av upp till 12 timmar vid 15 °C - 25 °C i omgivningsljus. Vid förvaring i kylskåp, låt lösningen nå omgivningstemperatur innan administrering.
Administrering
- Injicera 15 ml DARZALEX injektionsvätska, lösning för subkutan injektion i den subkutana vävnaden i buken cirka 7,5 cm till höger eller vänster om naveln under cirka 3‑5 minuter. Injicera inte DARZALEX injektionsvätska, lösning för subkutan injektion på andra ställen på kroppen eftersom det inte finns tillgängliga data.
- Växla injektionsställen för injektioner som ges efter varandra.
- DARZALEX injektionsvätska, lösning för subkutan injektion ska aldrig injiceras i områden med röd, blånad, öm eller hård hud eller områden med ärrbildning.
- Pausa injektionen eller sänk injektionshastigheten om patienten upplever smärta. Om smärtan inte lindras vid en långsammare injektion, kan ett andra injektionsställe på motsatt sida av buken väljas för administrering av den kvarvarande dosen.
- Under behandling med DARZLEX injektionsvätska, lösning för subkutan injektion ska inte andra läkemedel för subkutan användning administreras på samma ställe som DARZALEX.
- Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.
Spårbarhet
För att underlätta spårbarhet av biologiska läkemedel ska läkemedlets namn och tillverkningssatsnummer dokumenteras.
Direktiv för användaren
Följande uppgifter är endast avsedda för patienter och vårdare:
Bruksanvisning
Din vårdgivare kommer att ge de första injektionerna av DARZALEX subkutant (under huden), nedan kallat DARZALEX. Därefter kan du och din läkare bestämma att du eller en vårdare kan injicera DARZALEX. Om det blir så, får du eller vårdaren utbildning av vårdgivaren i hur man förbereder och injicerar DARZALEX. Tala med läkaren om du har några frågor om att ge dig själv en injektion.
Förvaring
Förvaring av oöppnad injektionsflaska
Förvaras i kylskåp vid 2 °C–8 °C. När injektionsflaskan med DARZALEX har tagits ut ur kylskåpet får den inte sättas in i kylskåpet igen.
Förvara detta läkemedel utom syn- och räckhåll för barn.
Tillbehör

1. Inspektera kartongen och kontrollera injektionsflaskan

2. Förbered för injektionen

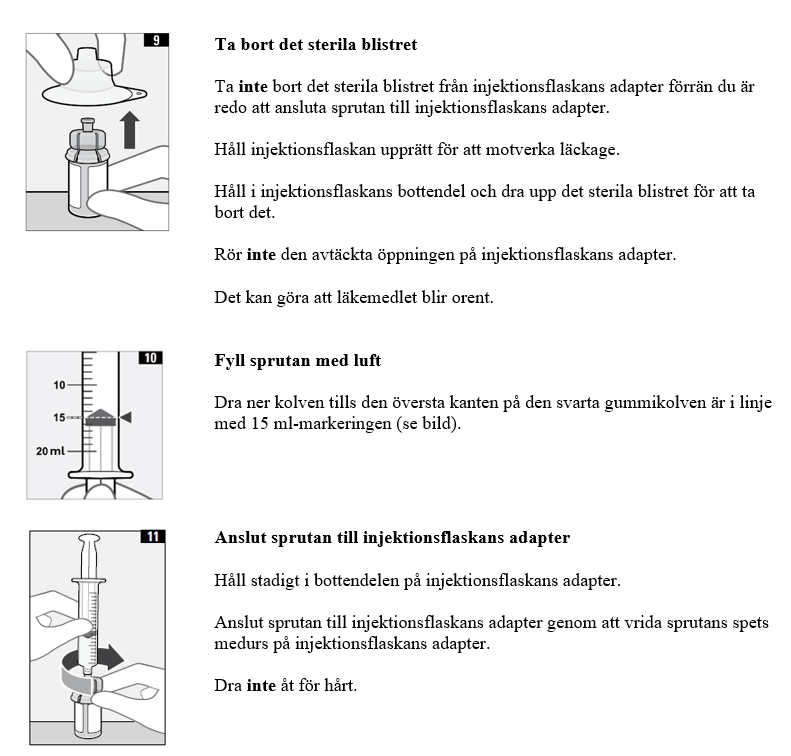
3. Förbered injektionsflaskan och sprutan






4. Injicera läkemedlet

