DARZALEX injektioneste, liuos 1800 mg
DARZALEX 1 800 mg injektioneste, liuos
daratumumabi
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin sinulle annetaan tätä lääkettä, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai sairaanhoitajan puoleen.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä DARZALEX on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin sinulle annetaan DARZALEX-valmistetta
3. Miten DARZALEX-valmistetta annetaan
4. Mahdolliset haittavaikutukset
5. DARZALEX-valmisteen säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Mitä DARZALEX on
DARZALEX on lääke, joka sisältää vaikuttavana aineena daratumumabia. Se kuuluu monoklonaalisiksi vasta-aineiksi kutsuttujen lääkkeiden ryhmään. Monoklonaaliset vasta-aineet ovat valkuaisaineita (proteiineja), joiden on tarkoitus tunnistaa elimistössä tietyt kohteet ja kiinnittyä niihin. Daratumumabi on kehitetty kiinnittymään tietyntyyppisiin poikkeaviin verisoluihin elimistössä, jotta immuunijärjestelmä voi tuhota ne.
Mihin DARZALEX-valmistetta käytetään
DARZALEX-valmistetta käytetään aikuisille (vähintään 18-vuotiaille), jotka sairastavat multippeliksi myeloomaksi kutsuttua syöpätyyppiä, joka on luuydinsyöpä.
DARZALEX-valmistetta käytetään aikuisille (vähintään 18-vuotiaille), jotka sairastavat indolentiksi multippeliksi myeloomaksi kutsuttua veri- ja luuydinsairautta, joka voi edetä multippeliksi myeloomaksi.
DARZALEX-valmistetta käytetään myös 18-vuotiaille tai vanhemmille aikuisille, joilla on tietyntyyppinen verisairaus nimeltään AL-amyloidoosi. AL-amyloidoosissa poikkeavat verisolut tuottavat liikaa poikkeavia valkuaisaineita eli proteiineja, jotka kertyvät eri elimiin, minkä vuoksi elimet eivät toimi kunnolla.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Sinulle ei saa antaa DARZALEX-valmistetta
- jos olet allerginen daratumumabille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
Älä käytä DARZALEX-valmistetta, jos edellä mainittu koskee sinua. Jos olet epävarma, käänny lääkärin tai sairaanhoitajan puoleen, ennen kuin sinulle annetaan DARZALEX-valmistetta.
Varoitukset ja varotoimet
Keskustele lääkärin tai sairaanhoitajan kanssa ennen kuin saat DARZALEX-valmistetta.
Infuusioon liittyvät reaktiot
DARZALEX annetaan injektiona ihon alle eli lääke annetaan pistoksena ihon alle käyttämällä pientä neulaa. Sinulle annetaan ennen jokaista injektiota ja jokaisen injektion jälkeen lääkkeitä, jotka vähentävät infuusioon liittyvien reaktioiden todennäköisyyttä (ks. kohta Miten valmistetta käytetään DARZALEX-hoidon aikana annettavat lääkkeet). Tällaiset reaktiot ovat todennäköisimpiä ensimmäisen pistoksen yhteydessä, ja ne ilmaantuvat useimmiten pistoksen antopäivänä. Jos sinulla on kerran ollut infuusioon liittynyt reaktio, sen ilmaantuminen uudelleen on epätodennäköisempää. Viivästyneitä reaktioita voi kuitenkin ilmetä enintään 3–4 päivää injektion jälkeen. Lääkäri saattaa päättää olla antamatta DARZALEX-pistoksia, jos injektioreaktio on voimakas.
Joissakin tapauksissa voi ilmaantua vaikea-asteinen allerginen reaktio, johon voi liittyä kasvojen, huulten, suun, kielen tai kurkun turpoamista, nielemis- tai hengitysvaikeuksia tai kutisevaa ihottumaa (nokkosihottumaa). Ks. kohta Mahdolliset haittavaikutukset.
Kerro heti lääkärille tai sairaanhoitajalle, jos sinulle ilmaantuu jokin kohdan Mahdolliset haittavaikutukset alussa mainituista infuusioon liittyvistä reaktioista tai muita vastaavia oireita. Jos sinulle ilmaantuu infuusioon liittyvä reaktio, saatat tarvita muita lääkkeitä tai pistosten anto saattaa olla tarpeen lopettaa. Pistoksen antamista voidaan jatkaa, kun reaktio häviää tai lievenee.
Vähentynyt verisolujen määrä
DARZALEX voi vähentää infektioiden torjuntaan osallistuvien veren valkosolujen määrää sekä veren hyytymiseen osallistuvien verihiutaleiksi kutsuttujen verisolujen määrää. Kerro terveydenhuollon ammattilaiselle, jos sinulle ilmaantuu infektion oireita, kuten kuumetta, hengitysvaikeuksia, yskää tai kirvelyä tai kipua virtsatessa, tai jos sinulla on verihiutaleiden määrän vähenemisestä aiheutuvia oireita, kuten mustelmia tai verenvuotoa.
Verensiirrot
Jos tarvitset verensiirron, sinulta otetaan ensin verikoe veriryhmäsi määrittämiseksi. DARZALEX voi vaikuttaa veriryhmämäärityksen tuloksiin. Kerro määrityksen tekijälle, että käytät DARZALEX-valmistetta.
B-hepatiitti
Kerro lääkärille, jos sinulla on joskus ollut tai saattaa parhaillaan olla B-hepatiitti‑infektio, sillä DARZALEX voi aktivoida hepatiitti B ‑viruksen uudelleen. Lääkäri tutkii sinulta tällaiseen infektioon viittaavat oireet ennen DARZALEX-hoitoa, hoidon aikana ja jonkin aikaa hoidon jälkeen. Kerro lääkärille heti, jos sinulla on lisääntyvää väsymystä tai ihosi tai silmänvalkuaisesi muuttuvat keltaisiksi.
Lapset ja nuoret
DARZALEX-valmistetta ei saa antaa lapsille eikä alle 18-vuotiaille nuorille, koska lääkkeen vaikutusta heihin ei tunneta.
Muut lääkevalmisteet ja DARZALEX
Kerro lääkärille tai sairaanhoitajalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä. Tämä koskee myös ilman lääkemääräystä saatavia lääkkeitä ja rohdosvalmisteita.
Raskaus
Jos olet raskaana, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä neuvoa ennen tämän lääkkeen käyttöä.
Jos tulet raskaaksi tämän lääkkeen käytön aikana, kerro siitä heti lääkärille tai sairaanhoitajalle. Päätät yhdessä lääkärin kanssa, onko lääkkeestä saatava hyöty suurempi kuin lapselle aiheutuva riski.
Raskauden ehkäisy
DARZALEX-hoitoa saavien naisten pitää käyttää tehokasta ehkäisyä hoidon aikana ja kolmen kuukauden ajan hoidon jälkeen.
Imetys
Päätät yhdessä lääkärin kanssa, ovatko imetyksen hyödyt suuremmat kuin vauvalle aiheutuvat riskit. Lääkettä saattaa erittyä rintamaitoon eikä tiedetä, miten se vaikuttaa lapseen.
Ajaminen ja koneiden käyttö
Sinua saattaa väsyttää DARZALEX-hoidon saamisen jälkeen, mikä saattaa vaikuttaa ajokykyyn ja kykyyn käyttää koneita.
Ihon alle annettava DARZALEX-injektioneste sisältää natriumia
Tämä lääkevalmiste sisältää alle 1 mmol natriumia (23 mg) per 15 ml eli sen voidaan sanoa olevan ”natriumiton”.
Ihon alle annettava DARZALEX-injektioneste sisältää sorbitolia
Sorbitoli on fruktoosin lähde. Jos lääkäri on kertonut, että sinulla on jokin sokeri-intoleranssi tai jos sinulla on todettu perinnöllinen fruktoosi-intoleranssi (HFI, harvinainen geneettinen sairaus, jossa elimistö ei kykene hajottamaan fruktoosia), keskustele lääkärin kanssa ennen tämän lääkkeen ottamista.
Ihon alle annettava DARZALEX-injektioneste sisältää polysorbaattia
Tämä lääkevalmiste sisältää 0,4 mg polysorbaatti 20:ta per ml, mikä vastaa 6,0 mg:aa per 15 ml:n injektiopullo. Polysorbaatit saattavat aiheuttaa allergisia reaktioita. Jos sinulla on allergioita, kerro asiasta lääkärille.
Miten valmistetta käytetään
Miten paljon lääkettä annetaan
Ihon alle annettavan DARZALEX-injektionesteen annos on 1 800 mg.
DARZALEX saatetaan antaa yksinään tai yhdessä muiden multippelin myelooman hoitoon käytettävien lääkkeiden kanssa tai yhdessä muiden AL-amyloidoosin hoitoon käytettävien lääkkeiden kanssa. DARZALEX annetaan tavallisesti seuraavasti:
- kahdeksan ensimmäisen viikon ajan kerran viikossa
- tämän jälkeen saat lääkettä 16 viikon ajan joka toinen viikko
- tämän jälkeen saat lääkettä joka neljäs viikko niin pitkään, kun sairautesi ei pahene.
Mikäli DARZALEX-valmistetta annetaan yhdessä muiden lääkkeiden kanssa, saattaa lääkäri muuttaa annosten välisen ajan pituutta sekä hoitokertojesi määrää.
Miten lääke annetaan
Lääkäri tai hoitaja antaa DARZALEX-valmisteen noin 3–5 minuutin kestoisena pistoksena ihon alle (ihonalaisena injektiona). Pistos annetaan mahan alueelle (vatsaan), mutta sitä ei saa antaa muualle kehoon eikä vatsassa alueille, joilla on punoitusta, mustelma, aristusta, kovettuma tai arpia.
Jos tunnet kipua pistoksen aikana, lääkäri tai sairaanhoitaja voi keskeyttää pistoksen antamisen ja antaa loput pistoksesta toiseen kohtaan vatsassa.
Lääkäri päättää, voitko sinä pistää DARZALEX-pistokset itse tai voiko sinua hoitava henkilö antaa pistokset sinulle asianmukaisen opastuksen saamisen jälkeen.
Käytä tätä lääkettä juuri siten kuin lääkäri on määrännyt tai sairaanhoitaja on neuvonut. Tarkista ohjeet lääkäriltä, apteekista tai sairaanhoitajalta, jos olet epävarma. Jos tunnet olosi huonovointiseksi, käänny lääkärin tai apteekkihenkilökunnan puoleen. Kysy lääkäriltä, milloin pistokset pitää pistää ja milloin seurantakäyntejä tehdään.
DARZALEX-hoidon aikana annettavat lääkkeet
Sinulle saatetaan antaa lääkettä vyöruusun todennäköisyyden vähentämiseksi.
Sinulle annetaan ennen jokaista DARZALEX‑pistosta lääkkeitä infuusioon liittyvien reaktioiden todennäköisyyden vähentämiseksi. Tällaisia lääkkeitä ovat
- allergisia reaktioita estävät lääkkeet (antihistamiinit)
- tulehdusta vaimentavat lääkkeet (kortikosteroidit)
- kuumelääkkeet (esim. parasetamoli).
Jokaisen DARZALEX‑pistoksen jälkeen sinulle annetaan lääkkeitä (esim. kortikosteroideja) infuusioon liittyvien reaktioiden todennäköisyyden vähentämiseksi.
Hengityselinsairaudet
Jos sinulla on hengityselinsairaus, kuten astma tai keuhkoahtaumatauti, sinulle annetaan inhaloitavia lääkkeitä, jotka lievittävät hengitysvaikeuksia
- keuhkoputkia laajentavia lääkkeitä (bronkodilaattoreita)
- keuhkojen turvotusta ja ärsytystä vähentäviä lääkkeitä (kortikosteroideja).
Jos sinulle annetaan enemmän DARZALEX-valmistetta kuin pitäisi
Tämän lääkkeen antaa lääkäri tai sairaanhoitaja. Jos kuitenkin saat lääkettä liikaa (yliannoksen), lääkäri seuraa sinua haittavaikutusten havaitsemiseksi.
Jos unohdat DARZALEX-hoitoa varten sovitun hoitokäynnin
On erittäin tärkeää käydä kaikilla sovituilla hoitokäynneillä sen varmistamiseksi, että hoito toimii. Jos sinulta jää menemättä sovitulle hoitokäynnille, varaa uusi aika mahdollisimman pian.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai sairaanhoitajan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Infuusioon liittyvät reaktiot
Kerro heti lääkärille tai sairaanhoitajalle, jos sinulle ilmaantuu jokin seuraavista oireista 3–4 päivän kuluessa pistoksen jälkeen. Saatat tarvita muita lääkkeitä tai pistoksen anto saattaa olla tarpeen keskeyttää tai lopettaa.
Tällaisia reaktioita ovat seuraavat oireet:
Hyvin yleiset (saattavat esiintyä useammalla kuin yhdellä potilaalla 10:stä):
- vilunväristykset
- kurkkukipu, yskä
- pahoinvointi
- oksentelu
- nenän kutina, vuotaminen tai tukkoisuus
- hengenahdistuksen tunne tai muut hengitysvaikeudet.
Yleiset (saattavat esiintyä enintään yhdellä potilaalla 10:stä) ovat:
- epämukavat tuntemukset rintakehässä
- heitehuimaus tai pyörrytyksen tunne (matala verenpaine)
- kutina
- hengityksen vinkuminen.
Harvinaiset (saattavat esiintyä useammalla kuin yhdellä potilaalla 1 000:sta):
- vaikea allerginen reaktio, johon saattaa liittyä kasvojen, huulten, suun, kielen tai kurkun turpoamista, nielemis- tai hengitysvaikeuksia tai kutisevaa ihottumaa (nokkosihottumaa). Ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä
- silmäkipu
- hämärtynyt näkö.
Jos sinulle ilmaantuu jokin edellä mainituista infuusioon liittyvistä reaktioista, kerro siitä heti lääkärille tai sairaanhoitajalle.
Pistoskohdan reaktiot
Ihon alle annettavan DARZALEX-pistoksen yhteydessä pistoskohdassa tai sen lähellä (paikallisesti) voi esiintyä ihoreaktioita, mukaan lukien pistoskohdan reaktioita. Tällaiset reaktiot ovat hyvin yleisiä (saattavat esiintyä useammalla kuin yhdellä potilaalla 10:stä). Pistoskohdassa havaittavia oireita voivat olla ihon punoitus, kutina, turpoaminen, kipu, mustelma, ihottuma, verenvuoto.
Muut haittavaikutukset
Hyvin yleiset (saattavat esiintyä useammalla kuin yhdellä potilaalla 10:stä):
- kuume
- voimakas väsymyksen tunne
- ripuli
- ummetus
- vatsakipu
- heikentynyt ruokahalu
- univaikeudet
- päänsärky
- hermovaurio, josta voi aiheutua kihelmöintiä, tunnottomuutta tai kipua
- ihottuma
- lihasspasmit
- lihas- ja nivelkipu (mukaan lukien selkäkipu ja lihaskipu rintakehässä)
- käsien, nilkkojen tai jalkaterien turpoaminen
- heikotuksen tunne
- keuhkoinfektio (keuhkokuume eli pneumonia)
- keuhkoputkitulehdus
- hengitysteiden (nenän, sivuonteloiden, nielun) tulehdus
- happea veressä kuljettavien veren punasolujen vähyys (anemia)
- infektioita elimistössä torjuvien veren valkosolujen vähyys (neutropenia, lymfopenia, leukopenia)
- veren hyytymiseen osallistuvien verisolujen eli verihiutaleiden vähyys (trombosytopenia)
- pieni veren kaliumpitoisuus (hypokalemia)
- koronavirustauti (covid-19).
Yleiset (saattavat esiintyä enintään yhdellä potilaalla 10:stä):
- sydämen rytmihäiriöt (eteisvärinä)
- nesteen kertyminen keuhkoihin, mistä saattaa aiheutua hengenahdistusta
- virtsatieinfektio
- vaikea-asteinen koko elimistön infektio (verenmyrkytys eli sepsis)
- elimistön kuivuminen
- suuri verensokeripitoisuus
- pieni veren kalsiumpitoisuus
- pieni immunoglobuliineiksi kutsuttujen vasta-aineiden pitoisuus veressä; immunoglobuliinit osallistuvat infektioiden torjumiseen (hypogammaglobulinemia)
- huimauksen tunne
- pyörtyminen
- vilunväristykset
- kutina
- epätavalliset tuntemukset ihossa (kuten pistelyn ja kihelmöinnin tunne)
- haimatulehdus
- korkea verenpaine.
Melko harvinaiset (saattavat esiintyä enintään yhdellä potilaalla 100:sta):
- maksatulehdus (hepatiitti)
- eräänlainen herpesvirusinfektio (sytomegalovirusinfektio).
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa ja injektiopullon etiketissä mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä jääkaapissa (2 °C – 8 °C). Ei saa jäätyä.
Säilytä alkuperäispakkauksessa. Herkkä valolle.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Terveydenhuollon ammattilainen hävittää mahdollisesti käyttämättä jäävät lääkkeet. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä DARZALEX sisältää
- Vaikuttava aine on daratumumabi. Yksi millilitra liuosta sisältää 120 mg daratumumabia. Yksi 15 ml:n injektiopullo injektionestettä, liuosta, sisältää 1 800 mg daratumumabia.
- Muut aineet ovat rekombinantti ihmisen hyaluronidaasi (rHuPH20), L‑histidiini, L‑histidiinihydrokloridimonohydraatti, L‑metioniini, polysorbaatti 20 (E432), sorbitoli (E420) ja injektionesteisiin käytettävä vesi (ks. DARZALEX sisältää natriumia kohdassa Mitä sinun on tiedettävä ennen valmisteen käyttöä).
Lääkevalmisteen kuvaus ja pakkauskoko (-koot)
Ihon alle annettava DARZALEX-injektioneste, liuos, on väritön tai keltainen liuos.
Ihon alle annettavaa DARZALEX-injektionestettä, liuosta, on saatavana pakkauksina, jotka sisältävät 1 kerta-annoksen lasisessa injektiopullossa.
Myyntiluvan haltija
Janssen-Cilag International NV
Turnhoutseweg 30
B-2340 Beerse
Belgia
Valmistaja
Janssen Biologics B.V.
Einsteinweg 101
NL-2333 CB Leiden
Alankomaat
Janssen Pharmaceutica NV
Turnhoutseweg 30
B-2340 Beerse
Belgia
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Suomi/Finland Janssen-Cilag Oy Puh/Tel: +358 207 531 300 jacfi@its.jnj.com |
Tämä pakkausseloste on tarkistettu viimeksi 03/2026.
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla https://www.ema.europa.eu.
Ohjeet terveydenhuollon ammattilaiselle
Terveydenhuollon ammattilainen antaa ihon alle annettavan DARZALEX-injektionesteen, liuoksen.
Lääkitysvirheiden välttämiseksi on tärkeää tarkistaa injektiopullon etiketistä, että potilaalle annetaan asianmukaista valmistetta (laskimoon tai ihon alle annettava valmiste) ja että potilaalle annetaan lääkemääräyksen mukainen annos. DARZALEX-injektionesteen, liuoksen, saa antaa vain ihon alle mainittuna annoksena. Ihon alle annettava DARZALEX-valmiste ei ole tarkoitettu annettavaksi laskimoon.
Ihon alle annettava DARZALEX-injektioneste on käyttövalmis ja tarkoitettu vain yhteen käyttökertaan.
- Ihon alle annettava DARZALEX-injektioneste on yhteensopiva polypropeenista tai polyeteenista valmistettujen ruiskujen kanssa, polypropeenista, polyeteenista tai polyvinyylikloridista (PVC) valmistettujen ihon alle antoon tarkoitettujen infuusiovälineiden kanssa sekä ruostumattomasta teräksestä valmistettujen siirto- ja injektioneulojen kanssa.
- Ihon alle annettavan DARZALEX-injektionesteen pitää olla kirkas tai opalisoiva ja väritön tai keltainen liuos. Jos liuoksessa on läpinäkymättömiä hiukkasia, värimuutoksia tai muita vieraspartikkeleita, älä käytä sitä.
- Ota ihon alle annettavan DARZALEX-injektionesteen sisältävä injektiopullo jääkaappisäilytyksestä (2 °C – 8 °C), ja anna sen lämmetä vallitsevaan lämpötilaan (15 °C – 30 °C). Avaamatonta injektiopulloa voidaan säilyttää vallitsevassa lämpötilassa ja vallitsevassa valossa enintään 24 tunnin ajan alkuperäispakkauksessa. Herkkä valolle. Pidä poissa suorasta auringonvalosta. Ei saa ravistaa.
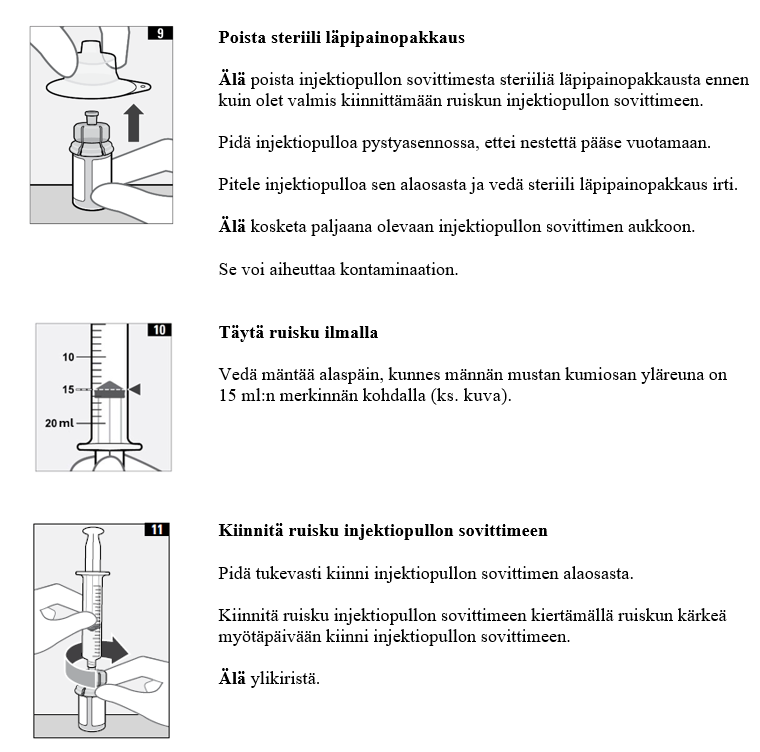
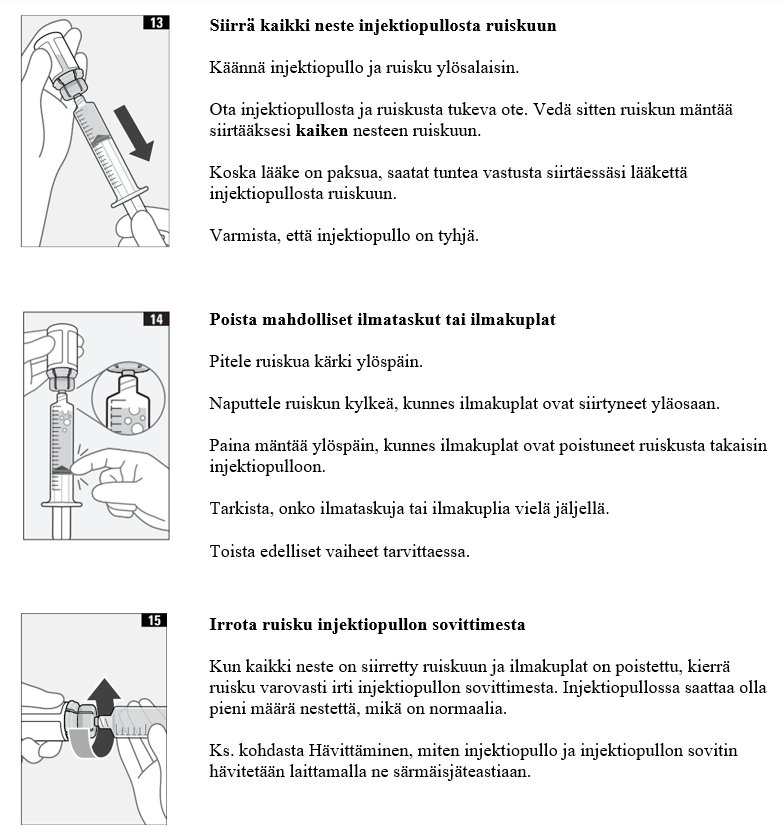
- Valmistele annosteluruisku antoa varten kontrolloiduissa ja validoiduissa aseptisissa olosuhteissa. Vedä injektiopullosta 15 ml ruiskuun käyttämällä 18–22G:n siirtoneulaa, jossa on tavanomainen viistokärki, jotta tulpan materiaalin irtoamisen riski minimoituu. Työnnä neula injektiopulloon kohtisuoraan (90°:n kulmassa) tulpan renkaaseen nähden ja minimoi lävistyskerrat tulpan rikkoutumisen välttämiseksi. Tarkista ruiskun sisältö varmistaaksesi, ettei siinä ole hiukkasia, värimuutoksia eikä muita vierashiukkasia.
- Kiinnitä hypoderminen injektioneula tai ihon alle antoon käytettävä infuusiolaite ruiskuun juuri ennen injektion antamista, jotta vältetään neulan tukkeutuminen.
Käyttövalmiin ruiskun säilyttäminen
- Jos ruiskussa olevaa DARZALEX-injektionestettä ei käytetä heti, säilytä DARZALEX-injektionestettä enintään 24 tuntia jääkaapissa ja sen jälkeen enintään 12 tuntia 15 °C ‑ 25 °C:ssa ja vallitsevassa valossa. Anna jääkaapissa säilytetyn liuoksen lämmetä vallitsevaan lämpötilaan ennen antoa.
Anto
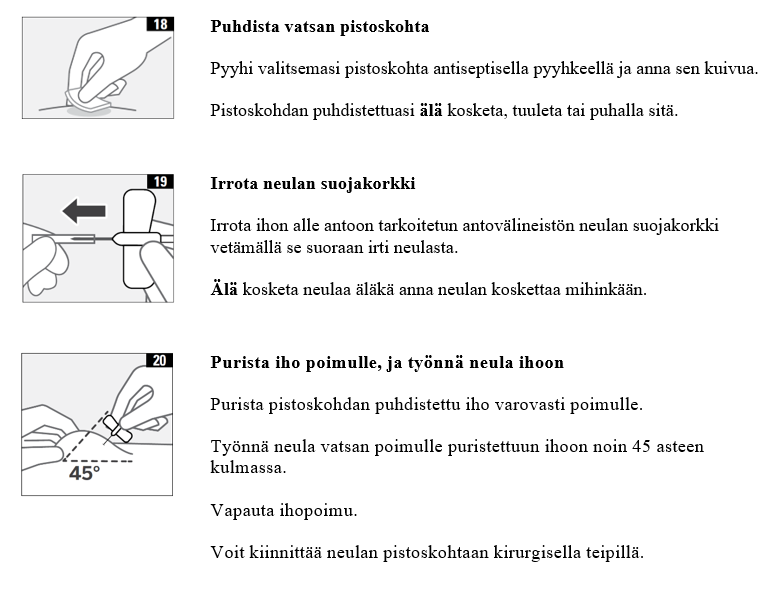
- Injisoi 15 ml DARZALEX-injektionestettä vatsan ihonalaiskudokseen noin 7,5 cm navan oikealle tai vasemmalle puolelle noin 3–5 minuutin kestoisena injektiona. Älä injisoi ihon alle annettavaa DARZALEX-injektionestettä muualle kehoon, sillä siitä ei ole tietoja saatavissa.
- Peräkkäisissä injektioissa on käytettävä eri injektiokohtaa.
- Ihon alle annettavaa DARZALEX-injektionestettä ei pidä koskaan injisoida ihoalueille, joilla on punoitusta, mustelma, aristusta, kovettuma tai arpia.
- Jos injektiosta aiheutuu potilaalle kipua, injektion antoa voidaan tauottaa tai hidastaa. Jos kipu ei lievity injektion antoa hidastamalla, loput annoksesta voidaan antaa toiseen injektiokohtaan vatsan toiselle puolelle.
- Ihon alle annettavan DARZALEX-valmisteen käytön aikana DARZALEX-valmisteen antokohtiin ei saa antaa ihon alle muita lääkevalmisteita.
- Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Jäljitettävyys
Biologisten lääkevalmisteiden jäljitettävyyden parantamiseksi on annetun valmisteen nimi ja eränumero dokumentoitava selkeästi.
Ohjeet käyttäjälle
Seuraavat tiedot on tarkoitettu vain potilaille ja potilaita hoitaville henkilöille:
Käyttöohjeet
Terveydenhuollon ammattilainen antaa ensimmäiset ihon alle annettavat DARZALEX-pistokset. Sen jälkeen sinä ja lääkäri voitte yhdessä päättää, että sinä voit pistää DARZALEX-pistokset itse tai sinua hoitava henkilö voi antaa pistokset sinulle. Siinä tapauksessa terveydenhuollon ammattilainen opastaa sinulle tai sinua hoitavalle henkilölle, miten DARZALEX-valmiste valmistellaan ja pistetään. Jos sinulla on kysyttävää pistoksen pistämisestä itse, käänny lääkärin puoleen.
Säilytys
Avaamattoman injektiopullon säilytys
Säilytä jääkaapissa (2 °C – 8 °C). Kun DARZALEX-injektiopullo on otettu jääkaapista, sitä ei saa enää laittaa takaisin jääkaappiin.
Pidä lääke poissa lasten ulottuvilta ja näkyviltä.
Tarvikkeet

1. Tarkista kartonkikotelo ja injektiopullo

2. Valmistele pistos


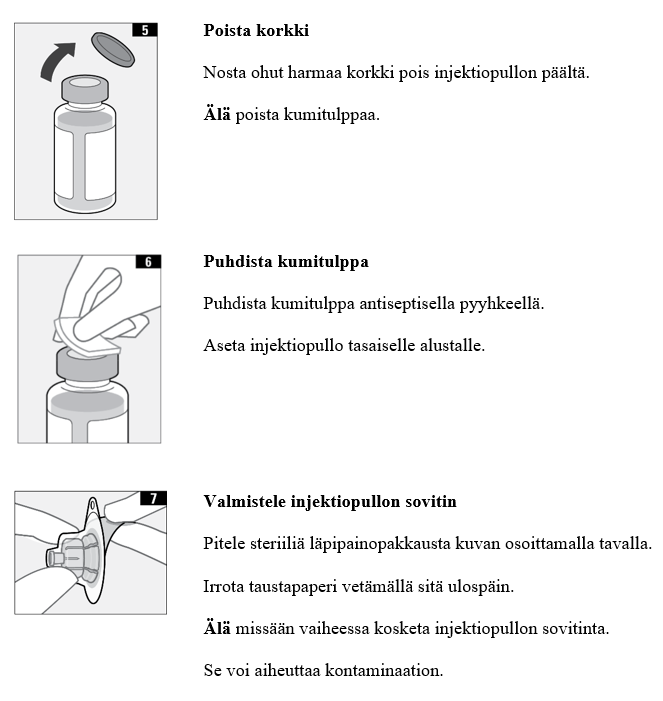
3. Valmistele injektiopullo ja ruisku




4. Pistä lääke