ASPAVELI infusionsvätska, lösning 1080 mg
Tilläggsinformation
ASPAVELI 1 080 mg infusionsvätska, lösning
pegcetakoplan
Utökad övervakning
▼ Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar du eventuellt får. Information om hur du rapporterar biverkningar finns i slutet av avsnitt Eventuella biverkningar.
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad ASPAVELI är och vad det används för
2. Vad du behöver veta innan du använder ASPAVELI
3. Hur du använder ASPAVELI
4. Eventuella biverkningar
5. Hur ASPAVELI ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Vad är ASPAVELI
ASPAVELI är ett läkemedel som innehåller den aktiva substansen pegcetakoplan. Pegcetakoplan har utformats för att binda till komplementproteinet C3 som är en del av kroppens immunologiska försvarssystem som kallas ”komplementsystemet”.
Vad ASPAVELI används för
Paroxysmal nokturn hemoglobinuri (PNH)
ASPAVELI är avsett för behandling av vuxna patienter med en sjukdom som kallas paroxysmal nokturn hemoglobinuri (PNH) som har anemi till följd av denna sjukdom.
Hos patienter med PNH är komplementsystemet överaktivt och attackerar de röda blodkropparna, vilket kan leda till lågt antal blodkroppar (anemi), trötthet, funktionssvårigheter, smärta, buksmärta, mörkfärgad urin, andfåddhet, sväljsvårigheter, impotens och blodproppar. Genom att binda till och blockera C3‑proteinet kan detta läkemedel förhindra komplementsystemet från att attackera röda blodkroppar och därmed kontrollera sjukdomssymtomen. Detta läkemedel har visat sig öka antalet röda blodkroppar (minska anemi), vilket kan förbättra dessa symtom.
C3-glomerulopati (C3G) och primär immunkomplexmedierad membranoproliferativ glomerulonefrit (IC-MPGN)
ASPAVELI är avsett för behandling av vuxna och ungdomar (i åldern 12 till 17 år) med sjukdomar som kallas komplement C3-glomerulopati (C3G) eller primär immunkomplexmedierad membranoproliferativ glomerulonefrit (primär IC-MPGN). Vid dessa sjukdomar används ASPAVELI tillsammans med en renin‑angiotensin-systemblockerare (RAS-blockerare), utom i fall då en RAS-blockerare inte är lämplig.
Glomerulonefrit är en njursjukdom med inflammation i njuren. C3G och primär IC-MPGN är olika typer av glomerulonefrit. Hos patienter med C3G eller primär IC-MPGN är det så kallade komplementsystemet överaktivt, och när detta system inte är i balans kan det leda till skada på glomerulus, det nätverk av små blodkärl i njuren som filtrerar blodet. Med tiden hindrar det njuren från att avlägsna slaggprodukter från blodet. Om slaggprodukterna inte avlägsnas ansamlas de i kroppen och kan leda till njurinflammation, njurskada och njursvikt. Detta kan leda till blod i urinen (hematuri), för stora mängder protein i urinen (proteinuri), nedsatt njurfunktion (detta mäts med glomerulär filtrationshastighet [GFR]), höga kreatininnivåer i blodet, trötthet och svullnad (ödem) av händerna, fötterna eller vristerna. Detta läkemedel har visats minska mängden protein i urinen och kan stabilisera njurfunktionen.
Vad du behöver veta innan produkten används
Använd inte ASPAVELI
- om du är allergisk mot pegcetakoplan eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
- om du har en infektion orsakad av så kallade inkapslade bakterier.
- om du inte är vaccinerad mot Neisseria meningitidis, Streptococcus pneumoniae och Haemophilus influenzae.
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du använder ASPAVELI.
Symtom på infektion
Innan du börjar använda ASPAVELI ska du informera din läkare om du har några infektioner.
Eftersom läkemedlets mål är komplementsystemet, som är en del av kroppens försvar mot infektion, ökar användningen av detta läkemedel risken för infektioner, inklusive de som orsakas av de så kallade inkapslade bakterierna, t.ex. Streptococcus pneumoniae, Neisseria meningitidis och Haemophilus influenzae. Detta är svåra infektioner som drabbar slemhinnorna i näsan, svalget och lungorna eller hjärnhinnan och kan sprida sig ut i blodet och hela kroppen.
Tala med läkaren innan du börjar använda ASPAVELI för att säkerställa att du blir vaccinerad mot Streptococcus pneumoniae, Neisseria meningitidis och Haemophilus influenzae om du inte har fått dessa vacciner tidigare. Om du har fått dessa vacciner tidigare kan du fortfarande behöva ytterligare vaccinationer innan du börjar använda detta läkemedel. Dessa vaccinationer ska ges minst 2 veckor innan du påbörjar behandling. Om du inte kan vaccineras 2 veckor i förväg kommer läkaren att ordinera antibiotika för att minska risken för infektion till 2 veckor efter att du har blivit vaccinerad. Efter vaccination kan läkaren kontrollera dig mer noggrant för symtom på infektion.
Infektionssymtom
Om du upplever något av följande symtom ska du omedelbart kontakta läkaren:
- huvudvärk och feber
- feber och utslag
- feber med eller utan skakningar och frossa
- andfåddhet
- hög hjärtfrekvens
- kallsvettig hud
- huvudvärk med stel nacke eller stel rygg
- huvudvärk med illamående eller kräkningar
- ljuskänsliga ögon
- muskelvärk med influensaliknande symtom
- förvirring
- extrem smärta eller extremt obehag.
Säkerställ att dina vaccinationer är aktuella. Du ska känna till att vaccin minskar risken för allvarliga infektioner men att det inte förhindrar alla allvarliga infektioner. I enlighet med nationella rekommendationer kan läkaren överväga att vidta ytterligare åtgärder såsom antibakteriella läkemedel för att förhindra infektion.
Allergiska reaktioner
Allergiska reaktioner kan förekomma hos vissa patienter. Om en allvarlig allergisk reaktion inträffar, avbryt ASPAVELI-infusionen och sök omedelbart läkarvård. Allvarliga allergiska reaktioner kan visa sig som andningssvårigheter, bröstsmärtor eller tryck över bröstet, och/eller yrsel-/svimfärdighetskänsla, kraftig klåda eller upphöjda knölar i huden, svullnad i ansikte, läppar, tunga och/eller svalg som kan orsaka sväljsvårigheter eller svimning.
Reaktioner vid injektionsstället
Reaktioner vid injektionsstället har rapporterats med användning av ASPAVELI. Du ska få lämplig utbildning om korrekt injektionsteknik innan du administrerar läkemedlet till dig själv.
Laboratorieövervakning för PNH
Under behandlingen med ASPAVELI kommer läkaren att genomföra regelbundna kontroller, inklusive blodprov för att kontrollera nivåer av laktatdehydrogenas (LDH) och njurfunktionstester, och kan vid behov justera dosen.
Effekter på laboratorietester
Användning av kiselreagens vid koagulationstester ska undvikas eftersom det kan resultera i artificiellt förlängd aktiverad partiell tromboplastintid (aPTT).
Barn och ungdomar
Ge inte detta läkemedel till barn med PNH under 18 års ålder eftersom det inte finns några tillgängliga data om säkerhet och effekt i denna grupp.
Ge inte detta läkemedel till barn med C3G eller primär IC-MPGN under 12 års ålder eftersom det inte finns tillgängliga data om säkerhet och effekt i denna grupp.
Andra läkemedel och ASPAVELI
Tala om för läkare eller apotekspersonal om du använder eller nyligen har använt andra läkemedel.
Graviditet, amning och fertilitet
Fertila kvinnor
Läkemedlets effekt på ett ofött barn är inte känd. Kvinnor som kan bli gravida bör använda effektivt preventivmedel under behandling och upp till 8 veckor efter avslutad behandling. Rådfråga läkare innan du tar detta läkemedel.
Graviditet/amning
ASPAVELI rekommenderas inte under graviditet och amning. Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare innan du använder detta läkemedel.
Körförmåga och användning av maskiner
Detta läkemedel har ingen eller försumbar påverkan på körförmågan och användning av maskiner.
ASPAVELI innehåller sorbitol
Sorbitol är en källa till fruktos. Om du inte tål vissa sockerarter, eller om du har diagnostiserats med hereditär fruktosintolerans, en sällsynt, ärftlig sjukdom som gör att man inte kan bryta ner fruktos, kontakta läkare innan du använder detta läkemedel.
ASPAVELI innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per dos, d.v.s. är näst intill ”natriumfritt”.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens anvisningar. Rådfråga läkare om du är osäker.
Minst 2 veckor innan du börjar använda detta läkemedel kommer läkaren att gå igenom din journal och kan ge dig en eller flera vaccinationer. Om du inte kan vaccineras 2 veckor innan du påbörjar behandling med ASPAVELI kommer läkaren att ordinera antibiotika under 2 veckor efter att du har blivit vaccinerad för att minska risken för infektion.
Om du använder detta läkemedel för att behandla PNH
Dos för vuxna:
Startdosen som rekommenderas till vuxna med PNH är 1 080 mg två gånger per vecka. Du ska ta dosen, som ges två gånger per vecka, dag 1 och dag 4 per behandlingsvecka.
Om du byter till ASPAVELI från en annan typ av PNH-läkemedel, en så kallad C5-hämmare, ska du ta ASPAVELI i tillägg till din aktuella dos av C5-hämmare under 4 veckor. Efter 4 veckor ska du sluta ta C5‑hämmaren.
Du ska inte ändra dosen eller doseringsintervallet utan att tala med läkaren. Läkaren kan justera dosen till 1 080 mg var tredje dag (t.ex. dag 1, dag 4, dag 7, dag 10, dag 13 osv.) om lämpligt. Om du har glömt att ta en dos ska du tala med läkaren så snart som möjligt.
Om du använder detta läkemedel för att behandla C3G eller primär IC-MPGN
Dos för vuxna:
Startdosen som rekommenderas till vuxna med C3G eller primär IC-MPGN är 1 080 mg två gånger per vecka. Du ska ta dosen, som ges två gånger per vecka, dag 1 och dag 4 per behandlingsvecka.
Dos för ungdomar:
Startdosen som rekommenderas två gånger per vecka till ungdomar med C3G eller primär IC-MPGN baseras på patientens kroppsvikt. Läkaren kommer att räkna ut din dos baserat på doseringstabellen nedan. Du ska ta dosen, som ges två gånger per vecka, dag 1 och dag 4 per behandlingsvecka.
| Kroppsvikt | Första dosen (infusionsvolym) |
Andra dosen (infusionsvolym) |
Underhållsdos (infusionsvolym) |
| 50 kg och över | 1 080 mg två gånger i veckan (20 ml) | ||
| 35 till under 50 kg | 648 mg (12 ml) | 810 mg (15 ml) | 810 mg två gånger i veckan (15 ml) |
| 30 till under 35 kg | 540 mg (10 ml) | 540 mg (10 ml) | 648 mg två gånger i veckan (12 ml) |
Administreringssätt och administreringsväg
ASPAVELI är avsett att ges som en infusion under huden med:
- en infusionspump eller
- ett kroppsburet infusionssystem.
Dina första doser av läkemedel får du av hälso- och sjukvårdspersonal på en klinik eller behandlingsmottagning. Om behandlingen går bra kan läkaren diskutera möjligheten att du får ge dig själv läkemedlet i hemmet. Om detta är lämpligt kommer hälso- och sjukvårdspersonal lära dig eller en vårdgivare hur du ger infusionen.
Infusionshastighet(er)
Vid användning av en infusionspump är infusionstiden cirka 30 minuter om du använder 2 infusionsställen eller cirka 60 minuter om du använder 1 infusionsställe.
Vid användning av ett kroppsburet infusionssystem är infusionstiden vanligtvis mellan 30 och 60 minuter (beroende på hur snabbt läkemedlet flödar in i kroppen).
Infusionen måste påbörjas omedelbart efter att detta läkemedel har dragits upp i sprutan och avslutas inom 2 timmar efter beredning av sprutan.
Bruksanvisning – förbereda sprutan
| Steg 1 | Förbered för infusion Innan du börjar:
i. Vid användning av en infusionspump (figur 1): A. Infusionspump med sprutsystem och tillverkarens bruksanvisning (visas inte) B. Kompatibel spruta C1. Överföringsnål ELLER C2. Nål-lös överföringsenhet för att dra upp läkemedel ur injektionsflaskan D. Infusionsset (visas inte, varierar beroende på tillverkarens anvisningar för utrustningen) E. Infusionsslang och Y‑anslutning (om sådan krävs) F. Behållare för vassa och skärande föremål G. Alkoholservetter H. Gasbinda och tejp eller transparent förband ELLER ii. Vid användning av ett kroppsburet infusionssystem (figur 2): A. Kroppsburet infusionssystem och tillverkarens bruksanvisning (visas inte) B. Kompatibel spruta C1. Överföringsnål ELLER C2. Nål-lös överföringsenhet för att dra upp läkemedel ur injektionsflaskan F. Behållare för vassa och skärande föremål G. Alkoholservetter |
 |
| Rengör noggrant arbetsytan med en alkoholservett. | ||
| Tvätta händerna noggrant med tvål och vatten. Torka händerna. | ||
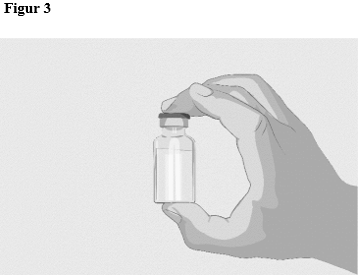
| Steg 2 | Kontrollera injektionsflaskan och vätskan Ta ut injektionsflaskan ur kartongen. Titta noggrant på vätskan i injektionsflaskan. ASPAVELI är en klar, färglös till lätt gulaktig vätska. Kontrollera om det finns partiklar eller färgförändringar (figur 3). Använd inte injektionsflaskan om:
|
 |
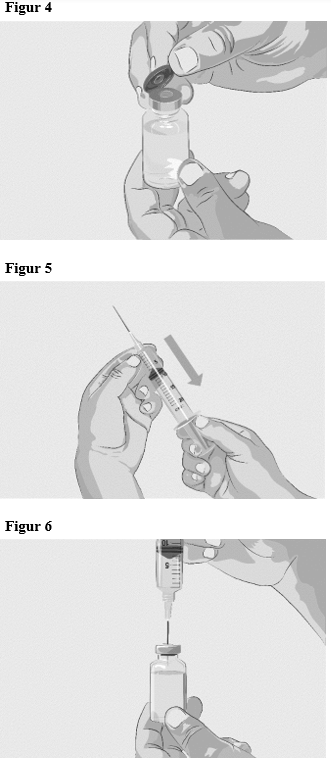
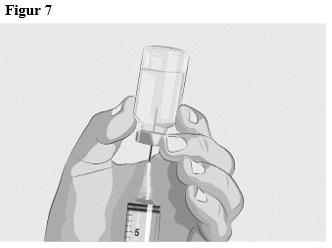
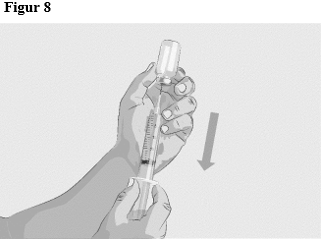
| Steg 3 | Bered och fyll sprutan Ta bort skyddslocket på injektionsflaskan för att exponera den centrala delen av injektionsflaskans grå gummipropp (figur 4). Kasta locket. Rengör proppen med en ny alkoholservett och låt proppen torka. Alternativ 1: Vid användning av en nål-lös överföringsenhet (såsom en adapter för injektionsflaska), följ anvisningarna från tillverkaren av enheten/utrustningen. ELLER Alternativ 2: Vid användning av en överföringsnål och en spruta, följ anvisningarna nedan:
|
   |
Vid infusion av läkemedlet med användning av ett kroppsburet infusionssystem (OBDS): följ anvisningarna för utrustningen från tillverkaren. Kassera allt använt engångsmaterial samt ej använt läkemedel och den tomma injektionsflaskan enligt rekommendationer från hälso- och sjukvårdspersonal.
Vid infusion av läkemedlet med användning av en infusionspump med ett sprutsystem: följ stegen nedan.
| Steg 4 | Förbered infusionspumpen med sprutsystemet och slangen Samla ihop materialet till infusionspumpen och följ anvisningarna från tillverkaren för utrustningen för att förbereda infusionspumpen och slangen. |
|
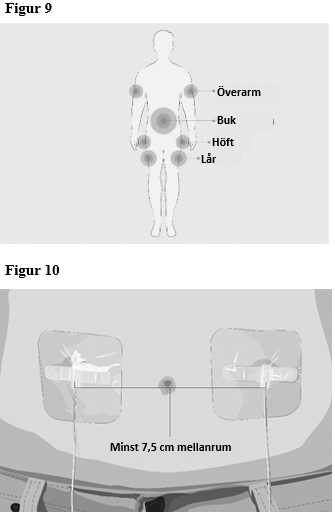
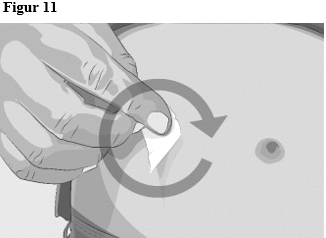
| Steg 5 | Förbered infusionsstället/infusionsställena
|
|
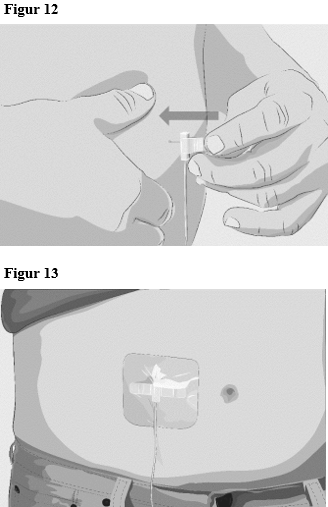
| Steg 6 | Stick in och fäst infusionsnålen/infusionsnålarna
|
 |
| Steg 7 | Starta infusionen Följ anvisningarna från tillverkaren för utrustningen för att starta infusionen. Starta infusionen omedelbart efter att du har dragit upp lösning i sprutan. |
|
| Steg 8 | Genomföra infusionen Följ anvisningarna från tillverkaren för utrustningen för att genomföra infusionen. |
|
| Steg 9 | Registrera infusionen Registrera behandlingen enligt hälso- och sjukvårdspersonalens anvisningar. |
|
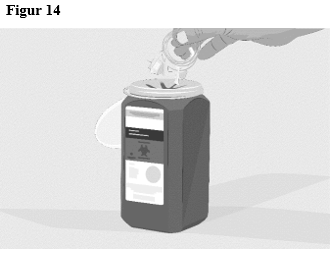
| Steg 10 | Avsluta
|
 |
Om du har glömt att använda ASPAVELI
Om du har glömt en dos ska den tas så snart som möjligt. Ta därefter nästa dos vid vanlig, planerad tidpunkt.
Om du slutar att använda ASPAVELI för att behandla PNH
PNH är en livslång sjukdom och därför förväntas du använda detta läkemedel under lång tid. Om du vill sluta använda läkemedlet ska du först tala med läkaren. Om du plötsligt slutar att ta detta läkemedel finns en risk för att dina symtom förvärras.
Om läkaren beslutar att avbryta behandlingen med detta läkemedel ska du följa hans/hennes anvisningar om hur du slutar. Läkaren kommer att kontrollera dig noggrant under minst 8 veckor efter avslutad behandling för tecken på nedbrytning av röda blodkroppar (hemolys) på grund av PNH. Symtom eller problem som kan uppkomma på grund av nedbrytning av röda blodkroppar inkluderar:
- trötthet
- andfåddhet
- blod i urinen
- magont (buksmärta)
- minskat antal röda blodkroppar
- blodproppar (trombos)
- sväljsvårigheter
- impotens hos män.
Kontakta läkaren om du har något av dessa tecken eller symtom.
Om du slutar att använda ASPAVELI för att behandla C3G eller primär IC-MPGN
C3G och primär IC-MPGN är livslånga sjukdomar och därför förväntas du använda detta läkemedel under lång tid. Om du vill sluta använda läkemedlet ska du först tala med läkaren.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Läkaren kommer att diskutera eventuella biverkningar med dig och förklara riskerna och fördelarna med ASPAVELI före behandlingen.
De allvarligaste biverkningarna är svår infektion.
Om du upplever något av följande infektionssymtom (se avsnitt Vad du behöver veta innan produkten används ”Infektionssymtom”) ska du omedelbart kontakta din läkare.
Om du är osäker på biverkningarna nedan, be läkaren förklara dem för dig.
Biverkningar som rapporterats hos patienter med PNH anges nedan:
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare):
- Reaktioner vid infusionsstället: Dessa inkluderar rodnad, svullnad, klåda, blåmärken och smärta, eller förhårdnad av huden. Dessa reaktioner försvinner vanligtvis inom några dagar.
- Infektioner i näsa, svalg eller luftvägar (övre luftvägsinfektion)
- Diarré
- Nedbrytning av röda blodkroppar (hemolys)
- Magsmärta (buksmärta)
- Huvudvärk
- Trötthet
- Feber eller hög temperatur (pyrexi)
- Hosta
- Urinvägsinfektion
- Komplikationer i samband med de obligatoriska vaccinationerna
- Smärta i armar och ben (extremitetssmärta)
- Yrsel
- Ledsmärta (artralgi)
- Ryggsmärta.
Vanliga (kan förekomma hos upp till 1 av 10 användare):
- Infektion i öra, mun eller hud
- Halsont
- Minskat antal b lodplättar (trombocytopeni) som kan leda till blödning eller till att du får blåmärken lättare
- Illamående
- Sänkt nivå av kalium i blodet (hypokalemi)
- Näsblödning (epistaxis)
- Hudrodnad (erytem)
- Muskelsmärta (myalgi)
- Infektion i magsäcken och tarmarna, som kan orsaka symtom på lätt till svårt illamående, kräkningar, kramper, diarré (infektion i mag‑tarmkanalen)
- Förhöjda levervärden
- Andningssvårigheter (dyspné)
- Minskat antal vita blodkroppar (neutropeni)
- Nedsatt njurfunktion
- Ändrad färg på urinen
- Högt blodtryck
- Muskelspasmer
- Nästäppa
- Hudutslag
- Infektion i blodet (sepsis)
- Virusinfektion
- Svampinfektion
- Luftvägsinfektion
- Ögoninfektion
- Nässelutslag
- Covid-19
- Bakteriell infektion
- Vaginal infektion.
Mindre vanliga (kan förekomma hos upp till 1 av 100 användare):
- Inflammation i livmoderhalsen
- Infektion i ljumsken
- Ficka med var i näsan (nasal abscess)
- Lunginflammation
- Tuberkulos
- Jästsvampinfektion i matstrupen
- Ficka med var i analöppningen (anal abscess).
Biverkningar som rapporterats hos patienter med C3G eller primär IC-MPGN anges nedan:
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare):
- Reaktioner vid infusionsstället
- Infektioner i näsa, svalg eller luftvägar (övre luftvägsinfektion)
- Allergisk reaktion (inklusive hudutslag och eksem)
- Feber eller hög temperatur (pyrexi)
- Huvudvärk
- Diarré
- Illamående
- Nedsatt njurfunktion
- Influensa.
Vanliga (kan förekomma hos upp till 1 av 10 användare):
- Hosta
- Lunginflammation
- Trötthet
- Opportunistiska infektioner (inklusive bältros och andra infektioner som uppstår när immunförsvaret är försvagat)
- Urinvägsinfektion
- Infektion i örat
- Minskat antal blodplättar (trombocytopeni)
- Muskelvärk (myalgi)
- Näsblod (epistaxis)
- Minskat antal vita blodkroppar (neutropeni)
- Sänkt nivå av kalium i blodet (hypokalemi)
- Smärta i armar och ben (smärta i extremiteter).
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet. Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
Suomi/Finland
[Finnish]
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
[Swedish]
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
- Förvara detta läkemedel utom syn- och räckhåll för barn.
- Används före utgångsdatum som anges på kartongen efter ”EXP”. Utgångsdatumet är den sista dagen i angiven månad.
- Förvaras i kylskåp (2 °C‑8 °C).
- Förvara injektionsflaskan i originalkartongen. Ljuskänsligt.
- Läkemedel ska inte kastas i avloppet. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
Den aktiva substansen är pegcetakoplan 1 080 mg (54 mg/ml i en 20 ml injektionsflaska).
Övriga innehållsämnen är sorbitol (E 420) (se avsnitt Vad du behöver veta innan produkten används ”ASPAVELI innehåller sorbitol”) ättiksyra, koncentrerad, natriumacetattrihydrat (se avsnitt Vad du behöver veta innan produkten används ”ASPAVELI innehåller natrium”), natriumhydroxid (se avsnitt Vad du behöver veta innan produkten används ”ASPAVELI innehåller natrium”) och vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar
ASPAVELI är en klar, färglös till lätt gulaktig vattenlösning för subkutan infusion (54 mg/ml i en 20 ml injektionsflaska). Lösningar som är grumliga eller har partiklar eller ändrar färg får inte användas.
Förpackningsstorlekar
ASPAVELI finns i en förpackning med 1 injektionsflaska eller som multipack med 1 x 8 injektionsflaskor.
Observera att alkoholtorkar, nålar och andra tillbehör eller annan utrustning inte medföljer förpackningen.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning
Swedish Orphan Biovitrum AB (publ)
SE-112 76 Stockholm
Sverige
Tillverkare
Swedish Orphan Biovitrum AB (publ)
Norra Stationsgatan 93
113 64 Stockholm
Sverige
Denna bipacksedel ändrades senast 1/2026.
Övriga informationskällor
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats https://www.ema.europa.eu. Där finns också länkar till andra webbplatser rörande sällsynta sjukdomar och behandlingar.