TISSEEL lösningar till vävnadslim
Tilläggsinformation
Humant fibrinogen, humant trombin, syntetiskt aprotinin, kalciumkloriddihydrat
Allmänna direktiv
- Spara denna bipacksedel. Du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad Tisseel är och vad det används för
- Vad du behöver veta innan du använder Tisseel
- Hur du använder Tisseel
- Eventuella biverkningar
- Hur Tisseel ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Tisseel är ett tvåkomponents vävnadslim som innehåller fibrinogen och trombin. Det är två blodproteiner som är viktiga för blodets koagulation.
Tisseel används som stödjande behandling när kirurgisk standardteknik inte är tillräcklig:
- För att förbättra hemostasen.
- Som vävnadslim för att förbättra sårläkning eller för att försegla suturer vid kirurgiska ingrepp i blodkärlen eller i mag-tarmkanalen, vid kirurgi i nervsystemet och kirurgiska ingrepp där kontakt med cerebrospinalvätska eller dura mater kan uppstå (t.ex. ENT-, oftalmisk och spinalkirurgi).
- Som vävnadslim, t ex vid vidhäftning av hudtransplantat.
Tisseel är även effektivt på patienter som behandlas med det koagulationshämmande medlet heparin.
Vad du behöver veta innan produkten används
Använd inte Tisseel:
- Om du är allergisk (överkänslig) mot någon av de aktiva substanserna eller något annat innehållsämne i detta läkemedel.
- Tisseel får inte appliceras in i blodkärl (vener eller artärer) eller vävnader.
- Enbart Tisseel är inte indicerat för behandling av stora och häftiga arteriella eller venösa blödningar.
- Tisseel ersätter inte sutura användning vid slutning av kirurgiska sår.
Varningar och försiktighet
Eftersom allergiska överkänslighetsreaktioner kan uppstå.
De första tecknen på en allergisk reaktion kan innefatta:
- övergående rodnad av huden
- klåda
- utslag
- illamående, kräkningar
- allmän sjukdomskänsla
- frossbrytningar
- tryck över bröstet
- svullnad av läppar och tunga
- andningssvårigheter/andnöd
- blodtrycksfall
- ökning eller minskning av pulsfrekvensen.
Om något av dessa symptom uppträder skall applikationen avbrytas omedelbart. Allvarliga symptom kan kräva omedelbar intensivvårdsbehandling.
- Eftersom Tisseel innehåller ett syntetiskt protein som heter aprotinin. Även om detta protein bara förekommer i små mängder och appliceras direkt på sårytan finns det en risk för allvarlig allergisk reaktion. Risken tenderar att öka hos de patienter som tidigare behandlats med Tisseel eller aprotinin, även om det tåldes väl under det förra behandlingstillfället. Därför bör behandling med aprotinin eller produkter innehållande aprotinin noteras i journalen.
- Eftersom livshotande komplikationer på grund av koagel som följer med in i blodbanan kan uppstå vid oavsiktlig applicering i ett blodkärl. Det kan öka risken för plötslig överkänslighetsreaktion och reaktionens svårighet. Speciellt under hjärtkirurgi måste läkaren vara extra uppmärksam på att inte applicera Tisseel i ett blodkärl. Det är även viktigt att applicering i nässlemhinnan undviks eftersom det kan resultera i blodkoagel i området kring ögonartären.
- Eftersom det finns en risk för lokal vävnadsskada vid applicering in i vävnaden.
- För att förhindra vävnadslimning i oönskade områden ska de delar av kroppen som inte ska behandlas täckas före applicering av Tisseel.
- Eftersom ett alltför tjockt lager fibrinkoagel kan ha en negativ inverkan på produktens säkerhet och förmåga till sårläkning ska Tisseel endast appliceras som ett tunt lager.
- Livshotande/dödlig luft‑ eller gasembolism (luft kommer in i blodomloppet, vilket kan vara allvarligt eller livshotande) har inträffat i mycket sällsynta fall när sprayset med tryckregulatorer används för att administrera fibrinvävnadslim. Detta tycks vara relaterat till användning av spraysetet vid högre tryck än vad som rekommenderas och/eller nära vävnadsytan. Risken förefaller vara större när fibrinvävnadslim sprayas med luft jämfört med CO2 och kan därför inte uteslutas när Tisseel sprayas vid öppen kirurgi.
- Sprayseten och tillhörande spetsar har bruksanvisningar med rekommendationer för tryckintervall och sprayningsavstånd från vävnadsytan.
- Tisseel ska endast administreras i strikt enlighet med instruktionerna och endast tillsammans med de anordningar som rekommenderas för denna produkt.
- När Tisseel sprayas på ska förändringar i blodtryck, puls, syremättnad och sluttidal CO2 övervakas med tanke på eventuell gasembolism.
Andra läkemedel och Tisseel
Tala om för läkare eller apotekspersonal om du tar/använder eller nyligen har tagit/använt andra läkemedel, även receptfria sådana.
Det finns inga kända interaktioner med andra läkemedel.
Liksom för andra jämförbara produkter eller trombinlösningar kan denna produkt förstöras vid kontakt med lösningar som innehåller alkohol, jod eller tungmetaller (t ex antiseptiska lösningar). Det måste säkerställas att sådana substanser har avlägsnats så mycket som möjligt innan denna produkt används.
Produkter som innehåller oxiderad cellulosa kan minska effektiviteten hos Tisseel och ska inte användas som hjälpmedel vid applicering.
Graviditet, amning och fertilitet
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du använder detta läkemedel.
Läkaren bestämmer om du kan använda Tisseel under graviditet eller amning.
Körförmåga och användning av maskiner
Tisseel påverkar inte din förmåga att köra bil eller använda verktyg eller maskiner.
Viktig information om några innehållsämnen i Tisseel
När mediciner framställs av humant blod eller plasma, vidtas speciella åtgärder för att förhindra att infektioner överförs till patienter. Detta inkluderar noggrant urval av blod- och plasmagivare för att försäkra sig om att personer med risk för att vara smittbärare utesluts, samt test av enskilda donationer och plasmapooler för tecken på virus eller infektion.
Tillverkarna av dessa produkter inkluderar dessutom steg i hanteringen av blod eller plasma för att inaktivera eller avskilja virus. Trots detta kan risken för överföring av infektion inte helt uteslutas när läkemedel framställda av humant blod eller plasma ges. Detta gäller även nya, hittills okända virus samt andra typer av infektioner. Dessa åtgärder anses effektiva för höljeförsedda virus, såsom humant immunbristvirus (HIV), hepatit B-virus och hepatit C-virus och för det icke-höljeförsedda hepatit A-viruset.
Åtgärderna kan vara av begränsat värde mot icke-höljeförsedda virus som parvovirus B19 (det virus som orsakar infektiöst erytem (femte sjukan)). En parvovirus B19-infektion kan vara allvarlig för gravida kvinnor (infektion av fostret) och för individer med försämrat immunförsvar eller som har vissa typer av anemi (t.ex. sicklecell-anemi eller hemolytisk anemi).
Din läkare kan rekommendera vaccination mot hepatit A och B, om du regelbundet eller upprepat får human plasma deriverat vävnadslim.
Det rekommenderas att produktens namn och satsnummer noteras varje gång du får en dos Tisseel med hjälp av den självhäftande etiketten som finns i förpackningen.
Polysorbat 80 kan orsaka lokala hudreaktioner som kontaktdermatit.
Tisseel ska enbart abliceras i ett tunt lager. Alltför tjock lager kan påverka produktens effektivitet och sårläkningsprocessen negativt.
Hur produkten används
Användningen av Tisseel begränsas till erfarna kirurger som fått utbildning i användningen av Tisseel.
Säkerhet och effekt har inte påvisats hos barn.
Innan Tisseel appliceras måste sårets ytområde torkas med standardteknik (t.ex. upprepad applicering av kompresser eller bomullspinnar, eller med hjälp av suganordningar).
Använd inte tryckluft eller trycksatt gas för att torka området.
Tisseel skall endast sprayas på områden som är synliga
Dosen som administreras avgörs alltid av dina individuella behov.
Den dos av Tisseel som används beror på ett antal faktorer inklusive typ av operation, storleken på området som ska behandlas under operationen, sättet Tisseel appliceras på och antalet appliceringar. Din läkare bestämmer hur mycket som är lämpligt och kommer att applicera tillräckligt för att bilda ett tunt lager över såret. Om mängden inte verkar vara tillräcklig, kan appliceringen behöva upprepas. Undvik dock att upprepa applicering på ett redan polymeriserat lager Tisseel eftersom Tisseel inte fäster på ett polymeriserat lager. Applicering av de två komponenterna separat, i följd, ska undvikas.
I kliniska studier har individuella doser på 4 till 20 ml administrerats. För vissa typer av kirurgi (t.ex. skador på levern eller läkning av stora brännsår) kan större mängder krävas.
Som en riktlinje för läkning av sårytor så är 1 förpackning med Tisseel 2 ml (dvs 1 ml Tisseel lösning plus 1 ml trombinlösning) tillräcklig för en yta på åtminstone 10 cm2.
När Tisseel sprayas på såret, räcker samma mängd till att täcka en avsevärt större yta.
Iakttag försiktighet om Tisseel appliceras med hjälp av tryckluft
Applicering utanför avsett område ska undvikas.
För att undvika bildning av granulationsvävnad i överskott och för att säkerställa gradvis absorption av det stelnade fibrinlimmet, ska endast ett så tunt lager som möjligt av Tisseel appliceras.
För att säkerställa adekvat blandning av komponent 1 och komponent 2 bör de första dropparna av produkt från applikationskanylen tryckas ut och kasseras omedelbart före användning.
Vid applicering av Tisseel med hjälp av ett sprayset, var noga med att använda ett tryck och ett avstånd från vävnaden som ligger inom det intervall som rekommenderas av tillverkaren enligt följande:
| Rekommenderat tryck, avstånd och anordning för sprayning av Tisseel | |||||
| Typ av ingrepp | Sprayset som ska användas | Applikatorspetsar som ska användas | Tryckregulator som ska användas | Rekommenderat avstånd från mål-vävnaden | Rekommenderat spraytryck |
| Öppna ingrepp | Tisseel/Artiss sprayset | inte tillämpligt | EasySpray | 10‑15 cm | 1,5‑2,0 bar (21,5‑28,5 psi). |
| Tisseel/Artiss sprayset 10 pack | inte tillämpligt | EasySpray | |||
| Laparoskopiska/minimalt invasiva ingrepp | inte tillämpligt | Duplo-spray MIS applikator 20 cm | Duplo-spray MIS regulator 1,5 bar | 2 –5 cm | 1,2–1,5 bar (18–22 psi) |
Duplo-spray MIS applikator 30 cm | |||||
Duplo-spray MIS applikator 40 cm | |||||
| Spray Set 360 endoskopisk applikator med Snap Lock | |||||
| Spray Set 360 endoskopiskn applikator med säkerhetsspärr | |||||
| Utbytbar spets | |||||
Vid öppen kirurgi – en tryckregulator som kan ge ett tryck på högst 2,0 bar (28,5 psi) ska användas.
Vid minimalt invasiva/laparoskopiska ingrepp – en tryckregulator som kan ge ett tryck på högst 1,5 bar (22 psi) och som använder endast koldioxidgas får användas.
När Tisseel sprayas på ska förändringar i blodtryck, puls, syremättnad och sluttidal CO2 övervakas med tanke på risken för luft‑ eller gasembolism (se avsnitt Vad du behöver veta innan produkten används).
Om du använt för stor mängd av Tisseel
Tisseel appliceras endast under ett kirurgiskt ingrepp. Mängden som används bestäms av kirurgen. Det finns inga kända fall av överdosering.
Om du har ytterligare frågor om detta läkemedel kontakta läkare eller apotekspersonal.
Användning för barn
Säkerhet och effekt för barn har inte fastställts.
Eventuella biverkningar
Liksom alla läkemedel kan Tisseel orsaka biverkningar men alla användare behöver inte få dem. Informera din läkare eller apotekspersonal om någon av de biverkningar som listas här påverkar dig mycket eller om du märker någon biverkning som inte finns nämnd i denna information.
Hos patienter som behandlas med fibrinlim kan överkänslighetsreaktioner eller allergiska reaktioner förekomma. De är sällsynta men kan vara allvarliga.
De första tecknen på en allergisk reaktion kan vara:
- Övergående rodnad av huden (flush)
- Klåda
- Utslag
- Illamående, kräkningar
- Huvudvärk
- Dåsighet
- Rastlöshet
- Brännande och stickande känsla på applikationsstället
- Stickande, krypande känsla
- Frossa
- Tryck över bröstet
- Svullnad av läppar, tunga, hals (vilket kan resultera i svårigheter att andas och/eller svälja)
- Andningssvårigheter
- Lågt blodtryck
- Ökad eller minskad pulsfrekvens
- Medvetslöshet till följd av blodtrycksfall.
I vissa fall kan dessa reaktioner leda till allvarliga allergiska reaktioner (anafylaxi). Sådana reaktioner kan uppträda särskilt om läkemedlet appliceras flera gånger, eller används på patienter som tidigare har visat överkänslighet mot aprotinin eller andra komponenter i produkten.
Även om upprepad behandling med Tisseel har tolererats väl, kan ytterligare en administrering av Tisseel eller en infusion av aprotinin resultera i allvarliga allergiska (anafylaktiska) reaktioner. Syntetisk aprotinin liknar strukturalt nötaprotinin. För patienter med allergi mot nötproteiner måste användning av Tisseel övervägas noggrant.
Det ansvariga kirurgteamet är väl medvetna om risken för denna typ av reaktioner och kommer omedebart att avbryta appliceringen av Tisseel vid första tecken på överkänslighet. Allvarliga symtom kan kräva akutvård.
Om Tisseel appliceras i mjukdelar kan det orsaka lokal vävnadsskada.
Om Tisseel appliceras i blodkärl (vener eller artärer) kan det leda till att koagel bildas (trombos). Det kan även öka risken och allvarlighetsgraden av akuta överkänslighetsreaktioner hos känsliga patienter.
Eftersom Tisseel är utvunnet ur plasma från blodgivare kan risken för infektion inte helt uteslutas, men tillverkaren vidtar flera åtgärder för att minska risken (se avsnitt Vad du behöver veta innan produkten används).
Antikroppar mot komponenter i fibrinlimmet kan uppträda i sällsynta fall.
Följande biverkningar har observerats vid behandling med Tisseel
Biverkningar har utvärderats enligt följande frekvenser:
Mycket vanliga: Förekommer hos fler än 1 av 10 behandlade patienter.
Vanliga: Förekommer hos 1 till 10 av 100 behandlade patienter.
Mindre vanliga: Förekommer hos 1 till 10 av 1000 behandlade patienter.
Sällsynta: Förekommer hos 1 till 10 av 10 000 behandlade patienter.
Mycket sällsynta: Förekommer hos färre än 1 av 10 000 behandlade patienter.
Ingen känd frekvens: Frekvensen kan inte bedömas utifrån tillgängliga data.
| Organklass | MedDRA-term | Frekvens |
| Infektioner och infestationer | postoperativ sårinfektion | vanliga |
| Immunsystemet | överkänslighetsreaktioner | ingen känd frekvens |
| anafylaktiska reaktioner | ingen känd frekvens | |
| anafylaktisk chock | ingen känd frekvens | |
| Centrala och periferala nervsystemet | parestesier | vanliga |
| hypaesthesia | ingen känd frekvens | |
| Hjärtat | bradykardi | ingen känd frekvens |
| takykardi | ingen känd frekvens | |
| Blodkärl | thrombosis i axelhålan | vanliga |
| låg blodtryck | sällsynta | |
| blodutgjutning nos | ingen känd frekvens | |
| tromboemboli | ingen känd frekvens | |
| luftemboli* | ingen känd frekvens | |
| cerebralartäremboli | ingen känd frekvens | |
| cerebralinfarkt | ingen känd frekvens | |
| Andningsvägar, bröstkorg och mediastinum | andnöd | ingen känd frekvens |
| bronkospasm | ingen känd frekvens | |
| väsande andning | ingen känd frekvens | |
| Magtarmkanalen | illamående | mindre vanliga |
| tarmobstruktion | ingen känd frekvens | |
| Hud och subcutan vävnad | urtikaria | ingen känd frekvens |
| erytem | vanliga | |
| pruritus | ingen känd frekvens | |
| (röd) eksem | ingen känd frekvens | |
| försämrad sårläkning | ingen känd frekvens | |
| angioödem | ingen känd frekvens | |
| Muskuloskeletala systemet och binbdväv | värk i extremiteter | vanliga |
| Allmänna symptom och/eller symptom vid administreringsstället | postoperativ smärta | mindre vanliga |
| smärta | vanliga | |
| feber | vanliga | |
| rodnad | ingen känd frekvens | |
| svullnad | ingen känd frekvens | |
| Skador och förgiftningar och behandlingskomplikationer | serom | mycket vanliga |
| Undersökningar | ökad mängd nedbrytningsprodukter från fibrin | mindre vanliga |
| d-dimerer ökad i fibrin | mindre vanliga |
* Luft- eller gasbubblor i blodflödet har förekommit i samband med att fibrinlim har applicerats med sprayset med tryckluft eller trycksatt gas. Detta tros vara orsakat av felaktig användning av spraysetet (t.ex högre tryck än vad som rekommenderas och nära vävnadsytan).
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller sjuksköterska. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets‐ och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55, 00034 FIMEA
Hur produkten ska förvaras
Förvaras utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på etiketten efter EXP.
Förvaras och transporteras fruset (≤ -20 °C) fram till användning.
Förvaras i originalförpackningen. Ljuskänsligt.
Förvaring efter upptining:
Den vid högst 25°C tinade lösningen kan användas i upp till 72 timmar om den förvaras i oöppnad, oskadad, steril förpackning vid högst 25°C. Om Tisseel inte används inom 72 timmar efter upptining, måste lösningarna kasseras.
Efter upptining får lösningarna inte frysas igen eller förvaras i kylskåp!
Medicinen ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man gör med mediciner som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
Tisseel innehåller två komponenter:
Komponent 1 = Proteinlösning (Tisseel lösning):
De aktiva substanserna i 1 ml proteinlösning är: Humant fibrinogen, 91 mg/ml, syntetiskt aprotinin 3000 KIE/ml.
Hjälpämnen är humant albumin, L-histidin, niacinamid, polysorbat 80 (Tween 80), natriumcitratdihydrat och vatten för injektionsvätskor.
Komponent 2 = Trombinlösning:
Den aktiva substansen i 1 ml trombinlösning är: Humant trombin 500 IE/ml, kalciumkloriddihydrat 40 µmol/ml.
Hjälpämnen är humant albumin, natriumklorid och vatten för injektionsvätskor.
| Efter blandning | 1 ml | 2 ml | 4 ml | 10 ml |
Komponent 1: Proteinlösning (Tisseel) Humant fibrinogen (som koagulerbart protein) syntetiskt aprotinin | 45,5 mg 1500 KIE | 91 mg 3000 KIE | 182 mg 6000 KIE | 455 mg 15000 KIE |
Komponent 2: Trombinlösning Humant trombin Kalciumkloriddihydrat | 250 IE 20 μmol | 500 IE 40 μmol | 1000 IE 80 μmol | 2500 IE 200 μmol |
Tisseel innehåller 0,6 – 5 IE/ml human faktor XIII vilket är isolerat från plasma tillsammans med humant fibrinogen.
Läkemedlets utseende och förpackningsstorlekar
Vävnadslimningar.
Både proteinlösningen (Tisseel, komponent 1) och trombinlösningen (komponent 2) tillhandahålls i en endos tvåkammarspruta för engångsbruk färdig för användning.
I djupfryst tillstånd är lösningarna färglösa till svagt gula och ogenomskinliga.
Efter tining är lösningarna färglösa till svagt gula.
Förpackningens innehåll:
Innehåll i förpackningen med PRIMA-sprutan:
- En förfylld spruta med två behållare (av polypropylen) innehållande 1 ml, 2 ml eller 5 ml proteinlösning respektive 1 ml, 2 ml eller 5 ml trombinlösning. Sprutspetsen är försedd med en skyddskapsel. Sprutan är förpackad i två påsar och som tillbehör medföljer 2 huvudmunstycken och 4 applikationskanyler.
Förpackningsstorlekar:
Tisseel tillhandahålls i följande förpackningsstorlekar: 1 x 2 ml (1 ml + 1 ml), 10 x 2 ml, 1 x 4 ml (2 ml + 2 ml) 10 x 4 ml, 1 x 10 ml (5 ml + 5 ml), 10 x 10 ml
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning
Baxter Oy, Box 35, 01531 Vanda
Tillverkare
Takeda Manufacturing Austria AG, Industriestraße 67, A-1221 Wien, Österrike
Denna bipacksedel ändrades senast 01.10.2025
Direktiv för experterna inom hälsovården
Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal (slutgiltig behållare: PRIMA-spruta):
Allmänt
- Före applicering av Tisseel ska de delar av kroppen som inte ska behandlas täckas för att förhindra vävnadslimning i oönskade områden.
- För att förhindra Tisseel från att fästa vid handskar och instrument, fukta dessa med saltlösning före användning.
- Använd följande riktmärke vid limning av ytor: En förpackning Tisseel 2 ml (d.v.s. 1 ml proteinlösning plus 1 ml trombinlösning) till ett område på minst 10 cm2.
- Den exakta dosen är beroende av hur stor yta som ska limmas.
- De två Tisseel-komponenterna får INTE appliceras separat. Båda komponenterna måste appliceras samtidigt.
- Tisseel får INTE utsättas för högre temperaturer än 37°C. Värm INTE produkten i mikrovågsugn.
- Tina INTE produkten genom att hålla den mellan händerna.
- Tisseel får INTE användas förrän produkten har tinat helt och värmts upp till 33 – 37°C.
- Ta inte av skyddskapseln från sprutan förrän produkten har tinats och värmts och är klar för användning. Det lättaste sättet att ta av skyddskapseln från sprutan är att försiktigt vicka den fram och tillbaka och sedan dra av den från sprutan.
- Tryck ut all luft från sprutan och montera sedan huvudmunstycket och applikationskanylen.
Anvisningar för hantering och beredning
Både proteinlösningen och trombinlösningen tillhandahålls i en förfylld spruta som är färdig att användas. Produkten är förpackad i två sterila påsar under aseptiska förhållanden. Innerpåsen och dess innehåll är sterila så länge som den yttre förpackningen är obruten. Använd steril teknik för att ta ut den sterila innerpåsen och dess innehåll på det sterila området.
Den förfyllda sprutan kan tinas OCH värmas på något av följande sätt:
- Snabb tining/värmning (sterilt vattenbad) – Rekommenderas
- Tining/värmning i ett icke-sterilt vattenbad
- Tining/värmning i inkubator
- Den förfyllda sprutan kan också tinas och förvaras i rumstemperatur (maximalt 25°C) i upp till 72 timmar. Produkten måste värmas innan den används.
1) Snabb tining/värmning (sterilt vattenbad) – Rekommenderas
Den rekommenderade metoden är att tina och värma de två komponenterna i ett sterilt vattenbad vid 33 – 37°C.
- Vattenbadets temperatur får inte överskrida 37°C. Övervaka värmningen genom att mäta vattentemperaturen med termometer, och byt vatten vid behov.
- Om ett sterilt vattenbad används för tining och värmning ska den förfyllda sprutan tas ur förpackningspåsarna innan den placeras i vattenbadet.
Anvisningar:
Placera innerpåsen i det sterila området, ta ut den förfyllda sprutan och placera den direkt i det sterila vattenbadet. Kontrollera att allt innehåll i den förfyllda sprutan är helt nedsänkt under vattenytan.
Tabell 1 – PRIMA-spruta: Minimitid för tining och värmning i sterilt vattenbad
| Förpackningsstorlek | Minimitid för tining och värmning 33 – 37°C, sterilt vattenbad Produkt utan påsar |
| 2 ml | 5 minuter |
| 4 ml | 5 minuter |
| 10 ml | 10 minuter |
2) Tining/värmning i ett icke-sterilt vattenbad
Anvisningar:
Låt den förfyllda sprutan vara kvar i båda förpackningspåsarna och placera den i ett vattenbad utanför det sterila området under så lång tid som anges i tabell 2. Se till att påsarna förblir helt nedsänkta i vattnet under hela tiningstiden. Efter tining ska påsarna tas upp ur vattenbadet. Torka av den yttre påsen och flytta över innerpåsen med den förfyllda sprutan och kolven till det sterila området.
Tabell 2 – PRIMA-spruta: Minimitid för tining och värmning i icke-sterilt vattenbad
| Förpackningsstorlek | Minimitid för tining och värmning 33 – 37°C, icke-sterilt vattenbad Produkt i påsar |
| 2 ml | 15 minuter |
| 4 ml | 20 minuter |
| 10 ml | 35 minuter |
3) Tining/värmning i inkubator
Anvisningar:
Låt den förfyllda sprutan vara kvar i båda förpackningspåsarna och placera den i en inkubator utanför det sterila området under så lång tid som anges i tabell 3. Efter tining/värmning ska påsarna tas upp ur inkubatorn. Ta av den yttre påsen och flytta över innerpåsen med den förfyllda sprutan och kolven till det sterila området.
Tabell 3 – PRIMA-spruta: Minimitid för tining och värmning i inkubator
| Förpackningsstorlek | Minimitid för tining och värmning 33 – 37°C, inkubator Produkt i påsar |
| 2 ml | 40 minuter |
| 4 ml | 50 minuter |
| 10 ml | 90 minuter |
4) Tining vid rumstemperatur (maximalt 25°C) FÖRE värmning
Anvisningar:
Låt den förfyllda sprutan vara kvar i båda förpackningspåsarna och tina upp den vid rumstemperatur utanför det sterila området under så lång tid som anges i tabell 4. När produkten har tinats kan den värmas i en inkubator, utan att tas ur ytterpåsen.
Tabell 4 – PRIMA-spruta: Minimitid för tining vid rumstemperatur utanför det sterila fältet, samt värmningstid i inkubator (till 33 – 37°C)
| Förpackningsstorlek | Minimitid för tining av produkten vid rumstemperatur (maximalt 25°C) produkt i påsar | Uppvärmningstider inför användning till 33 – 37°C i inkubator, efter tining i rumstemp. produkt i påsar |
| 2 ml | 80 minuter + 11 minuter | |
| 4 ml | 90 minuter + 13 minuter | |
| 10 ml | 160 minuter + 25 minuter | |
Efter tining vid rumstemperatur måste produkten användas inom 72 timmar efter att den först togs ut ur frysen.
Stabilitet efter tining
Efter tining och värmning (vid temperaturer mellan 33 – 37°C, med metod 1, 2 eller 3) har kemisk och fysikalisk stabilitet påvisats för produkten i 12 timmar vid 33 – 37°C.
För produkter som tinats vid rumstemperatur i oöppnad förpackning (metod 4) har kemisk och fysikalisk stabilitet påvisats för produkten i 72 timmar vid maximalt 25°C. Värm till 33 – 37°C omedelbart före användning.
Ur en mikrobiologisk synvinkel bör produkten användas omedelbart efter värmning till 33 – 37°C, såvida inte metoden för öppning av förpackningen eller tiningen utesluter risken för mikrobiell kontamination.
Om produkten inte används omedelbart är förvaringstiderna och förhållandena användarens ansvar.
Produkten får inte frysas på nytt eller placeras i kylskåp efter att tining har påbörjats.
Hantering efter tining/innan applicering
För att uppnå optimal blandning av de två lösningarna och bästa möjliga solidifiering av fibrinvävnadslimmet ska de två komponenterna förvaras vid 33 – 37°C tills de appliceras.
Protein- och trombinlösningarna ska vara klara eller något ogenomskinliga. Använd inte lösningar som är grumliga eller har fällningar. Tinade produkter ska inspekteras visuellt före användning för att upptäcka eventuella främmande partiklar, missfärgning eller andra förändringar. Om en lösning har förändrats på något av dessa sätt ska den kasseras.
Den tinade proteinlösningen ska vara en något trögflytande vätska. Om lösningens konsistens är som en fast gel måste man anta att den har blivit denaturerad (t.ex. på grund av avbruten kylkedja eller överhettning vid värmning). Tisseel får då INTE användas under några omständigheter.
- Ta ut sprutan från förpackningspåsarna omedelbart före användning.
- Använd endast Tisseel om produkten har tinats och värmts upp helt (har flytande konsistens).
- Ta av skyddskapseln från sprutan omedelbart före appliceringen.
Det lättaste sättet att ta av skyddskapseln från sprutan är att försiktigt vicka den fram och tillbaka och sedan dra av den från sprutan.
Administrering med PRIMA-spruta:
Inför applicering ska den förfyllda sprutan med två behållare (som innehåller proteinlösning respektive trombinlösning) kopplas till ett huvudmunstycke och en applikationskanyl, som finns bland de medföljande tillbehören. Den gemensamma kolven på den förfyllda sprutan med två behållare säkerställer att lika stora volymer av de två vävnadslimkomponenterna pressas genom huvudmunstycket innan de blandas i applikationskanylen och sprutas ut.
Bruksanvisning för PRIMA-sprutan
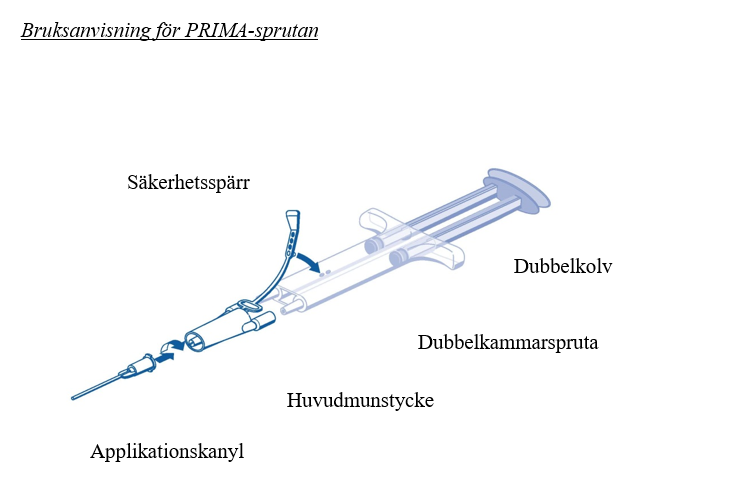
- Tryck ut all luft från sprutan innan den kopplas till någon applikationsdel.
- Placera huvudmunstycket och säkerhetsspärren på sidan av sprutan så att hålet i säkerhetsspärren hamnar rätt.
- Anslut munstyckena på den förfyllda sprutan med två behållare till huvudmunstycket, och se till att de sitter fast ordentligt.
- Säkra huvudmunstycket genom att fästa säkerhetsspärren på den förfyllda sprutan med två behållare.
- Om säkerhetsspärren går sönder ska det medföljande reservmunstycket användas.
- Om det inte finns något extra munstycke tillgängligt kan produkten fortfarande användas, men det är viktigt att se till att munstycket sitter fast för att förhindra läckage.
- Tryck INTE ut den luft som finns kvar inuti i huvudmunstycket.
- Fäst en applikationskanyl på huvudmunstycket.
- Tryck INTE ut den luft som finns kvar i huvudmunstycket och applikationskanylen förrän appliceringen inleds, eftersom det kan göra att applikationskanylen täpps till.
Administrering
Innan Tisseel appliceras måste sårytan torkas med standardteknik (t.ex. upprepad applicering av kompresser eller bomullspinnar, eller med hjälp av suganordningar). Använd inte tryckluft eller trycksatt gas för att torka området.
- Applicera den blandade protein- och trombinlösningen på mottagarytan eller ytorna på de områden som ska behandlas genom att långsamt trycka ned den gemensamma kolven.
- Vid kirurgiska ingrepp där minsta möjliga volym av fibrinvävnadslim ska användas bör de första dropparna av produkten kasseras.
- När Tisseel har applicerats, låt minst 2 minuter passera för att uppnå tillräcklig polymerisering.
Obs! Om appliceringen av fibrinvävnadslimmet avbryts kan kanylen täppas igen. I sådana fall ska applikationskanylen ersättas med en ny precis innan appliceringen påbörjas igen. Om huvudmunstyckets öppningar har täppts igen, använd det medföljande reservmunstycket.
Efter att vävnadslimkomponenterna har blandats börjar fibrinlimmet stelna inom några sekunder på grund av den höga trombinkoncentrationen (500 IU/ml).
Fibrinvävnadslimmet kan också appliceras med andra tillbehör från Baxter som är speciellt anpassade för t.ex. endoskopisk användning, minimal invasiv kirurgi eller applicering på stora eller svåråtkomliga områden. Om sådana appliceringstillbehör används ska bruksanvisningarna för respektive tillbehör följas noggrant.
Beredningar som innehåller oxiderad cellulosa ska inte användas tillsammans med Tisseel, eftersom det låga pH-värdet kan påverka trombinets verkningsmekanism
I vissa sammanhang används biokompatibelt material, till exempel kollagenmaterial, som bärarsubstans eller i förstärkningssyfte.
Applicering genom sprayning
Vid applicering av Tisseel med hjälp av ett sprayset, var noga med att använda ett tryck och ett avstånd från vävnaden som ligger inom det intervall som rekommenderas av tillverkaren enligt följande:
| Rekommenderat tryck, avstånd och anordning för sprayning av Tisseel | |||||
| Typ av ingrepp | Sprayset som ska användas | Applikatorspetsar som ska användas | Tryckregulator som ska användas | Rekommenderat avstånd från målvävnaden | Rekommenderat spraytryck |
| Öppna ingrepp | Tisseel/Artiss sprayset | inte tillämpligt | EasySpray | 10-15 cm | 1,5-2,0 bar (21,5-28,5 psi). |
| Tisseel/Artiss sprayset, 10-pack | inte tillämpligt | EasySpray | |||
| Laparoskopiska/minimalt invasiva ingrepp | inte tillämpligt | Duplospray MIS applikator 20 cm | Duplospray MIS regulator 1,5 bar | 2-5 cm | 1,2-1,5 bar (18-22 psi) |
| Duplospray MIS applikator 30cm | |||||
| Duplospray MIS applikator 40cm | |||||
| Spray Set 360 endoskopisk applikator med Snap Lock | |||||
| Spray Set 360 endoskopisk applikator med säkerhetsspärr | |||||
| Utbytbar spets | |||||
Vid öppen kirurgi – en tryckregulator som kan ge ett tryck på högst 2,0 bar (28,5 psi) ska användas.
Vid minimalt invasiva/laparoskopiska ingrepp – en tryckregulator som kan ge ett tryck på högst 1,5 bar (22 psi) och som använder endast koldioxidgas får användas.
När Tisseel sprayas på ska förändringar i blodtryck, puls, syremättnad och sluttidal CO2 övervakas på grund av risken för luft- eller gasembolism (se avsnitt Vad du behöver veta innan produkten används).
För applicering av Tisseel i inneslutna områden i bröst och buk rekommenderas DuploSpray MIS-systemet med applikator och regulator. Följ bruksanvisningen för DuploSpray MIS-enheten.
Destruktion
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.