TISSEEL liuokset kudosliimaa varten
Ihmisen fibrinogeeni, ihmisen trombiini, synteettinen aprotiniini, kalsiumklorididihydraatti
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Jos havaitset haittavaikutuksia, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä Tisseel on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin käytät Tisseel -valmistetta
- Miten Tisseel -valmistetta käytetään
- Mahdolliset haittavaikutukset
- Tisseel -valmisteen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Tisseel on kaksikomponenttikudosliima, jossa on fibrinogeenia ja trombiinia. Nämä proteiinit ovat tärkeitä veren hyytymisessä.
Tisseel -valmistetta käytetään hoitona silloin, kun tavanomaiset kirurgiset tekniikat eivät riitä:
- Hemostaasin parantamiseen.
- Kudosliimana edistämään haavan paranemista, tai ommelten tukena verisuonikirurgiassa, gastrointestinaalianastomooseissa, neurokirurgiassa ja sellaisissa kirurgisissa toimenpiteissä, joissa ollaan kosketuksissa aivo-selkäydinnesteeseen tai kovakalvoon (esim. korva-, nenä- ja kurkkukirurgiassa, silmä- ja spinaalikirurgiassa).
- Kudosten liimauksessa parantamaan erillään olevien kudospintojen kiinnittymistä (esim. kudoskielekkeet, siirteet, ohutihosiirteet; meshatut siirteet).
Teho on osoitettu myös täysin heparinisoiduilla potilailla.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä Tisseel -valmistetta:
- jos olet allerginen (yliherkkä) vaikuttaville aineille tai tämän lääkkeen jollekin muulle aineelle.
- Tisseel -valmistetta ei saa applikoida verisuoniin (laskimoihin tai valtimoihin) tai kudoksiin.
- Tisseel -valmistetta ei saa käyttää yksinään runsaan ja suihkuavan valtimo- tai laskimoverenvuodon hoitoon.
- Tisseel ei korvaa ompeleita kirurgisen haavan sulkemisessa.
Varoitukset ja varotoimet
Allergiset yliherkkyysreaktiot ovat mahdollisia.
Allergisen reaktion ensimmäisiä merkkejä voivat olla:
- ihon ohimenevä punastelu
- kutina
- rakkulaihottuma
- pahoinvointi, oksentelu
- yleinen huonovointisuus
- vilunväreet
- rinnan ahdistus
- huulien ja kielen turpoaminen
- hengitysvaikeudet, hengenahdistus
- verenpaineen lasku
- kiihtynyt tai hidastunut sydämen lyöntitiheys.
Jos mitään yllämainituista havaitaan, applikointi on heti keskeytettävä. Vaikeat oireet vaativat heti tehohoitoa.
- Tisseelissä on synteettistä proteiinia (aprotiniinia). Vaikka tätä proteiinia olisi applikoitu vain vähäisiä määriä ja vain kudosvaurion päälle, on olemassa vakavan allergisen reaktion vaara. Riski näyttää kasvavan potilailla, jotka ovat aiemmin saaneet Tisseeliä tai aprotiniinia, vaikka he olisivat edellisellä antokerralla sietäneet niitä hyvin. Siksi potilastietoihin on aina merkittävä aprotiniinin tai sitä sisältävien valmisteiden käyttö.
- Vahingossa verisuoneen applikoitu valmiste voi aiheuttaa hengenvaarallisia haittavaikutuksia, jos hyytymät lähtevät liikkeelle verisuonissa. Se voi myös lisätä äkillisen yliherkkyysreaktion todennäköisyyttä ja vaikeutta.
- Erityisesti sydänkirurgiassa lääkärin on varottava applikoimasta Tisseeliä verisuoniin. Samoin ei ehdottomasti saa applikoida nenän limakalvoille, koska tällöin voisi muodostua hyytymiä silmien verisuonien valtimoihin.
- Paikallinen kudosvaurion vaara on olemassa, jos applikoidaan kudokseen.
- Ennen Tisseel -valmisteen käyttöä on suojattava käyttöalueen ulkopuoliset kehon osat, jotta liimataan vain suunnitellut kohteet.
- Tisseel -valmistetta applikoidaan mahdollisimman ohut kerros, jotta granulaatiokudosta ei muodostu liikaa eikä vaikeuteta haavan paranemista.
- Hengenvaarallisia / kuolemaan johtaneita ilma‑ tai kaasuembolioita (ilman pääseminen verenkiertoon, mikä voi olla vakavaa tai hengenvaarallista) on esiintynyt hyvin harvoin käytettäessä ruiskutuslaitteita, joissa on paineensäätölaite levittämään kudosliimoja. Tämä vaikuttaa liittyvän ruiskutuslaitteen käyttämiseen suositeltua korkeammilla paineilla ja/tai lähellä kudoksen pintaa. Riski vaikuttaa olevan suurempi, kun kudosliimoja ruiskutetaan ilman avulla kuin CO2:n avulla, ja siten riskiä ei voida sulkea pois Tisseel ‑valmisteen yhteydessä avotoimenpiteissä.
- Ruiskutuslaitteissa ja lisävarustekärjessä on käyttöohjeita ja suosituksia painealueista ja ruiskutusetäisyydestä kudoksen pinnasta.
- Tisseel ‑kudosliimaa saa levittää vain tälle tuotteille annettujen ohjeiden mukaisesti ja vain suositelluilla laitteilla.
- Ruiskutettaessa Tisseel ‑kudosliimaa verenpaineen, sykkeen, happisaturaation ja kertahengityksen CO2‑pitoisuuden vaihteluja on seurattava mahdollisen kaasuembolian esiintymisen takia.
Muut lääkevalmisteet ja Tisseel
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät tai olet äskettäin käyttänyt muita lääkkeitä, myös lääkkeitä, joita lääkäri ei ole määrännyt.
Ei tunneta yhteisvaikutuksia muiden lääkevalmisteiden kanssa.
Muiden verrattavissa olevien valmisteiden tai trombiiniliuosten kaltaisesti valmiste voi denaturoitua altistuessaan alkoholia, jodia tai raskasmetallia sisältäville liuoksille (esimerkiksi antiseptisille liuoksille). Tällaiset aineet tulee poistaa mahdollisimman huolellisesti ennen valmisteen applikointia.
Hapetettua selluloosaa sisältävät tuotteet voivat vähentää Tisseelin tehoa eikä niitä pidä käyttää kuljettimina.
Raskaus, imetys ja hedelmällisyys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
Lääkäri päättää, voitko käyttää Tisseel -valmistetta raskauden tai imetyksen aikana.
Ajaminen ja koneiden käyttö
Tisseel ei vaikuta kykyysi ajaa tai käyttää koneita.
Tärkeää tietoa Tisseelin sisältämistä aineista
Tiseel on valmistettu ihmisen plasmasta (veren nestemäisestä osasta). Ihmisen verestä tai plasmasta valmistettujen lääkkeiden välittämien infektioiden estämiseksi käytetään vakiintuneita toimenpiteitä. Näitä ovat luovuttajien valinta, yksittäisten luovutusten ja plasmapoolien tutkiminen tiettyjen infektiomarkkereiden suhteen sekä viruksia tehokkaasti inaktivoivat ja poistavat valmistusvaiheet. Tästä huolimatta taudinaiheuttajien siirtymismahdollisuutta ei voida täysin sulkea pois, kun annetaan ihmisen verestä tai plasmasta valmistettuja lääkkeitä. Tämä koskee myös tuntemattomia tai uusia viruksia ja muita patogeenejä.
Käytetyt toimenpiteet tehoavat vaipallisiin viruksiin, kuten ihmisen immuunikatovirukseen (HIV), hepatiitti B-virukseen ja hepatiitti C-virukseen, sekä vaipattomaan hepatiitti A-virukseen. Toimenpiteet tehoavat vain vähän vaipattomiin viruksiin, kuten parvovirukseen B19. Parvovirus B19 voi olla vaarallinen raskaana oleville naisille (sikiöinfektio) ja potilaille, joiden immuunijärjestelmä on heikentynyt tai joilla on jonkintyyppinen anemia (kuten sirppisoluanemia tai hemolyyttinen anemia).
Hepatiitti A- ja ‑B-rokotuksia on syytä harkita silloin, kun potilaat saavat säännöllisesti/toistuvasti ihmisen plasmasta valmistettuja kudosliimoja.
Aina annettaessa Tisseel -valmistetta on tärkeää kirjata valmisteen nimi ja eränumero potilastietoihin. Pakkauksen etiketissä on liimattava osa potilastietoihin liimattavaksi.
Polysorbaatti 80 voi aiheuttaa paikallista ihoärsytystä, kuten kosketusihottumaa.
Tisseel -valmistetta käytetään vain ohut kerros. Liian paksu hyytymä voi heikentää valmisteen tehoa ja haavan paranemista. Paineilmalaitteen tai painekaasulaitteen käyttö kudosliimaa sumutettaessa on aiheuttanut ilmaembolian tai kaasuembolian, kudoksen repeämisen tai ilmataskun aiheuttamaa kudospainetta, mikä voi olla hengenvaarallista. Nämä tapaukset näyttävät liittyvän suositeltua suuremman paineen käyttöön kudosliimaa applikoitaessa ja sumutettaessa hyvin läheltä kudoksen pinnalle.
Miten valmistetta käytetään
Tisseel -valmistetta saavat käyttää vain kirurgit, jotka on koulutettu käyttämään Tisseel -valmistetta.
Valmisteen tehoa ja turvallisuutta ei ole osoitettu lapsilla.
Ennen Tisseel -valmisteen applikoimista haavan pinta on kuivattava vakiotekniikoilla (esim. käyttämällä vuorotellen painesiteitä, vanutuppoja, imulaitetta). Lääkäri määrää applikoitavan annoksen kullekin potilaalle yksilöllisesti.
Älä käytä painekaasua haavan pinnan kuivaamiseen.
Tisseel -kudosliimaa saa applikoida vain näkyvillä oleviin haavapintoihin.
Applikoitava annos riippuu eri tekijöistä, kuten esim. kirurgisen toimenpiteen tyypistä, käsiteltävän pinnan koosta, applikointimenetelmästä sekä applikointikertojen määrästä.
Kliinisissä tutkimuksissa yksittäiset annokset ovat olleet tavallisesti 4 - 20 ml. Joissakin toimenpiteissä (esimerkiksi maksavaurioiden tai suurien palovammojen hoidossa) voidaan tarvita suurempia määriä.
Applikoitavan alkuannoksen on riitettävä peittämään koko valittu käsiteltävä alue. Applikointi voidaan toistaa tarvittaessa. On kuitenkin vältettävä applikoimasta Tisseeliä uudestaan aiemman, polymeroituneen Tisseel -kerroksen päälle, koska Tisseel ei kiinnity polymeroituneisiin kerroksiin. Tisseelin kahden komponentin erillisiä, peräkkäisiä applikointeja pitää välttää.
Pintojen yhdistämisessä 2 ml:n pakkaus Tisseel -valmistetta (eli 1 ml proteiiniliuosta sekä 1 ml trombiiniliuosta) riittää vähintään 10 cm2:n alueelle.
Sumutettaessa Tisseel -valmistetta sama määrä riittää huomattavasti suuremmalle alueelle käyttöaiheesta ja tapauksesta riippuen. Varovaisuutta pitää noudattaa applikoitaessa kudosliimaa painekaasun avulla.
Vältä applikointia suunnitellun alueen ulkopuolelle.
Tisseel -valmistetta applikoidaan mahdollisimman ohut kerros, jotta granulaatiokudosta ei muodostu liikaa ja fibriinihyytymä absorboituu vähitellen.
Varmistaaksesi proteiiniliuoksen ja trombiiniliuoksen täydellisen sekoittumisen, hävitä applikointineulasta pari ensimmäistä tippaa juuri ennen applikoinnin aloitusta.
Kun applikoit Tisseel ‑kudosliimaa ruiskutuslaitteen avulla, muista käyttää ruiskutuslaitteen valmistajan suosittelemaa painetta ja etäisyyttä kudoksesta seuraavasti:
| Tisseel -valmisteen applikointiin suositeltu paine, etäisyys ja ruiskutuslaitteet | |||||
| Leikkaus | Käytettävä ruiskutuslaite | Käytettävät applikaattorikärjet | Käytettävä paineensäätölaite | Suositeltu etäisyys kohdekudoksesta | Suositeltu ruiskutuspaine |
| Avohaava | Tisseel / Artiss Spray Set | Ei ole | EasySpray | 10-15 cm | 1,5-2,0 bar (21,5-28,5 psi). |
| Tisseel / Artiss Spray Set, 10 kpl:n pakkaus | Ei ole | EasySpray | |||
| Laparoskooppiset/mini-invasiiviset toimenpiteet | Ei ole | Duplospray MIS Applicator 20 cm | Duplospray MIS Regulator 1,5 bar
| 2-5 cm | 1,2-1,5 bar (18-22 psi) |
| Duplospray MIS Applicator 30 cm | |||||
| Duplospray MIS Applicator 40 cm | |||||
| Spray Set 360 endoskooppinen applikaattori Snap Lock -kiinnityksellä | |||||
| Spray Set 360 endoskooppinen applikaattori lukituspidikkeellä | |||||
| Vaihdettava kärki | |||||
Avoleikkauksissa on käytettävä painesäätelylaitetta, joka tuottaa korkeintaan 2,0 bar:n (28,5 psi:n) paineen.
Minimaalisesti kajoavissa / laparoskooppisissa toimenpiteissä on käytettävä painesäätelylaitetta, joka tuottaa korkeintaan 1,5 bar:n (22 psi:n) paineen ja käyttää vain hiilidioksidikaasua.
Ruiskutettaessa Tisseel ‑valmistetta verenpaineen, sykkeen, happisaturaation ja kertahengityksen CO2‑pitoisuuden vaihteluja on seurattava mahdollisen ilma‑ tai kaasuembolian esiintymisen varalta (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä).
Jos käytät enemmän Tisseel -valmistetta kuin sinun pitäisi
Kirurgi käyttää Tisseel -valmistetta vain leikkaustoimenpiteessä. Hän päättää myös Tisseel -valmisteen tarvittavan määrän. Ei tunneta yliannostustapauksia.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Käyttö lapsille
Valmisteen tehoa ja turvallisuutta ei ole osoitettu lapsilla.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa. Jos havaitset sellaisia haittavaikutuksia, joita ei ole tässä pakkausselosteessa mainittu, tai kokemasi haittavaikutus on vakava, kerro niistä lääkärille tai apteekkihenkilökunnalle.
Kudosliimalla hoidetut potilaat voivat saada yliherkkyysreaktioita tai allergisia reaktioita. Vaikka nämä ovat harvinaisia, ne voivat olla vaikeita.
Allergisen reaktion ensimmäisiä merkkejä voivat olla:
- ohimenevä ihon punastelu
- kutina
- rakkulaihottuma
- pahoinvointi, oksentelu
- päänsärky
- uneliaisuus
- levottomuus
- polttelu ja kirvely applikointikohdalla
- pistely
- vilunväreet
- rinnan ahdistus
- huulten, kielen, kurkun turpoaminen (mistä voi seurata hengitysvaikeuksia ja/tai nielemisvaikeuksia)
- hengitysvaikeuksia
- matala verenpaine
- sydämen lyöntitiheyden kiihtyminen tai hidastuminen
- tajuttomuus, joka johtuu verenpaineen laskusta.
Yksittäisissä tapauksissa näistä reaktioista on kehittynyt vaikea anafylaksia. Näitä reaktioita esiintyy erityisesti silloin, kun valmistetta applikoidaan uudestaan tai käytetään potilailla, joiden tiedetään olevan yliherkkiä aprotiniinille tai muille valmisteen sisältämille aineille.
Vaikka potilas olisi sietänyt Tisseel -valmistetta hyvin ensimmäisillä kerroilla, Tisseel -valmisteen seuraavat antokerrat tai aprotiniinin systeeminen anto voivat aiheuttaa vakavia anafylaktisia reaktioita. Synteettinen aprotiniini rakenteeltaan on samanlainen kuin naudan aprotiniini. Tisseelin käyttöä naudan proteiineille allergisilla potilailla tulee harkita erittäin huolellisesti.
Leikkaussalihenkilökunta tietää hyvin tämäntyyppisten reaktioiden riskin ja keskeyttää Tisseelin applikoinnin heti ensimmäisten yliherkkyysoireiden ilmaannuttua. Vaikeat oireet voivat vaatia tehohoitoa.
Tisseel -valmisteen applikointi pehmytkudoksiin voi aiheuttaa paikallisia kudosvaurioita.
Tisseel -valmisteen applikointi verisuoniin (laskimoihin tai valtimoihin) voi aiheuttaa hyytymiä (tromboosin). Verisuoneen applikointi voi lisätä herkillä potilailla äkillisen yliherkkyysreaktion todennäköisyyttä ja vaikeutta.
Koska Tisseel valmistetaan verenluovutuksessa saadusta plasmasta, taudinkantajien siirtymisvaaraa ei voida täydellisesti sulkea pois, mutta valmistaja vähentää tätä vaaraa useilla toimenpiteillä (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä).
Kudosliiman komponenteille voi muodostua harvoin vasta-aineita.
Seuraavia haittavaikutuksia on havaittu Tisseel -valmistetta käytettäessä
Haittavaikutukset luokitellaan seuraavasti esiintyvyyden mukaisesti:
Hyvin yleiset: useammalla kuin 1 potilaalla 10:stä hoidetusta potilaasta
Yleiset: 1–10 potilaalla 100:sta hoidetusta potilaasta
Melko harvinaiset: 1–10 potilaalla 1000:sta hoidetusta potilaasta
Harvinaiset: 1–10 potilaalla 10000:sta hoidetusta potilaasta
Hyvin harvinaiset: harvemmalla kuin 1 potilaalla 10000:sta hoidetusta potilaasta
Tuntematon: esiintyvyyttä ei voida arvioida saatavilla olevien tietojen perusteella
| Elinluokitus | Haittavaikutukset | Yleisyys |
| Infektiot | leikkaushaavan infektio | yleinen |
| Immuunijärjestelmä | yliherkkyysreaktiot | tuntematon |
| anafylaktiset reaktiot | tuntematon | |
| anafylaktinen sokki | tuntematon | |
| Hermosto | aistien tuntohäiriöt | yleinen |
| tuntoharha | tuntematon | |
| Sydän | sydämen harvalyöntisyys | tuntematon |
| sydämen tiheälyöntisyys | tuntematon | |
| Verisuonisto | kainalolaskimon tukos | yleinen |
| matala verenpaine | harvinainen | |
| verenpurkauma NOS | tuntematon | |
| veritulppa | tuntematon | |
| ilma-/kaasuembolia* | tuntematon | |
| aivovaltimon tukos | tuntematon | |
| aivoinfarkti | tuntematon | |
| Hengityselimet, rintakehä ja välikarsina | hengenahdistus | tuntematon |
| keuhkoputkien kouristus | tuntematon | |
| vinkuva hengitys | tuntematon | |
| Ruoansulatuselimistö | pahoinvointi | melko harvinainen |
| suolentukkeuma | tuntematon | |
| Iho ja ihonalainen kudos | nokkosihottuma | tuntematon |
| ihottuma | yleinen | |
| kutina | tuntematon | |
| punoittava ihottuma | tuntematon | |
| heikentynyt paraneminen | tuntematon | |
| angioödeema | tuntematon | |
| Luusto, lihakset ja sidekudos | raajojen särky | yleinen |
| Yleisoireet ja antopaikassa todettavat haitat | toimenpiteen aiheuttama kipu | melko harvinainen |
| kipu | yleinen | |
| kuume | yleinen | |
| punastelu | tuntematon | |
| turvotus | tuntematon | |
| Vammat ja myrkytykset | serooma | hyvin yleinen |
| Tutkimukset | fibriinin hajoamistuotteiden määrän lisääntyminen | melko harvinainen |
| D-dimeerien lisääntyminen fibriinissä | melko harvinainen |
* ilma- ja kaasukuplia on esiintynyt verenkierrossa kun kudosliimoja applikoidaan käyttäen ruiskutuslaitteita, joissa on paineensäädin. Tämä tapahtuma vaikuttaa liittyvän ruiskutuslaitteen käyttöön ohjeiden vastaisesti (esim. suositeltua suuremmalla paineella ja/tai lähellä kudoksen pintaa).
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus‐ ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55, 00034 FIMEA
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen.
Säilytä ja kuljeta pakastettuna (vähintään -20 °C) ennen käyttöä.
Säilytä alkuperäispakkauksessa. Herkkä valolle.
Säilyttäminen sulattamisen jälkeen:
Avaamattomat alle 25 °C:ssa sulatetut pussit, voidaan säilyttää 72 tuntia valvotussa huoneenlämmössä (alle 25 °C).
Sulattamisen jälkeen liuoksia ei saa pakastaa uudelleen tai säilyttää jääkaapissa!
Lääkkeitä ei tule heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Tisseel sisältää
Tisseel -valmisteessa on kaksi komponenttia:
Komponentti 1 = proteiiniliuos (Tisseel -liuos):
1 ml proteiiniliuoksessa on seuraavat vaikuttavat aineet: ihmisen fibrinogeeni 91 mg/ml, synteettinen aprotiniini 3 000 KIU/ml.
Apuaineet ovat: ihmisen albumiini, L-histidiini, niasiiniamidi, polysorbaatti 80 (Tween 80), natriumsitraattidihydraatti, injektionesteisiin käytettävä vesi.
Komponentti 2 = trombiiniliuos:
1 ml trombiiniliuoksessa on seuraavat vaikuttavat aineet: ihmisen trombiini 500 IU/ml, kalsiumklorididihydraatti 40 mikromol/ml.
Apuaineet ovat: ihmisen albumiini, natriumkloridi ja injektionesteisiin käytettävä vesi.
| Sekoituksen jälkeen | 1 ml | 2 ml | 4 ml | 10 ml |
| Komponentti 1, proteiiniliuos (Tisseel -liuos): | ||||
| ihmisen fibrinogeeni (hyytyvä proteiini) | 45,5 mg | 91 mg | 182 mg | 455 mg |
| synteettinen aprotiniini | 1500 KIU | 3000 KIU | 6000 KIU | 15000 KIU |
| Komponentti 2, trombiini liuos: | ||||
| ihmisen trombiini | 250 IU | 500 IU | 1000 IU | 2500 IU |
| kalsiumklorididihydraatti | 20 mikromol | 40 mikromol | 80 mikromol | 200 mikromol |
Tisseel -valmisteessa on 0,6 – 5 IU/ml ihmisen hyytymistekijä XIII, joka kerapuhdistuu ihmisen fibrinogeenin puhdistamisen yhteydessä.
Lääkevalmisteen kuvaus ja pakkauskoot
Kudosliimat.
Sekä proteiiniliuos (Tisseel -liuos) että trombiiniliuos ovat kertakäyttöisessä kaksisäiliöisessä ruiskussa, sulatuksen jälkeen käyttövalmiina.
Pakastetut liuokset ovat värittömiä tai hieman kellertäviä ja opalisoivia. Sulatuksen jälkeen liuokset ovat värittömiä tai vaalean kellertäviä.
Pakkauksessa on
PRIMA -ruisku:
- 1 ml, 2 ml tai 5 ml proteiiniliuosta ja 1 ml, 2 ml tai 5 ml trombiiniliuosta esitäytetyssä kaksisäiliöisessä ruiskussa (polypropyleeniä), jossa on kärkisuojus ja joka on pakattu kahteen pussiin
- laite, jossa on 2 yhdyskappaletta ja 4 applikointineulaa
Pakkauskoot:
1 x 2ml (1 ml + 1 ml), 10 x 2ml, 1 x 4 ml (2 ml + 2 ml), 10 x 4 ml, 1 x 10 ml (5 ml + 5 ml), 10 x 10 ml.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija
Baxter Oy, PL 35, 01531 Vantaa
Valmistaja
Takeda Manufacturing Austria AG, Industriestrasse 67, A-1221 Wien, Itävalta
Tämä pakkausseloste on päivitetty viimeksi 01.10.2025
Ohjeet terveydenhuollon ammattilaiselle
Seuraavat tiedot on tarkoitettu vain hoitoalan ammattilaisille (lopullinen pakkaus: PRIMA -ruisku):
Yleistä tietoa
- Ennen Tisseel -valmisteen käyttöä on suojattava käyttöalueen ulkopuoliset kehon osat, jotta liimataan vain suunnitellut kohteet.
- Kostuta leikkauskäsineet ja instrumentit natriumkloridiliuoksella ennen kuin käytät Tisseel -valmistetta, jotta Tisseel ei tartu niihin.
- Ohjeet pintojen yhdistämiseen: Yksi 2 ml:n pakkaus Tisseel -valmistetta (eli 1 ml proteiiniliuosta sekä 1 ml trombiiniliuosta) riittää vähintään 10 cm2:n alueelle.
- Tarvittava annos riippuu käsiteltävän alueen koosta.
- ÄLÄ applikoi Tisseel -valmisteen komponentteja erikseen. Komponentit on applikoitava yhdessä.
- ÄLÄ altista Tisseel -valmistetta yli 37 °C:n lämpötiloille. ÄLÄ laita valmistetta mikroaaltouuniin.
- ÄLÄ sulata valmistetta pitämällä sitä kädessä.
- ÄLÄ käytä Tisseel -valmistetta, ennen kuin se on täysin sulanut ja lämmennyt 33–37 °C:een.
- Poista ruiskun suojakorkki vasta kun valmiste on täysin sulanut ja lämmennyt. Ruiskun kärjen suojakorkki irtoaa helpommin, jos liikutat sitä edestakaisin, ennen kuin vedät sen irti ruiskusta.
- Poista ruiskusta kaikki ilma ja kiinnitä sitten yhdyskappale ja applikointineula.
Käsittely- ja valmisteluohjeet Sekä proteiiniliuos että trombiiniliuos ovat valmiina esitäytetyssä ruiskussa. Valmiste on pakattu kahteen steriiliin pussiin aseptisesti. Sisäpussi ja sen sisältö pysyvät steriileinä niin kauan kuin ulkopussi on ehjä. Siirrä steriili sisäpussi ja sen sisältö steriiliä tekniikkaa käyttäen steriilille alueelle.
Esitäytetyn ruiskun voi sulattaa JA lämmittää jollakin seuraavista menetelmistä:
- Nopea sulatus/lämmitys (steriilissä vesihauteessa) – suositeltu menetelmä
- Sulatus/lämmitys epästeriilissä vesihauteessa
- Sulatus/lämmitys inkubaattorissa
- Esitäytetyn ruiskun voi myös sulattaa ja sitä voi säilyttää huoneenlämmössä (enintään 25 °C) enintään 72 tunnin ajan. Valmiste on lämmitettävä ennen käyttöä.
1) Nopea sulatus/lämmitys (steriilissä vesihauteessa) – suositeltu menetelmä Kudosliimakomponentit on suositeltavaa sulattaa ja lämmittää steriilissä vesihauteessa 33–37 °C:n lämpötilassa.
- Vesihauteen lämpötila saa olla enintään 37 °C. Määrätyllä lämpötila-alueella pysyminen tulee varmistaa tarkkailemalla veden lämpötilaa lämpömittarilla ja vaihtamalla vesi tarvittaessa.
- Jos valmiste sulatetaan ja lämmitetään steriilissä vesihauteessa, esitäytetty ruisku on poistettava pusseista ennen steriiliin vesihauteeseen asettamista.
Ohjeet:
Siirrä sisäpussi steriilille alueelle, poista esitäytetty ruisku sisäpussista ja aseta se heti steriiliin vesihauteeseen. Varmista, että esitäytetyn ruiskun sisältö on kokonaan veden alla.
Taulukko 1 – PRIMA -ruisku: Vähimmäissulatus- ja lämmitysajat steriilissä vesihauteessa
| Pakkauskoko | Vähimmäissulatus-/lämmitysajat 33–37 °C, steriili vesihaude Valmiste poistettu pusseista |
| 2 ml | 5 minuuttia |
| 4 ml | 5 minuuttia |
| 10 ml | 10 minuuttia |
2) Sulatus/lämmitys epästeriilissä vesihauteessa
Ohjeet:
Pidä esitäytetty ruisku pusseissaan ja aseta se vesihauteeseen steriilin alueen ulkopuolelle riittävän pitkäksi ajaksi (ks. taulukko 2). Varmista, että pussit pysyvät veden alla koko sulatuksen ajan. Poista pussit vesihauteesta sulatuksen jälkeen, kuivaa ulkopussi ja siirrä sisäpussi esitäytettyine ruiskuineen ja mäntineen steriilille alueelle.
Taulukko 2 – PRIMA -ruisku: Vähimmäissulatus- ja lämmitysajat epästeriilissä vesihauteessa
| Pakkauskoko | Vähimmäissulatus-/lämmitysajat 33–37 °C, epästeriili vesihaude Valmiste pusseissa |
| 2 ml | 15 minuuttia |
| 4 ml | 20 minuuttia |
| 10 ml | 35 minuuttia |
3) Sulatus/lämmitys inkubaattorissa
Ohjeet:
Pidä esitäytetty ruisku pusseissaan ja aseta se inkubaattoriin steriilin alueen ulkopuolelle riittävän pitkäksi ajaksi (ks. taulukko 3). Poista pussit inkubaattorista sulatuksen/lämmityksen jälkeen, poista ulkopussi ja siirrä sisäpussi esitäytettyine ruiskuineen steriilille alueelle.
Taulukko 3 – PRIMA -ruisku: Vähimmäissulatus- ja lämmitysajat inkubaattorissa
| Pakkauskoko | Vähimmäissulatus-/lämmitysajat 33–37 °C, inkubaattori Valmiste pusseissa |
| 2 ml | 40 minuuttia |
| 4 ml | 50 minuuttia |
| 10 ml | 90 minuuttia |
4) Sulatus huoneenlämmössä (enintään 25 °C) ENNEN lämmitystä
Ohjeet:
Pidä esitäytetty ruisku pusseissaan ja anna sen sulaa huoneenlämmössä steriilin alueen ulkopuolella riittävän pitkän ajan (ks. taulukko 4). Sulatuksen jälkeen ulkopussissaan oleva valmiste lämmitetään käyttövalmiiksi inkubaattorissa.
Taulukko 4 – PRIMA -ruisku: Vähimmäissulatusajat huoneenlämmössä steriilin alueen ulkopuolella ja lisälämmitysajat inkubaattorissa 33–37 °C:n lämpötilassa
| Pakkauskoko | Valmisteen vähimmäissulatusajat huoneenlämmössä (enintään 25 °C) Valmiste pusseissa |
Käyttöä edeltävät lämmitysajat 33–37 °C:n lämpötilaan inkubaattorissa, kun valmiste on sulatettu huoneenlämmössä Valmiste pusseissa |
| 2 ml | 80 minuuttia + 11 minuuttia | |
| 4 ml | 90 minuuttia + 13 minuuttia | |
| 10 ml | 160 minuuttia + 25 minuuttia | |
Huoneenlämmössä sulatettu valmiste on käytettävä 72 tunnin kuluessa pakastimesta poistamisen jälkeen.
Säilyvyys sulatuksen jälkeen
Sulatuksen ja lämmityksen (33–37 °C:ssa, menetelmät 1, 2 ja 3) jälkeen valmisteen kemiallis-fysikaalinen säilyvyys on osoitettu 12 tunnin ajalta 33–37 °C:n lämpötilassa.
Huoneenlämmössä sulatetun, avaamattomassa pussissa olevan (menetelmä 4) valmisteen kemiallis-fysikaalinen säilyvyys on osoitettu 72 tunnin ajalta enintään 25 °C:n lämpötilassa. Lämmitä valmiste 33–37 °C:n lämpötilaan juuri ennen käyttöä.
Mikrobiologiselta kannalta valmiste tulee käyttää välittömästi 33–37 °C:n lämpötilaan lämmittämisen jälkeen, ellei avaamis-/sulatusmenetelmä estä mikrobiologista kontaminaatiota.
Jos valmistetta ei käytetä heti, käytön aikaiset säilytysolosuhteet ja -aika ovat käyttäjän vastuulla.
Osittain sulanutta valmistetta ei saa pakastaa tai jäähdyttää uudelleen.
Käsittely sulatuksen jälkeen/ennen applikointia
Jotta saadaan paras näiden kahden liuoksen seos ja kudosliima jähmettyy optimaalisesti, pidä nämä kaksi liimakomponenttia 33–37 °C:n lämpötilassa applikointiin asti.
Proteiini- ja trombiiniliuosten tulee olla kirkkaita tai hieman opalisoivia. Älä käytä sameita liuoksia tai liuoksia, joissa on saostumia. Sulatettu valmiste on tarkistettava silmämääräisesti hiukkasten, värimuutosten tai muiden muutosten varalta ennen käyttöä. Mainittuja seikkoja havaittaessa liuokset on hävitettävä.
Sulatetun proteiiniliuoksen tulee olla hieman viskoosinen neste. Jos liuoksen koostumus muistuttaa jähmeää geeliä, on oletettava, että se on denaturoitunut (esimerkiksi kylmäketjun katkeamisen tai lämmityksen yhteydessä tapahtuneen liiallisen kuumentamisen vuoksi). Tällöin Tisseel -valmistetta EI SAA missään tapauksessa käyttää.
- Ota ruisku pusseista juuri ennen käyttöä.
- Älä käytä Tisseel -valmistetta, ennen kuin se on täysin sulanut ja lämmennyt (nestemäinen koostumus).
- Irrota ruiskun suojakorkki juuri ennen käyttöä.
Ruiskun kärjen suojakorkki irtoaa helpommin, jos liikutat sitä edestakaisin ennen kuin vedät sen irti ruiskusta.
Applikointi PRIMA -ruiskulla:
Applikointia varten proteiini- ja trombiiniliuoksen sisältävä kaksisäiliöinen, esitäytetty ruisku on liitettävä yhdyskappaleeseen ja applikointineulaan, jotka ovat applikointilaitteen pakkauksessa mukana. Kaksisäiliöisen, esitäytetyn ruiskun yhteisen männän ansiosta yhdyskappaleen läpi syötetään sama määrä molempia kudosliiman komponentteja. Komponentit sekoittuvat applikointineulassa ennen annostelua.
PRIMA -ruiskun käyttöohjeet
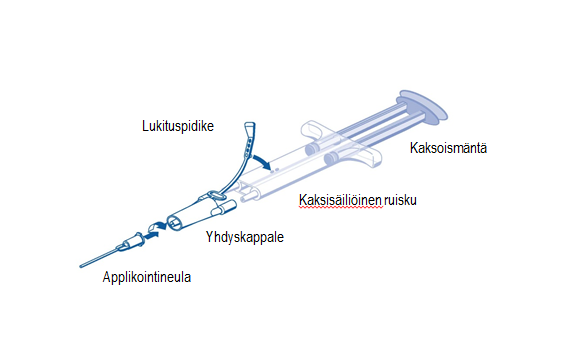
- Poista ruiskusta kaikki ilma ennen minkään applikointilaitteen kiinnittämistä.
- Kohdista yhdyskappale ja lukituspidike ruiskun kylkeen lukituspidikkeen reiän avulla.
- Kiinnitä yhdyskappale kaksisäiliöisen, esitäytetyn ruiskun suukappaleisiin ja varmista, että se on tiiviisti paikoillaan.
- Kiinnitä yhdyskappale lukituspidikkeen avulla kaksisäiliöiseen, esitäytettyyn ruiskuun.
- Jos lukituspidike katkeaa, käytä pakkauksessa olevaa varayhdyskappaletta.
- Jos käytettävissä ei ole yhtään varayhdyskappaletta, voit silti käyttää ruiskujärjestelmää, jos varmistat, että yhdyskappale on tiiviisti paikoillaan eikä vuoda.
- ÄLÄ poista jäljellä olevaa ilmaa yhdyskappaleesta.
- Kiinnitä applikointineula yhdyskappaleeseen.
- ÄLÄ poista jäljellä olevaa ilmaa yhdyskappaleesta ja applikointineulasta ennen varsinaista applikointia, sillä applikointineula voi tukkeutua.
Applikointi
Ennen Tisseel -valmisteen applikoimista haavan pinta on kuivattava vakiotekniikoilla (esim. käyttämällä vuorotellen painesiteitä, vanutuppoja, imulaitteita). Älä käytä paineilmaa tai -kaasua alueen kuivaamiseen.
- Applikoi proteiiniliuoksen ja trombiiniliuoksen seos kohdepinnalle tai liitettäville pinnoille painamalla yhteistä mäntää hitaasti.
- Kirurgisissa toimenpiteissä, joissa tarvitaan vain hyvin vähän kudosliimaa, on suositeltavaa hävittää valmisteen pari ensimmäistä tippaa.
- Odota vähintään 2 minuuttia Tisseel -valmisteen applikoinnin jälkeen riittävän polymeroitumisen aikaansaamiseksi.
Huomautus: Jos kudosliiman komponenttien applikointi keskeytetään, applikointineula saattaa tukkeutua. Vaihda tällöin applikointineula uuteen vasta juuri ennen applikoinnin jatkamista. Jos yhdyskappaleen aukot tukkeutuvat, käytä pakkauksessa olevaa varayhdyskappaletta.
Komponenttien sekoittamisen jälkeen kudosliima alkaa muutamassa sekunnissa jähmettyä korkean trombiinipitoisuutensa takia (500 IU/ml).
Kudosliima voidaan applikoida myös muilla Baxterin valmistamilla välineillä, jotka sopivat esimerkiksi endoskooppiseen käyttöön, mini-invasiiviseen kirurgiaan tai applikointiin suurille tai vaikeapääsyisille alueille. Käytä näitä applikaattoreita huolellisesti käyttöohjeiden mukaisesti.
Hapetettua selluloosaa sisältäviä valmisteita ei tule käyttää Tisseel -valmisteen kanssa, koska matala pH-arvo heikentää trombiinin vaikutusta.
Joillakin käyttöalueilla bioyhteensopivia materiaaleja, kuten kollageenihuopaa, käytetään kantaja-aineena tai vahvikkeena.
Applikointi ruiskuttamalla
Kun applikoit Tisseel -valmistetta ruiskutuslaitteen avulla, muista käyttää valmistajan suosittelemaa painetta ja etäisyyttä kudoksesta seuraavasti:
| Tisseel -valmisteen applikointiin suositeltu paine, etäisyys ja ruiskutuslaitteet | |||||
| Leikkaus | Käytettävä ruiskutuslaite | Käytettävät applikaattorikärjet | Käytettävä paineensäätölaite | Suositeltu etäisyys kohdekudoksesta | Suositeltu ruiskutuspaine |
| Avohaava | Tisseel / Artiss Spray Set | Ei ole | EasySpray | 10-15 cm | 1,5-2,0 bar (21,5-28,5 psi). |
| Tisseel / Artiss Spray Set, 10 kpl:n pakkaus | Ei ole | EasySpray | |||
| Laparoskooppiset/mini-invasiiviset toimenpiteet | Ei ole | Duplospray MIS Applicator 20 cm | Duplospray MIS Regulator 1,5 bar | 2-5 cm | 1,2-1,5 bar (18-22 psi) |
| Duplospray MIS Applicator 30 cm | |||||
| Duplospray MIS Applicator 40 cm | |||||
| Spray Set 360 endoskooppinen applikaattori Snap Lock -kiinnityksellä | |||||
| Spray Set 360 endoskooppinen applikaattori lukituspidikkeellä | |||||
| Vaihdettava kärki | |||||
Avoleikkauksissa on käytettävä painesäätelylaitetta, joka tuottaa korkeintaan 2,0 bar:n (28,5 psi:n) paineen.
Minimaalisesti kajoavissa / laparoskooppisissa toimenpiteissä on käytettävä painesäätelylaitetta, joka tuottaa korkeintaan 1,5 bar:n (22 psi:n) paineen ja käyttää vain hiilidioksidikaasua.
Ruiskutettaessa Tisseel -valmistetta verenpaineen, sykkeen, happisaturaation ja uloshengityksen CO2-pitoisuuden vaihteluja on seurattava mahdollisen ilma- tai kaasuembolian esiintymisen varalta (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä).
Jos Tisseel -valmistetta applikoidaan suljetuilla rintakehän ja vatsan alueilla, suositellaan DuploSpray MIS -applikaattorin ja paineensäätöjärjestelmän käyttöä. Tutustu DuploSpray MIS -laitteen käyttöohjeeseen.
Hävittäminen
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.