MAXITROL ögondroppar, suspension
Tilläggsinformation
Maxitrol ögondroppar, suspension
dexametason 1 mg/ml, neomycinsulfat motsvarande 3500 IU/ml neomycin och polymyxin B sulfat 6000 IU/ml
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad Maxitrol är och vad det används för
- Vad du behöver veta innan du använder Maxitrol
- Hur du använder Maxitrol
- Eventuella biverkningar
- Hur Maxitrol ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Maxitrol är en kombination av tre aktiva substanser: steroiden dexametason som används för att lindra symtom vid ögoninflammation och två antibiotika, polymyxin B sulfat och neomycinsulfat, vilka verkar mot organismer som orsakar ögoninflammationer.
Maxitrol används för att behandla kortvariga inflammationer i ögat då behandling med antibiotika är nödvändigt för att förhindra en infektion.
Dexametason, polymyxin B sulfat och neomycin som finns i Maxitrol kan också vara godkända för att behandla andra sjukdomar som inte nämns i denna bipacksedel. Fråga läkare, apotekspersonal eller annan hälso- och sjukvårdspersonal om du har ytterligare frågor och följ alltid deras instruktion.
Vad du behöver veta innan produkten används
Använd inte Maxitrol
- om du är allergisk mot dexametason, polymyxin B sulfat, neomycin eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar)
- om du har inflammation på hornhinnan orsakad av herpes simplex virus, smittkoppor, vattkoppor/bältros eller någon annan virusinfektion i ögat
- om du har en svampsjukdom i ögat eller en obehandlad parasitinfektion i ögat
- om du har ögontuberkulos eller någon annan mykobakterie-infektion i ögat
- om du har någon ögoninflammation som orsakar varigt sekret.
Varningar och försiktighet
Kontakta läkare om du upplever dimsyn eller andra synrubbningar.
Tala med din läkare om du får svullnad och viktökning kring bålen och i ansiktet, eftersom detta vanligen är de första tecknen på ett syndrom som kallas Cushings syndrom. Hämmad binjurefunktion kan utvecklas efter avslutande av en långtidsbehandling eller intensiv behandling med Maxitrol. Dessa risker är särskilt viktiga för barn och patienter som behandlas med läkemedel som kallas ritonavir eller kobicistat. Tala därför med din läkare innan du avslutar behandlingen själv.
Tala med läkare eller apotekspersonal innan du använder Maxitrol.
Om du upplever en allergisk reaktion med Maxitrol, avsluta behandlingen och kontakta läkaren. Allergiska reaktioner kan variera från lokal klåda eller hudrodnad till svåra allergiska reaktioner (anafylaktisk reaktion) eller allvarliga hudreaktioner. Dessa allergiska reaktioner kan uppkomma med andra lokala eller systemiska antibiotika av samma typ (aminoglykosider).
- Användning av detta läkemedel kan orsaka hudrodnad, irritation och obehagskänsla i huden.
- Om du använder andra antibiotika under behandling med Maxitrol, fråga läkaren om råd.
- Vid långvarig användning av Maxitrol, kan du:
- få förhöjt ögontryck, så ditt ögontryck skall kontrolleras regelbundet under behandling med Maxitrol. Detta är speciellt viktigt hos barnpatienter, då risken för förhöjt tryck i ögat orsakat av kortison kan vara högre hos barn och uppkomma tidigare än hos vuxna.
Maxitrol är inte godkänt för behandling av barn. Risken för förhöjt ögontryck orsakat av kortison och/eller uppkomst av starr är förhöjd hos patienter med benägenhet för detta (t.ex. diabetespatienter). - utveckla starr
- bli mera benägen för ögoninflammationer
- få förhöjt ögontryck, så ditt ögontryck skall kontrolleras regelbundet under behandling med Maxitrol. Detta är speciellt viktigt hos barnpatienter, då risken för förhöjt tryck i ögat orsakat av kortison kan vara högre hos barn och uppkomma tidigare än hos vuxna.
- Om symptomen förvärras eller snabbt återkommer, kontakta läkaren.
- Du kan bli känsligare för ögoninfektioner när du använder denna produkt
- Steroider som appliceras i ögat kan fördröja läkningen av sår i ögat. Man vet också att lokala anti-inflammatoriska värkmediciner hindrar och fördröjer läkning. Samtidig användning av lokala anti-inflammatoriska läkemedel och lokala steroider kan öka risken för möjliga läkningsproblem.
- Tala med läkare eller apotekspersonal innan användning av detta läkemedel, om du har en sjukdom som förtunnar ögonvävnad.
- Om du använder kontaktlinser:
- användning av kontaktlinser (mjuka eller hårda) rekommenderas inte under behandling av ögoninflammation eller infektion.
Andra läkemedel och Maxitrol
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
Tala särskilt om för läkare om du använder:
- lokala anti-inflammatoriska värkmediciner. Samtidig användning av lokala steroider och lokala anti-inflammatoriska värkmediciner kan öka läkningsproblem av hornhinnan
- ritonavir eller kobicistat, eftersom detta kan öka mängden dexametason i blodet.
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du använder detta läkemedel.
Maxitrol rekommenderas inte under graviditet eller amning.
Körförmåga och användning av maskiner
Din syn kan vara dimmig en tid efter att du har använt Maxitrol. Kör inte och använd inte maskiner innan dimsynen har försvunnit.
Du är själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbete som kräver skärpt uppmärksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användning av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med din läkare eller apotekspersonal om du är osäker.
Maxitrol innehåller bensalkoniumklorid
Detta läkemedel innehåller 0,2 mg bensalkoniumklorid per 5 ml motsvarande 0,04 mg/ml.
Bensalkoniumklorid kan tas upp av mjuka kontaktlinser och kan missfärga kontaktlinserna. Om din läkare anser att du kan använda kontaktlinser ta ut kontaktlinser innan du använder läkemedlet och vänta minst 15 minuter innan kontaktlinserna sätts in igen.
Bensalkoniumklorid kan vara irriterande för ögon, särskilt om du har torra ögon eller problem med hornhinnan (den klara hinnan längst fram i ögat). Om du känner irritation, stickningar eller smärta i ögat efter att ha använt läkemedlet, kontakta läkare
Hur produkten används
Använd alltid detta läkemedel enligt läkarens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Använd Maxitrol enbart till att droppas i ögonen.
Rekommenderad dos är
Vuxna: 1-2 droppar 4-6 gånger dagligen eller oftare, om du har en allvarlig ögoninfektion.
Läkaren avgör alltid hur länge behandlingen varar.
Hur Maxitrol används rätt:
Om plastringen, som försäkrar att flaskan är oöppnad, är lös efter att korken har öppnats, avlägsna den före användning.
- Ta fram Maxitrol-flaskan.
- Tvätta händerna och sätt dig framför spegeln.
- Skaka flaskan väl före användning.
- Skruva av korken på flaskan.
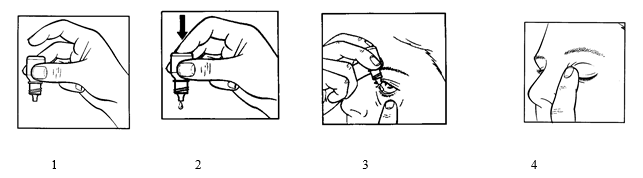
- Håll flaskan upp och ned, mellan tummen och långfingret (bild 1).
- Luta huvudet bakåt. Dra ner det undre ögonlocket med ett rent finger så att det bildas en ”ficka” mellan undre ögonlocket och ditt öga. Ögondroppen ska droppas i denna ficka.
- För flaskans spets nära ögat. Använd spegeln om det hjälper.
- Rör inte ögat eller ögonlocket, omgivande hud eller andra ytor med droppflaskan. Detta kan kontaminera ögondropparna.
- Tryck inte om flaskan: den är utvecklad så att ett litet tryck i bottnet på flaskan är allt som behövs (bild 2).
- Tryck lätt i bottnet på flaskan för att droppa en Maxitrol-droppe åt gången (bild 3).
- Efter att du använt Maxitrol, stäng ögonlocket och tryck lätt med fingret i ögonvrån vid näsan under 2 minuters tid (bild 4). På detta sätt undviker man att Maxitrol kommer annanstans i kroppen.
- Om du använder Maxitrol i båda ögonen, upprepa stegen 5-11 för det andra ögat.
- Skruva tillbaka korken ordentligt omedelbart efter användning.
- Använd endast en flaska åt gången. Öppna inte påsen innan du behöver använda flaskan.
Om en droppe missar ditt öga, försök igen.
Om du använder andra ögondroppar eller ögonsalva, ska du vänta minst 5 minuter mellan doseringarna av varje medicin. Ögonsalvor ska alltid doseras sist.
Om du har använt för stor mängd av Maxitrol
Om du fått i dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedlet av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel. 0800 147 111) för bedömning av risken samt rådgivning.
Skölj bort allt läkemedel från ögat med varmt vatten. Droppa inte i flera droppar innan det är dags för följande dos.
Om du har glömt att använda Maxitrol
Om du glömmer att dosera en dos, ta den så fort du kommer ihåg. Om det nästan är dags för din följande dos ska du hoppa över den missade dosen.
Ta inte dubbel dos för att kompensera för glömd dos.
Om du slutar att använda Maxitrol
Sluta inte att använda detta läkemedel för tidigt, även om symptomen har försvunnit. Om du slutar att ta detta läkemedel för tidigt, kan symptomen återkomma.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Vanliga (kan förekomma hos upp till 1 av 10 användare):
Allmänna biverkningar: allergi.
Mindre vanliga (kan förekomma hos upp till 1 av 100 användare):
Biverkningar i ögat: inflammation av ytan på ögat, förhöjt tryck i ögat, dimsyn, ljuskänslighet, förstorad pupill, hängande ögonlock, ögonsmärta, svullet öga, kliande öga, obehagskänsla i ögat, onormal känsla i ögat, rodnad i ögat, ökad tårproduktion, skada på ögonnerven, starr, ögonirritation.
Ingen känd frekvens (kan inte beräknas från tillgängliga data):
Biverkningar i ögat: förtunning av ytan på ögat, hål på ytan av ögat, inflammation inne i ögat, ögonsjukdom, grumling av ögat, dimsyn.
Hormonbesvär: extra hårväxt på kroppen (särskilt hos kvinnor), muskelsvaghet och -förtvining, lila bristningar i huden, högt blodtryck, oregelbundna eller inga menstruationer, förändringar i protein- och kalciumhalterna i kroppen, tillväxthämning hos barn och ungdomar samt svullnad och viktökning på kroppen och i ansiktet (kallas Cushings syndrom, se avsnitt Vad du behöver veta innan produkten används “Varningar och försiktighet”).
Allmänna biverkningar: huvudvärk, sår i hornhinnan, allvarliga hudreaktioner (Stevens-Johnsons syndrom).
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan) via det nationella rapporteringssystemet. Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på förpackningen. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras vid högst 25 °C. Förvaras i skydd mot kyla.
En öppnad flaska bör användas inom 4 veckor. Kasta bort flaskan efter denna tidpunkt. På detta sätt kan du undvika att infektionen sprids.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- De aktiva substanserna är dexametson, neomycinsulfat och polymyxin B sulfat. 1 ml av vätskan innehåller 1 mg dexametason, neomycinsulfat motsvarande 3500 IU (internationella enheter, IE) neomycin och polymyxin B sulfat 6000 IU (internationella enheter, IE).
- Övriga innehållsämnen är benzalkoniumklorid 0,04 mg (konserveringsmedel), polysorbat 20, hypromellos, natriumklorid, saltsyra/natriumhydroxid (för justering av pH) och renat vatten.
Läkemedlets utseende och förpackningsstorlekar
Maxitrol är en vätska (vit eller svagt gul, ogenomskinlig suspension) som är förpackad i en 5 ml:s plastflaska med skruvlock.
Innehavare av godkännande för försäljning:
Novartis Finland Oy
Norrskensgränden 1
02100 Esbo
Tillverkare:
Novartis Manufacturing NV
Rijksweg 14
2870 Puurs-Sint-Amands
Belgien
Novartis Farmacéutica, S.A.
Gran Via de les Corts Catalanes, 764
08013 Barcelona
Spanien
Denna bipacksedel ändrades senast 9.12.2025