VAXNEUVANCE injektioneste, suspensio, esitäytetty ruisku
Vaxneuvance injektioneste, suspensio, esitäytetty ruisku
pneumokokkipolysakkaridirokote, konjugoitu (15‑valenttinen, adsorboitu)
Lisäseuranta
▼ Tähän lääkevalmisteeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Voit auttaa ilmoittamalla kaikista sinun tai lapsesi mahdollisesti saamista haittavaikutuksista. Ks. kohdan Mahdolliset haittavaikutukset lopusta, miten haittavaikutuksista ilmoitetaan.
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin sinulle tai lapsellesi annetaan tämä rokote, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
- Tämä rokote on määrätty vain sinulle tai lapsellesi eikä sitä pidä antaa muiden käyttöön.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä Vaxneuvance on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin sinä tai lapsesi saatte Vaxneuvance-rokotteen
- Miten Vaxneuvance annetaan
- Mahdolliset haittavaikutukset
- Vaxneuvance-rokotteen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Vaxneuvance on pneumokokkirokote, jota annetaan
- vähintään 6 viikon ja alle 18 vuoden ikäisille lapsille antamaan suojaa sairauksia, kuten keuhkotulehdusta (keuhkokuumetta), aivoja ja selkäydintä peittävien kalvojen tulehdusta (aivokalvotulehdusta eli meningiittiä), veressä ilmenevää vaikeaa infektiota (bakteremiaa) ja korvatulehdusta (äkillistä välikorvatulehdusta), vastaan,
- vähintään 18‑vuotiaille henkilöille antamaan suojaa sairauksia, kuten keuhkotulehdusta (keuhkokuumetta), aivoja ja selkäydintä peittävien kalvojen tulehdusta (aivokalvotulehdusta eli meningiittiä) ja veressä ilmenevää vaikeaa infektiota (bakteremiaa), vastaan, kun sairauksien aiheuttajina ovat Streptococcus pneumoniae ‑bakteerin eli pneumokokin 15 eri tyyppiä.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
2. Mitä sinun on tiedettävä, ennen kuin sinä tai lapsesi saatte Vaxneuvance-rokotteen
Sinulle tai lapsellesi ei saa antaa Vaxneuvance-rokotetta
- jos olet tai lapsesi on allerginen vaikuttaville aineille tai tämän rokotteen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa) tai jollekin rokotteelle, joka sisältää kurkkumätätoksoidia.
Varoitukset ja varotoimet
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin sinulle tai lapsellesi annetaan Vaxneuvance-rokote:
- jos sinun tai lapsesi immuunijärjestelmä on heikentynyt (eli elimistön kyky torjua infektioita on tavallista huonompi) tai sinä tai lapsesi otatte eräitä lääkkeitä, jotka saattavat heikentää immuunijärjestelmää (esimerkiksi immuunisalpaajia tai steroideja)
- sinulla tai lapsellasi on korkea kuume tai vaikea infektio. Tällöin rokotusta on mahdollisesti lykättävä sinun tai lapsesi toipumiseen asti. Pelkkä lievä kuume tai infektio (esimerkiksi nuhakuume) ei kuitenkaan edellytä rokotuksen lykkäämistä.
- jos sinulla tai lapsellasi on jokin verenvuotohäiriö tai sinä tai lapsesi saatte helposti mustelmia tai käytätte veritulppien ehkäisyyn tarkoitettuja lääkkeitä.
Jos lapsesi on vauvaikäinen, kerro myös lääkärille, jos lapsi on syntynyt ennenaikaisesti (jos hän on keskonen).
Muiden rokotteiden tavoin Vaxneuvance-rokotekaan ei välttämättä anna täydellistä suojaa kaikille rokotetuille henkilöille.
Muut lääkevalmisteet/rokotteet ja Vaxneuvance
Lapsellesi voidaan antaa Vaxneuvance-rokote samanaikaisesti muiden tavanomaisten lapsuusiässä annettavien rokotteiden kanssa.
Aikuisilla Vaxneuvance voidaan antaa samanaikaisesti inaktivoidun influenssarokotteen kanssa.
Kerro lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle:
- jos sinä tai lapsesi parhaillaan otatte, olette äskettäin ottaneet tai saatatte ottaa reseptilääkkeitä (esimerkiksi immuunisalpaajia tai steroideja, jotka saattavat heikentää immuunijärjestelmää) tai lääkkeitä, joita saa ilman reseptiä
- jos sinä tai lapsesi olette äskettäin ottaneet tai aiotte ottaa jonkin muun rokotteen.
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä, apteekista tai sairaanhoitajalta neuvoa ennen kuin saat tämän rokotteen.
Ajaminen ja koneiden käyttö
Vaxneuvance-rokotteella ei ole haitallista vaikutusta ajokykyyn ja koneidenkäyttökykyyn. Jotkin kohdassa Mahdolliset haittavaikutukset ”Mahdolliset haittavaikutukset” mainitut vaikutukset saattavat kuitenkin tilapäisesti vaikuttaa kykyyn ajaa tai käyttää koneita.
Vaxneuvance sisältää natriumia ja polysorbaatti 20:tä
Tämä lääkevalmiste sisältää natriumia alle 1 mmol (23 mg) per annos eli sen voidaan sanoa olevan ”natriumiton”.
Tämä lääkevalmiste sisältää 1 mg polysorbaatti 20:tä per 0,5 ml:n annos. Polysorbaatit saattavat aiheuttaa allergisia reaktioita. Jos sinulla tai lapsellasi on allergioita, kerro asiasta lääkärille.
Miten valmistetta käytetään
Kerro lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle, jos sinä tai lapsesi olette saaneet aiemmin pneumokokkirokotteen.
Lääkäri tai sairaanhoitaja antaa rokotteen sinulle käsivarren lihakseen tai lapsellesi käsivarren tai jalan lihakseen.
Vähintään 6 viikon ja alle 2 vuoden ikäiset vauvat ja lapset
Lapsellesi annetaan perusrokotuksena kaksi rokotepistosta ja niiden jälkeen tehosteannos.
- Ensimmäinen pistos voidaan antaa jo 6 viikon iässä.
- Toinen pistos annetaan 2 kuukauden kuluttua.
- Kolmas pistos (tehosteannos) annetaan 11–15 kuukauden iässä.
Sinulle kerrotaan, milloin lapsesi pitää tulla ottamaan kukin pistos.
Maassasi noudatettavien virallisten suositusten mukaan terveydenhuollon ammattilaisilla saattaa olla käytössä vaihtoehtoinen rokotusohjelma, jossa annetaan kolme pistosta ja niiden jälkeen tehosteannos. Lisätietoja saat lääkäriltä, apteekkihenkilökunnalta tai sairaanhoitajalta.
Keskoset (ennen 37. raskausviikkoa syntyneet)
Lapsellesi annetaan perusrokotuksena kolme rokotepistosta ja niiden jälkeen tehosteannos.
- Ensimmäinen pistos voidaan antaa jo 6 viikon iässä.
- Toinen ja kolmas pistos annetaan tämän jälkeen niin, että annosten antamisen välillä on 4–8 viikkoa.
- Neljäs pistos (tehosteannos) annetaan 11–15 kuukauden iässä.
Vauvat, lapset ja nuoret, joiden rokotusohjelma aloitetaan vähintään 7 kuukauden iässä
Vähintään 7 kuukauden ja alle 12 kuukauden ikäisille vauvoille annetaan yhteensä kolme pistosta. Toinen pistos annetaan aikaisintaan 1 kuukauden kuluttua ensimmäisestä pistoksesta. Kolmas pistos (tehosteannos) annetaan yli 12 kuukauden iässä ja vähintään 2 kuukauden kuluttua toisen pistoksen antamisesta.
12 kuukauden – alle 2 vuoden ikäisille lapsille annetaan yhteensä kaksi pistosta. Toinen pistos annetaan aikaisintaan 2 kuukautta ensimmäisen pistoksen jälkeen.
Vähintään 2- ja alle 18‑vuotiaille lapsille ja nuorille annetaan yksi pistos.
Aikuiset
Aikuisille annetaan yksi pistos.
Erityisryhmät
Henkilöille, joilla on vähintään yksi pneumokokkitaudin riskiä suurentava perussairaus (esimerkiksi sirppisolutautia sairastaville, ihmisen immuunikatovirus[HIV]-positiivisille tai kantasolusiirteen saaneille henkilöille), voidaan antaa yksi tai useampia pistoksia Vaxneuvance-rokotetta.
Jos sinulla on kysymyksiä Vaxneuvance-rokotteen käytöstä, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki rokotteet, Vaxneuvance-rokotekin voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Hakeudu välittömästi lääkärin hoitoon, jos sinulla tai lapsellasi ilmenee allergisen reaktion oireita, joita saattavat olla
- hengityksen vinkuminen tai hengitysvaikeudet
- kasvojen, huulten tai kielen turvotus
- nokkosihottuma
- ihottuma.
Vaxneuvance-rokotteen käytön jälkeen vauvoilla, lapsilla ja nuorilla voi ilmetä seuraavia haittavaikutuksia:
Hyvin yleiset (voivat ilmetä yli 1 henkilöllä kymmenestä):
- kuume (ruumiinlämpö vähintään 38 °C; 6 viikon – alle 2 vuoden ikäisillä)
- ärtyneisyys (6 viikon – alle 2 vuoden ikäisillä)
- uneliaisuus (6 viikon – alle 2 vuoden ikäisillä)
- kipu, punoitus tai turvotus pistoskohdassa
- ruokahalun väheneminen (6 viikon – alle 2 vuoden ikäisillä)
- kovettuma pistoskohdassa (6 viikon – alle 2 vuoden ikäisillä)
- lihassäryt (2 vuoden – alle 18 vuoden ikäisillä)
- väsymys (2 vuoden – alle 18 vuoden ikäisillä)
- päänsärky (2 vuoden – alle 18 vuoden ikäisillä).
Yleiset (voivat ilmetä enintään 1 henkilöllä kymmenestä):
- kovettuma pistoskohdassa (2 vuoden – alle 18 vuoden ikäisillä)
- nokkosihottuma
- kuume (ruumiinlämpö vähintään 38 °C; 2 vuoden – alle 18 vuoden ikäisillä)
- oksentelu (6 viikon – alle 2 vuoden ikäisillä)
- ihottuma (6 viikon – alle 2 vuoden ikäisillä)
- ärtyneisyys (2 vuoden – alle 18 vuoden ikäisillä)
- uneliaisuus (2 vuoden – alle 18 vuoden ikäisillä)
- ruokahalun väheneminen (2 vuoden – alle 18 vuoden ikäisillä)
- pistoskohdan mustelma
- pahoinvointi (2 vuoden – alle 18 vuoden ikäisillä).
Melko harvinaiset (voivat ilmetä enintään 1 henkilöllä sadasta):
- oksentelu (2 vuoden – alle 18 vuoden ikäisillä).
Tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin):
- ihottuma (2 vuoden – alle 18 vuoden ikäisillä).
Vaxneuvance-rokotteen käytön jälkeen aikuisilla voi ilmetä seuraavia haittavaikutuksia:
Hyvin yleiset (voivat ilmetä yli 1 henkilöllä kymmenestä):
- kipu, turvotus tai punoitus pistoskohdassa
- väsymys
- lihassäryt
- päänsärky
- nivelkipu (18–49-vuotiailla).
Yleiset (voivat ilmetä enintään 1 henkilöllä kymmenestä):
- nivelkipu (vähintään 50-vuotiailla)
- pahoinvointi (18–49‑vuotiailla)
- kuume (18–49‑vuotiailla)
- pistoskohdan kutina
- heitehuimaus (18–49‑vuotiailla)
- vilunväristykset (18–49‑vuotiailla).
Melko harvinaiset (voivat ilmetä enintään 1 henkilöllä sadasta):
- kuume (vähintään 50‑vuotiailla)
- pistoskohdan kuumotus
- pistoskohdan mustelma
- heitehuimaus (vähintään 50‑vuotiailla)
- pahoinvointi (vähintään 50‑vuotiailla)
- oksentelu
- vilunväristykset (vähintään 50‑vuotiailla)
- ihottuma.
Harvinaiset (voivat ilmetä enintään 1 henkilöllä tuhannesta):
- allerginen reaktio, kuten nokkosihottuma, kielen turvotus, ohimenevä kasvojen punoitus tai kuristava tunne kurkussa.
Nämä haittavaikutukset ovat yleensä lieviä ja lyhytkestoisia.
Haittavaikutuksista ilmoittaminen
Jos havaitset itselläsi tai lapsellasi haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www‐sivusto: www.fimea.fi
Lääkealan turvallisuus‐ ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä rokotetta kotelossa ja ruiskun etiketissä mainitun viimeisen käyttöpäivämäärän (Käyt. viim. tai EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä jääkaapissa (2 °C – 8 °C). Ei saa jäätyä. Pidä esitäytetty ruisku ulkopakkauksessa. Herkkä valolle.
Vaxneuvance on annettava mahdollisimman pian jääkaapista ottamisen jälkeen. Jos Vaxneuvance-rokotetta kuitenkin tilapäisesti säilytetään jääkaapin ulkopuolella, se säilyy korkeintaan 25 C:n lämpötilassa 48 tunnin ajan.
Pakkauksen sisältö ja muuta tietoa
Mitä Vaxneuvance sisältää
Vaikuttavat aineet ovat
- bakteeriperäisiä sokereita pneumokokkityypeistä 1, 3, 4, 5, 6A, 7F, 9V, 14, 18C, 19A, 19F, 22F, 23F ja 33F (2,0 mikrogrammaa kustakin tyypistä)
- bakteeriperäistä sokeria pneumokokkityypistä 6B (4,0 mikrogrammaa).
Kaikki bakteeriperäiset sokerit on liitetty kantajaproteiiniin (CRM197). Bakteeriperäiset sokerit ja kantajaproteiini eivät ole eläviä eivätkä aiheuta tautia.
Yksi annos (0,5 ml) sisältää noin 30 mikrogrammaa kantajaproteiinia, joka on adsorboitu alumiinifosfaattiin (125 mikrogrammaa alumiinia [Al3+]). Rokote sisältää adjuvanttina alumiinifosfaattia. Rokotteisiin sisällytetään adjuvantteja rokotteiden aikaansaamien immuunivasteiden parantamiseksi.
Muut aineet ovat natriumkloridi (NaCl), L‑histidiini, polysorbaatti 20 ja injektionesteisiin käytettävä vesi.
Lääkevalmisteen kuvaus ja pakkauskoko (-koot)
Vaxneuvance on opaalinhohtoinen injektioneste, suspensio, joka on esitäytetyssä kerta-annosruiskussa (0,5 ml). Vaxneuvance-rokotetta on saatavilla 1 kappaleen ja 10 kappaleen pakkauksissa joko ilman neuloja tai niin, että jokaisen ruiskun mukana on 1 erillinen neula tai 2 erillistä neulaa.
Vaxneuvance-rokotetta on saatavilla myös kerrannaispakkauksissa, joissa on 5 koteloa, joista jokainen sisältää 10 esitäytettyä ruiskua ilman neuloja.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija ja valmistaja
Merck Sharp & Dohme B.V.
Waarderweg 39
2031 BN Haarlem
Alankomaat
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
MSD Finland Oy
Puh: +358 (0)9 804 650
info@msd.fi
Tämä pakkausseloste on tarkistettu viimeksi 12/2025.
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla http://www.ema.europa.eu.
Ohjeet terveydenhuollon ammattilaiselle
Seuraavat tiedot on tarkoitettu vain terveydenhuollon ammattilaisille:
Vaxneuvance-rokotetta ei saa antaa verisuoneen.
- Vaxneuvance saattaa ennen ravistamista näyttää kirkkaalta nesteeltä, jossa on sakkaa.
- Juuri ennen käyttöä (ja ennen neulan kiinnittämistä ja ilman poistamista ruiskusta) pidä esitäytettyä ruiskua vaakatasossa ja ravista sitä voimakkaasti, jotta muodostuu opaalinhohtoinen suspensio. Saatetaan tarvita useita yrityksiä, ennen kuin rokote on täysin suspendoitunut uudelleen. Älä käytä rokotetta, jos se ei suspendoidu uudelleen.
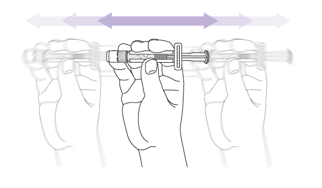
- Tarkasta suspensio silmämääräisesti hiukkasten ja värimuutosten varalta ennen antoa. Hävitä rokote, jos siinä näkyy hiukkasia voimakkaan ravistamisen jälkeen tai siinä on värimuutoksia.
- Kiinnitä ruiskuun neula, jossa on Luer-Lok-liitin, kiertämällä neulaa myötäpäivään, kunnes se on tiukasti kiinni ruiskussa.
- Anna pistos välittömästi lihakseen, mieluiten imeväisillä reiden anterolateraaliseen osaan ja lapsilla ja aikuisilla hartialihaksen alueelle olkavarteen.
- Toimi huolellisesti, jotta vältyt neulanpistotapaturmilta ja niiden aiheuttamilta haitoilta.
Saatavilla ei ole tietoja valmisteen annosta ihon sisään.
Vaxneuvance-rokotetta ei saa sekoittaa samassa ruiskussa muiden rokotteiden kanssa.
Vaxneuvance voidaan antaa samanaikaisesti muiden tavanomaisten lapsuusiässä annettavien rokotteiden kanssa.
Vaxneuvance voidaan antaa samanaikaisesti tetravalentin kausi-influenssarokotteen (virusfragmentit, inaktivoitu) kanssa aikuisille. Injektoitavat rokotteet on aina annettava eri pistoskohtiin.
Säilytä jääkaapissa (2 °C – 8 °C). Ei saa jäätyä.
Pidä esitäytetty ruisku ulkopakkauksessa. Herkkä valolle.
Vaxneuvance on annettava mahdollisimman pian jääkaapista ottamisen jälkeen.
Jos ohjeen mukaisesta säilytyslämpötilasta poiketaan tilapäisesti, säilyvyystiedot viittaavat siihen, että Vaxneuvance säilyy korkeintaan 25 C:n lämpötilassa 48 tunnin ajan.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.