VENTOLINE EVOHALER inhalationsspray, suspension 0,1 mg/dos
Tilläggsinformation
Ventoline Evohaler 0,1 mg/dos inhalationsspray, suspension
salbutamolsulfat
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad Ventoline Evohaler är och vad det används för
- Vad du behöver veta innan du använder Ventoline Evohaler
- Hur du använder Ventoline Evohaler
- Eventuella biverkningar
- Hur Ventoline Evohaler ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Det aktiva innehållsämnet i Ventoline Evohaler, salbutamol, minskar muskelspänningen i luftrörens väggar och vidgar dem, vilket gör att andningen underlättas.
Ventoline Evohaler är avsett för behandling av akuta astmaanfall och andra luftvägssjukdomar samt för förebyggande av belastningsastma.
Ventoline Evohaler är avsett för vuxna, ungdomar och över 4 år. Barn under 4 år enligt läkarordination.
Vad du behöver veta innan produkten används
Använd inte Ventoline Evohaler
- om du är allergisk mot salbutamol eller den drivgas som ingår i preparatet (se avsnitt Förpackningens innehåll och övriga upplysningar).
Varningar och försiktighet
Tala med läkare innan du använder Ventoline Evohaler om du
- har eller har haft hjärtsjukdom, arytmi eller bröstsmärta eller
- konstaterats ha ökad sköldkörtelfunktion (hypertyreos) eller låga kaliumvärden i blodet.
Om dina astmabesvär tilltar eller effekten av Ventoline försämras, kontakta läkare utan dröjsmål.
Din inhalator innehåller tillräckligt med salbutamol för att räcka till 200 puffar (oavsett om de inhaleras och/eller släpps ut i luften för testning) och den innehåller en drivgas för att leverera läkemedlet. Efter 200 puffar kan dock inhalatorn fortsätta spraya drivgas, men utan den rätta dosen salbutamol, så du kan inte vara säker på att du får läkemedel efter 200 puffar. Inhalatorn har ingen dosräknare. Metoder för att avgöra om inhalatorn är tom, såsom att skaka den, väga den eller låta den flyta i vatten, är inte tillförlitliga och rekommenderas inte. Fall av allvarlig försämring av astmasymtom efter oavsiktlig användning av tomma inhalatorer har rapporterats. Du kan överväga att anteckna antalet puffar som används. Det rekommenderas att du har en reservinhalator tillgänglig. Om du använder mer än en inhalator rekommenderas det att hålla reda på antalet puffar för varje inhalator separat.
Andra läkemedel och Ventoline Evohaler
Tala om för läkare eller apotekspersonal om du använder, nyligen har använt eller kan tänkas använda andra läkemedel.
Samtidig användning av vissa andra läkemedel kan påverka effekten av din behandling med Ventoline Evohaler. Tala därför med läkare innan du tar något annat läkemedel samtidigt med Ventoline.
Vissa blodtryckssänkande medel (betablockerare) kan försämra effekten av Ventoline Evohaler.
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare innan du använder detta läkemedel.
Det är sannolikt att salbutamol går över i modersmjölk. Rådfråga därför läkare innan du ammar ditt barn i samband med behandling med Ventoline Evohaler.
Körförmåga och användning av maskiner
Ventoline Evohaler inverkar varken på din prestationsförmåga i trafiken eller på din förmåga att använda maskiner.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Ventoline Evohaler används vanligen som symtomatisk behandling och inte som kontinuerlig, daglig medicinering.
Dosering för vuxna och för barn är 1– 2 inhalationsdoser vid behov högst fyra gånger om dagen. Åt barn under skolåldern rekommenderas användning av andningsbehållare (Babyhaler eller Volumatic) enligt läkarordination.
Din individuella dosering bestäms ändå av läkare, som avpassar den särskilt för dig. Följ alltid läkarens doseringsanvisningar. Överskrid inte ordinerad dosering. Konsultera alltid läkare innan dosen eller doseringsfrekvensen ändras. Fråga läkare eller apotekspersonal om du är osäker på vilken dos du ska ta.
Ventoline Evohaler ska användas inte regelbundet utan vid behov.
Om din astma är aktiv (om du exempelvis ofta har astmaanfall eller symtom, t.ex. andfåddhet som gör det svårt att tala, äta eller sova, hosta, väsande andning, trånghet i bröstet eller begränsning av fysisk aktivitet), ska du omedelbart tala om det för din läkare, som kan sätta in eller öka dosen av exempelvis inhalerade kortikosterioder för att kontrollera din astma.
Effekten av Ventoline Evohaler varar i regel i 4–6 timmar. Om läkaren ordinerat mer än en inhalation per doseringstillfälle, vänta 30 sekunder mellan varje inhalation.
Sök omedelbart medicinsk rådgivning om ditt läkemedel inte verkar fungera lika bra som förut (om du exempelvis behöver högre dos för att lindra andningsbesvär eller det inhalerade läkemedlet inte ger snabb lindring i minst 3 timmar efter administrering) eftersom din astma kan vara på väg att försämras och du kan behöva ett annat läkemedel.
Tala om för din läkare om din astma blir värre eller om denna medicin inte ger lika mycket lindring för din astma som tidigare.
Om du använder Ventoline Evohaler oftare än två gånger i veckan för att behandla astmasymtom, bortsett från förebyggande behandling före ansträngning, tyder det på dåligt kontrollerad astma, vilket kan öka risken för svåra astmaanfall (förvärrad astma) som kan ha allvarliga följder och kan vara livshotande eller t.o.m. dödliga. Du bör kontakta din läkare så snart som möjligt för översyn av din astmabehandling.
Om du dagligen använder ett läkemedel mot inflammation i lungorna, t.ex. inhalerade kortikosteroider, är det viktigt att du fortsätter att använda det regelbundet, även om du mår bättre.
Detta läkemedel är avsett att användas endast som inhalation. En korrekt inhalationsteknik är viktig för att bästa möjliga effekt skall kunna uppnås. Vid inandning rekommenderas användning av andningsbehållare (Babyhaler eller Volumatic), speciellt hos barn. Bruksanvisning för denna inhalationsspray finns nedan.
Om du upplever att effekten av Ventoline Evohaler är för stark eller för svag vänd dig till läkare eller apotekspersonal.
Bruksanvisning
Innan du använder inhalationssprayen
Innan du använder inhalationssprayen för första gången, ta av skyddshuven genom att lätt trycka på båda sidorna, skaka den väl och kontrollera att sprayen fungerar genom att spraya två gånger i luften. Om sprayen inte har använts under fem dagar eller mera, skaka den väl och spraya två doser i luften.
Inhalatorn har ingen dosräknare, du kan överväga att anteckna antalet puffar du tar. Om du använder mer än en inhalator rekommenderas det att hålla reda på antalet puffar för varje inhalator separat.
1. Ta av skyddshuven genom att lätt trycka på båda sidorna.

2. Kontrollera att inhalationssprayen är rent på in- och utsidan, inklusive munstycket och se till att det är fritt från lösa främmande föremål.
3. Skaka inhalationssprayen väl för att garantera att den är fri från främmande föremål och att inhalationssprayens innehåll blandas jämnt.

4. Håll inhalatorn upprätt mellan tummen och pekfingret, med tummen under munstycket.

5. Andas ut så långt som känns bekvämt. Sätt inhalatorn i munnen mellan tänderna. Slut läpparna om munstycket. Bit inte i munstycket.
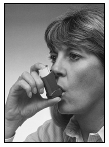
6. Andas in genom munnen. Just när du börjar andas in, tryck ned toppen på metallbehållaren. Fortsätt att andas in lugnt och så djupt som möjligt.

7. Håll andan, tag bort inhalatorn från munnen och fingret från toppen av metallbehållaren. Fortsätt att hålla andan så länge som det känns bekvämt.

8. Om du ska ta ytterligare en dos, håll inhalatorn upprätt och vänta ungefär 30 sekunder innan behandlingen upprepas från punkt 3–7.
9. Sätt tillbaka skyddshuven. Ett knäpp hörs när skyddshuven trycks på plats.
VIKTIGT
Skynda inte genom punkterna 5, 6 och 7. Det är viktigt att du påbörjar andas in så långsamt som möjligt före användningen av inhalatorn.
Kontrollera tekniken framför en spegel de första gångerna. Om det pyser från övre delen av sprayen eller ut genom sidorna av munnen, börja igen från punkt 2.
Då Ventoline Evohaler ges till barn fordras ofta översyn av vuxen för att garantera att inhalationen utförs korrekt. Andningsbehållare, såsom Babyhaler och Volumatic, rekommenderas speciellt för barn om intagningen av läkemedlet annars är besvärligt. Användning av andningsbehållare underlättar doseringen av läkemedlet. Bruksanvisning finns i andningsbehållarens bipacksedel.
Rengöring
Rengör inhalatorn minst en gång i veckan.
- Ta bort metallbehållaren från plastinhalatorn och ta av skyddshuven.
- Skölj plastinhalatorn väl med varmt rinnande vatten.
- Torka av VÄL in- och utsidan av plastinhalatorn.
- Sätt tillbaka behållaren och skyddshuven.
LÄGG INTE METALLBEHÅLLAREN I VATTEN.
Om du har tagit för stor mängd av Ventoline Evohaler
Om du fått i dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedel av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel. 0800 147 111 ) för bedömning av risken samt rådgivning.
Om du har ytterligare frågor om detta läkemedel kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
I samband med normal användning framkallar Ventoline Evohaler i allmänhet inga biverkningar.
Kontakta läkare omedelbart och sluta använda detta läkemedel, om du får följande symtom:
- om din andning försvåras eller börjar väsa/pipa genast efter att du tagit läkemedlet (paradoxal bronkospasm). Om du har tillgång till ett annat snabbverkande läkemedel för astma ska du pröva det så fort som möjligt.
- om du får överkänslighetsreaktioner såsom svullnad i ögonen, ansiktet, läpparna och svalget, hudutslag, sammandragningar i luftrören, lågt blodtryck och svimning.
Vanliga biverkningar (hos mer än 1 patient av hundra):
- skakning, huvudvärk
- ökad hjärtfrekvens.
Mindre vanliga biverkningar (hos färre än 1 patient av hundra):
- hjärtklappning
- irritation i munnen och halsen
- muskelspasmer.
Sällsynta biverkningar hos färre än 1 patient av tusen):
- lågt kaliumvärde i blodet
- utvidgning av perifera blodkärl.
Mycket sällsynta biverkningar (hos färre än 1 patient av tiotusen):
- överkänslighetsreaktioner såsom svullnad i ögonen, ansiktet, läpparna och svalget, hudutslag, sammandragningar i luftrören, lågt blodtryck och svimning
- hyperaktivitet
- hjärtrytmstörningar
- pipande andning efter intagandet av läkemedlet (s.k. paradoxal bronkospasm).
Okänd (upgifterna är tagna från biverkningsrapporter som givits under klinisk användning varför frekvensen inte kan beräknas):
- bröstsmärta.
Tala om för läkare, om du har dessa symtom när du tar salbutamol. Sluta ändå inte att ta läkemedlet utan att rådgöra med läkare.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
- Sätt tillbaka skyddshuven genast efter att du använt inhalatorn. Ett knäpp hörs när skyddshuven trycks på plats.
- Förvaras vid högst 30 °C, i skydd mot direkt solljus. Får ej frysas.
- Risk för försämrad funktion och effekt om inhalationssprayen är kall.
- Används före utgångsdatum som anges på förpackningen. Utgångsdatumet är den sista dagen i angiven månad.
- Behållaren innehåller tryckvätska. Utsätt inte för temperaturer över 50 °C. Punktera, bryt eller bränn aldrig metallbehållaren även om den är tom.
Förvara detta läkemedel utom syn- och räckhåll för barn.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är salbutamolsulfat. En dos innehåller en mängd som motsvarar 0,1 mg salbutamol.
- Övrigt innehållsämne är norfluran. Norfluran är en drivgas utan negativ inverkan på ozonsiktet.
- Detta läkemedel innehåller fluorerade växthusgaser. Varje inhalator innehåller 18 g HFC-134a (även kallad norfluran), motsvarande 0,0257 ton CO2 (global warming potential GWP = 1 430).
Läkemedlets utseende och förpackningsstorlek
Ventoline Evohaler är förpackad i en metallbehållare med 200 läkemedelsdoser. Metallbehållaren är förpackad i en blågrå plastinhalator. Inhalatorns munstycke täcks av en blå skyddshuv.
Innehavare av godkännande för försäljning och tillverkare
Innehavare av godkännande för försäljning
GlaxoSmithKline Oy
Porkalagatan 20 A
00180 Helsingfors
tfn. 010 303 030
Tillverkare
Glaxo Wellcome Production, Evreux, Frankrike eller
Glaxo Wellcome S.A., Aranda de Duero, Spanien
Denna bipacksedel ändrades senast 9.12.2025
© GlaxoSmithKline Oy 2025