HAVRIX injektionsvätska, suspension i förfylld spruta 1440 ELISA U/ml
Tilläggsinformation
Havrix 720 ELISA U, injektionsvätska, suspension, förfylld spruta
Hepatit A- (inaktiverat) vaccin (adsorberat)
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du eller ditt barn får detta vaccin. Den innehåller information som är viktig för dig/ditt barn.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor, vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Detta vaccin har ordinerats enbart åt dig eller ditt barn. Ge det inte till andra.
- Om du eller ditt barn får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
Denna bipacksedel har skrivit under antagandet att den person som får vaccinet läser bipacksedeln, men men det kan ges till barn och ungdomar så du kan behöva läsa den för ditt barn.
I denna bipacksedel finns information om följande
1. Vad Havrix 720 är och vad det används för
2. Vad du behöver veta innan du får Havrix 720
3. Hur du får Havrix 720
4. Eventuella biverkningar
5. Hur Havrix 720 ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Vad Havrix 720 används för
Havrix 720 är ett vaccin som används för att skydda barn och ungdomar i åldern 1 till och med 15 år mot infektioner orsakade av hepatit A-virus.
Havrix 720 kan även ges till ungdomar i åldern 16 till och med 18 år, vid behov.
Vad hepatit A är
- Hepatit A är en leversjukdom som orsakas av hepatit A-virus.
- Hepatit A-virus kan överföras från person till person, eller via förorenade livsmedel t.ex. vatten, mat och dryck.
- Symtom på hepatit A varierar från lindriga till svåra och kan vara feber, sjukdomskänsla, aptitlöshet, diarré, illamående, magbesvär, mörkfärgad urin och gulsot (gulfärgning av ögon och hud). De flesta blir helt återställda men sjukdomen kan ibland vara så allvarlig att man behöver läggas in på sjukhus och den kan i sällsynta fall leda till akut leversvikt.
Vad Havrix 720 används för
- Havrix 720 hjälper kroppen att tillverka sitt eget skydd (antikroppar) mot viruset. Antikropparna bidrar till att skydda dig mot sjukdomen.
- Som med alla vacciner kan det hända att Havrix 720 inte ger fullständigt skydd till alla personer som vaccineras.
Vad du behöver veta innan produkten används
Du ska inte få Havrix 720 om:
- du är allergisk mot den aktiva substansen eller något annat innehållsämne i detta vaccin (anges i avsnitt Förpackningens innehåll och övriga upplysningar) eller mot neomycin eller formaldehyd
- du tidigare har fått en allergisk reaktion mot hepatit A-vaccin.
Tecken på en allergisk reaktion kan vara kliande hudutslag, andnöd och svullnad av ansikte eller tunga.
Havrix 720 ska inte ges om något av det ovanstående gäller. Om du är osäker, tala med läkare, apotekspersonal eller sjuksköterska innan du får Havrix 720.
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du får Havrix 720 om:
- du har en allvarlig infektion med hög feber. Du kan vaccineras senare när du är frisk igen. En lättare infektion, t.ex. förkylning, bör inte vara något problem men tala först med läkaren.
- du har dåligt immunförsvar på grund av sjukdom och/eller läkemedelsbehandling. Läkaren avgör om du måste få fler injektioner
- du har en blödningssjukdom eller får lätt blåmärken.
Svimning kan förekomma före eller efter en injektion med nålstick. Tala därför om för läkaren, apotekspersonalen eller sjuksköterskan om du har svimmat när du fått en injektion tidigare.
Andra läkemedel och Havrix 720
Tala om för läkare, apotekspersonal eller sjuksköterska om du tar, nyligen har tagit eller kan tänkas ta andra vacciner eller läkemedel.
Havrix 720 kan ges samtidigt med andra vaccin och immunglobuliner. Olika injektionsställen ska användas för varje injektion.
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare, apotekspersonal eller sjuksköterska innan du får Havrix 720.
Körförmåga och användning av maskiner
Havrix 720 har ingen eller försumbar påverkan på förmågan att köra bil och använda maskiner.
Havrix 720 innehåller fenylalanin, polysorbat 20, natrium och kalium
Detta vaccin innehåller 0,083 mg fenylalanin per dos.
Fenylalanin kan vara skadligt om du har fenylketonuri (PKU), en sällsynt ärftlig sjukdom som gör att fenylalanin ansamlas i höga halter eftersom kroppen inte kan bryta ner det ordentligt.
Detta vaccin innehåller 0,025 mg polysorbat 20 per dos. Polysorbater kan orsaka allergiska reaktioner. Tala om för din läkare om du har några kända allergier.
Detta vaccin innehåller mindre än 1 mmol (23 mg) natrium per dos, d.v.s är näst intill ”natriumfritt”.
Detta vaccin innehåller mindre än 1 mmol (39 mg) kalium per dos, d.v.s. är näst intill ”kaliumfritt”.
Hur produkten används
Hur du får vaccinet
- Läkaren eller sjuksköterskan ger Havrix 720 som injektion i en muskel. Till barn och ungdomar används oftast överarmen.
- Till små barn kan injektionen ges i lårmuskeln.
- I undantagsfall kan Havrix 720 ges under huden om du har trombocytopeni eller någon allvarlig blödningssjukdom.
Hur mycket vaccin du får
- Du får en dos Havrix 720 (0,5 ml suspension) på en dag som du och läkaren eller sjuksköterskan kommer övereens om.
- Ytterligare en dos (boosterdos) rekommenderas 6 till 12 månader efter den första dosen, men den kan ges upp till 5 år efter den första dosen för att garantera långtidsskydd.
Om du får för stor mängd av Havrix 720
Det är mycket osannolikt att vaccinet överdoseras eftersom det levereras i en engångsflaska eller engångsspruta och ges av läkare eller sjuksköterska. Ett fåtal fall av oavsiktlig administrering har rapporterats och de rapporterade biverkningarna var samma som de som rapporterats vid normal administrering av vaccinet (anges i avsnitt Eventuella biverkningar).
Om du tror att du har missat en dos av Havrix 720
Kontakta läkaren, som avgör om du behöver få en dos och när du ska få den.
Eventuella biverkningar
Liksom alla läkemedel kan detta vaccin orsaka biverkningar, men alla som vaccineras behöver inte få dem.
Allvarliga biverkningar
Tala omedelbart om för läkaren om du får någon av följande allvarliga biverkningar. Du kan behöva akut medicinsk behandling:
- Allergiska reaktioner – tecken på detta kan vara hudutslag som är lokalt eller utbrett och kan klia eller ge blåsor, svullnad av ögon och ansikte, svårigheter att andas eller svälja, plötsligt blodtrycksfall och medvetslöshet.
Dessa reaktioner kan visa sig innan du lämnar läkarens klinik.
Tala omedelbart om för läkaren om du får någon av de allvarliga biverkningar som räknas upp ovan.
Under kliniska studier av Havrix 720 har följande biverkningar förekommit:
Mycket vanliga (kan förekomma vid fler än 1 av 10 vaccindoser):
- irritabilitet
- smärta och rodnad på injektionsstället.
Vanliga (kan förekomma vid upp till 1 av 10 vaccindoser):
- aptitlöshet
- huvudvärk
- dåsighet
- illamående
- allmän sjukdomskänsla
- feber på 37,5 °C eller mer
- svullnad på injektionsstället.
Mindre vanliga (kan förekomma vid upp till 1 av 100 vaccindoser):
- täppt eller rinnande näsa
- kräkningar
- diarré
- hudutslag
- förhårdnad vid injektionsstället.
Efter marknadsintroduktionen av Havrix 720 har följande biverkningar förekommit:
- krampanfall eller konvulsioner
- inflammation i blodkärl som ledde till förträngning eller stopp (vaskulit)
- allvarlig allergisk reaktion med svullnad av ansikte, tunga eller svalg, vilket kan leda till svårigheter att svälja eller andas
- nässelutslag, röda och ofta kliande prickar som börjar på armar och ben och ibland även förekommer i ansiktet och övriga kroppen
- ledvärk.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvaras utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på kartongen. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras i kylskåp (2 - 8°C). Får ej frysas.
Förvaras i originalförpackningen. Ljuskänsligt.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
Den aktiva substansen är hepatit A-virus (inaktiverarat) adsorberat på aluminiumhydroxid. Varje dos på 0,5 ml innehåller 720 ELISA-enheter av hepatit A-virus.
Övriga innehållsämnen är: aminosyror för injektion (innehåller fenylalanin), dinatriumfosfat, kaliumdivätefosfat, polysorbat 20 (E432), kaliumklorid, natriumklorid och vatten för injektionsvätskor (se avsnitt Vad du behöver veta innan produkten används).
Läkemedlets utseende och förpackningsstorlekar
Injektionsvätska, suspension i förfylld spruta.
Havrix 720 är en grumlig injicerbar vätska.
Havrix 720 kommer i en förfylld spruta med en dos med eller utan nålar, i förpackningsstorlekarna 1, 5, 10 eller 25.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning och tillverkare
GlaxoSmithKline Biologicals s.a. Rue de l´Institut 89 B-1330 Rixensart Belgien
Ytterligare upplysningar om detta läkemedel erhålls hos den nationella representanten för innehavaren av godkännandet för försäljning.
GlaxoSmithKline Oy
Porkalagatan 20 A
00180 Helsinki
Tfn. +358 10 30 30 30
Detta läkemedel är godkänt inom Europeiska ekonomiska samarbetsområdet under namnen:
| Belgien, Cypern, Luxemburg | Havrix Junior 720 |
| Bulgarien | HAVRIX 720 suspension for injection (Junior monodose) Хаврикс 720 инжекционна суспензия (доза за деца) |
| Danmark, Finland, Island, Norge | Havrix |
| Estland | Havrix, 720 ELISA ühikut/ml süstesuspensioon |
| Frankrike | HAVRIX NOURRISSONS ET ENFANTS 720 U/0,5 ml |
| Grekland, Italien | HAVRIX |
| Irland | Havrix Junior Monodose |
| Lettland | Havrix 720 ELISA vienības/0,5 ml suspensija injekcijām |
| Litauen | Havrix 720 ELISA vienetų/0,5 ml injekcinė suspensija |
| Malta | Havrix Junior Monodose Vaccine |
| Nederländerna | Havrix Junior |
| Polen | HAVRIX 720 JUNIOR |
| Portugal | Havrix 720 Júnior |
| Rumänien | HAVRIX JUNIOR 720 VACCIN HEPATITIC A |
| Slovakien | HAVRIX 720 Junior monodose |
| Slovenien | HAVRIX 720 PAEDIATRIC |
| Spanien | Havrix 720 Junior suspensión inyectable en jeringa precargada |
| Sverige | Havrix 720 ELISA U |
| Tjeckien | Havrix Junior monodose |
| Tyskland | Havrix 720 Kinder |
| Ungern | Havrix 720 Junior |
| Österrike | Havrix (Hepatitis A-Impfstoff) Junior 720 EI.U/0,5 ml |
Denna bipacksedel ändrades senast 08.04.2025
Övriga informationskällor
Ytterligare upplysningar finns att tillgå på Säkerhets- och utvecklingscentret för läkemedelsområdets nätsida:
http://www.fimea.fi
Direktiv för experterna inom hälsovården
Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal:
Följande information är till den som administrerar vaccinet:
Havrix är en grumlig vätska, suspension. Under förvaring kan innehållet uppvisa en tunn vit bottensats med klar, färglös supernatant.
Vaccinet ska inspekteras visuellt med avseende på främmande partiklar och/eller fysikaliska förändringar före administrering.
Före användning av Havrix 720, ska sprutan omskakas väl, så att en nästan ogenomskinlig vit suspension erhålls.
Använd inte vaccinet om det ser ut på annat vis.
Instruktioner för den förfyllda sprutan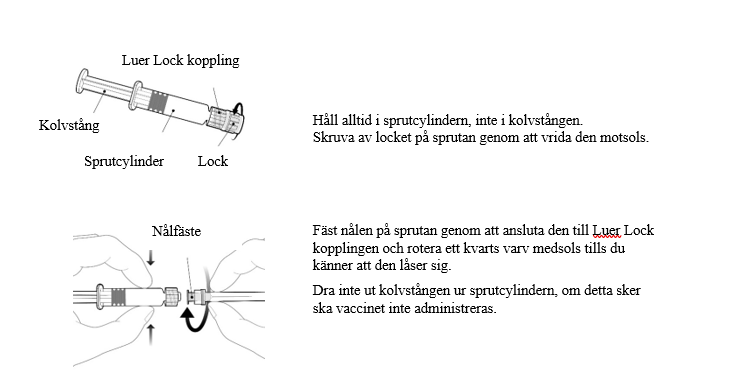
Destruktion
Ej använt vaccin och avfall ska kasseras enligt gällande anvisningar.