LUMIVELA filmdragerad tablett 150/20 mikrog
Tilläggsinformation
Lumivela 150 mikrogram/20 mikrogram filmdragerade tabletter
desogestrel/etinylestradiol
Allmänna direktiv
Viktig information om kombinerade hormonella preventivmedel:
- Kombinerade hormonella preventivmedel är en av de mest pålitliga reversibla preventivmetoder som finns om de används korrekt.
- Risken för en blodpropp i vener eller artärer ökar något, speciellt under det första året eller när kombinerade hormonella preventivmedel börjar användas igen efter ett uppehåll på 4 veckor eller längre.
- Var uppmärksam och kontakta läkare om du tror att du har symtom på en blodpropp (se avsnitt Vad du behöver veta innan produkten används ”Blodproppar”).
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
|
I denna bipacksedel finns information om följande
1. Vad Lumivela är och vad det används för
2. Vad du behöver veta innan du använder Lumivela
3. Hur du använder Lumivela
4. Eventuella biverkningar
5. Hur Lumivela ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Sammansättning och typ av p-piller
Lumivela är ett kombinerat p-piller.
- Var och en av de 21 vita tabletterna innehåller en liten mängd av två olika kvinnliga könshormoner: desogestrel (ett hormon som fungerar på liknande sätt som gulkroppshormon) och etinylestradiol (ett hormon som fungerar på liknande sätt som östrogen). Eftersom Lumivela innehåller hormoner i så små mängder kallas det för ett lågdos‑p‑piller. Eftersom alla vita tabletter i tablettkartan innehåller lika mycket av vartdera hormonet kallas preparatet för ett enfasigt kombinerat p‑piller.
- De 7 gröna tabletterna innehåller inga aktiva substanser och kallas också placebotabletter.
För vilket ändamål används Lumivela
Lumivela används för att förebygga graviditet. När p-pillren används korrekt (man minns att ta alla tabletterna) är sannolikheten för graviditet mycket liten.
Desogestrel och etinylestradiol som finns i Lumivela kan också vara godkända för att behandla andra sjukdomar som inte nämns i denna produktinformation. Fråga läkare, apotek eller annan hälsovårdspersonal om du har ytterligare frågor
Vad du behöver veta innan produkten används
Allmän information Innan du börjar använda Lumivela ska du läsa informationen om blodproppar i avsnitt Vad du behöver veta innan produkten används. Det är särskilt viktigt att du läser symtomen om blodpropp – se avsnitt Vad du behöver veta innan produkten används, ”Blodproppar”). I denna bipacksedel beskrivs ett flertal situationer när du ska sluta använda Lumivela, eller när tillförlitligheten av Lumivela kan vara nedsatt. I sådana situationer ska du inte ha samlag eller också ska du skydda dig med ett preventivmedel som inte innehåller hormoner, t.ex. kondom eller någon annan så kallad barriärmetod. Använd inte säkra perioder eller temperaturmetoder. De kan vara osäkra p.g.a. att Lumivela påverkar de normala förändringarna i temperaturen och slemmet i slidan som sker under menstruationscykeln. I likhet med andra p-piller kommer inte heller Lumivela att skydda dig mot HIV (AIDS) eller någon annan sexuellt överförbar sjukdom. |
Använd inte Lumivela
Använd inte Lumivela om du har något av de tillstånd som anges nedan. Om du har något av dessa tillstånd måste du tala om det för läkaren. Din läkare kommer att diskutera med dig vilken annan typ av preventivmedel som kan vara mer lämpligt. Se också ”Varningar och försiktighet”.
- om du har (eller har haft) en blodpropp i ett blodkärl i benen (djup ventrombos, DVT), i lungorna (lungemboli, PE) eller något annat organ.
- om du vet att du har en sjukdom som påverkar blodkoaguleringen – t.ex. protein C‑brist, protein S‑brist, antitrombin III-brist, Faktor V Leiden eller antifosfolipidantikroppar.
- om du behöver genomgå en operation eller om du blir sängliggande en längre period (se avsnitt ”Blodproppar”).
- om du har haft en hjärtinfarkt eller en stroke (slaganfall).
- om du har (eller har haft) kärlkramp (ett tillstånd som orsakar svår bröstsmärta och kan vara ett första tecken på en hjärtinfarkt) eller transitorisk ischemisk attack (TIA – övergående strokesymtom).
- om du har någon av följande sjukdomar som kan öka risken för en blodpropp i artärerna:
- svår diabetes med skadade blodkärl
- mycket högt blodtryck
- en mycket hög nivå av fett i blodet (kolesterol eller triglycerider)
- ett tillstånd som kallas hyperhomocysteinemi.
- om du har (eller har haft) en typ av migrän som kallas ”migrän med aura”.
- om du har (eller har haft) pankreatit (inflammation i bukspottskörteln) kombinerat med höga nivåer av blodfetter.
- om du har (eller har haft) gulsot (gulfärgning av hud eller ögon) eller en svår leversjukdom och din lever ännu inte fungerar normalt.
- om du har (eller har haft) cancer som påverkas av könshormoner (bröstcancer eller cancer i könsorganen).
- om du har (eller har haft) en tumör i levern.
- om du har underlivsblödningar utan känd orsak.
- om du har onormal svullnad i livmoderslemhinnan.
- om du är allergisk mot något innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
- om du är allergisk mot jordnötter eller soja.
Om du har något av tillstånden som beskrivs ovan eller drabbas av något av dem för första gången medan du använder Lumivela ska du omedelbart sluta ta det och kontakta din läkare så snart som möjligt. Under tiden ska du använda ett preventivmedel som inte innehåller hormoner. Se också ”Allmän information” i början av avsnitt Vad du behöver veta innan produkten används.
Använd inte Lumivela om du har hepatit C och tar läkemedel som innehåller ombitasvir/paritaprevir/ritonavir och dasabuvir, glekaprevir/pibrentasvir eller sofosbuvir/velpatasvir/voxilaprevir (se även avsnitt ”Andra läkemedel och Lumivela”).
Varningar och försiktighet
När ska du kontakta läkare?
Sök omedelbart läkare
- om du märker möjliga tecken på en blodpropp som kan betyda att du har en blodpropp i benet (dvs. djup ventrombos), en blodpropp i lungan (dvs. lungemboli), en hjärtinfarkt eller stroke (se avsnitt ”Blodproppar” nedan).
För en beskrivning av symtomen vid dessa allvarliga biverkningar gå till ”Så här känner du igen en blodpropp”.
Tala om för din läkare om något av följande tillstånd gäller dig.
Om tillståndet uppstår eller försämras när du använder Lumivela, ska du också kontakta din läkare.
- om du röker
- om du har diabetes
- om du är överviktig
- om du har högt blodtryck
- om du har klaffel eller en viss typ av rytmrubbningar
- om du har en inflammation i venerna under huden (ytlig tromboflebit)
- om du har åderbråck
- om någon i din närmaste familj har haft en blodpropp, hjärtinfarkt eller stroke
- om du har haft migrän
- om du har epilepsi
- om du har ökade nivåer av blodfetter (hypertriglyceridemi) eller ärftlighet för detta tillstånd. Hypertriglyceridemi har förknippats med en ökad risk att utveckla pankreatit (bukspottkörtelinflammation)
- om du behöver genomgå en operation eller blir sängliggande en längre period (se "Blodproppar" i avsnitt Vad du behöver veta innan produkten används)
- om du nyss har fött barn löper du ökad risk för blodproppar. Fråga läkare hur snart efter förlossningen du kan börja ta Lumivela.
- om någon i din närmaste familj har haft bröstcancer
- om du har en lever- eller gallblåsesjukdom
- om du har Crohns sjukdom eller ulcerös kolit (kronisk inflammatorisk tarmsjukdom)
- om du har systemisk lupus erythematosus (SLE – en sjukdom som påverkar ditt naturliga immunsystem)
- om du har hemolytiskt uremiskt syndrom (HUS – en störning av blodkoaguleringen som leder till njursvikt)
- om du har sicklecellanemi (en ärftlig sjukdom i de röda blodkropparna)
- om du har ett tillstånd som uppträdde för första gången eller förvärrades under graviditet eller tidigare användning av könshormoner (t.ex. hörselnedsättning, en ämnesomsättningssjukdom som kallas porfyri, en hudsjukdom som orsakar blåsor under graviditet och som kallas herpes gestationis, en neurologisk sjukdom som orsakar plötsliga rörelser och som kallas Sydenhams korea)
- om du har eller har haft kloasma (gulbruna pigmentfläckar på huden, framför allt i ansiktet och på halsen som kallas graviditetsfläckar); i så fall ska du undvika direkt solljus eller ultravioletta strålar
- om du får symtom på angioödem, t.ex. svullnad i ansiktet, tungan och/eller svalget och/eller sväljningssvårigheter eller nässelutslag, eventuellt med andningssvårigheter, kontakta omedelbart läkare. Produkter som innehåller östrogen kan framkalla eller förvärra symtom på ärftligt och förvärvat angioödem.
P‑piller och blodproppar
BLODPROPPAR
Om du använder kombinerade hormonella preventivmedel som Lumivela ökar risken för blodpropp jämfört med om du inte använder dessa preparat. I sällsynta fall kan en blodpropp blockera blodkärlen och orsaka allvarliga problem.
Blodproppar kan bildas
- i vener (kallas venös trombos, venös tromboembolism eller VTE)
- i artärer (kallas arteriell trombos, arteriell tromboembolism eller ATE).
Det går inte alltid att återhämta sig helt efter blodproppar. I sällsynta fall kan de ha allvarliga kvarstående effekter och, i mycket sällsynta fall, vara dödliga.
Det är viktigt att komma ihåg att den totala risken för en farlig blodpropp på grund av Lumivela är liten.
SÅ HÄR KÄNNER DU IGEN EN BLODPROPP
Sök omedelbart läkare om du märker något av följande tecken eller symtom.
| Upplever du något av dessa tecken? | Vad kan du eventuellt lida av? |
| Djup ventrombos |
Om du är osäker, kontakta läkare eftersom vissa av dessa symtom t.ex. hosta och andfåddhet av misstag kan tolkas som ett lättare tillstånd som luftvägsinfektion (t.ex. en vanlig förkylning). | Lungemboli |
Symtom som vanligtvis förekommer i ett öga:
| Retinal ventrombos (blodpropp i ögat) |
| Hjärtinfarkt |
Ibland kan symtomen på stroke vara kortvariga med nästan omedelbar eller fullständig återhämtning, men du ska ändå omedelbart söka läkare eftersom du löper risk att drabbas av en ny stroke. | Stroke |
| Blodproppar som blockerar andra blodkärl |
BLODPROPPAR I EN VEN
Vad kan hända om en blodpropp bildas i en ven?
- Användning av kombinerade hormonella preventivmedel har förknippats med en ökning av risken för blodproppar i en ven (venös trombos). Dessa biverkningar är dock sällsynta. De inträffar oftast under det första årets användning av ett kombinerat hormonellt preventivmedel.
- Om en blodpropp bildas i en ven i benet eller foten kan det leda till en djup ventrombos (DVT).
- Om en blodpropp förflyttar sig från benet och stannar i lungan kan det leda till en lungemboli.
- I mycket sällsynta fall kan en blodpropp bildas i en ven i ett annat organ, som t.ex. ögat (retinal ventrombos).
När är risken för att utveckla en blodpropp i en ven störst?
Risken för att utveckla en blodpropp i en ven är störst under det första året som du för första gången använder kombinerade hormonella preventivmedel. Risken kan också vara högre om du börjar om med ett kombinerat hormonellt preventivmedel (samma produkt eller en annan produkt) efter ett uppehåll på 4 veckor eller längre. Efter det första året minskar risken, men den är alltid något högre än om du inte använder ett kombinerat hormonellt preventivmedel. När du slutar använda Lumivela återgår risken för en blodpropp till det normala inom några veckor.
Hur stor är risken för att utveckla en blodpropp?
Risken beror på din naturliga risk för VTE och vilken typ av kombinerat hormonellt preventivmedel du tar.
Den totala risken för en blodpropp i benet eller lungorna med Lumivela är liten.
- Av 10 000 kvinnor som inte använder ett kombinerat hormonellt preventivmedel och inte är gravida utvecklar cirka 2 en blodpropp under ett år.
- Av 10 000 kvinnor som använder ett kombinerat hormonellt preventivmedel som innehåller levonorgestrel, noretisteron eller norgestimat utvecklar cirka 5–7 en blodpropp under ett år.
- Av 10 000 kvinnor som använder ett kombinerat hormonellt preventivmedel som innehåller desogestrel så som Lumivela utvecklar cirka 9–12 en blodpropp under ett år.
- Risken för blodpropp varierar beroende på din sjukdomshistoria (se ”Faktorer som kan öka risken för en blodpropp” nedan).
| Risk för att utveckla en blodpropp under ett år | |
| Kvinnor som inte använder ett kombinerat hormonellt p‑piller/plåster/ring och som inte är gravida | Cirka 2 av 10 000 kvinnor |
| Kvinnor som använder ett kombinerat hormonellt preventivmedel som innehåller levonorgestrel, noretisteron eller norgestimat | Cirka 5–7 av 10 000 kvinnor |
| Kvinnor som använder Lumivela | Cirka 9–12 av 10 000 kvinnor |
Faktorer som kan öka risken för en blodpropp i en ven
Risken för en blodpropp med Lumivela är liten men vissa tillstånd ökar risken. Risken är högre:
- om du är mycket överviktig (kroppsmasseindex eller BMI över 30 kg/m2)
- om någon nära släkting har haft en blodpropp i ben, lungor eller annat organ vid ung ålder (t.ex. under cirka 50 år). I det här fallet kan du ha en ärftlig blodkoaguleringssjukdom.
- om du behöver genomgå en operation eller blir sängliggande under en längre period på grund av skada eller sjukdom, eller om benet gipsas. Användningen av Lumivela kan behöva avbrytas i flera veckor innan en operation eller medan du är mindre rörlig. Om du måste sluta använda Lumivela, fråga din läkare när du kan börja använda det igen.
- med stigande ålder (särskilt om du är över cirka 35 år)
- om du har fött barn för några veckor sedan.
Risken för att utveckla en blodpropp ökar ju fler tillstånd du har.
Flygresor (> 4 timmar) kan tillfälligt öka risken för en blodpropp, särskilt om du har någon av de andra faktorerna som listas här.
Det är viktigt att du talar om för läkaren om något av dessa tillstånd gäller dig, även om du är osäker. Din läkare kan besluta att du måste sluta använda Lumivela.
Om något av ovanstående tillstånd ändras medan du använder Lumivela, t.ex. en nära släkting drabbas av en blodpropp med okänd orsak eller du går upp mycket i vikt, tala med din läkare.
BLODPROPPAR I EN ARTÄR
Vad kan hända om en blodpropp bildas i en artär?
På samma sätt som en blodpropp i en ven kan en propp i en artär leda till allvarliga problem. Det kan t.ex. orsaka hjärtinfarkt eller stroke.
Faktorer som kan öka risken för en blodpropp i en artär
Det är viktigt att du vet att risken för en hjärtinfarkt eller stroke till följd av användning av Lumivela är mycket liten men kan öka:
- med stigande ålder (efter cirka 35 års ålder)
- om du röker. När du använder kombinerade hormonella preventivmedel som Lumivela bör du sluta röka. Om du inte kan sluta röka och är över 35 år kan din läkare råda dig att använda en annan typ av preventivmedel.
- om du är överviktig
- om du har högt blodtryck
- om någon nära anhörig har haft en hjärtinfarkt eller en stroke i unga år (yngre än 50 år). I det här fallet kan du också löpa större risk för en hjärtinfarkt eller en stroke.
- om du eller någon nära släkting har höga blodfetter (kolesterol eller triglycerider)
- om du får migrän, speciellt migrän med en aura
- om du har problem med hjärtat (klaffsjukdom, en hjärtrytmstörning som kallas förmaksflimmer)
- om du har diabetes.
Om du har mer än ett av dessa tillstånd eller om något av dem är särskilt svårt kan risken för att utveckla en blodpropp vara ännu större.
Om något av ovanstående tillstånd ändras medan du använder Lumivela, t.ex. om du börjar röka, en nära släkting drabbas av en blodpropp av okänd orsak eller om du går upp mycket i vikt, tala med din läkare.
P-piller och cancer
Bröstcancer förekommer något oftare hos kvinnor som använder kombinerade p-piller än hos kvinnor som inte gör det. Det är okänt om den här skillnaden beror på p-pillren. Det kan vara så att kvinnorna som tar kombinerade p-piller går på fler kontroller så att bröstcancern upptäcks tidigare.
I sällsynta fall har godartade levertumörer, och i ännu mer sällsynta fall elakartade levertumörer, rapporterats bland kvinnor som använder p-piller. Kontakta omedelbart din läkare om du får ovanliga kraftiga buksmärtor.
Kronisk infektion med humant papillomvirus (HPV) är den enskilt viktigaste riskfaktorn för livmoderhalscancer. Hos kvinnor som använder p-piller under lång tid kan risken för livmoderhalscancer vara något förhöjd. Det är inte säkert att p-pillren i sig är orsaken, utan det kan även bero på sexualvanor och andra faktorer (t.ex. bättre kontroller av livmoderhalsen).
Psykiska störningar:
Vissa kvinnor som använder hormonella preventivmedel, inräknat Lumivela, har rapporterat depression eller nedstämdhet. Depressioner kan vara allvarliga och ibland leda till självmordstankar. Om du upplever humörförändringar och symtom på depression ska du snarast möjligt kontakta läkare för rådgivning.
Andra läkemedel och Lumivela
Tala om för läkare, apotekspersonal eller barnmorska om du använder, nyligen har använt eller kan tänkas använda andra läkemedel eller (traditionella) växtbaserade läkemedel utöver Lumivela. Tala också om för andra läkare eller tandläkare som förskriver läkemedel (eller för apotekspersonal) att du använder Lumivela. De kan tala om för dig om du behöver använda ett kompletterande icke-hormonellt preventivmedel, till exempel kondom, och i så fall under hur lång tid, eller om du måste byta ut något annat läkemedel som du behöver.
Använd inte Lumivela om du har hepatit C och tar läkemedel som innehåller ombitasvir/paritaprevir/ritonavir och dasabuvir, glekaprevir/pibrentasvir eller sofosbuvir/velpatasvir/voxilaprevir eftersom det kan orsaka förhöjda leverfunktionsvärden (förhöjning av leverenzymet ALAT).
Din läkare kommer förskriva en annan typ av preventivmedel före start av behandling med dessa läkemedel.
Lumivela kan börja användas igen ungefär 2 veckor efter att denna behandling har avslutats (se avsnitt ”Använd inte Lumivela”).
Vissa läkemedel:
- kan ha en inverkan på blodnivåerna av Lumivela
- kan hindra Lumivela från att förhindra graviditet
- kan orsaka oväntade blödningar.
Detta gäller läkemedel för behandling av:
- epilepsi (t.ex. primidon, fenytoin, fenobarbital, karbamazepin, oxkarbazepin, topiramat, felbamat)
- tuberkulos (t.ex. rifampicin, rifabutin)
- hiv-infektion (t.ex. ritonavir, nelfinavir, nevirapin, efavirenz)
- hepatit C-virusinfektion (t.ex. boceprivir, telaprevir)
- andra infektionssjukdomar (t.ex. griseofulvin)
- högt blodtryck i blodkärlen i lungorna (bosentan)
- nedstämdhet ([traditionella] växtbaserade läkemedel som innehåller johannesört).
Om du tar andra läkemedel eller växtbaserade läkemedel som skulle kunna minska effekten av Lumivela ska du även använda en barriärmetod. Eftersom vissa läkemedel kan påverka effekten av Lumivela i upp till 28 dagar efter avslutad behandling är det nödvändigt att använda barriärmetoden som tillägg under hela denna tid.
Lumivela kan påverka effekten av andra läkemedel, t.ex.
- läkemedel som innehåller ciklosporin
- epilepsiläkemedlet lamotrigin (detta kan öka antalet anfall).
Laboratorieprover
Om du ska genomgå laboratorieundersökningar ska du tala om för din läkare eller laboratoriepersonalen att du använder p-piller, eftersom hormonella preventivmedel kan påverka resultatet av vissa prover.
Graviditet och amning
Graviditet
Använd inte Lumivela om du är eller tror att du kan vara gravid. Om du tror att du kan vara gravid medan du använder Lumivela, kontakta läkare så fort som möjligt.
Amning
Det rekommenderas inte att Lumivela används under amning. Kontakta läkare om du ändå vill använda Lumivela när du ammar.
Körförmåga och användning av maskiner
Lumivela har ingen känd effekt på förmågan att framföra fordon eller använda maskiner.
Lumivela innehåller laktos och sojaolja
Om du inte tål vissa sockerarter, bör du kontakta din läkare innan du tar denna medicin.
Om du är allergisk mot jordnötter eller soja ska du inte använda detta läkemedel.
Barn och ungdomar
Det finns inga tillgängliga kliniska data om effekt och säkerhet hos ungdomar under 18 år.
När ska du kontakta läkare?
Regelbundna kontroller
Din läkare kan uppmana dig att gå på regelbundna kontroller när du använder kombinerade p‑piller. Din individuella situation bestämmer hur ofta du behöver gå på kontroll och vilka tester som ska göras.
Kontakta din läkare snarast:
- om du märker möjliga tecken på en blodpropp. Detta kan betyda att du har en blodpropp i ett blodkärl i benet (djup ventrombos) eller i lungan (lungemboli), en hjärtattack eller stroke (se avsnittet ”P‑piller och blodproppar”).
För en beskrivning av symtomen på dessa allvarliga biverkningar, se avsnittet "Så här känner du igen en blodpropp". - om du noterar förändringar i din hälsa, särskilt om de är relaterade till något av de fall som nämns i denna bipacksedel (se även ”Använd inte Lumivela” och ”Varningar och försiktighet”); glöm inte heller fall som rör din närmaste familj
- om du känner en knöl i bröstet
- om du får symtom på angioödem, såsom svullet ansikte, tunga och/eller svalg och/eller svårigheter att svälja eller nässelutslag, eventuellt med andningssvårigheter (se även avsnittet ”Varningar och försiktighet”)
- om du ska börja använda andra läkemedel (se även ”Andra läkemedel och Lumivela”)
- om din rörlighet är begränsad under en lång tid eller om du ska genomgå en operation (tala med din läkare minst 4 veckor på förhand)
- om du har blödningsrubbningar som är långvariga eller förvärras
- om du glömde tabletter den första veckan och hade samlag under den första veckan
- om du har svår diarré
- om din mens uteblir två gånger i rad. Börja inte ta tabletter från en ny förpackning förrän din läkare säger att du kan göra det.
Hur produkten används
Ta alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
När och hur du ska ta tabletterna
Lumivela är förpackat i tablettkartor med 28 tabletter. Varje tablettkarta innehåller 21 aktiva vita tabletter och 7 gröna placebotabletter.
Tabletterna i två olika färger är placerade i ordning.
På tablettkartan finns markeringar som anger vilken veckodag respektive tablett ska tas. Ta tabletterna vid ungefär samma tidpunkt varje dag, med lite vätska om det behövs.
Blanda inte ihop tabletterna: Följ pilarnas riktning på tablettkartan tills du har tagit alla 21 vita tabletter, och ta sedan en grön tablett varje dag under de resterande 7 dagarna. Sedan ska du påbörja en ny tablettkarta (21 vita tabletter och 7 gröna tabletter). Därför blir det ingen tablettfri vecka mellan tablettkartorna.
På grund av tabletternas olika sammansättning måste du börja med den första tabletten uppe till vänster och ta tabletterna varje dag. Följ pilens riktning på kartan för att ta tabletterna i rätt ordning.
Förberedelse av tablettkartan
För att hjälpa dig hålla reda på vilken tablett du ska ta innehåller förpackningen 7 klisterremsor med 7 veckodagar för varje tablettkarta av Lumivela. Välj den klisterremsa som börjar med den veckodag då du börjar ta tabletterna. Om du t.ex. börjar på en onsdag ska du använda klisterremsan som börjar med ”ONS”.
Klistra remsan i tablettkartans överkant där det står ”Klistra remsan här”, så att den första dagen hamnar ovanför tabletten som märkts med ”1”. Nu finns en dag angiven ovanför varje tablett och du kan se om du har tagit en viss tablett. Pilarna visar i vilken ordning du ska ta tabletterna.
Under de 7 dagarna när du tar de gröna placebotabletterna (placebodagarna) bör du ha blödning (s.k. bortfallsblödning). Den börjar i allmänhet på andra eller tredje dagen efter den sista vita aktiva tabletten. När du har tagit den sista gröna tabletten ska du påbörja nästa tablettkarta, oavsett om din blödning har slutat eller inte. Detta betyder att du ska påbörja varje tablettkarta samma veckodag och att bortfallblödningarna bör infalla samma dagar varje månad.
Om du använder Lumivela på det sättet är du skyddad mot graviditet även under de 7 dagar när du tar placebotabletter.
När kan du börja med den första tablettkartan?
- När du inte har använt p-piller månaden innan
Börja ta Lumivela på menstruationscykelns första dag (dvs. den första blödningsdagen). Lumivela kommer att börja verka direkt, du behöver inte använda något extra skydd. Du kan också börja på dag 2–5 av din cykel, men då måste du använda extra skydd, t.ex. kondom, under de första 7 dagarna.
När du byter från ett annat kombinerat p-piller, p‑ring eller p-plåster
Du kan börja ta Lumivela dagen efter den sista tabletten i tablettkartan med ditt tidigare p-piller (alltså utan att göra något tablettuppehåll). Om förpackningen med ditt tidigare p-piller innehåller inaktiva tabletter kan du börja med Lumivela dagen efter att du tar den sista aktiva tabletten (om du är osäker på vilken som är den sista aktiva tabletten, fråga din läkare eller apotekspersonal). Du kan också börja senare, men aldrig senare än dagen efter tablettuppehållet med ditt tidigare p-piller (eller dagen efter den sista inaktiva tabletten av ditt tidigare p-piller).
Om du använder en p‑ring eller ett p‑plåster ska du börja med Lumivela den dag du tar ut ringen eller tar bort plåstret. Du kan också börja ta Lumivela senare, men allra senast sju dagar efter att du avlägsnat ringen eller det sista plåstret.
Om du har använt p‑piller, p‑plåster eller p‑ring enligt ordinationen och är säker på att du inte är gravid kan du också när som helst under menstruationscykeln sluta med det kombinerade hormonella preventivmedlet i fråga och direkt börja ta Lumivela.
Om du följer de här råden behöver du inte använda något extra skydd, såsom kondom.
- När du byter från ett preventivmedel med enbart gestagen (minipiller)
Du kan sluta med minipiller vilken dag som helst och börja ta Lumivela dagen efter, vid vilken tidpunkt som helst. Du ska dock också använda extra skydd, t.ex. kondom, de första 7 dagarna du tar Lumivela.
- När du byter från p-spruta, implantat eller hormonspiral
Börja ta Lumivela samma dag som du skulle ha fått nästa spruta eller den dag då ditt implantat eller din hormonspiral tas ut. Du ska också använda extra skydd, t.ex. kondom, de första 7 dagarna du tar Lumivela.
- Efter att ha fött barn
Om du just fött barn kan din läkare be dig vänta med att börja ta Lumivela tills du haft en normal menstruationsblödning. I vissa fall är det möjligt att börja tidigare. Din läkare kommer att ge dig råd. Detsamma gäller om du ammar och vill börja ta Lumivela.
- Efter missfall
Följ läkarens anvisningar.
Om du har tagit för stor mängd av Lumivela
Det finns inga rapporter om allvarliga skador till följd av intag av för många Lumivela-tabletter. Om du tar flera tabletter samtidigt kan du få symtom på illamående eller kräkningar. Unga flickor kan få blödningar från underlivet.
Om du fått i dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedlet av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel. 0800 147 111) för bedömning av risken samt rådgivning.
Om du har glömt att ta Lumivela
Tabletterna i den 4:e raden på tablettkartan är placebotabletter. Om du glömmer att ta någon av dessa tabletter har det ingen effekt på tillförlitligheten av Lumivela. Kasta bort den glömda placebotabletten.
Om du glömmer att ta en vit aktiv tablett från den 1:a, 2:a eller 3:e raden på tablettkartan ska du göra följande:
- Om den glömda tabletten tas inom 12 timmar kommer skyddet mot graviditet inte att bli nedsatt. Ta tabletten så snart du kommer ihåg det och ta sedan de följande tabletterna vid den vanliga tidpunkten.
- Om det har gått mer än 12 timmar sedan du skulle ta en tablett kan skyddet mot graviditet vara nedsatt. Ju fler tabletter i följd du har glömt, desto större är risken för att skyddet mot graviditet blir nedsatt.
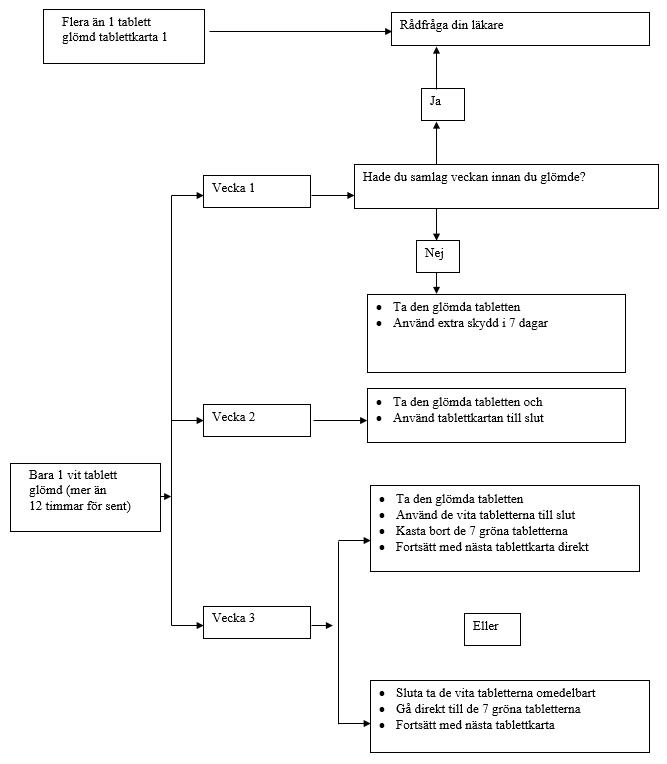
Risken för att bli gravid är särskilt stor om du glömmer tabletter i början eller i slutet av tablettkartan. Därför ska du alltid följa de anvisningar som ges nedan (se diagrammet):
- Fler än 1 glömd tablett i tablettkartan:
Kontakta din läkare för råd.
- 1 tablett glömd under vecka 1:
Ta den glömda tabletten så snart du kommer ihåg det, även om det betyder att du tar två tabletter samtidigt. Ta de följande tabletterna vid den vanliga tidpunkten. Använd extra skydd under de följande 7 dagarna. Om du hade samlag under veckan innan du glömde en tablett eller om du glömt att börja en ny tablettkarta efter placebotablettperioden finns en risk att du blir gravid. Kontakta i så fall din läkare.
- 1 tablett glömd under vecka 2:
Ta den glömda tabletten så snart du kommer ihåg det, även om det betyder att du tar två tabletter samtidigt. Ta de följande tabletterna vid den vanliga tidpunkten. P-pillret skyddar fortfarande mot graviditet. Du behöver inte använda extra skydd.
- 1 tablett glömd under vecka 3:
Du kan välja ett av de nedanstående alternativen utan att behöva använda extra skydd:
- Ta den glömda tabletten så snart du kommer ihåg det, även om det betyder att du tar två tabletter samtidigt. Ta de följande tabletterna vid den vanliga tidpunkten. När du tagit alla aktiva tabletterna i den nuvarande tablettkartan, börja direkt på nästa tablettkarta följande dag utan att ta de gröna placebotabletterna. Du kommer kanske inte att få någon bortfallsblödning förrän du kommer till slutet av den andra tablettkartan, men du kan få stänkblödningar eller genombrottsblödning medan du tar tabletter från den andra tablettkartan.
- Sluta ta de aktiva vita tabletterna från den aktuella tablettkartan och gå direkt till de 7 gröna placebotabletterna (räkna alltid dagen då du glömde att ta en tablett som en placebotablettdag). Fortsätt sedan med nästa tablettkarta. Om du gör på det här sättet kan du alltid börja på en ny tablettkarta på samma veckodag som du är van vid.
- Om du har glömt att ta någon av de aktiva (vita) tabletterna och du inte får menstruation under de normala placebotablettdagarna kan du ha blivit gravid. Kontakta läkare innan du börjar med nästa tablettkarta.
Om du har magbesvär (t.ex. kräkningar eller svår diarré)
Om du kräks eller har mycket svår diarré kan det hända att kroppen inte får den vanliga hormondosen från p-pillren. Om du kräks inom 3–4 timmar efter att du tagit en aktiv tablett motsvarar det en situation då du glömt att ta en tablett. Då ska du följa samma råd som gäller i händelse av glömda tabletter. Tala med din läkare om du har svår diarré.
Om du vill skjuta upp menstruationen
Du kan skjuta upp menstruationen, även om det inte är något som rekommenderas. I undantagsfall kan du skjuta upp menstruationen genom att fortsätta på en ny tablettkarta med Lumivela, i stället för att ta placebotabletterna, och använda den nya tablettkartan till slut. Du kan fortsätta med denna tablettkarta så länge du önskar, tills den är slut. Medan du använder den andra tablettkartan kan du få en genombrottsblödning eller stänkblödning. Börja med nästa tablettkarta efter den vanliga 7 dagar långa placebotablettperioden.
Om du vill ändra menstruationens startdag
Om du tar dina tabletter enligt anvisningarna kommer du att få din mens på ungefär samma dag under veckorna när du tar placebotabletter. Om du vill ändra detta ska du bara förkorta (aldrig förlänga) placebotablettperioden. Om du t.ex. normalt börjar ta placebotabletter på en fredag och du vill byta till tisdag (3 dagar tidigare) ska du börja på den nya tablettkartan 3 dagar tidigare än vanligt. Om du gör placebotablettperioden mycket kort (t.ex. 3 dagar eller kortare) kan det hända att du inte får någon blödning under denna placebotablettperiod. Det kan hända att du får genombrottsblödning eller stänkblödningar när du tar tabletterna i nästa karta.
Om du får en oväntad blödning
Under de första månaderna som du använder någon typ av kombinerade p-piller kan du få oregelbundna underlivsblödningar (stänkblödningar eller genombrottsblödning) mellan menstruationerna. Du kan behöva använda menstruationsskydd, men fortsätt i alla fall att ta dina tabletter som vanligt. De oregelbundna blödningarna brukar upphöra när kroppen har anpassat sig till de kombinerade p-pillren (vanligtvis efter cirka 3 tablettkartor). Tala med din läkare om du fortsätter att ha oregelbundna blödningar, om de blir rikligare eller om de återkommer.
Om du inte får någon mens
Om du har tagit alla dina tabletter vid rätt tidpunkt och du inte har kräkts, haft svår diarré eller samtidigt använt andra läkemedel är det mycket osannolikt att du är gravid. Fortsätt på nästa tablettkarta som vanligt.
Om mensen uteblir två gånger i rad kan du vara gravid. Kontakta omedelbart din läkare. Börja inte på nästa tablettkarta med Lumivela förrän läkaren har bekräftat att du inte är gravid.
Om du vill sluta att ta Lumivela
Du kan sluta ta Lumivela när du vill. Om du inte vill bli gravid ska du rådgöra med läkaren om vilken annan tillförlitlig preventivmetod du kan använda. Om du slutar ta Lumivela för att du vill bli gravid rekommenderas vanligen att du väntar tills du haft en naturlig menstruationsblödning innan du försöker bli gravid. Det gör det lättare för dig att beräkna när babyn förväntas födas.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem. Om du får någon biverkning, framför allt om den är svår eller ihållande, eller om din hälsa förändras och du tror det kan bero på Lumivela, tala med din läkare.
En ökad risk för blodproppar i venerna (venös tromboembolism [VTE]) eller blodproppar i artärerna (arteriell tromboembolism [ATE]) finns för alla kvinnor som använder kombinerade hormonella preventivmedel. Mer information om de olika riskerna vid användning av kombinerade hormonella preventivmedel finns i avsnitt Vad du behöver veta innan produkten används ”Vad du behöver veta innan du använder Lumivela”.
Kontakta omedelbart läkare om du får något av följande symtom på angioödem: svullnad i ansiktet, tungan och/eller svalget och/eller sväljningssvårigheter eller nässelutslag, eventuellt med andningssvårigheter (se även avsnittet ”Varningar och försiktighet”).
Liksom med alla kombinerade p-piller kan ditt blödningsmönster förändras.
Förändringen kan återspegla sig i blödningsfrekvensen (utebliven, mer sällan, oftare eller kontinuerligt), blödningsmängden eller i hur länge blödningen pågår.
Vanliga (kan förekomma hos upp till 1 av 10 kvinnor):
- Depression eller humörsvängning
- huvudvärk
- illamående, buksmärta
- ömhet eller smärta i brösten
- viktökning.
Mindre vanliga (kan förekomma hos upp till 1 av 100 kvinnor):
- vätskeansamling
- minskad sexuell lust
- migrän
- kräkningar, diarré
- utslag eller nässelutslag
- bröstförstoring.
Sällsynta (kan förekomma hos upp till 1 av 1 000 kvinnor):
- farliga blodproppar i en ven eller en artär, till exempel:
- i ett ben eller en fot (dvs. djup ventrombos)
- i lungorna (dvs. lungemboli)
- hjärtinfarkt
- stroke
- mini-stroke eller övergående strokeliknande symtom som kallas transitorisk ischemisk attack (TIA)
- blodproppar i levern, magen/tarmen, njurarna eller ögonen. Risken för att drabbas av en blodpropp kan vara högre om du har andra tillstånd som ökar den här risken (se avsnitt Vad du behöver veta innan produkten används för mer information om de tillstånd som ökar risken för blodproppar och symtomen på en blodpropp).
- överkänslighetsreaktioner
- ökad sexuell lust
- obehag i ögonen om du använder kontaktlinser
- erythema nodosum (svullnader som liknar blåmärken på smalbenen), erythema multiforme (ett utslag med röda, oregelbundna fläckar eller sår)
- mjölkaktig vätskeutsöndring från bröstvårtorna, förändringar i sekretet i underlivet
- viktminskning.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Förvaras vid högst 30 ºC.
Förvaras i originalförpackningen. Ljuskänsligt.
Utgångsdatum
Används före utgångsdatum som anges på kartongen efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Använd inte Lumivela om du märker färgförändring, krossade tabletter eller andra synliga tecken på försämring.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
En tablettkarta av Lumivela innehåller 21 vita aktiva tabletter på den 1:a, 2:a och 3:e raden av kartan och 7 gröna placebotabletter på den 4:e raden.
Aktiva tabletter
- De aktiva substanserna är desogestrel och etinylestradiol. En vit tablett innehåller 150 mikrogram desogestrel och 20 mikrograms etinylestradiol.
- Övriga innehållsämnen är: Laktosmonohydrat, majsstärkelse, povidon K-30 (E1201), rrr-alfa-tokoferol (E307), sojaolja, hydratiserad kolloidal kiseldioxid (E551), vattenfri kolloidal kiseldioxid (E551), stearinsyra (E570), hypromellos 2910 (E464), makrogol 400 och titandioxid (E171).
Gröna inaktiva tabletter
Laktosmonohydrat, majsstärkelse, povidon K-30 (E1201), vattenfri kolloidal kiseldioxid (E551), magnesiumstearat (E572), hypromellos 2910 (E464), triacetin (1518), polysorbat, titandioxid (E171), indigokarmin aluminiumlack (E132) och gul järnoxid (E172).
Läkemedlets utseende och förpackningsstorlekar
- En aktiv filmdragerad tablett är vit och rund. Varje tablett är märkt med ”C” på ena sidan och ”5” på andra sidan.
- En inaktiv filmdragerad tablett är grön och rund.
- Lumivela finns i tablettkartor med 28 tabletter: 21 vita aktiva tabletter och 7 gröna inaktiva tabletter.
Förpackningsstorlekar: 1, 3, 6 eller 13 tablettkartor; varje karta innehåller 28 tabletter. Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning och tillverkare
Innehavare av godkännande för försäljning
Exeltis Healthcare S.L.
Av.Miralcampo 7-Poligono Ind.Miralcampo
19200 Azuqueca de Henares
Guadalajara, Spanien
Tillverkare
Laboratorios León Farma, S.A.
C/ La Vallina s/n, Pol. Ind. Navatejera.
24193 - Villaquilambre, León.
Spanien
Denna bipacksedel ändrades senast 24.01.2025