MYRELEZ injektionsvätska, lösning i förfylld spruta 60 mg, 90 mg, 120 mg
Tilläggsinformation
Myrelez 60 mg injektionsvätska, lösning i förfylld spruta
Myrelez 90 mg injektionsvätska, lösning i förfylld spruta
Myrelez 120 mg injektionsvätska, lösning i förfylld spruta
lanreotid
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad Myrelez är och vad det används för
2. Vad du behöver veta innan du använder Myrelez
3. Hur du använder Myrelez
4. Eventuella biverkningar
5. Hur Myrelez ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Myrelez innehåller den aktiva substansen lanreotid som tillhör en grupp av läkemedel som kallas tillväxthämmande hormoner. Denna substans är snarlik en annan substans (ett hormon) som heter somatostatin.
Lanreotid som finns i Myrelez kan också vara godkänd för att behandla andra sjukdomar som inte nämns i denna produktinformation. Fråga läkare, apoteks- eller annan hälso- och sjukvårdspersonal om du har ytterligare frågor och följ alltid deras instruktion.
Lanreotid sänker nivåerna av hormoner i kroppen, t.ex. tillväxthormon (GH) och insulinliknande tillväxtfaktor 1 (IGF‑1) och hämmar frisättningen av vissa hormoner i mag–tarmkanalen och i tarmsekret. Läkemedlet har dessutom en effekt på vissa avancerade former av tumörer (så kallade neuroendokrina tumörer) i tarmen och i bukspottkörteln genom att det stoppar eller fördröjer deras tillväxt.
Vad Myrelez används för
- Behandling av akromegali (ett tillstånd där din kropp producerar för mycket tillväxthormon)
- Lindring av symtom såsom värmevallningar och diarré som ibland uppstår hos patienter med neuroendokrina tumörer (NET)
- Behandling och kontroll av tillväxten av vissa avancerade tumörer i tarmen och i bukspottkörteln, så kallade gastroenteropankreatiska neuroendokrina tumörer, eller GEP‑NET. Läkemedlet används när dessa tumörer inte kan avlägsnas genom operation.
Vad du behöver veta innan produkten används
Använd inte Myrelez:
- om du är allergisk mot lanreotid, somatostatin eller läkemedel från samma familj (somatostatinanalog) eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du använder Myrelez:
- om du har diabetes, eftersom Myrelez kan påverka dina blodsockernivåer. Läkaren kan komma att kontrollera dina blodsockernivåer och eventuellt ändra din diabetesmedicinering medan du får Myrelez
- om du har gallsten, eftersom Myrelez kan leda till bildning av gallstenar i gallblåsan. I detta fall kan du behöva kontrolleras regelbundet. Läkaren kan fatta beslutet att avbryta behandling med lanreotid om komplikationer från gallstenar uppstår.
- om du har problem med sköldkörteln, eftersom Myrelez kan sänka sköldkörtelfunktionen något
- om du har hjärtsjukdom, eftersom bradykardi (långsam hjärtfrekvens) kan förekomma under behandling med Myrelez. Särskild försiktighet ska iakttas när patienter med bradykardi påbörjar behandling med Myrelez.
Om något av ovanstående gäller dig, tala med läkare eller apotekspersonal innan du använder Myrelez.
Barn
Myrelez rekommenderas inte till barn.
Andra läkemedel och Myrelez
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
Särskild försiktighet ska iakttas vid samtidig behandling med:
- ciklosporin (ett immunhämmande läkemedel som minskar immunreaktionen efter en transplantation eller vid autoimmun sjukdom)
- bromokriptin (en dopaminagonist som används för att behandla Parkinsons sjukdom och vissa typer av tumörer i hjärnan, eller för att förhindra mjölkbildning efter förlossning)
- bradykardiinducerande läkemedel (läkemedel som sänker hjärtrytmen, t.ex. betablockerare).
Läkaren kan överväga att justera dosen av dessa läkemedel om de används samtidig.
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du tar detta läkemedel.
Om du är gravid eller ammar ska du endast använda Myrelez om det är absolut nödvändigt.
Körförmåga och användning av maskiner
Myrelez har sannolikt inte någon effekt på förmågan att köra bil och använda maskiner, men möjliga biverkningar såsom yrsel kan förekomma med Myrelez. Om du drabbas ska du vara försiktig när du kör eller använder maskiner.
Du är själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbeten som kräver skärpt uppmärksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användning av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med läkare eller apotekspersonal om du är osäker.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens anvisningar. Kontrollera med läkare eller apotekspersonal om du är osäker.
Rekommenderad dos
Behandling av akromegali
Rekommenderad dos är en injektion var 28:e dag. Läkaren kan anpassa dosen med hjälp av någon av de tre tillgängliga styrkorna av Myrelez (60 mg, 90 mg eller 120 mg).
Om du kontrolleras väl på din behandling kan läkaren rekommendera en annan doseringsfrekvens av injektioner med Myrelez 120 mg till en injektion var 42:e eller 56:e dag. Alla dosändringar beror på dina symtom och hur pass väl du svarar på läkemedlet.
Läkaren avgör även hur lång behandlingstiden ska vara.
Lindring av symtom (t.ex. värmevallningar och diarré) i samband med neuroendokrina tumörer
Rekommenderad dos är en injektion var 28:e dag. Läkaren kan anpassa dosen med hjälp av någon de tre tillgängliga styrkorna av Myrelez (60 mg, 90 mg eller 120 mg).
Om du kontrolleras väl på din behandling kan läkaren rekommendera en annan doseringsfrekvens av injektioner med Myrelez 120 mg till en injektion var 42:e eller 56:e dag.
Läkaren avgör även hur lång behandlingstiden ska vara.
Behandling avancerade tumörer i tarmen och i bukspottkörteln, så kallade gastroenteropankreatiska neuroendokrina tumörer, eller GEP-NET. Används när dessa tumörer inte kan avlägsnas genom operation.
Rekommenderad dos är 120 mg var 28:e dag. Läkaren avgör hur länge du ska behandlas med Myrelez för tumörkontroll.
Administreringssätt
Myrelez ska administreras som en djup injektion i underhuden.
Om injektionen ges av hälso- eller sjukvårdspersonal eller någon annan som har fått övning (anhörig eller vän) ges injektionen i den övre, yttre fjärdedelen av skinkan (se bilderna i avsnitt B6 nedan).
Om du ger injektionen till dig själv och har fått lämplig övning ska injektionen ges i den övre delen av lårets utsida (se bilderna i avsnitt B6 nedan).
Det är upp till hälso- och sjukvårdspersonal att bestämma om injektionen ska ges av dig själv eller av någon som fått övning. Om du när som helst känner dig osäker på hur denna injektion ska ges, kontakta din läkare eller sjukvårdspersonal för råd eller vidare övning.
BRUKSANVISNING
Observera: Läs alla instruktioner noggrant innan du påbörjar injektionen. Injektionen ges djupt under huden och administreringen kräver en annan teknik än en traditionell injektion under huden.
A. Vad kartongen innehåller
I följande instruktion beskrivs hur Myrelez ska injiceras.
Läs hela bruksanvisningen noggrant innan du påbörjar injektionen.
Innehållet i den förfyllda sprutan är halvfast, gelliknande och trögflytande. Färgen varierar från vitt till svagt gult. Den övermättade lösningen kan också innehålla mikrobubblor som kan försvinna under injektionen. Dessa skillnader är normala och påverkar inte produktens kvalitet.
B. Innan du börjar
B1. Ta ut Myrelez ur kylskåpet 30 minuter innan injektionen ska ges. På så sätt hinner lanreotidlösningen uppnå rumstemperatur vilket minimerar eventuell smärtreaktion som kan uppstå om läkemedlet är kallt. Öppna inte den laminerade skyddspåsen förrän precis innan injektionen ska ges.

B2. Kontrollera att skyddspåsen är intakt innan du öppnar den och att utgångsdatumet inte har passerat. Utgångsdatum är angivet på ytterkartongen och på skyddspåsen. Använd inte läkemedlet om utgångsdatumet har passerat eller om skyddspåsen är skadad.
B3. Tvätta händerna med tvål och torka dem noga innan du sätter igång.
B4. Kontrollera att det finns en ren yta för iordningställandet.
B5. Välj injektionsställe. De olika ställena visas nedan.
B6: Var noga med att rengöra injektionsstället.
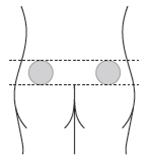 | Om du ger injektionen till någon annan: Ge injektion i den övre yttre delen av skinkan. |
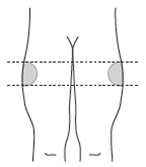 | Om du ger injektionen till dig själv: Ge injektion i den övre yttre delen av låret. |
Växla injektionsstället mellan höger och vänster sida för varje injektion av Myrelez. Undvik områden med födelsemärken, ärrvävnad, röd hud eller hud som känns ojämn. Observera att injektionsstället inte kan bytas när nålen har förts in.
B7. Riv upp skyddspåsen och ta ut den förfyllda sprutan.

Efter att du har öppnat den laminerade skyddspåsen ska läkemedlet ges omedelbart.
C. Gör iordning sprutan
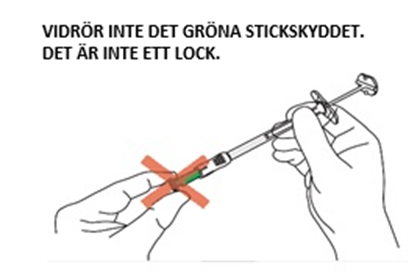
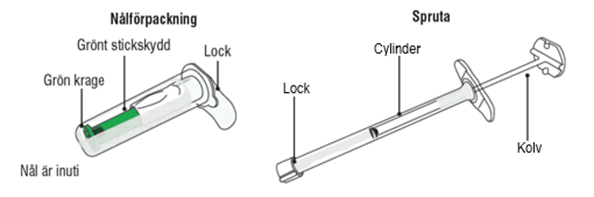
 | C1: Öppna nålförpackningen
|
 | C2: Ta av locket på sprutan
|
 | C3: För in ändan av sprutan i nålförpackningens öppna ända.
Viktigt: Skruva åt ordentligt för att undvika läckage. |
| C4: Ta ut nålen ur nålförpackningen
Försiktighet: Nålen är delvis exponerad från och med detta steg.
|
| D. Ge injektionen | |
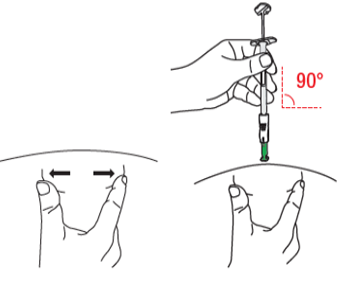 | D1: Positionera sprutan
|
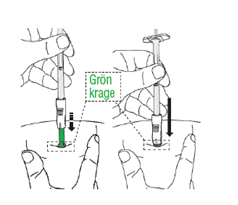 | D2: Sätt in nålen
|
| Obs: Fortsätt trycka nålen under injektionen för att undvika att säkerhetsmekanismen täcker och låser nålen. | |
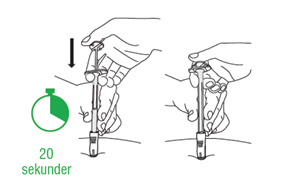 | D3: Tryck ner kolven
|
| E. Dra ut sprutan och kasta den | |
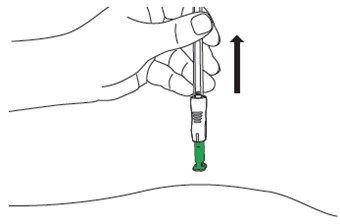 | E1: Ta bort från huden
|
 | E2: Applicera lätt tryck
|
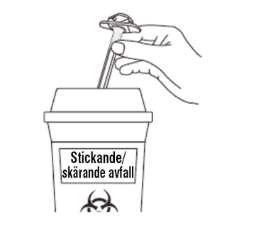 | E3: Kasta
|
Om du använt för stor mängd av Myrelez
Om du injicerat för stor mängd av Myrelez ska du informera läkaren.
Vid för stor mängd injicerat Myrelez kan du uppleva ytterligare eller mer allvarliga biverkningar (se avsnitt Eventuella biverkningar, Eventuella biverkningar).
Om du har glömt att använda Myrelez
Kontakta sjukvården så fort du upptäcker att du har missat en injektion. De kommer att ge dig råd om när du ska ta nästa injektion. Ge inga extra egeninjektioner för att kompensera för glömd injektion utan att tala med hälso- och sjukvårdspersonal.
Om du slutar att använda Myrelez
Ett behandlingsuppehåll på mer än en dos eller ett för tidigt avbrytande av Myrelez-behandlingen kan påverka behandlingens resultat. Tala med läkaren innan du avbryter behandlingen.
Om du har ytterligare frågor om detta läkemedel kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Tala omedelbart om för läkaren om du upplever någon av följande biverkningar:
- Ökad törst eller trötthet och muntorrhet. Detta kan vara tecken på höga blodsockernivåer eller begynnande diabetes.
- Hungerkänslor, skakningar, ökad svettning eller förvirring. Detta kan vara tecken på låga blodsockernivåer.
Frekvensen av dessa biverkningar är vanlig, det vill säga kan förekomma hos upp till 1 av 10 personer.
Tala omedelbart om för läkaren om du upplever något av följande:
- Ansiktsrodnad eller ansiktssvullnad, eller fläckar eller utslag i ansiktet
- Tryck över bröstet, andfåddhet eller väsande andning
- Svimningskänsla, möjligen till följd av blodtrycksfall.
Detta kan vara följden av en allergisk reaktion.
Frekvensen av dessa biverkningar är inte känd; kan inte beräknas från tillgängliga data.
Övriga biverkningar
Tala om för läkare eller apotekspersonal om du märker någon av nedanstående biverkningar.
De vanligaste förväntade biverkningarna är mag–tarmbesvär, problem med gallblåsan och reaktioner vid injektionsstället. De biverkningar som kan uppstå med Myrelez listas nedan enligt frekvens.
Mycket vanliga (kan förekomma hos mer än 1 av 10 användare):
- diarré, lös avföring*, buksmärta
- gallstenar och andra problem med gallblåsan. Du kan få symptom som svår och plötslig buksmärta, hög feber, gulsot (gulfärgning av hud och ögonvitor), frossa, aptitlöshet, kliande hud.
Vanliga (kan förekomma hos upp till 1 av 10 personer):
- viktminskning
- brist på energi
- långsam hjärtfrekvens
- stark trötthetskänsla
- minskad aptit
- allmän svaghetskänsla
- stor mängd fett i avföringen
- yrsel, huvudvärk
- håravfall eller minskad hårväxt på kroppen
- smärta i muskler, ledband, senor eller skelett
- reaktioner på injektionsstället såsom smärta eller hård hud
- onormala lever- och bukspottkörteltestresultat och förändringar i blodsockernivåer
- illamående, kräkningar, förstoppning, gaser, uppsvälld mage eller obehagskänsla i magen, matsmältningsbesvär
- biliär dilatation (utvidgning av gallgångarna mellan levern och gallblåsan och tarmen). Du kan få symtom som magsmärtor, illamående, gulsot och feber
Mindre vanliga (kan förekomma hos upp till 1 av 100 användare):
- värmevallningar
- sömnsvårigheter
- förändrad färg på avföringen
- förändrade nivåer av natrium och alkaliskt fosfatas, vilket påvisas i blodprov
Har rapporterats (förekommer hos ett okänt antal personer):
- plötslig, svår smärta i nedre delen av magen. Detta kan vara ett tecken på inflammation i bukspottkörteln (pankreatit)
- varböld vid injektionsstället som kan kännas vätskefylld när man trycker på den (rodnad, smärta, värme och svullnad som kan vara förknippad med feber)
- inflammation i gallblåsan (kolecystit). Du kan ha symtom såsom svår och plötslig smärta i övre högra eller centrala delen av buken, smärtan kan sprida sig till axlar eller rygg, ömhet i buken, illamående, kräkningar och hög feber
- smärta i den övre delen av buken, feber, frossa, gulnande hud och ögonvitor (gulsot), illamående, kräkningar, lerfärgad avföring, mörk urin, trötthet. Detta kan vara tecken på inflammation i gallgången (kolangit).
Eftersom lanreotid kan förändra dina blodsockernivåer kan din läkare vilja kontrollera ditt blodsocker, särskilt i början av behandlingen.
På samma sätt som att det kan uppstå problem med gallblåsan med denna typ av läkemedel, kan läkaren vilja kontrollera gallblåsans funktion när du påbörjar behandlingen med Myrelez och emellanåt därefter.
Tala om för läkare eller apotekspersonal om du märker någon av biverkningarna ovan.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på kartongen och etiketten efter [EXP]. Utgångsdatumet är den sista dagen i angiven månad.
Produkten ska användas omedelbart efter att aluminiumfoliepåsen öppnats.
Förvaras i kylskåp (2 °C–8 °C) i originalförpackningen. Ljuskänsligt.
Preparat som tagits ur kylskåpet och fortfarande ligger i den förseglade påsen kan återföras till kylskåpet (antal temperaturavvikelser får inte överstiga tre gånger) för vidare förvaring och senare användning, förutsatt att den har förvarats i totalt högst 72 timmar vid en maximal temperatur på 40 °C.
Varje spruta är individuellt förpackad.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är lanreotid (60 mg, 90 mg eller 120 mg)
- Övriga innehållsämnen är vatten för injektionsvätskor och koncentrerad ättiksyra (för pH-justering).
Läkemedlets utseende och förpackningsstorlekar
Myrelez är en trögflytande injektionsvätska i en 0,5 ml halvgenomskinlig plastspruta samförpackad med en stickskyddande nål för engångsbruk. Läkemedlet är en vit till svagt gul halvfast beredning.
Varje förfylld spruta är förpackad i en aluminiumpåse och i en kartong.
Kartong med 0,5 ml spruta och en samförpackad stickskyddande nål (1,2 mm × 20 mm).
Flerpack med 3 kartonger, som var och en innehåller en 0,5 ml spruta och en stickskyddande nål (1,2 mm × 20 mm) i samma förpackning.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning och tillverkare
Innehavare av godkännande för försäljning
Amdipharm Limited
Unit 17
Northwood House
Northwood Crescent
Northwood
Dublin 9
D09 V504
Irland
Tillverkare
Pharmathen S.A
Dervenakion 6,
Pallini Attiki, 15351,
Grekland
Pharmathen International S.A
Industrial Park Sapes,
Rodopi Prefecture, Block No 5,
Rodopi 69300,
Grekland
Denna bipacksedel ändrades senast 01.09.2025