COMTESS tabletti, kalvopäällysteinen 200 mg
Comtess 200 mg tabletti, kalvopäällysteinen
entakaponi
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin aloitat tämän lääkkeen ottamisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä pidä antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä Comtess on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin otat Comtess -valmistetta
- Miten Comtess -valmistetta otetaan
- Mahdolliset haittavaikutukset
- Comtess -valmisteen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Comtess-tabletit sisältävät entakaponia ja niitä käytetään yhdessä levodopan kanssa Parkinsonin taudin hoitoon. Comtess auttaa levodopaa lievittämään Parkinsonin taudin oireita. Comtessilla ei ole tehoa Parkinsonin taudin oireiden lievittämisessä, jos sitä ei käytetä levodopan kanssa.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä Comtess -valmistetta:
- jos olet allerginen entakaponille, maapähkinälle tai soijalle, tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa)
- jos sinulla on lisämunuaisen kasvain (eli feokromosytooma; tämä saattaa lisätä vaikean verenpaineen kohoamisen riskiä)
- jos käytät tiettyjä masennuslääkkeitä (kysy lääkäriltä tai apteekista, voiko sinun masennuslääkettäsi käyttää yhdessä Comtessin kanssa)
- jos sinulla on maksasairaus
- jos sinulla on ollut harvinainen psykoosilääkkeen aiheuttama reaktio, jota kutsutaan pahanlaatuiseksi neuroleptioireyhtymäksi (MNS). Ks. MNS:lle tunnusomaiset piirteet kohdasta Mahdolliset haittavaikutukset.
- jos sinulla on ollut rabdomyolyysiksi kutsuttu harvinainen lihassairaus, joka ei ole aiheutunut mistään vammasta.
Varoitukset ja varotoimet
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin otat Comtess -valmistetta:
- jos sinulla on ollut sydänkohtaus tai mikä tahansa muu sydänsairaus
- jos käytät lääkettä, joka voi aiheuttaa huimausta tai pyörrytystä (verenpaineen laskua) noustessa seisomaan tuolilta tai sängystä
- jos sinulla on pitkittynyttä ripulia, keskustele lääkärisi kanssa, sillä se saattaa olla merkki paksusuolen tulehduksesta
- jos sinulla on ripulia, painon seuranta on suositeltava liiallisen painonlaskun estämiseksi
- jos sinulla on lyhyessä ajassa lisääntyvää ruokahaluttomuutta, heikkoutta, voimattomuutta ja painonlaskua, yleistä lääkärintarkastusta (sisältäen maksan toimintakokeet) on harkittava.
Kerro lääkärille, jos sinä, perheenjäsenesi tai omaishoitajasi huomaatte, että sinulla on voimakas halu tai tarve käyttäytyä tavalla, joka on epätavallista sinulle tai et pysty vastustamaan mielihaluja, pakonomaisia tarpeita tai houkutuksia sellaiseen toimintaan, joka voi olla vahingollista sinulle tai muille. Tällaista käytöstä kutsutaan impulssikontrollin häiriöksi. Se voi ilmetä peliriippuvuutena, ylensyömisenä tai tuhlaamisena, epätavallisen voimakkaana seksuaalisena haluna tai seksuaalisten ajatusten tai tuntemusten lisääntymisenä. Lääkärin tekemä hoidon uudelleen arviointi voi olla tarpeen.
Koska Comtess-tabletit otetaan yhdessä levodopalääkkeiden kanssa, lue myös näiden lääkkeiden pakkausselosteet huolellisesti.
Muiden Parkinsonin taudin hoitoon käytettyjen lääkkeiden annosta voi olla tarpeen muuttaa, kun aloitat Comtessin käytön. Noudata lääkärin ohjeita.
Pahanlaatuinen neuroleptioireyhtymä (MNS) on vakava, mutta harvinainen reaktio tietyille lääkkeille, ja se voi ilmetä erityisesti, kun Comtess tai muut Parkinsonin taudin hoitoon käytetyt lääkkeet äkillisesti lopetetaan tai annosta äkillisesti pienennetään. Ks. MNS:lle tunnusomaiset piirteet kohdasta Mahdolliset haittavaikutukset. Lääkärisi saattaa kehottaa sinua lopettamaan Comtess-hoidon ja muut Parkinsonin taudin hoitoon käytettävät lääkkeet hitaasti.
Comtess voi yhdessä levodopan kanssa aiheuttaa uneliaisuutta ja joskus äkillisiä nukahtamisia. Jos tällaista tapahtuu, sinun ei pidä ajaa tai käyttää koneita tai laitteita (ks. Ajaminen ja koneiden käyttö).
Muut lääkevalmisteet ja Comtess
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä. Kerro lääkärillesi erityisesti, jos otat mitä tahansa seuraavista lääkkeistä:
- rimiterolia, isoprenaliinia, adrenaliinia, noradrenaliinia, dopamiinia, dobutamiinia, alfa-metyylidopaa, apomorfiinia
- masennuslääkkeitä, kuten desipramiinia, maprotiliinia, venlafaksiinia, paroksetiinia
- varfariinia verenohennukseen
- rautavalmisteita. Comtess voi vaikeuttaa raudan imeytymistä. Vältä sen vuoksi rautavalmisteiden ottamista samanaikaisesti Comtessin kanssa. Pidä ainakin 2–3 tunnin tauko näiden valmisteiden välillä.
Raskaus, imetys ja hedelmällisyys
Älä käytä Comtessia raskauden tai imetyksen aikana. Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
Ajaminen ja koneiden käyttö
Comtess yhdessä levodopan kanssa saattaa aiheuttaa verenpaineen laskua, mikä ilmenee pyörrytyksen tai huimauksen tunteena. Ole erityisen varovainen, kun ajat autoa tai käytät koneita tai laitteita.
Lisäksi Comtess-lääkitys yhdessä levodopan kanssa saattaa aiheuttaa uneliaisuutta ja joskus yhtäkkistä nukahtamista.
Mikäli sinulla esiintyy näitä oireita, vältä autolla ajamista ja koneiden käyttöä.
Comtess sisältää soijalesitiiniä ja natriumia
Comtess sisältää soijalesitiiniä. Jos olet allerginen maapähkinälle tai soijalle, älä käytä tätä lääkevalmistetta.
Tämä lääke sisältää 7,9 mg natriumia (ruokasuolan toinen ainesosa) per tabletti. Korkein suositeltu annos (10 tablettia vuorokaudessa) sisältää 79 mg natriumia. Tämä vastaa 4 %:a suositellusta natriumin enimmäisvuorokausiannoksesta aikuiselle.
Miten valmistetta käytetään
Ota tätä lääkettä juuri siten kuin lääkäri on määrännyt. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma.
Comtessia käytetään yhdessä levodopaa sisältävien lääkkeiden kanssa (joko levodopa/karbidopa-valmisteiden tai levodopa/benseratsidi-valmisteiden). Voit myös käyttää muita Parkinsonin taudin hoitoon tarkoitettuja lääkkeitä samanaikaisesti.
Suositeltu Comtess-annos on yksi 200 mg:n tabletti jokaisen levodopa-annoksen yhteydessä. Korkein suositeltu annos on 10 tablettia päivässä eli 2 000 mg:aa Comtessia.
Jos olet dialyysihoidossa munuaisten vajaatoiminnan vuoksi, lääkärisi saattaa määrätä pidemmän annosvälin.
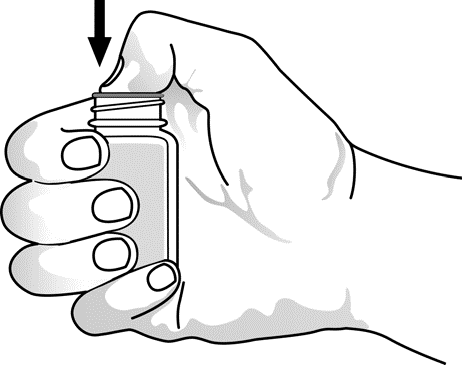
| Purkin avaaminen ensimmäistä kertaa: avaa turvasuljin ja paina sitten peukalolla sinettiä, kunnes se murtuu. Ks. kuva 1. |
Kuva 1 |
Käyttö lapsille ja nuorille
Kokemusta Comtessin käytöstä alle 18-vuotiailla potilailla on rajoitetusti. Sen vuoksi Comtessin käyttöä lapsilla tai nuorilla ei voida suositella.
Jos otat enemmän Comtess -valmistetta kuin sinun pitäisi
Yliannostustapauksessa ota välittömästi yhteys lääkäriin, apteekkihenkilökuntaan tai lähimpään sairaalaan.
Jos unohdat ottaa Comtess -valmistetta
Jos unohdat ottaa Comtess-tabletin levodopa-annoksen yhteydessä, jatka lääkitystä ottamalla seuraava Comtess-tabletti seuraavan levodopa-annoksen yhteydessä.
Älä ota kaksinkertaista annosta korvataksesi unohtamasi tabletin.
Jos lopetat Comtess -valmisteen käytön
Älä lopeta Comtess-hoitoa, ellei lääkäri näin määrää.
Hoidon lopettamisen yhteydessä lääkäri saattaa joutua muuttamaan muiden Parkinsonin taudin lääkkeiden annostusta. Comtessin ja muiden Parkinsonin taudin lääkkeiden käytön äkillinen lopettaminen voi aiheuttaa haittavaikutuksia. Ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä Varoitukset ja varotoimet.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa. Yleensä Comtessin aiheuttamat haittavaikutukset ovat lieviä tai keskivaikeita.
Jotkin haittavaikutuksista aiheutuvat usein levodopahoidon lisääntyneistä vaikutuksista ja ovat yleisimpiä hoidon alussa. Jos sinulla esiintyy sellaisia vaikutuksia Comtess-hoidon alussa sinun on otettava yhteyttä lääkäriisi, joka saattaa päättää muuttaa levodopa-annostustasi.
Hyvin yleinen (yli 1 käyttäjällä 10:stä)
- tahattomat liikkeet, jotka haittaavat tahdonalaisien liikkeiden suorittamista (dyskinesia)
- pahoinvointi
- vaaraton virtsan värjäytyminen punaruskeaksi.
Yleinen (enintään 1 käyttäjällä 10:stä)
- liialliset liikkeet (hyperkinesia), Parkinsonin taudin oireiden paheneminen, pitkittyneet lihaskouristukset (dystonia)
- oksentelu, ripuli, vatsakipu, ummetus, suun kuivuminen
- huimaus, väsymys, lisääntynyt hikoilu, kaatuminen
- hallusinaatiot (sellaisten asioiden näkeminen, kuuleminen, tunteminen, haistaminen, joita ei todellisuudessa ole), unettomuus, vilkkaat unet, sekavuus
- sydän- tai valtimosairaustapahtumat (esim. rintakipu).
Melko harvinainen (enintään 1 käyttäjällä 100:sta)
- sydänkohtaus.
Harvinainen (enintään 1 käyttäjällä 1 000:sta)
- ihottumat
- normaaliarvoista poikkeavia tuloksia maksan toimintakokeissa.
Hyvin harvinainen (enintään 1 käyttäjällä 10 000:sta)
- kiihtymys
- vähentynyt ruokahalu, painonlasku
- nokkosihottuma.
Tuntematon (saatavissa oleva tieto ei riitä esiintymistiheyden arviointiin)
- paksunsuolen tulehdus (koliitti), maksatulehdus (hepatiitti), johon liittyy ihon ja silmänvalkuaisten keltaisuus
- ihon, hiusten, parran ja kynsien värjääntyminen.
Kun Comtessia annostellaan korkeammilla annoksilla:
Annoksilla 1 400–2 000 mg päivässä voivat seuraavat haittavaikutukset olla yleisempiä
- tahattomat liikkeet
- pahoinvointi
- vatsakipu.
Muita tärkeitä haittavaikutuksia, joita voi esiintyä:
- Comtess levodopan kanssa otettuna voi harvoin aiheuttaa lisääntynyttä uneliaisuutta päiväsaikaan ja äkillisen nukahtamisen.
- Pahanlaatuinen neuroleptioireyhtymä (MNS) on harvinainen vakava reaktio lääkkeisiin, joita käytetään keskushermostohäiriöiden hoitoon. MNS:lle tyypillisiä piirteitä ovat jäykkyys, lihasnykäykset, vapina, kiihtymys ja sekavuus, kooma, kuume, nopeutunut pulssi ja epävakaa verenpaine.
- harvinainen ja vaikea lihassairaus (rabdomyolyysi), joka aiheuttaa kipua, arkuutta ja heikkoutta lihaksissa ja saattaa johtaa munuaisongelmiin.
Seuraavia haittavaikutuksia saattaa esiintyä:
- Hallitsematon tarve toimia mahdollisesti haitallisten mielijohteiden mukaan, kuten:
- voimakas pelihimo itselle tai perheelle aiheutuvista seurauksista huolimatta
- muuttunut tai lisääntynyt seksuaalinen mielenkiinto ja käyttäytyminen, esimerkiksi lisääntynyt seksuaalinen halu, joka haittaa merkittävästi sinua tai muita
- kontrolloimaton ja liiallinen ostelu tai tuhlaaminen
- ahmiminen (suurten ruokamäärien syöminen lyhyessä ajassa) tai pakkomielteinen syöminen (syöminen enemmän kuin normaalisti ja enemmän kuin on tarpeen).
Kerro lääkärille, jos sinulla on tällaista käyttäytymistä. Lääkäri keskustelee kanssasi oireiden hoito- tai vähentämiskeinoista.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös kansallisen ilmoitusjärjestelmän kautta. Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa ja etiketissä mainitun viimeisen käyttöpäivämäärän jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Tämä lääkevalmiste ei vaadi erityisiä säilytysolosuhteita.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Comtess sisältää
- Vaikuttava aine on entakaponi, jota on 200 mg:aa yhdessä tabletissa.
- Muut aineet tablettiytimessä ovat mikrokiteinen selluloosa, kroskarmelloosinatrium, povidoni ja magnesiumstearaatti.
- Muut aineet kalvopäällysteessä ovat osittain hydrolysoitu polyvinyylialkoholi, talkki, makrogoli, soijalesitiini, keltainen rautaoksidi (E 172), punainen rautaoksidi (E 172) ja titaanidioksidi (E 171).
Lääkevalmisteen kuvaus ja pakkauskoot
Comtess 200 mg kalvopäällysteinen tabletti on ruskehtavan-oranssi, ovaali tabletti, jonka toisella puolella on merkintä ”COMT”. Lääke on pakattu purkkiin.
Pakkauskokoja on neljä (30, 60, 100 tai 175 tabletin pakkaukset). Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija
Orion Corporation
Orionintie 1
FI-02200 Espoo
Suomi
Valmistaja
Orion Corporation Orion Pharma
Joensuunkatu 7
FI-24100 Salo
Suomi
Orion Corporation Orion Pharma
Orionintie 1
FI-02200 Espoo
Suomi
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
| België/Belgique/Belgien Orion Corporation Tél./Tel: +358 10 4261 | Lietuva UAB Orion Pharma Tel: +370 5 276 9499 |
България Orion Corporation Тел.: +358 10 4261 | Luxembourg/Luxemburg Orion Corporation Tél./Tel: +358 10 4261 |
Česká republika Orion Corporation Tel: +358 10 4261 | Magyarország Orion Corporation Tel.: +358 10 4261 |
| Danmark Orion Pharma A/S Tlf: +45 8614 0000 | Malta Orion Corporation Tel: +358 10 4261 |
Deutschland Orion Pharma GmbH Jürgen-Töpfer-Straße 46 22763 Hamburg Tel: +49 40 899 689-0 | Nederland Orion Corporation Tel: +358 10 4261 |
Eesti Orion Pharma Eesti OÜ Tel: +372 66 44 550 | Norge Orion Pharma AS Tlf.: +47 40 00 42 10 |
| Ελλάδα Orion Corporation Tηλ: +358 10 4261 | Österreich Orion Corporation Tel: +358 10 4261 |
| España Orion Corporation Tel: +358 10 4261 | Polska Orion Pharma Poland Sp. z o.o. Tel.: +48 22 8333177 |
| France Orion Corporation Tél.: +358 10 4261 | Portugal Orion Corporation Tel: +358 10 4261 |
Hrvatska Orion Corporation Tel: +358 10 4261 | România Orion Corporation Tel: +358 10 4261 |
Ireland Orion Pharma (Ireland) Ltd. c/o Allphar Services Ltd. Tel: +353 1 428 7777 | Slovenija Orion Corporation Tel: +358 10 4261 |
Ísland Vistor hf. Sími: +354 535 7000 | Slovenská republika Orion Corporation Tel: +358 10 4261 |
| Italia Orion Corporation Tel: +358 10 4261 | Suomi/Finland Orion Corporation Puh./Tel: +358 10 4261 |
Κύπρος Orion Corporation Tηλ: +358 10 4261 | Sverige Orion Pharma AB Tel: +46 8 623 6440 |
Latvija Orion Corporation Orion Pharma pārstāvniecība Tel: +371 20028332 |
Tämä pakkausseloste on tarkistettu viimeksi 09/2024
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivuilla https://www.ema.europa.eu .