Pakkausseloste
MONOPROST ögondroppar, lösning i endosbehållare 50 mikrog/ml
Tilläggsinformation
Monoprost 50 mikrogram/ml, ögondroppar, lösning i endosbehållare
latanoprost
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad Monoprost är och vad det används för
2. Vad du behöver veta innan du använder Monoprost
3. Hur du använder Monoprost
4. Eventuella biverkningar
5. Hur Monoprost ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Monoprost tillhör en grupp läkemedel som kallas prostaglandiner. Det sänker trycket i ditt öga genom att öka det naturliga utflödet av vätska från ögats insida ut i blodet.
Monoprost används för att behandla tillstånd som kallas öppenvinkelglaukom och okulär hypertension. Båda dessa tillstånd är förknippade med en ökning av trycket i ögat, som så småningom kan påverka synen.
Latanoprost som finns i Monoprost kan också vara godkänd för att behandla andra sjukdomar som inte nämns i denna produktinformation. Fråga läkare, apotekspersonal eller sjuksköterska om du har ytterligare frågor och följ alltid deras instruktion.
Vad du behöver veta innan produkten används
Använd inte Monoprost
- Om du är allergisk (överkänslig) mot latanoprost eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du använder Monoprost om du tror att något av det följande gäller dig:
- Om du ska genomgå eller har genomgått en ögonoperation (inklusive starroperation).
- Om du lider av ögonproblem (som ögonvärk, irritation eller inflammation, dimsyn).
- Om du har svår astma eller om din astma inte är välkontrollerad.
- Om du bär kontaktlinser. Du kan fortfarande använda Monoprost, men följ instruktionerna för kontaktlinsbärare i avsnitt Hur produkten används.
- Om du har haft eller har en virusinfektion i ögat orsakad av herpes simplex-virus (HSV).
Barn
Monoprost har inte studerats hos barn (under 18 år).
Andra läkemedel och Monoprost
Monoprost kan interagera med andra läkemedel. Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
Graviditet och amning
Använd inte Monoprost om du är gravid eller ammar.
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du använder detta läkemedel.
Körförmåga och användning av maskiner
När du använder Monoprost kan du få dimsyn. Om detta händer dig, kör inte eller använd inte verktyg eller maskiner förrän din syn blir klar igen.
Du är själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbeten som kräver skärpt uppmärksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användning av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med din läkare eller apotekspersonal om du är osäker.
Monoprost innehåller makrogolglycerolhydroxistearat
Monoprost innehåller makrogolglycerolhydroxistearat (från ricinolja) som kan orsaka hudreaktioner.
Hur produkten används
Vanlig dosering
- Använd alltid Monoprost enligt läkarens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
- Vanlig dos till vuxna (inklusive äldre) är en droppe dagligen i det påverkade ögat (ögonen). Den bästa tiden att göra detta är på kvällen.
- Använd inte Monoprost mer än en gång om dagen eftersom behandlingseffekten kan minskas om det används för ofta.
- Använd alltid Monoprost exakt enligt beskrivning i denna bipacksedel eller enligt anvisningar från läkare tills läkaren säger åt dig att sluta. Rådfråga läkare, apotekspersonal eller sjuksköterska om du är osäker.
Om du bär kontaktlinser
Om du använder kontaktlinser bör du ta bort dem innan du använder Monoprost. Efter att ha använt Monoprost ska du vänta 15 minuter innan du sätter tillbaka kontaktlinserna.
Instruktioner för användning
Ögondropparna tillhandahålls i endosbehållare. Påbörjade endosbehållare ska slängas genast efter användning. Eftersom sterilitet inte kan bibehållas efter öppnandet av endosbehållaren, måste en ny behållare öppnas före varje användning och slängas omedelbart efter administreringen.
Följ dessa instruktioner vid användning av ögondropparna:
1. Tvätta händerna och sitt eller stå bekvämt.
2. Öppna påsen. Skriv datumet för första öppnandet på påsen.
3. Bryt av en endosbehållare från remsan.
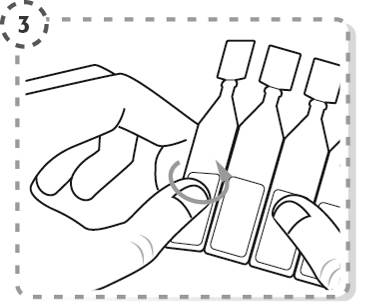
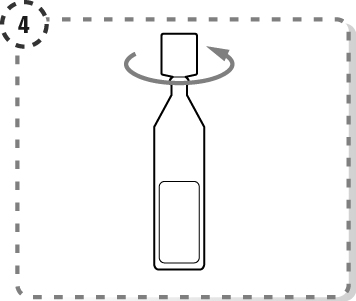
4. Vrid av toppen på endosbehållaren enligt bilden. Vidrör inte spetsen efter att endosbehållaren har öppnats.
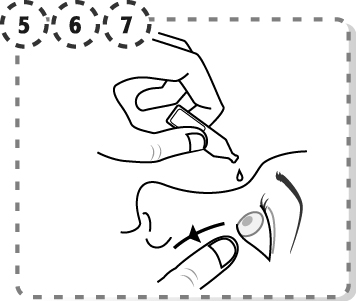
5. Använd ditt finger för att försiktigt dra ner det undre ögonlocket på det påverkade ögat.
6. Placera spetsen av endosbehållaren nära, men utan att vidröra ditt öga.
7. Kläm försiktigt på endosbehållaren så att endast en droppe kommer in i ögat, släpp sedan det undre ögonlocket.
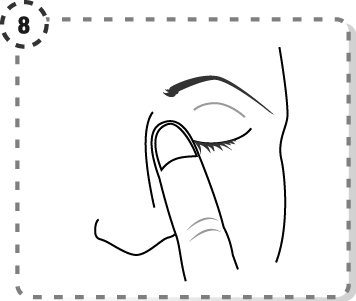
8. Tryck ett finger mot den inre ögonvrån, håll i 1 minut samtidigt som du blundar.
9. Upprepa i det andra ögat om din läkare har sagt till dig att göra detta. Varje endosbehållare innehåller tillräckligt med lösning för båda ögonen.
10. Släng endosbehållaren efter användning. Spar den inte för senare användning. En ny endosbehållare måste öppnas vid varje tillfälle då ögonen ska droppas, eftersom lösningen inte förblir steril efter att endosbehållaren öppnats.
Om du använder Monoprost med andra ögondroppar
Vänta minst 5 minuter mellan användning av Monoprost och användning av andra ögondroppar.
Om du har använt för stor mängd av Monoprost
Om du tillsätter för många droppar i ögat kan du känna viss lättare irritation i ögat och dina ögon kan tåras och bli röda, detta borde gå över, men om du är orolig, kontakta läkare för rådgivning.
Om Monoprost sväljs av misstag, bör du kontakta din läkare så snart som möjligt.
Om du fått i dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedlet av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel. 0800 147 111) för bedömning av risken samt rådgivning.
Om du har glömt att ta Monoprost
Fortsätt med den vanliga doseringen när det är dags för nästa dos. Ta inte dubbel dos för att kompensera för glömd dos. Om du är osäker, kontakta läkare eller apotekspersonal för rådgivning.
Om du slutar att använda Monoprost
Du ska prata med din läkare om du vill sluta använda Monoprost.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare, apotekspersonal eller sjuksköterska.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Följande biverkningar är kända vid användning av Monoprost:
Mycket vanliga (förekommer hos fler än 1 av 10 användare):
- Gradvis förändring av ögonfärgen genom en ökning av mängden brunt pigment i den färgade delen av ögat (iris).
- Om du har melerad ögonfärg (blåbruna, gråbruna, gulbruna eller grönbruna) är det mer sannolikt att du ser denna förändring än om du har enfärgade ögon (blåa, gråa, gröna eller bruna ögon).
- Förändringar av din ögonfärg kan ta åratal att utvecklas även om det normalt uppträder inom de åtta första behandlingsmånaderna.
- Färgförändringen kan vara permanent och kan vara mer märkbar om du använder Monoprost i endast ett öga.
- Det verkar inte finnas några andra problem förknippade med förändringen av ögonfärg.
- Förändringen i ögonfärg fortsätter inte efter avslutad behandling med Monoprost.
- Röda ögon.
- Ögonirritation (en brännande känsla, känsla av grynighet, klåda, sveda eller en känsla av att ha något främmande föremål i ögat).
- Gradvis förändring av ögonfransar vid det behandlade ögat och de fina hårstråna runt det behandlade ögat, mestadels sett hos individer av japanskt ursprung. Dessa förändringar omfattar ökning av färgen (förmörkning), längd, tjocklek och antal ögonfransar.
Vanliga (förekommer hos upp till 1 av 10 användare):
- Irritation eller skada på ytan av ögat, ögonlocksinflammation (blefarit), ögonsmärta, ljuskänslighet (fotofobi), inflammation i ögats bindhinna (konjunktivit).
Mindre vanliga (förekommer hos upp till 1 av 100 användare):
- Svullna ögonlock, torra ögon, inflammation eller irritation på ytan av ögat (keratit), dimsyn, inflammation i den färgade hinnan av ögat (uveit), svullnad av näthinnan (makulärt ödem).
- Hudutslag.
- Kärlkramp (angina pectoris) och medvetenhet om hjärtrytmen (hjärtklappning).
- Astma, andnöd (dyspné).
- Bröstsmärta.
- Huvudvärk, yrsel.
- Muskel- och ledvärk.
- Illamående, kräkning.
Sällsynta (förekommer hos upp till 1 av 1000 användare):
- Inflammation i iris (irit), symtom på svullnad eller skada på ögats yta, svullnad runt ögonen (periorbitalt ödem) inåtväxande ögonfransar eller en extra rad av ögonfransar, vätskefyllt område inom det färgade området av ögat (iriscysta).
- Hudutslag på ögonlock, mörkfärgning av huden på ögonlocken.
- Förvärrade astmasymtom.
- Svår klåda i huden.
- Utveckling av en ögoninfektion orsakad av herpes simplex-virus (HSV).
Mycket sällsynta (förekommer hos upp till 1 av 10000 användare):
- Förvärrad kärlkramp (angina pectoris) hos patienter som även har hjärtsjukdom, insjunkna ögon (fördjupning av ögonfåran).
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
Webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
FI-00034 Fimea
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på ytterkartongen, påsen och endosbehållaren efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras vid högst 25 °C.
Efter att påsen öppnats: Använd endosbehållarna inom 10 dagar.
Kassera öppnad endosbehållare och eventuellt kvarbliven lösning omedelbart efter första användning.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är latanoprost.
- En ml lösning innehåller 50 mikrogram latanoprost.
- Övriga innehållsämnen är makrogolglycerolhydroxistearat 40, sorbitol, karbomer 974P, makrogol 4000, dinatriumedetat, natriumhydroxid (för pH-justering), vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar
Monoprost ögondroppar, lösning i endosbehållare är en svagt gul, pärlemorskimrande lösning, utan konserveringsmedel, förpackad i påsar om 5 eller 10 endosbehållare.
Varje endosbehållare innehåller 0,2 ml.
Förpackningsstorlekar: Kartonger med påsar om 5 (1 x 5), 10 (2 x 5), 10 (1 x 10), 30 (6 x 5), 30 (3 x 10), 90 (18 x 5) eller 90 (9 x 10) endosbehållare.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning och tillverkare
Innehavare av godkännande för försäljning
Laboratoires THEA
12 rue Louis Blériot
63017 Clermont-Ferrand Cedex 2
Frankrike
Tillverkare
Excelvision
27, Rue de la Lombardière
Zi la Lombardière
07100 Annonay
Frankrike
Eller
Laboratoires THEA
12 rue Louis Blériot
63017 Clermont-Ferrand Cedex 2
Frankrike
Eller
Laboratoire Unither
1 rue de l’Arquerie
50200 Coutances
Frankrike
Lokal företrädare:
Théa Nordic AB, Frösundaviks Allé 1, 169 70 Solna, Sverige
info.nordic@theapharma.com
Denna bipacksedel ändrades senast 07.03.2025
Ytterligare information om detta läkemedel finns på Fimeas webbplats www.fimea.fi.