PRIORIX pulver och vätska till injektionsvätska, lösning
Tilläggsinformation
Priorix, pulver och vätska till injektionsvätska, lösning i förfylld spruta
Vaccin mot mässling, påssjuka och röda hund, levande
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du får detta vaccin. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta vaccin har ordinerats enbart åt dig. Ge det inte till andra.
- Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
Denna bipacksedel har skrivits under förutsättningen att personen som får vaccinet är den som läser den. Men vaccinet kan ges till vuxna och barn så att du kan läsa den för ditt barn.
I denna bipacksedel finns information om följande
1. Vad Priorix är och vad det används för
2. Vad du behöver veta innan du får Priorix
3. Hur Priorix ges
4. Eventuella biverkningar
5. Hur Priorix ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Priorix är ett vaccin som används till barn från 9 månader och uppåt, ungdomar och vuxna för att skydda mot mässling, påssjuka och röda hund.
Hur Priorix verkar
När en person vaccinerats med Priorix bildar immunsystemet (kroppens naturliga försvarssystem) antikroppar som skyddar personen från att bli infekterad av virus som orsakar mässling, påssjuka och röda hund.
Trots att Priorix innehåller levande virus är dessa virus för svaga för att orsaka mässling, påssjuka eller röda hund hos friska människor.
Vad du behöver veta innan produkten används
Priorix ska inte ges om
- du är allergisk mot något av innehållsämnena i detta vaccin (anges i avsnitt Förpackningens innehåll och övriga upplysningar). Tecken på en allergisk reaktion kan vara kliande hudutslag, andfåddhet och svullnad av ansikte eller tunga,
- du har en känd allergi mot neomycin (ett antibiotikum). Känd kontaktdermatit (hudutslag då huden kommer i direkt kontakt med allergenet, till exempel neomycin) bör inte vara något problem, men tala med läkaren först,
- du har en svår infektion med hög feber. I dessa fall ska vaccinationen skjutas upp till efter tillfrisknande. En lättare infektion såsom en förkylning bör inte vara något problem, men tala med läkaren först,
- du har någon sjukdom (t.ex. humant immunbristvirus (HIV) eller förvärvat immunbristsyndrom (AIDS)) eller har nyligen tagit eller tar någon medicin som försvagar immunsystemet (förutom lågdos kortikosteroidbehandling för astma eller substitutionsbehandling). Om du får vaccinet beror på ditt immunförsvars nivå,
du är gravid. Dessutom bör graviditet undvikas under 1 månad efter vaccination.
Varningar och försiktighet
Tala med läkare eller apotekspersonal innan du får Priorix om:
- om du har någon neurologisk sjukdom, har haft feberkramper eller om någon annan i familjen har haft kramper. Vid hög feber efter vaccinationen kontakta omedelbart din läkare för råd,
- du tidigare fått en allvarlig allergisk reaktion mot äggprotein,
- du efter vaccination mot mässling, påssjuka eller röda hund tidigare fått en biverkning som gjorde det lättare att få blåmärken eller gav förlängd blödningstid (se avsnitt Eventuella biverkningar),
- du har ett nedsatt immunförsvar (t.ex. HIV-infektion) eller ska påbörja en behandling med en medicin som försvagar immunsystemet. Du ska kontrolleras noggrant då svaret på vaccin kanske inte är tillräckligt för att säkerställa skydd mot sjukdomen (se avsnitt Vad du behöver veta innan produkten används ”Priorix ska inte ges om”).
Svimning kan förekomma (främst hos ungdomar) efter, eller även före, all nålinjektion. Tala därför om för läkaren eller sjuksköterskan om du har svimmat vid tidigare injektion.
Om du vaccineras inom 72 timmar efter kontakt med någon med mässling skyddar Priorix dig mot sjukdomen i viss utsträckning.
Barn under 12 månaders ålder
Barn som vaccineras under sitt första levnadsår får eventuellt inte fullständigt skydd. Läkaren ger råd om ytterligare vaccindoser behövs.
Liksom för alla vacciner ger Priorix eventuellt inte fullständigt skydd hos alla vaccinerade.
Andra läkemedel och Priorix
Tala om för läkare om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel (eller vacciner).
Priorix kan ges samtidigt som du får andra vacciner som t.ex. difteri-, tetanus-, pertussis (acellulär)-, Haemophilus influenzae typ b-, oralt eller inaktiverat polio-, hepatit A och B-vaccin, varicella-, meningokock serogrupp B-vacciner samt meningokock serogrupp C-, meningokock serogrupperna A-, C-, W-135- och Y-vacciner samt konjugatvaccin mot pneumokocker. Vänd dig till läkare eller sjukskötare för mera information.
Varje injektion ska ges på olika injektionsställen.
Om vaccinerna inte ges samtidigt rekommenderas ett intervall på minst en månad mellan administrering av Priorix och andra levande försvagade vacciner.
Din läkare kan komma att skjuta upp vaccinationen med minst 3 månader om du nyligen fått en blodtransfusion eller humana antikroppar (immunglobuliner).
Om tuberkulinprov ska utföras bör det göras antingen före, samtidigt eller tidigast 6 veckor efter vaccination med Priorix.
Graviditet, amning och fertilitet
Priorix ska inte ges till gravida kvinnor.
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du tar detta vaccin. Det är även viktigt att du inte blir gravid inom en månad efter att du fått vaccinet. Under denna tid ska du använda ett effektivt preventivmedel för att undvika graviditet.
Priorix innehåller sorbitol, para-aminobensoesyra, fenylalanin, natrium och kalium
Detta läkemedel innehåller 9 mg sorbitol per dos.
Priorix innehåller para-aminobensoesyra som kan ge allergisk reaktion (eventuellt fördröjd) och undantagsvis kramp i luftrören.
Detta vaccin innehåller 334 mikrogram fenylalanin per dos. Fenylalanin kan vara skadligt om du har fenylketonuri (PKU), en sällsynt, ärftlig sjukdom som leder till ansamling av höga halter av fenylalanin i kroppen.
Detta vaccin innehåller mindre än 1 mmol (23 mg) natrium per dos, d.v.s. är näst intill “natriumfritt”.
Detta vaccin innehåller mindre än 1 mmol (39 mg) per dos kalium, d.v.s är näst intill “kaliumfritt”.
Hur produkten används
Priorix injiceras under huden eller i en muskel, antingen i övre armen eller yttre låret.
Priorix är avsett för barn från 9 månaders ålder och uppåt, ungdomar och vuxna.
Läkaren bestämmer lämplig tidpunkt och antal injektioner som ges till dig baserat på gällande officiella rekommendationer.
Vaccinet ska aldrig ges i en ven.
Eventuella biverkningar
Liksom alla läkemedel kan detta vaccin orsaka biverkningar, men alla användare behöver inte få dem.
Vid kliniska studier med Priorix rapporterades följande biverkningar:
Mycket vanliga (dessa kan förekomma vid fler än 1 av 10 vaccindoser):
- rodnad vid injektionsstället
- feber (38 °C eller högre).
Vanliga (dessa kan förekomma vid upp till 1 av 10 vaccindoser):
- smärta och svullnad vid injektionsstället
- feber (över 39,5 °C)
- hudutslag
- infektioner i övre luftvägarna.
Mindre vanliga (dessa kan förekomma vid upp till 1 av 100 vaccindoser):
- infektioner i mellanörat
- svullna lymfkörtlar (körtlar i nacke, armhåla och ljumske)
- aptitlöshet
- oro
- ihållande gråt
- sömnlöshet (insomni)
- röda, irriterade och rinnande ögon (konjunktivit)
- bronkit
- hosta
- svullna öronspottkörtlar (körtlar i kinden)
- diarré
- kräkning.
Sällsynta (dessa kan förekomma vid upp till 1 av 1 000 vaccindoser):
- kramper i samband med hög feber
- allergiska reaktioner.
Efter lansering av Priorix har vid några få tillfällen följande biverkningar rapporterats:
- smärta i leder och muskler
- punktvisa småblödningar i huden eller lättare att få blåmärken än normalt på grund av minskat antal blodplättar
- plötsligt livshotande allergisk reaktion
- infektion eller inflammation i hjärnan, ryggmärgen och perifera nerver, vilket leder till tillfälliga svårigheter att gå (ostadigheter) och/eller tillfälligt förlorad kontroll över kroppsrörelser, inflammation av vissa nerver, eventuellt med myrstickningar eller förlorad känsel eller förlust av normal rörlighet (Guillain-Barrés syndrom)
- förträngning eller blockering av blodkärl
- erythema multiforme (symtom är röda, ofta kliande fläckar liknande mässlingsutslag som börjar på armarna eller benen och ibland i ansiktet och på övriga kroppen)
- mässling- eller påssjukeliknande symtom (inklusive övergående, smärtsam svullnad av testiklarna och svullna körtlar i nacken).
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på kartongen efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras och transporteras kallt (2 °C – 8 °C).
Får ej frysas.
Förvaras i originalkartongen. Ljuskänsligt.
Vaccinet ska injiceras omedelbart efter färdigställande. Om detta inte är möjligt ska det förvaras vid 2 °C – 8 °C (i kylskåp) och användas inom 8 timmar efter färdigställande.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
De aktiva substanserna är: levande försvagade mässlingvirus, påssjukevirus och röda hundvirus.
Övriga innehållsämnen är:
Pulver: aminosyror (innehåller fenylalanin), laktos (vattenfritt), mannitol (E 421), sorbitol (E 420), medium 199 (innehåller fenylalanin, para-aminobensosyra, natrium och kalium).
Spädningsvätska: vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar
Priorix tillhandahålls som ett pulver och vätska för injektionsvätska, lösning i en förfylld spruta (pulver i en injektionsflaska för en dos och spädningsvätska i en förfylld spruta) (0,5 ml) med eller utan nålar i följande förpackningsstorlekar:
- med 2 separata nålar: förpackningar om 1 eller 10
- utan nål: förpackningar om 1 eller 10.
Priorix tillhandahålls som en vitaktig till svagt rosafärgad pulverkaka, som delvis kan vara gulaktig eller svagt orange, och en klar färglös spädningsvätska (vatten för injektionsvätskor) för beredning av vaccinet.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning och tillverkare
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart
Belgien
Ytterligare upplysningar om detta läkemedel erhålls hos den nationella representanten för innehavaren av godkännandet för försäljning.
GlaxoSmithKline Oy
Porkalagatan 20 A
00180 Helsingfors
Tfn. +358 10 30 30 30
Denna bipacksedel ändrades senast 25.2.2026
Övriga informationskällor
Ytterligare information om detta läkemedel finns på webbplatsen www.fimea.fi.
Direktiv för experterna inom hälsovården
Som med alla vacciner för injektion ska lämplig beredskap för medicinsk behandling och övervakning finnas lätt tillgänglig i händelse av sällsynt anafylaktisk reaktion efter administrering av vaccinet.
För att undvika inaktivering av de försvagade virus som finns i vaccinet ska alkohol och andra desinfektionsmedel avdunsta från huden före injektion.
Priorix får under inga omständigheter administreras intravaskulärt.
Då blandbarhetsstudier saknas ska detta vaccin inte blandas med andra läkemedel.
Spädningsvätskan och det färdigberedda vaccinet ska inspekteras visuellt med avseende på främmande partiklar och/eller fysikaliska förändringar före beredning eller administrering. Om sådana förändringar observeras ska spädningsvätskan eller det färdigberedda vaccinet inte användas.
Vaccinet bereds genom att all spädningsvätska i den förfyllda sprutan överförs till injektionsflaskan med pulver.
Läs noggrant instruktionerna som ges till bilderna 1 och 2 när nålen ska fästas på sprutan. Den spruta som följer med Priorix kan dock skilja sig något (utan skruvgäng) från den spruta som ses på bilden. I så fall ska nålen fästas utan att skruvas.
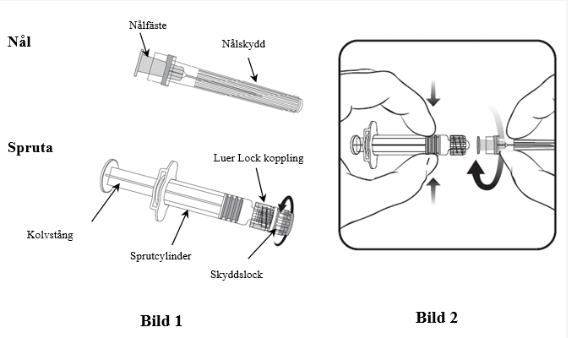
Håll alltid i sprutcylindern, inte i kolvstången eller Luer Lock kopplingen (LLA), och håll nålen i linje med sprutan (såsom visas på den Bild 2). Om du inte gör detta kan Luer Lock kopplingen bli förvrängd och läcka.
Om Luer Lock kopplingen faller av under monteringen ska en ny vaccindos (ny spruta och injektionsflaska) användas.
1. Skruva av skyddslock genom att vrida den motsols (såsom visas på Bild 1)
Oavsett om Luer Lock kopplingen roterar eller inte, följ nedanstående steg:
2. Fäst nålen på sprutan genom att försiktigt ansluta den till Luer Lock kopplingen och rotera ett kvarts varv medsols tills du känner ett klick (såsom visas på den Bild 2).
3. Ta bort nålskyddet, som i vissa fall kan sitta lite hårt.
4. Överför spädningsvätskan till pulvret. Blandningen ska omskakas väl tills allt pulver har lösts fullständigt i spädningsvätskan.
Det färdigberedda vaccinet kan variera i färg från klar persikofärgad till fuchsia rosa på grund av mindre pH-variationer. Detta påverkar inte vaccinets effekt.
5. Dra upp injektionsflaskans hela innehåll i sprutan.
6. En ny nål ska användas för administrering av vaccinet. Skruva av nålen från sprutan och fäst injektionsnålen genom att repetera steg 2 ovan.
Vaccinet ska administerasomedelbart efter färdigställande. Om detta ej är möjligt ska det förvaras i kylskåp (2 °C – 8 °C) och användas inom 8 timmar efter upplösning.
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.