Pakkausseloste
MITOMYCIN MEDAC jauhe ja liuotin liuosta varten, virtsarakkoon 40 mg
Mitomycin medac, 40 mg, jauhe ja liuotin liuosta varten, virtsarakkoon
mitomysiini
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin aloitat lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
• Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
• Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
• Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä Mitomycin medac on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin käytät Mitomycin medac -valmistetta
3. Miten Mitomycin medac -valmistetta käytetään
4. Mahdolliset haittavaikutukset
5. Mitomycin medac -valmisteen säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Mitomycin medac on syöpälääke (sytostaatti), eli se estää tai viivästyttää merkittävästi aktiivisten solujen jakautumista vaikuttamalla eri tavoin niiden aineenvaihduntaan. Hoito syöpälääkkeillä perustuu siihen, että syöpäsolut jakautuvat normaaleihin soluihin verrattuna nopeammin, koska niiden kasvua ei voi hallita.
Käyttöaiheet
Valmistetta käytetään virtsarakon sisäisesti (intravesikaalisesti) pinnallisen virtsarakon syövän uusiutumisen ehkäisemiseksi sen jälkeen, kun syövän vaurioittamaa kudosta on poistettu virtsaputken kautta (transuretraalinen resektio).
Mitomysiiniä, jota Mitomycin medac sisältää, voidaan joskus käyttää myös muiden kuin tässä pakkausselosteessa mainittujen sairauksien hoitoon. Kysy neuvoa lääkäriltä, apteekkihenkilökunnalta tai muulta terveydenhuollon ammattilaiselta tarvittaessa ja noudata aina heiltä saamiasi ohjeita.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Mitomysiiniä saa käyttää ainoastaan tarkasti käyttöaiheiden mukaisesti ja lääkärien toimesta, joilla on kokemusta tämän tyyppisestä hoidosta.
Älä käytä Mitomycin medac –valmistetta
• jos olet allerginen mitomysiinille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa),
• imetyksen aikana: sinä et saa imettää mitomysiinihoidon aikana,
• jos virtsarakkosi seinämä on puhjennut,
• jos sinulla on virtsarakon tulehdus (kystiitti).
Varoitukset ja varotoimet
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin käytät Mitomycin medac ‑valmistetta.
Erityistä varovaisuutta on noudatettava käytettäessä Mitomycin medac ‑valmistetta
- jos yleinen terveydentilasi on heikko,
- jos sinulla on keuhkojen, maksan tai munuaisten toimintahäiriö,
- jos saat sädehoitoa,
- jos sinua hoidetaan muilla sytostaateilla (solujen kasvua ja jakaantumista estävillä aineilla),
- jos sinulle on kerrottu että sinulla on luuydindepressio (eli luuytimesi ei pysty valmistamaan tarvitsemiasi verisoluja). Se saattaa pahentua (erityisesti jos olet iäkäs tai saat mitomysiinihoitoa pitkään); infektio saattaa pahentua vähäisen solumäärän vuoksi ja voi aiheuttaa kuolemaan johtavia tiloja,
- jos kykenet tulemaan raskaaksi, sillä mitomysiini saattaa vaikuttaa kykyysi saada lapsia tulevaisuudessa.
Jos sinulle tulee vatsan tai lantion alueen kipua heti sen jälkeen, kun Mitomycin medac ‑valmistetta on annettu virtsarakkoon, tai useiden viikkojen tai kuukausien kuluttua valmisteen antamisesta, kerro asiasta heti lääkärille. Lääkärin on ehkä tehtävä vatsan alueen kaikukuvaus kipujesi syyn selvittämiseksi.
Mitomysiini on aine, joka voi aiheuttaa merkitseviä periytyviä muutoksia perimään, ja se voi mahdollisesti aiheuttaa syöpää ihmisille.
Vältä kosketusta ihoon ja limakalvoille.
Lue ohjeet, jotka koskevat koskien yleistä hygieniaa virtsarakkoon tapahtuvan annon jälkeen:
On suositeltavaa virtsata istuen, jotta virtsaa ei roisku sekä pestä kädet ja sukuelinten alue virtsaamisen jälkeen. Tämä koskee erityisesti ensimmäistä virtsauskertaa mitomysiinin annon jälkeen.
Lapset ja nuoret
Mitomycin medac ‑valmisteen käyttöä lapsille ja nuorille ei suositella.
Muut lääkevalmisteet ja Mitomycin medac
Yhteisvaikutuksia muiden lääkevalmisteiden kanssa ei tiedetä olevan, jos mitomysiiniä annetaan virtsarakkoon (intravesikaalinen anto).
Injektiona tai infuusiona suoneen (laskimoon) tapahtuvan annon jälkeiset mahdolliset haittavaikutukset
Käytettäessä muita hoitomuotoja (etenkin muita syöpälääkkeitä, sädehoitoa), jotka myös vaikuttavat haitallisesti luuytimeen kun niitä käytetään samanaikaisesti, on mahdollista, että luuytimeen kohdistuva haitallinen vaikutus voimistuu.
Yhdistelmä vinka-alkaloidien tai bleomysiinin (sytostaattien ryhmään kuuluvien lääkkeiden) kanssa voi voimistaa keuhkoihin kohdistuvaa haitallista vaikutusta.
Munuaissairauden erityisen muodon (hemolyyttis-ureeminen oireyhtymä) lisääntynyttä riskiä on ilmoitettu esiintyneen potilailla, jotka ovat saaneet samanaikaisesti laskimoon annettua mitomysiiniä ja 5-fluorourasiiliä tai tamoksifeeniä.
Eläimillä tehdyistä tutkimuksista on raportoitu, että mitomysiinin vaikutus häviää, jos sitä annetaan yhdessä B6-vitamiinin kanssa.
Sinua ei saa rokottaa elävillä rokotteilla mitomysiinihoidon aikana, koska silloin elävän rokotteen aiheuttaman infektion riski saattaa lisääntyä.
Adriamysiinin (doksorubisiinin, sytostaattien ryhmään kuuluvan lääkkeen) haitallinen vaikutus sydämeen voi voimistua mitomysiinin ansiosta.
Raskaus, imetys ja hedelmällisyys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
Raskaus
Mitomysiini voi aiheuttaa perinnöllisen vaurion perimään ja sillä voi olla haitallista vaikutusta alkion kehitykseen.
Sinun ei pidä tulla raskaaksi mitomysiinihoidon aikana. Jos tulet raskaaksi, sinulle pitää tarjota perinnöllisyysneuvontaa. Sinun ei pidä käyttää mitomysiiniä raskauden aikana.
Lääkärin täytyy arvioida hoidon hyödyt verrattuna lapseen kohdistuvien haitallisten vaikutusten riskiin, jos mitomysiinihoito on tarpeen raskauden aikana.
Imetys
On todennäköistä, että mitomysiini kulkeutuu ihmisen rintamaitoon. Rintaruokinta on lopetettava Mitomycin medac -hoidon ajaksi.
Hedelmällisyys/ehkäisy miehille ja naisille
Jos olet sukukypsässä iässä oleva potilas, sinun on käytettävä ehkäisymenetelmiä tai luovuttava seksuaalisesta kanssakäymisestä solunsalpaajahoidon ajaksi ja 6 kuukauden ajaksi hoidon jälkeen.
Mitomysiini voi aiheuttaa perinnöllisen vaurion perimään. Jos olet mitomysiinihoitoa saava mies, sinua neuvotaan sen vuoksi olemaan siittämättä lasta hoidon ajan ja 6 kuukauden ajan hoidon jälkeen, sekä hakemaan ohjeita sperman säilyttämistä varten ennen hoidon aloittamista sillä mitomysiinihoito saattaa aiheuttaa palautumatonta hedelmättömyyttä.
Ajaminen ja koneiden käyttö
Ohjeiden mukaisestikin käytettynä tämä lääke voi aiheuttaa pahoinvointia ja oksentelua ja siten lyhentää reaktionopeutta sellaisessa määrin, että ajokyky tai koneiden käyttökyky heikkenee. Tämä pätee erityisesti, jos käytät samanaikaisesti alkoholia.
Miten valmistetta käytetään
Mitomycin medac -valmistetta saavat antaa vain koulutetut hoitoalan ammattilaiset.
Tämä lääke on tarkoitettu käytettäväksi virtsarakkoon (rakonsisäisenä instillaationa) liuottamisen jälkeen.
Lääkäri määrää sinulle sopivan annoksen.
Mitomycin medac viedään tyhjään virtsarakkoon alhaisella paineella katetrin avulla. Terveydenhuollon ammattilainen tyhjentää virtsarakkosi katetrilla ennen hoitoa. Älä käy wc:ssä juuri ennen käyntiä terveydenhuollon ammattilaisen luona. Lääkkeen pitää pysyä rakossa 1‑2 tunnin ajan. Jotta tämä onnistuisi, sinun ei pidä juoda liikaa nestettä ennen hoitoa, sen aikana eikä jälkeen. Liuoksen ollessa virtsarakossasi sen on oltava riittävässä kosketuksessa rakon koko limakalvopintaan, ja liikkuminen auttaa hoidon onnistumisessa. Tyhjennä rakko 2 tunnin kuluttua istuma-asennossa roiskumisen välttämiseksi.
Jos käytät enemmän Mitomycin medac ‑valmistetta kuin sinun pitäisi
Jos sinulle on vahingossa annettu määrättyä suurempi annos mitomysiiniä, saatat saada oireita, kuten kuumetta, pahoinvointia, oksentelua ja verihäiriöitä. Lääkäri saattaa antaa sinulle tukihoitoa mahdollisten oireiden hoitamiseksi.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Jos olet ottanut liian suuren lääkeannoksen tai vaikkapa lapsi on ottanut lääkettä vahingossa, ota aina yhteyttä lääkäriin, sairaalaan tai Myrkytystietokeskukseen (puh. 0800 147 111) riskien arvioimiseksi ja lisäohjeiden saamiseksi.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Virtsarakkoon instillaation jälkeen esiintyvät mahdolliset haittavaikutukset
Kerro heti lääkärille, jos huomaat minkä tahansa seuraavista reaktioista (joita on havaittu hyvin harvoin virtsarakkoon instillaation jälkeen), sillä mitomysiinihoito täytyy silloin lopettaa:
• vaikea allerginen reaktio, jonka oireita ovat esim. pyörrytys, ihottuma tai nokkosihottuma, kutina, huulten, kasvojen ja hengitysteiden turvotus, johon liittyy hengitysvaikeuksia, tajuttomuutta,
• vaikea keuhkosairaus, jonka oireita ovat hengästyneisyys, kuiva yskä ja rahinat sisään hengittäessä (interstitiaalinen keuhkosairaus),
• vaikea munuaisten vajaatoiminta: munuaissairaus, jolloin virtsaaminen on vähäistä tai puuttuu kokonaan.
Yleiset: saattaa esiintyä enintään yhdellä 10:stä henkilöstä
• virtsarakon tulehdus (kystiitti), johon saattaa liittyä verta virtsarakossa/virtsassa
• kivulias virtsaaminen (dysuria)
• tiheä virtsaamistarve yöllä (nokturia)
• liiallinen tiheä virtsaaminen (pollakisuria)
• verta virtsassa (hematuria)
• virtsarakon seinämän paikallinen ärsytys
• paikallinen ihottuma (paikallinen eksanteema)
• allerginen ihottuma
• mitomysiini-kontaktista aiheutuva ihottuma (kosketusdermatiitti)
• kämmenien ja jalkapohjien puutuminen, turvotus ja kivulias punaisuus (palmaaris-plantaarinen eryteema)
Harvinaiset: saattaa esiintyä enintään yhdellä 1 000:sta henkilöstä
• ihottumaa koko kehossa (yleistynyt eksanteema)
Hyvin harvinaiset: saattaa esiintyä enintään yhdellä 10 000:sta henkilöstä
• virtsarakon tulehdus, johon liittyy virtsarakon kudoksen vaurio (nekrotisoiva kystiitti)
• allerginen (eosinofiilinen) virtsarakon tulehdus (kystiitti)
• virtsateiden ahtauma (stenoosi)
• virtsarakon pienentynyt kapasiteetti
• kalsiumin aiheuttamat kovettumat virtsarakon seinämässä (virtsarakon seinämän kalsifikaatio)
• virtsarakon seinämän kudoksen osittainen muuttuminen sidekudokseksi (virtsarakon seinämän fibroosi)
• valkosolujen määrän vähentyminen (leukopenia), joka lisää infektioiden riskiä
• verihiutaleiden määrän vähentyminen (trombopenia), joka aiheuttaa mustelmia ja verenvuotoa
• systeemiset allergiset reaktiot
• keuhkosairaus, jonka oireita ovat hengästyneisyys, kuiva yskä ja rahinat sisään hengittäessä (interstitiaalinen keuhkosairaus)
• kohonnut maksaentsyymien taso (kohonneet transaminaasit)
• hiustenlähtö (alopesia)
• pahoinvointi ja oksentelu
• ripuli
• munuaistauti (munuaisten vajaatoiminta) jolloin virtsaaminen on vähäistä tai puuttuu kokonaan
• kuume
Tuntematon: koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin
Jos mitomysiiniä pääsee vahingossa muualle kuin virtsarakkoon:
• virtsarakon vaurio
• märkäpesäke (absessi) vatsassa
• (rasva-) kudoksen kuolio (nekroosi) ympäröivällä alueella
• virtsarakkofisteli.
Injektiona tai infuusiona verisuoneen (laskimoon) tapahtuvan annon jälkeiset mahdolliset haittavaikutukset
Hyvin yleiset: saattaa esiintyä useammalla kuin yhdellä 10:stä henkilöstä
• verisolujen tuoton estyminen luuytimessä (luuydinsuppressio)
• valkosolujen määrän vähentyminen (leukopenia), joka lisää infektioiden riskiä
• verihiutaleiden määrän vähentyminen (trombopenia), joka aiheuttaa mustelmia ja verenvuotoa
• pahoinvointi ja oksentelu
Yleiset: saattaa esiintyä enintään yhdellä 10:stä henkilöstä
• keuhkosairaus, jonka oireita ovat hengästyneisyys, kuiva yskä ja rahinat sisään hengittäessä (interstitiaalinen keuhkosairaus)
• hengitysvaikeudet (dyspnea), yskä, hengästyneisyys
• ihottuma (eksanteema)
• allerginen ihottuma
• mitomysiini-kontaktista aiheutuva ihottuma (kosketusdermatiitti)
• kämmenien ja jalkapohjien puutuminen, turvotus ja kivulias punaisuus (palmaaris-plantaarinen eryteema)
• munuaissairaudet (munuaisten vajaatoiminta, nefrotoksisuus, glomerulopatia, kreatiniinin tason kohoaminen veressä) jolloin virtsaaminen on vähäistä tai puuttuu kokonaan
Jos mitomysiiniä injektoidaan tai jos sitä vuotaa ympäröivään kudokseen (ekstravasaatio)
• sidekudoksen tulehdus (selluliitti)
• kudoskuolema (kudosnekroosi)
Melko harvinaiset: saattaa esiintyä enintään yhdellä 100:sta henkilöstä
• limakalvotulehdus (mukosiitti)
• suun limakalvojen tulehdus (stomatiitti)
• ripuli
• hiustenlähtö (alopesia)
• kuume
• ruokahaluttomuus
Harvinaiset: saattaa esiintyä enintään yhdellä 1 000:sta henkilöstä
• henkeä uhkaava infektio
• verenmyrkytys (sepsis)
• vähentynyt määrä punaisia verisoluja näiden solujen poikkeavan hajoamisen vuoksi (hemolyyttinen anemia)
• mustelmat (purppura) ja punaiset ja purppuranväriset täplät (pienet verenpurkaumat) iholla (tromboottinen trombosytopeeninen purppura)
• sydämen vajaatoiminta aikaisempien syöpälääkkeiden (antrasykliinien) käytön vuoksi
• keuhkoverenpaineen nousu aiheuttaen esim. hengästyneisyyttä, huimausta ja pyörrytystä (pulmonaalinen hypertensio)
• sairaus, johon liittyy keuhkoverisuonien tukkeutuminen (pulmonaalinen veno-okklusiivinen tauti)
• maksasairaus (maksan vajaatoiminta)
• maksaentsyymien (transaminaasien) tasojen kohoaminen
• ihon ja silmän valkuaisten keltaisuus (ikterus)
• sairaus, johon liittyy maksan verisuonien tukkeutuminen (veno-okklusiivinen maksatauti)
• ihottuma koko kehossa (yleistynyt eksanteema)
• munuaisten vajaatoiminnan erityinen muoto (hemolyyttinen ureeminen oireyhtymä, HUS), joka johtuu punasolujen tuhoutumisesta nopeammin kuin mitä luuydin tuottaa niitä, ja jonka luonteenomaisia piirteitä ovat hemolyyttinen anemia, akuutti munuaisten vajaatoiminta ja verihiutaleiden vähäinen määrä
• hemolyyttisen anemian tyyppi, jonka aiheuttajat ovat pienten verisuonten tekijät (mikroangiopaattinen hemolyyttinen anemia)
Tuntematon: koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin
• infektio
• punasolujen määrän väheneminen (anemia)
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www‐sivusto: www.fimea.fi
Lääkealan turvallisuus‐ ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 Fimea
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä etiketissä ja pakkauksessa mainitun viimeisen käyttöpäivämäärän “EXP” jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Tämä lääke ei vaadi lämpötilan suhteen erityisiä säilytysolosuhteita.
Pidä injektiopullo ulkopakkauksessa. Herkkä valolle.
Käytönaikainen fysikaalinen ja kemiallinen säilyvyys on osoitettu 48 tunnin ajalta, kun valmiste säilytetään valolta suojattuna huoneenlämmössä (15–25 °C), ja 72 tunnin ajalta, kun valmiste säilytetään valolta suojattuna jääkaapissa (2–8 °C).
Mikrobiologiselta kannalta lääkevalmiste tulisi käyttää välittömästi.
Jos valmistetta ei käytetä välittömästi, käytönaikaiset säilytysajat ja säilytysolosuhteet ennen käyttöä ovat käyttäjän vastuulla eivätkä tavallisesti saa ylittää 24 tuntia 2–8 °C:ssa valolta suojattuna, ellei käyttökuntoon saattamista ole tehty valvotuissa ja validoiduissa aseptisissa olosuhteissa.
Suojaa käyttökuntoon saatettu liuos valolta.
Lääkkeitä ei tule heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Mitomycin medac sisältää
- Vaikuttava aine on mitomysiini.
1 injektiopullo jauhetta sisältää 40 mg mitomysiiniä. Käyttövalmiiksi saattamisen jälkeen, sen jälkeen kun siihen on sekoitettu 40 ml liuotinta, 1 ml liuosta virtsarakkoon sisältää 1 mg mitomysiiniä.
- Muut aineet ovat:
Jauhe liuosta varten, virtsarakkoon: urea.
Liuotin liuosta varten, virtsarakkoon: natriumkloridi, injektionesteisiin käytettävä vesi, pH:ta säätävät aineet (1 M natriumhydroksidi, 1 M kloorivetyhappo).
Lääkevalmisteen kuvaus ja pakkauskoko
Mitomycin medac on harmaa tai harmaan sininen jauhe. Liuotin on kirkas ja väritön liuos.
Mitomycin medac (instillaatiopakkaus) on saatavissa pakkauksissa, jotka sisältävät 1, 4 tai 5 kirkkaasta lasista valmistettua injektiopulloa (50 ml), joissa on pinnoitettu kumikorkki ja
alumiinisinetti. Instillaatiopakkaukset virtsarakkoon antoa varten sisältävät myös 1, 4 tai 5 APP*- pussia, joiden tilavuus on 40 ml sisältäen 9 mg/ml (0,9 %) natriumkloridi-injektioliuosta.
Saatavissa olevat pakkaukset sisältävät tai eivät sisällä katetreja ja/tai liittimiä (Luer-Lock-liitin kartionmuotoiseen liittimeen).
*APP = kehittynyt polypropeeni (Advanced Polypropylene) (polyolefiini/polypropeeni/styreenilohko- kopolymeeri).
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija ja valmistaja
medac Gesellschaft für klinische Spezialpräparate mbH Theaterstr. 6
22880 Wedel Saksa
Puh: +49 4103 8006-0
Faksi: +49 4103 8006-100
Tällä lääkevalmisteella on myyntilupa Euroopan talousalueeseen kuuluvissa jäsenvaltioissa seuraavilla kauppanimillä:
Alankomaat, Belgia, Irlanti, Islanti, Itävalta, Latvia, Liettua, Norja, Puola, Ruotsi, Slovakia, Suomi, Tanska, Viro:
Mitomycin medac
Saksa:
mito-extra
Italia:
Miturox
Portugali:
Mitomicina medac
Slovenia Mitomicin medac
Iso-Britannia:
Mitomycin medac
Tämä pakkausseloste on tarkistettu viimeksi 05.02.2025.
Ohjeet terveydenhuollon ammattilaiselle
Seuraavat tiedot on tarkoitettu vain terveydenhuollon ammattilaisille:
Tärkeitä tietoja Mitomycin medac -valmisteen käytöstä
Mitomycin medac -valmistetta saavat käyttää vain asianmukaisen koulutuksen saaneet terveydenhuollon ammattilaiset.
Varmista, että valmistetta on säilytetty asianmukaisissa olosuhteissa (ks. kohta Valmisteen säilyttäminen) ja että pakkaus on ehjä.
Hoito-ohjelmat
On olemassa useita virtsarakkoon annettavia mitomysiinihoitoja, joissa käytetty mitomysiiniannos, instillaatioiden annon tiheys ja hoidon kesto vaihtelevat.
Ellei muuta ole määritetty, mitomysiinin annostus on 40 mg virtsarakkoon instilloituna kerran viikossa. Voidaan myös käyttää hoitoja, joissa instillaatio tapahtuu joka toinen viikko, kerran kuukaudessa tai kolmen kuukauden välein.
Erikoislääkärin on päätettävä parhaasta hoidosta, annon tiheydestä ja hoidon pituudesta yksilöllisesti kunkin potilaan kohdalla.
Tätä lääkevalmistetta suositellaan käytettävän sen optimaalisessa pH:ssa (virtsan pH > 6). Mitomysiinin laimentumista virtsarakossa voidaan vähentää vähentämällä nesteiden nauttimista ennen instillaatiota, sen aikana ja sen jälkeen. Virtsarakko on tyhjennettävä ennen instillaatiota. Mitomysiini instilloidaan virtsarakkoon katetrilla alhaisella paineella. Liuoksen pitäisi pysyä virtsarakossa katetrin poistamisen jälkeen 1–2 tuntia. Tänä aikana liuoksen pitäisi olla riittävässä kosketuksessa virtsarakon koko limakalvopintaan. Tämän vuoksi on huolehdittava, että potilas vaihtaa asentoa 15 minuutin välein. 2 tunnin kuluttua potilaan tulee virtsata instilloitu liuos, mieluiten istuma-asennossa.
Mitomycin medac -valmisteen käyttöön liittyvät perusperiaatteet ja suojaavat toimenpiteet
Suoraa kosketusta Mitomycin medac -valmisteeseen tulee yleisesti välttää. Mitomycin medac on ihmisille ja ympäristölle vaarallinen sytostaatti. Seurauksena voi olla vaaratilanteita, jos lääkevalmistetta pääsee kehoon haavojen tai suojaamattoman pehmitetyn ihon kautta, jos lääkevalmisteesta muodostunutta aerosolia hengitetään, valmistetippoja pääsee silmiin tai limakalvoille tai jos lääkevalmistetta niellään. Älä syö, juo tai tupakoi tiloissa, joissa valmistetta käsitellään, äläkä säilytä näissä tiloissa ruokaa, juomaa tai tupakkatuotteita.
Valmisteen käsittelyn aikana suositellaan suljetun, roiskeenkestävän suojatakin, kertakäyttökäsineiden, soveltuvan hengitysmaskin ja myös sivuilta suojaavien suojalasien käyttöä henkilösuojaimina.
Mitomycin medac -valmistetta saa kuljettaa vain suljetuissa astioissa (katso säilytysolosuhteet käyttökuntoon saattamisen jälkeen kohdasta Valmisteen säilyttäminen).
Pese kädet käsittelyn ja mahdollisen ihokosketuksen jälkeen runsaalla vedellä ja käytä ihonhoitotuotteita.
Käyttökuntoon saatetun virtsarakkoon annosteltavan liuoksen valmistelu
Ennen käyttöä lääkevalmiste pitää liuottaa aseptisissa olosuhteissa steriiliin 0,9 % (9 mg/ml) natriumkloridiliuokseen (katso Ohjeet Mitomycin medac valmisteen käyttäjille, vaihe 7). Liuota yhden Mitomycin medac –valmisteen injektiopullon sisältö (joka vastaa 40 mg mitomysiiniä) 40 ml:aan steriiliä 0,9 % (9 mg/ml) natriumkloridiliuosta. Injektiopullon sisällön täytyy liueta niin, että tuloksena on sinipunainen kirkas liuos 2 minuutin kuluessa. Vain kirkkaita sinipunaisia liuoksia saa käyttää.
Liukasteen käyttöä suositellaan pienentämään katetroinnin aikana syntyvien vaurioiden riskiä ja lisäämään toimenpiteen miellyttävyyttä. Miehet saattavat tarvita enemmän liukastetta kuin naiset. Tyhjennä virtsarakko katetroinnin jälkeen, jotta mahdollisesti sisään viedyn liukasteen määrä olisi mahdollisimman pieni ennen Mitomycin medac -valmisteen annostelua.
Injektiopullon sisältö on tarkoitettu vain kertakäyttöä ja yhtä antokertaa varten. Käyttämättä jäänyt liuos on hävitettävä.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Lisätietoja katetrista on sen käyttöohjeissa.
Ohjeet Mitomycin medac -valmisteen käyttäjille
Instillaatiopakkauksen <jossa katetri ja liitin> osat ja käyttö
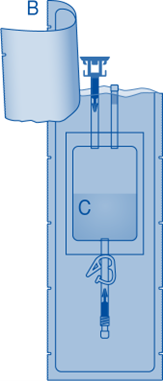
Instillaatiopakkauksen pääasialliset osat
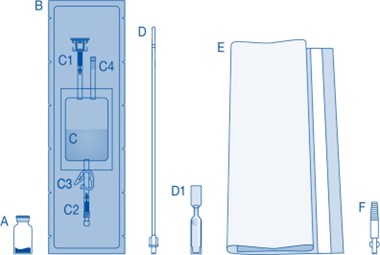
Osat | Kuvaus |
A | Injektiopullo, jossa jauhetta |
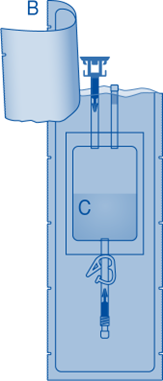
B | Suojakuori |
C | Liuotinpussi, jossa 0,9 % (9 mg/ml) natriumkloridiliuosta |
C1 | Injektiopulloliitin, jossa suojakorkki ja murrettava sinetti |
C2 | Luer-Lock-katetriliitin, jossa suojakorkki ja murrettava sinetti |
C3 | Painesuljin |
C4 | Täyttöportti, ei toiminnallinen |
D | Luer-Lock-katetri |
D1 | Liukaste |
E | Jätepussi |
F | Luer-Lock-liitin kartioliittimeen |
Injektiopullon liittäminen liuotinpussiin
- Avaa jätepussi (E) valmiiksi pakkauksen sisällön välitöntä instillaation jälkeistä hävittämistä varten, jotta vältetään kontaminaatio.
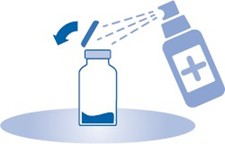
2. Poista injektiopullon (A) repäisysinetti ja desinfioi korkki paikallisten säädösten mukaisesti.
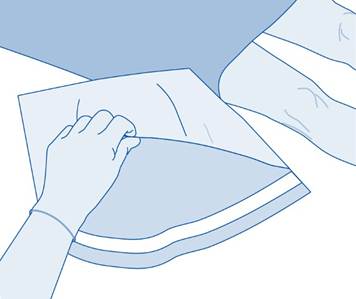
3. Repäise liuotinpussin (C) suojakuori (B) auki ja poista suojakuori kokonaan.
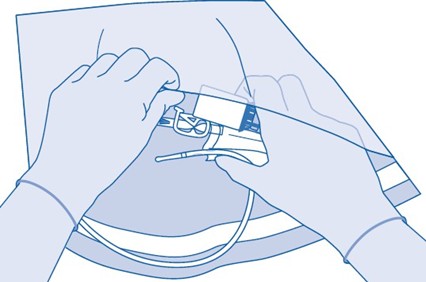
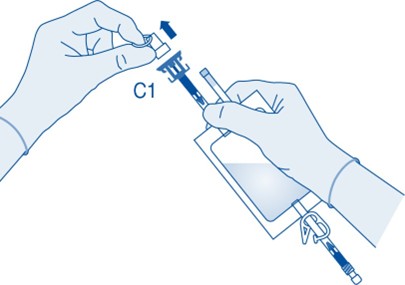
4. Poista injektiopulloliittimen (C1) suojakorkki.
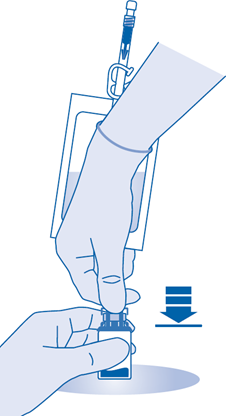
5. Työnnä liitin injektiopulloon pysäyttimeen asti.
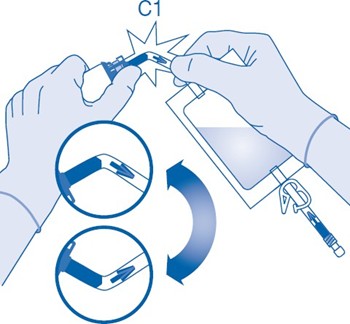
Jauheen ja liuottimen sekoittaminen
6. Murra injektiopulloliittimen (C1) putken sisällä oleva murrettava sinetti taivuttamalla sitä ylös ja alas useita kertoja.
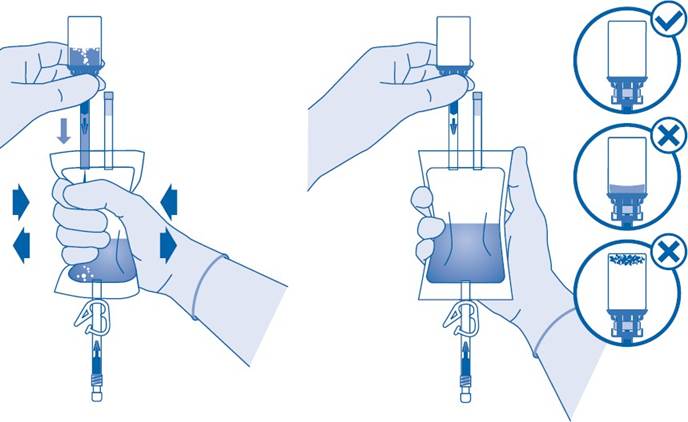
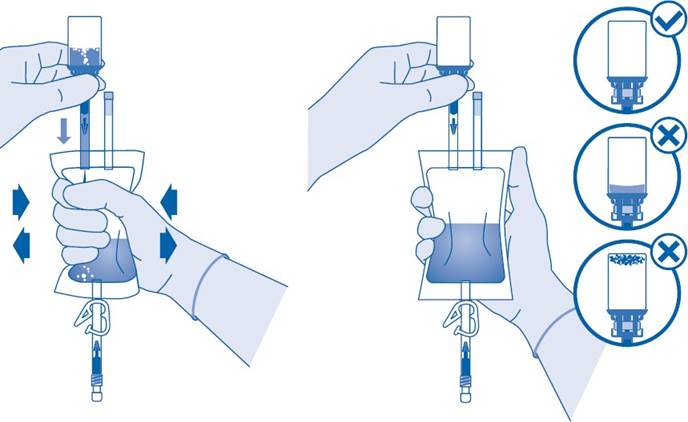
7. Pitele liuotinpussia niin, että injektiopullo on sen alapuolella.
Puristele liuotinpussia useita kertoja, jotta injektiopulloon siirtyy riittävästi liuotinta.
Varmista, että injektiopullo ei täyty kokonaan, jotta liuos voidaan vielä siirtää liuotinpussiin. Pussin sisään saa jäädä liuotinta.
Pyöritä injektiopulloa hitaasti, jotta lääkevalmiste liukenee liuottimeen.
Injektiopullon sisällön on liuettava kokonaan niin, että tuloksena on sinipunainen kirkas liuos 2 minuutin kuluessa.
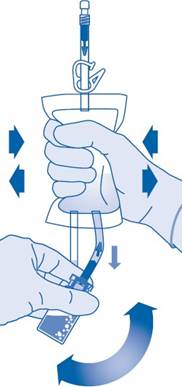
8. Käännä liuotinpussi ylösalaisin niin, että injektiopullo on sen yläpuolella.
Pidä kiinni injektiopullosta.
Puristele liuotinpussia useita kertoja, kunnes injektiopullo on täysin tyhjä.
Jos injektiopullon sisään jää jauhetta, toista vaiheet 7 ja 8.
Mikrobiologiselta kannalta lääkevalmiste tulisi käyttää välittömästi.
Jos lääkevalmistetta ei käytetä välittömästi, katso kohta Valmisteen säilyttäminen ”Mitomycin medac -valmisteen säilyttäminen”.
Käytä vain kirkasta sinipunaista liuosta. Jääkaappilämpötilassa olevaa liuosta ei saa annostella, jotta potilaalle ei synny virtsaamistarvetta, joka johtaa lyhempään altistusaikaan.
Katetrointi
9. Katetroi potilas paikallisten säännösten ja käyttöohjeiden mukaisesti pakkaukseen kuuluvalla Luer-Lock-katetrilla (D) ja liukasteella (D1) tai muulla soveltuvalla katetrilla ja liukasteella.
Tyhjennä virtsarakko katetrilla.
Huomaa, jos käytät omavalintaista katetria ja kartioliitintä:
Pakkaukseen kuuluvaa kartioliittimeen liitettävää Luer-Lock-liitintä (F) on käytettävä liitettäessä pussi katetriin, jossa on kartioliitin (ei kuvassa).
Tätä toimenpidettä varten on suoritettava seuraavat lisätoimenpiteet:
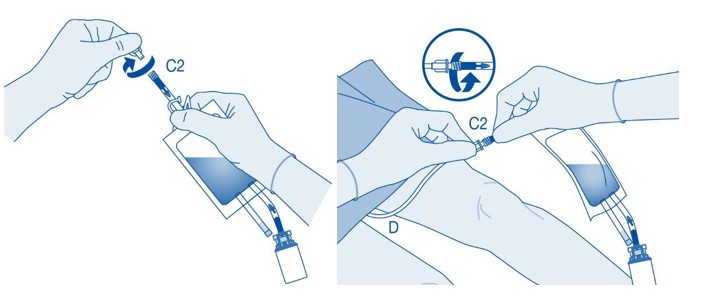
- Poista suojakorkki katetriliittimestä (C2, katso vaihe 10).
- Liitä kartioliittimeen liitettävä Luer-Lock-liitin (F) pussin katetriliittimeen (C2).
- Liitä varovasti pussi, johon kartioliittimeen liitettävä Luer-Lock-liitin (F) on liitetty, potilaan pysyvään katetriin.
- Jatka vaiheeseen 11.
Katetrin liittäminen liuotinpussiin
10. Käännä ja pyörittele pussia ennen liittämistä.
Älä annostele jääkaappilämpötilassa olevaa liuosta.
Poista suojakorkki katetriliittimestä (C2).
Liitä potilaan Luer-Lock-katetri (D) liuotinpussin katetriliittimeen (C2).
Instillointi
11. Murra katetriliittimen (C2) putken sisällä oleva murrettava sinetti taivuttamalla sitä ylös ja alas useita kertoja.
Pidä samalla potilaan katetri vakaana.
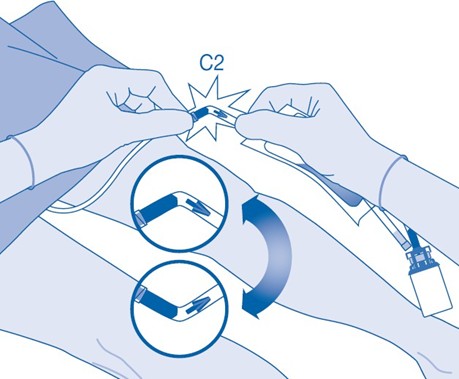
12. Pitele liuotinpussia injektiopullo ylösalaisin pussin yläpuolella.
Puristele liuotinpussia varovasti toisella kädellä, jotta lääkevalmiste instilloituu hitaasti potilaan virtsarakkoon.
Jatka puristelua, kunnes liuotinpussi ja injektiopullo ovat tyhjiä.
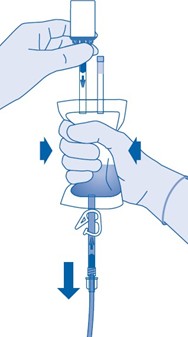
13. Purista liuotinpussissa oleva ilma ulos, jotta katetri tyhjenee mahdollisimman hyvin.
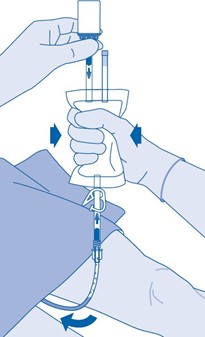
Instilloinnin jälkeen
14. Painesulkimen (C3) sulkeminen estää nesteen takaisinvirtauksen katetriin ja pienentää kontaminaatioriskiä. Voit myös pitää liuotinpussin puristettuna tyhjäksi, kun suoritat vaiheet 15 ja 16.
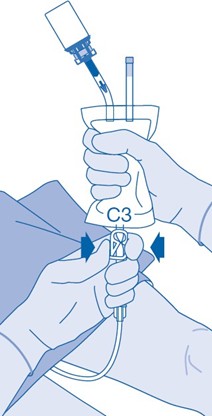
15. Kun instillaatiopakkaus on tyhjennetty, poista katetri välittömästi varovasti virtsarakosta irrottamatta liuotinpussia katetrista. Kun katetri on poistettu, liuoksen pitää pysyä virtsarakossa 1–2 tunnin ajan. Vältä roiskuvien pisaroiden aiheuttamaa kontaminaatiota.
Huomaa, jos käytät omavalintaista katetria ja kartioliitintä:
Irrota pussi ja Luer-Lock-liittimeen liitettävä kartioliitäntä pysyvästä katetrista. Sulje pysyvä katetri esimerkiksi katetritulpalla tai sulkimella, jotta lääkevalmiste pysyy virtsarakossa aiotun vaikutusajan.
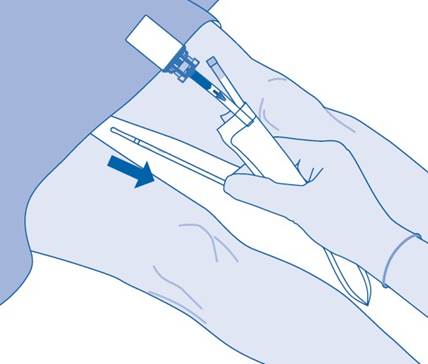
16. Hävitä tuote kansallisten säädösten mukaisesti, käytä jätepussia.
Injektiopullon sisältö on tarkoitettu vain kertakäyttöä ja yhtä antokertaa varten. Kaikki jäljelle jäänyt liuos on hävitettävä.
Ohjeet Mitomycin medac -valmisteen käyttäjille
Instillaatiopakkauksen <jossa katetri, ilman liitintä> osat ja käyttö
Instillaatiopakkauksen pääasialliset osat
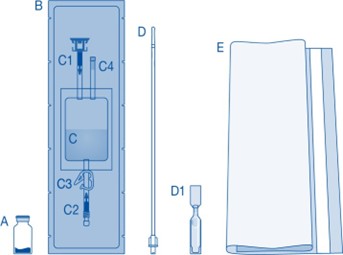
Osat | Kuvaus |
A | Injektiopullo, jossa jauhetta |
B | Suojakuori |
C | Liuotinpussi, jossa 0,9 % (9 mg/ml) natriumkloridiliuosta |
C1 | Injektiopulloliitin, jossa suojakorkki ja murrettava sinetti |
C2 | Luer-Lock-katetriliitin, jossa suojakorkki ja murrettava sinetti |
C3 | Painesuljin |
C4 | Täyttöportti, ei toiminnallinen |
D | Luer-Lock-katetri |
D1 | Liukaste |
E | Jätepussi |
Injektiopullon liittäminen liuotinpussiin
- Avaa jätepussi (E) valmiiksi pakkauksen sisällön välitöntä instillaation jälkeistä hävittämistä varten, jotta vältetään kontaminaatio.
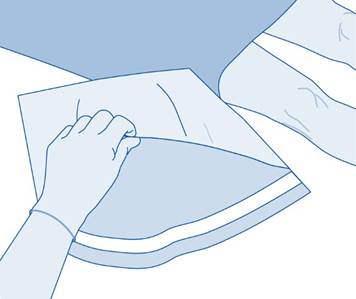
2. Poista injektiopullon (A) repäisysinetti ja desinfioi korkki paikallisten säädösten mukaisesti.
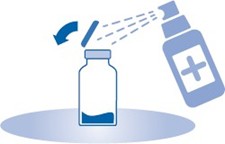
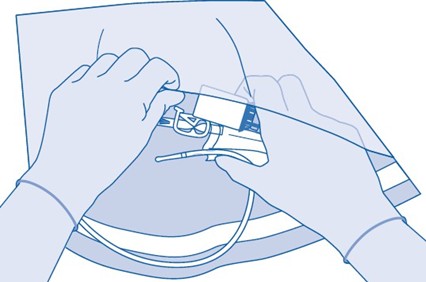
3. Repäise liuotinpussin (C) suojakuori (B) auki ja poista suojakuori kokonaan.
4. Poista injektiopulloliittimen (C1) suojakorkki.
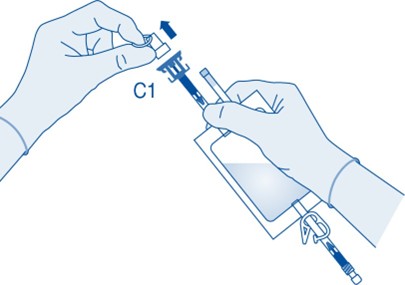
5. Työnnä liitin injektiopulloon pysäyttimeen asti.
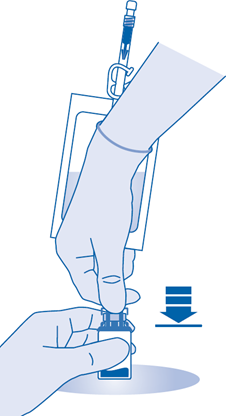
Jauheen ja liuottimen sekoittaminen
6. Murra injektiopulloliittimen (C1) putken sisällä oleva murrettava sinetti taivuttamalla sitä ylös ja alas useita kertoja.

7. Pitele liuotinpussia niin, että injektiopullo on sen alapuolella.
Puristele liuotinpussia useita kertoja, jotta injektiopulloon siirtyy riittävästi liuotinta.
Varmista, että injektiopullo ei täyty kokonaan, jotta liuos voidaan vielä siirtää liuotinpussiin. Pussin sisään saa jäädä liuotinta.
Pyöritä injektiopulloa hitaasti, jotta lääkevalmiste liukenee liuottimeen.
Injektiopullon sisällön on liuettava kokonaan niin, että tuloksena on sinipunainen kirkas liuos 2 minuutin kuluessa.
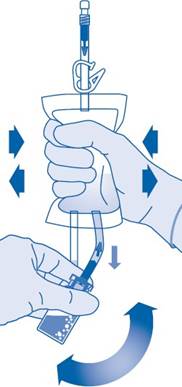
8. Käännä liuotinpussi ylösalaisin niin, että injektiopullo on sen yläpuolella.
Pidä kiinni injektiopullosta.
Puristele liuotinpussia useita kertoja, kunnes injektiopullo on täysin tyhjä.
Jos injektiopullon sisään jää jauhetta, toista vaiheet 7 ja 8.
Mikrobiologiselta kannalta lääkevalmiste tulisi käyttää välittömästi.
Jos lääkevalmistetta ei käytetä välittömästi, katso kohta Valmisteen säilyttäminen ”Mitomycin medac -valmisteen säilyttäminen”.
Käytä vain kirkasta sinipunaista liuosta. Jääkaappilämpötilassa olevaa liuosta ei saa annostella, jotta potilaalle ei synny virtsaamistarvetta, joka johtaa lyhempään altistusaikaan.
Katetrointi
9. Katetroi potilas paikallisten säännösten ja käyttöohjeiden mukaisesti pakkaukseen kuuluvalla Luer-Lock-katetrilla (D) ja liukasteella (D1) tai muulla soveltuvalla katetrilla ja/tai liukasteella.
Tyhjennä virtsarakko katetrilla.
Katetrin liittäminen liuotinpussiin
10. Käännä ja pyörittele pussia ennen liittämistä.
Älä annostele jääkaappilämpötilassa olevaa liuosta.
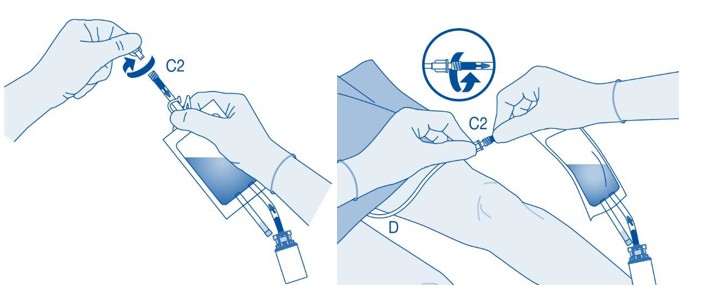
Poista suojakorkki katetriliittimestä (C2).
Liitä potilaan Luer-Lock-katetri (D) liuotinpussin katetriliittimeen (C2).
Instillointi
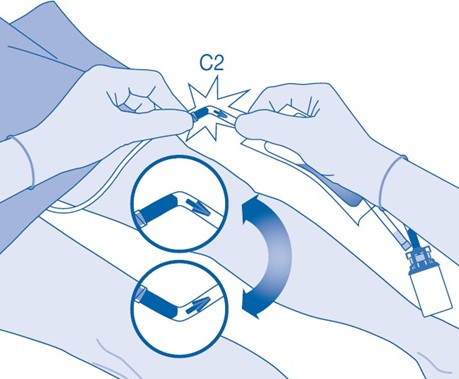
11. Murra katetriliittimen (C2) putken sisällä oleva murrettava sinetti taivuttamalla sitä ylös ja alas useita kertoja.
Pidä samalla potilaan katetri vakaana.
12. Pitele liuotinpussia injektiopullo ylösalaisin pussin yläpuolella.
Puristele liuotinpussia varovasti toisella kädellä, jotta lääkevalmiste instilloituu hitaasti potilaan virtsarakkoon.
Jatka puristelua, kunnes liuotinpussi ja injektiopullo ovat tyhjiä.
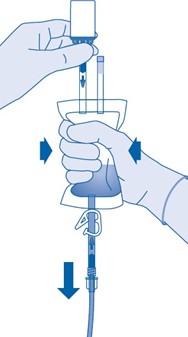
13. Purista liuotinpussissa oleva ilma ulos, jotta katetri tyhjenee mahdollisimman hyvin.
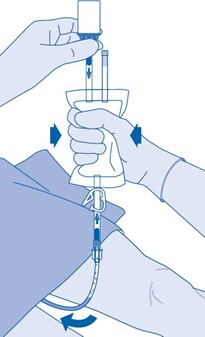
Instilloinnin jälkeen
14. Painesulkimen (C3) sulkeminen estää nesteen takaisinvirtauksen katetriin ja pienentää kontaminaatioriskiä. Voit myös pitää liuotinpussin puristettuna tyhjäksi, kun suoritat vaiheet 15 ja 16.
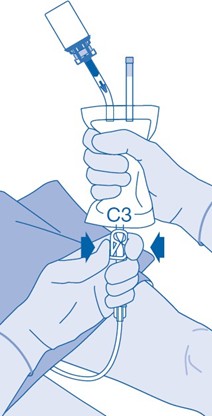
15. Kun instillaatiopakkaus on tyhjennetty, poista katetri välittömästi varovasti virtsarakosta irrottamatta liuotinpussia katetrista. Kun katetri on poistettu, liuoksen pitää pysyä virtsarakossa 1–2 tunnin ajan. Vältä roiskuvien pisaroiden aiheuttamaa kontaminaatiota.

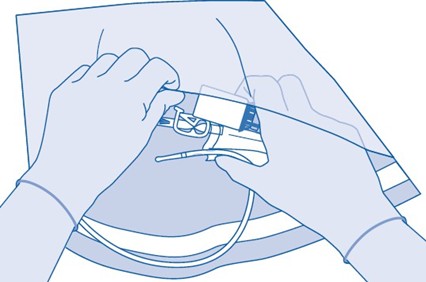
16. Hävitä tuote kansallisten säädösten mukaisesti, käytä jätepussia.
Injektiopullon sisältö on tarkoitettu vain kertakäyttöä ja yhtä antokertaa varten. Kaikki jäljelle jäänyt liuos on hävitettävä.
Ohjeet Mitomycin medac -valmisteen käyttäjille
Instillaatiopakkauksen <jossa liitin, ilman katetria> osat ja käyttö
Instillaatiopakkauksen pääasialliset osat
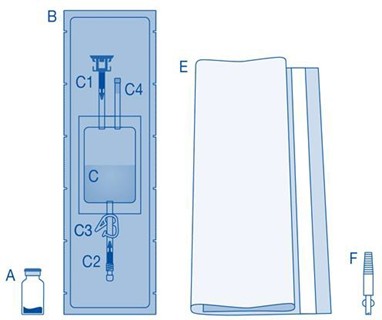
Osat | Kuvaus |
A | Injektiopullo, jossa jauhetta |
B | Suojakuori |
C | Liuotinpussi, jossa 0,9 % (9 mg/ml) natriumkloridiliuosta |
C1 | Injektiopulloliitin, jossa suojakorkki ja murrettava sinetti |
C2 | Luer-Lock-katetriliitin, jossa suojakorkki ja murrettava sinetti |
C3 | Painesuljin |
C4 | Täyttöportti, ei toiminnallinen |
E | Jätepussi |
F | Luer-Lock-liitin kartioliittimeen |
Injektiopullon liittäminen liuotinpussiin
- Avaa jätepussi (E) valmiiksi pakkauksen sisällön välitöntä instillaation jälkeistä hävittämistä varten, jotta vältetään kontaminaatio.

2. Poista injektiopullon (A) repäisysinetti ja desinfioi korkki paikallisten säädösten mukaisesti.
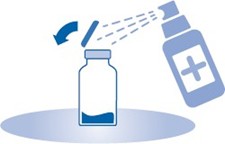
3. Repäise liuotinpussin (C) suojakuori (B) auki ja poista suojakuori kokonaan.
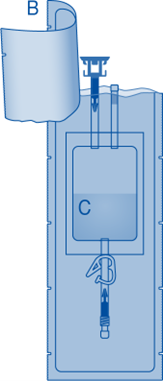
4. Poista injektiopulloliittimen (C1) suojakorkki.
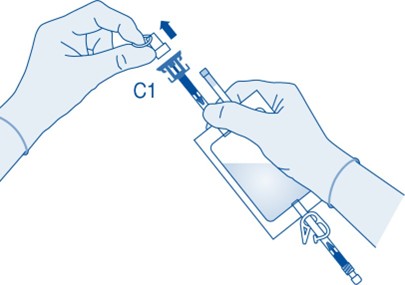
5. Työnnä liitin injektiopulloon pysäyttimeen asti.
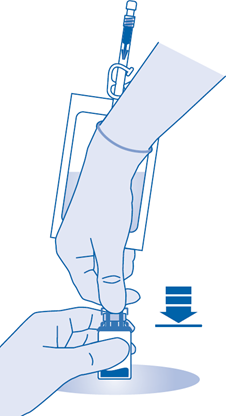
Jauheen ja liuottimen sekoittaminen
6. Murra injektiopulloliittimen (C1) putken sisällä oleva murrettava sinetti taivuttamalla sitä ylös ja alas useita kertoja.
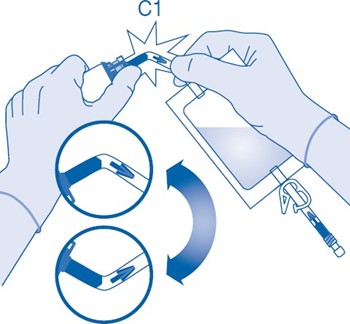
7. Pitele liuotinpussia niin, että injektiopullo on sen alapuolella.
Puristele liuotinpussia useita kertoja, jotta injektiopulloon siirtyy riittävästi liuotinta.
Varmista, että injektiopullo ei täyty kokonaan, jotta liuos voidaan vielä siirtää liuotinpussiin. Pussin sisään saa jäädä liuotinta.
Pyöritä injektiopulloa hitaasti, jotta lääkevalmiste liukenee liuottimeen.
Injektiopullon sisällön on liuettava kokonaan niin, että tuloksena on sinipunainen kirkas liuos 2 minuutin kuluessa.

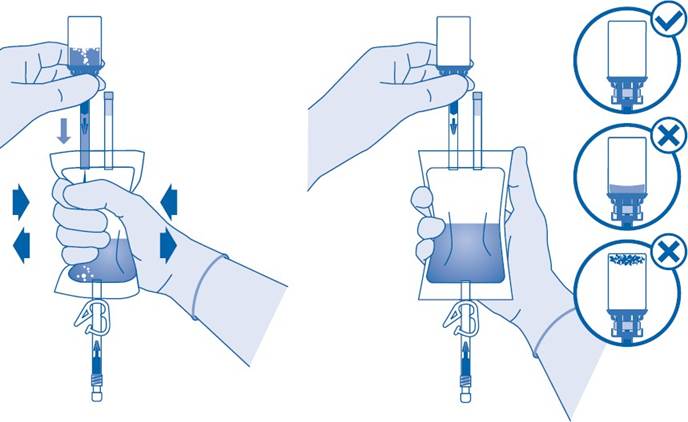
8. Käännä liuotinpussi ylösalaisin niin, että injektiopullo on sen yläpuolella.
Pidä kiinni injektiopullosta.
Puristele liuotinpussia useita kertoja, kunnes injektiopullo on täysin tyhjä.
Jos injektiopullon sisään jää jauhetta, toista vaiheet 7 ja 8.
Mikrobiologiselta kannalta lääkevalmiste tulisi käyttää välittömästi.
Jos lääkevalmistetta ei käytetä välittömästi, katso kohta Valmisteen säilyttäminen Mitomycin medac -valmisteen säilyttäminen.
Käytä vain kirkasta sinipunaista liuosta. Jääkaappilämpötilassa olevaa liuosta ei saa annostella, jotta potilaalle ei synny virtsaamistarvetta, joka jotaa lyhempään altistusaikaan.
Katetrointi
9. Katetroi potilas paikallisten säännösten ja käyttöohjeiden mukaisesti soveltuvalla katetrilla ja liukasteella.
Tyhjennä virtsarakko katetrilla.
Huomaa, kun käytät omavalintaista katetria ja kartioliitintä:
Tähän pakkaukseen ei kuulu katetria. Pakkaukseen kuuluvaa kartioliittimeen liitettävää Luer- Lock-liitintä (F) on käytettävä pussin liittämiseen katetriin, jossa on kartioliitin (ei kuvassa).
Tätä toimenpidettä varten on suoritettava seuraavat lisätoimenpiteet:
- Poista suojakorkki katetriliittimestä (C2, katso vaihe 10).
- Liitä kartioliittimeen liitettävä Luer-Lock-liitin (F) pussin katetriliittimeen (C2).
- Liitä varovasti pussi, johon kartioliittimeen liitettävä Luer-Lock-liitin (F) on liitetty, potilaan pysyvään katetriin.
- Jatka vaiheeseen 11.
Katetrin liittäminen liuotinpussiin
10. Käännä ja pyörittele pussia ennen liittämistä.
Älä annostele jääkaappilämpötilassa olevaa liuosta.
Poista suojakorkki katetriliittimestä (C2).
Liitä potilaan katetri liuotinpussin katetriliittimeen (C2).
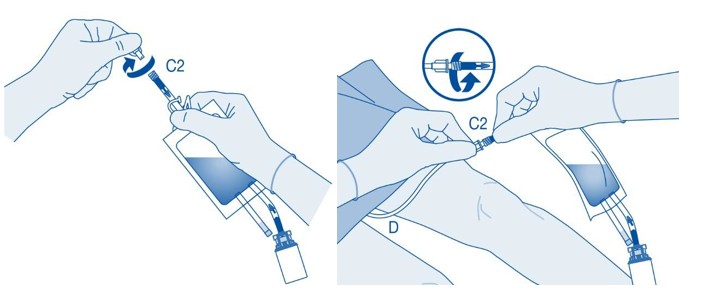
Instillointi
11. Murra katetriliittimen (C2) putken sisällä oleva murrettava sinetti taivuttamalla sitä ylös ja alas useita kertoja.
Pidä samalla potilaan katetri vakaana.
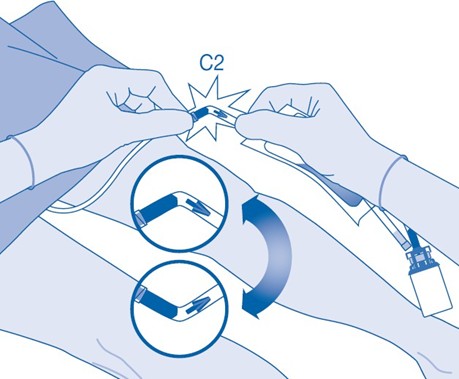
12. Pitele liuotinpussia injektiopullo ylösalaisin pussin yläpuolella.
Puristele liuotinpussia varovasti toisella kädellä, jotta lääkevalmiste instilloituu hitaasti potilaan virtsarakkoon.
Jatka puristelua, kunnes liuotinpussi ja injektiopullo ovat tyhjiä.
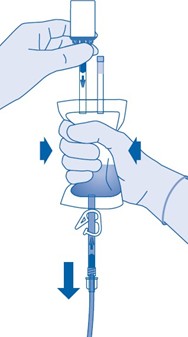
13. Purista liuotinpussissa oleva ilma ulos, jotta katetri tyhjenee mahdollisimman hyvin.
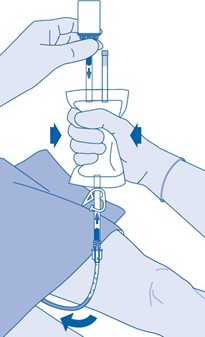
Instilloinnin jälkeen
14. Painesulkimen (C3) sulkeminen estää nesteen takaisinvirtauksen katetriin ja pienentää kontaminaatioriskiä. Voit myös pitää liuotinpussin puristettuna tyhjäksi, kun suoritat vaiheet 15 ja 16.
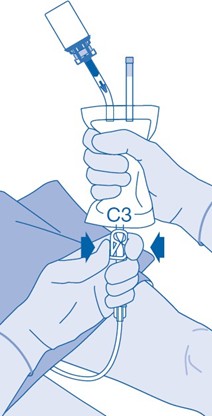
15. Kun instillaatiopakkaus on tyhjennetty, poista katetri välittömästi varovasti virtsarakosta irrottamatta liuotinpussia katetrista. Kun katetri on poistettu, liuoksen pitää pysyä virtsarakossa 1–2 tunnin ajan. Vältä roiskuvien pisaroiden aiheuttamaa kontaminaatiota.
Huomaa, kun käytät omavalintaista katetria ja kartioliitintä:
Irrota pussi ja Luer-Lock-liittimeen liitettävä kartioliitäntä pysyvästä katetrista. Sulje pysyvä katetri esimerkiksi katetritulpalla tai sulkimella, jotta lääkevalmiste pysyy virtsarakossa aiotun vaikutusajan.
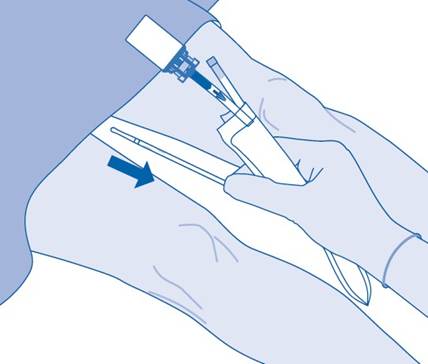
16. Hävitä tuote kansallisten säädösten mukaisesti, käytä jätepussia.
Injektiopullon sisältö on tarkoitettu vain kertakäyttöä ja yhtä antokertaa varten. Kaikki jäljelle jäänyt liuos on hävitettävä.
Ohjeet Mitomycin medac -valmisteen käyttäjille
Instillaatiopakkauksen <ilman katetria, ilman liitintä> osat ja käyttö
Instillaatiopakkauksen pääasialliset osat
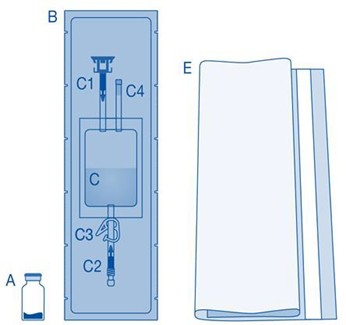
Osat | Kuvaus |
A | Injektiopullo, jossa jauhetta |
B | Suojakuori |
C | Liuotinpussi, jossa 0,9 % (9 mg/ml) natriumkloridiliuosta |
C1 | Injektiopulloliitin, jossa suojakorkki ja murrettava sinetti |
C2 | Luer-Lock-katetriliitin, jossa suojakorkki ja murrettava sinetti |
C3 | Painesuljin |
C4 | Täyttöportti, ei toiminnallinen |
E | Jätepussi |
Injektiopullon liittäminen liuotinpussiin
- Avaa jätepussi (E) valmiiksi pakkauksen sisällön välitöntä instillaation jälkeistä hävittämistä varten, jotta vältetään kontaminaatio.
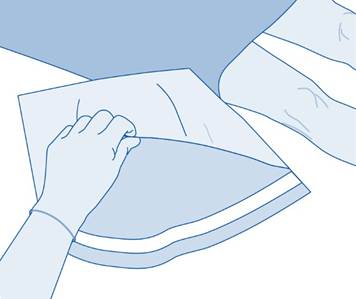
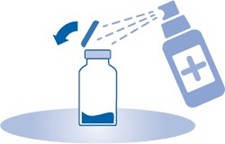
2. Poista injektiopullon (A) repäisysinetti ja desinfioi korkki paikallisten säädösten mukaisesti.
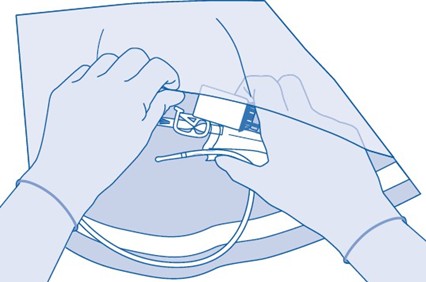
3. Repäise liuotinpussin (C) suojakuori (B) auki ja poista suojakuori kokonaan.
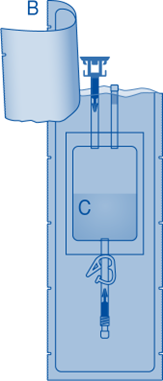
4. Poista injektiopulloliittimen (C1) suojakorkki.
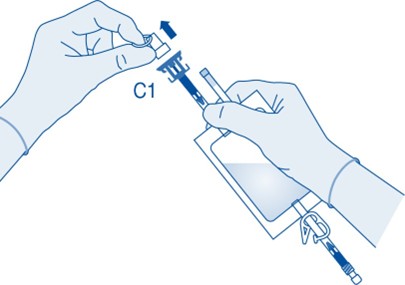
5. Työnnä liitin injektiopulloon pysäyttimeen asti.
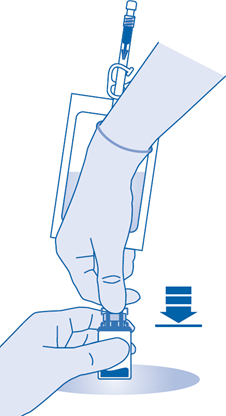
Jauheen ja liuottimen sekoittaminen
6. Murra injektiopulloliittimen (C1) putken sisällä oleva murrettava sinetti taivuttamalla sitä ylös ja alas useita kertoja.
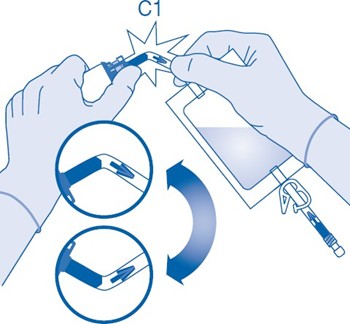
7. Pitele liuotinpussia niin, että injektiopullo on sen alapuolella.
Puristele liuotinpussia useita kertoja, jotta injektiopulloon siirtyy riittävästi liuotinta.
Varmista, että injektiopullo ei täyty kokonaan, jotta liuos voidaan vielä siirtää liuotinpussiin. Pussin sisään saa jäädä liuotinta.
Pyöritä injektiopulloa hitaasti, jotta lääkevalmiste liukenee liuottimeen.
Injektiopullon sisällön on liuettava kokonaan niin, että tuloksena on sinipunainen kirkas liuos 2 minuutin kuluessa.
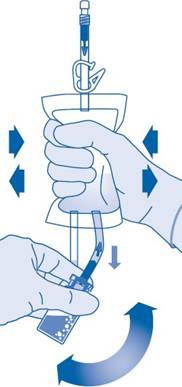
8. Käännä liuotinpussi ylösalaisin niin, että injektiopullo on sen yläpuolella.
Pidä kiinni injektiopullosta.
Puristele liuotinpussia useita kertoja, kunnes injektiopullo on täysin tyhjä.
Jos injektiopullon sisään jää jauhetta, toista vaiheet 7 ja 8.
Mikrobiologiselta kannalta lääkevalmiste tulisi käyttää välittömästi.
Jos lääkevalmistetta ei käytetä välittömästi, katso kohta Valmisteen säilyttäminen ”Mitomycin medac -valmisteen säilyttäminen”.
Käytä vain kirkasta sinipunaista liuosta. Jääkaappilämpötilassa olevaa liuosta ei saa annostella, jotta potilaalle ei synny virtsaamistarvetta, joka johtaa lyhempään altistusaikaan.
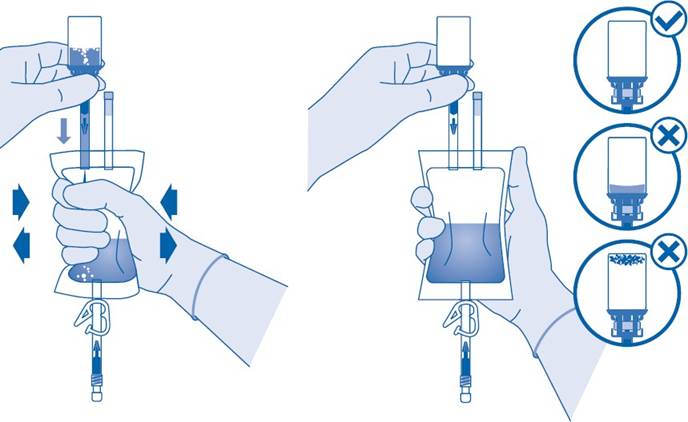
Katetrointi
9. Katetroi potilas paikallisten säännösten ja käyttöohjeiden mukaisesti soveltuvalla katetrilla jaliukasteella.
Tyhjennä virtsarakko katetrilla.
Katetrin liittäminen liuotinpussiin
10. Käännä ja pyörittele pussia ennen liittämistä.
Älä annostele jääkaappilämpötilassa olevaa liuosta.
Poista suojakorkki katetriliittimestä (C2).
Liitä potilaan katetri liuotinpussin katetriliittimeen (C2).
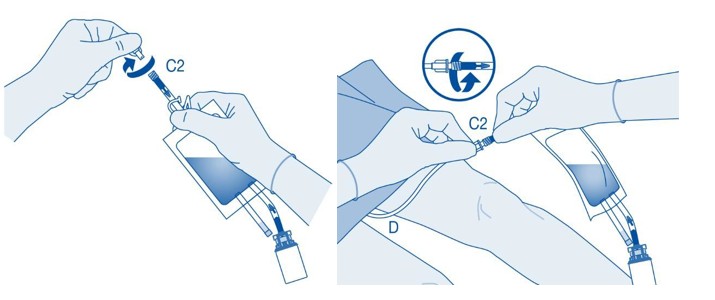
Instillointi
11. Murra katetriliittimen (C2) putken sisällä oleva murrettava sinetti taivuttamalla sitä ylös ja alas useita kertoja.
Pidä samalla potilaan katetri vakaana.
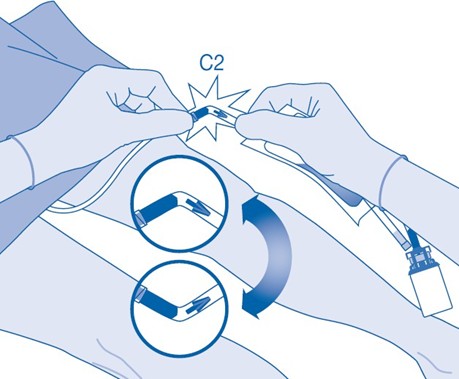
12. Pitele liuotinpussia injektiopullo ylösalaisin pussin yläpuolella.
Puristele liuotinpussia varovasti toisella kädellä, jotta lääkevalmiste instilloituu hitaasti potilaan virtsarakkoon.
Jatka puristelua, kunnes liuotinpussi ja injektiopullo ovat tyhjiä.
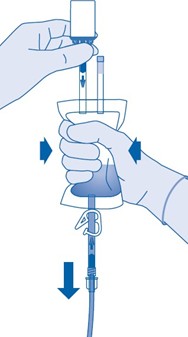
13. Purista liuotinpussissa oleva ilma ulos, jotta katetri tyhjenee mahdollisimman hyvin.
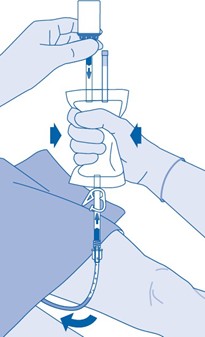
Instilloinnin jälkeen
14. Painesulkimen (C3) sulkeminen estää nesteen takaisinvirtauksen katetriin ja pienentää kontaminaatioriskiä. Voit myös pitää liuotinpussin puristettuna tyhjäksi, kun suoritat vaiheet 15 ja 16.
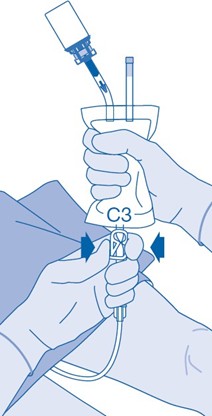
15. Kun instillaatiopakkaus on tyhjennetty, poista katetri välittömästi varovasti virtsarakosta irrottamatta liuotinpussia katetrista. Kun katetri on poistettu, liuoksen pitää pysyä virtsarakossa 1–2 tunnin ajan. Vältä roiskuvien pisaroiden aiheuttamaa kontaminaatiota.

16. Hävitä tuote kansallisten säädösten mukaisesti, käytä jätepussia.
Injektiopullon sisältö on tarkoitettu vain kertakäyttöä ja yhtä antokertaa varten. Kaikki jäljelle jäänyt liuos on hävitettävä.