TAPTIQOM silmätipat, liuos, kerta-annospakkaus 15 mikrog/ml+5 mg/ml
Taptiqom 15 mikrogrammaa/ml + 5 mg/ml
Silmätipat, liuos kerta-annospakkaus
tafluprosti/timololi
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin aloitat tämän lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä pidä antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä Taptiqom on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin käytät Taptiqom-valmistetta
- Miten Taptiqom-valmistetta käytetään
- Mahdolliset haittavaikutukset
- Taptiqom-valmisteen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Millainen lääke se on ja kuinka se vaikuttaa?
Taptiqom-silmätipat sisältävät tafluprostia ja timololia. Tafluprosti kuuluu prostaglandiinianalogeiksi kutsuttuun lääkeryhmään ja timololi kuuluu beetasalpaajiksi kutsuttuun lääkeryhmään. Tafluprosti ja timololi toimivat yhdessä ja alentavat silmänpainetta. Taptiqom-valmistetta käytetään silmänpaineen ollessa liian korkea.
Mihin lääkettäsi käytetään?
Taptiqom-valmistetta käytetään avokulmaglaukoomaksi kutsutun glaukoomatyypin ja myös silmän hypertension (kohonneen silmänpaineen) hoitoon aikuisille. Molempiin sairauksiin liittyy silmän sisäisen paineen kohoaminen, ja ne voivat lopulta vaikuttaa näkökykyyn.
Tafluprostia ja timololia, joita Taptiqom sisältää, voidaan joskus käyttää myös muiden kuin tässä pakkausselosteessa mainittujen sairauksien hoitoon. Kysy neuvoa lääkäriltä, apteekkihenkilökunnalta tai muulta terveydenhuollon ammattilaiselta tarvittaessa ja noudata aina heiltä saamiasi ohjeita.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä Taptiqom-valmistetta:
- jos olet allerginen tafluprostille, timololille, beetasalpaajille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa)
- jos sinulla on tai on joskus ollut hengitystieongelmia, kuten astma, vaikea krooninen ahtauttava keuhkoputkitulehdus (vakava keuhkosairaus, joka voi aiheuttaa vinkuvaa hengitystä, hengitysvaikeuksia ja/tai pitkäkestoista yskää)
- jos sinulla on hidas syke, sydämen vajaatoimintaa tai rytmihäiriöitä (epäsäännöllinen syke).
Varoitukset ja varotoimet
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin käytät Taptiqom-valmistetta.
Ennen tämän lääkkeen käyttöä kerro lääkärille, jos sinulla on tai on joskus ollut:
- sepelvaltimotauti (oireita voivat olla rintakipu tai puristava tunne rinnassa, hengenahdistus tai tukehtumisen tunne), sydämen vajaatoiminta, alhainen verenpaine
- häiriöitä sydämensykkeessä, kuten sydämen harvalyöntisyyttä
- hengitysongelmia, astma tai keuhkoahtaumatauti
- ääreisvaltimotauti (kuten Raynaud'n tauti tai Raynaud'n oireyhtymä)
- diabetes, koska timololi saattaa peittää alhaisesta verensokerista johtuvat merkit ja oireet
- kilpirauhasen liikatoiminta, koska timololi saattaa peittää kilpirauhassairauden merkit ja oireet
- allergioita tai anafylaktisia reaktioita
- myasthenia gravis (harvinainen tauti, joka aiheuttaa lihasten heikkoutta)
- muita silmäsairauksia, esimerkiksi sarveiskalvon sairaus (sarveiskalvo on silmän etuosaa peittävä kudos) tai silmäleikkausta edellyttävä sairaus.
Kerro lääkärillesi, jos sinulla on
- munuaisvaivoja
- maksavaivoja.
Huomaa että Taptiqom-valmisteella voi olla seuraavia vaikutuksia ja että jotkin niistä saattavat olla pysyviä:
- Taptiqom voi lisätä silmäripsien pituutta, paksuutta, väriä ja/tai lukumäärää ja aiheuttaa epätavallista karvan kasvua silmäluomissasi.
- Taptiqom voi aiheuttaa silmiä ympäröivän ihon värin tummumista. Pyyhi kaikki ylimääräinen liuos iholta. Tämä vähentää ihon tummumisen riskiä.
- Taptiqom voi muuttaa värikalvon (silmän värillinen osa) väriä. Jos Taptiqom-valmistetta käytetään vain yhteen silmään, hoidettu silmä voi muuttua pysyvästi eriväriseksi kuin toinen silmä.
- Taptiqom voi aiheuttaa karvankasvua alueilla, joilla liuos pääsee toistuvasti kosketuksiin ihon pinnan kanssa.
Kerro lääkärille ennen leikkausta, että käytät Taptiqom-valmistetta, koska timololi voi muuttaa joidenkin nukutuksessa käytettävien lääkkeiden vaikutusta.
Lapset ja nuoret
Taptiqom-valmistetta ei suositella alle 18-vuotiaille lapsille ja nuorille, koska tästä ikäryhmästä ei ole tehoa ja turvallisuutta koskevia tietoja.
Muut lääkevalmisteet ja Taptiqom
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan otat tai olet äskettäin ottanut tai saatat ottaa muita lääkkeitä.
Taptiqom saattaa vaikuttaa muihin käyttämiisi lääkkeisiin tai ne voivat vaikuttaa siihen.
Kerro erityisesti lääkärille, jos käytät tai aiot käyttää:
- muita silmätippoja glaukooman hoitoon
- lääkkeitä verenpaineen alentamiseen
- sydänlääkettä
- diabeteslääkkeitä
- kinidiiniä (käytetään sydänsairauksien ja joidenkin malariatyyppien hoitoon)
- masennuslääkkeitä nimeltä fluoksetiini ja paroksetiini.
Jos käytät muita lääkkeitä silmään, pidä vähintään 5 minuutin väli Taptiqom-valmisteen ja muun lääkkeen silmään laittamisen välillä.
Piilolinssit
Poista piilolinssit ennen tippojen laittamista ja odota vähintään 15 minuuttia ennen linssien asettamista takaisin.
Raskaus, imetys ja hedelmällisyys
Jos voit tulla raskaaksi, sinun on käytettävä tehokasta ehkäisymenetelmää Taptiqom-hoidon aikana. Älä käytä Taptiqom-valmistetta, jos olet raskaana. Älä käytä Taptiqom-valmistetta, jos imetät. Kysy neuvoa lääkäriltä.
Ajaminen ja koneiden käyttö
Taptiqom-valmisteeseen liittyy haittavaikutuksia, kuten näön sumeneminen, jotka voivat vaikuttaa kykyysi ajaa ja/tai käyttää koneita. Älä aja tai käytä koneita, ennen kuin voit hyvin ja näkösi on kirkas.
Lääke voi heikentää kykyä kuljettaa moottoriajoneuvoa tai tehdä tarkkaa keskittymistä vaativia tehtäviä. On omalla vastuullasi arvioida, pystytkö näihin tehtäviin lääkehoidon aikana. Lääkkeen vaikutuksia ja haittavaikutuksia on kuvattu muissa kappaleissa. Lue koko pakkausseloste opastukseksesi. Keskustele lääkärin tai apteekkihenkilökunnan kanssa, jos olet epävarma.
Taptiqom sisältää fosfaattipuskureita
Tämä lääkevalmiste sisältää noin 0,04 mg fosfaatteja per tippa, mikä vastaa 1,3 mg:aa/ml. Jos sinulla on vakava vaurio silmän etuosan läpinäkyvässä kerroksessa (sarveiskalvossa), fosfaatit voivat hyvin harvinaisissa tapauksissa aiheuttaa sameita laikkuja sarveiskalvoon johtuen kalsiumin kertymisestä hoidon aikana.
Miten valmistetta käytetään
Käytä tätä lääkettä juuri siten kuin lääkäri on määrännyt tai apteekkihenkilökunta on neuvonut. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma.
Suositeltu annos on yksi tippa Taptiqom-valmistetta silmään tai silmiin kerran päivässä. Älä käytä useampia tippoja tai käytä useammin kuin lääkäri on neuvonut. Tämä voi huonontaa Taptiqom-valmisteen tehoa.
Käytä Taptiqom-valmistetta molempiin silmiin vain jos lääkäri on niin määrännyt. Hävitä avattu pakkaus jäljelle jääneine sisältöineen heti käytön jälkeen.
Käytä vain silmätippoina. Älä niele.
Älä anna kerta-annospakkauksen koskettaa silmää tai silmiä ympäröiviä alueita. Se voi vaurioittaa silmääsi. Se voi myös saastua bakteereilla, jotka voivat aiheuttaa silmäinfektioita. Nämä voivat johtaa silmän vakavaan vaurioitumiseen, jopa näön menetykseen. Välttääksesi mahdollista kerta-annospakkauksen saastumista älä anna kerta-annospakkauksen kärjen olla kosketuksissa minkään pinnan kanssa.
Käyttöohjeet:
Kun aloitat uuden pussin:
Älä käytä kerta-annospakkauksia, jos pussi on rikki. Avaa pussi katkoviivaa pitkin. Kirjoita pussin avauspäivä pussiin siihen varattuun kohtaan.
Aina kun käytät Taptiqom-valmistetta:
- Pese kätesi.
- Ota kerta-annospakkausliuska pussista.
- Irrota yksi kerta-annospakkaus liuskasta.
- Pane jäljellä oleva liuska takaisin pussiin ja sulje pussi taittamalla reuna.
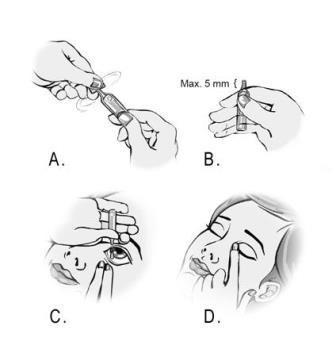
- Avaa kerta-annospakkaus kiertämällä kärki auki. (Kuva A)
- Pidä kerta-annospakkausta peukalon ja etusormen välissä. Huomaa, että kerta-annospakkauksen kärki ei saa näkyä yli 5 mm etusormeasi ylempänä. (Kuva B)
- Kallista päätäsi taaksepäin tai asetu makuulle. Aseta käsi otsalle. Etusormen pitäisi olla samansuuntainen kulmakarvan kanssa tai levätä nenänvarrella. Katso ylöspäin. Vedä alempaa silmäluomea alaspäin toisella kädellä. Älä anna kerta-annospakkauksen minkään osan koskettaa silmää tai mitään silmää ympäröivää aluetta. Purista kerta-annospakkausta kevyesti, jolloin tippa putoaa alaluomen ja silmän väliin. (Kuva C)
- Sulje silmäsi ja paina silmän sisäkulmaa sormella noin kahden minuutin ajan. Näin estät silmätipan valumisen kyynelkanavaan. (Kuva D)
- Pyyhi pois ylimääräinen liuos silmää ympäröivältä iholta.
Jos tippa ei osu silmään, yritä uudelleen.
Jos lääkäri on määrännyt sinua käyttämään tippoja molempiin silmiin, toista vaiheet 7–9 toiselle silmälle.
Yhden kerta-annospakkauksen sisältö riittää molempiin silmiin. Hävitä avattu kerta-annospakkaus jäljelle jääneine sisältöineen heti käytön jälkeen.
Jos käytät muita lääkkeitä silmään, pidä vähintään 5 minuutin väli Taptiqom-valmisteen ja muun lääkkeen silmään laittamisen välillä.
Jos käytät enemmän Taptiqom-valmistetta kuin sinun pitäisi, sinua saattaa huimata tai sinulla voi olla päänsärkyä, sydänoireita tai hengitysvaikeuksia.
Jos olet ottanut liian suuren lääkeannoksen tai vaikkapa lapsi on ottanut lääkettä vahingossa, ota aina yhteyttä lääkäriin, sairaalaan tai Myrkytystietokeskukseen (puh. 0800 147 111) riskien arvioimiseksi ja lisäohjeiden saamiseksi.
Jos nielet vahingossa lääkettä, kysy neuvoja lääkäriltä.
Jos unohdat käyttää Taptiqom-valmistetta, käytä yksi tippa heti kun muistat ja palaa sitten säännölliseen rutiiniisi. Jos kuitenkin on lähes seuraavan annoksen aika, jätä väliin jäänyt annos ottamatta. Älä käytä kaksinkertaista annosta korvataksesi unohtamasi annoksen.
Älä lopeta Taptiqom-valmisteen käyttöä kysymättä lääkäriltäsi. Jos lopetat Taptiqom-valmisteen käytön, paine silmässä kohoaa uudelleen. Tämä voi aiheuttaa pysyvän vaurion silmään.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa. Useimmat haittavaikutukset eivät ole vakavia.
Voit yleensä jatkaa tippojen käyttöä, jos vaikutukset eivät ole vakavia. Jos olet huolestunut, puhu lääkärin tai apteekkihenkilökunnan kanssa.
Seuraavat ovat tunnettuja Taptiqom-valmisteen käyttöön liittyviä haittavaikutuksia:
Yleiset haittavaikutukset
Seuraavia voi esiintyä alle 1 henkilöllä 10:stä:
Silmät
Silmän kutina. Silmän ärsytys. Silmäkipu. Silmän punoitus. Muutokset silmäripsien pituudessa, paksuudessa ja lukumäärässä. Roskan tunne silmässä. Silmäripsien värimuutokset. Valonarkuus. Näön sumeneminen.
Melko harvinaiset haittavaikutukset
Seuraavia voi esiintyä alle 1 henkilöllä 100:sta:
Hermosto
Päänsärky.
Silmät
Kuivasilmäisyys. Silmäluomien punoitus. Pienet pistemäiset tulehduskohdat silmän pinnalla. Vetiset silmät. Turvonneet silmäluomet. Väsyneet silmät. Silmäluomien tulehdus. Silmän sisäinen tulehdus. Epämukava tunne silmässä. Silmäallergia. Silmän tulehdus. Epänormaali tuntemus silmässä.
Seuraavia muita haittavaikutuksia on havaittu Taptiqom-valmisteen sisältämillä lääkkeillä (tafluprosti ja timololi) ja näin ollen niitä saattaa ilmetä Taptiqom-valmistetta käytettäessä:
Seuraavia haittavaikutuksia on havaittu tafluprostilla:
Silmät
Näöntarkkuuden huononeminen. Värikalvon värin muutos (voi olla pysyvä). Silmiä ympäröivän ihon värin muutos. Silmän pintakalvojen turpoaminen. Rähmiminen. Silmän pintakalvojen värjäytyminen. Follikkeleita silmän pintakalvoissa. Silmän painuminen sisäänpäin. Iriitti/uveiitti (tulehdus silmän väriosassa). Makulaturvotus / rakkulainen makulaturvotus (silmän sisällä sijaitsevan verkkokalvon turvotus, joka johtaa näön heikkenemiseen).
Iho
Epätavallinen karvan kasvu silmäluomilla.
Hengityselimet
Astman paheneminen, hengenahdistus.
Seuraavia haittavaikutuksia on havaittu timololilla:
Immuunijärjestelmä
Allergiset reaktiot, mukaan lukien ihonalainen turvotus, nokkosihottuma, ihottuma. Vakava, äkillinen, hengenvaarallinen allerginen reaktio. Kutina.
Aineenvaihdunta ja ravitsemus
Matala verensokeri.
Psyykkiset häiriöt
Masennus. Univaikeudet. Painajaiset. Muistin menetys. Hermostuneisuus. Hallusinaatiot.
Hermosto
Huimaus. Pyörtyminen. Epätavalliset tuntemukset (kuten pistely). Myasthenia gravis -taudin (lihassairaus) merkkien ja oireiden lisääntyminen. Aivohalvaus. Aivojen vähentynyt verenkierto.
Silmät
Sarveiskalvon tulehdus. Alentunut sarveiskalvon herkkyys. Näköhäiriöt, taittovirheet mukaan lukien (johtuvat joskus mustuaista supistavan (mioottisen) hoidon lopettamisesta). Yläluomen roikkuminen. Kahtena näkeminen. Näön sumeneminen ja verkkokalvon alaisen, verisuonia sisältävän kerroksen irtoaminen filtroivan silmäleikkauksen jälkeen, mikä voi aiheuttaa näköhäiriöitä. Sarveiskalvon eroosio.
Kuulo
Tinnitus (korvien soiminen).
Sydän
Hidas syke. Rintakipu. Sydämentykytys. Turvotus (nesteen kertyminen). Muutokset sydämen sykkeen rytmissä tai nopeudessa. Kongestiivinen sydämen vajaatoiminta (sydäntauti, johon liittyy hengenahdistusta ja nesteen kertymisestä johtuva jalkaterien ja säärien turvotus). Erään tyyppinen rytmihäiriö. Sydänkohtaus. Sydämen vajaatoiminta.
Verisuonisto
Alhainen verenpaine. Ontuminen. Raynaud'n oireyhtymä, kylmät kädet ja jalat.
Hengitys
Keuhkoputkien supistuminen (etupäässä potilailla, joilla on jo sairaus). Hengitysvaikeudet. Yskä.
Ruoansulatuselimistö
Pahoinvointi. Ruoansulatushäiriö. Ripuli. Kuiva suu. Makuhäiriöt. Vatsakipu. Oksentelu.
Iho
Hiustenlähtö. Hopeanhohtoisen valkea ihottuma (psoriasin kaltainen ihottuma) tai psoriasiksen paheneminen. Ihottuma.
Lihakset ja luusto
Lihaskipu, jonka syynä ei ole liikunta. Nivelkipu.
Sukupuolielimet ja rinnat
Peyronien tauti (joka voi aiheuttaa peniksen käyristymisen). Seksuaalinen toimintahäiriö. Alentunut sukupuolivietti.
Yleisoireet
Lihasheikkous/-väsymys. Jano.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä kerta-annospakkauksessa, pussissa ja kotelossa mainitun viimeisen käyttöpäivämäärän jälkeen, joka on merkitty lyhenteen ”EXP” jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä avaamattomat foliopussit jääkaapissa (2–8°C). Älä avaa pussia ennen kuin aiot aloittaa silmätippojen käyttämisen, koska avatussa pussissa olevat käyttämättömät kerta-annospakkaukset on hävitettävä 28 päivän kuluttua pussin avaamisesta ensimmäisen kerran.
Foliopussin avaamisen jälkeen:
- Säilytä kerta-annospakkaukset alkuperäisessä foliopussissa. Herkkä valolle.
- Säilytä alle 25°C.
- Hävitä käyttämättömät kerta-annospakkaukset 28 päivän kuluttua foliopussin avaamisesta ensimmäisen kerran.
- Hävitä avattu kerta-annospakkaus jäljelle jääneine sisältöineen heti käytön jälkeen.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Taptiqom sisältää
- Vaikuttavat aineet ovat tafluprosti ja timololi. 1 ml liuosta sisältää 15 mikrogrammaa tafluprostia ja 5 mg timololia.
- Muut aineosat ovat glyseroli, dinatriumfosfaattidodekahydraatti, dinatriumedetaatti, polysorbaatti 80, kloorivetyhappo ja/tai natriumhydroksidi (pH:n säätöön) ja injektionesteisiin käytettävä vesi.
Lääkevalmisteen kuvaus ja pakkauskoko (-koot)
Taptiqom on kirkas, väritön neste (liuos). Se toimitetaan muovisissa kerta-annospakkauksissa, joista kukin sisältää 0,3 ml liuosta. Yhdessä pussissa on kymmenen kerta-annospakkausta. Taptiqom toimitetaan pakkauksissa, jotka sisältävät 30 tai 90 kerta-annospakkausta.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija ja valmistaja
Myyntiluvan haltija
Santen Oy
Niittyhaankatu 20
33720 Tampere
Valmistaja
Santen Oy
Kelloportinkatu 1
33100 Tampere
Tällä lääkevalmisteella on myyntilupa Euroopan talousalueeseen kuuluvissa jäsenvaltioissa ja Yhdistyneessä kuningaskunnassa (Pohjois-Irlannissa) kauppanimellä Taptiqom:
Itävalta, Belgia, Bulgaria, Kroatia, Kypros, Tšekin tasavalta, Tanska, Viro, Suomi, Ranska, Saksa, Kreikka, Unkari, Islanti, Irlanti, Latvia, Liettua, Luxemburg, Alankomaat, Malta, Norja, Puola, Portugali, Romania, Slovakia, Slovenia, Espanja, Ruotsi, Yhdistynyt kuningaskunta (Pohjois-Irlanti)
Loyada: Italia
Tämä pakkausseloste on tarkistettu viimeksi 15.7.2022